文章信息
- 张馨月, 王广龙, 黄蔚, 王枫, 倪桢燚, 熊爱生.
- ZHANG Xinyue, WANG Guanglong, HUANG Wei, WANG Feng, NI Zhenyi, XIONG Aisheng.
- 胡萝卜抗坏血酸过氧化物酶基因的分离及其对非生物胁迫的响应
- Cloning of the gene encoding ascorbate peroxidase from carrot and its response to abiotic stress
- 南京农业大学学报, 2016, 39(01): 55-62
- Journal of Nanjing Agricultural University, 2016, 39(01): 55-62.
- http://dx.doi.org/10.7685/jnau.201503014
-
文章历史
- 收稿日期:2015-03-06
植物生长发育期间,高温、低温、干旱、盐害等非生物胁迫会损伤植物细胞,引起渗透和氧化胁迫等次生伤害,继而影响植物的渗透调节作用和离子平衡,产生大量活性氧(reactive oxygen species,ROS),破坏膜系统结构和功能,严重阻碍植物正常生长和发育[1]。为了响应和抵御不利环境所造成的氧化胁迫,植物自身形成了一系列防御机制来清除或降低活性氧所造成的损害。
抗坏血酸(AsA)-谷胱甘肽(GSH)循环是植物响应环境信号的重要机制之一[2]。其中,抗坏血酸过氧化物酶(ascorbate peroxidase,APX)是该循环过程中的关键酶[3]。APX利用抗坏血酸作为电子供体,清除植物体内过量的过氧化物[4]。在植物中,APX主要存在于叶绿体、过氧化物酶体和线粒体中。前人研究表明,APX与植物的生长发育和逆境抗性也有着密切的关系[5, 6]。目前,在草莓[7]、番茄[8]、烟草[9]、小麦[10]、黑麦草[11]等植物中的研究已经证实,APX基因参与植物生长发育和多种逆境胁迫的响应过程。
胡萝卜(Daucus carota L.)属于伞形科二年生草本植物,是一种世界性的重要栽培蔬菜,具有丰富的营养品质。胡萝卜生长发育期间,经常会受到高温、低温、干旱、盐害等不利环境的侵袭,最终影响胡萝卜的产量和品质。因此研究胡萝卜非生物胁迫响应相关基因对于揭示和发掘胡萝卜抗逆能力、提高其产量和品质具有重要意义。本试验以胡萝卜品种‘黑田五寸’为研究材料,克隆获得胡萝卜中编码抗坏血酸过氧化物酶的DcAPX基因,并对该基因进行了较为详尽的序列分析。同时利用实时定量PCR技术对其不同组织和非生物胁迫下的表达进行研究,以明确胡萝卜DcAPX基因在非生物胁迫过程中的作用。
1 材料与方法 1.1 菌种、质粒与植物材料大肠杆菌菌株DH5α为南京农业大学农业部华东地区园艺作物生物学与种质创制重点实验室保存;质粒载体pMD18-T、Ex Taq聚合酶、DL2000 Marker、Prime Script RT reagent Kit、SYBR Premix Ex Taq Kit购自大连TaKaRa公司,RNA simple Total RNA Kit购于天根生化科技有限公司(北京)。DNA回收试剂盒购自杭州唯特洁公司。
供试胡萝卜品种为‘黑田五寸’,种植于南京农业大学作物遗传与种质创新国家重点实验室人工气候室。将2月龄的植株进行逆境处理(包括38 ℃高温、4 ℃低温、200 g· L-1 PEG干旱和200 g· L-1 NaCl盐处理),每个处理6株,处理时间分别为1、2、4、8和24 h,取植株中心生长点往下第3片真叶的叶片,以同期未经过逆境处理的植株作为对照,同时取对照植株中根、叶柄和叶片等材料,用于RNA的提取以及cDNA的合成。
1.2 RNA的提取及cDNA的合成采用RNA simple Total RNA Kit提取总RNA,利用Prime Script RT reagent Kit将提取的总RNA反转录成cDNA。
1.3 胡萝卜DcAPX基因的克隆根据本实验室测定的胡萝卜‘黑田五寸’基因组数据,检索并拼接出DcAPX序列,设计一对引物DcAPXF(5′-ATGGGAAAGTGCTACCCAACAGTGAG-3′)和DcAPXR(5′-TTAA-GCCTCAGCAAACCCAAGT- TCAG-3′)。以‘黑田五寸’cDNA为模板进行扩增,PCR反应程序为:94 ℃ 5 min;94 ℃ 30 s,54 ℃ 30 s,72 ℃ 1 min,共30个循环;72 ℃ 10 min。PCR产物用12 g· L-1琼脂糖凝胶电泳回收目的条带,与pMD18-T载体连接过夜,并转化至大肠杆菌DH5α中,提取质粒经PCR鉴定后委托南京金斯瑞生物科技有限公司测序。
1.4 序列分析其他植物的APX序列均来自于NCBI数据库,使用BLAST进行序列比对。先用软件DNAMAN 6.0.3.99 对序列进行多重比对,然后构建同源进化树,并用MEGA 5对进化树进行测试和编辑,生成报告图形[12]。用http://www.expasy.org网站相关软件完成蛋白质基本性质分析[13, 14]。用http://npsa-pbil.ibcp.fr网站预测蛋白二级结构[15];采用DNAMAN软件进行蛋白质亲水性/疏水性分析。通过SWISS-MODEL(http://swiss-model.expase.org)建立蛋白质空间结构模型[16, 17, 18]。
1.5 实时定量PCR荧光定量PCR采用ABI 7300 Real-time PCR System和7300 System software完成。用胡萝卜actin基因 作为参考基因,与目标基因一起扩增,表达检测引物为actin-F(5′-CGGTATTGTGTTGGACTCTGGTGAT-3′)和actin-R(5′-CAGCAAGGTCAAGACGGAGTATGG-3′)。根据从‘黑田五寸’中扩增的DcAPX序列设计表达检测引物BDDcAPX-F(5′-AACAGTGAGCGAGGAGTACAAGGT-3′)和BDDcAPX-R(5′-CAAGACGAAGCATAAGAGGAGCACAA-3′)。采用SYBR Premix Ex Taq试剂盒并按照操作说明进行实时定量PCR测定。以胡萝卜actin基因作为内参[19, 20],计算目的基因的相对表达水平2-ΔΔCT。其中ΔΔCT=(CT靶基因-CT内参)处理组-(CT靶基因-CT内参)对照组。
1.6 数据分析采用Excel 2003和SPSS 16.0进行数据整理和统计分析,采用Duncan′s法测验分析数据差异显著性。
2 结果与分析 2.1 胡萝卜DcAPX基因的克隆以胡萝卜品种‘黑田五寸’的cDNA为模板,分别以DcAPXF和DcAPXR作为上游和下游引物,PCR扩增后得到750 bp左右的片段(图 1)。序列测定与分析表明,来源于‘黑田五寸’的APX基因含有1个753 bp的开放阅读框,编码250个氨基酸(图 2)。将DcAPX基因序列提交GenBank,登录号为KR364573。预测其蛋白质相对分子质量为27.76×103,等电点(pI)为5.65。
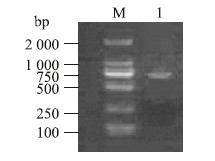 | 图 1 RT-PCR克隆胡萝卜DcAPX基因 Fig. 1 DcAPX gene amplified by RT-PCR from carrot M:分子量标准Marker;1:黑田五寸Kurodagosun |
将胡萝卜DcAPX分别与短果茴芹(Pimpinella brachycarpa)、茶树(Camellia sinensis)、烟草(Nicotiana tabacum)、甘薯(Ipomoea batatas)、辣椒(Capsicum annuum)、苹果(Malus domestica)、草莓(Fragaria × ananassa)、马铃薯(Solanum tuberosum)、玉米(Zea mays)、枸杞(Lycium chinense)、棉花(Gossypium hirsutum)、甘蓝(Brassica oleracea)、芜菁(Brassica napus)、枣树(Ziziphus jujube)、番茄(Solanum lycopersicum)、萝卜(Raphanus sativus)、大豆(Glycine max)、蒺藜苜蓿(Medicago truncatula)、拟南芥(Arabidopsis thaliana)和茄子(Solanum melongena)等植物的APX氨基酸序列进行BLAST同源性比对,发现胡萝卜的APX基因编码的蛋白序列与其他物种的APX氨基酸序列相似程度较高,其中短果茴芹的氨基酸序列与本试验中克隆的APX同源性达到96.80%。对这些氨基酸序列进行多重比对后,结果发现它们均含有3类结合位点(图 2),即亚铁血红素结合位点、底物结合位点和K+结合位点。
 | 图 2 胡萝卜APX与其他物种APX氨基酸序列保守区域的多重比较 Fig. 2 Alignment of conserved domains of APX from carrot and other plant species #亚铁血红素结合位点 Heme binding site;*底物结合位点 Substrate binding site;▼K+结合位点 K+ binding site |
对胡萝卜和其他植物的APX氨基酸序列进行理化性质分析。由表 1可见:这些植物中的氨基酸残基数均为250个左右,相对分子质量为(27.05~27.76)×103。碱性氨基酸和酸性氨基酸比例相近,脂肪族氨基酸远多于芳香族氨基酸。同时不同物种间的APX氨基酸物理性质类似,表明该基因在这些植物间具有高度同源性。
| 植物Plant species | 氨基酸残基数No.ofamino acid | 理论相对分子质量/10 3Theoretical relativemolecular mass | 理论等电点TheoreticalpI | 碱性氨基酸比例/%Rate of basicamino acid | 酸性氨基酸比例/%Rate of acidicamino acid | 脂肪族氨基酸比例/%Rate of aliphaticamino acid | 芳香族氨基酸比例/%Rate of aromaticamino acid |
| 胡萝卜 D.carota | 250 | 27.76 | 5.65 | 14.8 | 14.8 | 36.0 | 9.2 |
| 短果茴芹 P.brachycarpa | 250 | 27.75 | 5.92 | 14.4 | 14.8 | 35.6 | 9.2 |
| 茶树 C.sinensis | 250 | 27.53 | 6.24 | 14.4 | 15.6 | 38.4 | 8.8 |
| 烟草 N.tabacum | 250 | 27.39 | 5.39 | 14.8 | 14.4 | 38.4 | 8.8 |
| 甘薯 I.batatas | 250 | 27.59 | 5.19 | 14.8 | 14.0 | 37.2 | 9.6 |
| 辣椒 C.annuum | 250 | 27.49 | 5.39 | 14.8 | 14.4 | 38.0 | 9.2 |
| 苹果 M.domestica | 250 | 27.39 | 5.62 | 14.0 | 14.0 | 36.8 | 8.8 |
| 草莓 F.ananassa | 250 | 27.27 | 5.91 | 14.0 | 14.4 | 39.2 | 8.8 |
| 马铃薯 S.tuberosum | 250 | 27.42 | 6.10 | 14.4 | 15.2 | 38.4 | 8.8 |
| 玉米 Z.mays | 250 | 27.37 | 5.86 | 14.4 | 14.8 | 38.0 | 8.8 |
| 枸杞 L.chinense | 250 | 27.48 | 5.86 | 14.8 | 15.2 | 38.4 | 8.8 |
| 棉花 G.hirsutum | 250 | 27.43 | 5.85 | 13.2 | 13.6 | 38.0 | 8.4 |
| 甘蓝 B.oleracea | 250 | 27.56 | 5.58 | 14.8 | 14.8 | 36.4 | 8.8 |
| 芜菁 B.napus | 250 | 27.64 | 5.99 | 14.4 | 15.2 | 37.6 | 8.4 |
| 枣树 Z.jujube | 250 | 27.56 | 6.04 | 14.4 | 15.2 | 37.6 | 8.8 |
| 番茄 S.lycopersicum | 250 | 27.42 | 5.82 | 14.8 | 15.2 | 38.4 | 8.4 |
| 萝卜 R.sativus | 250 | 27.69 | 5.57 | 15.2 | 15.2 | 36.8 | 8.4 |
| 大豆 G.max | 250 | 27.05 | 5.60 | 14.4 | 14.4 | 39.2 | 9.2 |
| 蒺藜苜蓿 M.truncatula | 250 | 27.13 | 5.61 | 14.4 | 14.4 | 39.2 | 9.2 |
| 拟南芥 A.thaliana | 250 | 27.56 | 6.04 | 14.8 | 15.6 | 36.4 | 8.8 |
| 茄子 S.melongena | 250 | 27.46 | 6.18 | 14.4 | 15.6 | 37.2 | 8.4 |
对本试验中克隆所得的胡萝卜DcAPX基因推导的氨基酸序列进行疏水性/亲水性分析,结果(图 3)表明:该蛋白的第19位半胱氨酸亲水性最强,其次是第121位天冬氨酸以及第169位的组氨酸。疏水性最强的位点是第102位的缬氨酸,较强的位点为第104位丙氨酸及第101位甘氨酸。
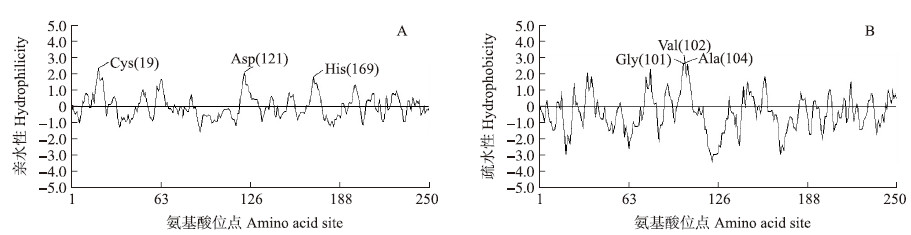 | 图 3 预测的胡萝卜DcAPX氨基酸序列的亲水性和疏水性 Fig. 3 Predicted hydrophilicity and hydrophobicity of deduced amino acid sequence of DcAPX from carrot |
选取21个物种,分析胡萝卜DcAPX与这些物种中APX的进化关系。从构建的同源进化树可以看出:胡萝卜DcAPX与短果茴芹的进化最为相似;茄科当中番茄、马铃薯、枸杞、茄子、辣椒、烟草的APX同属一个分支;十字花科中甘蓝、拟南芥、芜菁、萝卜的APX同属于一个分支;豆科中蒺藜苜蓿、大豆的APX同属于一个分支(图 4)。
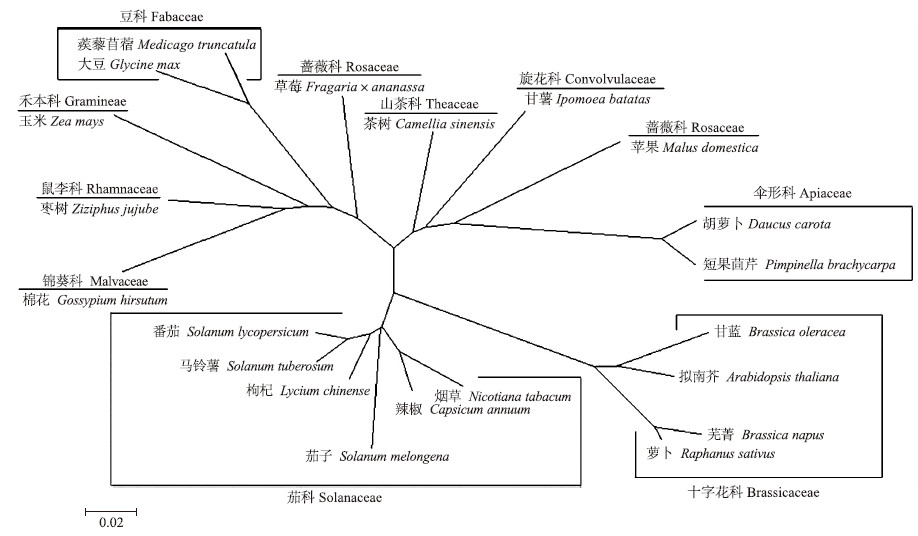 | 图 4 部分物种的APX氨基酸序列的系统进化树 Fig. 4 Phylogenetic tree of amino acid sequences of APX from several plant species |
对胡萝卜DcAPX基因推导的氨基酸序列进行分析得知,胡萝卜DcAPX二级结构由38.40%的α-螺旋、10.40%的延伸主链和 51.20%的随机卷曲构成。α-螺旋和随机卷曲是构成胡萝卜DcAPX二级结构的 主要形式(图 5)。对胡萝卜APX分析可以发现,其三级结构由10个α-螺旋以及4个β-折叠构成(图 6)。
 |
图 5 胡萝卜DcAPX的二级结构分析 Fig. 5 The secondary structures of DcAPX
蓝色:α-螺旋;红色:延伸主链;紫色:无规则卷曲 Blue:Alpha helix;Red:Extended strand;Purple:Random coil |
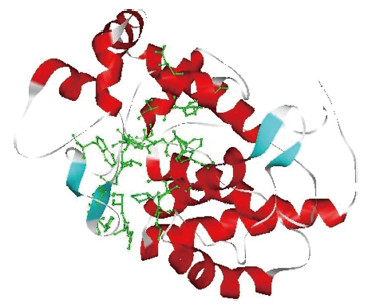 | 图 6 胡萝卜DcAPX三级结构 Fig. 6 The tertiary structural model of DcAPX from carrot 绿色表示亚铁血红素结合位点。Green represents heme binding site. |
利用荧光定量PCR技术检测发现,‘黑田五寸’DcAPX基因在不同组织(根、叶柄、叶片)中的表达不同(图 7)。‘黑田五寸’DcAPX基因在根、叶柄、叶片中均可表达,其中叶片中表达量最高,分别为根和叶柄中的22和25倍。
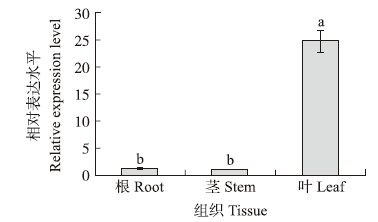 | 图 7 DcAPX基因在‘黑田五寸’不同组织中的表达水平 Fig. 7 Expression levels of DcAPX gene in different tissues of‘Kurodagosun’ 不同字母表示在0.05水平上差异显著。Different letters indicate significant difference at 0.05 level. The same as follows. |
由图 8可见:‘黑田五寸’中DcAPX基因在受到外界高温(38 ℃)、低温(4 ℃)、干旱(200 g· L-1 PEG)和盐害(200 g· L-1 NaCl)逆境胁迫后,其表达量较对照条件下有显著变化,高温处理后的基因表达变化最大。高温可以显著诱导‘黑田五寸’DcAPX基因的表达,并在2 h后达到最大值,之后随着时间推移,表达逐渐减弱。干旱处理后1 h表达量升至最大,随后减弱,并趋于稳定。盐害处理条件下,于1~2 h期间表达最大,随后减弱,并趋于稳定。低温处理条件下,DcAPX基因表达量在前期较稳定,但在24 h后显著上升。盐胁迫下,DcAPX基因表达呈现先升高后降低的趋势,其表达量也在1 h时达到最大(图 8)。
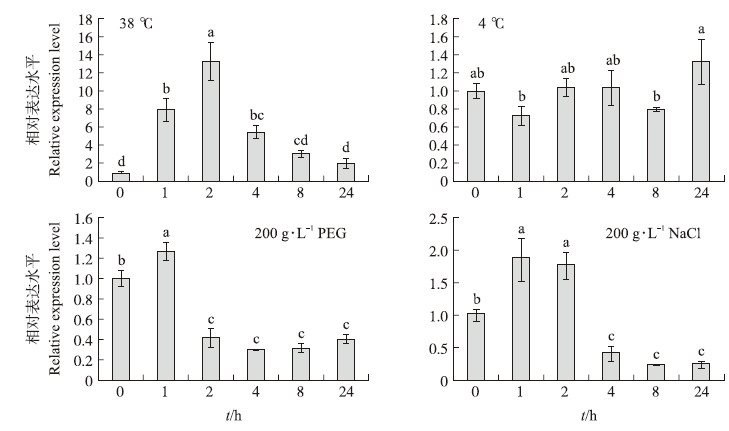 | 图 8 不同逆境条件下‘黑田五寸’中DcAPX基因的表达水平 Fig. 8 Expression level analysis of DcAPX gene under different abiotic stresses in‘Kurodagosun’ |
植物遭受逆境胁迫时,植物内产生和清除活性氧(ROS)的平衡机制遭到破坏[21]。活性氧在细胞内大量积累,引起胁迫,造成细胞结构和大分子物质的氧化损伤,阻碍植物个体生长和发育,进而影响作物产量和品质[22, 23]。抗坏血酸过氧化物酶(APX)利用抗坏血酸(AsA)作为电子供体,将H2O2还原为H2O,是植物抵抗逆境胁迫的重要分子机制之一[24, 25]。因此,研究APX有利于揭示植物生长和抵御胁迫的机制,对于提高作物产量和品质具有重要意义。
本研究中克隆获得的胡萝卜DcAPX基因编码的蛋白质与短果茴芹、拟南芥、茶树、烟草、甘薯等20种植物中预测的蛋白质高度同源,具有类似的理化性质,说明APX在进化上相对保守。进化树分析进一步表明,胡萝卜DcAPX与同属伞形科的短果茴芹APX进化关系最为接近,在不同种属的植物中呈现一定的进化相似性。对胡萝卜DcAPX氨基酸序列分析发现,其三维结构大部分由α-螺旋构成。将胡萝卜与其他20种同源性较高的植物进行氨基酸序列多重比对,结果显示APX基因编码的蛋白均含有3类结合位点,即亚铁血红素结合位点、底物结合位点和K+结合位点,这3个位点在植物清除体内过氧化物上面发挥着重要的作用,而其中的H-162、L-165、G-166、A-168既是亚铁血红素结合位点又是底物结合位点,在空间位置上也较为接近,表明它们可能共同参与清除植物体内积累的过氧化物,从而提高植物抗逆性[26]。
前人研究表明,APX与植物个体的生长发育相关[27],并在植物根、叶柄、叶片等组织中具有表达特异性[28, 29],另外APX基因可以响应高温、低温、干旱、盐害等非生物胁迫[29, 30, 31]。本文研究结果也证实,胡萝卜中DcAPX基因表达呈现出明显的组织特异性,其在胡萝卜叶片中的表达量最高,在叶柄和根中表达较低。在不同非生物胁迫中也呈现不同的响应情况,DcAPX在低温前期表达相对稳定,但在后期表达升高,这可能是因为在不同逆境胁迫下DcAPX响应的时间和强度不同。本文是第一次从胡萝卜中克隆获得该类基因,对进一步研究伞形科植物APX基因及其功能也具有重要的意义。
| [1] | Zou J,Liu C F,Liu A L,et al. Overexpression of OsHsp17.0 and OsHsp23.7 enhances drought and salt tolerance in rice[J]. Journal of Plant Physiology,2012,169:628-635. |
| [2] | Wang Z N,Xiao Y,Chen W S,et al. Increased vitamin C content accompanied by an enhanced recycling pathway confers oxidative stress tolerance in Arabidopsis[J]. Journal of Integrative Plant Biology,2010,52(4):400-409. |
| [3] | Asada K. Ascorbate peroxidase:a hydrogen peroxide-scavenging enzyme in plants[J]. Physiologia Plantarum,1992,85:235-241. |
| [4] | Ishikawa T,Shigeoka S. Recent advances in ascorbate biosynthesis and the physiological significance of ascorbate peroxidase in photosynthesizing organisms[J]. Bioscience,Biotechnology and Biochemistry,2008,72(5):1143-1154. |
| [5] | Noctor G,Foyer C H. Ascorbate and glutathione:keeping active oxygen under control[J]. Annual Review of Plant Physiology and Plant Molecular Biology,1998,49:249-279. |
| [6] | Annalisa P,Franca T,Laura D G,et al. Alteration in ascorbate and ascorbate peroxidase in programmed cell death and oxidative stress[J]. BMC Plant Biology,2005,5(1):28. |
| [7] | Hou Y X,Tang H R,Zhang Y,et al. Cloning and expression analysis of ascorbate peroxidase gene during fruit development and ripening in Fragaria×ananassa cv.Toyonaka[J]. World Journal of Agricultural Sciences,2009,5(6):675-679. |
| [8] | Liu K L,Shen L,Wang J Q,et al. Rapid inactivation of chloroplastic ascorbate peroxidase is responsible for oxidative modification to Rubisco in tomato(Lycopersicon esculentum)under cadmium stress[J]. Journal of Integrative Plant Biology,2008,50(4):415-426. |
| [9] | Orvar B L,Ellis B E. Isolation of a cDNA encoding cytosolic ascorbate peroxidase in tobacco[J]. Plant Physiology,1995,108:839-840. |
| [10] | Chen Y P,Wang H Z,Wang X E,et al. Cloning and expression of peroxisomal ascorbate peroxidase gene from wheat[J]. Molecular Biology Reports,2006,33:207-213. |
| [11] | Hu L X,Li H Y,Pang H C,et al. Responses of antioxidant gene,protein and enzymes to salinity stress in two genotypes of perennial ryegrass(Lolium perenne)differing in salt tolerance[J]. Journal of Plant Physiology,2012,169:146-156. |
| [12] | Tamura K,Peterson D,Peterson N,et al. MEGA5:molecular evolutionary genetics analysis using maximum likelihood,evolutionary distance,and maximum parsimony methods[J]. Molecular Biology and Evolution,2011,28(10):2731-2739. |
| [13] | Gasteiger E,Gattiker A,Hoogland C,et al. ExPASy:the proteomics server for in-depth protein knowledge and analysis[J]. Nucleic Acids Research,2003,31:3784-3788. |
| [14] | Harrison R G,Bagajewicz M J. Predicting the solubility of recombinant proteins in Escherichia coli[J]. Nature Biotechnology,1991,9:443-448. |
| [15] | Combet C,Blanchet C,Geourjon C,et al.NPS@:network protein sequence analysis[J]. Trends in Biochemical Sciences,2000,25(3):147-150. |
| [16] | Guex N,Peitsch M C. SWISS-MODEL and the Swiss-PdbViewer:an environment for comparative protein modeling[J]. Electrophoresis,1997,18:2714-2723. |
| [17] | Schwede T,Kopp J,Guex N,et al. SWISS-MODEL:an automated protein homology-modeling server[J]. Nucleic Acids Research,2003,31:3381-3385. |
| [18] | Arnold K,Bordoli L,Kopp J,et al. The SWISS-MODEL workspace:a web-based environment for protein structure homology modeling[J]. Bioinformatics,2006,22:195-201. |
| [19] | Tian C,Jiang Q,Wang F,et al. Selection of suitable reference genes for qPCR normalization under abiotic stresses and hormone stimuli in carrot leaves[J]. PLoS ONE,2015,10(2):e0117569. |
| [20] | Cora B,Valérie L C,Mathilde B,et al. Impact of carrot resistance on development of the Alternaria leaf blight pathogen(Alternaria dauci)[J]. European Journal of Plant Pathology,2008,121(1):55-66. |
| [21] | Andréia C,Gisele P,Silvia B R,et al. Plant responses to stresses:role of ascorbate peroxidase in the antioxidant protection[J]. Genetics and Molecular Biology,2012,35:1011-1019. |
| [22] | Kumar R R,Goswami S,Kumar N,et al. Expression of novel ascorbate peroxidase isoenzymes of wheat(Triticum aestivum L.)in response to heat stress[J]. International Journal of Plant Physiology and Biochemistry,2011,3(11):188-194. |
| [23] | Guan Q J,Li L,Takano T,et al. Cloning of an ascorbate peroxidase gene from Puccinellia tenuiflora and its expression analysis[J]. Genomics and Applied Biology,2009,28(4):631-639. |
| [24] | Ron M,Feng X Q,Mira C. Post-transcriptional suppression of cytosolic ascorbate peroxidase expression during pathogen-induced programmed cell death in tobacco[J]. The Plant Cell,1998,10:461-473. |
| [25] | Fortunato A S,Lidon F C,Santos P B,et al. Biochemical and molecular characterization of the antioxidative system of Coffea sp.under cold conditions in genotypes with contrasting tolerance[J]. Plant Physiology,2010,167(5):333-342. |
| [26] | Shigeoka S,Ishikawa T,Tamoi M,et al. Regulation and function of ascorbate peroxidase isoenzymes[J]. Journal of Experimental Botany,2002,53:1305-1319. |
| [27] | Li Y J,Hai R L,Du X H,et al. Over-expression of a Populus peroxisomal ascorbate peroxidase(PpAPX)gene in tobacco plants enhances stress tolerance[J]. Plant Breeding,2009,128:404-410. |
| [28] | Liu H C,Tian D Q,Liu J X,et al. Cloning and functional analysis of a novel ascorbate peroxidase(APX)gene from Anthurium andraeanum[J]. Journal of Zhejiang University-Science B(Biomedicine and Biotechnology),2013,14(12):1110-1120. |
| [29] | 刘维信,曹寿椿. 高温对不结球白菜细胞膜透性过氧化物酶活性等的影响[J]. 南京农业大学学报,1992,15(3):115-117. DOI:10.7685/j.issn.1000-2030.1992.03.022. Liu W X,Cao S C. Influences of high temperature on cell membrane permeability,peroxidase activity and other biochemical indices in non-heading Chinese cabbage[J]. Journal of Nanjing Agricultural University,1992,15(3):115-117(in Chinese). |
| [30] | Wang Y J,Michael W,Richaed M,et al. Overexpression of cytosolic ascorbate peroxidase in tomato confers tolerance to chilling and salt stress[J]. Journal of the American Society for Horticultural Science,2005,130(2):167-173. |
| [31] | Oidaira H,Sano S,Koshiba T,et al. Enhancement of antioxidative enzyme activities in chilled rice seedlings[J]. Plant Physiology,2000,156(5/6):811-813. |




