文章信息
- 李蕾, 李季, 孟永娇, 张璐, 娄群峰, 钱春桃, 陈劲枫.
- LI Lei, LI Ji, MENG Yongjiao, ZHANG Lu, LOU Qunfeng, QIAN Chuntao, CHEN Jinfeng.
- 黄瓜T-DNA插入突变体库的构建
- Construction of cucumber(Cucumis sativus L.) T-DNA insertion mutant library
- 南京农业大学学报, 2016, 39(01): 40-47
- Journal of Nanjing Agricultural University, 2016, 39(01): 40-47.
- http://dx.doi.org/10.7685/jnau.201504014
-
文章历史
- 收稿日期:2015-04-12
黄瓜(Cucumis sativus L.)属葫芦科甜瓜属,是一种重要的蔬菜作物,在全世界广泛栽培。其染色体数目为2x=2n=14,基因组大小约350 Mb。2009年以来,随着黄瓜基因组测序工作完成[1, 2],黄瓜基因组学研究进入后基因组时代。
通过研究突变体来分析和鉴定基因功能,是基因功能组学研究最直接、有效的方法之一[3]。植物突变体库构建方法主要有物理诱变、化学诱变、基因沉默和插入突变等。其中,插入突变是将外源的已知插入元件随机插入植物基因组中,引起插入位点基因的变化,影响其正常表达,产生插入突变体,并以此插入元件为标记来分离和克隆因插入而失活的基因[4]。插入突变的插入元件主要有:T-DNA、转座子和逆转录转座子。由于T-DNA多为单拷贝插入,而且能在后代中稳定遗传[5, 6],T-DNA插入突变已经广泛应用于功能基因组学的研究。农杆菌介导的遗传转化技术的日益成熟和T-DNA插入位点鉴定方法[4]的丰富完善,也为T-DNA插入突变应用奠定了基础。目前,在拟南芥中已经建立了接近饱和的T-DNA插入突变体库,该突变体库包含超过225 000个独立的T-DNA插入株系[7];在水稻中也建立了一定规模的插入突变体库,获得了大约47 932个T-DNA插入株系[8]。此外T-DNA插入突变也逐渐用于番茄[9]、矮牵牛[10]、香蕉[11]、豆类[12]等作物的研究中。葫芦科作物中,任海英等[13]利用T-DNA插入获得甜瓜突变体,筛选到一个蔓枯病抗性明显增强的突变体,命名为edr 2 。
根据Huang等[1]的测序结果,黄瓜基因组中重复序列约占24%,根据已知重复,这其中51.5%可以被分类;注释基因数量为26 682个,平均基因长度为1 046 bp。利用黄瓜基因组序列与甜瓜、西瓜比较分析发现,黄瓜7条染色体中的5条是由祖先的10条染色体融合形成。由于黄瓜与西瓜、甜瓜和南瓜等葫芦科作物的基因组大小相似,但染色体数目不同,推测葫芦科作物有一套相同的基因,只是染色体发生了重排。因此构建黄瓜T-DNA插入突变体库不仅对研究黄瓜基因功能有重要作用,也对葫芦科其他作物功能基因组学研究具有重要借鉴意义。自1986年Trulson等[14]采用农杆菌介导法成功获得了转基因黄瓜材料后,国内外研究者对农杆菌介导的黄瓜遗传转化体系做了大量研究,并不断进行优化完善,现已成功将ICE 1 [15]、Tu[16]等基因转到黄瓜中,这为T-DNA插入突变在黄瓜中的应用提供了前提条件。但有关于黄瓜T-DNA插入突变体的研究还未见报道。本研究以植物插入突变体构建常用的表达载体pROK2为T-DNA插入突变载体,采用农杆菌介导的方法转化黄瓜,构建黄瓜插入突变体库,旨在为黄瓜功能基因组学研究奠定基础。
1 材料与方法 1.1 材料用于遗传转化的黄瓜栽培品种‘长春密刺’由南京农业大学葫芦科作物遗传与种质创新实验室高代自交保存。农杆菌C58由本实验室保存,植物表达载体pROK2购自拟南芥生物资源中心(http://abrc.osu.edu/),载体上携带标记基因NPT- Ⅱ (卡那霉素抗性基因)、CaMV 35 S启动子,图谱[17]如图 1所示。
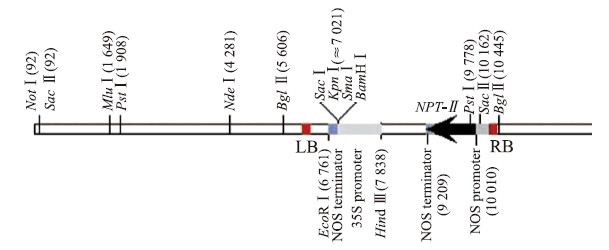 | 图 1 植物表达载体pROK2的图谱 Fig. 1 Maps of vector pROK2 |
MS基本培养基(M5519)、脱乙酰吉兰糖胶、6-BA和ABA等均购自Sigma(上海)生物技术公司;水解酪蛋白、乙酰丁香酮、AgNO3、特美汀、卡那霉素(Kan)、利福平、庆大霉素、四环素、MgSO4、酵母粉、胰蛋白胨和牛肉膏均购自北京鼎国生物技术公司。PCR扩增试剂购自TaKaRa宝生物工程(大连)有限公司,尼龙膜为Hybond产品,Dig探针标记和检测试剂盒为Roche公司产品。
1.2 方法 1.2.1 农杆菌介导的子叶节法转化黄瓜取饱满的‘长春密刺’种子,在超净工作台上用70%乙醇消毒30 s,2%次氯酸钠溶液消毒15 min。灭菌水冲洗3~4次后用无菌滤纸吸干种子表面水分,接种于无菌苗培养基上。(25±2)℃条件下黑暗培养至种子萌发后转到光下培养3~4 d。切取子叶节,接种于预培养基上(25±2)℃条件下黑暗培养1 d。
挑取携带植物表达载体pROK2的农杆菌C58单菌落,接种于含有100 mg·L-1卡那霉素、50 mg·L-1利福平、20 mg·L-1庆大霉素和10 mg·L-1四环素的YEB液体培养基中,28 ℃、250 r·min-1条件下振荡过夜培养18~24 h。5 000 r·min-1离心5 min后弃去上清液,加入MS液体培养基(pH5.3)重悬至D600=0.8作为侵染液。将经预培养的外植体置于农杆菌重悬液中侵染15 min,取出置于共培养基上(25±2)℃条件下黑暗培养3 d,再转移到含适合浓度Kan的选择培养基上光照培养,15 d继代1次,继代2~3次。
抗性芽长到约2 cm后,将其从外植体上切下转接到生根培养上,15 d继代1次。将正常生根生长的植株移出,洗净根系表面的培养基种植于灭菌基质中,浇透水,保鲜膜保湿至植株长出新叶后揭掉保鲜膜,转入正常日光温室中生长。
1.2.2 遗传转化培养基无菌苗MS培养基:预培养基:MS+6-BA 1.0 mg·L-1+ABA 0.2 mg·L-1+AgNO3 2.0 mg·L-1;共培养基:MS+6-BA 1.0 mg·L-1+ABA 0.2 mg·L-1+AgNO3 2.0 mg·L-1+ 乙酰丁香酮50 μmol·L-1;选择培养基MS+6-BA 1.0 mg·L-1+ABA 0.2 mg·L-1+AgNO3 2.0 mg·L-1+卡那霉素(适宜浓度)+特美汀200 mg·L-1+水解酪蛋白1.0 g·L-1;生根培养基:1/2 MS+卡那霉素75 mg·L-1+特美汀200 mg·L-1。除共培养 基pH值为5.3外,其余各阶段培养基pH值均为5.8。所有MS培养基均含有4.47 g·L-1 MS干粉、30 g·L-1 蔗糖和2.5 g·L-1的脱乙酰吉兰糖胶。
1.2.3 Kan浓度敏感试验预培养结束后,不经菌液侵染,将外植体分别接种于含有0、50、100、150和200 mg·L-1 Kan的选择培养基上。3次重复,每次重复12个外植体。15 d继代1次,30 d后统计每个处理外植体不定芽分化情况。以外植体分化率(有不定芽分化的外植体总数/外植体总数×100%)作为评价指标,以完全抑制子叶节不定芽分化,且外植体状态良好的浓度为最适筛选浓度。
1.2.4 T0代和T1代植株PCR检测以表达载体上的特有的CaMV 35 S和NPT- Ⅱ 基因序列作为检测转化植株的报告基因,根据其序列设计特异引物,引物序列如下: 35 S-F:5′-ACAGAACTCGCCGTAAAG-3′; 35 S-R:5′-AGTGGGATTGTGCGTCAT-3′;NPT- Ⅱ -F:5′-CTGGGCACAACAGACAATC-3′;NPT- Ⅱ -R:5′TACCGTAAAGCACGAGGAA-3′。PCR引物由英潍捷基(上海)贸易有限公司合成。
采用改良CTAB法提取T0代和T1代植株的叶片基因组DNA。以其为模板进行PCR扩增,重组质粒为阳性对照,非转化植株和水为阴性对照。PCR反应体系为:模板DNA1.0 μL,上、下游引物各1.0 μL,2 mmol·L-1 dNTPs 2.0 μL,10×Buffer 2.0 μL,25 mmol·L-1 MgCl2 1.2 μL,1 U的Taq DNA聚合酶0.2 μL,加ddH2O补齐至20 μL。PCR程序为:CaMV 35 S:94 ℃ 5 min;94 ℃ 30 s,58 ℃ 30 s,72 ℃ 1 min,35个循环;72 ℃ 10 min;NPT- Ⅱ :94 ℃ 5 min;94 ℃ 30 s,52 ℃ 40 s,72 ℃ 1 min,35个循环;72 ℃ 10 min。扩增产物在10 g·L-1琼脂糖凝胶中电泳,在Alpha Innotech凝胶成像系统中观察拍照。
1.2.5 T1代植株斑点杂交检测采用CTAB法提取14S1自交后代植株叶片基因组大量DNA。以Dig标记的 35 S和NPT- Ⅱ 引物PCR扩增条带作为探针。将5 μL高温变性的DNA样品(2~10 μg)点于尼龙膜上,重组质粒为阳性对照,非转化植株为阴性对照,紫外交联4 min以固定样品。探针标记、预杂交、杂交和显色等步骤按照Roche地高辛试剂盒说明书进行。
1.2.6 T-DNA插入植株表型观察以未转化‘长春密刺’植株为对照,对T1代植株表型进行调查统计。2014年秋季(8月1日)在南京农业大学人工气候箱进行育苗。将未转化的‘长春密刺’的种子和T0代自交种子经浸种、28 ℃催芽后,播种于穴盘中。育苗期间平均昼/夜温度为25 ℃/18 ℃,相对湿度为60%~70%,光照强度500 μmol·m-2·s-1。待幼苗长至2叶1心时,移至南京农业大学园艺学院牌楼试验站温室中生长,正常栽培管理。生长条件为:12 h光周期,平均昼夜气温29 ℃/17 ℃,相对湿度85%,光照强度800 μmol·m-2·s-1。
调查内容:1)整个植株的株型,包含矮壮株、高细株等;2)叶片,包含叶片形状、叶片颜色、叶片大小等;3)花器官,包含花色、花器官的大小、开花与否等;4)果实,包括果实的长短,粗细,刺瘤情况等;5)育性及性型。
2 结果与分析 2.1 优化的农杆菌介导的黄瓜子叶节遗传转化再生过程将经农杆菌菌液侵染、共培养3 d后的子叶节转移到添加了1.0 g·L-1的水解酪蛋白的选择培养基上培养,培养基固化剂由2.5 g·L-1的脱乙酰吉兰糖胶代替8 g·L-1的琼脂粉。在此优化的条件下抗性芽分化率达67.15%(未发表数据)。选择培养初期外植体逐渐由黄绿色变绿且不断生长,1周左右外植体达到最大。培养2周左右部分外植体子叶节部位出现绿色芽点,3周左右部分芽点发育成再生芽。在Kan筛选作用下,抗性芽保持绿色继续生长,无抗性的再生芽生长点出现变黄现象,停止生长。抗性芽生长至2 cm左右时,将其切下转到生根培养基上进行培养(图 2)。2周左右抗性芽生根,将完整植株驯化后转移到灭菌基质中,覆膜保湿。待长出新叶后,揭膜,将其移至日光温室中生长。
 | 图 2 黄瓜遗传转化的主要阶段 Fig. 2 Major steps of the procedure of cucumber transformation A.预培养Pre-culture;B.子叶节再生Cotyledon node regeneration;C.诱导生根Rooting culture |
由表 1可以看出:当Kan为0和50 mg·L-1时,子叶节有不定芽产生,分化率分别为83.3%和50.0%,子外植体保持绿色正常生长;当Kan为100 mg·L-1时,子叶节没有不定芽产生,外植体边缘变黄;当Kan大于100 mg·L-1时,子叶节没有不定芽分化且外植体出现不同程度的黄斑。说明100 mg·L-1的Kan可以完全抑制芽的分化,因此选用100 mg·L-1作为最适Kan筛选浓度。
| ρ(Kan)/(mg·L -1) | 外植体数No.ofexplants | 有芽外植体数No.of explantswith shoots | 分化率Rate ofdifferentiation | 生长情况Growing status condition |
| 0 | 36 | 30 | 83.3 | 外植体保持绿色,有大量的绿色不定芽分化Explants kept green and had amounts of adventitious buds differentiation |
| 50 | 36 | 18 | 50.0 | 外植体保持绿色,有部分绿色的不定芽分化Explants kept green and had someadventitious buds differentiation |
| 100 | 36 | 0 | 0 | 外植体边缘变黄,未有芽分化Explants hadno adventitious buds differentiation and the edge turned yellow |
| 150 | 36 | 0 | 0 | 外植体出现小范围黄色,未有芽分化Small part of explants turned yellow and hadnoadventitious buds differentiation |
| 200 | 36 | 0 | 0 | 外植体出现较大范围黄色,未有芽分化Most part of explants turned yellow and hadnoadventitious buds differentiation |
凝胶电泳结果(图 3)显示:阳性对照重组质粒和抗性植株14S1、14S2均可扩增出 35 S和NPT- Ⅱ 片段,长度分别为440和733 bp,而阴性对照水和非转化植株则不能扩增出 35 S和NPT- Ⅱ 片段,初步证明pROK2重组质粒已成功整合到14S1、14S2两个株系的基因组中。
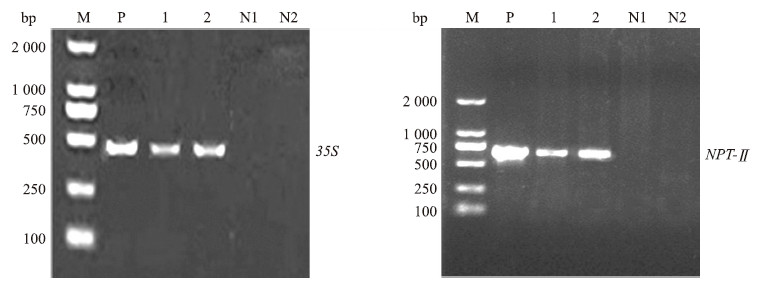 |
图 3 T0代植株PCR检测 Fig. 3 PCR detection of T0 transgenic plants
M:DL2000 DNA marker;P:阳性对照;1:转化植株14S1;2:转化植株14S2;N1:水;N2:非转化植株 M:DL2000 DNA marker;P:Positive control;1:Transgenic plant 14S1;2:Transgenic plant 14S2;N1:Water;N2:Wild type |
选取14S1自交后代单株进行PCR检测,由图 4可见:编号为2~11、13、14号的单株和阳性对照均可扩增出 35 S和NPT- Ⅱ 片段,而阴性对照水和非转化植株则不能扩增出 35 S和NPT- Ⅱ片段,表明pROK2重组质粒由14S1中遗传到了其自交后代植株中,也进一步证明了14S1整合了pROK2重组质粒。
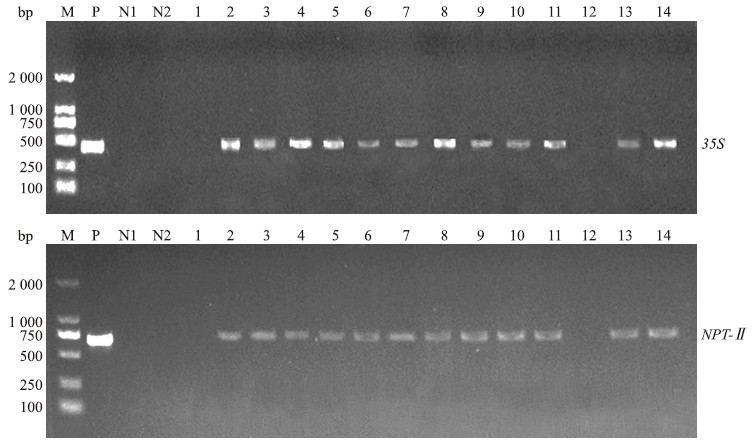 |
图 4 部分T1代植株PCR检测 Fig. 4 PCR detection of part of T1 transgenic plants
M:DL2000 DNA marker;P:阳性对照 Positive control;N1:水 Water;N2:非转化植株 Wild type;1~14:T1代植株T1 transgenic plants 1:14S1-1;2:14S1-3;3:14S1-8;4:14S1-10;5:14S1-12;6:14S1-17;7:14S1-24;8:14S1-27;9:14S1-30;10:14S1-33;11:14S1-34;12:14S1-40;13:14S1-44;14:14S1-46 |
以Dig标记的 35 S和NPT- Ⅱ 引物PCR扩增条带作为探针,对能扩增出 35 S和NPT- Ⅱ 片段的12株单株及从剩余T1代中随机选取的11株单株进行斑点杂交检测。由图 5可以看出:阳性对照重组质粒(a1)显示有杂交信号,阴性对照非转基因植株(a2)无杂交信号,c5和d4均有 35 S和NPT- Ⅱ 杂交信号。c5、d4对应的T1代植株编号分别为14S1-27和14S1-34。结合T1代植株PCR检测结果,可以确定pROK2重组质粒由14S1成功遗传到其自交后代中,14S1为T-DNA插入突变体。
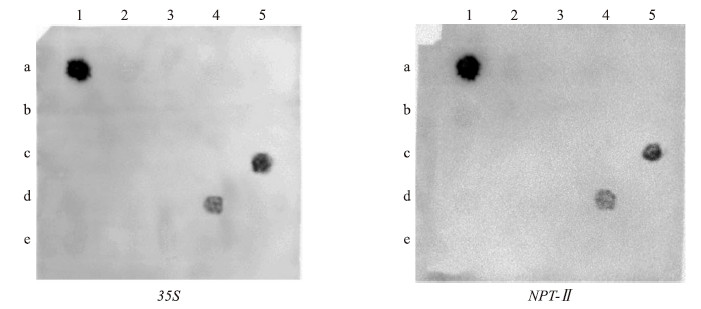 | 图 5 T1代植株斑点杂交检测 Fig. 5 Dot blotting detection of T1 transgenic plants a1:阳性对照 Positive control;a2:阴性对照 Negative control;a3~e5:T1代植株T1 transgenic plants |
在正常的栽培管理条件下,以未转化的‘长春密刺’植株为对照,对14S1自交后代55株单株表型进行观察记录。性状统计调查显示:55株单株的性状与野生型相比并无明显差异,未观察到突变表型。14S1自交后代植株和对照植株在幼苗期和成株期长势均较好,成株期茎粗、节间较短;叶片呈掌状,颜色深绿,同一节位叶片大小基本相同;雌花、雄花颜色均为亮黄色,能正常开花;雌雄株,可育,单性结实能力弱。
3 讨论目前,黄瓜突变体库的构建主要采用物理、化学诱变的方法。李加旺等[18]利用23.22 C·kg-1 60Coγ射线辐射处理具有某些优良特性的黄瓜自交系种子,并在其变异后代群体中筛选出2个综合性状优良的单株;Fraenkel等[19]通过EMS诱变黄瓜获得了大约1 000个M2家系,在苗期发现了植株矮化、子叶自发病变、黄叶、白化苗、叶片卷曲、窄型黑色子叶等表型突变。但传统的物理、化学诱变方法存在突变位点多、突变体复杂以及突变基因克隆困难等缺点,T-DNA插入突变则具有插入随机且多为单拷贝、遗传稳定、能对目标基因进行快速定位并确定其功能等优点。本研究将T-DNA插入突变应用于黄瓜突变体库构建中,对获得的转化植株T0和T1代进行PCR和斑点杂交检测,确定14S1为插入突变体,证明了T-DNA插入突变在黄瓜中应用的可行性,对黄瓜突变体库构建和黄瓜功能基因组学研究具有重要意义,并可为葫芦科其他作物相关研究提供有力参考。在下一步研究中将采用与植物表达载体pROK2配套的加接头PCR法[20]对14S1植株插入位点进行分离鉴定。
Alonso等[7]在建立的拟南芥T-DNA插入突变体库中,确定了88 000个T-DNA插入位点,共有21 700个基因被突变。通过T-DNA插入突变体在拟南芥中已经分离克隆到CLA 1 [21]、DWF 4 [22]等30多个基因。在水稻中,我国于2002年完成了国内第1个水稻T-DNA插入突变体库的建立,该突变体库突变体4 500份。可见,T-DNA在拟南芥和水稻上应用已经非常成熟。本研究中获得的插入突变体较少,相对于拟南芥和水稻还有很大差距,主要是因为黄瓜遗传转化还存在效率低、稳定性差的问题。因此要获得大规模黄瓜T-DNA插入突变体还需进一步优化黄瓜遗传转化体系,并且进行大批量的遗传转化工作,获得更多的插入突变体。
T0代转化植株通常为杂合子,根据孟德尔遗传法则,当T-DNA为单拷贝插入时,T0自交后代中有3/4的植株携带T-DNA插入序列,即14S1自交的55株后代中应有40~42株单株可以检测到T-DNA标记。但PCR检测结果显示55个单株中只有12株呈阳性,选取的23个单株进行斑点杂交也仅有2株有杂交信号,这与孟德尔遗传法则不符。分析原因可能有以下两点:一是T-DNA插入影响了黄瓜的正常生殖过程,使其自交后代偏离了正常的分离比例;二是T0代植株可能是嵌合体,其自交后代会出现嵌合体或者非转基因植株,仅嵌合体检测呈阳性。同时PCR结果与斑点杂交结果不一致,推测其原因可能是T1代植株仍旧存在农杆菌污染,所以PCR鉴定出的假阳性转化子较多,也说明了斑点杂交技术较PCR技术检测转基因植株更具准确性。14S2植株由于还未得到自交后代,所以未做进一步的研究。
突变体的表型筛选能为基因功能分析提供重要线索,但本研究得到的插入突变体没有明显的突变表型,其原因主要是由于T-DNA插入自身存在缺陷。当T-DNA插入到无功能的基因区域[5]、功能冗余的基因或者基因家族时[23],就会产生无义突变,无明显突变表型。在拟南芥和水稻的T-DNA插入标签系中,只有10%的标签基因能产生明显的表型变化[24, 25, 26]。黄瓜基因组中存在24%的重复序列[1],所以产生无义突变的概率很大,并且本研究得到的突变体较少。此外,某些插入的基因仅在特定情况下才能表达,在正常生长条件下不表达从而不产生突变[27],Krysan等[28]研究中得到的17个拟南芥突变体在正常生长情况下均未观察到突变表型。本研究的插入突变体是在正常栽培管理条件下种植生长,这种环境可能无法诱导插入基因的表达,因此未产生突变表型。另外,T-DNA插入多为隐性突变,T1代中只有纯合突变体才表现出突变表型。根据孟德尔遗传法则,单拷贝插入时T1代中1/4是纯合突变体,1/2是杂合株,1/4是野生型。但根据斑点杂交检测的结果推断55株T1中纯合突变体极少或近乎没有,这也是观察不到突变表型的可能原因之一。为克服T-DNA插入存在的缺陷,在植物突变体库构建的研究中越来越多的采用激活标签法。激活标签法是对T-DNA插入的改进,其载体携带多聚化的CaMV 35 S增强子,它能使插入附近的基因过表达而产生显性功能获得型突变,在T0代就能观察到突变表型。1992年,Hayashi等[29]首次发现激活标签法并将该技术用于拟南芥基因的分离和鉴定。在今后的黄瓜插入突变体库构建工作中可采用激活标签为插入元件,以克服T-DNA插入存在的缺陷,以便更好、更快地进行黄瓜插入突变体库的构建及黄瓜基因功能的研究工作。
| [1] | Huang S W,Li R Q,Zhang Z H,et al. The genome of the cucumber,Cucumis sativus L.[J]. Nature Genetics,2009,41(12):1275-1281. |
| [2] | Woycicki R,Witkowicz J,Gawronski P,et al. The genome sequence of the North-European cucumber(Cucumis sativus L.)unravels evolutionary adaptation mechanisms in plants[J]. PLoS ONE,2011,6(7):e22728. |
| [3] | The Arabidopsis Genome Initiative. Analysis of the genome sequenceof the flowering plant Arabidopsis thaliana[J]. Nature,2000,408(6814):796-815. |
| [4] | Krysan P J,Young J C,Sussman M R. T-DNA as an insertionalmutagen in Arabidopsis[J]. Plant Cell,1999,11(12):2283-2290. |
| [5] | Azpiroz-Leehan R,Feldmann K A. T-DNA insertion mutagenesisin Arabidopsis:going back and forth[J]. Trends Genet,1997,13(4):152-156. |
| [6] | Jeon J S,Lee S,Jung K H,et al. T-DNA insertional mutagenesisfor functional genomics in rice[J]. Plant Journal,2000,22(6):561-570. |
| [7] | Alonso J M,StepanovaA N,Leisse T J,et al. Genome wide insertional mutagenesis of Arabidopsis thaliana[J]. Science,2003,301(5633):653-657. |
| [8] | An G,Lee S,Kim S H,et al. Molecular genetics using T-DNA in rice[J]. Plant Cell Physiology,2005,46(1):14-22. |
| [9] | Mathews H,Clendennen S K,Caldwell C G,et al. Activation tagging in tomato identifies a transcriptional regulator of anthocyanin biosynthesis,modification,and transport[J]. Plant Cell,2003,15(8):1689-1703. |
| [10] | Zubko E,Adams C J,Macháèková I,et al. Activation tagging identifies a gene from Petunia hybrida responsible for the production of active cytokinins in plants[J]. Plant Journal,2002,29(6):797-808. |
| [11] | Imaizumi R,Sato S,Kameya N,et al. Activation tagging approach in a model legume,Lotus japonicus[J]. Journal of Plant Research,2005,118(6):391-399. |
| [12] | Pérez-Hernández J B,Swennen R,Sági L. Numberand accuracy of T-DNA insertions in transgenic banana(Musa spp.)plants characterized by an improved anchored PCR technique[J]. Transgenic Research,2006,15(2):139-150. |
| [13] | 任海英,方丽,茹水江,等. 抗蔓枯病甜瓜突变体edr2抗病现象的初步研究[J]. 中国农业科学,2009,42(9):3131-3138. Ren H Y,Fang L,Ru S J,et al. A preliminary investigation of a mutant melon plant edr2 on resistance to gummy stem blight[J]. Scientia Agricultura Sinica,2009,42(9):3131-3138(in Chinese with English abstract). |
| [14] | Trulson A J,Simpson R B,Shahin E A. Transformation of cucumber(Cucumis sativus L.)plants with Agrobacterium rhizogenes[J]. Theo Appl Genet,1986,73(1):11-15. |
| [15] | Wang J,Zhang S J,Wang X,et al. Agrobacterium-mediated transformation of cucumber(Cucumis sativus L.)using a sense mitogen-activated protein kinase gene(CsNMAPK)[J]. Plant Cell,Tissue and Organ Culture,2013,113(2):269-277. |
| [16] | Yang X Q,Zhang W W,He H L,et al. Tuberculate fruit gene Tu encodes a C2H2 zinc finger protein that is required for the warty fruit phenotype in cucumber(Cucumis sativus L.)[J]. The Plant Journal,2014,78(6):1034-1046. |
| [17] | Baulcombe D C,Saunders G R,Bevan M W,et al. Expression of biologically active viral satellite RNA from the nuclear genome of transformed plants[J]. Nature,1986,321(6068):446-449. |
| [18] | 李加旺,孙忠魁,杨森,等. 60Coγ射线在黄瓜诱变育种中的应用初报[J]. 中国蔬菜,1997(2):22-24. Li J W,Sun Z K,Yang S,et al. Primary study on the application of60Coγ radiation on cucumber mutation breeding[J]. China Vegetables,1997(2):22-24(in Chinese with English abstract). |
| [19] | Fraenkel R,Kovalski I,Troadec C,et al. A TILLING population forcucumber forward and reverse genetics[C]//Solmaz S,Aras S. Proceedings of the Xth EUCARPIA meeting on genetics and breeding of Cucurbitaceae. Antalya(Turkey),2012:598-603. |
| [20] | Mandel M A,Feldmann K A,Herrera-Estrella L,et al. CLA1,a novel gene required for chloroplast development,is highly conserved in evolution[J]. Plant Journal,1996,9(5):649-658. |
| [21] | Choe S,Dilkes B P,Fujioka S,et al. The DWF4 gene of Arabidopsis encodes a cytochrome P450 that mediates multiple 22α-hydroxylation steps in brassinosteroid biosynthesis[J]. The Plant Cell,1998,10:231-243. |
| [22] | Ronan C O,Jose M A,Christopher J K,et al. An adapter ligation-mediated PCR method for high-throughput mapping of T-DNA inserts in the Arabidopsis genome[J]. Nature Protocols,2007,2(11):2910-2917. |
| [23] | Springer P S. Gene traps:tools for plant development and genomics[J]. The Plant Cell,2000,12:1007-1020. |
| [24] | Feldmann K A. T-DNA insertion mutagenesis in Arabidopsis:mutational spectrum[J]. The Plant Journal,1991,1(1):71-82. |
| [25] | Bouché N,Bouchez D. Arabidopsis gene knockout:phenotypes wanted[J]. Current Opinion Plant Biology,2001,4(2):111-117. |
| [26] | Jeon J S,An G. Gene tagging in rice:a high throughput system for functional genomics[J]. Plant Science,2001,161(2):211-219. |
| [27] | Hirsch R E,Lewis B D,Spalding E P,et al. A role for the AKT1 potassium channel in plant nutrition[J]. Science,1998,280(5365):918-921. |
| [28] | Krysan P J,Young J C,Tax F,et al. Identification of transferred DNA insertions within Arabidopsis genes involved in signal transduction and ion transport[J]. Proc Natl Acad Sci USA,1996,93(15):8145-8150. |
| [29] | Hayashi H,Czaja I,Lubenow H,et al. Activation of a plant gene by T-DNA tagging:auxin-independent growth in vitro[J]. Science,1992,258(5086):1350-1353. |




