文章信息
- 王慧利, 王婧, 孟春花, 李静心, 曹少先. 2015.
- WANG Huili, WANG Jing, MENG Chunhua, LI Jingxin, CAO Shaoxian. 2015.
- 组蛋白H3S10及H3S28磷酸化对小鼠卵母细胞成熟的调控
- Phosphorylation of histone H3S10 and H3S28 regulates oocyte maturation in mouse
- 南京农业大学学报, 38(5): 850-856
- Journal of Nanjing Agricultural University, 38(5): 850-856.
- http://dx.doi.org/10.7685/j.issn.1000-2030.2015.05.022
-
文章历史
- 收稿日期:2014-12-02
组蛋白修饰,如磷酸化、乙酰化、甲基化、核糖基化及泛素化等对基因表达意义重大[1]。组蛋白修饰通过改变染色质结构或影响蛋白复合体与染色质的募集发挥了重要的生物学功能,可调控细胞周期进程、DNA复制和损伤修复及重组等[2, 3, 4]。磷酸化是组蛋白修饰的重要组成部分,哺乳动物卵母细胞中,组蛋白磷酸化可调控减数分裂进程,参与染色体凝集和分离并可影响纺锤体和微管组织中心组装[5, 6]。但总体而言,相关研究多集中于有丝分裂,卵母细胞减数分裂过程中组蛋白磷酸化的研究偏少且部分研究结果间存在矛盾[7]。在猪生发泡(germinal vesicle,GV)期卵母细胞中,Bui等[8]发现,组蛋白H3S10和H3S28均未磷酸化,但Gu等[9]却检测到低水平的H3S10/H3S28磷酸化。Wang等[10]发现,小鼠GV期卵母细胞中,组蛋白H3S10高度磷酸化;与之相反,Swain等[11]在GV期卵母细胞中并未观察到H3S10磷酸化。因此,哺乳动物卵母细胞中组蛋白的磷酸化模式有待明确。
有丝分裂过程中,组蛋白H3磷酸化主要由Aurora激酶家族(Aurora A/B/C)中的Aurora B调控[12]。减数分裂过程中,利用Aurora激酶广谱抑制剂ZM447439处理小鼠卵母细胞后,组蛋白H3S10/H3S28磷酸化消失,染色体及纺锤体发生异常[5, 10],这表明,Aurora激酶同样可调控卵母细胞组蛋白H3的磷酸化并对发育过程产生影响,但研究者从不同角度得到的结果有所不同。在小鼠卵母细胞中,Swain等[13]利用RNA干扰技术下调Aurora A表达后,染色体和纺锤体发生异常,组蛋白H3S10磷酸化下降,但H3S28磷酸化未受影响。而另有研究者[14]发现,过表达Aurora B而非Aurora A或C,可恢复ZM447439处理导致的染色体异常,表明Aurora B而非Aurora A负责小鼠卵母细胞染色体的调控。最近又有序列和功能分析表明:Aurora C与Aurora B非常类似,但Aurora C的稳定性远超Aurora B,并可弥补因Aurora B降解导致的酶活性下降,进而支持小鼠卵母细胞减数分裂和早期胚胎发育[15]。因此,小鼠卵母细胞中,虽然组蛋白磷酸化可能由Aurora激酶调控,但具体哪种酶以何种方式调控并如何影响发育值得进一步研究。
本试验以小鼠卵母细胞为研究对象,经ZM447439处理,通过检测处理后卵母细胞成熟能力、组蛋白磷酸化、染色体及Aurora激酶的变化情况,以期揭示组蛋白H3S10/H3S28磷酸化调控卵母细胞成熟的机制,为深入了解组蛋白修饰的分子机制提供理论基础。
1 材料与方法 1.1 主要材料试验所用ICR小鼠购自南京市青龙山动物繁殖场。孕马血清促性腺激素(PMSG)和人绒毛膜促性腺激素(hCG)购自宁波市三生药业有限公司,成熟培养液中除TCM199购自Gibco公司外,其余成分均购自Sigma公司。组蛋白H3S10磷酸化一抗(Anti-phospho-Histone H3(Ser10)Antibody)和H3S28磷酸化一抗均购自Millipore公司。Aurora激酶磷酸化一抗(P-A/B/C,Phospho-Aurora A(Thr288)/Aurora B(Thr232)/Aurora C(Thr198)(D13A11)XP® Rabbit mAb)购自CST公司,相应FITC标记的二抗均购自Sigma公司。
1.2 试验方法 1.2.1 体内成熟(in vivo maturation,IVO)卵母细胞的获取6~8周龄性成熟雌鼠,每只腹腔注射10 IU的PMSG,46~48 h后,腹腔注射10 IU的hCG,16 h后,脱颈椎法杀鼠,摘除输卵管,置于M2操作液(自制)中,于体视镜下刺破腹部获得处于第2次减数分裂中期(MⅡ)的卵母细胞,即IVO卵母细胞。
1.2.2 体外成熟(in vitro maturation,IVM)卵母细胞获取及培养6~8周龄性成熟雌鼠,腹腔注射10 IU的PMSG后46~48 h,脱颈椎法杀鼠并摘除卵巢,于体视镜下刺破卵泡,收集GV期卵丘卵母细胞复合体(cumulus-oocyte complexs,COCs),经M2操作液充分洗涤后转移到成熟培养液中培养16 h,培养结束后,自培养液中取出COCs,1 mg · mL-1透明质酸酶处理1~2 min,利用合适口径的玻璃口吸管反复吹吸脱去卵丘,随后以第一极体排出为第2次减数分裂中期(MⅡ)标志。成熟培养液为TCM-199添加3.05 mmol · L-1葡萄糖、1 mg · mL-1牛血清白蛋白、0.91 mmol · L-1丙酮酸钠、10 ng · mL-1表皮生长因子、0.5 IU · mL-1促卵泡素、0.5 IU · mL-1促黄体素。培养条件为37 ℃、5% CO2、100%湿度。ZM447439处理试验中,在成熟培养液中添加不同浓度(0、2.5、5、10和20 μmol · L-1)的ZM447439(购自Selleck公司)。
1.2.3 卵母细胞免疫荧光检测自培养液中取出卵母细胞脱去卵丘后,置于体积分数为4%多聚甲醛室温固定1~2 h,然后经体积分数为0.2% Triton X-100(磷酸盐缓冲液PBS稀释)处理10~15 min,经封闭液(PBS含2 mg · mL-1 BSA和体积分数为0.01% Tween-20)处理1 h,然后加一抗(用封闭液1 :200稀释)4 ℃孵育过夜,经PBS充分洗涤后加入二抗(用封闭液1 :200稀释)37 ℃处理2 h,10 μg · mL-1 Hoechst 33342室温染色5 min以标记卵母细胞染色体DNA,染色完毕后充分清洗,最后将卵母细胞压片经荧光显微镜观察结果并采集图片。其中,GV期卵母细胞不经成熟培养液培养,经刺破卵巢收集COCs后,脱去卵丘进行 固定,后续步骤同上所述。采集DNA图片,将DNA染色形态分为两类:一类为NSN(nonsurrounded nucleolus),即细胞核内染色质不环绕核仁;一类为SN(surrounded nucleolus),即细胞核内染色质环绕核仁。具体分类标准见文献[16]。
1.3 数据处理与统计每组试验至少重复3次,每次至少25枚卵母细胞。试验数据利用SPSS 11.5统计软件的ANOVA模块分析。数据先经LSD转换( t 测验)后,进行单因素方差分析。
2 结果与分析 2.1 小鼠卵母细胞成熟期间组蛋白磷酸化的表达模式免疫荧光结果显示,GV及MⅡ期卵母细胞中,组蛋白H3S10均呈现磷酸化状态(图 1)。在GV期,H3S10磷酸化位点与染色质DNA基本重合,NSN构型卵母细胞磷酸化程度弱于SN构型;在MⅡ期,体外成熟(IVM)和体内成熟(IVO)卵母细胞均呈现明显的H3S10磷酸化,其磷酸化位点与染色体DNA重合,中期染色体和极体染色体同时磷酸化。
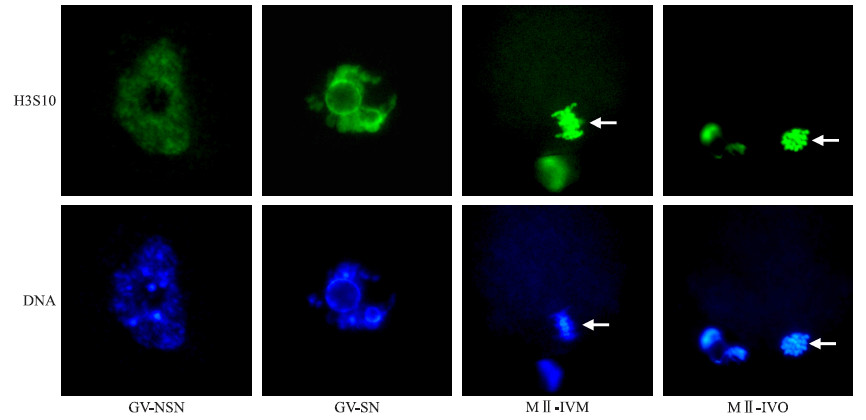 | 图 1 小鼠卵母细胞成熟期间组蛋白H3S10磷酸化的表达模式(×400) Fig. 1 Expression patterns of H3S10 phosphorylation during mouse oocyte maturation 箭头所示为中期染色体,另一团不规则染色体为极体染色体。For the images of MⅡ oocytes,metaphase chromosomes were marked by arrows and the other irregular chromosomes in the same image were the chromosomes of polar bodies.The following figures were same as Fig.1. |
卵母细胞成熟期间组蛋白H3S28磷酸化状态如图 2所示。GV期,与H3S10磷酸化不同,NSN和SN构型卵母细胞H3S28磷酸化位点均遍布细胞核,并在核仁处加重。MⅡ期染色模式与H3S10相同,IVM和IVO卵母细胞均呈现明显的H3S28磷酸化,中期染色体和极体染色体均同时着色。
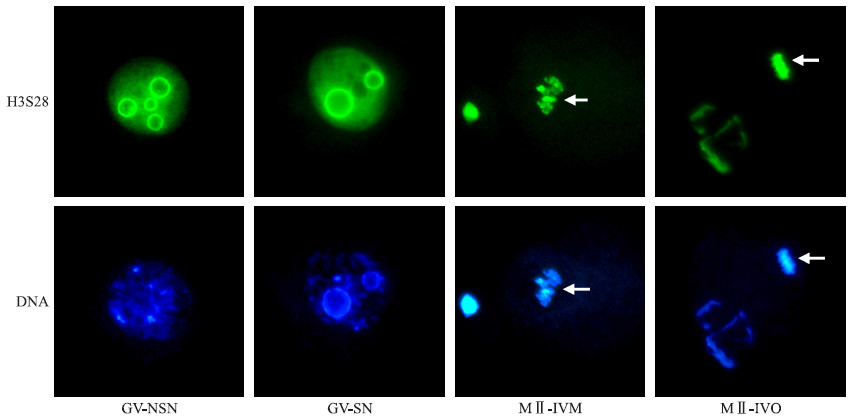 | 图 2 小鼠卵母细胞成熟期间组蛋白H3S28磷酸化的表达模式(×400) Fig. 2 Expression patterns of H3S28 phosphorylation during mouse oocyte maturation |
ZM447439可抑制组蛋白H3磷酸化,因此,在成熟培养液中添加ZM447439可抑制H3磷酸化,以研究组蛋白H3S10/H3S28磷酸化对卵母细胞成熟的影响。结果(表 1)显示:不同浓度ZM447439处理不影响卵母细胞减数分裂恢复[100%生发泡破裂(GVBD)],但对卵母细胞成熟产生浓度依赖性的影响。与对照组相比(0 μmol · L-1),随ZM447439浓度增加,卵母细胞成熟率显著下降,ZM447439浓度为5 μmol · L-1时,成熟率降为48.5%,20 μmol · L-1时,卵母细胞不能成熟。
| ZM447439浓度/(μmol·L-1) Concentration of ZM447439 | 培养卵母细胞数 Number of oocytes cultured | GVBD 比例/% GVBD rate | 成熟率/% MⅡ rate |
| 0 | 87 | 100 | 100a |
| 2.5 | 88 | 100 | 88.7±2.8b |
| 5 | 90 | 100 | 48.5±3.2c |
| 10 | 83 | 100 | 6.9±5.2d |
| 20 | 87 | 100 | 0.0±0.0d |
| 注: 1)GVBD:生发泡破裂Germinal vesicle breakdown; 2)同一列不同字母表示在0.05水平差异显著。The different letters in a column mean significant difference at 0.05 level. | |||
由图 3可见:随ZM447439浓度增加,H3S10磷酸化逐渐减弱,直至消失。与对照组相比(0 μmol · L-1),5 μmol · L-1的ZM447439处理后,H3S10磷酸化明显减弱,20 μmol · L-1处理后,H3S10磷酸化完全消失,表明ZM447439可浓度依赖性地降低卵母细胞体外成熟期间组蛋白H3S10磷酸化的水平。
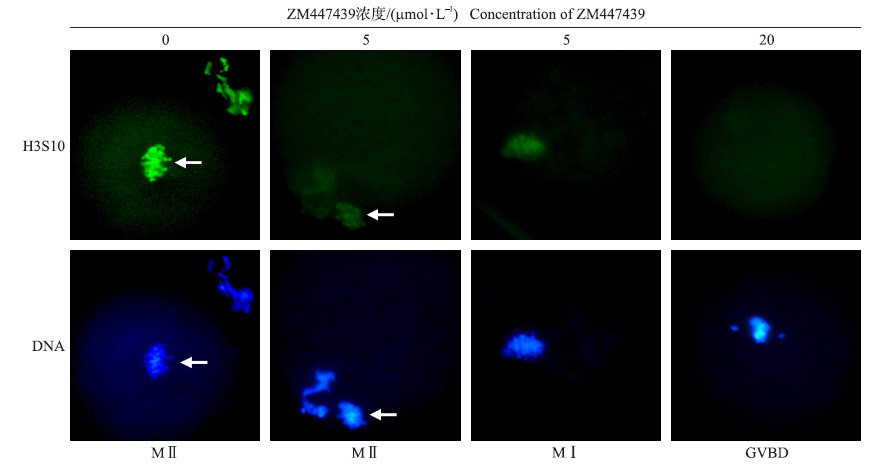 | 图 3 不同浓度ZM447439处理对组蛋白H3S10磷酸化的影响(×400) Fig. 3 Effect of different concentration ZM447439 treatments on H3S10 phosphorylation | |
ZM447439处理同样影响了组蛋白H3S28的磷酸化(图 4),但与H3S10不同,5 μmol · L-1的ZM447439处理后,H3S28磷酸化即完全消失,表明组蛋白H3中不同的磷酸化位点对ZM447439的敏感性存在差异。
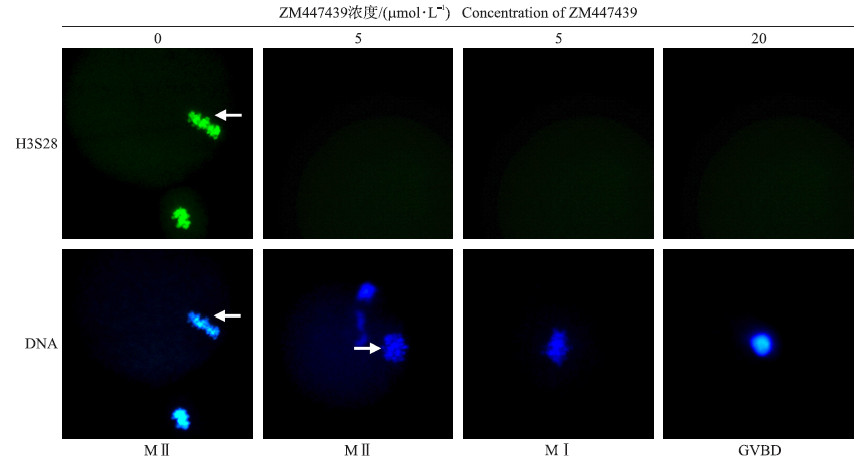 | 图 4 不同浓度ZM447439处理对组蛋白H3S28磷酸化的影响(×400) Fig. 4 Effect of different concentration ZM447439 treatments on H3S28 phosphorylation | ||
与对照组相比(0 μmol · L-1),5 μmol · L-1的ZM447439处理后,约半数卵母细胞仍可成熟,到达MⅡ期(表 1),另半数卵母细胞则停滞在MⅠ期。如图 3及图 4所示:染色体具有MⅡ和MⅠ两种形态,MⅡ期染色体形态正常,并且具有完整的极体;MⅠ期染色体排列也无明显异常。但当ZM447439浓度增加到20 μmol · L-1后,染色体形态明显异常,凝集成不规则的团块状。
2.3.3 ZM447439处理后小鼠卵母细胞Aurora激酶磷酸化状态的变化如图 5所示:对照组中(0 μmol · L-1),Aurora激酶磷酸化(P-A/B/C)位点主要定位于中期染色体和纺锤体两极。5 μmol · L-1的ZM447439处理组中,Aurora激酶存在两种磷酸化形态,MⅡ期卵母细胞磷酸化形态与对照组相似(MⅡ),而MⅠ期卵母细胞中,磷酸化集中于纺锤体两极,中期染色体位置磷酸化消失(MⅠ)。20 μmol · L-1处理组中,也存在两种磷酸化形态,一种集中于纺锤体两极(GVBD-1),另一种磷酸化发生紊乱,除在纺锤体两极外,胞质中也有分布(GVBD-2)。
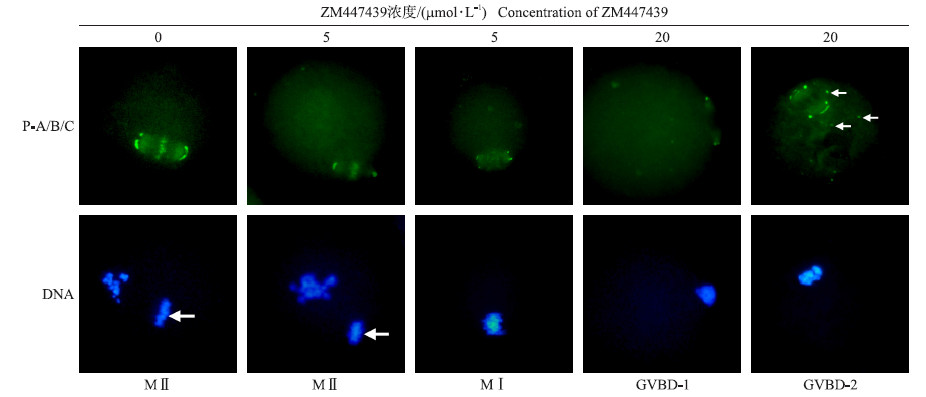 | 图 5 不同浓度ZM447439处理对Aurora激酶磷酸化(P-A/B/C)的影响(×400) Fig. 5 Effect of different concentration ZM447439 treatments on phosphorylation of Aurora kinases(P-A/B/C) | |||
核心组蛋白在N末端结构域均含有磷酸化受体位点,组蛋白H2A和H4的磷酸化位点为丝氨酸1,H2B为丝氨酸14/32,H3为丝氨酸10/28及苏氨酸3/11[17, 18, 19],哺乳动物卵母细胞中,H3S10/H3S28是研究最为广泛的2个组蛋白磷酸化位点[6]。本研究中,组蛋白H3S10/H3S28在小鼠卵母细胞减数分裂过程中一直处于磷酸化状态,与Wang等[10]的研究结果一致,但Swain等[11]在GV期小鼠卵母细胞中未检测到H3S10磷酸化,H3S10磷酸化发生在GVBD后。GV期,即第1次减数分裂的双线期,与有丝分裂的G2期相当,而在同为G2期的小鼠早期胚胎中,H3S10发生磷酸化[7],这一结果可能具有一定的参考价值。因此,我们推测,GV期小鼠卵母细胞中的H3S10发生磷酸化。Swain等[11]得到的不同结果可能与小鼠品系或所用抗体有关。
Aurora激酶是一个丝氨酸/苏氨酸蛋白激酶家族,包括Aurora A/B/C 3种,在细胞周期调控中作用重大[20]。ZM447439是Aurora激酶的广谱抑制剂,ZM447439处理可降低小鼠卵母细胞成熟率,组蛋白H3S10/H3S28磷酸化消失[5],本研究证实了这一结论。进一步研究发现,ZM447439处理可浓度依赖性地导致H3S10/H3S28磷酸化消失及染色体排列异常。其中,5 μmol · L-1的ZM447439处理可导致H3S10磷酸化减弱,20 μmol · L-1处理后磷酸化消失,而对于H3S28,5 μmol · L-1处理即可导致磷酸化消失。与此同时,5 μmol · L-1处理后,约半数染色体停滞在MⅠ期,排列方式尚无明显异常,但经20 μmol · L-1处理后,染色体均凝集成团。上述结果表明,H3S10/H3S28两个磷酸化位点及染色体的调控可能存在差异。
有丝分裂过程中,组蛋白H3磷酸化主要由Aurora B调控[12],卵母细胞减数分裂过程中,Aurora激酶同样参与了组蛋白H3磷酸化的调控及染色体的排列和分离[6],但具体到小鼠卵母细胞,究竟是Aurora激酶家族中的哪一个激酶调控了组蛋白H3磷酸化和染色体形态尚有争议[13, 14, 15]。ZM447439通过抑制Aurora激酶的活性进而调控组蛋白的磷酸化,体细胞中,ZM447439对Aurora激酶A/B/C的半抑制浓度分别为1 000、50 和250 nmol · L-1[21];卵母细胞中,可能同样存在浓度依赖性地对激酶种类的抑制。据此,H3S28/H3S10磷酸化及染色体形态有可能分别由不同的Aurora激酶所调控,浓度不同的ZM447439处理分别抑制了不同的Aurora激酶活性,由此导致磷酸化消失及染色体异常的浓度依赖性变化。
Aurora激酶主要由调控结构域和催化结构域组成,其酶活性受磷酸化调节,催化结构域中苏氨酸(Threonine,Thr)残基上的磷酸化对激酶活性的调节至关重要,Aurora激酶A/B/C的活性分别由Thr288/Thr232/Thr198位点的磷酸化调控[22, 23, 24]。关于组蛋白H3磷酸化对卵母细胞成熟事件的影响,研究者主要从两个方面进行了研究,一是利用抑制剂ZM447439处理,引起组蛋白磷酸化消失并研究相关成熟事件的变化[5, 10];二是利用特异性siRNA下调Aurora激酶的蛋白表达,进而检测下调后成熟事件的变化[13, 14]。从Aurora激酶家族自身磷酸化的角度研究ZM447439处理与卵母细胞成熟事件的关联,目前尚未见报道。本研究发现:经ZM447439处理,Aurora激酶A/B/C的磷酸化状态发生改变,随药物浓度增加,磷酸化开始消失或发生紊乱,这与卵母细胞成熟率下降、组蛋白磷酸化消失及染色体排列异常等成熟事件相对应,为组蛋白磷酸化调控的研究提供了一个新的视角。
| [1] | de La Fuente R. Chromatin modifications in the germinal vesicle(GV)of mammalian oocytes[J]. Dev Biol,2006,292(1):1-12 |
| [2] | Wu J,Grunstein M. 25 years after the nucleosome model:chromatin modifications[J]. Trends Biochem Sci,2000,25(12):619-623 |
| [3] | Kouzarides T. Chromatin modifications and their function[J]. Cell,2007,128(4):693-705 |
| [4] | Wolffe A P,Hayes J J. Chromatin disruption and modification[J]. Nucleic Acids Res,1999,27(3):711-720 |
| [5] | Swain J E,Ding J,Wu J,et al. Regulation of spindle and chromatin dynamics during early and late stages of oocyte maturation by aurora kinases[J]. Mol Hum Reprod,2008,14(5):291-299 |
| [6] | Gu L,Wang Q,Sun Q Y. Histone modifications during mammalian oocyte maturation:dynamics,regulation and functions[J]. Cell Cycle,2010,9(10):1942-1950 |
| [7] | Teperek-Tkacz M,Meglicki M,Pasternak M,et al. Phosphorylation of histone H3 serine 10 in early mouse embryos:active phosphorylation at late S phase and differential effects of ZM447439 on first two embryonic mitoses[J]. Cell Cycle,2010,9(23):4674-4687 |
| [8] | Bui H T,van Thuan N,Kishigami S,et al. Regulation of chromatin and chromosome morphology by histone H3 modifications in pig oocytes[J]. Reproduction,2007,133(2):371-382 |
| [9] | Gu L,Wang Q,Wang C M,et al. Distribution and expression of phosphorylated histone H3 during porcine oocyte maturation[J]. Mol Reprod Dev,2008,75(1):143-149 |
| [10] | Wang Q,Wang C M,Ai J S,et al. Histone phosphorylation and pericentromeric histone modifications in oocyte meiosis[J]. Cell Cycle,2006,5(17):1974-1982 |
| [11] | Swain J E,Ding J,Brautigan D L,et al. Proper chromatin condensation and maintenance of histone H3 phosphorylation during mouse oocyte meiosis requires protein phosphatase activity[J]. Biol Reprod,2007,76(4):628-638 |
| [12] | Hsu J Y,Sun Z W,Li X,et al. Mitotic phosphorylation of histone H3 is governed by Ipl1/aurora kinase and Glc7/PP1 phosphatase in budding yeast and nematodes[J]. Cell,2000,102(3):279-291 |
| [13] | Swain J E,Ding J,Filipiak W,et al. Aurora kinase-A regulates oocyte spindle organization during early stages of meiosis[J]. Biol Reprod,2009,81(Suppl 1):29 |
| [14] | Shuda K,Schindler K,Ma J,et al. Aurora kinase B modulates chromosome alignment in mouse oocytes[J]. Mol Reprod Dev,2009,76(11):1094-1105 |
| [15] | Schindler K,Davydenko O,Fram B,et al. Maternally recruited Aurora C kinase is more stable than Aurora B to support mouse oocyte maturation and early development[J]. Proc Natl Acad Sci USA,2012,109(33):E2215-E2222 |
| [16] | Tan J H,Wang H L,Sun X S,et al. Chromatin configurations in the germinal vesicle of mammalian oocytes[J]. Mol Hum Reprod,2009,15(1):1-9 |
| [17] | Sarmento O F,Digilio L C,Wang Y,et al. Dynamic alterations of specific histone modifications during early murine development[J]. J Cell Sci,2004,117(Pt 19):4449-4459 |
| [18] | Polioudaki H,Markaki Y,Kourmouli N,et al. Mitotic phosphorylation of histone H3 at threonine 3[J]. FEBS Lett,2004,560(1/2/3):39-44 |
| [19] | Preuss U,Landsberg G,Scheidtmann K H. Novel mitosis-specific phosphorylation of histone H3 at Thr11 mediated by Dlk/ZIP kinase[J]. Nucleic Acids Res,2003,31(3):878-885 |
| [20] | Saskova A,Solc P,Baran V,et al. Aurora kinase A controls meiosisⅠprogression in mouse oocytes[J]. Cell Cycle,2008,7(15):2368-2376 |
| [21] | Girdler F,Gascoigne K E,Eyers P A,et al. Validating Aurora B as an anti-cancer drug target[J]. J Cell Sci,2006,119(17):3664-3675 |
| [22] | Fu J,Bian M,Jiang Q,et al. Roles of Aurora kinases in mitosis and tumorigenesis[J]. Mol Cancer Res,2007,5(1):1-10 |
| [23] | Yasui Y,Urano T,Kawajiri A,et al. Autophosphorylation of a newly identified site of Aurora-B is indispensable for cytokinesis[J]. J Biol Chem,2004,279(13):12997-13003 |
| [24] | Ohashi S,Sakashita G,Ban R,et al. Phospho-regulation of human protein kinase Aurora-A:analysis using anti-phospho-Thr288 monoclonal antibodies[J]. Oncogene,2006,25(59):7691-7702 |
 2015, Vol. 38
2015, Vol. 38


