文章信息
- 邹彩连, 赵国成, 蒋翊宸, 林栋青, 顾向阳. 2015.
- ZOU Cailian, ZHAO Guocheng, JIANG Yichen, LIN Dongqing, GU Xiangyang. 2015.
- 具有自絮凝特性的乙酸降解菌的筛选及其降解特性
- Screening of a flocculent acetic acid degrading bacterium and its degradative characteristics
- 南京农业大学学报, 38(5): 830-837
- Journal of Nanjing Agricultural University, 38(5): 830-837.
- http://dx.doi.org/10.7685/j.issn.1000-2030.2015.05.019
-
文章历史
- 收稿日期:2015-03-31
2. 建湖县农业技术推广服务中心, 江苏 盐城 224700
2. Service Center for Popularization of Agrotechnique of Jianhu County, Yancheng 224700, China
液态聚硫橡胶是一种应用十分广泛的特种合成橡胶品种,工业上多以二氯乙基缩甲醛与多硫化钠缩聚生成。在液态聚硫橡胶生产过程中会产生大量的工艺废水,其主要污染物有Na2S2O3、NaCl、Na2SO4及少量的乙酸和环硫醚类化合物,是一种典型的高盐含硫废水[1, 2]。硫胶废水的化学需氧量(COD)质量浓度高达8 000mg·L-1,氯离子质量浓度高达17 000mg·L-1,由于其盐度高,生物毒性大,不经治理直接排放必然造成严重的环境污染。
在硫胶废水中硫代硫酸盐所引起的COD占80%以上,因此硫代硫酸盐的氧化是硫胶废水处理的关键。国内外已报道的处理方法有化学氧化法和生物氧化法两类。化学氧化法对硫代硫酸盐有较好的氧化效果,但是氯气和次氯酸钠等化学氧化剂对设备有较强的腐蚀性,再加上药剂的投加量大,处理成本高,故尚未见工程应用[2]。目前,其工程化治理主要依赖于化能自养型硫杆菌的生物氧化法,其优点是无需添加化学药剂,运行成本较低。例如:我国锦西化工研究院采用四级串联曝气池处理硫胶废水,COD去除率达90%,其优势菌种为Thiobacillus thioparus和Acidithiobacillus thiooxidans[2];林栋青等[3]将优势菌种Halothiobacillus sp.TX应用于硫胶废水处理工程获得成功,S2O2-3去除率可达100%。然而,自养型硫杆菌具有对小分子有机酸敏感的特性,研究显示乙酸的质量浓度高于250mg·L-1时可对硫杆菌的生长产生强烈的抑制作用,从而造成硫胶废水处理工程中硫代硫酸盐氧化速率较低,水力停留时间较长的现象[4, 5, 6]。如果能将硫胶废水中的乙酸先行去除,解除乙酸对硫杆菌的抑制作用,可望缩短停留时间,降低工程运行成本。考虑到游离生长的菌种在反应器中难以保持,而且硫胶废水含有较高的盐度不利于活性污泥的生物絮凝,因此本研究目的在于分离耐盐絮凝细菌降解硫胶废水中的乙酸,以期利用其解除乙酸对化能自养型硫细菌的抑制作用,加快硫胶废水中硫代硫酸盐的生物氧化,为硫胶废水的工程化处理积累菌种资源。
1 材料与方法 1.1 硫胶废水硫胶废水取自江苏省泰兴市某化学有限公司污水处理站配水罐,其主要污染物的成分及其质量浓度分别为:S2O32-离子4 015mg·L-1,乙酸1 067mg·L-1,NaCl 18.67g·L-1。
1.2 试验菌种及其培养基硫代硫酸盐氧化细菌Halothiobacillus sp.TX为本实验室保存菌株,其种子液制备采用硫代硫酸钠矿物盐培养基:Na2S2O3 8.47g·L-1,NaCl 20g·L-1,NH4Cl 0.25g·L-1,MgSO4·7H2O 0.25g·L-1,K2HPO4 0.25g·L-1,pH 4.5[3]。絮凝细菌分离自江苏省射阳市某地盐碱土,其菌种分离及种子液制备均采用乙酸矿物盐培养基:CH3COOH 1.8g·L-1,NaCl 30g·L-1,NH4Cl 0.25g·L-1,MgSO4·7H2O 0.25g·L-1,K2HPO4 0.25g·L-1,pH 8.5。
絮凝细菌的分离方法如下:在250 mL三角瓶中加入100 mL硫胶废水和3 g土样,置于30 ℃、170r·min-1摇床培养,定期取样测定培养液中乙酸的质量浓度,待乙酸完全降解后,将所得富集液进行梯度稀释并涂布于乙酸培养基平板,30 ℃培养3 d,从平板上挑取单菌落划线纯化后,接种至乙酸培养基摇瓶培养,将具有絮凝性能的菌种制成斜面置4 ℃冰箱保存备用。
1.3 絮凝细菌的形态学特征及生理生化特性的测定分离菌株在固体平板上的菌落形态及液体培养基中的絮体形态均采用体视显微镜观察,细胞形态采用扫描电镜观察并用数码相机照相。革兰氏染色及各种生理生化特性的测定按照文献[7]进行。碳源谱通过摇瓶试验测定,将分离菌种以10%(体积分数)接种量接种于含有相应碳源的液体培养基中,于30 ℃、170r·min-1摇床培养24 h,取样测定培养液中总菌体蛋白和游离生长的菌体蛋白的质量浓度,计算絮凝指数(FI)。FI=(总菌体蛋白-游离生长的菌体蛋白)/总菌体蛋白×100%。式中:游离生长的菌体蛋白是指培养液静置沉淀30 min后上层悬浮液中的菌体蛋白的质量浓度。将摇瓶培养的细菌絮体浓缩至2g·L-1,加入到250 mL量筒中测定沉降曲线,同时以等浓度的普通活性污泥为对照,以30g·L-1的NaCl溶液为沉淀介质测定其沉降曲线,比较两者的沉降性能。
1.4 分离菌种的16S rDNA序列鉴定用无菌牙签从乙酸培养基平板上挑取少量幼嫩菌体直接进行16S rDNA序列扩增,用于PCR扩增的正向引物为5′-AGAGTTTGATCCTGGCTCA-3′,反向引物为5′-GGTTACCTTGTTACGACTT-3′[8]。扩增体系为:灭菌双蒸水34 μL,10×PCR Buffer 5 μL,MgCl2(25 mmol·L-1)3 μL,dNTPs(2.5 mmol·L-1)5 μL,引物(25 pmol·μL-1)各1 μL,Taq DNA聚合酶(2.5 U·μL-1)1 μL。扩增程序:94 ℃ 2 min;94 ℃ 30 s,52 ℃ 30 s,72 ℃ 1 min,30个循环;72 ℃ 20 min。扩增产物送上海英骏生物技术有限公司测序,测定所得序列递交到GenBank,采用MEGA 5软件同数据库中已有的16S rDNA序列进行相似性比较,构建系统发育树。
1.5 分离菌株的降解特性研究通过一系列摇瓶试验研究温度、起始pH、盐浓度及底物浓度等因素对分离菌株降解性能的影响,各参 数的试验范围分别为温度20~45 ℃,初始pH 6~10,NaCl质量浓度0~150g·L-1,底物质量浓度1~12g·L-1。试验在500 mL三角摇瓶中进行,各三角瓶均含有180 mL乙酸培养基和20 mL种子液,除温度试验外均置于30 ℃摇床中培养,培养过程中每隔2 h取样2 mL,离心沉淀菌体,上清液用于乙酸质量浓度的测定。
1.6 分离菌株在硫胶废水中的降解性能及其对硫代硫酸盐生物氧化的影响向500 mL三角瓶中加入180 mL硫胶废水,接入6 g絮凝细菌的湿菌体(折合菌体干质量为1.6g·L-1),混匀后置于30 ℃、170r·min-1摇床培养,定期取样测定硫胶废水中乙酸的质量浓度,计算降解速率。待乙酸完全降解后将培养液过滤除去细菌絮体,取135 mL滤液加入500 mL三角瓶,另取1个500 mL三角瓶加入135 mL硫胶废水原水作为对照,然后接入15 mL活化培养的Halothiobacillus sp.TX菌株,并将混合液的起始pH调节至4.5,置于30 ℃、170r·min-1摇床培养,定时取样测定培养液pH值及硫代硫酸根的质量浓度,比较硫代硫酸盐的降解速率。
1.7 取样与分析方法为了避免细菌絮体的沉淀,从三角摇瓶中取样时须在轻轻摇动中均匀吸取菌液,然后将菌液离心沉淀菌体,沉淀部分用0.5 mol·L-1 NaOH溶液溶解后用于菌体蛋白的测定,上清液用于乙酸或硫代硫酸盐的测定。采用Folin酚试剂法[9]测定菌体蛋白的质量浓度,采用比色法[10]测定乙酸的质量浓度,采用碘量法[11]测定硫代硫酸盐的质量浓度,采用比色法[12]测定硫酸根离子的质量浓度。采用加热法[13]提取细菌的胞外聚合物,采用蒽酮比色法[14]测定提取液中的多糖含量,采用Folin酚试剂法[9]测定蛋白含量。
2 结果与分析 2.1 菌株SS1的形态学特征从盐碱土中分离到1株具有絮凝生长特性的细菌SS1,该菌株在乙酸培养基上形成淡黄色、不规则的菌落。菌落初期呈一层薄薄的且颜色较浅的菌膜,易挑起;随着培养时间延长菌落中心明显隆起,表面凹凸不平,菌落边缘紧紧黏附在培养基表面,难挑起。菌株SS1为革兰氏阴性的短杆状细胞,大小2.08 μm×0.62 μm,不产芽孢,在电镜下可见细胞呈聚集生长,细胞之间有胞外聚合物黏连。在液体培养基中菌株SS1呈絮状生长,静置时其絮体可自由沉降,培养液静置沉淀30 min后上部悬浮液较清澈(图 1)。从图 2可以看出:SS1絮体的沉降速率明显高于活性污泥,静置沉降10 min后即进入压缩区,而普通活性污泥沉降较慢,静置沉降60 min后才进入压缩区。经计算沉降30 min时SS1絮体的沉降体积指数(SVI)为172mL·g-1,明显低于活性污泥的SVI(292mL·g-1),说明在30g·L-1的盐水中SS1絮体较普通活性污泥具有更为出色的沉降性能。
 | 图 1 菌株SS1的细胞形态(A)及其在液体培养基中形成的絮体形态(B) Fig. 1 Morphology of the cells(A)of strain SS1 and the flocs formed in liquid medium(B) |
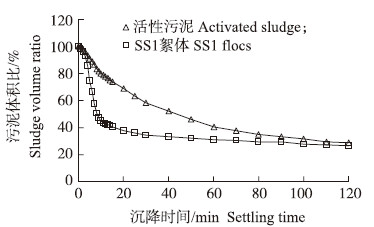 | 图 2 SS1絮体与普通活性污泥的沉降性能比较 Fig. 2 Comparison of the settling properties of SS1 flocs and conventional activated sludge |
研究了菌株SS1对50种碳源物质的利用情况。从表 1可知:该菌株能利用的碳源较多,但不能以蔗糖、乳糖、半乳糖、木糖、阿拉伯糖、核糖、甲醇、异丙醇、山梨醇、甲酸、草酸、甲硫氨酸、赖氨酸、苏氨酸、苯丙氨酸、半胱氨酸、丝氨酸、组氨酸和色氨酸为唯一碳源进行生长。菌株SS1利用不同碳源物质生长时都具有明显的絮凝生长的特点,絮凝指数介于32.32%~98.40%之间,平均絮凝指数为76.36%,说明絮凝生长是该菌株固有的生物学特性。碳源物质的种类对絮凝指数有一定的影响,其中利用果糖、麦芽糖、乙醇、丙三醇、天冬酰胺和异戊酸为碳源生长时絮凝指数最高达90%以上,利用葡萄糖、纤维二糖、淀粉、异戊醇、乙酸、丙酸、丁酸、谷氨酸、谷氨酰胺、脯氨酸、酪氨酸和缬氨酸为碳源生长时絮凝指数为80%~89%,利用异丁酸、白氨酸、异亮氨酸、丙氨酸、甘氨酸和蛋白胨为碳源生长时絮凝指数为70%~79%,利用正丁醇、天冬氨酸和酵母粉为碳源生长时絮凝指数为60%~69%,利用乙二醇、戊酸、乳酸和柠檬酸为碳源生长时絮凝指数低于60%。
| 碳源Carbon source | 菌体蛋白/(mg·L -1)Cellular protein | 絮凝指数/%Flocculent index | 碳源Carbon source | 菌体蛋白/(mg·L -1)Cellular protein | 絮凝指数/%Flocculent index | |
| 葡萄糖Glucose | 179.15 | 87.69 | 乳酸Lactic acid | 93.34 | 55.35 | |
| 果糖Fructose | 175.16 | 91.40 | 柠檬酸Citric acid | 110.63 | 57.22 | |
| 麦芽糖Maltose | 169.18 | 97.97 | 谷氨酸Glutamate | 119.28 | 88.76 | |
| 纤维二糖Cellubiose | 67.23 | 82.18 | 谷氨酰胺Glutamine | 103.32 | 82.19 | |
| 淀粉Starch | 164.52 | 81.54 | 脯氨酸Proline | 96.00 | 82.57 | |
| 乙醇Ethanol | 113.30 | 90.52 | 酪氨酸Tyrosine | 101.99 | 84.25 | |
| 乙二醇Ethylene glycol | 116.62 | 32.32 | 白氨酸Leucine | 73.38 | 73.12 | |
| 丙三醇Glycerol | 92.67 | 98.10 | 天冬氨酸Aspartic acid | 60.74 | 67.52 | |
| 正丁醇Butyl alcohol | 89.35 | 65.26 | 天冬酰胺Asparagine | 59.41 | 91.43 | |
| 异戊醇Isoamyl alcohol | 80.70 | 80.50 | 异亮氨酸Isoleucine | 67.39 | 72.70 | |
| 乙酸Acetic acid | 113.30 | 86.41 | 丙氨酸Alanine | 59.41 | 78.55 | |
| 丙酸Propionic acid | 98.66 | 80.34 | 甘氨酸Glycine | 53.42 | 78.64 | |
| 丁酸Butyric acid | 107.97 | 80.50 | 缬氨酸Valine | 68.72 | 80.98 | |
| 异丁酸Isobutyric acid | 96.99 | 77.18 | 酵母粉Yeast extract | 218.40 | 61.73 | |
| 戊酸Valeric acid | 75.38 | 34.11 | 蛋白胨Peptone | 74.57 | 71.47 | |
| 异戊酸Isovaleric acid | 89.35 | 98.40 | ||||
| 注:菌体生长量以培养24 h时细胞蛋白浓度表示,培养基起始时菌体蛋白含量约为17 mg · L -1。Note: Bacterial growth was expressed as the cellular protein after 24 h incubation.Initial concentration of cellular protein in the medium was around 17 mg · L -1. | ||||||
菌株SS1对明胶液化试验、吲哚试验、甲基红试验和石蕊牛乳试验均为阴性,过氧化氢酶试验、淀粉水解试验、乙酰甲基甲醇试验和产硫化氢试验结果均呈阳性。菌株SS1不能发酵葡萄糖、麦芽糖和果糖生长,但能以硝酸盐为电子受体通过无氧呼吸获得能量进行生长,因此为兼性好氧细菌。
将新鲜的SS1菌体直接加入PCR扩增体系,以细菌16S rDNA基因通用引物进行PCR扩增并进行测序,得到1 558 bp的片段,将测序结果提交至GenBank(登录号为KP257571),与GenBank中其他菌株的16S rDNA进行相似性比较,并构建系统发育树(图 3)。结果显示:SS1菌株与Pseudomonas属中各种的相似度为97%~99%,与Pseudomonas stutzeri的相似性最高达99%,按照目前普遍接受的聚类标准,当一个分离菌株同参考菌株16S rDNA同源性大于97%时,可归为相同的属,因此根据上述16S rDNA序列同源性比对结果,将菌株SS1初步鉴定为假单胞菌属的一个种,并命名为Pseudomonas sp.SS1。
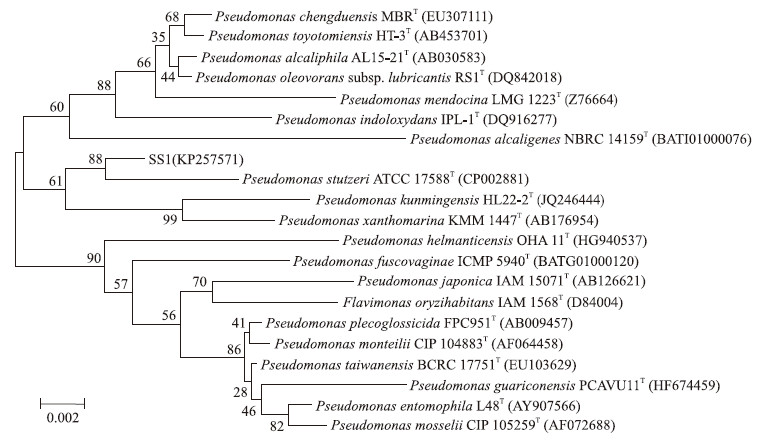 | 图 3 菌株SS1基于16S rDNA基因序列同源性构建的系统发育树 Fig. 3 Phylogenetic tree of strain SS1 based on the 16S rDNA gene homology |
图 4-A的结果显示:在不同的培养温度下,培养基中乙酸的质量浓度均呈持续下降趋势,而培养温度对其降解速率有显著影响。菌株SS1生长及降解乙酸的最适温度为35 ℃,此时平均降解速率最高达100mg·L-1·h-1,18 h乙酸即可完全降解。超过或低于35 ℃时乙酸降解速率明显下降,乙酸完全降解所需的时间也明显延长。例如,当培养温度上升至40 ℃时,其降解速率下降为69.23mg·L-1·h-1,完全降解的时间延长为26 h;而继续升至45 ℃时,培养基中的乙酸质量浓度只在前4 h内有细微下降,随后乙酸的质量浓度基本不变,说明在此温度下菌株SS1的降解活性被完全抑制。另一方面,当培养温度下降为30和25 ℃时,其降解速率分别下降为81.82和69.23mg·L-1·h-1,完全降解所需的时间分别延长为22和26 h,而当培养温度继续下降至20 ℃时,其降解速率只有52.94mg·L-1·h-1,需培养34 h才能完全降解。
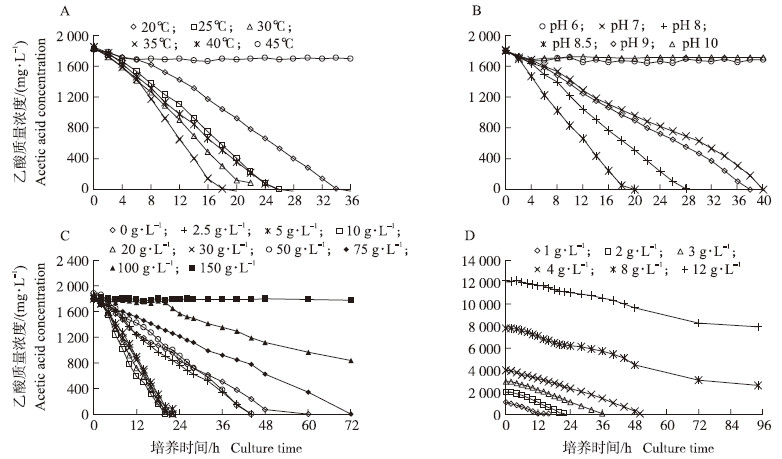 | 图 4 菌株SS1的降解特性 Fig. 4 Degradative characteristics of strain SS1 影响因素分别为:温度(A)、培养基起始pH值(B)、氯化钠质量浓度(C)和底物质量浓度(D)。Influential factors were:temperature(A),initial medium pH value(B),NaCl concentration(C)and substrate concentration(D),respectively. |
图 4-B的结果显示:菌株SS1不能在pH 6和pH 10的培养基中生长和降解乙酸,只有在pH 7~9之间有明显生长,在此pH值范围内培养基的起始pH值对菌株SS1的乙酸降解速率有明显影响。菌株SS1降解乙酸的最适pH值为8.5,此时其平均降解速率最高达100mg·L-1·h-1,培养18 h即可完全降解。当起始pH值下降至pH 8和pH 7时,其降解速率分别下降为64.29和45.00mg·L-1·h-1,完全降解所需的时间分别延长至28和40 h;而当起始pH值上升至9时,其降解速率下降为47.37mg·L-1·h-1,完全降解所需的时间延长为38 h。总的来看,菌株SS1适宜的pH值范围为8~8.5。
从图 4-C可以看出:菌株SS1可以适应0~100g·L-1 NaCl并以乙酸为唯一碳源生长,但NaCl的质量浓度对菌株SS1的降解活性有很大影响。当NaCl质量浓度为5~30g·L-1时,菌株SS1对乙酸的降解速率最高,此时乙酸的降解无明显延滞期,平均降解速率介于81.82~90.00mg·L-1·h-1之间,并于20~22 h内可完全降解。当NaCl的质量浓度高于该浓度范围时,乙酸降解速率开始逐渐下降。例如:当NaCl质量浓度提高至50和75g·L-1时,乙酸降解速率分别下降至40.91和25.00mg·L-1·h-1,其完全降解分别需要44和72 h,说明高浓度的盐分对菌株SS1的活性开始产生抑制作用,当NaCl质量浓度提 高至100g·L-1时菌株SS1受到的抑制作用更强,甚至出现了20 h的延滞期,之后才开始以17.37mg·L-1·h-1 的速率缓慢降解,试验结束时乙酸降解率仅为53.35%。而当NaCl质量浓度提高到150g·L-1时,整个试验期内无明显降解,菌株SS1的菌体活性已被完全抑制。另一方面,较低的盐分浓度也导致乙酸降解速率的 下降,例如:当NaCl质量浓度下降至2.5和0g·L-1时其乙酸降解速率分别下降至40.91和37.50mg·L-1·h-1,其完全降解分别需要44和48 h,这说明菌株SS1是嗜盐型菌株,一定质量浓度NaCl的存在对于维持SS1正常的生长与代谢活动是必不可少的。
图 4-D示不同底物浓度下菌株SS1对乙酸的降解曲线。结果显示:当乙酸质量浓度小于等于4g·L-1时,其平均降解速率差别不大(80.00~90.91mg·L-1·h-1),但乙酸完全降解所需的时间随底物质量浓度的提高而逐渐延长,当培养基中乙酸的起始质量浓度为1、2、3和4g·L-1时,乙酸完全降解所需的时间分别为12、22、36和50 h。当乙酸的质量浓度高于4g·L-1时,菌株SS1降解乙酸的能力有所下降。例如:当乙酸的质量浓度达8g·L-1时,较高浓度的乙酸对SS1的活性产生抑制作用,乙酸降解速率出现下降趋势。48 h之前乙酸平均降解速率为73.04mg·L-1·h-1,48~96 h内乙酸的平均降解速率降为57.07mg·L-1·h-1,之后仅为18.28mg·L-1·h-1,培养至第8天时乙酸才完全降解。当乙酸的质量浓度进一步增加至12g·L-1时对菌株SS1的抑制作用更强,乙酸降解速率同样出现下降趋势。例如:72 h内乙酸平均降解速率为51.43mg·L-1·h-1,72~96 h内乙酸的平均降解速率降为32.18mg·L-1·h-1,96~120 h内乙酸的平均降解速率降为9.90mg·L-1·h-1,之后乙酸的质量浓度再无明显下降,乙酸总降解率仅39.28%,说明菌株SS1已失去活性,因此不能将乙酸完全降解。
2.5 菌株SS1对硫胶废水中乙酸及硫代硫酸盐生物降解的影响将离心浓缩的SS1絮体接种于硫胶废水以检验菌株SS1的降解能力,发现在接种量为1.6g·L-1的条件下,菌株SS1对原水中乙酸的降解能力达200mg·L-1·h-1,乙酸完全降解仅需5.34 h,该降解速率大大高于三角摇瓶中的降解速率,说明加大接种量可以显著提高菌株SS1对乙酸的降解速率,同时也说明菌株SS1对硫胶废水原水有很好的适应和降解能力。
图 5示乙酸降解对硫胶废水中硫代硫酸盐生物氧化的影响。结果显示:在含有乙酸的原水中,Halothiobacillus sp.TX的氧化活性明显受到抑制,硫代硫酸根的质量浓度缓慢下降,培养6 d后硫代硫酸盐的氧化率仅36.56%,pH值下降也较为缓慢,到第6天硫胶废水的pH值才下降至最低值3.81;而通过预培养将乙酸去除后,Halothiobacillus sp.TX只需2 d就可以将废水中的硫代硫酸盐完全氧化,由于硫代硫酸盐经生物氧化产生硫酸,导致废水的pH值由初始值4.5迅速下降至3.01。上述结果说明:去除乙酸后,Halothiobacillus sp.TX菌株对硫代硫酸盐的氧化速率显著提高,乙酸对Halothiobacillus sp.TX菌株氧化活性的抑制作用已经成功解除。
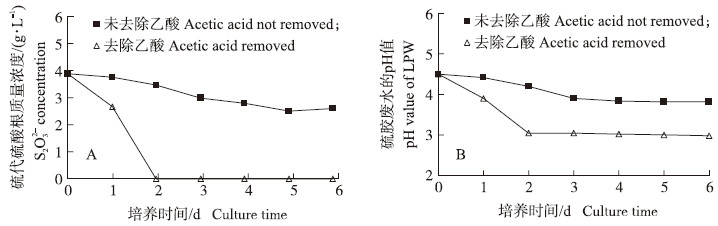 | 图 5 接种SS1及预培养对硫胶废水中硫代硫酸盐生物氧化的影响 Fig. 5 Effects of SS1 inoculation and preincubation on biooxidation of thiosulfate present in liquid polysulfide wastewater(LPW) |
在硫胶废水生物处理工程中,硫代硫酸盐的降解主要依赖于Halothiobacillus sp.的氧化活性,而较高浓度乙酸对Halothiobacillus sp.具有抑制作用,严重影响硫代硫酸盐的降解效率[3]。为了解决这一问题我们从盐碱土中分离筛选了1株耐盐且具有絮凝功能的乙酸降解菌,以期利用该菌株将硫胶废水中的乙酸先行降解,以解除乙酸对自养型硫杆菌的抑制作用。
根据形态学、生理生化特性和16S rDNA同源性比较,菌株SS1初步鉴定为Pseudomonas sp.。菌株SS1是1株中度嗜盐菌,而且具有絮凝生长的特性,以乙酸为碳源生长时絮凝指数达86.41%。虽然在Pseudomonas属中形成生物膜有较多的文献报道,但大多是非耐盐菌株[15],耐盐菌株较少有文献报道[16, 17],在含盐条件下具有絮凝功能的菌株尚未见报道。细菌絮凝生长的机制一般认为同细菌产生的胞外多糖有关[18, 19, 20],化学分析发现菌株SS1菌体产生的胞外多糖达226.88 mg·g-1,同时还产生135.36 mg·g-1的胞外蛋白,据此推测菌株SS1絮凝生长的特性可能是其胞外多糖与胞外蛋白两种组分交互作用的结果,事实上,胞外蛋白与胞外多糖交互作用促进生物膜形成或维持其稳定性已有文献报道[21, 22]。
乙酸不属于难降解的有机污染物,然而由于硫胶废水中高盐条件引起的抑菌作用,即使是经过高度驯化的活性污泥对其降解也是十分缓慢的,由于乙酸对Halothiobacillus sp.的抑制作用,造成硫胶废水生物处理时其水力停留时间(HRT)长达90 h。本研究的结果表明:菌株SS1形成的絮体可有效解除乙酸对盐生硫细菌的抑制作用,加快硫代硫酸盐的降解,在1.6g·L-1的接种量条件下SS1降解乙酸仅需6 h,且后续硫代硫酸盐的生物氧化可缩短至48 h,将两段衔接起来理论上可使硫胶废水生物处理的HRT由现行工程的90 h缩短至54 h,有利于降低运行成本。本研究没有采用游离生长的耐盐菌株,主要原因是采用游离生长的菌株需要解决细胞固定化的问题,增加了应用成本;菌株SS1可以形成沉降性能良好的絮体,实际应用时无需细胞固定化或生物膜挂膜所需的填料,可像普通活性污泥一样通过沉淀池及污泥回流系统回流至曝气池内,从而避免菌体流失,因而在硫胶废水的生物处理中具有更好的应用潜力。
| [1] | Tenc-Popovic M E, Bogunovic L J, Jankovic D, et al. New synthesis of liquid polysulfide polymers in the presence of hydrazine.Ⅰ. Synthesis of linear polysulfide polymers from 1, 1'-[methylenebis(oxy)]-bis-[2-chloroethane]and sodium tetrasulfide[J]. J Polym Sci A:Polym Chem, 1997, 35:1363-1367 |
| [2] | 杨庆林. 聚硫橡胶含硫污水的治理[J]. 辽宁化工, 1992, 27(4):18-22[Yang Q L. Treatment of polysulfide rubber sulfur-bearing wastewater[J]. Liaoning Chemical Engineering, 1992, 27(4):18-22(in Chinese)] |
| [3] | 林栋青, 张彦科, 顾向阳. 硫代硫酸盐氧化菌TX 的分离、鉴定及其生物学特性[J]. 微生物学通报, 2009, 36(11):1638-1644[Lin D Q, Zhang Y K, Gu X Y. Isolation, identification and characterization of thiosulfate-oxidizing bacterium TX[J]. Microbiology(China), 2009, 36(11):1638-1644(in Chinese with English abstract)] |
| [4] | Gu X Y, Wong J W C. Identification of inhibitory substances affecting bioleaching of heavy metals from anaerobically digested sewage sludge[J]. Environ Sci Technol, 2004, 38:2934-2939 |
| [5] | Frattini C J, Leduc L G, Ferroni G D. Strain variability and the effects of organic compounds on the growth of the chemolithotrophic bacterium Thiobacillus ferrooxidans[J]. Anton Leeuw Int J G, 2000, 77:57-64 |
| [6] | 林栋青. 硫胶废水处理的生物学机理研究[D]. 南京:南京农业大学, 2009:23-24[Lin D Q. Biological mechanisms involved in the treatment of polysulfide wastewater[D]. Nanjing:Nanjing Agricultural University, 2009:23-24(in Chinese with English abstract)] |
| [7] | 东秀珠, 蔡妙英. 常见细菌系统鉴定手册[M]. 北京:科学出版社, 2001:364-398[Dong X Z, Cai M Y. Manual for Systematic Identification of Common Bacteria[M]. Beijing:Science Press, 2001:364-398(in Chinese)] |
| [8] | Julia R M, Takuichi S, Andrew J W. Design and evaluation of useful bacterium-specific PCR primers that amplify genes coding for bacterial 16S rRNA[J]. Appl Environ Microbiol, 1998, 64(2):795-799 |
| [9] | Walker J M. The Protein Protocols Handbook[M]. 3rd ed. New York:Humana Press, 2009 |
| [10] | 任南琪, 王爱杰. 厌氧生物技术原理与应用[M]. 北京:化学工业出版社, 2004:315-317[Ren N Q, Wang A J. Principles and Applications for Anaerobic Biotechnology[M]. Beijing:Chemical Engineering Press, 2004:315-317(in Chinese)] |
| [11] | 舒红英. 脱硫液中硫代硫酸钠的测定[J]. 江西冶金, 2002, 22(3):38-39[Shu H Y. Determination of thiosulfate present in the desulfurization liquids[J]. Jiangxi Metallurgy, 2002, 22(3):38-39(in Chinese with English abstract)] |
| [12] | 国家环境保护总局. 水和废水检测分析方法[M]. 4版. 北京:中国环境科学出版社, 2002:164-165[State Environmental Protection Administration. Analytical Methods for Monitoring of Water and Wastewater[M]. 4th ed. Beijing:China Environmental Science Press, 2002:164-165(in Chinese)] |
| [13] | 张丽丽, 姜理英, 方芳, 等. 好氧颗粒污泥胞外多聚物的提取及成分分析[J]. 环境工程学报, 2007, 1(4):127-130[Zhang L L, Jiang L Y, Fang F, et al. Extraction and composition analysis of EPS for aerobic granular sludge[J]. Chinese Journal of Environmental Engineering, 2007, 1(4):127-130(in Chinese with English abstract)] |
| [14] | Dubois M, Gilles K A, Hamilton J K, et al. Colorimetric method for determination of sugars and related substances[J]. Analytical Chemistry, 1956, 28:350-356 |
| [15] | Mann E E, Wozniak D J. Pseudomonas biofilm matrix composition and niche biology[J]. FEMS Microbiology Reviews, 2011, 36:893-916 |
| [16] | Romanenko L A, Uchino M, Falsen E, et al. Pseudomonas xanthomarina sp.nov., a novel bacterium isolated from marine ascidian[J]. J Gen Appl Microbiol, 2005, 51:65-71 |
| [17] | Paraneeiswaran A, Shukla S K, Rao T S, et al. Removal of toxic Co-EDTA complex by a halophilic solar-salt-pan isolate Pseudomonas aeruginosa SPB-1[J]. Chemosphere, 2014, 95:503-510 |
| [18] | Byrd M S, Sadovskaya I, Vinogradov E, et al. Genetic and biochemical analyses of the Pseudomonas aeruginosa Psl exopolysaccharide reveal overlapping roles for polysaccharide synthesis enzymes in Psl and LPS production[J]. Mol Microbiol, 2009, 73:622-638 |
| [19] | Ma L, Lu H, Sprinkle A, et al. Pseudomonas aeruginosa Psl is a galactose- and mannose-rich exopolysaccharide[J]. J Bacteriol, 2007, 189:8353-8356 |
| [20] | Spiers A J, Rainey P B.The Pseudomonas fluorescens SBW25 wrinkly spreader biofilm requires attachment factor, cellulose fibre and LPS interactions to maintain strength and integrity[J]. Microbiology, 2005, 151:2829-2839 |
| [21] | Borlee B, Goldman A, Murakami K, et al. Pseudomonas aeruginosa uses a cyclicdi-GMP-regulated adhesin to reinforce the biofilm extracellular matrix[J]. Mol Microbiol, 2010, 75:827-842 |
| [22] | Dueholm M S, Petersen S V, Sønderkr M, et al. Functional amyloid in Pseudomonas[J]. Mol Microbiol, 2010, 77:1009-1020 |
 2015, Vol. 38
2015, Vol. 38


