文章信息
- 马清华, 陈晓峰, 牟晋华, 侯喜林. 2015.
- MA Qinghua, CHEN Xiaofeng, MU Jinhua, HOU Xilin. 2015.
- 灰霉菌侵染大白菜后ADF7和ADF10基因表达分析
- The expression of ADF7 and ADF10 genes after Botrytis cinerea infection in Chinese cabbage
- 南京农业大学学报, 38(5): 742-747
- Journal of Nanjing Agricultural University, 38(5): 742-747.
- http://dx.doi.org/10.7685/j.issn.1000-2030.2015.05.007
-
文章历史
- 收稿日期:2014-11-25
2. 中国农业大学烟台研究院, 山东 烟台 264670
2. Yantai Research Institute of China Agricultural University, Yantai 264670, China
肌动蛋白解聚因子/丝切蛋白家系(actin depolymerizing factor/cofilin,ADF/cofilin)作为一类肌动蛋白结合蛋白,广泛存在于真核细胞的细胞骨架中,它作为一个重要的肌动蛋白调节因子在植物防御真菌侵染过程中起重要作用。ADF基因通过调控微丝的解聚和聚合,以切割肌动蛋白的形式调节细胞骨架的动态装配,从而调节肌动蛋白的功能[1, 2, 3, 4, 5]。通过对大麦抗病性研究发现,肌动蛋白细胞骨架对于植物体抵抗外界真菌侵染有保护作用,药物干扰肌动蛋白细胞骨架的调节作用可以加剧真菌对大麦的侵染[6]。肌动蛋白解聚因子和cofilin家族能调节细胞内肌动蛋白动力学,肌动蛋白丝末端的G单体蛋白与F丝状蛋白之间存在一种动态转化,当植物受到外界刺激时肌动蛋白的周转率增加,ADF基因通过调节ADF蛋白的功能来调控细胞骨架的活动[7, 8, 9]。田磊等[10]用反义遗传技术证实拟南芥AtADF 4 在植物防御中起调控作用,认为该基因是植物防御病原菌侵染信号传递途径的新成员,通过信号转导途径进行细胞骨架的再分配。另外,Geddes等[11]通过大麦赤霉病蛋白组分析发现ADF在细胞抵御外界病原菌侵染过程中起重要的调控作用。魏芳等[12]利用禾谷镰刀菌侵染小麦后,分析抗赤霉病品种‘望水白’和感病品种‘Alondra’中穗部ADF基因的表达,发现两品种在受真菌侵染的72 h内均呈现上调表达。
本研究对大白菜ADF基因在防御真菌病害侵染中的作用进行了分析,并研究了肌动蛋白解聚因子在受灰霉菌侵染过程中的动态变化。我们从拟南芥基因组数据库中获得11个ADF基因,将其与大白菜基因组数据库比对得到19个大白菜ADF基因。对它们进行生物信息学分析,对同源性相对较高的ADF7和ADF10基因进行了灰霉菌侵染诱导表达特点分析,以期为大白菜ADF基因和真菌病原菌抗性关系的研究奠定理论基础。
1 材料与方法 1.1 材料试验所用大白菜为抗真菌病害品种‘新烟杂3号’和感病品种‘包头莲’(中国农业大学烟台研究院提供),种植于南京农业大学人工气候室。灰霉菌菌株由江苏省农业科学院蔬菜作物研究所提供。
1.2 方法 1.2.1 生物信息学分析从拟南芥基因组数据库(http://www.arabidopsis.org/)找到全部的AtADF基因,进行序列比对分析,在大白菜基因组数据库(http://brassicadb.org/brad/index.php)中找到对应的基因序列。利用Clustal软件对多种植物ADF7基因进行系统进化树分析;用MEGA 6.05[13]对ADF家族中同源性较高的ADF7和ADF10基因进行氨基酸序列比对分析;利用BioXM 2.6软件预测ADF氨基酸残基的相对分子质量和等电点;利用Signal P 4.1 server预测2个ADF基因是否存在信号肽;利用SOPMA软件预测其氨基酸序列的二级结构。
1.2.2 灰霉菌小孢子悬浮液的制备及侵染大白菜种子经1 g·L-1的HgCl2灭菌后播种于装有灭菌基质的穴盘中,在人工气候室25 ℃、光周期12 h/12 h条件下培养,待长至4叶期时进行处理。
灰霉病菌液制备参考王利英[14]的方法:先用PDA培养基活化灰霉菌菌株,再用血球计数法配制浓度为1.0×105 mL-1的灰霉孢子悬浮液,均匀喷洒在叶片上,对照组同时喷等量的清水。接种后在湿度为90%、20 ℃黑暗条件下保湿24 h后正常管理。于接种后0、6、12、24、36、48和72 h分别取相同部位的根、茎、叶各0.1 g,保存于-70 ℃冰柜中待测。每个处理设3次重复。
1.2.3 叶片中总RNA提取及cDNA合成采用RNA simple Total RNA Kit试剂盒提取大白菜样品总RNA,用Prime Script RT reagent Kit将总RNA反转录成cDNA。
1.2.4 半定量PCR反应以根、茎、叶的cDNA为模板,按照以下程序进行定量PCR反应:95 ℃预反应4 min;之后是循环反应:95 ℃ 30 s,55 ℃ 30 s,72 ℃ 30 s,29个循环。PCR产物用15 g·L-1的琼脂糖凝胶电泳检测。
1.2.5 实时定量PCR反应采用SYBR Premix Ex Taq试剂盒进行实时定量PCR反应,以大白菜actin基因作为内参,内参及ADF基因的引物序列由Primer Premier 5.0软件设计。按照以下程序进行实时定量PCR反应:95 ℃预反应30 s;40个循环反应:95 ℃ 10 s,58 ℃ 30 s。熔解曲线测定进行61个循环,65 ℃反应10 s。试验数据分析采用2-ΔΔCT法进行相对表达量分析,每处理3次重复。
2 结果与分析 2.1 不同植物ADF基因编码的氨基酸序列比较及同源性分析不同植物的ADF基因均有高度的序列同源性,特别是N端和C端区域具有与肌动蛋白结合功能的结构域。用拟南芥ADF7基因编码的氨基酸与大白菜、不结球白菜、荠菜、烟草等16种植物进行序列比对(图 1),系统进化树结果显示:大白菜与不结球白菜的ADF7基因编码的蛋白同源性最高,其次是荠菜和拟南芥,与烟草、杨树、马铃薯、菜豆、葡萄、黄瓜、甜橙、大豆、蒺藜苜蓿和野草莓的同源性相对较低。大白菜与单子叶植物苜蓿、玉米、水稻和高粱不在同一个分支上,与它们的进化关系最远,亲缘关系最远。
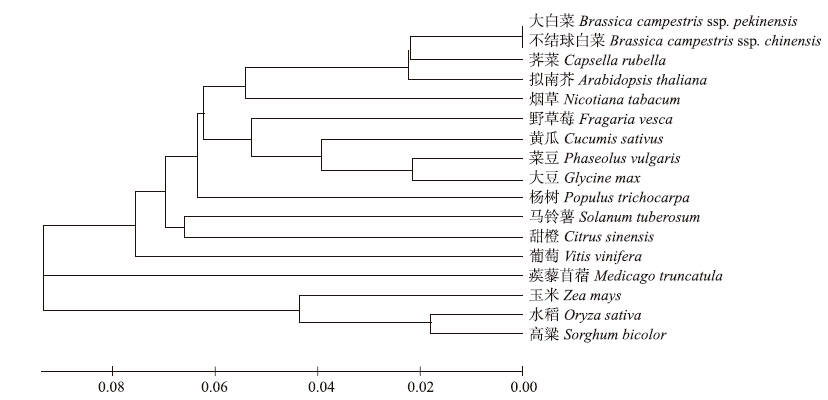 | 图 1 不同植物ADF7基因氨基酸序列的系统进化树Fig. 1 Phylogenetic tree of diverse plants on amino acid sequences of ADF7 gene |
对ADF7和ADF10基因编码的氨基酸序列进行比对,结果(图 2)显示:ADF7与ADF10的同源性高达97.69%。由此可见,ADF7和ADF10亲缘关系较近。
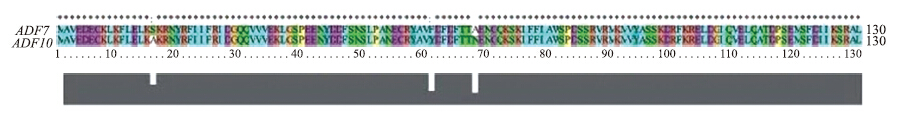 | 图 2 ADF7和ADF10基因编码的氨基酸序列的多重比对结果Fig. 2 Alignment result of amino acid sequences encoded by ADF7 and ADF10 genes |
由ADF7和ADF10编码的蛋白相对分子质量及等电点极其相近,相对分子质量分别为31.54×103和31.68×103,等电点均为5.11。对2个基因的信号肽进行预测分析,2个基因的Cmax和Smean均小于0.5,没有信号肽存在。由图 3可见:2个基因编码的蛋白均由130个氨基酸残基组成,其中ADF7有47个α螺旋、41个无规则卷曲和38条延伸链,分别占总长度的30%左右,还有4个β转角;ADF10有49个α螺旋、42个无规则卷曲和34条延伸链,5个β转角。2个基因都主要由α螺旋、无规则卷曲和延伸链组成,同时伴有少量的β转角。
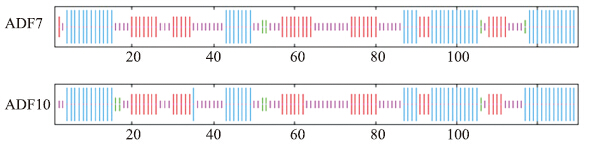 | 图 3 ADF7和ADF10基因编码蛋白的二级结构分析Fig. 3 Analysis of secondary structure of the protein encoded by ADF7 and ADF10 genes |
受灰霉菌侵染后,‘新烟杂3号’ADF7和ADF10基因的表达结果显示:2个基因的表达情况相似,但在植株的不同部位明显不同。经灰霉菌侵染的大白菜根在72 h内条带不明显,基因几乎不表达(图 4)。茎中的ADF7和ADF10在12和48 h时的条带亮度略高于其他处理时间,表明茎中这2个基因在灰霉菌处理12和48 h后均出现表达高峰。大白菜叶中各个处理时间段的条带亮度明显高于根和茎,但是不同的处理时间亮度不同,48 h后亮度最高,其次是12 h,说明了ADF7和ADF10在叶中的表达均明显高于根和茎,灰霉菌处理12 h后出现第1次表达高峰,处理48 h后出现表达的最高峰。
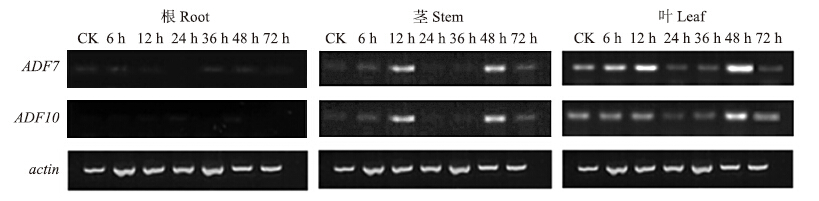 | 图 4 ADF7和ADF10在受灰霉菌侵染的大白菜品种‘新烟杂3号’根、茎、叶中的半定量表达Fig. 4 The semiquantitative expression of ADF7 and ADF10 infected by Botrytis cinerea in root,stem and leaf of Chinese cabbage variety ‘Xinyanza 3’ |
采用实时定量PCR检测未受灰霉菌侵染的大白菜‘新烟杂3号’和‘包头莲’中ADF7和ADF10的表达情况,结果(图 5)显示:基因在2个品种正常植株的根、茎、叶中72 h内几乎不表达,受灰霉菌侵染后ADF7和ADF10基因在2个品种叶中的表达量最高,茎次之,在根中表达不明显,基因在‘新烟杂3号’的茎和叶中的表达量比‘包头莲’高。2个基因在茎和叶中的表达特点相似,均呈现双波表达,侵染6 h后都出现较高的表达量,12 h后出现第1次表达高峰,在24和36 h时表达量降低,侵染48 h后出现表达最高峰,处理72 h后2个基因的表达量均与对照相近。可见,‘新烟杂3号’比‘包头莲’的抗性强,ADF7和ADF10的表达趋势相近,均抗真菌且呈现组织特异性表达。
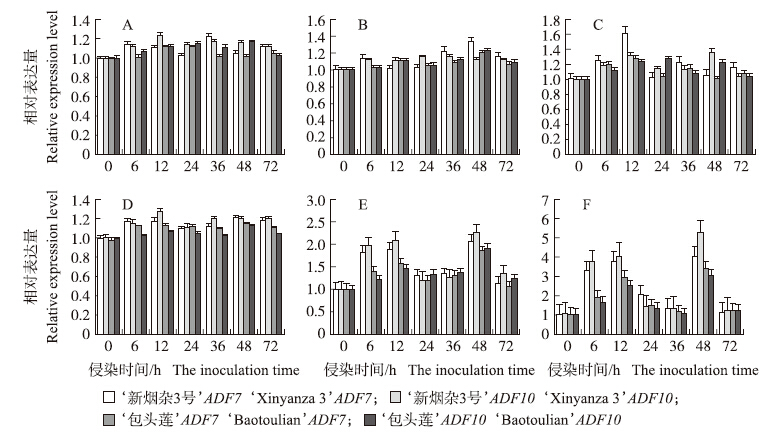 |
图 5 大白菜受到灰霉菌侵染时ADF7和ADF10基因在根、茎、叶中的定量表达Fig. 5 The quantitative expression of ADF7 and ADF10 infected by Botrytis cinerea in root,stem and leaf of Chinese cabbage
A、B和C分别代表未受侵染时的根、茎和叶;D、E和F分别代表受灰霉菌侵染的根、茎和叶。 A,B and C represent the roots,stem and leaf of plants with mock-inoculation;D,E and F represent the roots,stem and leaf infected by Botrytis cinerea. |
一系列肌动蛋白结合蛋白维持其正常的生理状态才能使其发挥正常的生物学功能[15]。肌动蛋白结合蛋白是与微丝或肌动蛋白特异结合并影响其结构和功能的一类辅助蛋白,这些蛋白从多种水平调节微丝的形成和交联[16]。肌动蛋白解聚因子(ADF)是肌动蛋白细胞骨架的一个重要调节因子,在调节微丝的动态结构方面发挥着双重特性,既可以促进肌动蛋白纤丝的聚合,也可以促进其解聚[17]。ADF作为一种特殊的病原相关蛋白,在受到灰霉菌侵染后,表达量出现明显变化,通过G单体蛋白与F丝状蛋白的转化调节细胞骨架的再整合,以抵御真菌侵染。比较肌动蛋白解聚因子在灰霉菌侵染前后的表达差异发现,侵染初期开始反应,即微丝在侵染后12 h内开始聚合,引起肌动蛋白解聚因子的过量表达,24 h时表达量几乎降到最低,48 h时又达到一个较高水平。真菌侵染引起了肌动蛋白骨架的聚合,可能是由于ADF基因对其聚合发生调控。彭世清等[18]将拟南芥AtADF4 转入烟草体内,明显影响转基因植株形态的改变,证明肌动蛋白解聚因子的过表达会破坏肌动蛋白的动态平衡。本研究通过探讨2个大白菜品种受灰霉菌侵染时ADF7和ADF10基因在根、茎、叶中的表达变化可知,抗病品种‘新烟杂3号’比感病品种‘包头莲’的抗性高。2个基因在灰霉菌处理的植株中表达量均升高,在根、茎、叶中的表达呈现组织差异性,在叶中的表达量最高,其次是茎,在根中的调控作用不明显。未来的研究方向是对受真菌侵染的大白菜微管骨架进行分析,通过观察微管与微丝的动态结构变化进一步验证大白菜ADF基因家族对真菌的抗性作用。本研究为进一步探讨大白菜在生物胁迫下ADF基因家族对细胞骨架的调控作用提供了重要的理论依据。
| [1] | 陈晓波,王冬梅,刘娟,等. 植物细胞微丝骨架对真菌侵染的反应[J]. 河北农业大学学报,2001,24(3):100-104 [Chen X B,Wang D M,Liu J,et al. Advances of the studies of microfilament cytoskeleton responses to fungus infection in plants[J]. Journal of Hebei Agricultural University,2001,24(3):100-104(in Chinese with English abstract)] |
| [2] | 叶佳. 低温胁迫下拟南芥肌动蛋白解聚因子ADF5的功能研究[D]. 兰州:兰州大学,2010:36-37 [Ye J. The research on the function of actin depolymerization factor ADF5 under low temperature stress in Arabidopsis[D]. Lanzhou:Lanzhou University,2010:36-37(in Chinese with English abstract)] |
| [3] | Ruzicka D R,Kandasamy M K,McKinney E C,et al. The ancient subclasses of Arabidopsis ACTIN DEPOLYMERIZING FACTOR genes exhibit novel and differential expression[J]. The Plant Journal,2007,52(3):460-472 |
| [4] | Smertenko A P,Allwood E G,Khan S,et al. Interaction of pollen specific actin-depolymerizing factor with actin[J]. The Plant Journal,2001,25(2):203-212 |
| [5] | Tholl S,Moreau F,Hoffmann C,et al. Arabidopsis actin-depolymerizing factors(ADFs)1 and 9 display antagonist activities[J]. FEBS Letters,2011,585(12):1821-1827 |
| [6] | Miklis M,Consonni C,Bhat R A,et al. Barley MLO modulates actin-dependent and actin-independent antifungal defense pathways at the cell periphery[J]. Plant Physiology,2007,144(2):1132-1143 |
| [7] | Carlier M F,Laurent V,Santolini J,et al. Actin depolymerizing factor(ADF/Cofilin)enhances the rate of filament turnover:implication in actin-based motility[J]. The Journal of Cell Biology,1997,136(6):1307-1323 |
| [8] | Theriot J A,Mitchison T J. Actin microfilament dynamics in locomoting cells[J]. Nature,1997,352(11):126-131 |
| [9] | 赵微,苏玉虹,巴彩凤,等. Cofilin蛋白功能及活性调节[J]. 中国生物化学与分子生物学报,2007,23(9):706-710 [Zhao W,Su Y H,Ba C F,et al. Function and activity regulation of cofilin[J]. Chinese Journal of Biochemistry and Molecular Biology,2007,23(9):706-710(in Chinese with English abstract)] |
| [10] | 田磊,廖明芳,李冀洲,等. 细胞骨架蛋白中 ADF/cofilin 蛋白家系的作用:如何与肌动蛋白结合及发挥解聚作用[J]. 中国组织工程研究与临床康复,2009,13(50):9941-9945 [Tian L,Liao M F,Li J Z,et al. ADF/cofilins proteinic family constellation in cytoskeletal protein:how does depolymerization occur through combination of ADF/cofilins with actin[J]. Journal of Clinical Rehabilitative Tissue Engineering Research,2009,13(50):9941-9945(in Chinese with English abstract)] |
| [11] | Geddes J,Eudes F,Laroche A,et al. Differential expression of proteins in response to the interaction between the pathogen Fusarium graminearum and its host Hordeum vulgare[J]. Plant Proteomics,2008,8(3):545-548 |
| [12] | 魏芳,马鸿翔. 小麦中一个ADF基因克隆与表达分析[J]. 分子植物育种,2011,9(5):554-560 [Wei F,Ma H X. Cloning and expression characterization of one ADF gene in Triticum aestivum[J]. Molecular Plant Breeding,2011,9(5):554-560(in Chinese with English abstract)] |
| [13] | Tamura K,Peterson D,Peterson N,et al. MEGA5:molecular evolutionary genetics analysis using maximum likelihood,evolutionary distance and maximum parsimony methods[J]. Molecular Biology and Evolution,2011,28(10):2731-2739 |
| [14] | 王利英. 不结球白菜黑斑病抗性机制初步研究[D]. 南京:南京农业大学,2008:40 [Wang L Y. Study on mechanisms of resistance to black spot disease in non-heading Chinese cabbage[D]. Nanjing:Nanjing Agricultural University,2008:40(in Chinese with English abstract)] |
| [15] | David W,McCurdy D W,Kovar D R,et al. Actin and actin-binding proteins in higher plants[J]. Protoplasma,2001,215(1/2/3/4):89-104 |
| [16] | Sun H Q,Kwlatkowska K,Yin H L. Actin monomer binding proteins[J]. Cell Biology,1995,7(1):102-110 |
| [17] | Staiger C J,Gibbon B C,Kovar D R,et al. Profilin and actin-depolymerizing factor:modulators of actin organization in plants[J]. Trends in Plant Science,1997,2(7):275-281 |
| [18] | 彭世清,黄冬芬. 拟南芥肌动蛋白解聚因子ADF4基因(AtADF4)在烟草中表达引起植株形态变化[J]. 植物生理与分子生物学学报,2006,32(1):52-56 [Peng S Q,Huang D F. The morphological change in tobacco on the expression of actin depolymerization for ADF4 gene(AtADF4)from Arabidopsis thaliana[J]. Journal of Plant Physiology and Molecular Biology,2006,32(1):52-56(in Chinese with English abstract)] |
 2015, Vol. 38
2015, Vol. 38


