文章信息
- 刘丽华, 沈卫德, 李兵, 秦佳梅, 郁有兰, 马鹏宇. 2015.
- LIU Lihua, SHEN Weide, LI Bing, QIN Jiamei, YU Youlan, MA Pengyu. 2015.
- 家蚕细胞cyclinA基因的干涉对家蚕细胞增殖的影响
- RNA interference impact on silkworm cyclinA gene and cell proliferation
- 南京农业大学学报, 38(1): 168-171
- Journal of Nanjing Agricultural University, 38(1): 168-171.
- http://dx.doi.org/10.7685/j.issn.1000-2030.2015.01.025
-
文章历史
- 收稿日期:2014-02-18
2. 苏州大学基础医学与生物科学学院/现代丝绸国家工程实验室, 江苏 苏州 215123;
3. 吉林省抚松县第一中学, 吉林 白山 134500
2. School of Basic Medicine and Biological Sciences/National Engineering Laboratory for Modern Silk, Soochow University, Suzhou 215123, China;
3. No.1 Middle School in Fusong County Jilin Province, Baishan 134500, China
细胞周期蛋白(cyclin)是调节细胞周期活动的蛋白质,在细胞增殖分化及肿瘤发生中起重要作用[1]。cyclinA作为细胞周期蛋白家族的一员,是在S期和G2/M期起重要作用的周期蛋白,cyclinA的合成起始接近于G1-S期过渡点,此时,cyclinD及E降解,随着cyclinA的合成增加,在S期它取代cyclinE的作用与CDK2结合,该复合物进入核内,参与DNA复制调控,进一步促进其合成;在G2期cyclinA与CDC2结合,在G2-M转变过程中与cyclinB-CDC2复合物一起发挥作用,使细胞进入M期[2]。
RNA干扰(RNAi)是由与生物体内源靶基因mRNA同源的双链RNA(siRNA)特异性引发的靶mRNA降解,导致目的基因表达沉默的一种反向遗传学技术[3],是近年来发现和发展起来的特异性强、效率高的新型基因阻断技术。已有研究证实,利用RNA干扰技术在抗肿瘤[4, 5]、抗病毒[6]及治疗遗传病研究等[7]方面都取得了良好的效果。
家蚕(Bombyx mori)是完全变态昆虫,也是鳞翅目昆虫的典型代表[8],其细胞周期调控机制的解析将有助于推动家蚕模式生物化研究的进程。cyclinA是G1期向S期转移的限速因素,并与CDC2结合来促进G2/M时相的转换。目前在家蚕中仅对cyclinA基因进行了克隆和表达研究,但对其功能研究还未见相关报道。本研究采用RNA干扰技术,靶向抑制家蚕cyclinA基因的表达,探讨cyclinA对细胞增殖的影响,为进一步研究家蚕cyclinA基因功能奠定基础。
1 材料与方法 1.1 试验材料
家蚕卵巢细胞系(BmN)为苏州大学蚕桑实验室保存。TC-100培养基、胎牛血清(FBS)和脂质体(lipofectine2000)购自Invitrogen公司;荧光标记的siRNA片段由上海吉玛制药技术有限公司合成;Trizol RNA提取试剂盒、SYBR PrimeScriptTM RT-PCR试剂盒及其他试剂均购自宝生物工程(大连)有限公司。
1.2 干扰靶位点的选择及siRNA的设计
根据NCBI数据库中家蚕cyclinA基因序列,设计靶向cyclinA基因的siRNA片段,引物对序列:5′-UGAU- GAGCAUGUCACCGUUTT-3′,5′-AACGGUGACAUGCUCAUCATT-3′;设计与其他编码序列均无同源性的阴性对照引物对序列(NC):5′-UACAGACCCCUCGAUCGGUTT-3′,5′-ACCGAUCGAGGGGUCUGU-ATT-3′。
1.3 细胞培养及siRNA转染
家蚕BmN细胞用含体积分数为10%胎牛血清的TC-100培养液,置于27 ℃培养。转染前1 d,将(0.5~2)×105个细胞接种于6孔培养板中,每孔中加500 μL培养基,使转染时的细胞密度能够达到50%~80%。设正常对照组(不进行转染)、无义对照组(转染无义siRNA)和siRNA-cyclinA转染组。用Oligofectamine脂质体转染试剂转染,具体步骤按说明书进行。转染后3 h,将转染液换为含10%胎牛血清的培养液于27 ℃培养,转染后24 h观察并计算转染效率。48 h后收获细胞。
1.4 实时荧光定量PCR检测cyclinA mRNA的表达
按照Trizol RNA试剂盒说明书提取转染组和对照组细胞总RNA,紫外分光光度计测定其纯度和浓度。用M-MLV反转录试剂盒将总RNA反转录成cDNA。引物采用Primer Premier 5.0软件,按照Real-time PCR要求设计家蚕actin 3 内参基因和cyclinA基因的引物对。actin 3 扩增引物对F/R:5′-CGGCTACTCGTTCACTACC-3′,5′-CCGTCGGGAAGTTCGTAAG-3′,扩增产物长度147 bp。cyclinA扩增引物对F/R:5′-CTCTCAACACCCACCTCAC-3′,5′-CGCTGCTATTACTGAGGGT-3′,扩增产物长度153 bp。采用SYBR PrimeScriptTM RT-PCR试剂盒进行测定,具体试验步骤按照说明书进行。反应程序:95 ℃ 1 min;95 ℃ 15 s,60 ℃ 31 s,40个循环。每个样品设3个重复。RT-PCR的试验数据用ABI7300仪器中的Sequence detection software version 1.3.1软件处理,并参照Schefe等[9]的方法进行效率校正,图表采用SPSS 16.0软件制作。
1.5 流式细胞仪检测细胞周期
转染后培养48 h,收集细胞,PBS(pH 7.0)清洗2次,加入体积分数为70%的冷乙醇,轻轻混合细胞,在-20 ℃下固定12 h以上,然后用PBS洗涤后1 000 r · min-1离心6 min除去乙醇,加入50 μg · mL-1碘化丙啶(PI)染色液1 mL,室温避光染色30 min后用流式细胞仪检测。
图 1 Fig. 1 2 结果与分析 2.1 siRNA转染效率的观察
将siRNA-cyclinA经脂质体介导转染进细胞24 h后,在共聚焦荧光显微镜下观察发出绿色荧光的转染细胞(图 1),统计转染效率达78%左右,说明转染效率较高。
2.2 siRNA对家蚕BmN细胞中cyclinA表达的影响
家蚕BmN细胞分别转染siRNA-cyclinA、无义siRNA-cyclinA后,继续培养48 h,用荧光定量PCR检测对cyclinA基因表达的影响。结果显示:siRNA-cyclinA转染组使BmN细胞cyclinA基因表达量比对照降低37.4%;无义对照组的cyclinA基因表达量与正常对照组无明显差异(图 2)。表明转染针对cyclinA的特异性siRNA可有效下调cyclinA基因的表达。
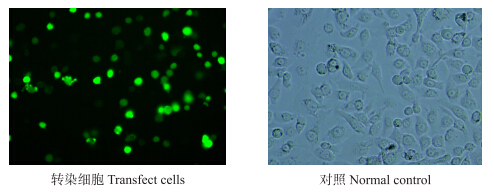 | 图 1 荧光显微镜下荧光标记siRNA转染后的细胞 Fig. 1 Transfect cells under a fluorescence microscopeafter fluorescence labeling siRNA transfection |
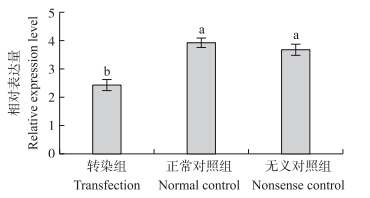 | 图 2 siRNA-cyclinA对家蚕BmN细胞中cyclinA基因表达的影响 Fig. 2 The influence of siRNA-cyclinA on cyclinA gene expression in Bombyx mori BmN cell不同字母表示差异显著(P<0.05)。The different letters indicate significant difference at 0.05 level. |
转染后48 h,流式细胞仪检测结果(表 1和图 3)显示:相对于正常及无义对照组,siRNA-cyclinA转染组G0/G1期细胞比例显著增加(P<0.05),S期和G2/M期细胞比例显著减少(P<0.05),而正常对照组与无义对照组的各个期细胞比例的差异不显著(P>0.05)。说明cyclinA基因能使细胞周期阻滞于G1期,从而抑制细胞的增殖。
| % | |||
| 组别Group | 细胞周期Cell cycle | ||
| G0/G1 | S | G2/M | |
| 正常对照组Normal control | 47.39±0.56 | 26.43±0.68 | 26.17±0.79 |
| 无义对照组Nonsense control | 49.73±0.83 | 25.70±0.49 | 24.57±0.61 |
| siRNA-cyclinA转染组siRNA-cyclinA transfection | 64.59±2.48* | 19.68±1.35* | 15.73±1.12* |
| 注: *表示与正常对照组相比差异显著(P<0.05)。* indicates significant difference at 0.05 level compared with the normal control. | |||
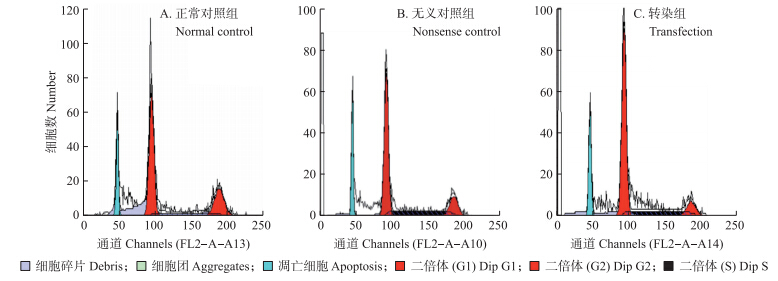 | 图 3 siRNA-cyclinA对家蚕BmN细胞周期影响的流式细胞分析 Fig. 3 The flow cytometry of influence of siRNA-cyclinA on Bombyx mori BmN cell cycle |
已有研究表明,肿瘤的发生与细胞周期调控异常有关,细胞周期信号通道的失控是癌变发生的重要因素,因此,哺乳动物的细胞周期一直是研究的热点,相比较而言,家蚕在细胞周期调控的研究较为滞后。在哺乳动物中,细胞周期蛋白A家族成员有2种类型:cyclinA1和cyclinA2,cyclinA 1与cyclinA2 基因有48%同源基因。在许多组织中,cyclinA 1和cyclinA2 基因表达并不同步,说明两者的功能不能相互替代[10]。
在家蚕中,目前已发现cyclinA基因有3种剪接变体,长度分别是2 141、2 210和2 173 bp,分别命名为cyclinA 1 [11]、cyclinA 2 [12]和cyclinA 3 [11]。其中,cyclinA 1和cyclinA3 具有相同的2个连续周期蛋白盒,在近N端有一段由9个氨基酸组成的特殊序列——周期蛋白破坏盒,但cyclinA 2 仅有典型周期蛋白的N端序列,缺乏2个连续的周期蛋白盒。测定家蚕cyclinA基因(总cyclinA表达量)在5龄3 d不同组织中的转录表达,发现其在精巢中高表达,表明该基因在家蚕精巢精母细胞发育分裂成精子时起重要作用;同时在进行核内有丝分裂的丝腺中也有一定丰度的表达[13],这与鼠类cyclinA基因在进行核内有丝分裂的滋养层细胞表达结果相似,但在果蝇中进行核内有丝分裂的唾液腺细胞中则检测不到该基因的表达,推测cyclinA在不同物种中进行核内有丝分裂组织间差异性表达,可能与这些组织中染色体的复制存在差异有关。
本试验以家蚕cyclinA基因为靶标,针对其3个剪接变体共同的特异性位点设计合成了RNA干扰片段,通过脂质体介导转染至家蚕BmN细胞中,荧光定量PCR检测结果显示,转染siRNA-cyclinA后,BmN细胞cyclinA基因表达量较对照降低了37.4%;细胞周期分析表明,siRNA转染使G0/G1期细胞比例显著增加,S期和G2/M期细胞比例显著减少,细胞增殖受到明显抑制。这些结果表明:在家蚕细胞周期调控中,cyclinA基因是家蚕细胞完成细胞周期必不可少的,是细胞周期中G1/S期的限速因素,是S期的特征性细胞周期蛋白。但cyclinA基因的3种剪接变体是否存在其他方面的不同功能还有待深入研究。
| [1] | 李志琴,章静波. 细胞周期调控与肿瘤[J]. 癌症进展杂志,2004,2(1):70-75 [Li Z Q,Zhang J B. Cell cycle regulation and tumor[J]. Cancer Progress,2004,2(1):70-75(in Chinese with English abstract)] |
| [2] | Bandaral L R,Adamczewski J P,Hunt T,et al. Cyclin A and the retinoblastoma gene product complex with a common transcrition factor[J]. Nature,1991,352(6332):249-251 |
| [3] | 马丽,张庆春. RNA干扰机制及应用研究进展[J]. 北方园艺,2012(10):191-193 [Ma L,Zhang Q C. Mechanism of RNA interference and progress of its application[J]. Northern Horticulture,2012(10):191-193(in Chinese)] |
| [4] | 燕慧,王捷,杨自飞,等. BSP基因RNA干扰对乳腺癌MDA-MB-231BO细胞生物学特性的影响[J]. 生物技术通报,2010,27(6):142-145 [Yan H,Wang J,Yang Z F,et al. The influence of RNA interference BSP gene on breast cancer MDA-MB-231BO cell biological characteristics[J]. Biotechnology Bulletin,2010,27(6):142-145(in Chinese with English abstract)] |
| [5] | Boren T,Xiong Y,Hakam A,et al. MicroRNAs and their targetmessenger RNAs associated with ovarian cancer response to chemotherapy[J]. Cynecologic Oncology,2009,113(2):249-255 |
| [6] | Deng L,Li G Q,Xi L S,et al. Hepatitis B virus inhibition in mice by lentiviral vector mediated short hairpin RNA[J]. BMC Gastroenterol,2009,6(9):73 |
| [7] | Orlacchio A,Bernardi G,Orlacchio A,et al. RNA interference as a tool for Alzheimer's disease therapy[J]. Mini Reviews in Medicinal Chemistry,2007,7(11):1166-1176 |
| [8] | 中国农业科学院蚕业研究所. 中国养蚕学[M]. 上海:上海科学技术出版社,1991:228-230 [Sericultural Research Institute Chinese Academy of Agricultural Sciences. The Sericultural Science in China[M]. Shanghai:Shanghai Science and Technology Press,1991:228-230(in Chinese)] |
| [9] | Schefe J H,Lehmann K E,Buschmann I R,et al. Quantitative real-time RT-PCR data analysis:current concepts and the novel"gene expression's CT difference" formula[J]. J Mol Med,2006,84:901-910 |
| [10] | 刘引引,潘泽民. CCNA1基因与肿瘤的相关性[J]. 生命的化学,2012,32(5):404-406 [Liu Y Y,Pan Z M. The correlation of CCNA1 with tumorigenesis[J]. Chemistry of Life,2012,32(5):404-406(in Chinese)] |
| [11] | 刘丽华,李兵,沈卫德. 家蚕细胞周期素家族基因的克隆及结构特征与表达分析[J]. 蚕业科学,2010,36(5):754-758 [Liu L H,Li B,Shen W D. Cloning,structural characterization and expression analysis of cyclin family genes in silkworm Bombyx mori[J]. Science of Sericulture,2010,36(5):754-758(in Chinese with English abstract)] |
| [12] | 张春冬,谈娟,赵丹红,等. 家蚕周期蛋白A基因(BmcyclinA)的克隆和表达谱分析[J]. 蚕业科学,2009,35(2):761-767 [Zhang C D,Tan J,Zhao D H,et al. Molecular cloning and expression pattern analysis of cyclinA gene in the silkworm,Banbyx mori[J]. Science of Sericulture,2009,35(2):761-767(in Chinese with English abstract)] |
| [13] | 刘丽华,李兵,沈卫德,等. 家蚕细胞周期蛋白家族基因在5龄幼虫组织中的表达谱分析[J]. 西北农林科技大学学报:自然科学版,2012,40(11):13-17 [Liu L H,Li B,Shen W D,et al. Expression profile analysis of the cyclin gene in the silk gland cell from silkworm,Bombyx mori[J]. Journal of Northwest A&F University:Natural Science Edition,2012,40(11):13-17(in Chinese with English abstract)] |




