文章信息
- 熊春华, 吴扬
- Xiong Chunhua, Wu Yang
- 竹炭对水溶液中Ni(Ⅱ)的吸附
- Adsorption of Ni (Ⅱ) from Aqueous Solution by Bamboo Charcoal
- 林业科学, 2012, 48(10): 125-130.
- Scientia Silvae Sinicae, 2012, 48(10): 125-130.
-
文章历史
- 收稿日期:2011-11-07
- 修回日期:2012-03-14
-
作者相关文章
Ni(Ⅱ)是人体必需的生命元素, 但过量的Ni(Ⅱ)会对人体造成危害, 对水生生物也有明显的毒害作用。近年来, Ni(Ⅱ)及化合物对机体器官、系统以及“三致”毒作用机制有较多的研究报道。环境中的重金属Ni(Ⅱ)可通过食物链而积累,导致人体慢性中毒。Ni(Ⅱ)污染主要源自工业生产过程,如电镀、冶炼、采矿、电池制造、金属深加工等(Elouear et al., 2009)。因此,去除废水中Ni(Ⅱ)离子具有重要意义。
含Ni(Ⅱ)废水常用的处理方法有化学沉淀法、蒸发回收法、离子交换法、吸附法、反渗透法以及电渗析法等(Diniz et al., 2005)。吸附法因操作简单、投资少、处理效果好而被广泛应用于去除废水中重金属离子。目前采用吸附法去除废水中重金属已有很多研究,但是高昂的处理费用迫切要求人们寻找可替代的廉价吸附材料。
近年研究表明,竹炭在保暖、去湿、调温、净化水质、改良土壤等方面均有明显作用, 可广泛用于农业、工业、电子、军事、环境保护、医疗卫生、纺织等领域, 目前在国际市场上需求量日益增大。作为功能性的环境保护材料,竹炭由于其独特的性质和产品的高附加值越来越受到人们的重视,成为竹材研究领域的一个新热点。
我国是竹类资源最丰富的国家之一,目前竹林面积720万hm2,有竹子40多属、500多种,竹林种类、面积和蓄积量均居世界前列。竹炭是一种多孔性物质,分子结构呈六角形,质地坚硬,细密多孔,吸附力可达木炭的5倍以上,能有效吸附空气中的各种浮游物质,对氢化物、甲醇、苯、硫化物、酚等有害化学物质起到吸收、分解异味和消臭作用;而且竹炭吸附速度快, 吸附设备简单、易操作, 尤其适宜于低浓度重金属废水的处理,是近几年研究较多的一种新型吸附剂(Wang M et al., 2011;Wang S Y et al., 2008;Halil,2003;Wang F Y et al., 2010)。热解后的竹炭具有较高的孔隙度,其孔隙度包括大孔隙、中孔和微孔,竹炭丰富的孔隙分布特征和高比表面积使其具有良好的吸附特性(Hameed et al., 2007;Wang S Y et al., 2008)。
本文研究了介质pH、竹炭粒径等条件下竹炭对水溶液中Ni(Ⅱ)离子吸附的影响,并进一步应用吸附热力学、动力学、等温吸附曲线、动态吸附和Thomas模型了解吸附过程,最后运用红外光谱分析吸附机制,同时也为竹炭吸附水溶液中Ni(Ⅱ)的应用提供一定的理论依据。
1 材料与方法 1.1 主要试剂和仪器试剂:竹炭(安吉竹圃炭业公司);0.1%二甲酚橙;pH=2.7~5.0缓冲液由NaAc-HAc配制;Ni(Ⅱ)离子标准溶液由纯度为99.9%的六水合硫酸Ni(Ⅱ)配制;其他试剂均为分析纯。
仪器:SK5200LH超声波清洗仪;AL204型电子天平;DELA320型酸度计;UV-2550型紫外分光光度计;DSHZ-300A型旋转式恒温振荡器;Nicolet380型红外分光光度仪;THZ-C-1型台式冷冻恒温振荡器。
1.2 竹炭预处理竹炭由浙江安吉竹圃炭业公司提供,磨碎至20~80目,然后用6 mol·L-1 NaOH浸泡24 h,再微波(高火)处理15 min,最后用蒸馏水洗净烘干备用。
1.3 静态吸附平衡试验称取预先处理好的一定量竹炭于碘量瓶中,加入一定量的特定pH的NaAc-HAc缓冲溶液浸泡24 h后,加入一定量的Ni(Ⅱ)离子标准溶液于恒温振荡器中振荡至平衡,振荡频率为100 r·min-1。检测方法:以0.1%的二甲酚橙作为显色剂,pH=5.73的NaAc-HAc溶液作为缓冲溶液,在波长570 nm处用分光光度法测水相中Ni(Ⅱ)的平衡浓度,按下式计算分配比(D)及吸附量(Q)(Erol et al., 2006;Fethiye et al., 2006):
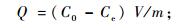
|
(1) |
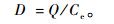
|
(2) |
式中:Q为平衡时刻竹炭的吸附量(mg·g-1);C0和Ce分别为起始时刻和平衡时刻溶液中Ni(Ⅱ)的浓度(mg·mL-1);m为竹炭干质量(g);V为溶液体积(mL)。
1.4 动态吸附平衡试验准确称取一定量的竹炭,用最佳pH的NaAc-HAc缓冲溶液浸泡24 h后装柱。加入一定体积的Ni(Ⅱ)标准液C0,控制液体流速为0.083 mL·min-1。以25.0 mL的流出液为单位收集,检测流出液中Ni(Ⅱ)离子的浓度(Ce),直至吸附达到饱和为止,即Ce=C0。
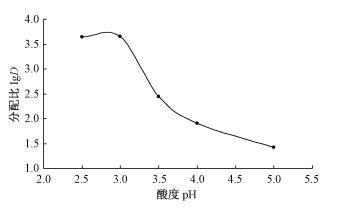
2 结果与讨论 2.1 溶液pH对吸附的影响准确称取5份50.0 mg的竹炭于碘量瓶中,在Ni(Ⅱ)离子的初始浓度C0=0.113 mg·mL-1,T=298 K条件下,考查介质溶液pH在2.5~5.0范围内对吸附分配比的影响,结果如图 1所示。由图 1可知,竹炭在pH=2.5,3.0时吸附分配比最大。因此,以下试验均在pH=3.0的HAc-NaAc缓冲溶液中进行。
|
图 1 pH对分配比的影响 Fig.1 Effect of pH on distribution ratio |
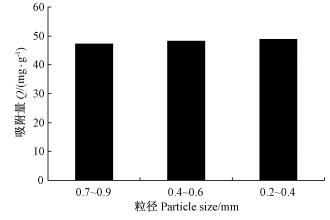
准确称取3份50.0 mg不同粒径竹炭,在pH=3.0的HAc-NaAc缓冲体系中,Ni(Ⅱ)的初始浓度为C0=0.113 mg·mL-1,溶液总体积为26.5 mL,置于恒温振荡器(100 r·min-1)在T=298 K条件下振荡至平衡,结果如图 2所示。由图 2可知,竹炭粒径变小,吸附能力有所增强,这是因为竹炭颗粒越小其比表面积越大。由于竹炭粒径大小对吸附量存在影响,因此以下所有试验中竹炭的粒径大小为0.2~0.4 mm。
|
图 2 粒径大小对吸附的影响 Fig.2 Effect of average particle size on adsorption |
吸附动力学是研究吸附过程中化学反应速率和反应机制的方法。通过动力学研究,可以知道如何控制反应条件,提高反应速率。通过反应速率的定量研究,还可以为科研成果的工业化进行最优设计和最优控制,为现有的生产选择最适宜的操作条件。吸附动力学可分为一级反应动力学模型和二级反应动力学模型,其表达式分别如下(Keskinkan et al., 2004;Ho et al., 2001):
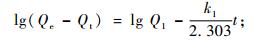
|
(3) |

|
(4) |
式中:Qe和Qt分别为吸附平衡时刻及t时刻的竹炭吸附量(mg·g-1);Q1和Q2分别为一级动力学和二级动力学竹炭的理论吸附量;k1和k2分别为一级动力学常数(g·mg-1min-1)和二级动力学常数(g·mg-1min-1)。
准确称取3份100.0 mg竹炭于碘量瓶中,分别在T=288,298和308 K,pH=3.00缓冲液,Ni(Ⅱ)离子初始浓度C0=0.214 mg·mL-1,振荡频率为100 r·min-1的条件下,每隔一定时间测定竹炭的吸附量。以Q~t作图得到图 3。由图 3可知,吸附过程基本发生在开始的1 h内,在这段时间内竹炭吸附速率较快,因为此期间溶液中Ni(Ⅱ)离子浓度较高,竹炭上的活性位点也较多。1 h以后,竹炭上的大多数活性位点被Ni(Ⅱ)离子占据,溶液中游离Ni(Ⅱ)离子与吸附在竹炭上的Ni(Ⅱ)离子又有相互排斥作用,因此使得吸附速率逐渐减小,最后达到吸附平衡。3种不同温度下竹炭对Ni(Ⅱ)的吸附平衡时间大致相同,都为100 min。

|
图 3 吸附的穿透曲线 Fig.3 Breakthrough curve for adsorption |
将图 3所得吸附穿透曲线数据用式(3)与式(4)动力学模型进行分析,动力学参数结果见表 1。
|
|
根据表 1,通过比较一级动力学和二级动力学的线性相关系数(R2),可以得到竹炭的吸附过程较为符合二级动力学模型,表明吸附过程有化学作用存在(Rao et al., 2008;Ho et al., 1998)。
2.4 温度对吸附的影响在一定温度下,吸附量与平衡浓度之间的关系称为吸附等温曲线。Langmuir模型和Freundlich模型是其中应用最为广泛的2种模型。
2.4.1 Freundlich等温吸附曲线(Freundlich, 1906)准确称取30.0,40.0,50.0,60.0和70.0 mg竹炭5份,在pH=3.00缓冲体系中浸泡24 h,加入2.5 mL 2 mg·mL-1的Ni(Ⅱ)离子标准液,分别在T=288,298和308 K,振荡频率为100 r·min-1的条件下振荡至平衡。测得平衡浓度Ce,求得吸附量Qe,按Freundlich等温式处理数据:
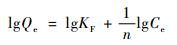
|
(5) |
式中:n为Freundlich常量;KF为Freundlich吸附系数;Qe为平衡时刻竹炭吸附量。
2.4.2 Langmuir等温吸附曲线(Langmuir, 1917)准确称取50.0 mg竹炭5份于碘量瓶中,分别在T=288,298,308 K,pH=3.00,C0分别为0.107,0.143,0.179,0.214和0.250 mg·mL-1,振荡频率为100 r·min-1的条件下振荡至平衡。测得平衡浓度Ce,求得吸附量Qe,按Langmuir吸附等温式处理数据:
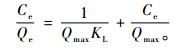
|
(6) |
式中:Qmax为竹炭的Langmuir饱和吸附量;KL为Langmuir常量。
根据式(5)和(6)对所得试验数据进行方程拟合,结果见表 2。
|
|
根据表 2,通过比较Freundlich曲线和Langmuir曲线的线性相关系数(R2),可知竹炭对Ni(Ⅱ)的吸附过程能较好地符合Langmuir吸附等温线,表明竹炭对Ni(Ⅱ)的吸附可能为单分子层吸附。
2.4.3 吸附热力学(Xiong et al.,2009a)准确称取3份50.0 mg竹炭,在C0=0.179 mg·mL-1,pH=3.00,振荡频率为100 r·min-1的条件下,分别研究在288,298和308K下,竹炭吸附Ni(Ⅱ)的分配比的变化。根据热力学公式对试验数据处理:

|
(7) |
式中:D为分配比;ΔH为焓变;ΔS是熵变;R为摩尔气体常数(8.314 J·mol-1K-1);T为绝对温度(K)。
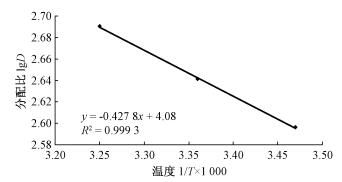
以lgD对1/T作图,结果如图 4所示,直线线性相关系数为R2=0.999 3。由图 4可知,温度升高吸附分配比增大,说明吸附可能是吸热反应,同样可以认为吸附有化学吸附作用存在(Unlu et al.,2006)。根据图 4可以得到ΔH=8.19 kJ·mol-1,ΔS=78.12 J·mol-1K-1。根据吉布斯方程:
|
图 4 温度对分配比的影响 Fig.4 Effect of temperature on distribution ratio |
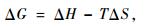
|
(8) |
恒温恒压下,化学反应的净推动力或趋势可用吉布斯函数变化来量度。当T=298 K时,ΔG=ΔH-TΔS=-15.08 kJ·mol-1,ΔG < 0表明竹炭吸附Ni(Ⅱ)反应在T=298 K下自发进行。热力学结果表明,自由能的减小和熵值的增大对竹炭吸附Ni(Ⅱ)有推动作用。
2.5 动态吸附准确称取200.0 mg竹炭,在T=298 K,pH=3.00缓冲溶液,振荡速率100 r·min-1下浸泡24 h后装柱,将初始浓度为C0=0.024 mg·mL-1的Ni(Ⅱ)标准溶液以0.083 mL·min-1的速率进行动态吸附试验,以25 mL的流出液为单位分段收集,测其吸光度,求得流出液中Ni(Ⅱ)离子的浓度(Ce),直至流出液中Ni(Ⅱ)浓度Ce等于C0为止,以Ce/C0对流出液体积V作动态吸附曲线。动态吸附量(Q)根据下式计算(Tabakci et al., 2008):
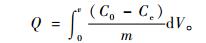
|
(9) |
式中:V为流出液体积(mL);m为干竹炭质量(g)。
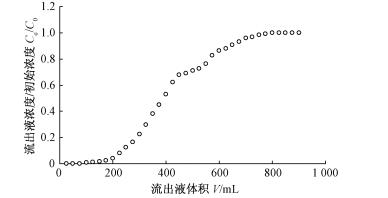
竹炭对Ni(Ⅱ)离子的动态吸附曲线见图 5。从图 5可知,当V<100 mL时,从离子柱子底部流出液中Ni(Ⅱ)金属离子接近0,同样Ce/C0值也接近于0,表明流出液中的Ni(Ⅱ)离子全部被竹炭吸附; 当100<V<800 mL时,流出液中Ni(Ⅱ)离子浓度逐渐增大,这是由于随着吸附的进行,竹炭的吸附容量有限,竹炭表面上有效活性位点大多被Ni(Ⅱ)离子占据,导致吸附量急速下降; 当V>800 mL时,流出液中Ni(Ⅱ)离子浓度Ce=C0,说明竹炭失去吸附能力,柱子失去作用,动态吸附到达饱和状态。
|
图 5 动态吸附曲线 Fig.5 Dynamic adsorption curve |
根据动态吸附情况,本文用Thomas模型预测试验相关数据准确性(Chen,2010),其公式表示为:
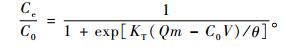
|
(10) |
式中:KT为Thomas常数(mL·min-1mg-1);Q为竹炭饱和吸附容量(mg·g-1);m为干竹炭质量(g);V为流出液体积(mL);C0为Ni(Ⅱ)金属离子的初始浓度(mg·mL-1);θ为Ni(Ⅱ)离子过柱速率(mL·min-1)。其公式也可如下表达:

|
(11) |
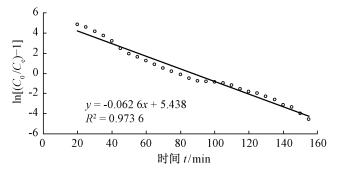
以ln[(C0/Ce)-1]对t作图,根据图 6可得KT与Q。Thomas模型拟合试验数据得到其相关参数:KT=4.3×10-2 mL·mg-1min-1,Q=52.5 mg·g-1,R2=0.973 6。
|
图 6 Thomas模型 Fig.6 Thomas model |
结果表明:试验数据能较好地符合Thomas模型,因为线性相关系数R2=0.973 6。Thomas模型所得饱和吸附容量值Q=52.5 mg·g-1,与试验所得饱和吸附容量值Q=55.57 mg·g-1接近,可知Thomas模型能较好地拟合竹炭吸附Ni(Ⅱ)离子的穿透曲线。
2.6 红外光谱分析(Xiong et al., 2009b;2009c)红外光谱能分析一些重要的官能团的变化。图 7中显示竹炭在吸附前后1 000~3 500 cm-1范围内官能团的伸缩和弯曲振动变化。图中曲线a是吸附前竹炭;曲线b是吸附后竹炭。对比可知:吸附后1 696 cm-1处CO的特征吸收峰消失,表明竹炭中的功能基CO发生配位反应;吸附后竹炭的功能基—OH的伸缩振动发生红移现象, 由原来的3 439 cm-1移到3 412 cm-1,表明功能基—OH中的O发生配位反应。

|
图 7 竹炭的红外光谱 Fig.7 Infrared spectra of bamboo charcoal |
研究显示,竹炭吸附水溶液中的Ni(Ⅱ)离子受到溶液酸碱度、平均粒径、初始浓度、接触时间、反应时间和温度的影响。用一级反应动力学模型和二级反应动力学模型研究吸附动力学,结果发现二级动力学方程能更好地反映吸附过程。同样,相比Freundlich曲线,吸附行为能更好地符合Langmuir曲线。ΔH=8.19 kJ·mol-1说明吸附是吸热反应,温度的升高有利于吸附的进行。Thomas模型在预测试验柱合理性中表现良好。红外光谱分析竹炭吸附前后相关官能团的变化:1)竹炭中的功能基CO发生配位反应;2)竹炭的功能基—OH的伸缩振动发生红移现象, 由原来的3 439 cm-1移到3 412 cm-1。总之, 竹炭可以有效地用于去除水溶液中的Ni(Ⅱ)离子。
| [] | Chen Q. 2010. Study on the adsorption of Lanthanum (Ⅲ) from aqueous solution by bamboo charcoal. Journal of Rare Earths, 28(1): 125–131. |
| [] | Diniz V, Volesky B. 2005. Biosorption of La, Eu and Yb using Sargassum biomass. Water Research, 39(1): 239–247. DOI:10.1016/j.watres.2004.09.009 |
| [] | Elouear Z, Bouzid J, Boujelben N. 2009. Removal of nickel and cadmium from aqueous solutions by sewage sludge ash: study in single and binary systems. Environmental Technology, 30(6): 561–570. DOI:10.1080/09593330902824940 |
| [] | Erol P, Turkan A. 2006. The study of various parameters affecting the ion exchange of Cu2+, Zn2+, Ni(Ⅱ), Cd2+, and Pb2+ from aqueous solution on Dowex 50W synthetic resin. Journal of Hazardous Materials, 134(1/3): 149–156. |
| [] | Fethiye G, Erol P. 2006. Removal of chromium(Ⅲ) from aqueous solutions using Lewatit S 100: the effect of pH, time, metal concentration and temperature. Journal of Hazardous Materials, 136(2): 330–337. DOI:10.1016/j.jhazmat.2005.12.021 |
| [] | Freundlich H M F. 1906. Over the adsorption in solution. Zeitschrift für Physikalische Chemie, 57: 385–470. |
| [] | Halil H. 2003. Adsorption of nickel(Ⅱ) from aqueous solution onto activated carbon prepared from almond husk. Journal of Hazardous Materials, 97(1/3): 49–57. |
| [] | Hameed B H, Din A T M, Ahmad A L. 2007. Adsorption of methylene blue onto bamboo-based activated carbon: kinetics and equilibrium studies. Journal of Hazardous Materials, 141(3): 819–825. DOI:10.1016/j.jhazmat.2006.07.049 |
| [] | Ho Y S, McKay G. 1998. A comparison of chemisorption Kinetic models applied to pollutant removal on various sorbents. Process Safety and Environmental Protection: Transactions of the Institution of Chemical Engineers, 76(4): 332–340. DOI:10.1205/095758298529696 |
| [] | Ho Y S, Ng J C Y, McKay G. 2001. Removal of lead (Ⅱ) from effluents by sorption on peat using second-order kinetics. Separation Science and Technology, 36(2): 241–261. DOI:10.1081/SS-100001077 |
| [] | Keskinkan O, Goksu M Z L, Basibuyuk M, et al. 2004. Heavy metal adsorption properties of a submerged aquatic plant (Ceratophyllum demersum). Bioresource Technology, 92(2): 197–200. DOI:10.1016/j.biortech.2003.07.011 |
| [] | Langmuir I. 1917. The constitution and fundamental properties of solids and liquids. Journal of the American Chemical Society, 39(9): 1848–1906. DOI:10.1021/ja02254a006 |
| [] | Rao M M, Rao G P, Seshaiah K. 2008. Activated carbon from Ceiba pentandra hulls, an agricultural waste, as an adsorbent in the removal of lead and zinc from aqueous solutions. Waste Management, 28(5): 849–858. DOI:10.1016/j.wasman.2007.01.017 |
| [] | Tabakci M, Yilmaz M. 2008. Sorption characteristics of Cu(Ⅱ) ions onto silica gel-immobilized calixarene polymer in aqueous solutions: batch and column studies. Journal of Hazardous Materials, 151(2/3): 331–338. |
| [] | Unlu N, Ersoz M. 2006. Adsorption characteristics of heavy metal ions onto a low cost biopolymeric sorbent from aqueous solutions. Journal of Hazardous Materials, 136(2): 272–280. DOI:10.1016/j.jhazmat.2005.12.013 |
| [] | Wang F Y, Wang H, Ma J W. 2010. Adsorption of cadmium (Ⅱ) ions from aqueous solution by a new low-cost adsorbent—bamboo charcoal. Journal of Hazardous Materials, 177(1/3): 300–306. |
| [] | Wang M, Huang Z H, Liu G J. 2011. Adsorption of dimethyl sulfide from aqueous solution by a cost-effective bamboo charcoal. Journal of Hazardous Materials, 190(1/3): 1009–1015. |
| [] | Wang S Y, Tsai M H, Lo S F. 2008. Effects of manufacturing conditions on the adsorption capacity of heavy metal ions by Makino bamboo charcoal.. Bioresource Technolog, 99(15): 7027–7033. DOI:10.1016/j.biortech.2008.01.014 |
| [] | Xiong C H, Yao C P. 2009a. Preparation and application of acrylic acid grafted polytetrafluoroethylene fiber as a weak acid cation exchanger for adsorption of Er(Ⅲ). Journal of Hazardous Materials, 170(2/3): 1125–1132. |
| [] | Xiong C H, Yao C P. 2009b. Study on the adsorption of cadmium(Ⅱ) from aqueous solution by D152 resin. Journal of Hazardous Materials, 166(2/3): 815–820. |
| [] | Xiong C H, Yao C P, Wang L. 2009c. Adsorption behavior of Cd(Ⅱ) from aqueous solutions onto gel-type weak acid resin.. Hydrometallurgy, 98(3/4): 318–324. |
 2012, Vol. 48
2012, Vol. 48