文章信息
- 王献玲, 方桂珍, 戴晓峰, 张锐
- Wang Xianling, Fang Guizhen, Dai Xiaofeng, Zhang Rui
- 二醛基纤维素的制备及其对尿素的吸附性能
- Preparation of Dialdehyde Cellulose and Adsorption for Urea
- 林业科学, 2011, 47(4): 141-146.
- Scientia Silvae Sinicae, 2011, 47(4): 141-146.
-
文章历史
- 收稿日期:2009-06-29
- 修回日期:2009-12-03
-
作者相关文章
2. 康龙化成新药技术有限公司 北京 100176
2. Kanglonghuacheng New Medicine Technology Limited Company Beijing 100176
慢性肾衰竭(CRF)是一种严重威胁患者生命的疾病,我国每年新增加肾衰病人20万人。慢性肾衰竭病人由于肾功能障碍,引起代谢产物在体内潴留,血中尿素氮(BUN)和血肌酐(Cr)浓度升高,导致肠中BUN和Cr的浓度也明显升高(王虹等,2001;黄铮等,2000)。口服吸附剂是最近发展起来的慢性肾衰竭的一种新的治疗方法,采用口服吸附剂对胃肠道中积聚的毒素进行吸附,然后经消化道排出体外,能够延迟肾衰发展进程、减少尿毒症的发生和血液透析的次数,对慢性肾衰竭的早期预防和防治是非常重要的(王少敏等,2003;于九皋等,2002;Koide et al., 1991)。
目前,市场上使用的治疗慢性肾衰竭的口服吸附剂主要有活性炭类和氧化淀粉类。活性炭吸附靶性差、吸附容量低、患者服用剂量大、生物相容性较差。氧化淀粉与氧化纤维素化学结构相似,可以利用其活性醛基与尿素的—NH2发生schiff反应,形成schiff’s碱排出体外,达到延迟慢性肾衰竭发展进程的作用。由于纤维素具有无毒、不被人体消化吸收、可用作膳食纤维、生物相容性好、醋酸纤维素膜很早用作血液透析的材料(Hoenich et al., 1995)的特点,目前国内外对具有纤维素特征的氧化纤维素的研究比较活跃,关于其用作慢性肾衰竭毒素的口服吸附剂的研究也有一些。本文研究了碱活化后微晶纤维素的氧化和二醛基纤维素对尿素的吸附性能,探讨了醛基含量与尿素吸附容量之间的关系,分析了二醛基纤维素对尿素的吸附动力学曲线和吸附等温线,为二醛基纤维素作为慢性肾衰竭毒素的吸附剂研究提供了基础数据。
1 材料与方法 1.1 试剂与仪器微晶纤维素(MCC),A型,湖州展望药业有限公司;高碘酸钠、乙二醇、氢氧化钠、硫酸、尿素和对二甲氨基苯甲醛等均为分析纯。
D/max-r B型X射线衍射仪,日本理学;Magna-560傅里叶变换红外光谱仪,美国尼高力公司;EA3000型元素分析仪,意大利Euro公司;Tu-1800PC紫外分光光度计,北京普析通用仪器有限责任公司。
1.2 微晶纤维素的碱预处理称取一定量的微晶纤维素加入到质量分数为14%的氢氧化钠溶液中,浸泡24 h,蒸馏水充分洗涤至中性,抽滤,真空干燥,研碎备用。
1.3 二醛基纤维素的制备及试验设计棕色三口烧瓶中加入一定量的蒸馏水和高碘酸钠,用硫酸调节pH值,快速加入碱活化,加热到预定温度,恒温搅拌一定时间,用乙二醇分解未反应的高碘酸钠,过滤,滤饼用蒸馏水充分洗涤至IO3-消失,45 ℃真空干燥24 h。分别改变单因素反应温度、pH介质、反应时间、物料比等对醛基的含量进行检测,每个条件进行2次重复确认。
1.4 二醛基纤维素的结构表征 1.4.1 醛基含量的测定采用碱熔法测定(郑昌戈等,1996)。
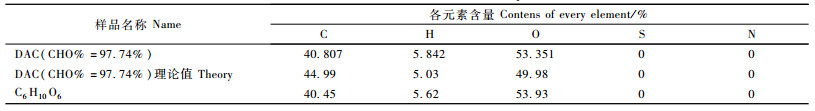
1.4.2 元素分析样品经真空干燥后,用意大利Euro公司的EA3000型元素分析仪测定C,H,N元素含量。
1.4.3 X射线衍射(XRD)测试采用日本理学D/max-r B型X射线衍射仪观察MCC、二醛基纤维素的结晶结构,Cu靶,Ka射线,Ni片滤光,λ=1.540 5×10-10 m,管压45 kV,电流40 mA,扫描范围:2θ=1~90°;分峰法计算结晶度(Xc),以谢乐公式计算晶粒大小,即Lhkl= Kλ/βcosθ,β为半峰宽,K为谢乐常数,取0.94。
1.4.4 红外光谱测试微晶纤维素和二醛基纤维素经真空干燥后,KBr压片法测其红外光谱。
1.5 尿素吸附性能的测定精确称取0.2 g二醛基纤维素试样,移取10 mL尿素氮浓度为6.0 g·L-1尿素透析液,在37 ℃的振荡水浴上吸附5 h后,过滤,滤液用对二甲氨基苯甲醛比色法测定残余尿素的浓度(蒋萌阳等,2005)。按下式计算出二醛基纤维素对尿素的吸附容量:
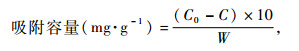
|
式中:C0为吸附前溶液中尿素氮的浓度,mg·mL-1;C为吸附后溶液中尿素氮的浓度,mg·mL-1;W为称取吸附剂的干基质量,g。
吸附等温线:准确称取相同质量的二醛基纤维素,测定二醛基纤维素在不同尿素质量浓度的透析液(pH=7)中对尿素的吸附容量。
吸附动力学曲线:在吸附时间为1,2,3,4,6,8,10,12 h的条件下,测定二醛基纤维素对尿素的吸附容量。
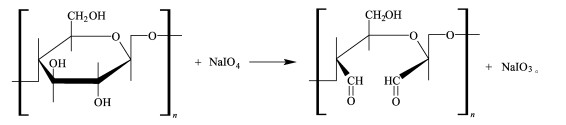
2 结果与讨论纤维素与高碘酸钠发生选择性氧化反应,使2,3位羟基发生断裂(Sussich et al., 2000),生成二醛基纤维素,反应方程式如下:
|
尿素上的胺基与二醛基纤维素上的醛基发生schiff’s碱反应(武越寰等,2002),生成尿素衍生物,随消化道排出体外,可达到降低胃肠中尿素浓度的作用。反应方程式如下:
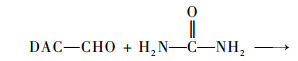
|
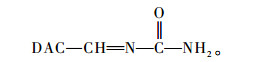
|
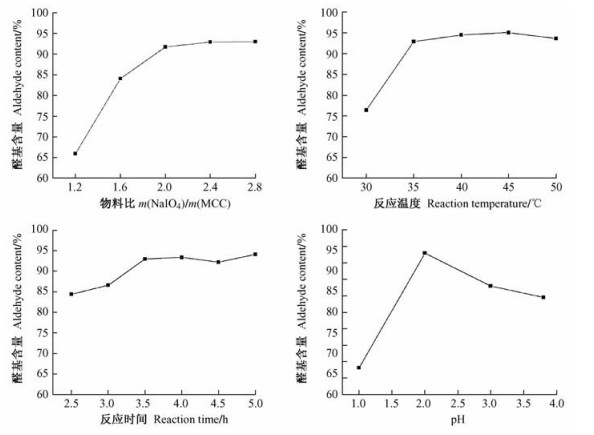
醛基含量是微晶纤维素氧化程度的量化指标,它的大小直接反映了纤维素的氧化水平。影响醛基含量的因素主要有高碘酸钠和微晶纤维素的质量比、反应温度、反应时间和反应介质的pH值。采用单因素试验,探讨各因素对醛基含量的影响,制订出二醛基纤维素合成较佳条件(图 1)。
|
图 1 物料比、反应温度、反应时间和介质pH对DAC醛基含量的影响 Figure 1 The influence of aldehyde content of DAC on the amount of substance, temperature of reaction, the time of reaction and the medium of reaction |
结果表明,二醛基纤维素合成的较佳条件为:高碘酸钠与二醛基纤维素的质量比为2.4:1,反应温度为35 ℃,反应时间为3.5 h,反应介质的pH为2,此时二醛基纤维素的醛基含量为97.74%,得率为75.67%。
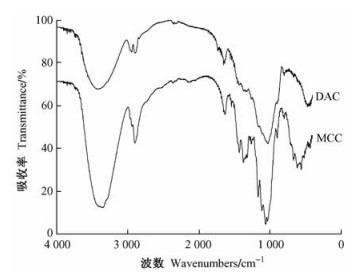
2.2 二醛基纤维素的结构分析 2.2.1 红外谱图分析图 2是微晶纤维素和二醛基纤维素的FTIR图。从FTIR图中可以看出:二醛基纤维素DAC在1 730 cm-1处有醛基峰出现(Zhbankov,1966),但是强度比较小,因为醛基很少以游离醛基的形式存在,而是形成了水合半醛醇和分子内及分子间的半缩醛(Varmat et al., 1995)的形式,DAC图中1 026 cm-1处C—O伸缩振动吸收峰,进一步说明羰基是以半缩醛或缩醛的形式存在的。MCC和DAC在1 641 cm-1都有一吸收峰,表明MCC和DAC强烈吸附水分用一般的方法未能除去。DAC中3 360 cm-1处羟基O—H伸缩振动吸收峰比MCC明显减弱,1 112,1 058 cm-1处羟基的C—O特征吸收峰减弱或消失,可见纤维素被氧化为二醛基纤维素。
|
图 2 微晶纤维素和氧化纤维素的红外谱 Figure 2 FTIR spectra of MCC and DAC |
醛基含量为97.74%的二醛基纤维素的元素分析结果如表 1所示。从表中可以看出:二醛基纤维素的实测值与理论值相差较大,但是与单元式C6H10O6的C,H,O含量相符。二醛基纤维素其理论的单元结构式为C6H8.04O5,元素分析结果表明其单元式符合C6H10O6,正是二醛基纤维素葡萄糖残基结合1个水分子后的单元式。因此,二醛基纤维素中的醛基并不是以游离状态存在的,而是二醛基纤维素每个葡萄糖单元残基中吸着1个水分子,形成水合半缩醛的形式,这与DAC的FTIR图中羰基吸收峰峰强较小相符。二醛基纤维素每个葡萄糖残基结合1个水分子后的元素分析值与理论值相符,表明产品有较高的纯度。
|
|
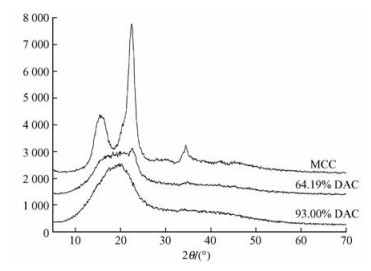
醛基含量为64.19%和93.00%的二醛基纤维素和微晶纤维素的XRD图见图 3。从图中可以看出:纤维素内部明显存在结晶区;MCC经NaIO4氧化生成DAC后,结晶结构被破坏,衍射角2θ=22.7°处衍射峰的峰强大幅度下降,且峰强下降的程度与氧化度成正比(Varmat et al., 1997)。醛基含量为64.19%的氧化纤维素在衍射角2θ=22.7°处仍存在一个小的衍射峰,说明微晶纤维素未反应完全,二醛基纤维素仍保留部分微晶纤维素的峰型,具有部分纤维素的性质;而醛基含量为93.00%的二醛基纤维素的峰型已完全发生改变,没有保留纤维素的特征衍射峰,仅在2θ=20.5°附近存在一个弥散峰,说明纤维素的结晶结构基本被完全破坏,二醛基纤维素已基本呈无序状态。表明纤维素被氧化后生成的醛基对其结晶结构造成了一定的破坏,使结晶度大幅度下降,从而起到对纤维素活化的作用。
|
图 3 微晶纤维素和氧化纤维素的X射线衍射图谱 Figure 3 XRD spectra of MCC and DAC |
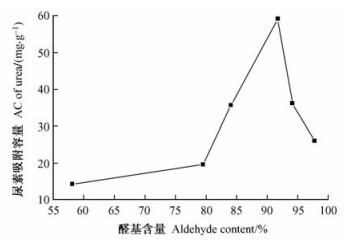
二醛基纤维素中的醛基与人体内的尿素结合生成西佛碱,随粪便排出体外。本试验模拟人体尿素透析液,考察醛基含量为58.11%,79.50%,84.09%,91.74%,94.10%和97.74%的二醛基纤维素在相同的条件下(6.0 g·L-1尿素透析液,吸附时间为5 h,吸附温度为37 ℃)对尿素的吸附容量,测定结果如图 4所示。从图中可以看出:随着DAC醛基含量的增大,尿素吸附容量相应增大。在高碘酸钠与微晶纤维素的质量比为2、反应温度为35 ℃、反应时间为3.5 h、反应介质的pH为2反应条件下,所制备的醛基含量为91.74%的DAC对尿素的吸附容量最大为59.23 mg·g-1;醛基含量为94.10%的DAC尿素吸附容量反而下降。这主要是由于醛基含量较低时,醛基与尿素的接触几率小,因而吸附容量较小; 而二醛基纤维素的醛基含量过高,氧化程度大,无定形区占的比例大,二醛基纤维素在吸附过程中有部分溶解,吸附到二醛基纤维素上的尿素随二醛基纤维素的溶解而脱落,因此醛基含量过高时吸附容量不高。
|
图 4 DAC的醛基含量对尿素吸附性能的影响 Figure 4 The influence of aldehyde content of DACon urea adsorption capacity |
二醛基纤维素对尿素的吸附容量最大为59.23 mg·g-1,是包醛氧淀粉尿素吸附容量的10倍(6 mg·g-1),是包醛酶淀粉吸附容量的4倍(15 mg·g-1),高于目前市售的氧化淀粉口服吸附剂。
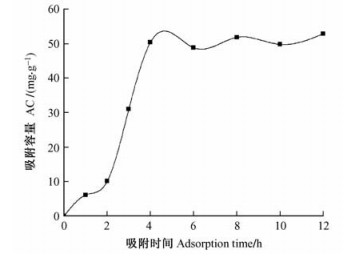
2.3.2 二醛基纤维素对尿素的吸附动力学曲线图 5是在37 ℃时、醛基含量为91.74%的DAC对尿素的吸附动力学曲线。从图中可以看出:开始阶段,二醛基纤维素的吸附容量增长较快,随着吸附时间的增加,吸附速率逐渐减缓,二醛基纤维素对尿素的吸附平衡时间为4 h左右,4 h之后达到一个平台期,接近吸附平衡。主要是因为吸附剂上有大量的亲水基,在透析液中易溶胀,故达到吸附平衡较为容易。食物在胃中的停留时间约为1 h,在肠中的停留时间为7~8 h。因此,尿素在DAC上的平衡时间与人体的消化周期基本一致,符合药物代谢动力学要求。
|
图 5 DAC对尿素的吸附动力学曲线 Figure 5 The kinetic curves of urea onto DAC |
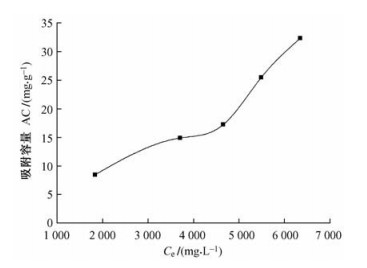
通过分析吸附等温线可以判断二醛基纤维素对尿素的吸附作用方式,图 6是醛基含量为97.74%的DAC,分别在尿素初始质量浓度为2,4,5,6,7 g·L -1的透析液中,温度37 ℃吸附5 h时对尿素的吸附等温线。从图中可以看出:随着初始尿素质量浓度的增大,DAC对尿素的吸附容量增大。
|
图 6 DAC对尿素的吸附等温线 Figure 6 The adsorption isotherm curve of urea onto DAC |
在吸附平衡研究中,描述吸附等温线最常用的表达式是Freundich方程和Langmuir方程。图 6显然不符合Langmuir方程,因此以Freundich方程对平衡数据进行线性拟合。Freundich方程的线性化形式为:

|
式中:AC为吸附平衡时二醛基纤维素对尿素的吸附容量,mg·g-1;Ce为吸附后尿素透析液中尿素的平衡浓度,mg·L-1;k为常数。
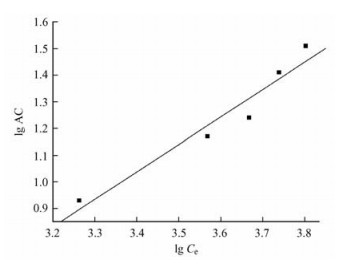
尿素在二醛基纤维素上的吸附平衡数据对Freundich方程拟合结果见图 7,并产生线性方程:lgAC=1.021 8lgC0+ 0.591 9,相关系数R2=0.952 3。由此方程可以计算出参数k=3.91,n=0.98,Freundich方程为AC=3.91Ce1.02。因此二醛基纤维素具有一定的化学吸附性。
|
图 7 DAC对尿素平衡吸附的Freundich等温线 Figure 7 The Freundich adsorption istherm curve of urea onto DAC |
二醛基纤维素制备条件为:高碘酸钠与纤维素的质量比为2.4,反应温度为35 ℃,反应时间为3.5 h,反应介质的pH为2,此时二醛基纤维素的醛基含量为97.74%,得率为75.67%。
通过红外光谱、元素分析、X射线衍射以及化学官能团测定(碱熔法测醛基含量)等手段对二醛基纤维素的结构进行表征,结果表明:二醛基纤维素已生成,且纯度较高。
二醛基纤维素是一种很有潜力的治疗慢性肾衰竭的药物。二醛基纤维素在37 ℃、pH=7的透析液中,对尿素的最大吸附容量是59.23 mg·g-1, 是包醛氧淀粉尿素吸附容量的10倍(6 mg·g-1),是包醛酶淀粉吸附容量的4倍(15 mg·g-1)。二醛基纤维素对尿素的吸附平衡时间为4 h左右, 吸附等温线能很好地符合Freundich方程,对尿素具有一定的化学吸附。
黄铮, 蒋云生, 罗季安. 2000. 慢性肾衰与胃肠道的鸟毒素清除[J]. 国外医学泌尿系统分册, 20(S1): 13-15. |
蒋萌阳, 包淼清. 2005. 对二甲氨基苯甲醛比色法在常量尿素测定中的应用[J]. 浙江化工, 36(2): 36-38. |
王虹, 徐家毅, 袁直, 等. 2001. 尿毒症毒素及其清除方法——兼论临床上的血液灌流治疗[J]. 离子交换与吸附, 17(5): 377-384. |
王少敏, 于九皋. 2003. 仲胺型硝化纤维素的合成及应[J]. 应用化学, 20(11): 1080-1083. DOI:10.3969/j.issn.1000-0518.2003.11.014 |
武越寰, 李伟昶, 申晓明. 2002. 有机化学[M]. 合肥: 中国科学技术大学出版社: 338.
|
于九皋, 杨冬芝. 2002. 3, 5-二硝基苯甲酸淀粉酯的合成及应用[J]. 应用化学, 19(9): 858-861. |
郑昌戈, 姚笑红, 何艳辉, 等. 1996. 双醛淀粉的合成及其氧化度的测定[J]. 湘潭大学自然科学学报, 18(1): 70-73. |
Sussich F, Cesàro A. 2000. The kinetics of periodate oxidation of carbohydrates:a calorimetric approach[J]. Carbohydr Res, 329(1): 87-95. DOI:10.1016/S0008-6215(00)00158-0 |
Hoenich N A, Woffindin C, Mathews J N S, et al. 1995. Biocompatibility of membranes used in the treatment of renal failure[J]. Biomaterials, 16(8): 587-592. DOI:10.1016/0142-9612(95)93855-8 |
Koide K, Sano M, Takeda F, et al. 1991. A study of oral adsorbent in chronic renal failure[J]. Artificial Cells, and Blood Substitutes Biotechnology, 19(1): 147-166. DOI:10.3109/10731199109117822 |
Varmat A J, Chavan V B. 1995. A study of crystallinity changes in oxidized cellulose[J]. Polym Degrad and Stab, 49(2): 245-250. DOI:10.1016/0141-3910(95)87006-7 |
Varmat A J, Chavan V B, Rajmohanan P R, et al. 1997. Some observations on the high-resolution solid-state CP-MAS 13C-NMR spectra of periodate-oxidised cellulose[J]. Polym Degrad and Stab, 58(3): 257-260. DOI:10.1016/S0141-3910(97)00049-9 |
Zhbankov R G. 1966. Infrared spectra of cellulose and its derivatives[M]. New York: Consultants Bureau: 122.
|
 2011, Vol. 47
2011, Vol. 47