氧气是人体赖以生存的基本化学物质,也是潜艇内部柴电动力系统正常运转的必需气体。潜艇舱室环境中的氧气浓度不仅直接关系艇员的生命安全,同时显著影响着潜艇整体战斗力的生成,被公认为是制约潜艇水下潜航能力的主要因素。因此,潜艇舱室空气中的氧气必须维持在适宜浓度范围内,通常在体积浓度18%~21%之间,以保障艇员各项生理活动和作战行动的需要。然而,与开放流动的陆地空气环境不同,对于潜航期间与外界空气隔绝的密闭潜艇舱室而言,氧气浓度的有效控制极大程度地依赖先进物理化学供氧技术与装置的发展[1 - 2]。
目前,电解水制氧、压缩氧气或液氧转化、固体化学制氧装置供氧是潜艇舱室的主要供氧方式。其中,以氯酸盐热分解制氧为代表的固体化学制氧技术作为最先发展的供氧技术之一,具有比储氧量高(储氧密度可达压缩氧气的3倍,与液氧相近)、供氧速率快、使用时无需外源供能、结构和使用简便等特点,可作为潜艇舱室的常备或应急供氧源[3 − 7]。自二战期间美国海军成功开发氯酸盐化学供氧技术以来,当前世界各国海军潜艇普遍采用氯酸盐化学供氧装置作为氧源。氯酸盐化学供氧装置是多数常规潜艇的唯一供氧来源,也是核潜艇的备用和应急供氧装备,为潜艇安全航行提供了可靠的氧气保障,一直受到舰船科学技术领域的持续关注[8 − 9]。
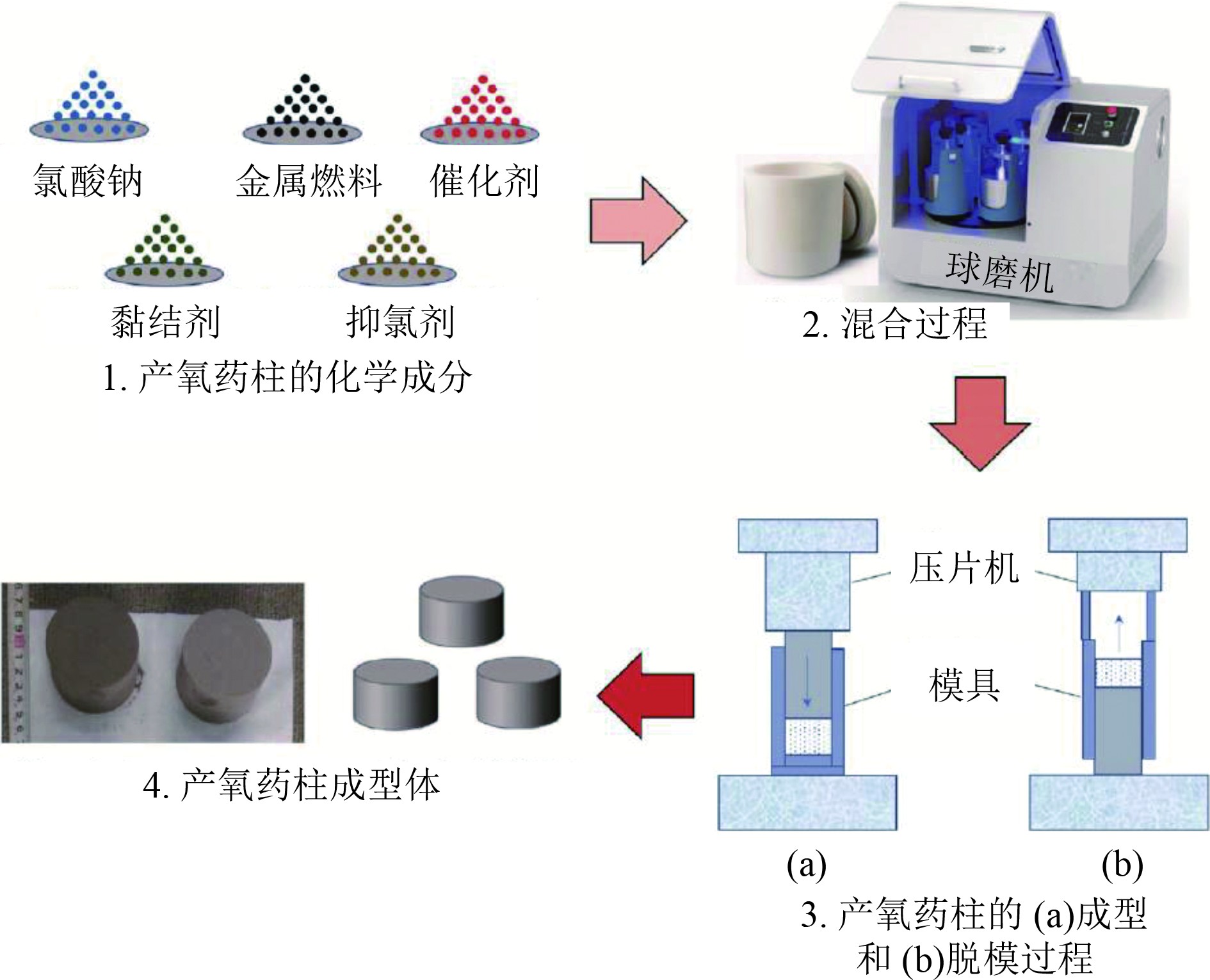
1 工作原理与装置组成潜艇舱室氯酸盐化学供氧技术基于产氧药柱的高温分解反应释放氧气。研究表明[3,10],产氧药柱的分解可划分为初始反应阶段、快速上升阶段、快速衰减阶段和稳定结束阶段4个阶段,过程中可能涉及的化学反应如式(1)~式(4)所示。通常,产氧药柱以氯酸盐(一般为NaClO3、KClO3或NaClO4、KClO4)为主体储氧物质,以金属粉体(Fe粉、Al粉、Mg粉等)作为燃料,同时添加一定比例的催化剂(金属氧化物)、抑氯剂和黏结剂等功能助剂,混合均匀后经干法压制、湿法压制或浇铸成型制成[8]。其中,金属燃料燃烧释放出大量热量以维持氯酸盐分解反应自持进行,催化剂用以提高氯酸盐分解反应速率并降低分解温度,抑氯剂则用于主要去除Cl2等含氯副产物(式(5))。采用干法压制工艺制备产氧药柱的过程如图1所示。
|
图 1 干法压制工艺制备产氧药柱过程的示意图[3] Fig. 1 Schematic diagram of the preparation of chemical oxygen generation blocks via dry pressing process[3] |
| $ {\mathrm{MClO}}_{3} \mathop {\longrightarrow}\limits^{\text{催化剂}}_{\Delta}{\mathrm{MCl}}+1.5{\mathrm{O}}_{2}\uparrow $ | (1) |
| $ {\mathrm{MClO}}_{3} \mathop {\longrightarrow}\limits^{\text{催化剂}}_{\Delta}0.75{\mathrm{MClO}}_{4}+0.25{\mathrm{MCl}} $ | (2) |
| $ {\mathrm{MClO}}_{4} \mathop {\longrightarrow}\limits^{\text{催化剂}}_{\Delta}{\mathrm{MCl}}+2{\mathrm{O}}_{2}\uparrow $ | (3) |
| $ 2{\mathrm{MClO}}_3 \mathop {\longrightarrow}\limits^{\mathrm{H_2O}}_{\Delta} {\mathrm{M}}_2{\mathrm{O}}+2.5{\mathrm{O}}_2\uparrow +{\mathrm{Cl}}_2\uparrow $ | (4) |
| $ \mathrm{BaO}_2+\mathrm{Cl}_2\longrightarrow\mathrm{BaCl}_2+\mathrm{O}_2 $ | (5) |
式中,M代表Na、K等碱金属。
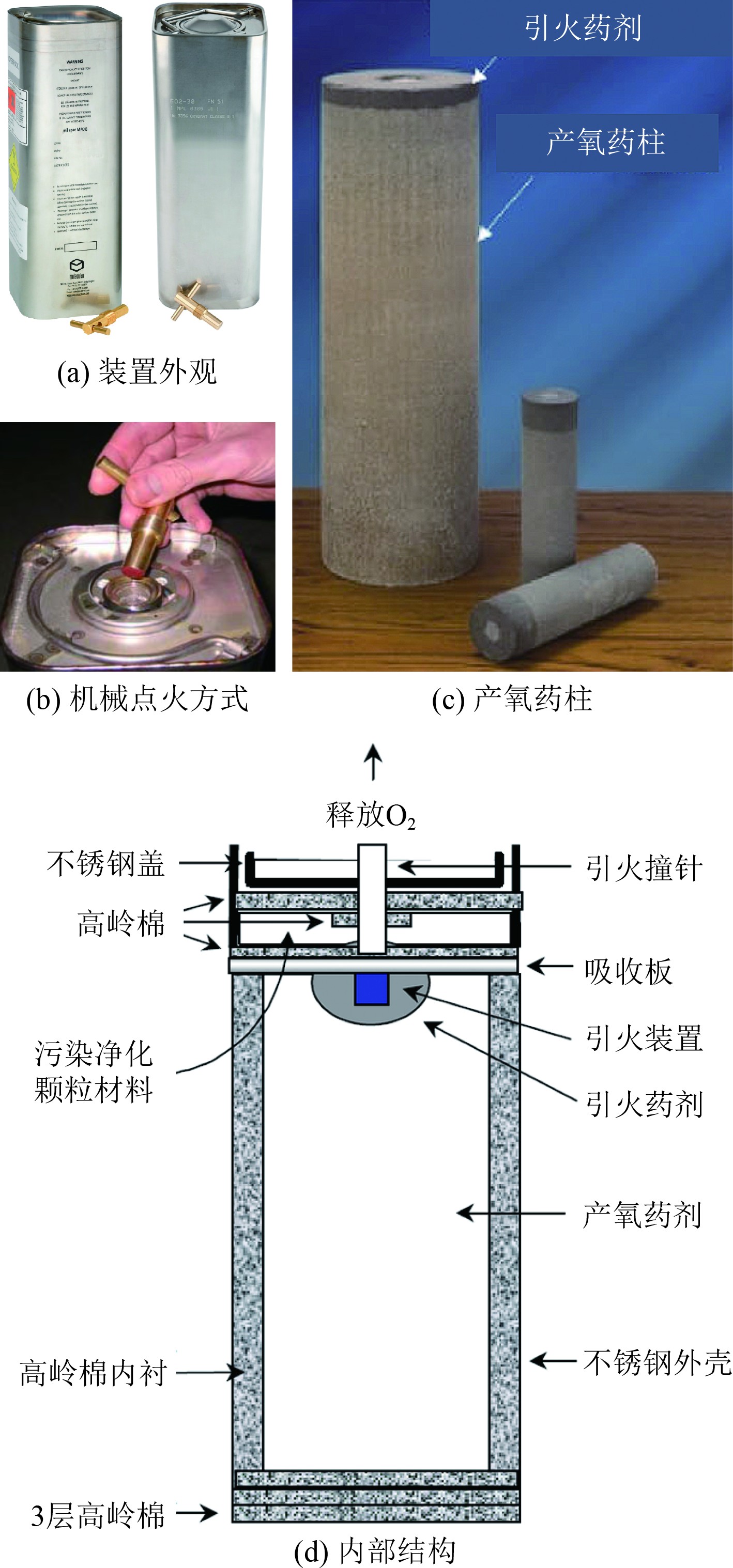
潜艇舱室氯酸盐化学供氧装置以产氧药柱为结构核心,主要由包覆在产氧药柱周围的隔热层、气体净化过滤层以及启动机构(含引火药剂)、机械外壳、外部防护净化装置等部分构成[5],如图2所示。在装置使用时,通过机械点火或电子点火等方式启动引火药剂产生足够的热量,进而引燃产氧药柱,并利用金属燃料燃烧释放的热量维持氯酸盐分解反应自持进行,不断释放氧气直至产氧药柱耗尽。在产氧药柱分解过程中,燃烧面能够沿药柱轴线方向自一端向另一端逐渐蔓延,这种燃烧方式与蜡烛燃烧十分相似,故亦将氯酸盐化学供氧装置称为“氧烛”。
|
图 2 潜艇舱室常见氯酸盐化学供氧装置和内部结构示意图[3,11] Fig. 2 Digital photographs and structure of the chlorate-based chemical oxygen generation apparatus for submarine cabins[3,11] |
潜艇舱室氯酸盐化学供氧技术与装置自诞生起,其发展一直受到潜艇环境控制与生命保障领域的长期关注,近年来的研究重点聚焦提高供氧稳定性、增强本质热安全性、防止外部污染和控制毒害气体释放4个方向。
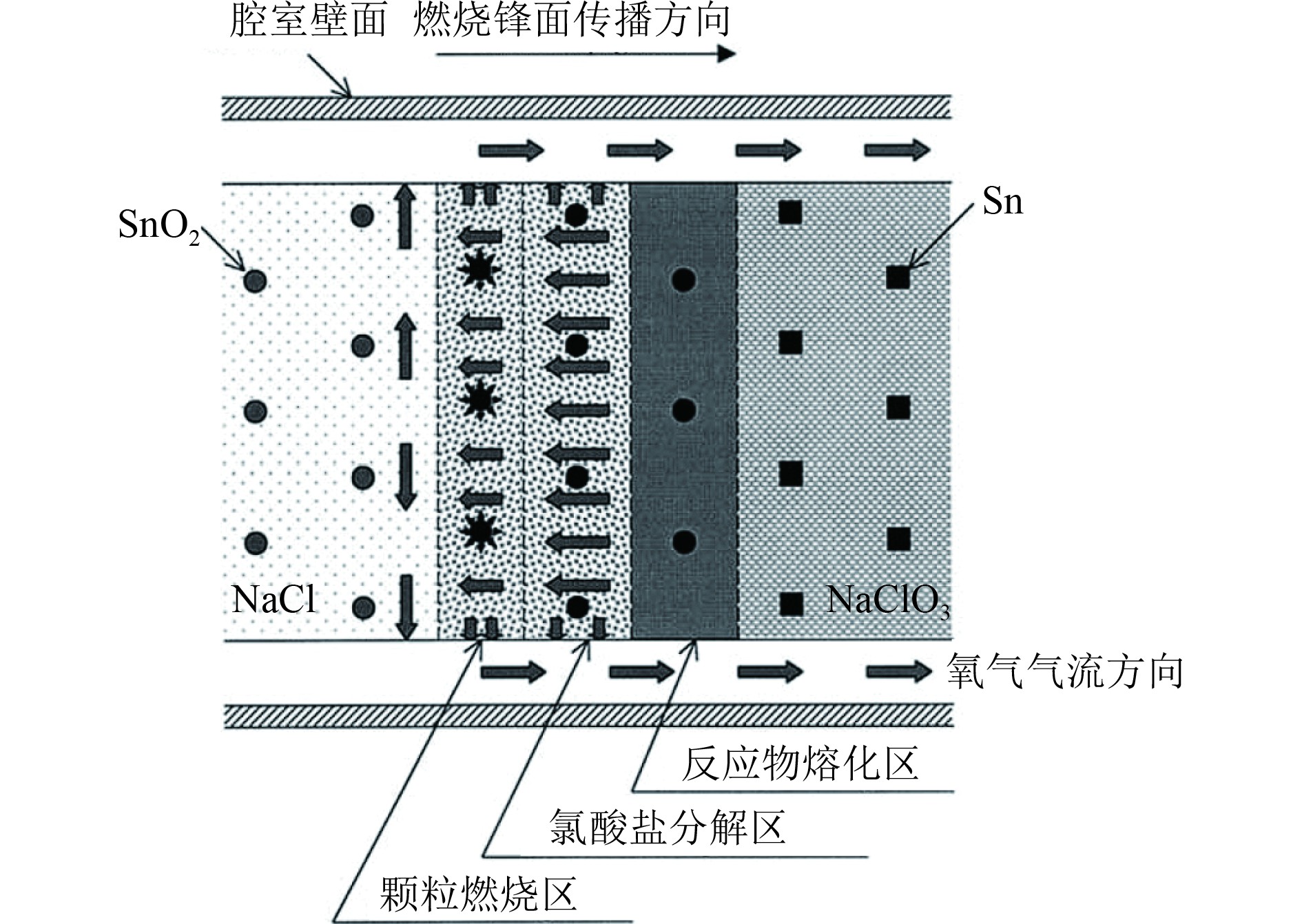
2.1 提高供氧稳定性潜艇舱室氯酸盐化学供氧装置在热力学上属于低放热凝聚态体系,其燃烧过程受到不稳定的反应前沿在产氧药柱内部低速传播的影响,释放氧气的速率大幅波动且无法人为控制,直接降低了装置的稳定性和可靠性[12]。分析引发氯酸盐化学供氧波动的机制是予以控制和改进的基础。Shafirovich等[13]利用嵌入式热电偶和热成像技术分析了产氧药柱的燃烧过程,将燃烧锋面的结构划分为颗粒燃烧区、氯酸盐分解区和反应物熔化区(见图3),提出在氯酸盐-金属燃料体系中存在低温和高温2种燃烧波传播构型,而金属氧化和氯酸盐分解2种相互耦合的界面反应速度差异则是导致高温构型不稳定进而引起产氧速率波动的重要因素。Diakov等[14]通过数值模拟分析了NaClO3分解产氧的过滤燃烧锋面稳定性,发现反应物熔化以及生成氧气与固体反应物间的对流传热是影响稳定性的重要因素。模拟结果表明,当反应活化能增大或对流传热减少时产氧波动增大,而当燃烧温度达到反应产物熔点时可对燃烧锋面传播形成强的稳定化作用。
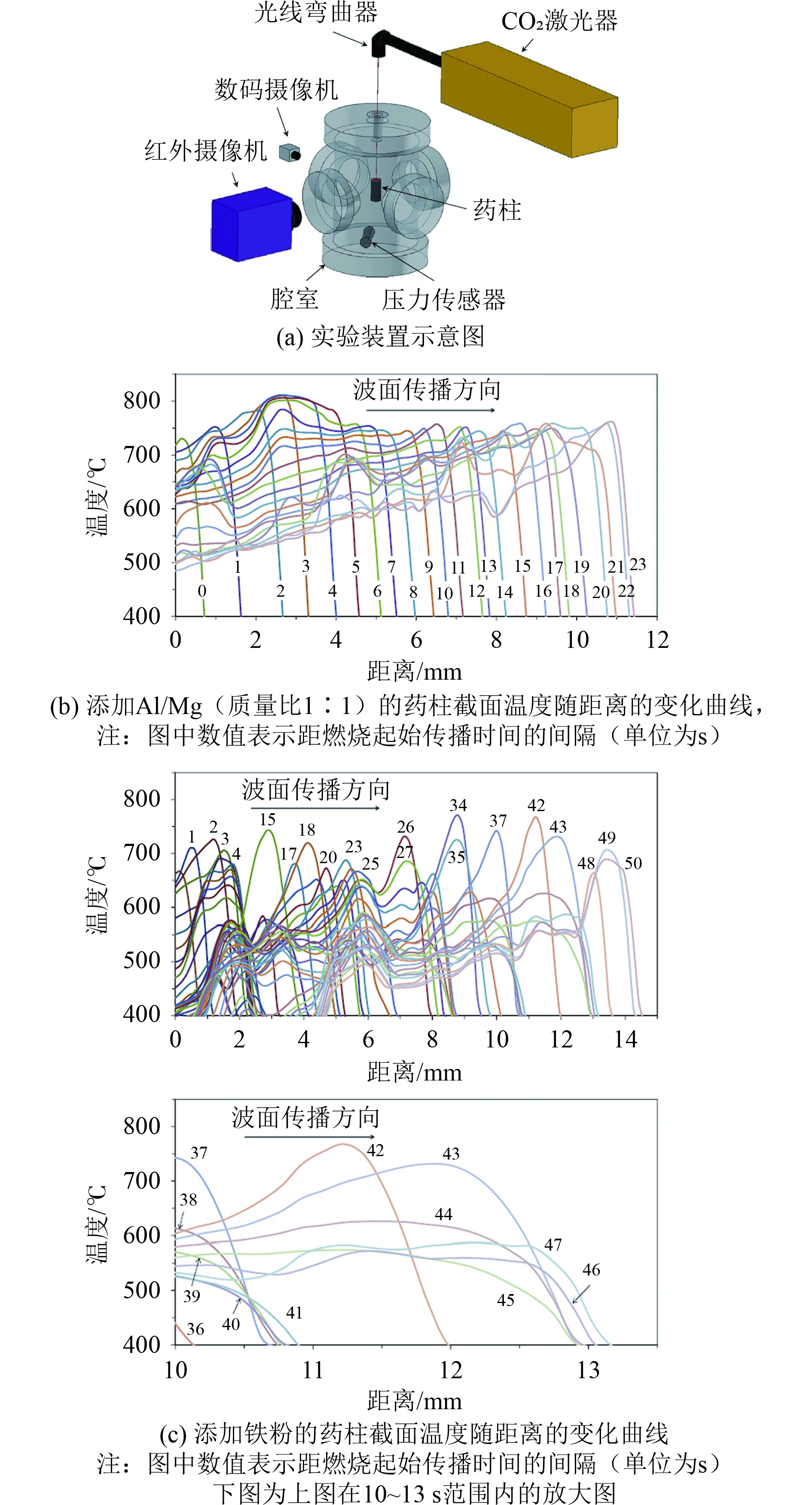
基于以上对氯酸盐化学供氧波动机制的研究,控制金属燃料的燃烧匹配性和添加比例等关键性质是提高供氧稳定性的一个有效思路。金属燃料的燃烧会释放大量热量并消耗部分生成的氧气,同时降低单位质量产氧药柱的供氧量。通过设计新型高效燃料,提高燃料氧化与氯酸盐分解的动力学匹配性,降低药柱中的金属燃料含量,不仅有助于减小产氧速率波动,同时可提高装置的比供氧能力。Machade等[15]利用反应抑制球磨法和机械合金化法制备了系列新颖的反应性合金化燃料,通过热力学计算证明了保持相同燃烧温度和产氧量所需的反应性合金燃料添加量相比金属粉体显著降低,并首次应用红外成像记录结合激光引燃实验,证明了更少量的合金化Al/Mg(质量比1∶1)燃料相比传统Fe粉燃料可维持更为稳定的燃烧波面传播(见图4)。
|
图 4 使用反应性合金化Al/Mg(质量比1∶1)燃料与传统铁粉燃料的燃烧波面传播性质对比[15] Fig. 4 Comparison of the combustion wave propagation in the pellets with Al/Mg (mass ratio 1∶1) and Fe powder as fuel[15] |
已有研究表明[16 − 17],Fe、Ni等常用的金属燃料对氯酸盐的分解也有不同程度的催化作用。在调控单一金属燃料组分的基础上,近年来研究者也试图利用金属与催化剂间的耦合效应调控产氧稳定性。Gao等[18]通过热重技术分析了Fe、Mg、Mn等3种不同金属燃料对氯酸钠在Co3O4催化下分解产氧过程的影响。实验结果表明,不同金属种类对氯酸钠的催化分解过程具有不同的影响。其中,高活性的Mg能够显著降低氯酸钠的分解稳定性,而添加Mn能够最有效地减小氯酸钠实际产氧量和理论值的差异。该结果充分证明了金属与催化剂间耦合效应的存在,揭示了通过金属与催化剂间的耦合效应调控产氧稳定性的可能。进一步,Gao等[10]研究了上述3种金属燃料与CoO3、Co3O4、Fe2O3 等3种不同催化剂之间的耦合效应,发现6% Mn与5% Co3O4组合对氯酸钠分解制氧具有最佳的耦合作用,产氧效率最高可达97.8%,平均产氧速率为1.647 L/min。
此外,近年来的研究发现,通过设计合理的产氧药柱成型体的结构也可有效提升氯酸盐化学供氧装置的供氧稳定性。在供氧装置内部,随着燃烧反应进行产生的热量会在产氧药柱内积聚,基于这一现象,Jin等[19 − 20]设计了具有双层结构的药柱成型体(见图5 (a)),利用上层药柱燃烧积聚的热量维持下层药柱氯酸盐分解,从而在下层药柱中避免添加高放热的金属燃料。实验结果表明,双层结构能够降低供氧装置燃烧过程中密封试验舱室的温度变化波动,反映了装置产氧的均匀性提升。Wang等[21]设计了系列孔径不同的中空结构药柱成型体(见图5(b)),证明了中空结构有助于提升供氧装置的供氧性能,其产氧比可达98.3%,相比传统结构的供氧装置提高了28.9%。
2.2 增强本质热安全性在潜艇舱室氯酸盐化学供氧装置运行时,产氧药柱的温度需维持不低于氯酸盐的催化分解温度,一般为300~350 ℃,以保持连续输出氧气。然而,较高的内部温度会造成装置机械外壳温度持续偏高,阻碍装置正常操作并引发安全风险。研究表明,在产氧药柱四周包覆传统玻璃纤维毡隔热材料的条件下,供氧装置的机械外壳温度最高仍可达到约300 ℃[22]。此外,加工过程装药不当、贮存过程污染等外部因素均有可能造成药柱局部过反应而烧穿装置机械外壳,甚至发生爆炸。因此,仍需在消除或减少金属燃料使用、开发更高效的催化剂以及设计新型隔热结构和隔热材料等方面开展研究,增强氯酸盐化学供氧装置的本质热安全性。
1)消除或减少金属燃料使用
为保障产氧药柱启动后不会中断分解,金属燃料的加入量通常过量。然而,过量加入的燃料不仅导致单位质量药柱产氧量降低,同时由于金属粉末燃烧产生的局部温度较高(可超
2)开发更高效的催化剂
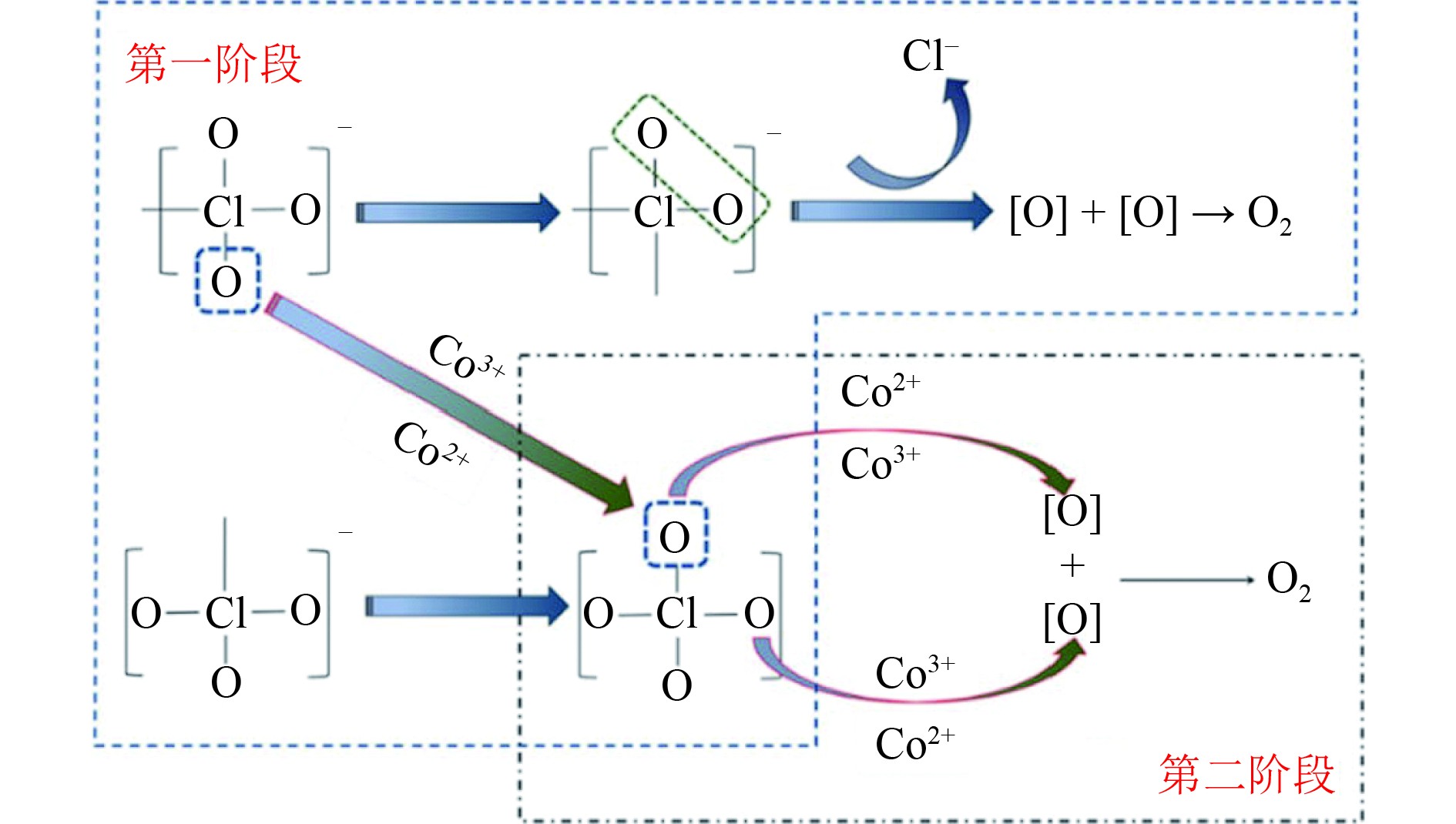
开发更高效的催化剂来分解氯酸盐,进而降低产氧药柱中金属燃料的含量,仍然是减少药柱燃烧放出热量、提高氯酸盐化学供氧装置本质热安全性的最有效途径。研究者围绕不同材料对氯酸盐的催化分解作用开展了大量系统的研究工作,发现Co3O4、MnO2、Fe2O3等过渡金属氧化物是最为有效的催化材料,并将氯酸盐在过渡金属氧化物催化下的分解过程划分为氯酸盐转化为高氯酸盐以及高氯酸盐分解2个阶段(见图6)[24 − 30]。
|
图 6 氯酸盐在过渡金属氧化物催化作用下的两阶段分解过程[18] Fig. 6 Diagram of the decomposition process of chlorate with the transition metal oxide catalysts[18] |
目前,学界对于过渡金属氧化物与其催化氯酸盐分解的构效关系理解尚存在争议,不同学者认为氯酸盐热解性能分别与过渡金属氧化物的p型半导体性质或金属阳离子d轨道的电子构型相关[24 − 26,29 − 30]。近年来后一种观点更为人们所接受,即过渡金属氧化物中金属组分有空的外层d轨道,能提供良好的电子转移,其催化作用机制是通过在氧化还原循环中加速电子转移,从而使氯酸盐在更低的温度下分解。因而,d轨道电子部分填充的金属氧化物对氯酸盐分解均呈现较高的催化活性,d轨道未填充电子的氧化物催化活性适中,d轨道全部填充的氧化物催化活性最低。这一催化活性顺序获得了良好的实验数据支持[10,17]。
基于对过渡金属氧化物催化机制的认知,研究者近年来不断尝试提升催化剂的催化效果,以更为显著地降低地氯酸盐分解温度。以NaClO3为例,其无催化条件下的起始分解温度约450℃,完全分解温度约580℃。使用催化剂虽可降低分解温度,但通常仍高于NaClO3的熔点(260℃),进而造成氯酸钠熔化流淌影响热安全性。张彦军等[31]通过实验成功制备了一种可将NaClO3分解温度降至熔点以下的高效钴催化剂,并开发了能在低温燃烧的无燃料便携氧烛,其放氧速率在0~5 L/min可调,氯气释放量低于0.001 mg/L。
3)设计新型隔热结构和隔热材料
氯酸盐化学供氧装置持续运行过程中产氧药柱产生的热量主要通过2种途径耗散,一部分经固相热传导至机械壳体,造成壳体温度不断上升,另一部分则随生成的氧气逸出扩散至周围空气环境[32]。与之对应,近年来对于供氧装置的隔热结构设计一方面采用夹套式隔热结构的形式,在装置机械壳体夹层内部填充隔热材料以降低固相热传导速率;另一方面,通过外加具有隔热功能的夹套式防护筒附件,在隔绝供氧装置的同时进一步冷却生成的氧气[33 − 34]。
王雅娟等[22]分别研究了上述2种结构形式的内填隔热材料,发现当采用夹套式供氧装置外壳结构时,在夹套内填充Al2(SO4)3·18H2O,利用其受热脱水反应吸收热量,可保障装置在供氧过程中外壳最高温度低于100℃,而以普通耐高温布为填充物则无法降低外壳温度;当将供氧装置置于填充二氧化硅纤维毡的夹套式防护筒内使用时,防护筒外表面最高温度不超过45℃,出气口最高温度55℃,均处于安全温度范围内。
朱耿溪等[35]基于一维热传导模型对某型军用氯酸盐化学供氧装置结构进行了热仿真分析(见图7),提出可在机械壳体表面敷设隔热材料以降低表面温度,并对比了市售常见隔热材料,认为二氧化硅气凝胶棉毡材料在隔热、减重及耐用等多方面性能均有优势,是目前综合较优的技术方案。

|
图 7 某型军用氯酸盐化学供氧装置启动不同时间后机械外壳的温度分布模拟云图[35] Fig. 7 Simulated temperature distribution for the shell of a military chemical oxygen generation apparatus at different time[35] |
除提升潜艇舱室氯酸盐化学供氧装置的自身安全性外,通过技术措施防止装置因外部因素引发热安全事故近年来也受到重视。2007年3月,英国海军特拉法加级“不懈”号(HMS Tireless)核潜艇内部SCOG 26型氧烛发生爆炸,致使2名艇员丧生。事故调查表明[36],氧烛内部产氧药柱在使用前受到液油污染,进而引发了爆炸。美国航空航天局(NASA)进一步分析液油污染造成氧烛爆炸的机制,确认了当产氧药柱处于密封状态且内部出现断层或裂纹时,液油污染将会引起氧烛剧烈爆炸[37]。需要指出的是,虽然自潜艇舱室氯酸盐化学供氧装置发展至今已有多起自燃或爆炸事故的报道,但TDA研究公司的评估结果仍然表明[38],当前没有可供替代的供氧技术或装置其本质安全性高于氯酸盐化学供氧装置。
基于上述背景,英国海军主导对SCOG 26型氧烛进行了改进(称EO2-26型),并随后开发出新一代MPOG型氧烛[39]。EO2-26和MPOG型氧烛相较上一代改进的核心是提升了防外部化学污染的能力。其中,EO2-26型氧烛的设计改进主要包括为氧烛设置内外两级密封系统(见图8(a)~图8(b)),即在外部增设了防污染的塑料软包装(见图8(b)),并为氧烛专门设计了抗污染的密封储柜(见图8(c)),以尽可能阻止氧烛在长期贮存期间其内部产氧药柱与外源污染物接触。在EO2-26型氧烛的基础上,MPOG型氧烛进一步优化了安全设计,将外部密封系统由塑料软包升级为金属壳体(见图8(d)),改进了氧烛储柜之具有防火能力(见图8(e)),同时在氧烛内部密封系统之外增设了一个潮湿指示圆盘(见图8(f))。该圆盘位于氧烛顶部的T形把手处,当外部密封系统破损时,渗透进入的水蒸气将会使圆盘变色,从而提示使用者氧烛可能已经受到了外源污染。

|
图 8 英国海军EO2-26和MPOG型潜用氧烛的防外源化学污染设计[39] Fig. 8 Design for preventing the EO2-26 and MPOG oxygen candles from external chemical pollution by the royal navy[39] |
就密闭的潜艇舱室应用场景而言,避免氯酸盐化学供氧装置使用时向周围环境释放毒害气体十分重要。已有研究表明[3],这些毒害气体来源多样,生成机制复杂。当前已知的毒害气体种类主要为Cl2、HClO等含氯产物和CO。其中,含氯气体主要是由产氧药柱直接高温分解(式(4))或其中少量氯化物杂质经水解、高温反应生成,而CO则来源于Fe粉等燃料中含有的C元素[3,8]。向药柱中添加碱性抑氯剂并将生成的气体通过过滤层净化是当前较为成熟的控制手段。在此基础上,近年来针对控制含氯副产物和CO释放的研究进展集中于以下3个方面:
1)设计新型净化过滤材料,提高毒害气体消除效率。Samuel等[40]通过将MnO2与CuO按3∶2比例混合后与NaOH形成复合过滤材料,该材料能够在脱除含氯酸性气体的同时,催化CO转化为CO2。杨振峰等[41]采用浸渍法在活性炭基体上复合活性组分LiOH,利用活性炭的物理吸附和LiOH的化学吸附协同作用提升对酸性含氯气体的净化能力。
2)开发新型多功能抑氯剂,不仅能够抑制Cl2释放,也能够调节分解反应过程进而抑制CO副产物的生成。目前,这一研究方向仍处于初期探索阶段[3,42]。
3)较高的燃烧温度通常会导致有毒含氯副产物大量生成,除末端治理手段外,通过避免药柱高温反应的方式进行毒害气体源头治理是更为有效的方法。马军等[43]通过向SiO2气凝胶中填充BaO2抑氯剂,设计了具有隔热和除氯一体化功能的隔热过滤层,氧烛产生的气体全部经隔热过滤层净化后流出,简化了氧烛结构,同时避免了向药柱中添加抑氯剂导致的分解温度升高。实验结果表明,氧烛内NaClO3在250℃左右即可分解,外壳温度可低至55℃,出口气体中Cl2浓度低于0.1×106,符合国军标对氯酸盐化学供氧装置的Cl2浓度要求。此外,部分研究者探索设计新型点火方式,尝试利用微波加热[44]、激光加热[45]等方式均匀加热并引燃产氧药柱,避免形成局部高温“热点”,减少含氯气体生成。
3 结 语近年来,针对潜艇舱室氯酸盐化学供氧装置的研究进展主要集中于提高供氧稳定性、增强本质热安全性、防止外部污染和控制毒害气体释放4个方面,呈现良好的持续发展态势。未来,仍需要在以下方面开展研究:
1)建立实际条件下的氯酸盐催化分解制氧过程及动力学特征的认知。潜艇舱室氯酸盐供氧装置的产氧速率由氯酸盐分解速率决定,而后者又受升温速率显著影响。现有的研究工作主要分析了氯酸盐在较低升温速率(通常小于20℃/min)时的分解特征,这一升温速率远低于产氧药柱实际燃烧时的升温速率(约700~800℃/s),却乏对氯酸盐在高升温速率下分解产氧化学过程与动力学行为的基础科学理解。未来仍需开展相关研究工作,通过控制氯酸盐在实际高升温速率下的催化分解反应,提高装置产氧稳定性。
2)深化对金属燃料与催化剂耦合效应的理解与运用。当前对于金属与催化剂的耦合效应研究仍处于初始阶段,对二者耦合效应的认识较为模糊且停留在定性层面,未来仍需要借助原位理化表征技术、量子化学计算、组合化学筛选等先进研究手段,加深对金属与催化剂耦合机理、构建模式、定量调控等方面的认识,充分发挥金属与催化剂“1+1>2”的协同作用,进一步改善装置的产氧稳定性和热安全性。
3)明晰毒害气体来源与生成机制。当前对于潜艇舱室氯酸盐供氧装置燃烧产生的毒害气体来源和生成机制缺乏清晰的认识,对毒害气体主要依靠添加抑氯剂、过滤净化等末端控制方法。随着实验技术和理论计算方法的不断发展,未来可借助原位光谱、超快光谱和量子化学计算等手段,深化对毒害气体生成的源项与过程认知,从而针对性通过源头控制更为有效地降低因供氧装置燃烧导致的潜艇舱室环境污染。
| [1] |
张传钊, 刘应书, 王浩宇, 等. 密闭建筑空间缺氧环境下富氧特性研究[J]. 工程科学学报, 2018, 40(11): 1380-1388. |
| [2] |
姜磊, 何再明, 李栋梁. 基于氧烛供氧的“奋斗者”号载人舱内一氧化碳浓度分析[J]. 舰船科学技术, 2022, 44(21): 30-35. JIANG L, HE Z M, LI D L. Analysis of carbon monoxide concentration in manned compartment of Fen dou zhe when chemical oxygen generator was used for oxygen supply[J]. Ship Science and Technology, 2022, 44(21): 30-35. DOI:10.3404/j.issn.1672-7649.2022.21.007 |
| [3] |
LIU J, JIN L, GAO N, et al. A review on chemical oxygen supply technology within confined spaces: challenges, strategies, and opportunities toward chemical oxygen generators (COGs)[J]. International Journal of Minerals, Metallurgy, and Materials, 2019, 26(8): 925-937. DOI:10.1007/s12613-019-1809-6 |
| [4] |
朱耿溪, 李艳, 孔庆平. 密闭空间化学制氧技术研究进展[J]. 现代制造技术与装备, 2022, 58(8): 105-107+115. |
| [5] |
姜磊, 刘帅, 高成君, 等. 氧烛在全海深载人潜水器中应用的适用性分析[J]. 中国造船, 2019, 60(2): 196-206. DOI:10.3969/j.issn.1000-4882.2019.02.020 |
| [6] |
田朴. 高原小型便携式供氧装置的现状及发展趋势[J]. 现代盐化工, 2021(3): 106-108. DOI:10.3969/j.issn.1005-880X.2021.03.051 |
| [7] |
马帅, 石梅生, 张利芳, 等. 野战条件下制氧技术与装备的研究进展[J]. 医疗卫生装备, 2021, 42(08): 67-74. |
| [8] |
范敏. 氧烛的研究现状与发展[J]. 舰船科学技术, 2008, 28(7): 16-20. FAN M. The research on actuality and development of oxygen candle[J]. Ship Science and Technology, 2008, 28(7): 16-20. |
| [9] |
倪伟, 颜欢, 王朋辉, 等. 潜艇舱室供氧技术研究进展[J]. 舰船科学技术, 2016, 38(9): 138-141. NI W, YAN H, WANG P H, et al. Oxygen supplying technologies in submarine cabin: a review[J]. Ship Science and Technology, 2016, 38(9): 138-141. DOI:10.3404/j.issn.1672-7619.2016.05.029 |
| [10] |
GAO N, MA C, KARIMAN K, et al. Coupling effect of metals and oxides on the oxygen supply performance of sodium chlorate oxygen candle[J]. Journal of Chemistry, 2021, e6088484. |
| [11] |
GRAF J, DUNLAP C, HAAS J, et al. Development of a solid chlorate backup oxygen delivery system for the international space station[C]//30th International Conference on Environmental Systems. Toulouse, France, 2000.
|
| [12] |
SHAFIROVICH E, ZHOU C, MUKASYAN A S, et al. Combustion fluctuations in low-exothermic condensed systems for emergency oxygen generation[J]. Combustion and Flame, 2003, 135(4): 557-561. DOI:10.1016/j.combustflame.2003.08.001 |
| [13] |
SHAFIROVICH E, MUKASYAN A S, VARMA A, et al. Mechanism of combustion in low-exothermic mixtures of sodium chlorate and metal fuel[J]. Combustion and Flame, 2002, 128(1): 133-144. |
| [14] |
DIAKOV V, SHAFIROVICH E, VARMA A. A Numerical study of combustion stability in emergency oxygen generators[J]. AIChE Journal, 2006, 52(4): 1495-1501. DOI:10.1002/aic.10726 |
| [15] |
MACHADO M A, RODRIGUEZ D A, ALY Y, et al. Nanocomposite and mechanically alloyed reactive materials as energetic additives in chemical oxygen generators[J]. Combustion and Flame, 2014, 161(10): 2708-2716. DOI:10.1016/j.combustflame.2014.04.005 |
| [16] |
SHAFIROVICH E, ZHOU C, EKAMBARAM S, et al. Catalytic effects of metals on thermal decomposition of sodium chlorate for emergency oxygen generators[J]. Industrial & Engineering Chemistry Research, 2007, 46(10): 3073-3077. |
| [17] |
范敏, 卜建杰, 郑邯勇, 等. 钴的氧化物对氧烛药块分解的催化作用[J]. 舰船科学技术, 2007(6): 126-129. FAN M, BU J J, ZHENG H Y, et al. Cobalt oxide compounds and its catalytic performance for decomposition of oxygen-generating candle[J]. Ship Science and Technology, 2007(6): 126-129. |
| [18] |
GAO N, DAI Y, JIN L, et al. Effect of metals and Co3O4 on the thermal decomposition reaction of sodium chlorate in an area of refuge[J]. Chemical Papers, 2020, 74(10): 3475-3480. DOI:10.1007/s11696-020-01186-2 |
| [19] |
JIN L Z, WANG S, LIU S C, et al. Development of a low oxygen generation rate chemical oxygen generator for emergency refuge spaces in underground mines[J]. Combustion Science and Technology, 2015, 187(8): 1229-1239. DOI:10.1080/00102202.2015.1031223 |
| [20] |
王伟象, 金龙哲, 高娜, 等. 井下避险空间双层结构氧烛供氧性能研究[J]. 煤炭技术, 2016, 35(6): 201-203. |
| [21] |
WANG W, JIN L, GAO N, et al. The Oxygen generation performance of hollow-structured oxygen candle for refuge space[J]. Journal of Chemistry, 2018, e7469783. |
| [22] |
王雅娟. 氧烛隔热结构的设计[J]. 舰船科学技术, 2010, 32(12): 95-98. WANG Y J. Design of thermal insulation for the oxygen generating candles[J]. Ship Science and Technology, 2010, 32(12): 95-98. DOI:10.3404/j.issn.1672-7649.2010.12.024 |
| [23] |
SHAFIROVICH E, GARCIA A, NARAYANA SWAMY A K, et al. On feasibility of decreasing metal fuel content in chemical oxygen generators[J]. Combustion and Flame, 2012, 159(1): 420-426. DOI:10.1016/j.combustflame.2011.07.004 |
| [24] |
RUDLOFF W, FREEMAN E. Catalytic effect of metal oxides on thermal-decomposition reactions. I. The mechanism of the molten-phase thermal decomposition of potassium chlorate in mixtures with potassium chloride and potassium perchlorate[J]. Journal of Physical Chemistry, 1969, 73(5): 1209-1215. DOI:10.1021/j100725a006 |
| [25] |
RUDLOFF W, FREEMAN E. Catalytic effect of metal oxides on thermal decomposition reactions. II. Catalytic effect of metal oxides on the thermal decomposition of potassium chlorate and potassium perchlorate as detected by thermal analysis methods[J]. Journal of Physical Chemistry, 1970, 74(18): 3317-3324. DOI:10.1021/j100712a002 |
| [26] |
RUDLOFF W, FREEMAN E. The Catalytic effects of metal-oxides on thermal-decomposition reactions. III. The influence of structural and electronic defects in iron-oxides on their catalytic effectiveness with respect to the thermal-decomposition of potassium chlorate[J]. Journal of Thermal Analysis, 1980, 18(2): 359-369. DOI:10.1007/BF02055821 |
| [27] |
LIU P A, WANG M J, WANG L, et al. Study on nano-metal oxide and carbon nanotube composites on thermal decomposition of potassium perchlorate[J]. Bulletin of the Korean Chemical Society, 2019, 40(4): 324-331. DOI:10.1002/bkcs.11686 |
| [28] |
CHATURVEDI S, DAVE P N. Nano-metal oxide: Potential catalyst on thermal decomposition of ammonium perchlorate[J]. Journal of Experimental Nanoscience, 2012, 7(2): 205-231. DOI:10.1080/17458080.2010.517571 |
| [29] |
ZHANG Y, KSHIRSAGAR G, ELLISON J, et al. Catalytic effects of non-oxide metal-compounds on the thermal-decomposition of sodium-chlorate[J]. Industrial & Engineering Chemistry Research, 1993, 32(11): 2863-2865. |
| [30] |
ZHANG Y, KSHIRSAGAR G, ELLISON J, et al. Catalytic and inhibiting effects of barium peroxide and hydroxide on the decomposition of sodium-chlorate[J]. Thermochimica Acta, 1995, 261: 119-124. DOI:10.1016/0040-6031(95)02312-P |
| [31] |
张彦军. 便携式无燃料低温燃烧氧烛工艺研究[J]. 兵工学报, 2019, 40(6): 1317-1322. DOI:10.3969/j.issn.1000-1093.2019.06.024 |
| [32] |
王亚, 邓康清, 周兴明, 等. 固体氧气发生器温度场仿真分析[J]. 中国个体防护装备, 2023(1): 15-20. |
| [33] |
赵小平, 王雅娟, 马丽娥. 基于Ansys软件的氧烛防护筒的模拟与设计[J]. 舰船防化, 2012(2): 1-4. |
| [34] |
翟康. 大容量氧烛隔热防护与热损分析[J]. 四川兵工学报, 2015, 36(12): 35-38. |
| [35] |
朱耿溪. 化学产氧器隔热结构分析研究[J]. 现代制造技术与装备, 2023, 59(1): 13-16. DOI:10.3969/j.issn.1673-5587.2023.01.007 |
| [36] |
HESLOP P, BLAIR P S, FLEMING P, et al. The confidential inquiry into premature deaths of people with intellectual disabilities in the UK: a population-based study[J]. The Lancet, 2014, 383(9920): 889-895. DOI:10.1016/S0140-6736(13)62026-7 |
| [37] |
KEDDY C P, HAAS J P, STARRITT L. Investigation, analysis, and testing of self-contained oxygen generators: WSTF-IR-1129-001-08[R]. Las Cruces: U. S. National Aeronautics and Space Administration, 2008.
|
| [38] |
MCCARRICK A, HAAS J, JOHNSON K, et al. U. S. navy sodium chlorate oxygen candle safety[C]//41st International Conference on Environmental Systems. Portland, Oregon U. S. : American Institute of Aeronautics and Astronautics, 2011.
|
| [39] |
GOODALL A. The development of a Non-powered oxygen generator for royal navy submarines[C]//42nd International Conference on Environmental Systems. San Diego, California U. S.: American Institute of Aeronautics and Astronautics, 2012.
|
| [40] |
SAMUEL P S. Chlorine gas filtering material suitable for use in a chemical oxygen generator: US Patent 4687640[P]. 1987.
|
| [41] |
杨振峰, 孔庆平, 韩卫敏, 等. 活性炭-氢氧化锂复合材料的制备及性能研究[J]. 现代盐化工, 2021, 48(3): 29-31. DOI:10.3969/j.issn.1005-880X.2021.03.014 |
| [42] |
ZHANG Y, KSHIRSAGAR G, CANNON J C. Functions of barium peroxide in sodium chlorate chemical oxygen generators[J]. Industrial & Engineering Chemistry Research, 1993, 32(5): 966-969. |
| [43] |
马军, 张彦军, 田涛, 等. 一种化学氧烛制氧器及其制作方法与制氧方法: CN201811472700.5[P]. 2019.
|
| [44] |
韩旭, 茅靳丰, 程宝义, 等. 微波诱导技术用于氧烛制氧的理论研究[J]. 中国安全科学学报, 2006(4): 67-71+145. DOI:10.3969/j.issn.1003-3033.2006.04.013 |
| [45] |
MACHADO M A, RODRIGUEZ D A, SHAFIROVICH E, et al. Selection of nanocomposite reactive materials for using in oxygen and hydrogen generators[C]//51st AIAA Aerospace Sciences Meeting Including the New Horizons Forum and Aerospace Exposition. Grapevine, Texas U. S.: American Institute of Aeronautics and Astronautics, 2013.
|
 2025, Vol. 47
2025, Vol. 47