2. 第三军医大学健康教育教研室
环境污染对人群健康的影响已引起世界各国的高度关注。邻苯二甲酸酯(phthalic acid esters,PAEs)是一类重要的环境污染物,广泛用于工业生产和日常生活[1]。由于其具有致畸性、致突变性、致癌性及生殖毒性[2],已被美国环保署和中国环境监测总站列为优先控制污染物。邻苯二甲酸酯在塑料及其它制品中呈游离状态,随着时间推移,极易进入环境而广泛存在于大气、水体、土壤及生物体内[3]。前期研究发现重庆市孕产妇体内也存在邻苯二甲酸酯类污染,部分邻苯二甲酸酯可穿过血胎屏障在脐带血中被检出[4],进一步研究发现其可能诱导早产及影响胎儿发育[5]。
邻苯二甲酸酯孕期暴露影响早产及胎儿发育的机制至今尚无定论[6-9]。前期研究发现,邻苯二甲酸酯代谢产物邻苯二甲酸单乙基己酯可以上调大鼠子宫氧化物酶体增殖物激活受体G (peroxisome proliferator-activated receptor G,PPARG)的表达[10],人群研究也证实脐血邻苯二甲酸酯水平与胎盘PPARG表达正相关,推测胎盘PPARG可能参与邻苯二甲酸酯孕期生殖毒性。PPARG是核内受体转录因子超家族成员,参与调控多种基因的转录,包括雌激素合成关键酶、基质金属蛋白酶(MMPs)[11-12],其胎盘表达改变可能通过调节母体糖代谢、性激素、基质金属蛋白酶及前列腺素水平影响胎儿发育[13]。前期人群研究发现胎盘邻苯二甲酸酯暴露可能通过PPARG下调脐血雌激素、前列腺素E2和MMPs水平,细胞实验也发现邻苯二甲酸单乙基己酯可下调雌激素生物合成限速酶P450芳香化酶(P450arom) mRNA水平,上调17β-羟甾脱氢酶(17β-HSD) mRNA水平[14]。推测邻苯二甲酸酯可能通过调节PPARG表达从而调节其下游胎盘雌激素、前列腺素E2合成关键酶及MMPs mRNA表达来下调雌激素、前列腺素E2和MMPs在胎盘合成分泌[15],影响胎儿发育和妊娠[16-17]。
本研究以邻苯二甲酸(2-乙基己基)酯(DEHP)作为邻苯二甲酸酯类代表,通过构建DEHP染毒孕鼠模型,联用PPARG拮抗剂GW9662,验证PPARG在邻苯二甲酸酯染毒动物胎盘中的表达改变,及其对雌激素、前列腺素E2合成关键酶及MMPs mRNA表达的影响。
1 材料与方法 1.1 实验动物染毒及处理6周-7周龄健康雌性SPF级SD大鼠60只,体重168g±7g (许可证号SCXK-(军)-2002007,合格证号0020889)。染毒前适应性饲养1周,温度控制在22℃±3℃,相对湿度控制在30%~70%,人工控制照明12 h (昼/夜),动物自由进食、饮水。按随机数字法分为3组:对照组、染毒组和干预组各20只,连续灌胃染毒(表 1),染毒第30天与健康雄性SD大鼠合笼,以看见阴栓作为妊娠第0天,持续染毒至妊娠第20天,处理动物,取正常胎鼠称重,取相应胎盘检测蛋白及mRNA表达。
| 分组 | 染毒试剂及灌胃体积 | |
| 第1天-第27天 | 第28天-妊娠第20天 | |
| 对照组 | 玉米油2 mL/kg | 玉米油2.5 mL (含DMSO 0.02 mL)/kg |
| 染毒组 | DEHP 2 g/kg | DEHP 2 g/kg+玉米油0.5 mL (含DMSO 0.02 mL)/kg |
| 干预组 | DEHP 2 g/kg | DEHP 2 g/kg+玉米油0.5 mL (含DMSO 0.02 mL,GW9662 0.5 mg) /kg |
1.2 蛋白表达检测
大鼠胎盘剥去胎膜,使用IP细胞裂解液(碧云天)根据试剂说明书提取胎盘总蛋白,使用BCA试剂盒(碧云天)根据试剂说明书检测蛋白浓度,加蒸馏水稀释蛋白浓度到8 mg/mL。Western-blot检测PPARG蛋白表达:SDS-PAGE电泳分离蛋白,根据SDS-PAGE凝胶配制试剂盒(碧云天)使用说明配置浓缩胶和10%分离胶;每组蛋白样本混合上样每孔40 μL;垂直电泳槽(Biorad),4℃电泳(50 V浓缩胶,120 V分离胶);半干式转PVDF膜(Bio-Rad,15 V,30 min);37℃封闭1 h;混合一抗[鼠抗PPARG (SNATA)+鼠抗GAPDH (碧云天)]4℃孵育过夜;羊抗鼠(碧云天)37℃孵育1 h;ECL Kit化学发光(碧云天)检测各组细胞中蛋白的表达情况(图像采集:凝胶成像仪(Bio-rad);图象分析:ImageMaster 5.00)。
1.3 mRNA表达检测根据使用说明书Trizol法(ambion)提取总RNA,逆转录(TaKaRa)后以GAPDH (生工生物)为内参,通过SYBR Ⓒ Green I嵌合荧光法(TaKaRa)实时定量PCR (Bio-rad)检测PPARG、激素合成关键酶CYP191(P450Arom)、17HSDb1、17HSDb2、17HSDb3、17HSDb4、17HSDb7、17HSDb8、3HSDb1)、前列腺素E2合成代谢关键酶(PLA2G4A、PTGS2、PTGES2、HPGD)以及基质金属蛋白酶(MMP2、MMP9) mRNA表达(表 2)。
| 目的基因 | 引物序列 | |
| 正向 | 反向 | |
| PPARG | CCTCCCTGATGAATAAAGATGG | CACAGCAAACTCAAACTTAGGC |
| CYP191a1 | GCACTCCTTATCAAACCAAACA | CTCTCAGCGAAAATCAAATCAG |
| 17HSDb1 | TCCACCTGCTTCTCCTTCTG | CCCGACTACAGCCCTCTTATC |
| 17HSDb2 | CAGTGTTTGCTGGAGTGCTG | TATCTGCTCTGGCTTGGTGA |
| 17HSDb3 | GAAGCCGTGTGAAGGTTGTA | AATGACTTGGGAGCAGGTTG |
| 17HSDb4 | TGGGTCTCGCCAATACTCTC | GCATCACCGTCTCTGTCATC |
| 17HSDb7 | GCATTGTGCAGATGGATGTC | TTCCGGCGTTCAGGTATAAG |
| 17HSDb8 | TGATTCCGTTGGGACACAT | AAAGACCTCCACTGACTTCCAC |
| 3HSDb1 | AGCCGCATCCAGACTTTCTC | ACAAACCCTCCTGCTCCTGT |
| PLA2G4A | TTGGGAGTTTCTGGCTTACAG | CTTCATTCTCGGTGCCTTTG |
| PTGS2 | ACTACGCCTGAGTTTCTGAC | CAATGTTCCAGACTCCCTTGA |
| PTGES2 | ATGAAGCAGCCAACAAGTGG | ACTCGCAGCACACCATACAC |
| HPGD | CATTTGTCCAGGCTTTGTGA | GCACCATTGAGAGCATCATC |
| MMP2 | TGATCTTGACCAGAATACCATC | GGCTTGCGAGGGAAGAAGTTAG |
| MMP9 | CCTGGAGACCTGAGAACCAATC | CCACCCGAGTGTAACCATAGCG |
1.4 统计学处理
通过SPSS 13.0软件进行统计分子,采用卡方检测分析孕鼠妊娠情况,采用单因素方差分析胎鼠重、胎盘蛋白及mRNA表达差异。以P < 0.01为差异有统计学意义,mRNA在此基础上要求表达差异量差异值在1倍以上,才为差异有统计学意义。
2 结果 2.1 妊娠基本情况各组动物受孕率及正常妊娠比率(该组有活胎孕鼠占该组孕鼠比值)见表 3,染毒组和干预组正常妊娠的孕鼠比率显著低于对照组(P < 0.01),吸收胎比率显著高于对照组(P < 0.01),胎鼠体重显著低于对照组(P < 0.01)。
| 分组 | 受孕 率/% |
正常妊 娠率/% |
吸收胎率/% 均值±标准差 |
胎鼠重/g 均值±标准差 |
| 对照组 | 84.21 | 100.00 | 3.24±4.36 | 5.33±1.13 |
| 染毒组 | 72.22 | 46.15** | 41.24±32.49** | 4.14±0.80** |
| 干预组 | 58.82 | 30.00** | 32.58±36.95** | 3.79±0.48** |
| 注:**和对照比P < 0.01 | ||||
2.2 DEHP染毒对胎盘PPARG蛋白及基因表达
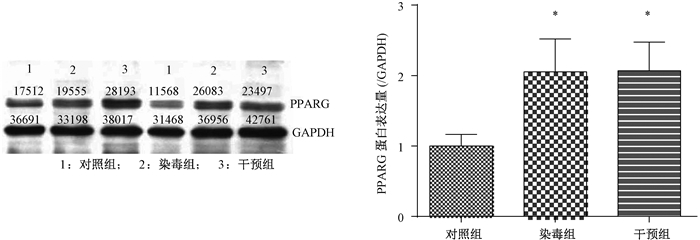
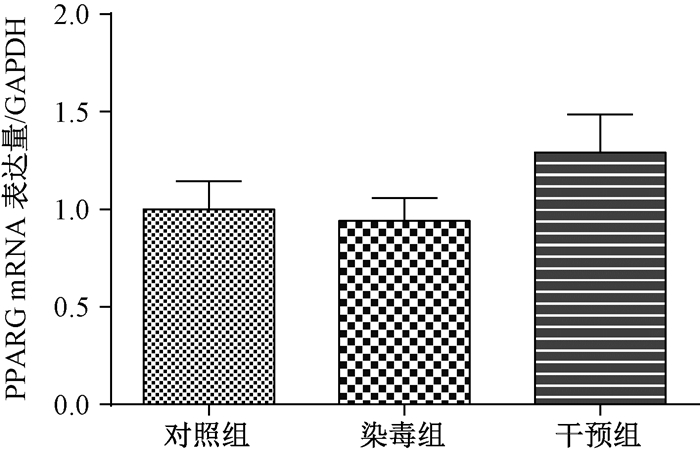
染毒组和干预组PPARG蛋白表达均显著高于对照组(P < 0.01;图 1);mRNA表达无明显改变(P>0.05;图 2)。
|
| 注:*和对照组比,P < 0.01 图 1 各组正常孕鼠胎盘PPARG蛋白表达 |
|
| 图 2 各组正常孕鼠胎盘PPARG mRNA表达 |
2.3 DEHP染毒胎盘激素合成相关酶mRNA表达的影响
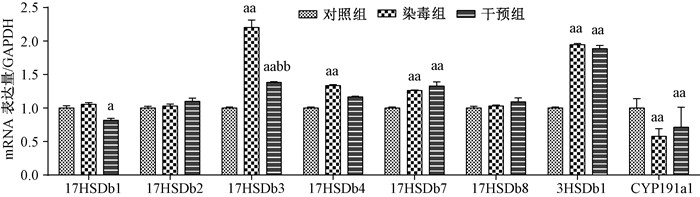
染毒组17HSDb3、3HSDb1表达显著高于对照组(P < 0.01;图 3),CYP191a1表达低于对照组(P < 0.01)。其中17HSDb3表达在干预组显著回复(17HSDb3干预组与染毒组比P < 0.01)。
|
| 注:a:与对照比P<0.05;aa:与对照比P < 0.01;bb:与染毒组比P < 0.01 图 3 各组正常孕鼠胎盘激素合成相关酶mRNA表达 |
2.4 胎盘前列腺组合成代谢酶及基质金属蛋白酶mRNA表达
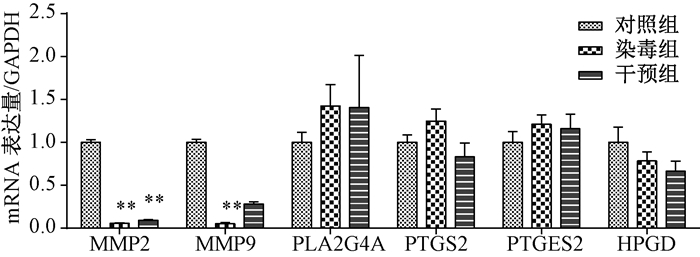
染毒组基质金属蛋白酶MMP2和MMP9表达显著高于对照组(P < 0.01;图 4),其中MMP9表达在干预组显著回复(与对照组比P > 0.05),前列腺组合成代谢酶PLA2G4A、PTGS2、PTGES2、HPGD各组间无明显改变(P > 0.05)。
|
| 注:**与对照比P < 0.01 图 4 各组正常孕鼠胎盘前列腺组合成代谢酶及基质金属蛋白酶mRNA表达 |
3 讨论
胎儿时期是发育的关键期,很容易受到各种外在因素的影响。在此期间,即使微量的化学物质接触都可能对神经、生殖、内分泌、心血管、免疫和呼吸等系统的发育产生不利影响。在本次研究中,染毒组和干预组正常妊娠率显著低于对照组,吸收胎率显著高于对照组,胎鼠体重显著下降,拮抗PPARG活性后并无明显好转,提示邻苯二甲酸酯类孕期暴露可能对孕鼠造成明显的生殖毒性,对PPARG表达调控可能只在其中发挥部分作用。
本研究证实邻苯二甲酸酯暴露可提高PPARG蛋白表达,但是PPARG基因表达无明显改变,且使用拮抗剂后影响不显著。提示邻苯二甲酸酯不是通过基因水平上调胎盘PPARG蛋白表达,可能来源于表达后调节[18]。
本研究显示DEHP孕期暴露可导致胎盘雌激素合成关键酶17HSDb3、3HSDb1 mRNA表达上调,CYP191a1 mRNA表达下调,基质金属蛋白酶MMP2、MMP9 mRNA表达下调,抑制PPARG活性后17HSDb3和MMP9 mRNA表达改变有一定恢复。提示邻苯二甲酸酯孕期暴露可通过PPARG上调胎盘17HSDb3 mRNA表达,下调MMP9 mRNA表达,从而阻碍孕期胎盘雌激素和基质金属蛋白酶的合成分泌,可能从两方面影响妊娠:①胎盘合成分泌雌激素能力下降[15],影响胎盘供血等胎儿发育关键因素[19],阻碍胎儿发育[16];②基质金属蛋白酶等炎症因子与滋养细胞侵入子宫内膜和螺旋动脉及母胎循环建立密切相关[20-22],其缺乏可导致母胎循环不足,胎盘缺血缺氧,胎儿生长受限[20]。
邻苯二甲酸孕期暴露对胎盘PPARG的影响研究较少[23],而胎盘PPARG在邻苯二甲酸酯孕期暴露生殖毒性中的作用更是缺乏相应研究。本研究不仅证实了邻苯二甲酸酯孕期暴露可上调胎盘PPARG蛋白表达,还发现胎盘PPARG蛋白表达可能参与邻苯二甲酸酯调控胎盘激素合成酶和基质金属蛋白酶的过程,为进一步研究邻苯二甲酸酯孕期暴露的生殖毒性机制提供了参考。
4 结论本研究通过动物模型证实DEHP孕期暴露可通过上调胎盘PPARG蛋白表达来调节胎盘雌激素合成关键酶、基质金属蛋白酶mRNA表达,这可能是DEHP孕期暴露导致胎盘雌激素和基质金属蛋白酶合成分泌受阻的途径之一。
| [1] | Chen JA, Li X, Li J, et al. Degradation of environmental endocrine disruptor di-2-ethylhexyl phthalate by a newly discovered bacterium, Microbacterium sp. strain CQ0110Y[J]. Appl Microbiol Biotechnol,, 2007, 74(3): 676–682. doi: 10.1007/s00253-006-0700-3 |
| [2] | Matsumoto M, Hirata-Koizumi M, Ema M. Potential adverse effects of phthalic acid esters on human health: a review of recent studies on reproduction[J]. Regul Toxicol Pharmacol, 2008, 50(1): 37–49. doi: 10.1016/j.yrtph.2007.09.004 |
| [3] | Jurewicz J, Hanke W. Exposure to phthalates: reproductive outcome and children health. A review of epidemiological studies[J]. Int J Occup Med Environ Health, 2011, 23(2): 115–141. |
| [4] | Chen JA, Liu HJ, Qiu ZQ, et al. Analysis of di-n-butyl phthalate and other organic pollutants in Chongqing women undergoing parturition[J]. Environ Pollut, 2008, 156(3): 849–853. doi: 10.1016/j.envpol.2008.05.019 |
| [5] | Huang Y, Li J, Garcia JM, et al. Phthalate levels in cord blood are associated with preterm delivery and fetal growth parameters in Chinese women[J]. PLoS One, 2014, 9(2): e87430. doi: 10.1371/journal.pone.0087430 |
| [6] | Ferguson KK, McElrath TF, Meeker JD. Environmental phthalate exposure and preterm birth[J]. JAMA Pediatr, 2014, 168(1): 61–67. doi: 10.1001/jamapediatrics.2013.3699 |
| [7] | Swan SH. Environmental phthalate exposure and the odds of preterm birth: an important contribution to environmental reproductive epidemiology[J]. JAMA Pediatr, 2014, 168(1): 14–15. doi: 10.1001/jamapediatrics.2013.4215 |
| [8] | Meeker JD, Hu H, Cantonwine DE, et al. Urinary phthalate metabolites in relation to preterm birth in Mexico city[J]. Environ Health Perspect, 2009, 117(10): 1587–1592. doi: 10.1289/ehp.0800522 |
| [9] | Tetz LM, Cheng AA, Korte CS, et al. Mono-2-ethylhexyl phthalate induces oxidative stress responses in human placental cells in vitro[J]. Toxicol Appl Pharmacol, 2013, 268(1): 47–54. doi: 10.1016/j.taap.2013.01.020 |
| [10] | Xu C, Chen JA, Qiu ZQ, et al. Ovotoxicity and PPAR-mediated aromatase downregulation in female Sprague-Dawley rats following combined oral exposure to benzo[a]pyrene and di-(2-ethylhexyl) phthalate[J]. Toxicol Lett, 2010, 199(3): 323-332. |
| [11] | Ernst J, Jann JC, Biemann R, et al. Effects of the environmental contaminants DEHP and TCDD on estradiol synthesis and aryl hydrocarbon receptor and peroxisome proliferator-activated receptor signalling in the human granulosa cell line KGN[J]. Mol Hum Reprod, 2014, 20(9): 919–928. doi: 10.1093/molehr/gau045 |
| [12] | Luo YM, Wan XH, Jiang DQ, et al. Effects of PPAR-gamma agonist rosiglitazone on MMP-9 and TIMP-1 expression of monocyte-derived macrophages isolated from patients with acute coronary syndrome[J]. Chin J Cardiol, 2009, 37(8): 739–745. |
| [13] | Matsuda S, Kobayashi M, Kitagishi Y. Expression and Function of PPARs in Placenta[J]. PPAR Res, 2013: 275–283. |
| [14] | 许川.邻苯二甲酸酯类和多环芳烃类代表物质联合雌性生殖毒性与健康风险评价研究[D].重庆:第三军医大学, 2009. http://cdmd.cnki.com.cn/Article/CDMD-90025-2009253596.htm |
| [15] | Heude B, Pelloux V, Forhan A, et al. Association of the Pro12Ala and C1431T variants of PPARgamma and their haplotypes with susceptibility to gestational diabetes[J]. J Clin Endocrinol Metab, 2011, 96(10): E1656–E1660. doi: 10.1210/jc.2011-0381 |
| [16] | Somasundaram DB, Selvanesan BC, Ramachandran I, et al. Lactational Exposure to Di (2-ethylhexyl) Phthalate Impairs the Ovarian and Uterine Function of Adult Offspring Rat[J]. Reprod Sci, 2016, 23(4): 549–559. doi: 10.1177/1933719115607995 |
| [17] | Rodie VA, Young A, Jordan F, et al. Human placental peroxisome proliferator-activated receptor delta and gamma expression in healthy pregnancy and in preeclampsia and intrauterine growth restriction[J]. J Soc Gynecol Investig, 2005, 12(5): 320–329. doi: 10.1016/j.jsgi.2005.03.004 |
| [18] | Parillo F, Maranesi M, Brecchia G, et al. In vivo chronic and in vitro acute effects of di (2-ethylhexyl) phthalate on pseudopregnant rabbit corpora lutea: possible involvement of peroxisome proliferator-activated receptor gamma[J]. Biol Reprod, 2014, 90(2): 41. doi: 10.1095/biolreprod.113.109223 |
| [19] | Hu JL, Du GZ, Zhang W, et al. Short-term neonatal/prepubertal exposure of dibutyl phthalate (DBP) advanced pubertal timing and affected hypothalamic kisspeptin/GPR54 expression differently in female rats[J]. Toxicology, 2013, 314(1): 65–75. doi: 10.1016/j.tox.2013.09.007 |
| [20] | Li W, Mata KM, Mazzuca MQ, et al. Altered matrix metalloproteinase-2 and -9 expression/activity links placental ischemia and anti-angiogenic sFlt-1 to uteroplacental and vascular remodeling and collagen deposition in hypertensive pregnancy[J]. Biochem Pharmacol, 2014, 89(3): 370–385. doi: 10.1016/j.bcp.2014.03.017 |
| [21] | Plaks V, Rinkenberger J, Dai J, et al. Matrix metalloproteinase-9 deficiency phenocopies features of preeclampsia and intrauterine growth restriction[J]. Proc Natl Acad Sci USA, 2013, 110(27): 11109–11114. doi: 10.1073/pnas.1309561110 |
| [22] | Swierczewski A, Kobos J, Pasiński J, et al. Expression of metalloproteinase MMP-9 and tissue inhibitor of metalloproteinase TIMP-2 in placenta of pregnant women with intrauterine growth restriction[J]. Ginekol Pol, 2012, 83(6): 439–445. |
| [23] | Xu Y, Agrawal S, Cook TJ, et al. Maternal di-(2-ethylhexyl)-phthalate exposure influences essential fatty acid homeostasis in rat placenta[J]. Placenta, 2008, 29(11): 962–969. doi: 10.1016/j.placenta.2008.08.011 |



