兽用抗生素用于动物疾病预防、治疗、提高饲料利用率和促进动物生长。兽用抗生素经过动物体内后主要以原药和代谢产物的形式随粪尿排出体外,进入土壤,从而导致土壤中抗生素的污染,对生态安全和人体健康产生威胁。
土壤样品基质复杂,含有大量的有机酸等干扰成分,兽药抗生素残留在土壤中的含量又很低,因此,对样品前处理和检测的仪器都有很高的要求。目前文献对土壤样品中兽用抗生素残留的检测方法报道还较少,对于兽用抗生素残留的检测主要采用高效液相色谱检测法[1-3]和液相色谱串联质谱法[4-6]。超高效液相色谱串联质谱技术具有分析速度快、灵敏度高的特点。本文采用超高效液相色谱串联质谱仪检测和双柱串联固相萃取法净化,建立了同时检测土壤中大环内酯类、喹诺酮类、林可霉素多种类型兽用抗生素残留方法。
1 材料与方法 1.1 仪器与试剂Waters UPLC-TQMS XevoTM 超高效液相色谱串联质谱仪(美国Waters 公司),配有电喷雾离子源;色谱柱ACQUITY UPLCTM BEH C18 (2.1 mm × 100 mm,1.7 μm,Waters 公司);Lab Tech全自动固相萃取仪器(北京莱伯泰科仪器股份有限公司);氮吹仪(美国 Organomation 公司),TGL-16B离心机(上海安亭有限公司);超声波清洗器(德国Elma公司)。Oasis HLB 固相萃取柱(6 mL/200 mg,Waters 公司);强阴离子交换柱SAX(6 mL/500 mg,Agilent 公司)。
抗生素标准品:替米考星,泰乐菌素,红霉素,恩诺沙星,环丙沙星,诺氟沙星,二氟沙星,沙拉沙星,林可霉素均购自德国Dr.Ehrenstorfer GmbH 公司,纯度均大于98%。甲酸、甲醇和乙腈(色谱纯,Merck 公司),水为MilliQ超纯水;其他试剂为分析纯。
1.2 标准储备液的配制分别称取9种兽用抗生素标准品0.01 g(精确至0.000l g),用50%(体积分数)乙腈水溶液溶解,定容至100 mL容量瓶中,制得100 mg/L的标准储备液。分别准确吸取9种抗生素的储备液1.00 mL于100mL容量瓶中,并用乙腈定容,使成1.00mg/L的混合标准储备液,置于4℃冰箱中避光保存。根据需要,用空白样品基质提取液稀释成系列标准工作液。
1.3 仪器条件 1.3.1 色谱条件柱温: 30℃;进样器温度:25℃;进样体积 10 μL;流速:0.4 mL/min;流动相:A为0.1%甲酸水溶液,B为乙腈;梯度洗脱程序:0 ~ 0.5 min A保持90 %,0.5 min ~ 5.5 min A由90%降至50%,5.5 min ~ 6 min A由50%降至10%,6.0 min ~ 6.5 min A由10%升至90%,6.5 min ~ 7.0 min 保持A为90%。
1.3.2 质谱条件电离方式采用电喷雾ESI正离子模式,毛细管电压:3.0 kV,离子源温度:150℃,去溶剂气流量:750 L/h,去溶剂气温度:450℃,锥孔反吹起流量为:50 L/h。多反应监测(MRM)模式定量测定,9种兽用抗生素母离子、子离子、锥孔电压及碰撞能量见表 1。
| 兽药 | 保留时间/min | 母离子/(m/z) | 子离子/(m/z) | 锥孔电压/V | 碰撞能量/eV |
| 替米考星 | 5.00 | 869.79 | 174.10* | 66 | 44 |
| 87.99 | 66 | 66 | |||
| 泰乐菌素 | 5.80 | 916.80 | 174.06* | 52 | 74 |
| 88.00 | 52 | 40 | |||
| 红霉素 | 5.53 | 734.62 | 158.07* | 36 | 30 |
| 116.02 | 36 | 44 | |||
| 恩诺沙星 | 3.55 | 360.13 | 316.20* | 32 | 18 |
| 245.08 | 32 | 26 | |||
| 环丙沙星 | 3.29 | 332.06 | 231.04* | 42 | 34 |
| 245.09 | 42 | 24 | |||
| 诺氟沙星 | 3.19 | 320.10 | 276.15* | 32 | 20 |
| 233.06 | 32 | 22 | |||
| 二氟沙星 | 3.98 | 399.98 | 355.95* | 32 | 28 |
| 298.9 | 32 | 19 | |||
| 沙拉沙星 | 3.91 | 385.96 | 298.92* | 36 | 20 |
| 341.90 | 36 | 28 | |||
| 林可霉素 | 2.71 | 407.18 | 359.22* | 34 | 26 |
| 126.03 | 34 | 18 | |||
| 注:*为定量离子 | |||||
1.4 样品前处理 1.4.1 样品提取
准确称取土壤样品2.00 g于50mL聚乙烯离心管中,加入20 mL提取液[V(乙腈):V(0.2 mol/L磷酸盐pH = 9.0缓冲溶液,其中含0.1 mol/L EDTA)= 1∶1],涡旋混合1 min后,超声提取20 min,以5 000 r/min离心5min,转移上清液于离心管中,残渣再重复提取一次,合并两次提取液在40℃水浴中,氮气浓缩溶液至10 mL。因乙腈比水容易挥发,两次提取体积乙腈总体积20 mL,水20mL,吹氮气到体积至10 mL时,剩余溶液以水为主,再加入纯水至200 mL,此时溶液乙腈体积小于2%,待净化。
1.4.2 样品净化利用全自动固相萃取仪,按仪器设定程序操作,活化体积10.0 L,流速3.0 mL/min;上样体积100 mL,流速5.0 mL/min;淋洗和洗脱体积均设定10.0 L,流速3.0 mL/min。采用SAX-HLB串联固相萃取小柱净化,先分别用10 mL甲醇、10 mL缓冲溶液(pH = 9.0)活化固相萃取小柱,再加样品,用10 mL超纯水淋洗串联柱除去极性大的杂质,而目标物保留在HLB固相萃取柱上,继续抽真空10 min 除去柱中残留水分,拆下SAX 小柱,用10 mL 甲醇将目标物洗脱下来,收集洗脱液,在40℃氮气浓缩仪上吹至近干,用乙腈水溶液[乙腈∶水=1∶9(v/v)]定容至1 mL,涡旋混匀,过0.2 μm滤膜,待UPLC-MS/MS进样分析。
1.5 标准曲线的制备为了消除基质效应,准确地定量,本实验采用基质匹配混合标准溶液的方式配置工作曲线。用不含抗生素的土壤样品经过1.4方法提取得到空白样品溶液,用该溶液逐级稀释标准混合工作液,配制成5 μg/L、10 μg/L、20 μg/L、50 μg/L、100 μg/L 5个不同质量浓度的系列混合标准溶液,分别进UPLC-MS/MS分析测定。以峰面积为横坐标,以质量浓度为纵坐标绘制标准曲线。
1.6 样品测定计算样品按上述方法进行测定。通过与校正溶液的保留时间和各离子对的相对丰度的比对,对试液中待测物进行定性分析。根据选择的定量离子对待测物进行定量分析,按照下式计算抗生素药物残留量。
| $X=\frac{C\times V}{m}$ |
式中:X—样品中待测组分的含量,μg/kg;
C—根据标准曲线得到的测定液中待测组分的质量浓度,μg /L
V—定容体积,mL;
m—样品称样量,g。
2 结果与讨论 2.1 流动相的优化本试验分别比较了甲醇—水和乙腈—水体系,发现用甲醇—水做流动相沙星类抗生素色谱峰拖尾,大环内酯类峰展宽,林可霉素响应变小。另外,又分别考察了水相中添加0.1%、0.2%甲酸或醋酸胺的影响,发现在水相中添加0.1%甲酸目标物峰型好且响应最大。因此,最终选择乙腈—0.1%甲酸水为流动相,在此条件下获得的的总离子流图见图 1。
|
| 图 1 不同提取溶剂的比较 |
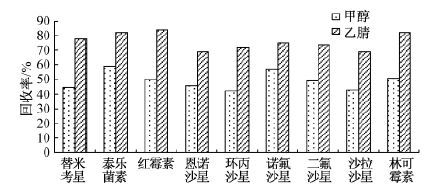
2.2 提取溶剂的选择
分别比较了甲醇—水和乙腈—水作为提取溶剂,对土壤中抗生素提取效率的影响。结果表明甲醇提取效率低而乙腈提取效率高(图 1)。因此,选择乙腈—水为提取溶剂。
2.3 提取条件pH值的考察由于所检测的抗生素种类多且理化性质有一定的差别,因此为了使多数目标物能获得较好的回收率,分别考察了不同pH值缓冲溶液(柠檬酸pH = 3.0、柠檬酸pH = 4.0、磷酸盐pH = 7.0、磷酸盐pH = 8.0和磷酸盐pH = 9.0)对提取效率的影响。结果表明,当用0.2 mol/L磷酸盐调节pH为9.0时,本实验中多数目标化合物可获得理想的回收率(表 2)。
| 缓冲溶液 | 替米考星 | 泰乐菌素 | 红霉素 | 恩诺沙星 | 环丙沙星 | 诺氟沙星 | 二氟沙星 | 沙拉沙星 | 林可霉素 |
| 柠檬酸pH=3.0 | 42% | 47% | 20% | 31% | 34% | 32% | 21% | 24% | 34% |
| 柠檬酸pH=4.0 | 51% | 67% | 42% | 69% | 54% | 63% | 64% | 71% | 42% |
| 磷酸盐pH=7.0 | 74% | 72% | 67% | 71% | 59% | 59% | 72% | 68% | 69% |
| 磷酸盐pH =8.0 | 84% | 74% | 72% | 78% | 62% | 61% | 79% | 75% | 74% |
| 磷酸盐pH= 9.0 | 90% | 75% | 83% | 76% | 69% | 65% | 87% | 82% | 80% |
2.4 净化条件的选择
土壤样品基质复杂,含有大量的腐蚀酸类有机质,对检测将会产生干扰,因此,在仪器分析前对样品进行净化显得尤为重要。本实验采用HLB萃取小柱和SAX柱串联的方式进行净化,其中SAX为强阴离子交换柱,可有效除去腐蚀酸性物质的干扰。经过对固相萃取条件的优化,该方法可有效去除样品中干扰物且对目标物吸附小,净化后目标物回收率替米考星82%、泰乐菌素87%、红霉素90%、恩诺沙星85%、环丙沙星81%、诺氟沙星80%、二氟沙星91%、沙拉沙星82%、林可霉素94%,均可以达到80%以上。
2.5 方法线性范围与检出限、检测限目标物在5 μg/L~ 100 μg/L范围内,9种抗生素线性关系良好,其相关系数(r)为0.9971~ 0.9997。当信噪比S/N等于3时,按照取样量2.0 g计算,方法检出限(LOD)为0.24 μg/kg ~ 2.90 μg/kg,当信噪比S/N = 10时,方法检测限(LOD)为0.82 μg/kg ~ 10.1 μg/kg。
2.6 方法的回收率和精密度空白土壤样品中分别添加不同量的混合标准溶液,使成抗生素在土壤中浓度为5 μg/kg、10 μg/kg、40 μg/kg,每个浓度设定5个平行样,按1.4方法测定方法的回收率和精密度(表 3)。土壤中9种抗生素的平均回收率在65.2% ~ 106.5%之间,相对标准偏差RSD为2.4% ~ 14.4%;满足残留分析的要求。土壤中添加9种抗生素使浓度为10 μg/kg后,按上述方法进行处理和测定后得到总离子流图(图 2)。
| 化合物 | 线性方程 | 相关系数(r) | 5.0 μg/kg | 10 μg/kg | 40 μg/kg | 检出限(μg/kg) | |||
| 回收率/% | RSD/% | 回收率% | RSD% | 回收率% | RSD% | ||||
| 替米考星 | Y= 7.36×105X+1437.9 | 0.9975 | 81.6 | 11.9 | 71.8 | 12.3 | 106.5 | 14.2 | 1.82 |
| 泰乐菌素 | Y= 1.98×106X+1592.9 | 0.9995 | 77.8 | 7.3 | 73.2 | 6.1 | 77.5 | 4.8 | 0.85 |
| 红霉素 | Y= 1.37×106X+728.7 | 0.9976 | 85.6 | 5.3 | 90.6 | 5.9 | 94.3 | 4.3 | 0.71 |
| 恩诺沙星 | Y= 1.32×106X+1089 | 0.9994 | 84.4 | 11.3 | 75.7 | 10.9 | 81.6 | 9.4 | 0.93 |
| 环丙沙星 | Y= 4.92×105X+513.3 | 0.9991 | 78.6 | 12.9 | 69.6 | 11.5 | 71.3 | 12.5 | 2.56 |
| 诺氟沙星 | Y= 8.26×105X+7453.8 | 0.9971 | 67.7 | 13.5 | 69.3 | 11.9 | 65.2 | 14.4 | 2.90 |
| 二氟沙星 | Y= 1.08×106X+7788.5 | 0.9976 | 87.2 | 4.5 | 92.8 | 3.9 | 93.3 | 2.4 | 1.34 |
| 沙拉沙星 | Y= 1.12×106X+8220.7 | 0.9977 | 72.1 | 7.8 | 69.8 | 9.1 | 78.9 | 8.3 | 1.92 |
| 林可霉素 | Y= 6.86×106X+4070.2 | 0.9997 | 93.8 | 3.9 | 98.9 | 4.7 | 89.7 | 5.1 | 0.24 |
|
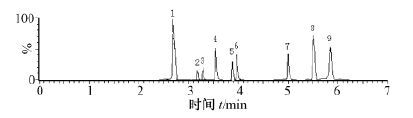
| 1、 林可霉素,2、诺氟沙星,3、环丙沙星,4、恩诺沙星,5、沙拉沙星,6、二氟沙星,7、替米考星,8、红霉素,9、泰乐菌素 图 2 土壤样品中加入9种兽用抗生素的总离子流图 |
2.7 样品测定
利用上述所建立的分析方法,对在广州市养猪场附采集的5份土壤样品进行检测,有2份样品检出含有喹诺酮类抗生素,其中一个样品检出恩诺沙星,浓度为2.1 μg/kg,另外一个样品检出诺氟沙星,浓度为1.7 μg/kg
3 小结本实验建立了同时检测土壤中不同类型的多种兽用抗生素SPE-UPLC-MS/MS分析方法,所用的超高效液相色谱法分析时间短,在7 min内完成所有抗生素的快速分离检测,实现了土壤样品中不同种类抗生素的快速、准确、灵敏的检测。
| [1] | 邰义萍, 莫测辉, 李彦文, 等. 固相萃取-高效液相色谱-荧光检测土壤中喹诺酮类抗生素[J]. 分析化学, 2009, 37 (12): 1733–1737. |
| Click to display the text | |
| [2] | 李艳霞, 李帷, 张雪莲, 等. 固相萃取-高效液相色谱法同时检测畜禽粪便中14种兽药抗生素[J]. 分析化学, 2012, 40 (2): 213–217. |
| Click to display the text | |
| [3] | 周爱霞, 苏小四, 高松, 等. 高效液相色谱测定地下水、土壤及粪便中4种磺胺类抗生素[J]. 分析化学, 2014, 42 (3): 397–402. |
| Click to display the text | |
| [4] | 马丽丽, 郭昌胜, 胡伟, 等. 固相萃取-高效液相色谱-串联质谱法同时测定土壤中氟喹诺酮、四环素和磺胺类抗生素[J]. 分析化学, 2010, 38 (1): 21–26. |
| Click to display the text | |
| [5] | 厉文辉, 史亚利, 高立红, 等. 加速溶剂萃取-高效液相色谱-串联质谱法同时检测鱼肉中喹诺酮、磺胺与大环内酯类抗生素[J]. 分析测试学报, 2010, 29 (10): 987–992. |
| Click to display the text | |
| [6] | 刘佳佳, 金芬, 佘永新, 等. 液相色谱-串联质谱法测定牛奶中5种多肽类抗生素[J]. 分析化学, 2011, 39 (5): 652–657. |
| Click to display the text |


