2,4-二硝基苯甲醚(2,4-dinitroanisole , DNAN )是一种熔铸不敏感载体炸药,具有冲击波感度低的特性,DNAN含有两个硝基,能量和密度损失较2,4,6-三硝基甲苯(TNT)小,被认为是TNT最有前景的替代物[1]。DNAN外观为无色(或黄色)针状或单斜晶体,溶于乙醇、乙醚、丙酮、苯等多数有机溶剂,微溶于热水。熔点94℃~96℃,密度1.34 g/cm3,低于TNT(1.654 g/cm3)。迄今,有关DNAN的研究资料主要集中在化工领域[2-2]。关于其毒性的研究资料较少,本文为综合评价一定时期内反复多次经口染毒DNAN引起的毒性效应,为确定慢性毒性试验的剂量及初步计算人群接触的安全水平提供理论依据。
1 材料与方法 1.1 主要仪器与试剂JJ2000天平(常熟双杰测试仪器厂),MP1002天平(上海恒平科学仪器有限公司),AU480全自动生化分析仪(美国贝克曼库尔特有限公司),XT-1800i血液分析仪,UF-500i尿液有形成分分析仪,CA-550血凝仪(日本希森美康公司)。
DNAN混悬液称取适量DNAN(纯度>99.0%,由某研究所提供)置于玛瑙研钵,加入少量4%淀粉溶液混匀,贴壁缓慢研磨成细小颗粒。研磨后用4%淀粉溶液配成4.00 mg/mL的DNAN淀粉混悬液。
1.2 实验动物选择健康SPF级初成年SD大鼠96只,雌雄各半,体重100 ±10 g,由西安交通大学实验动物中心提供。分笼饲养于空调室内,室温23±3℃,相对湿度55%~65%,每天光照12 h,灭菌全价营养颗粒饲料喂食,自由饮水。
1.3 染毒与观察按化学品啮齿类动物亚慢性经口毒性试验方法[5],将96只大鼠随机分为低、中、高3个剂量组和1个对照组,每组24只,雌雄各半。剂量组给予4%淀粉配制的DNAN混悬液灌胃,剂量为5.0、15.0、45.0 mg/kg,对照组给予4%淀粉溶液。每日染毒1次,为期90 d。每周1次称体重和饲料消耗量,以作为调整染毒量的依据。详细观察动物在DNAN染毒后所出现的中毒症状及出现各种症状的先后次序、时间等。试验结束前采集尿液进行尿常规检查。试验结束后,用10%水合氯醛麻醉大鼠,腹主动脉采血,进行血常规、血清生化指标的测定。对大鼠进行系统解剖,检查体表、体腔和各开口处,颅、胸、腹腔及其内容物。取肝、肺、肾等主要脏器称湿重后固定于10%福尔马林液中,常规石蜡包埋切片,HE染色,进行病理组织学检查。
1.4 统计学方法实验数据采用SPSS 13.0软件进行统计学分析。计量资料统计描述采用x±s,组间比较采用t检验,体重随时间变化趋势采用重复测量方差分析。若资料不满足球对称性检验,则对自由度进行Greenhouse-Geisser校正。计数资料采用
在染毒期间,部分动物出现异常症状及死亡现象,雄性对照组第2和4周各死亡1只,死亡前进食量减少,体重降低,解剖后未见明显异常;低剂量组第11周死亡1只,死前未见任何明显体征,解剖后未见明显异常;中剂量组第8周死亡1只,解剖后未见明显异常;高剂量组第8周死亡1只,死亡前发现左前肢肿大,活动僵硬,解剖后未见明显异常。雌性对照组未见异常症状,中剂量组第7周1只头偏向右侧,持续至实验结束;第9周1只右眼有出血现象,1周后消退;高剂量组第8周1只右耳后感染,2周后逐渐消退痊愈。其余大鼠活动正常,毛色光泽,尿液、粪便未发现异常情况,未见明显中毒症状。
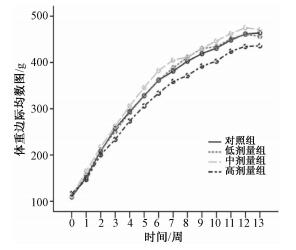
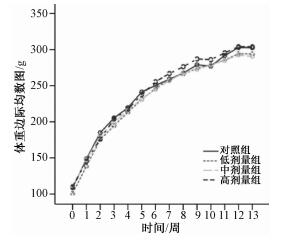
2.2 生长发育 2.2.1 体重变化情况各染毒组大鼠体重随染毒时间的延长呈增长趋势,与对照组比较差异无统计学意义(P>0.05;图 1、图 2)。
|
| 图 1 DNAN染毒雄性大鼠体重变化曲线 |
|
| 图 2 DNAN染毒雌性大鼠体重变化曲线 |
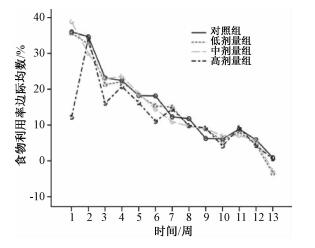
2.2.2 食物利用率
由图 3和图 4可见,雌雄性大鼠的食物利用率总体呈下降趋势,组间差别有统计学意义,经两两比较,高剂量组食物利用率显著低于对照组(P<0.05)。
|
| 图 3 DNAN染毒雄性大鼠食物利用率变化 |

|
| 图 4 DNAN染毒雌性大鼠食物利用率变化 |
2.3 尿常规
高剂量组尿白细胞含量升高,与对照组相比差异有统计学意义(P<0.05)。其余各指标(葡萄糖、尿胆原、胆红素、酮体、潜血、比重、酸碱度、蛋白质、亚硝酸盐、抗坏血酸)组间差别无统计学意义(P>0.05)。
2.4 血常规雄性大鼠低剂量组红细胞体积分布宽度标准差(RDW-SD)、红细胞分布宽度(RDW-CV)和白细胞(WBC)降低,平均红细胞体积(MCV)升高;中剂量组平均红细胞体积(MCV)降低;高剂量组血小板分布宽度(PDW)、RDW-SD、RDW-CV和WBC降低,与对照组比较差异均有统计学意义(P<0.05)。雌性大鼠低剂量组红细胞(RBC)、RDW-SD、RDW-CV、WBC、红细胞压迹(HCT)、血红蛋白(HGB)降低,平均血红蛋白量(MCH)、MCV升高;中剂量组PCT、PDW、血小板比值(P-LCR)、平均血小板体积(MPV)、RDW-CV升高;高剂量组P-LCR、MPV、RDW-CV、MCH、MCV升高,RBC、WBC、HCT、HGB和平均血红细胞浓度(MCHC)降低,与对照组比较差异均有统计学意义(P<0.05;表 1)。
| 性别 | 分组 | N | PCT/% | PDW/% | P-LCR/% | PLT/(109/L) | RBC/(1012/L) | RDW-SD | RDW-CV/% |
| 雄 | 对照组 | 10 | 0.99 ±0.37 | 8.70 ±0.33 | 9.06 ±1.70 | 1 309.70 ±490.35 | 8.70 ±3.06 | 18.40 ±2.05 | 28.86 ±1.81 |
| 低剂量 | 10 | 0.97 ±0.13 | 8.33 ±0.37 | 8.21 ±1.57 | 1 293.20 ±188.44 | 8.27 ±0.37 | 15.58 ±1.35** | 27.49 ±0.97* | |
| 中剂量 | 11 | 1.03 ±0.16 | 8.75 ±0.48 | 9.65 ±2.01 | 1 342.45 ±200.59 | 9.77 ±0.803 | 19.32 ±1.74 | 28.85 ±1.86 | |
| 高剂量 | 11 | 0.96 ±0.07 | 8.26 ±0.43* | 8.30 ±1.83 | 1 288.09 ±88.19 | 8.22 ±0.42 | 15.87 ±1.16* | 27.01 ±0.91* | |
| 雌 | 对照组 | 11 | 0.99 ±0.13 | 8.84 ±0.42 | 9.85 ±2.03 | 1 286.64 ±203.41 | 9.74 ±0.51 | 20.44 ±1.27 | 30.65 ±1.14 |
| 低剂量 | 12 | 0.92 ±0.10 | 8.73 ±0.67 | 10.30 ±3.25 | 1 177.08 ±127.02 | 8.51 ±0.57** | 17.04 ±1.74* | 27.53 ±1.12* | |
| 中剂量 | 12 | 1.11 ±0.14* | 9.66 ±0.63* | 13.67 ±2.54* | 1 354.00 ±190.19 | 9.65 ±0.65 | 21.99 ±2.47 | 33.60 ±2.68* | |
| 高剂量 | 12 | 1.07 ±0.15 | 9.30 ±0.61 | 12.83 ±2.66* | 1 310.25 ±162.19 | 8.22 ±0.49** | 19.76 ±1.83 | 33.01 ±4.05* | |
| 雄 | 对照组 | 10 | 8.50 ±3.79 | 44.56 ±15.63 | 145.70 ±1.37 | 15.08 ±5.33 | 294.40 ±103.58 | 51.11 ±1.48 | 7.58 ±0.23 |
| 低剂量 | 10 | 5.57 ±1.46* | 44.40 ±1.31 | 143.40 ±4.50 | 17.36 ±0.49 | 323.00 ±3.50 | 53.75 ±1.44** | 7.50 ±0.25 | |
| 中剂量 | 11 | 7.33 ±1.96 | 48.46 ±3.26 | 158.27 ±10.84 | 16.23 ±0.47 | 326.64 ±3.47 | 49.68 ±1.45* | 7.65 ±0.34 | |
| 高剂量 | 11 | 3.76 ±1.90** | 42.69 ±1.62 | 138.36 ±5.37 | 16.84 ±0.42 | 324.09 ±2.30 | 51.95 ±1.23 | 7.52 ±0.33 | |
| 雌 | 对照组 | 11 | 7.07 ±2.72 | 47.45 ±1.52 | 155.82 ±4.77 | 16.03 ±0.72 | 328.36 ±4.32 | 48.81 ±2.49 | 7.71 ±0.34 |
| 低剂量 | 12 | 2.49 ±2.59** | 43.68 ±2.03** | 142.92 ±7.08** | 16.81 ±0.54* | 327.17 ±3.74 | 51.38 ±1.79* | 7.83 ±0.48 | |
| 中剂量 | 12 | 7.89 ±3.30 | 46.42 ±2.60 | 151.58 ±7.37 | 15.74 ±0.86 | 326.83 ±5.31 | 48.23 ±3.22 | 8.24 ±0.35* | |
| 高剂量 | 12 | 4.50 ±2.24* | 42.78 ±2.35** | 136.58 ±8.74** | 16.63 ±0.66* | 319.17 ±4.00** | 52.11 ±2.17* | 8.18 ±0.35* | |
| 注:与对照组比较*P<0.05,**P<0.01。PCT:血小板压迹;PDW:血小板分布宽度;P-LCR:血小板比值;RBC:红细胞;RDW-SD:红细胞体积分布宽度标准差;RDW-CV:红细胞分布宽度;WBC:白细胞;HCT:红细胞压迹;HGB:血红蛋白;MCH:平均血红蛋白量;MCHC:平均血红细胞浓度;MCV:平均红细胞体积;MPV:平均血小板体积 | |||||||||
白细胞分类计数及百分数结果显示,雄性大鼠低剂量淋巴细胞(LYM)、单核细胞(MO)、中性粒细胞(NE)降低;中剂量组的LYM降低;高剂量组的LYM、淋巴细胞百分比(LYM%)、MO、NE、中性粒细胞百分比(NE%)降低,与对照组比较均有差异均有统计学意义(P<0.05)。雌性大鼠低、高剂量组嗜酸性粒细胞(EO)、LYM、MO、单核细胞百分比(MO%)、NE降低,NE%升高;高剂量组的EO、LYM、MO、MO%降低,与对照组比较差异均有统计学意义(P<0.05;表 2)。
| 性别 | 分组 | N | BAS/(109/L) | BAS/% | EO/(109/L) | EO/% | LYM/(109/L) |
| 雄 | 对照组 | 9 | 0.01 ±0.01 | 0.07 ±0.07 | 0.13 ±0.07 | 1.43 ±0.68 | 7.55 ±2.19 |
| 低剂量 | 10 | 0.00 ±0.00 | 0.02 ±0.06 | 0.09 ±0.04 | 1.61 ±0.72 | 4.31 ±1.28** | |
| 中剂量 | 11 | 0.00 ±0.00 | 0.03 ±0.06 | 0.13 ±0.13 | 1.65 ±1.43 | 5.71 ±1.49* | |
| 高剂量 | 11 | 0.00 ±0.00 | 0.05 ±0.08 | 0.06 ±0.03 | 1.69 ±0.52 | 2.77 ±1.54** | |
| 雌 | 对照组 | 11 | 0.00 ±0.00 | 0.03 ±0.05 | 0.10 ±0.03 | 1.37 ±0.44 | 5.58 ±2.28 |
| 低剂量 | 12 | 0.00 ±0.00 | 0.01 ±0.03 | 0.04 ±0.05* | 1.65 ±0.88 | 1.83 ±2.15** | |
| 中剂量 | 12 | 0.00 ±0.00 | 0.03 ±0.05 | 0.08 ±0.04 | 1.03 ±0.49 | 6.16 ±2.77 | |
| 高剂量 | 12 | 0.00 ±0.00 | 0.03 ±0.06 | 0.05 ±0.04* | 1.09 ±0.47 | 3.54 ±1.86* | |
| 雄 | 对照组 | 9 | 79.64 ±4.54 | 0.53 ±0.10 | 5.81 ±1.18 | 1.22 ±0.38 | 13.04 ±3.42 |
| 低剂量 | 10 | 76.49 ±4.86 | 0.28 ±0.10* | 5.01 ±1.46 | 0.89 ±0.17* | 16.87 ±4.21 | |
| 中剂量 | 11 | 78.13 ±3.70 | 0.48 ±0.26 | 6.24 ±1.50 | 1.01 ±0.28 | 13.96 ±3.29 | |
| 高剂量 | 11 | 71.72 ±5.29* | 0.19 ±0.11** | 4.84 ±1.47 | 0.73 ±0.24** | 21.71 ±6.02** | |
| 雌 | 对照组 | 11 | 78.37 ±3.82 | 0.52 ±0.31 | 6.94 ±2.24 | 0.88 ±0.22 | 13.29 ±3.15 |
| 低剂量 | 12 | 71.13 ±9.17 | 0.10 ±0.14* | 3.72 ±1.21* | 0.51 ±0.38* | 23.51 ±8.89* | |
| 中剂量 | 12 | 77.08 ±5.00 | 0.52 ±0.34 | 6.17 ±1.92 | 1.14 ±0.40 | 15.70 ±5.33 | |
| 高剂量 | 12 | 78.27 ±4.21 | 0.18 ±0.13* | 3.81 ±1.40* | 0.72 ±0.29 | 16.81 ±3.84 | |
| 注:与对照组比较*P<0.05,**P<0.01。BAS:嗜碱性粒细胞;BAS%:嗜碱性粒细胞百分比;EO:嗜酸性粒细胞;EO%:嗜酸性粒细胞百分比;LYM:淋巴细胞;LYM%:淋巴细胞百分比;MO:单核细胞;MO%:单核细胞百分比 | |||||||
2.5 血清生化
由表 3可见,雄性中剂量组血清白蛋白(ALB)、胆碱酯酶(CHE)降低,高剂量组尿素氮(BUN)、肌酐(CREA)、尿酸(UA)、胆固醇(CHOL)、ALB、CHE降低,高剂量组碱性磷酸酶(ALP)升高,与对照组比较差异均有统计学意义(P<0.05)。雌性中、高剂量组ALB、CREA、CHOL降低,低剂量组总蛋白(TP)和中剂量组葡萄糖(GLU)升高,与对照组比较差异均有统计学意义(P<0.05)。其余生化指标组间差异无统计学意义。
| 性别 | 分组 | N | ALB/(g/L) | CHE/(U/L) | TP/(g/L) | BUN/(mmol/L) | GLU/(mmol/L) |
| 雄 | 对照组 | 10 | 34.78 ±2.27 | 1.20 ±0.42 | 70.10 ±4.31 | 8.91 ±1.11 | 8.46 ±1.75 |
| 低剂量 | 10 | 34.84 ±2.05 | 1.00 ±0.00 | 69.40 ±3.27 | 8.11 ±1.05 | 7.42 ±1.33 | |
| 中剂量 | 11 | 32.65 ±2.45* | 0.36 ±0.50* | 67.73 ±4.88 | 8.97 ±0.66 | 9.14 ±2.29 | |
| 高剂量 | 11 | 31.64 ±2.23* | 0.00 ±0.00* | 66.00 ±3.41 | 7.97 ±1.05* | 9.39 ±2.08 | |
| 雌 | 对照组 | 11 | 35.11 ±1.18 | 1.00 ±0.00 | 71.09 ±2.26 | 8.56 ±0.52 | 7.16 ±1.35 |
| 低剂量 | 12 | 33.38 ±3.34 | 0.83 ±0.39 | 71.75 ±4.31* | 9.71 ±1.93 | 7.88 ±1.91 | |
| 中剂量 | 12 | 31.13 ±1.62* | 0.00 ±0.00 | 65.58 ±2.81 | 8.33 ±0.58 | 9.05 ±1.39* | |
| 高剂量 | 12 | 31.91 ±1.37* | 0.00 ±0.00 | 67.58 ±3.09 | 8.43 ±1.21 | 8.43 ±1.61 | |
| 雄 | 对照组 | 10 | 50.63 ±3.42 | 97.50 ±29.74 | 117.30 ±24.19 | 2.05 ±0.33 | |
| 低剂量 | 10 | 50.66 ±4.30 | 99.70 ±26.71 | 114.50 ±40.60 | 1.98 ±0.32 | ||
| 中剂量 | 11 | 49.76 ±5.11 | 100.45 ±32.42 | 116.91 ±44.60 | 1.88 ±0.81 | ||
| 高剂量 | 11 | 45.01 ±3.36* | 135.18 ±37.35* | 82.36 ±10.81* | 1.34 ±0.19* | ||
| 雌 | 对照组 | 11 | 49.68 ±2.75 | 92.45 ±21.53 | 103.64 ±22.08 | 2.07 ±0.33 | |
| 低剂量 | 12 | 50.09 ±4.10 | 144.75 ±106.23 | 134.67 ±42.24 | 2.03 ±0.34 | ||
| 中剂量 | 12 | 46.19 ±0.72* | 99.75 ±24.82 | 91.67 ±20.96 | 1.33 ±0.28* | ||
| 高剂量 | 12 | 45.74 ±4.34* | 118.75 ±19.63 | 101.33 ±21.71 | 1.35 ±0.37* | ||
| 注:与对照组比较*P<0.05,**P<0.001;ALB:血清白蛋白;CHE:胆碱酯酶:TP:总蛋白;BUN:尿素氮:GLU:葡萄糖:TBIL:总胆红素;DBIL:直接胆红素;CREA:肌酐;AST:天门冬氨酸转移酶;ALT:谷丙酸氨基转移酶;CK:肌酸激酶;LDH:乳酸盐脱氢酶;ALP:碱性磷酸酶;GGT:谷酰转肽酶;UA:尿酸;CHOL:胆固醇 | |||||||
2.6 血电解质
由表 4可见,雄性大鼠中、高剂量组离子钙(ICa)、总钙(TCa)升高,高剂量组钠(Na)降低,与对照组比较均有显著差异(P<0.05);雌性大鼠低、中、高剂量组Na、pH降低,低、中剂量组ICa和高剂量TCa升高,低剂量组氯(Cl)降低,与对照组比较均有显著差异(P<0.05)。
| mmol/L | ||||||||
| 性别 | 分组 | N | K | Na | Cl | ICa | TCa | pH |
| 雄 | 对照组 | 10 | 2.26 ±4.69 | 215.96 ±52.81 | 134.36 ±117.55 | 0.00 ±0.00 | 0.00 ±0.00 | 7.54 ±0.13 |
| 低剂量 | 10 | 0.64 ±0.03 | 221.27 ±9.66 | 15.03 ±1.51 | 8.23 ±3.12* | 16.04 ±6.08* | 7.44 ±0.01 | |
| 中剂量 | 11 | 6.23 ±20.57 | 208.75 ±100.85 | 2.77 ±1.72* | 10.65 ±7.33* | 3.33 ±3.34* | 7.27 ±0.36 | |
| 高剂量 | 11 | 0.99 ±0.45 | 143.08 ±27.66* | 124.45 ±57.05 | 6.33 ±3.2* | 12.34 ±6.24* | 7.39 ±0.32 | |
| 雌 | 对照组 | 11 | 0.62 ±0.20 | 261.25 ±30.62 | 290.70 ±253.96 | 0.82 ±2.70 | 3.43 ±5.83 | 7.47 ±0.05 |
| 低剂量 | 12 | 0.69 ±0.40 | 208.12 ±64.57* | 20.52±17.15* | 5.74 ±4.41* | 11.96 ±9.04 | 7.44 ±0.02* | |
| 中剂量 | 12 | 0.37 ±0.40 | 170.97 ±26.47* | 56.88±60.99 | 5.19 ±1.70* | 6.56 ±4.13 | 7.29 ±0.14* | |
| 高剂量 | 12 | 0.65 ±0.23 | 178.34 ±23.32* | 78.08±32.18 | 4.03 ±2.79 | 16.30 ±10.41* | 7.46 ±0.03* | |
| 注:与对照组比较*P<0.05,**P<0.01。K:钾;Na:钠;CL:氯;ICa:离子钙;TCa:总钙;pH:酸碱度 | ||||||||
2.7 凝血功能
由表 5可见,雄性中、高剂量组凝血酶原时间(PT-T)、凝血酶原国际标准化比值(PT-INR)与对照组相比显著降低(P<0.05),雌性低剂量组部分活化凝血活酶时间(APTT)与对照组显著降低(P<0.05)。其于指标各组间差异不显著。
| s | ||||||
| 性别 | 分组 | N | PT-T | PT-INR | APTT | TT |
| 雄 | 对照组 | 10 | 14.52±0.50 | 1.52±0.08 | 32.31±5.22 | 48.48±7.08 |
| 低剂量 | 10 | 15.09±0.92 | 1.58±0.11 | 32.52±5.59 | 53.01±10.23 | |
| 中剂量 | 11 | 14.21±0.41** | 1.47±0.06* | 36.31±15.01 | 46.13±9.91 | |
| 高剂量 | 11 | 14.01±0.85** | 1.44±0.12** | 36.33±5.65 | 47.05±6.23 | |
| 雌 | 对照组 | 11 | 14.18±0.92 | 1.44±0.14 | 35.28±1.83 | 47.03±5.93 |
| 低剂量 | 12 | 13.99±0.58 | 1.45±0.10 | 32.03±2.83* | 44.41±2.50 | |
| 中剂量 | 12 | 14.44±0.56 | 1.52±0.10 | 32.98±3.24 | 47.28±0.56 | |
| 高剂量 | 12 | 13.90±0.84 | 1.40±0.11 | 31.18±4.64 | 44.85±4.22 | |
| 注:雄性与低剂量组比较*P<0.05,**P<0.01;PT-T:凝血酶原时间;PT-INR:凝血酶原国际标准化比值;APTT:部分活化凝血活酶时间;TT:凝血酶时间 | ||||||
2.8 病理 2.8.1 大体解剖及病理组织学检查
对各组动物进行大体解剖并观察主要脏器(脑、心、肺、肝、脾、肾、胃、肾上腺、胸腺、睾丸、附睾、子宫、卵巢),发现雌性高剂量组1例肺部结节及肺部黏连,低剂量组1例出现肺部颗粒状病变。雄性高剂量组1例肺部出现结节,12例出现睾丸及附睾体积较小。其余脏器未见明显的外观异常。光学显微镜下对各组进行病理组织学检查发现各剂量组脑、心、肺、肝、脾、肾、胃、肾上腺、子宫、卵巢有轻度炎细胞浸润、水肿和充血等表现,其余各器官未见明显病变。
2.8.2 脏器系数雄性:高剂量组附睾系数低于对照组,肝、脾、肾系数高于对照组,中剂量组心、肝、肾和低剂量组肾系数高于对照组,差异均有统计学意义(P<0.05)。雌性:高剂量组肝、肾系数高于对照组,染毒组肾上腺系数低于对照组,差异均有统计学意义(P<0.05;表 6)
| 性别 | 分组 | N | 脑 | 心 | 胸腺 | 肺 | 肝 | 脾 | 肾 | 肾上腺 | 睾丸/卵巢 | 附睾/子宫 |
| 雄 | 对照组 | 10 | 0.39 ±0.06 | 0.28 ±0.03 | 0.12 ±0.09 | 0.49 ±0.15 | 2.53 ±0.15 | 0.18 ±0.02 | 0.59 ±0.03 | 0.02 ±0.01 | 0.77 ±0.06 | 0.32 ±0.04 |
| 低剂量 | 11 | 0.41 ±0.05 | 0.31 ±0.05 | 0.09 ±0.02 | 0.55 ±0.17 | 2.89 ±0.58 | 0.18 ±0.02 | 0.66 ±0.05* | 0.02 ±0.01 | 0.83 ±0.11 | 0.36 ±0.05 | |
| 中剂量 | 11 | 0.43 ±0.05 | 0.32 ±0.02* | 0.08 ±0.03 | 0.50 ±0.10 | 2.77 ±0.16* | 0.21 ±0.04 | 0.67 ±0.06* | 0.02 ±0.01 | 0.80 ±0.09 | 0.34 ±0.04 | |
| 高剂量 | 11 | 0.42 ±0.06 | 0.31 ±0.02 | 0.08 ±0.02 | 0.55 ±0.15 | 3.04 ±0.20** | 0.23 ±0.03* | 0.76 ±0.05** | 0.02 ±0.01 | 0.80 ±0.13 | 0.31 ±0.05* | |
| 雌 | 对照组 | 12 | 0.69 ±0.07 | 0.34 ±0.02 | 0.13 ±0.03 | 0.72 ±0.21 | 2.72 ±0.14 | 0.20 ±0.02 | 0.60 ±0.03 | 0.03 ±0.01 | 0.28 ±0.11 | 0.09 ±0.05 |
| 低剂量 | 12 | 0.63 ±0.12 | 0.34 ±0.06 | 0.13 ±0.04 | 0.73 ±0.33 | 2.74 ±0.18 | 0.21 ±0.03 | 0.63 ±0.06 | 0.02 ±0.00* | 0.28 ±0.15 | 0.08 ±0.08 | |
| 中剂量 | 12 | 0.64 ±0.12 | 0.32 ±0.03 | 0.11 ±0.04 | 0.61 ±0.16 | 2.74 ±0.14 | 0.22 ±0.03 | 0.64 ±0.05 | 0.03 ±0.01* | 0.30 ±0.18 | 0.08 ±0.08 | |
| 高剂量 | 12 | 0.63 ±0.09 | 0.34 ±0.03 | 0.14 ±0.07 | 0.87 ±0.82 | 3.12 ±0.14** | 0.28 ±0.09 | 0.70 ±0.06* | 0.03 ±0.01* | 0.25 ±0.14 | 0.08 ±0.05 | |
| 注:与对照组比较*P<0.05,**P<0.001 | ||||||||||||
3 讨论
试验结果显示,试验对部分大鼠造成了一定的损害,包括活动情况改变及死亡等,组间差异不显著,但前期进行急性毒性试验并未观察到异常改变及死亡,故考虑可能是由于染毒时间的延长造成DNAN或其代谢产物在体内蓄积所造成的结果。高剂量组食物利用率显著低于对照组,但体重变化各组间差异却不显著,与急性毒性结果相同,说明DNAN对体重影响不大,却可能影响代谢功能。
尿液指标的检测仅发现雌性高剂量组尿白细胞显著高于对照组,其余各指标染毒组与对照组比较差异不显著。在生化检测中,雌雄大鼠均发现CHOL和CREA降低,结合病理组织学和脏器系数的结果,肾脏出现炎细胞浸润、水肿、充血等表现及肾脏器系数与对照组相比明显升高,而各组间体重并未出现显著差异,提示DNAN对肾脏可能造成一定损害,可能影响到肾小管和集合管的重吸收功能。血液学指标的结果发现血常规及生化多个指标出现异常,凝血功能检测结果也显示DNAN可能对血液的凝血功能造成一定影响,提示DNAN可能对血液系统造成损害。
脏器系数的变化在一定程度上反应受试物对器官的损伤作用,对受试物的靶器官具有提示作用[6]。高剂量组附睾脏器系数显著降低,雌雄肝、肾脏器系数显著升高,雌性肾上腺脏器系数降低,而雄性却无异常。结合系统解剖发现多例附睾体积较小,血清检测ALB降低及多个指标的变化有性别差异,提示DNAN对肝、附睾、肺、肾有损害并且机体对DNAN的反应可能受性别影响。系统解剖发现雌雄高剂量组均出现肺损伤,而脏器系数和病理组织学检查却并无差异,这一方面可能是DNAN对肺造成损害,另一方面也可能是由于个体敏感性不同引起的。
综上所述,根据国家标准《化学品啮齿类动物亚慢性经口毒性试验方法》(GB/T 21763-2008)[5]中“亚慢性经口毒性试验”结果评定,在本实验条件下,DNAN可能影响血液系统,肝、肾、附睾造成损伤,对肺的影响值得注意,其对机体的毒作用可能存在性别差异,长期接触对动物和人都可能具有一定的毒性作用,因此从事相关工作的人员应注意做好个体防护。
| [1] | 张光全, 董海山. 2,4-二硝基苯甲醚为基熔铸炸药的研究进展[J]. 含能材料, 2010, 18(5): 604–609. |
| [2] | 赵晓明, 陈兴, 程侣柏. 2,4-二硝基苯甲醚液相加氢反应的研究[J]. 精细化工, 1997, 14(5): 41–43. |
| [3] | 罗观, 黄辉, 张帅, 等. RDX在2,4-二硝基苯甲醚(DNAN)低共熔体系中的溶解度[J]. 含能材料, 2012, 20(4): 437–440. |
| [4] | 王红星, 王浩, 高杰, 等. 2,4-二硝基苯甲醚应用基础性能研究[J]. 科学技术与工程, 2014, 14(25): 72–75. doi: 10.3969/j.issn.1671-1815.2014.25.014 |
| [5] | 中华人民共和国国家质量监督检验检疫总局,中国国家标准化管理委员会.GB/T 21763-2008 化学品 啮齿类动物亚慢性经口毒性试验方法[S].北京:中国标准出版社,2012. |
| [6] | 周隽隽, 原福胜, 陈慧敏, 等. 甲醛和三氯乙烯联合染毒对小鼠免疫系统的影响[J]. 环境与健康杂志, 2014, 31(10): 928–931. |

