邻苯二甲酸二乙基己酯 (di-2-ethylhexyl phthalate,DEHP) 是一种邻苯二甲酸酯类化合物,是塑料生产中最主要的增塑剂之一,广泛应用于食品包装材料、室内装修材料、清洁剂、工业溶剂、润滑剂、儿童玩具和塑料医疗设备[1]。DEHP具有脂溶性和难降解性,极易通过污染的大气、土壤、水体和食物进入生物体内,可对肝、肾、肺、心、生殖系统等脏器产生毒性损害[2],是公认的环境内分泌干扰物。生精细胞包括精原细胞,精母细胞,精子细胞和精子四类细胞[3]。与其他的体细胞相比,生精细胞由于其特殊的结构和组成成分更容易受到氧化应激的影响[4]。当细胞处于氧化应激状态时,可能引起凋亡相关基因表达的改变,激活细胞凋亡程序引起细胞凋亡[5]。因此,氧化应激可能是DEHP诱发生精细胞凋亡,引起生殖毒性的机制之一。动物研究表明,DEHP主要是诱导初级精母细胞的凋亡[6],本研究将以小鼠初级精母细胞GC-2 spd为研究对象,通过观察DEHP对GC-2 spd细胞氧化应激及凋亡的影响情况,探讨DEHP对男 (雄) 性生殖系统影响的作用机制。
1 材料与方法 1.1 细胞株GC-2 spd细胞由南京医科大学馈赠。
1.2 主要试剂与仪器考马斯量蓝蛋白检测试剂盒、超氧化物歧化酶 (SOD)、丙二醛 (MDA)、谷胱甘肽过氧化物酶 (GSH-Px) 试剂盒 (南京建成生物工程研究所);DEHP (纯度为99.8%,美国Sigma公司);DMSO (纯度99.5%,美国Sigma公司);AnnexinV/PI凋亡试剂盒 (杭州联科生物科技有限公司);改良型RPMI-1640培养基 (北京赛默飞世尔生物化学制品有限公司);胎牛血清 (美国Gibco公司);FACS420流氏细胞仪 (美国BD公司);ELX-800酶标仪 (美国BioTek公司)。
1.3 细胞培养将细胞接种于含10%胎牛血清和100 u/mL青霉素、100 u/mL链霉素的RPMI-1640培养基中,于37℃的CO2(5%) 湿润培养箱中培养。当细胞融合至70%~80%,用0.25%胰酶消化,每隔一天换液1次,2~3 d传代1次。
1.4 细胞活性的测定将对数生长期细胞用胰蛋白酶消化,配制成细胞悬液,用培养基调整细胞密度至1×105个/mL,以每孔200 μL的量接种至96孔板,置于37℃的CO2(5%) 培养箱中培养24 h。分别用终浓度为0.1% DMSO和终浓度为50、100、200和400 μmol/L的DEHP将细胞染毒24 h,每个剂量组设置6个平行样。染毒结束后,每孔加入MTT溶液 (5 mg/mL)50 μL,继续孵育4 h后终止培养。弃孔内培养上清液,每孔加DMSO (二甲基亚砜)200 μL,置于摇床上摇匀。用酶标仪于570 nm波长处测定吸光度值,按公式计算不同染毒剂量组细胞的相对存活率。存活率=实验组 (OD)/对照组 (OD)。
1.5 细胞染毒将生长状态良好的对数生长期的细胞用0.25%胰酶消化,用含10%胎牛血清的RPMI-1640培养基配成细胞悬液,吹打均匀后,以每孔1×105个/mL细胞接种于六孔培养板中,每孔体积1 mL,将培养板移入CO2培养箱,37℃培养24 h后,分别以DMSO终浓度为0.1%的细胞孔作为对照组,DEHP终浓度为50、100和200 μmol/L的细胞孔作为低、中、高剂量组染毒24 h。
1.6 SOD和GSH-Px活力以及MDA含量的检测选择生长状态良好的细胞,消化离心细胞,弃上清液,加培养基重悬细胞,吹打均匀后计数,再加培养基将细胞密度调整为4×105个/mL,以每孔2 mL的量接种到6孔板培养24 h,用0、50、100和200 μmol/L浓度的DEHP溶液染毒24 h。弃培养基,用PBS清洗细胞,消化离心收集细胞。用PBS重悬细胞,于碎冰上用超声细胞破碎仪破碎细胞。4℃条件下3 000 rpm/min离心10 min,取上清液,用考马斯亮蓝比色法测定蛋白质浓度,分别用黄嘌呤氧化酶法、二硫代二硝基苯甲酸比色法和硫代巴妥酸法 (TBA) 测定SOD、GSH-Px活力以及MDA含量。
1.7 流式细胞仪法检测GC-2 spd细胞凋亡细胞染毒结束,收集培养液,再用0.25%胰酶消化并收集细胞,离心弃上清,加入1 mL的1×Buffer重悬细胞,加入5 μL Annexin V-FITC和5 μL propidium iodide (PI),于室温下在暗处放置5 min,用流式细胞仪检测GC-2 spd细胞凋亡情况。
1.8 统计学方法体外实验重复3次,所得实验数据用x±s表示。采用SPSS 20.0统计软件进行分析。多组间比较采用方差齐行检验和单因素方差分析 (ANOVA),两两比较采用SNK法,检验水准为α=0.05。
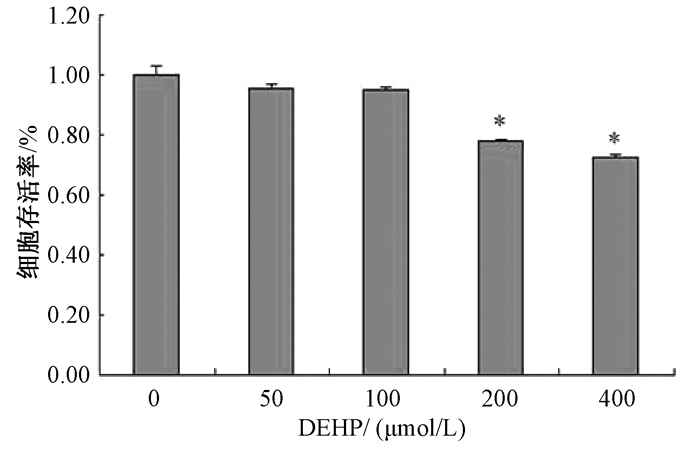
2 结果 2.1 DEHP对GC-2 spd细胞活性的影响采用MTT比色法检测不同浓度DEHP作用GC-2 spd细胞24 h后的存活率 (图 1)。随着DEHP浓度的增加 (DMSO、50、100、200和400 μmol/L),细胞存活率下降。细胞存活率分别为100%、95.68%、95.11%、78.09%和72.69%。50、100 μmol/L组与DMSO组比较细胞存活率差异没有统计学意义 (P > 0.05),200 μmol/L和400 μmol/L组存活率与DMSO组相比,差异有统计学意义 (P < 0.05)。50 μmol/L组与100 μmol/L组之间没有差异,但都与200 μmol/L和400 μmol/L组有差异 (P < 0.05);并且200 μmol/L组和400 μmol/L组的差异也具有统计学意义 (P < 0.05)。所以本次研究后续实验的最大染毒浓度确定为200 μmol/L。
|
| 图 1 DEHP对细胞存活率的影响 |
2.2 GC-2 spd细胞中SOD、GSH-Px活力以及MDA含量的变化
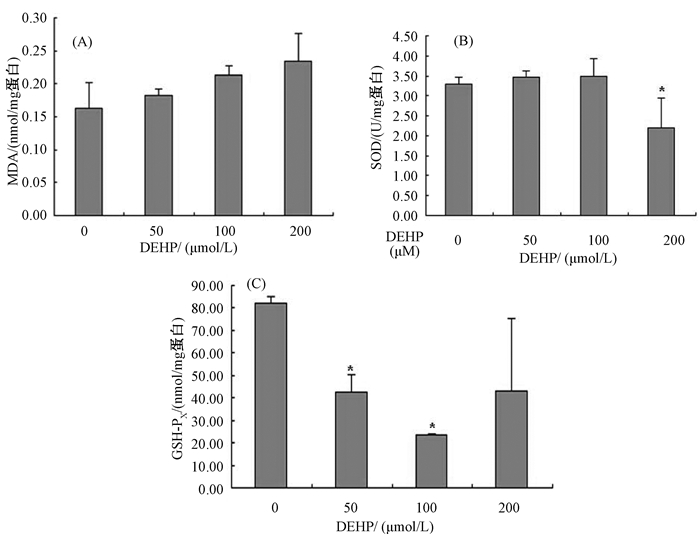
对于氧化应激的评价,核酸DNA/RNA损伤,如8-OHDG ELISA等方法比较可靠,但是通常是损伤严重的时候才可能检测出来,而传统MDA等脂质过氧化标志物/各种氧化酶化学检测比较简便,但稳定性较差。本次研究中所选择的MDA、SOD和GSH-Px 3个指标,由于稳定性较差,所以标准差较大。与对照组相比 (图 2),DEHP低、中、高剂量染毒组MDA含量依次升高,但差异无统计学意义 (P > 0.05),SOD活力在DEHP高剂量染毒组下降,差异有统计学意义 (P < 0.05),GSH-Px活力在DEHP低、中剂量染毒组明显下降,且差异具有统计学意义 (P < 0.05)。
|
| 注:(A) MDA含量;(B) SOD活力;(C) GSH-Px活力;*与对照组相比P < 0.05 图 2 不同DEHP染毒剂量组SOD、GSH-Px活力以及MDA含量的变化 |
2.3 DEHP对GC-2 spd细胞凋亡的影响
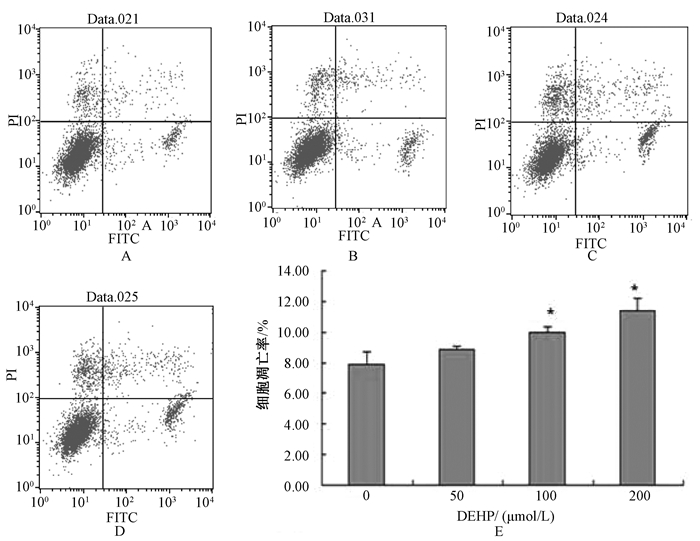
DEHP中、高剂量染毒组与对照组比较,细胞凋亡率明显升高,且差异有统计学意义 (P < 0.05;图 3)。
|
| 注:A、B、C和D分别代表DMSO,低、中、高剂量组;*与对照组比较P < 0.05 图 3 DEHP对GC-2 spd细胞凋亡的影响 |
3 讨论
近年来,DEHP作为环境内分泌干扰物对男 (雄) 性生殖系统的影响受到越来越多的关注。研究显示,DEHP具有抗雄性激素作用[7],可通过干扰机体的生殖内分泌功能而影响生殖细胞的分化、发育和成熟。Botelho等[8]研究报道,青春前期大鼠经口染毒DEHP后,出现睾丸重量下降,生精细胞凋亡和坏死,睾丸萎缩,血清中睾酮水平下降,阴茎包皮分离延迟。
细胞凋亡是为维持内环境稳定,由基因控制的细胞自主的有序死亡。凋亡在正常的精子发生中起着重要作用,75%的生精细胞通过自发性的凋亡而死亡,以维持正常的精子生成和精子质量[9]。但是当内源性和外源性的有害因素破坏这种程序化的细胞凋亡时,就会引起生精细胞过早、过多的凋亡,严重时引起成熟精子数量减少,甚至不育[10]。研究表明,诱导生精细胞凋亡是环境内分泌干扰物引起生殖毒性的主要原因之一,双酚A、己烯雌酚 (DES) 均能诱发生精细胞凋亡,导致生精障碍[3, 11]。本研究中显示,DEHP可导致GC-2 spd细胞凋亡率增加,且随着DEHP染毒剂量的增大而明显升高。
外源性有机物进入机体,体内高活性分子如活性氧自由基 (reactive oxygen species,ROS) 和活性氮自由基 (reactive nitrogen species,RNS) 产生过多,这些强氧化性物质的氧化程度超出氧化物的清除时,就会导致氧化系统和抗氧化系统失衡,进而引起组织损伤。超氧化物歧化酶 (SOD) 和GSH-Px都是重要的抗氧化酶,SOD能够催化超氧化物通过歧化反应转化为氧气和过氧化氢,GSH-Px能催化还原性谷胱甘肽 (GSH) 对过氧化氢和过氧化脂质的还原,进而消除氧化自由基的损伤[12],因此SOD和GSH-Px活力的强弱可以间接反映机体抗氧化能力的大小。MDA是细胞膜上的多聚不饱和脂肪酸发生过氧化反应时的氧化代谢产物之一[13],可间接反映氧化自由基的水平和细胞氧化损伤的程度。Kasahara等[6]对Wistar大鼠进行口服染毒后发现,DEHP会引起睾丸细胞活性氧产生增多。Erkekoglu等[14]进行的体外试验报道,DEHP暴露导致小鼠间质肿瘤细胞的ROS产生增多,抗氧化剂谷胱甘肽过氧化酶1(GPx1) 和还原性谷胱甘肽 (GSH) 水平下降。本次研究发现,DEHP染毒GC-2 spd细胞后,可导致细胞内MDA含量升高,SOD和GSH-Px两种酶活力下降,说明DEHP会引起男 (雄) 性生殖细胞内氧化—抗氧化系统失衡。研究表明,氧化—抗氧化系统的失衡会启动和加速细胞凋亡[5]。因此DEHP诱发男 (雄) 性生殖细胞氧化自由基产生增多,抗氧化酶活力下降,导致应激反应发生,进而诱发凋亡是DEHP诱导生精细胞毒性可能的机制之一,但确切的机制和信号通路还有待进一步研究。
4 结论DEHP通过诱发小鼠生精细胞氧化应激而诱导细胞凋亡是DEHP发挥男 (雄) 性生殖系统毒性的机制之一。
致谢:南京医科大学对课题组馈赠细胞。
| [1] | Lin CH, Chen TJ, Chen SS, et al. Activation of Trim17 by PPAR is involved in di (2-ethylhexyl) phthalate (DEHP)-induced apoptosis on neuro-2a cells[J]. Toxicol Letters, 2011, 206(3): 245–251. doi: 10.1016/j.toxlet.2011.08.002 |
| [2] | 吴维光, 史海霞, 韩建秋, 等. 邻苯二甲酸二乙基己酯在体外对大鼠卵巢颗粒细胞凋亡Caspase通路的影响[J]. 环境卫生学杂志, 2012, 2(4): 149–152. |
| [3] | Wang P, Luo CH, Li QY, et al. Mitochondrion-mediated apoptosis is involved inreproductive damage caused by BPA in male rats[J]. Environ Toxicicol and Pharmacology, 2014, 38(3): 1025–1033. doi: 10.1016/j.etap.2014.10.018 |
| [4] | Rao AV, Shaha C. Role of glutathione s-transferases in oxidative stress-induced male germ cell apoptosis[J]. Free Radical Biology & Medicine, 2000, 29(10): 1015–1027. |
| [5] | 王晓静, 易静. 氧化应激相关的细胞凋亡过程中基因表达改变[J]. 国外医学肿瘤学分册, 2004, 31(1): 10–14. |
| [6] | Kasaharak E, Sato EF, Miyoshi M, et al. Role of oxidative stress in germ cell apoptosis induced by di (2-ethylhexyl) phthalate[J]. Biochemical Society, 2002, 365(Pt3): 849–856. |
| [7] | Barlow, N J, Foster PM. Pathogenesis of male reproductive tract lesions from gestation through adulthood following in utero exposure to Di (n-butyl) phthalate[J]. Toxicol Pathol, 2003, 31(4): 397–410. |
| [8] | Botelho GG, Golin M, Bufalo AC, et al. Reproductive effects of di (2-ethylhexyl) phthalate in immature male rats and its relation to cholesterol, testosterone, and thyroxin levels[J]. Arch Environ Contam Toxicol, 2009, 57(4): 777–784. doi: 10.1007/s00244-009-9317-8 |
| [9] | Allan DJ, Harmon BV, Roberts SA. Spermatogonial apoptosis has three morphologically recognizable phases and shows no circadian rhythm during normal spermatogenesis in the rat[J]. Cell Prolif, 1992, 25(3): 241–250. doi: 10.1111/j.1365-2184.1992.tb01399.x |
| [10] | Lee J, Richburg JH, Shipp EB, et al. The fas system, a regulator of testicular germ cell apoptosis, is differentially up regulated in sertoli cell versus germ cell injury of the testis[J]. Endocrinology, 1999, 140(2): 852–858. doi: 10.1210/endo.140.2.6479 |
| [11] | 杨筱珍, 陈耀星, 王子旭. 己烯雌酚对成年仓鼠睾丸生精的影响[J]. 中国农业科学, 2005, 38(11): 2339–2343. doi: 10.3321/j.issn:0578-1752.2005.11.027 |
| [12] | Agarwal A, Makker K, Sharma R. Clinical relevance of oxidative stress in male factor infertility:an update[J]. Am J Reprod Immunol, 2008, 59(1): 2–11. |
| [13] | 吴维光, 史海霞, 韩建秋, 等. DEHP体外对大鼠睾丸支持细胞Bax和Bcl-2基因表达的影响[J]. 贵阳中医学院学报, 2013, 35(1): 261–264. |
| [14] | Erkekoglu P, Rachidi W, Yuzugullu OG, et al. Evaluation of cytotoxicity and oxidative DNA damaging effects of di (2-ethylhexyl)-phthalate (DEHP) and mono (2-ethylhexyl)-phthalate (MEHP) on MA-10 Leydig cells and protection by selenium[J]. Toxicol and Applied Pharmacology, 2010, 248(1): 52–62. doi: 10.1016/j.taap.2010.07.016 |



