2. 内蒙古巴彦淖尔市疾病预防控制中心
随着稀土钕需求量的不断扩大,其生产规模迅速发展,接触稀土钕的职业人群越来越多。稀土开采、生产加工以及应用等各个环节中,都可能存在作业人员的稀土暴露,长期暴露于稀土粉尘的工人有患尘肺病的风险[1]。稀土氧化钕粉尘通过呼吸道吸入的方式进入人体肺部,并对人体造成危害,主要是由于粉尘在肺内沉积导致肺组织发生炎症和纤维化[2-3]。近些年,随着分子生物学实验技术的发展及改进,逐渐发现较多细胞因子、炎症介质及多种细胞与肺组织炎症及纤维化的发生发展有关。白介素-12(IL-12) 通过复杂的细胞因子信号通路介导免疫应答及炎症反应,对肺组织早期炎症及肺纤维化的形成具有重要意义[4]。同时大量研究结果证实IL-12在肺纤维化发生发展中起着关键作用[5-6]。本研究采用非暴露气管灌注的方式,灌注一定量的稀土氧化钕粉尘建立大鼠暴露模型,通过分析暴露于稀土氧化钕粉尘大鼠肺组织中Ⅰ型和Ⅲ型胶原纤维含量、BALF上清液中IL-12含量的变化及染尘大鼠早期肺组织的病理变化,从整体水平上探讨暴露于稀土氧化钕粉尘对大鼠的影响以及IL-12在肺组织纤维化发展早期的作用,为深入研究稀土氧化钕粉尘致肺组织纤维化的机制提供理论依据。
1 实验材料 1.1 实验动物及饲养125只SPF级健康成年SD雄性大鼠,体重(220±16) g,购买于中国食品药品鉴定所,实验动物质量合格证明书编号:scxk(京)2011-0012。适应性饲养1周染毒,大鼠饲料购买于中国食品药品鉴定所。实验室环境:温度20℃~26℃,相对湿度40%~70%,空气压力梯度维持25 Pa。每周进行1次彻底性消毒,每天采用喷雾消毒1次。进入实验室的所有物品全部进行消毒处理。饲养期间实验大鼠全部正常饮食、饮水,且无意外伤害及死亡。
1.2 试剂及仪器 1.2.1 试剂稀土氧化钕(Nd2O3),购于包头市瑞鑫稀土冶炼厂,(经包头市稀土研究院火法实验室检测,D50=0.11 μm,粒径 < 0.29 μm占97%,纯度为99%),无放射性;甲醛(天津市风船化学试剂科技有限公司),苏木精,伊红,二甲苯,天狼猩红,苦味酸,树胶,戊巴比妥钠,无水乙醇(分析纯,天津市开通化学试剂有限公司);磷酸盐缓冲液(PBS),0.9%生理盐水;ELISA试剂盒(南京建成生物工程研究所)。
1.2.2 仪器切片机(M3500英国Bright),偏振光显微镜(Nikon E600POL日本),TDZ4-WS低速台式离心机(长沙湘仪离心机仪器有限公司),微量加样器(德国Eppendorf公司);LDZM-SOKCS立式压力蒸汽灭菌器(上海申安医疗器械厂);DW-HL388超低温冰箱(-86℃, 中科美菱低温科技有限责任公司);电子天平(AR224CN,CP3102,奥豪斯仪器上海有限公司);酶标仪(伯乐550型酶标仪,美国)。
2 实验方法 2.1 实验动物分组及动物模型的制备125只SPF级健康成年SD雄性大鼠,按体重随机分为染尘组和对照组,染尘组分为5个时间点,分别为染毒后第3、7、14、21和28 d,染尘组中每组15只大鼠,且每个时间点设置1个对照,对照组每组10只大鼠,大鼠按50 mg/mL剂量进行染尘。
2.2 大鼠染尘Nd2O3(D50=0.11 μm,粒径 < 0.29 μm占97%,纯度为99%),用生理盐水配制成50 mg/mL的Nd2O3悬液,经高压灭菌后备用。将实验大鼠用戊巴比妥钠轻度麻醉,将Nd2O3悬液0.8 mL采用非气管暴露的方式通过气管注入肺部,对照组大鼠采用同种方法注入等体积0.9%生理盐水。
2.3 支气管肺泡灌洗液(BALF)的收集染毒大鼠第3、7、14、21和28 d,采用腹主动脉放血的方法处死,然后切开颈部皮肤暴露气管,经口将7号腰穿针插入气管,细线固定,在无菌条件下共用6 mL无菌0.9%生理盐水进行支气管肺泡灌洗,分3次注入,每次用注射器抽取2 mL、37℃无菌0.9%生理盐水,反复灌洗3次,共收集灌洗液约5 mL,4℃ 1 500 r/min离心15 min(离心机离心半径12.3 cm),吸取上清液,1.5 mL EP管分装标记,-86℃冻存待测。
2.4 BALF上清液中IL-12含量的测定ELISA试剂盒测定BALF上清液中IL-12的含量。按试剂盒说明进行相应操作,终止反应后用酶标仪进行读数,记录结果。
2.5 肺组织的病理学观察灌洗完毕后, 采用钝性剥离的方法将连接于肺脏的气管、支气管结缔组织及心脏剔除,并将肺脏浸于0.9%生理盐水中漂洗1次,滤纸吸干水分,记录肉眼病理变化。然后将整个肺组织用10 %中性缓冲福尔马林液浸泡固定,石蜡包埋,切片厚度为5 μm。HE染色后,普通光镜下观察肺组织的病理学变化。
2.6 肺组织天狼猩红染色及胶原纤维含量检测切片后,于恒温干燥箱(63℃)中干燥13 min;分别将烘干后的肺组织切片浸泡于85%、90%和95%乙醇中,各脱水1 min;苏木精重度复染20 min,自来水冲洗返蓝10 min;在0.1%苦味酸—天狼猩红染色液中染色1 h,酸化水洗2次,无水乙醇浸泡3次,二甲苯透明2次;中性树胶封片。染色完成后使用偏振光显微镜观察,并采用Image-Pro Plus Version 4.5 for Windows TM图象分析系统对染色的肺组织切片进行分析,采用颜色分割法将胶原纤维从背景色中分离出来。
2.7 统计学处理分析采用Excel建立数据库,运用SPSS 17.0统计软件对数据进行分析。所有数据均采用(x±s)表示,多组间均数比较采用单因素方差分析对数据进行分析,两两比较采用LSD检验,以α=0.05为检验水准。用双变量相关分析计算Pearson相关系数,检验水准α=0.05,P < 0.05为差异有统计学意义。
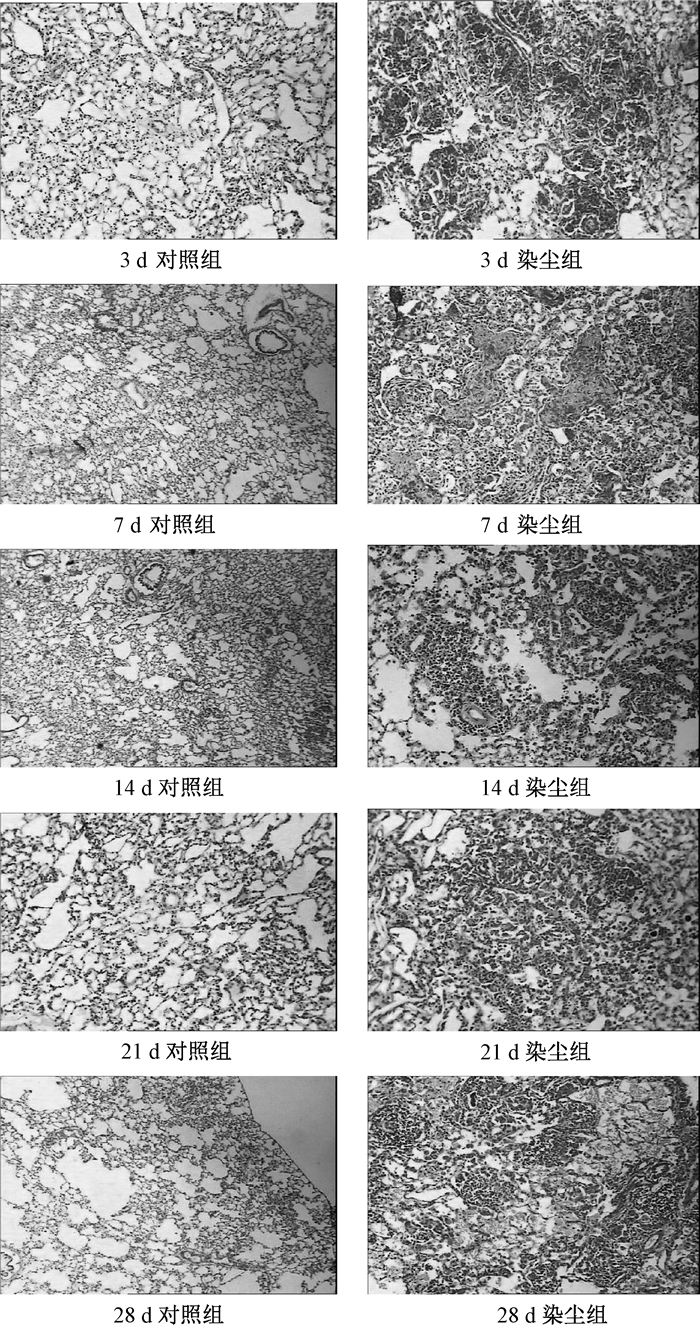
3 结果 3.1 不同时间点大鼠肺组织病理学观察本研究结果显示,对照组与染尘组相比较,各个时间点大鼠肺组织结构基本正常,仅存在轻微的炎症反应,未出现明显病变。第3 d时,染尘组大鼠肺组织开始出现充血,伴有浆液性蛋白渗出,巨噬细胞在肺泡腔内聚集,同时出现中性粒细胞浸润;第7 d时,染尘组大鼠出现肺泡间隔增宽增厚并伴有明显水肿,并有较多淋巴细胞及巨噬细胞浸润。局部肺泡腔内出现小肉芽肿弥漫,部分小肉芽肿融合成较大的肉芽肿,肉芽肿内出现成纤维细胞增生、玻璃样改变以及胶原纤维形成,使得病灶内肺泡腔变小;第14 d时,染尘组大鼠肺泡壁增厚,肺泡间隔进一步增宽增厚,肺泡隔内仍存在少数的中性粒细胞、以及较多的巨噬细胞和淋巴细胞侵润,并伴有成纤维细胞增生,肉芽肿内出现进行性纤维化可见胶原纤维聚集,造成部分肺泡结构破坏;第21 d时,染尘组大鼠肺泡间隔断裂现象严重,肉芽肿内出现大面积纤维化,肺泡结构遭到较严重破坏,淋巴细胞成为主要的炎性细胞;第28 d时,染尘组大鼠肺泡壁明显增厚,大部分肺泡结构遭到严重破坏,由于胶原纤维及成纤维细胞的占据,造成部分肺泡腔消失,同时肺组织出现广泛纤维化(图 1)。
|
| 图 1 不同时间点肺组织HE染色观察结果(HE×100) |
3.2 不同时间点大鼠肺组织中Ⅰ、Ⅲ型胶原纤维天狼猩红染色镜下形态
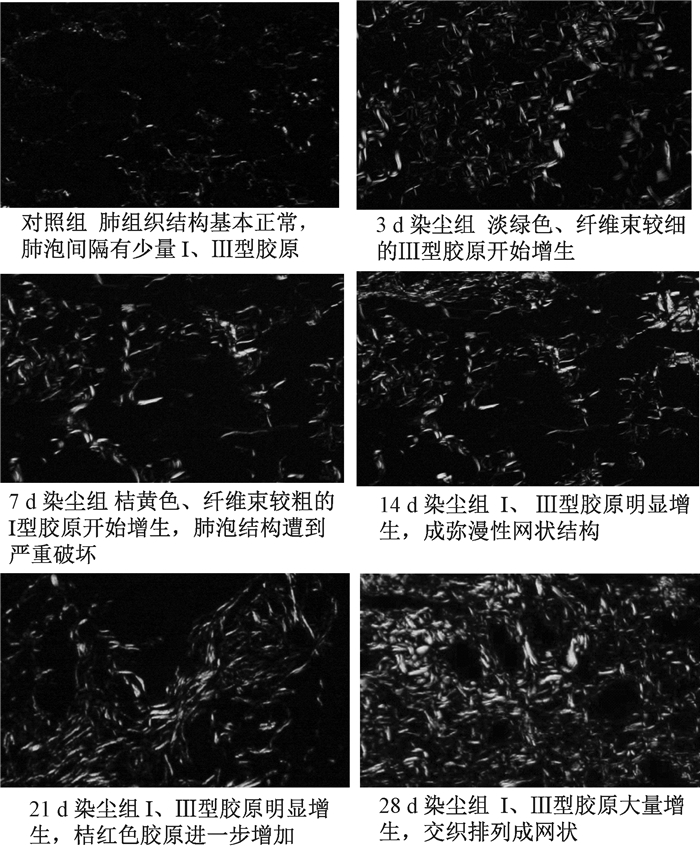
各个时间点大鼠肺泡结构基本正常,肺泡间隔仅有少量Ⅰ、Ⅲ型胶原纤维。染尘组第3 d时,肺泡结构轮廓模糊,肺泡间隔之外开始出现淡绿色、纤细且弯曲的Ⅲ型胶原纤维,呈现网织绳索状结构。第7 d时,正常肺泡结构遭到严重破坏,取而代之的则是两型相互交织存在的胶原纤维:一种较细,为Ⅲ型胶原纤维(呈淡绿色);另一种较粗,则为Ⅰ型胶原纤维,呈现桔黄、深红色。第14 d时,可见淡绿色且弯曲的胶原呈现网织状结构且弥漫性存在,其间夹杂少量粗大的桔黄色纤维。第21 d时,桔红色粗大的胶原纤维进一步增加,淡绿色纤细的胶原纤维则相对较少。第28d时,桔红色粗大的胶原纤维明显增多,淡绿色纤细的胶原纤维也大幅度增加,二者相互交错呈网织状结构存在,两型胶原纤维弥漫性分布于整个视野(图 2)。
|
| 图 2 不同时间点染尘大鼠肺组织天狼腥红染色结果(天狼腥红染色, ×200) |
3.3 不同时间点染尘大鼠肺组织中Ⅰ和Ⅲ型胶原面积百分比的改变
研究结果显示,染尘组大鼠肺组织Ⅰ型和Ⅲ型胶原纤维面积百分比随着暴露时间的延长呈现增加趋势(R值分别为0.979和0.745)。与对照组相比,染尘组大鼠肺组织中Ⅰ型和Ⅲ型胶原纤维表达增加,各时间点肺组织中Ⅰ、Ⅲ型胶原纤维面积百分比均高于对照组,经统计学检验,除第3 d外,其他差异均有统计学意义(P < 0.05;表 1)。
| 时间/d | Ⅰ型胶原面积比例的改变(1/103) | Ⅲ型胶原面积比例的改变(1/103) | |||
| 实验组(n=15) | 对照组(n=10) | 实验组(n=15) | 对照组(n=10) | ||
| 3 | 20.3±1.89 | 12.69±1.56 | 20.50±8.40 | 10.5±2.93 | |
| 7 | 24.5±1.38* | 14.40±2.88 | 25.60±5.64* | 11.21±1.97 | |
| 14 | 27.7±2.98* | 16.45±3.74 | 75.62±9.68** | 14.38±3.81 | |
| 21 | 32.7±5.37** | 14.20±2.58 | 50.97±2.69** | 13.41±3.78 | |
| 28 | 39.6±4.38** | 18.50±3.94 | 64.17±13.68** | 15.93±4.82 | |
| 注:经单因素方差分析LSD检验,与对照组比较,*P < 0.05,**P < 0.01 | |||||
3.4 大鼠BLAF上清液中IL-12含量变化
研究结果显示,稀土氧化钕粉尘暴露不同时间点,在第7 d时,IL-12含量低于对照组,其他实验组大鼠BALF上清中IL-12的含量均高于对照组,经统计学检验,差异有统计学意义(P < 0.05)。随着染毒时间的延长,BALF上清中IL-12的含量在第7 d时有短暂下降之后又呈现上升的趋势(表 2)。
| 时间/d | BALF中IL-12含量(pg/mL) | |
| 实验组(n=15) | 对照组(n=10) | |
| 3 | 1 138.53±233.99* | 1 059.99±197.17 |
| 7 | 1 103.76±267.20 | 1 111.53±202.84 |
| 14 | 1 290.89±262.33* | 1 169.21±154.93 |
| 21 | 1 299.58±293.38* | 1 186.69±158.06 |
| 28 | 1 339.16±214.98* | 1 236.08±229.88 |
| 注:经单因素方差分析LSD检验,与对照组比较,*P < 0.05 | ||
4 讨论
稀土氧化钕粉尘主要以呼吸道吸入的方式进入人体肺部,并对人体造成危害,主要是由于粉尘在肺内沉积导致肺组织发生炎症和纤维化;同时在肺组织发生损伤过程中,会引起肺内细胞因子表达增加以及胶原纤维的沉积[2-3]。粉尘进入肺泡内被巨噬细胞吞噬,使吞噬粉尘的巨噬细胞大量崩解死亡,释放出的粉尘又被其他巨噬细胞重新吞噬,如此反复形成恶性循环,并持续破坏肺组织[7]。同时,崩解死亡的巨噬细胞释放大量的细胞因子及巨噬细胞生长因子等,促进成纤维细胞生长和胶原形成[8]。在巨噬细胞吞噬作用及细胞病理性死亡的循环过程中始终存在炎症反应,而这种炎症反应在肺纤维化形成发展过程中起着重要的作用[9]。大量研究结果证明,在肺纤维化发生发展过程中,细胞因子发挥着重要作用[10-13]。本实验通过对染尘大鼠的肺组织进行病理学观察后证实,染尘早期肺组织以炎症反应为主,且实验大鼠的炎症反应程度随染尘时间的延长而呈现加重的趋势。胶原蛋白是构成细胞外基质的重要成分,同时也是稳定内环境及维持组织结构的重要因子。肺内沉积的胶原纤维成分为胶原蛋白,主要由Ⅰ型和Ⅲ型胶原构成。肺内Ⅰ型胶原纤维的含量最为丰富,主要分布于支气管树和血管树的周围,Ⅲ型胶原纤维主要见于肺泡间质内,是构成肺间质胶原纤维的主要成分。胶原纤维的沉积在肺纤维化发生进展过程中起着重要的作用[14]。研究显示,在肺纤维化发生发展过程中,不同时期肺组织中Ⅰ、Ⅲ型胶原纤维的含量存在不同变化[15]。本实验结果证实,染尘后大鼠肺组织内早期可见少量的Ⅰ型和Ⅲ型胶原纤维的出现,表明稀土粉尘可增加大鼠肺组织Ⅰ型和Ⅲ型胶原纤维合成。随着染尘时间的延长大鼠肺组织中Ⅰ型和Ⅲ型胶原纤维表现为含量逐渐增多且分布范围逐渐扩大。由此推断稀土氧化钕粉尘可能引起肺组织的纤维化,且随着染尘时间的延长纤维化程度更加明显。稀土氧化钕粉尘在引起肺组织纤维化过程中,不仅引起肺组织内Ⅰ型和Ⅲ型胶原纤维的含量发生变化,同时也引起BALF上清中IL-12的表达变化,二者共同反应肺纤维化过程。IL-12为多效性的细胞因子,在调节免疫应答过程中发挥着重要作用,同时具有抑制肺纤维化的作用。本实验发现大鼠BALF上清液中IL-12含量随着染尘时间的变化而变化,IL-12在第7 d时有短暂下降之后缓慢回升,可能是由于在肺损伤的早期首先出现炎症反应。受其他炎症因子的影响,未发挥生物学活性或作用不明显导致IL-12在7 d时出现下降的趋势。陈南芳等[16]相关研究证实大鼠气管暴露法染矽尘28 d,早期出现炎性细胞浸润,后期肺组织结构破坏严重,出现广泛纤维化。IL-12的含量随染尘时间的变化可以看出机体自我调节的过程,IL-12的分泌起到抗纤维化的作用[10]。一次性气管内灌注博莱霉素建立大鼠肺纤维化模型,该模型具有典型的从肺泡炎症到肺组织纤维化进行性发展的过程,给予IL-12干预,该过程被明显抑制,肺泡炎症及肺纤维化程度均减低,表明IL-12对博莱霉素所致的大鼠肺泡炎症及肺组织纤维化具有明显抑制作用[6]。博莱霉素诱导小鼠肺纤维化模型中,IL-12基因敲除的小鼠与对照组相比,肺内单核细胞浸润程度减轻但肺纤维化程度加重,提示IL-12能提高淋巴组织细胞的炎性反应,同时能够抑制肺纤维化的晚期发展[17]。Antoniou等[18]用IFN-γ-1b或秋水仙素治疗特发性肺纤维化时证实,治疗前后BALF上清液中IL-12水平无明显变化。因此推断检测IL-12可反映早期纤维化的趋势,同时为早期判断肺损伤出现及其恢复提供依据。
综上所述,通过呼吸道进入肺部的稀土氧化钕粉尘,可造成大鼠肺组织中Ⅰ型和Ⅲ型胶原纤维面积百分比的改变、肺组织病理变化及BALF上清液中IL-12含量的升高。这些变化彼此间及同肺纤维化之间的联系有待于进一步研究。
| [1] | 李智民, 张凯琳, 刘中韬. 农用稀土对喷施作业人员健康的影响[J]. 中国稀土学报, 2003, 21(5): 594–596. |
| [2] | 周效宝. 矽肺早期BALF中炎性因子变化规律的实验研究[D]. 济南大学, 2011. http://cdmd.cnki.com.cn/Article/CDMD-10427-1011159420.htm |
| [3] | 郑姗姗, 王素华, 王春虾, 等. 稀土氧化钕粉尘致大鼠肺纤维化过程中Ⅰ、Ⅲ型胶原及白介素-12表达的变化[J]. 职业与健康, 2014, 20: 2899–2901. |
| [4] | 喻婷, 夏永良. 肺纤维化中细胞因子作用机制的研究进展[J]. 河南中医学院学报, 2008, 3(23): 77-79–79. |
| [5] | 袁宝军, 丁秀荣, 刘志忠, 等. 矽肺患者血清白细胞介素-12和γ-干扰素水平变化[J]. 中国职业医学, 2006, 33(2): 111–113. |
| [6] | 罗玲. 白细胞介素-12对博莱霉素致大鼠肺纤维化的治疗作用[D]. 重庆医科大学, 2008. http://kns.cnki.net/KCMS/detail/detail.aspx?filename=zhjh200706024&dbname=CJFD&dbcode=CJFQ |
| [7] | 唐婷婷, 夏丹, 王璐, 等. 实验性矽肺大鼠肺泡灌洗液中巨噬细胞和白介素6的变化及意义[J]. 安徽医药, 2012, 07: 894–896. doi: 10.3969/j.issn.1009-6469.2012.07.008 |
| [8] | 胡永斌, 曾庆富. 矽肺纤维化细胞分子机制研究的进展[J]. 中华劳动卫生职业病杂志, 2003, 21(3): 210–221. |
| [9] | Barbarin V, Nihoul A, Misson P, et al. The role of pro-and anti-inflammatory responses in silica-induced lung fibrosis[J]. Respir Res, 2005, 6(1): 112. doi: 10.1186/1465-9921-6-112 |
| [10] | Ulker O, Yucesoy B, Demir O, et al. Serum and BAL cytokine and antioxidant enzyme levels at different stages of pneumoconiosis in coal workers[J]. Hum Exp Toxicol, 2008, 27(12): 871–877. doi: 10.1177/0960327108098332 |
| [11] | Prince P, Boulay Me, Pagé N, et al. Induced sputum markers of fibrosis and decline in pulmonary function in asbestosis and silicosis:a pilot study[J]. Int J Tuberc Lung Dis, 2008, 12(7): 813–819. |
| [12] | Cho WS, Choi M, Han BS, et al. Inflammatory mediators induced by intratracheal instillation of ultrafine amorphous silica particles[J]. Toxicol Lett, 2007, 175(1/2/3): 24–33. |
| [13] | Carlsten C, De Roos AJ, Kaufman JD, et al. Cell markers, cytokines, and immune parameters in cement mason apprentices[J]. Arthritis Rheum, 2007, 57(1): 147–153. doi: 10.1002/art.v57:1 |
| [14] | Rimal B, Greenberg AK, Rom WN, et al. Basic pathogenetic mechanisms in silicosis:current understanding[J]. Curt Opin Pulm Med, 2005, 11(2): 169–173. doi: 10.1097/01.mcp.0000152998.11335.24 |
| [15] | Lai CK, Wallace WD, Fishbein WC, et al. Histopathology of pulmonary fibrosis disorders[J]. Semin Respir Crit Care Med, 2006, 27(6): 613–622. doi: 10.1055/s-2006-957333 |
| [16] | 陈南芳, 何文彤, 高宏生, 等. 染尘大鼠Ⅰ和Ⅲ型胶原与相关细胞因子含量的变化关系[J]. 中国工业医学杂志, 2010, 23(2): 89-91–91. |
| [17] | Sakamoto H, Zhao LH, Jain F, et al. IL-12p40(-/-) mice treated with intratracheal bleomycin exhibit decreased pulmonary inflammation and increased fibrosis[J]. Exp Mol Pathol, 2002, 72(1): 1–9. doi: 10.1006/exmp.2001.2409 |
| [18] | Antoniou KM, Alexandrakis MG, Sfiridaki K. Th1 cytokine pattern (IL-12 and IL-18) in bronchoalveolar lavage fluid (BALF) before and after treatment with interferon gamma-1b (IFN-γ-1b) or colchi-cine in patient with idiopathic pulmonary fibrosis (IPF/UIP)[J]. Sarcoidosis Vasc Diffuse Lung Dis, 2004, 21(2): 105–110. |



