从20世纪70年代开始,溴代阻燃剂(BFRs)由于阻燃性好、热稳定性高以及性价比优异,被广泛应用于电子、塑料、建筑、纺织等材料与产品中。四溴双酚A(TBBPA)在所有的BFRs中产量最大、使用最广,占整个BFRs的60%左右 [1]。中国TBBPA产能在2007年已达到了1 800 t,并且生产和使用量还在逐年增加[2]。动物实验研究表明,TBBPA暴露能引起脂代谢异常[3]、诱导肝损伤[4]、影响内分泌干扰系统[5]和神经系统功能[6];大量体外研究也证实,TBBPA通过损伤线粒体对肝细胞具有毒性作用[7-8],通过抑制三碘甲状腺原氨酸与甲状腺运载蛋白的结合对甲状腺激素平衡产生影响[9],还会导致小脑颗粒细胞死亡并伴随细胞凋亡[10]。
细胞凋亡是机体正常生长发育及适应外界不利环境过程中一个积极主动的过程,具有广泛的生理和病理作用,大量细胞凋亡会导致机体功能或组织损伤。人肝癌细胞(HepG2细胞)是从人肝胚细胞瘤分离出的细胞株,本身具有完整的人类代谢活化Ⅰ相、Ⅱ相酶,并且酶活性较稳定,使目标化合物测试结果的准确性和可重复性较高;同时,该细胞株源于人体,可以减少从动物实验或动物源细胞株的测试结果向人外推的不确定性。目前,有关TBBPA致细胞凋亡的研究尚不多见,本研究拟利用HepG2细胞建立TBBPA染毒模型,研究TBBPA暴露后的HepG2细胞线粒体膜电位变化以及细胞凋亡情况,从而为探讨TBBPA的细胞毒性效应提供基础数据。
1 材料与方法 1.1 细胞株与主要试剂HepG2细胞株购至中国科学院细胞库;TBBPA购于梯希爱(上海)化成工业发展有限公司,纯度大于98%;线粒体膜电位检测试剂盒购于至江苏省碧云天生物技术研究所;双染色流式细胞检测试剂盒(AnnexinⅤ-FITC)购于北京宝赛生物技术有限公司。TBBPA高压灭菌后溶于二甲基亚砜(DMSO)配制成100 mmol/L母液,暴露时将母液溶于细胞培养液然后分别调至所需暴露浓度,DMSO最终浓度不超过0.1%。根据文献报道[11],DMSO浓度不超过0.1%,一般不会对细胞产生毒性,因此本研究仅设细胞培养液空白对照,不设DMSO溶剂对照处理组。
1.2 主要仪器MCO-15AC型CO2培养箱(日本Sanyo),MK3多功能酶标仪(美国Thermo),TH4-200荧光显微镜(日本Olympus),FACS420流式细胞分析仪(美国BD),3500型低温高速离心机(日本KUBOTA)。
1.3 细胞培养HepG2细胞培养于含l0%胎牛血清、100 U/mL青霉素和100 μg/mL链霉素的改良Eagle培养基(DMEM)中,CO2培养箱培养条件设置为5% CO2,37 ℃,饱和湿度。
1.4 细胞存活率测定及半数抑制率(IC50)计算采用MTS比色法测定细胞存活率。暴露前以1×104cells/孔的细胞密度接种到96孔板,每孔100 μL,培养24 h,以0、2.5、5、10、15、20、25、30、35和40 μmol/L的TBBPA作用24 h,每个浓度设4个重复样品。按要求加入MTS试剂,选择490 nm波长,在酶标仪上测定各孔吸光度(OD)值。细胞相对存活率计算公式为:
| $ 细胞相对存活率=\frac{O{{D}_{样品}}-O{{D}_{本底}}}{O{{D}_{对照}}-O{{D}_{本底}}}\times 100% $ | (1) |
以概率单位法[12]采用SPSS 11.5软件计算IC50(抑制率=100-细胞存活率)。首先拟合概率单位方程[13]:y=B x+A,其中:y为概率单位,x为TBBPA的处理浓度(μmol/L),B为回归系数,A为截距,则IC50即为y=0.50时的TBBPA浓度。
1.5 细胞线粒体膜电位检测碧云天线粒体膜电位检测试剂盒是一种以JC-1为荧光探针,快速检测细胞线粒体膜电位变化的试剂盒。暴露前以2×105 cells/孔的细胞密度接种到24孔板,每孔400 μL,培养24 h,以终浓度为0、10、20和30 μmol/L的TBBPA作用24 h,每个处理组设4个重复;按试剂盒说明书加入JC-1染色工作液,采用多功能酶标仪,以激发光485 nm,发射光535 nm检测绿光,以激发光530 nm,发射光600 nm检测JC-1红光,通过以下公式计算线粒体膜电位变化:
| $ \begin{array}{c} \frac{{JC - {1_{聚合物}}}}{{JC - {1_{单体}}}}\left( {\% \;\;{\rm{对照}}} \right) = \\ \frac{{\left( {样品红光强度/样品绿光强度} \right)}}{{\left( {对照红光强度/对照绿光强度} \right)}} \times 100\% \end{array} $ | (2) |
式中:JC-1聚合物-线粒体膜电位较高时,JC-1探针形成聚合物,产生的红色荧光强度;JC-1单体-线粒体膜电位较低时,JC-1探针为单体,产生的绿色荧光强度。
1.6 细胞凋亡检测以标记了FITC的AnnexinⅤ作为荧光探针,并与PI匹配使用,利用流式细胞仪可分别检测早期凋亡细胞、晚期凋亡细胞以及死细胞。暴露前以8×105cells/孔的细胞密度接种到6孔板,每孔1.5 mL,培养24 h,以终浓度为0、10、20和30 μmol/L的TBBPA作用24 h;用胰酶消化细胞,4 ℃,2000 rpm离心10 min,弃上清,加1 mL磷酸盐缓冲液(PBS)清洗细胞,离心弃上清,并重复上述步骤;然后加入10 μL AnnexinⅤ-FITC混匀并避光反应15 min,加入300 μL Binding Buffer以及5 μL PI,采用FACS 420流式细胞仪进行检测。
1.7 统计分析以均数±标准差(x±SD)表示所有实验数据,采用GraphPad Prism 5软件进行绘图;并进行单因素方差分析(One way ANOVA),如P < 0.05被认为具有显著差异,如P < 0.01被认为具有极显著差异。
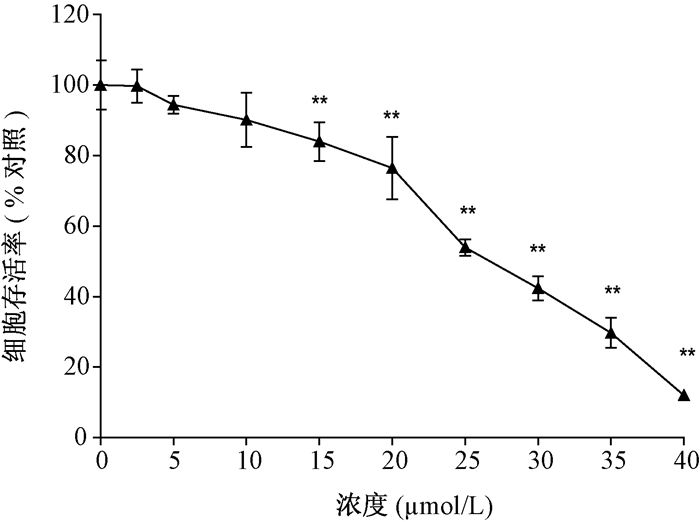
2 结果 2.1 TBBPA暴露影响HepG2细胞存活率以0、2.5、5、10、15、20、25、30、35和40 μmol/L的TBBPA处理HepG2细胞24 h,用MTS法检测细胞存活率,结果显示(图 1)HepG2细胞存活率随着TBBPA暴露浓度升高相应降低,其中15、20、25、30、35和40 μmol/L的TBBPA处理后HepG2细胞存活率与对照组相比具有极显著性差异(P < 0.01)。采用SPSS 11.5软件拟合的概率单位方程为y=0.08327x-2.26971(χ2=7.918,P=0.340),则TBBPA处理24 h HepG2细胞的IC50为27.26 μmol/L。
|
| 注:与对照组相比,*P < 0.05,**P < 0.01(x±SD,n=4) 图 1 TBBPA暴露24 h对HepG2细胞存活率的影响 |
2.2 TBBPA暴露影响HepG2细胞线粒体膜电位
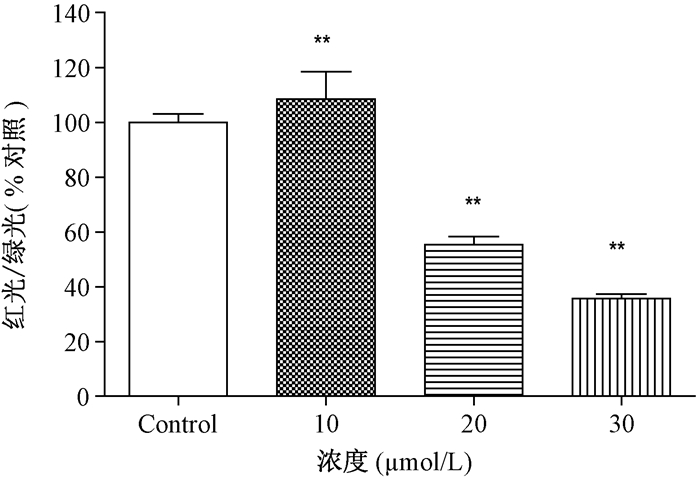
由图 2可以看出,与对照组相比,TBBPA暴露24 h后,20和30 μmol/L TBBPA处理组细胞JC-1聚合物/JC-1单体的值显著降低(P < 0.01)。
|
| 注:**与对照组相比,P < 0.01 (x±SD),n=3 图 2 TBBPA暴露24 h对HepG2细胞线粒体膜电位的影响 |
2.3 TBBPA暴露诱导HepG2细胞凋亡
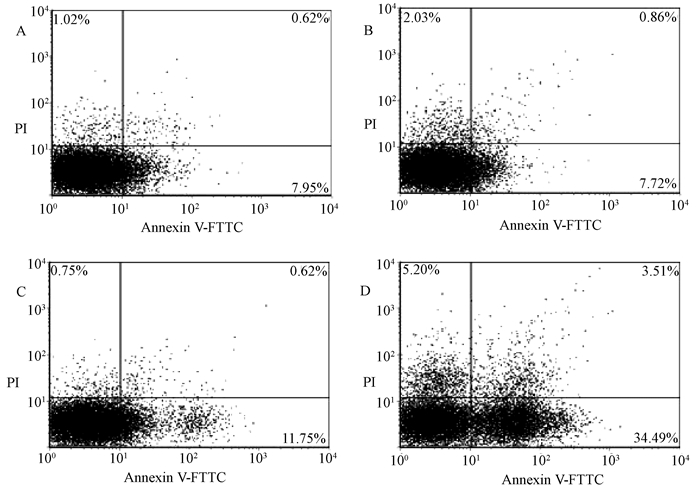
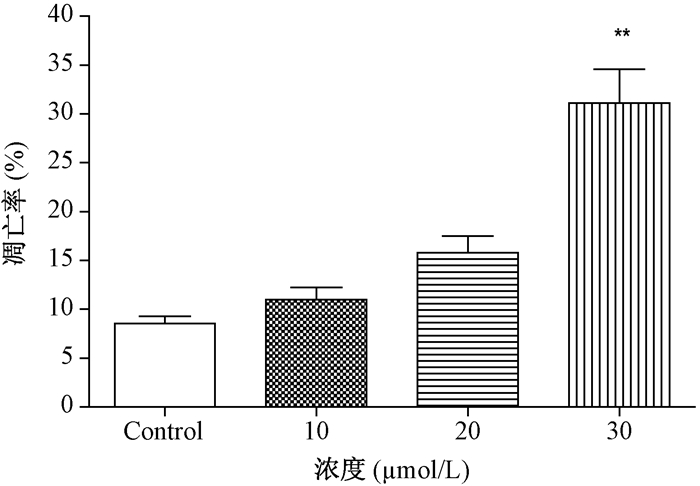
采用AnnexinⅤ与PI匹配染色作为荧光探针,通过流式细胞仪分析可以将位于第一象限的正常细胞、位于第二象限的凋亡早期细胞、位于第三象限的凋亡晚期细胞以及位于第四象限的坏死细胞进行区分。由图 3,图 4可以看出,随TBBPA暴露浓度升高,HepG2凋亡细胞(早期+晚期)有增加趋势,其中30 μmol/L TBBPA暴露组与对照组相比差异显著(P < 0.01)。
|
| A:Control;B:10 μmol/L TBBPA;C:20 μmol/L TBBPA;D:30 μmol/L TBBPA 图 3 流式细胞仪检测TBBPA暴露24 h诱导HepG2细胞凋亡 |
|
| 注:与对照组相比,**P < 0.01 (x±SD,n=3) 图 4 不同浓度TBBPA暴露24 h后HepG2细胞凋亡率 |
3 讨论
细胞死亡存在三种形式:坏死、凋亡和自噬。其中细胞凋亡是细胞的程序性死亡,是由基因控制的,是机体清除损伤的一种自我保护行为,机体大量的细胞凋亡会导致功能和组织损伤。凋亡细胞具有细胞膜完整、胞质浓缩、胞核皱缩、核碎裂等特征。诱导细胞凋亡的因素有细胞毒素、氧化应激、放射性以及有毒有害物质等。
大量研究表明,许多化学污染物如多溴联苯醚(PBDEs)、二噁英、多氯联苯(PCBs)都能诱导细胞凋亡[14]。如2, 2’, 4, 4’-四溴联苯醚(PBDE-47) 可通过引起线粒体膜通透性转运孔开放和细胞色素C的释放介导人神经母细胞瘤(SH-SY5Y)细胞凋亡,从而对SH-SY5Y细胞产生损伤[15];PBDE-47还可诱导大鼠胰岛细胞瘤细胞(INS-1) 细胞凋亡,氧化应激和线粒体信号通路可能参与PBDE-47对INS-1细胞的毒性作用[16];PCB153对胚胎发育具有明显影响且呈剂量—效应关系,且随PCB153浓度增加,凋亡细胞比值上升,表明PCB153能诱导胚胎细胞凋亡,可能是PCB153的致畸作用机制之一[17]。但有关TBBPA诱导细胞凋亡的文献尚不多见,本研究以标记了FITC的AnnexinⅤ作为荧光探针采用流式细胞仪检测细胞凋亡的发生,结果显示20和30 μmol/L TBBPA暴露组HepG2细胞凋亡率有增加的趋势,30 μmol/L TBBPA暴露组与对照组相比差异明显,该结果表明TBBPA能诱导HepG2细胞凋亡产生。
线粒体是有关细胞呼吸、氧的代谢、酶活性和能量供应的重要细胞器。线粒体功能与线粒体跨膜电位差有关,当细胞线粒体跨膜电位下降时,会导致线粒体形态和功能的改变[18]。线粒体对细胞凋亡过程也具有重要的调控作用,有研究表明线粒体膜电位是反映线粒体内膜通透性的重要指标之一[15],线粒体膜电位下降主要是由于其通透性转运孔道,即线粒体膜通透性转运孔开放所致。另外也有研究证实:线粒体膜电位下降是细胞凋亡的早期特征之一[19]。本研究采用JC-1荧光探针检测HepG2细胞线粒体膜电位变化,结果显示与对照组相比,细胞线粒体膜电位随TTBPA暴露浓度的升高显著下降。这是细胞早期凋亡的标志,同时该结果也表明TBBPA可能通过降低线粒体膜电位引起细胞凋亡,从而产生细胞毒性,但具体机制有待进一步深入研究。
4 结论本研究显示,随TBBPA处理浓度增加,HepG2细胞存活率相应降低,线粒体膜电位下降,细胞凋亡率增加。研究结果表明TBBPA可能通过降低线粒体膜电位引起细胞凋亡,从而产生细胞毒性。
| [1] | Hakk H. A Survey of Tetrabromobisphenol A[A]. Second International Workshop on Brominated Flame Retardants, BFR2001. Stockholm University, Sweden, 2001. http://www.nrcresearchpress.com/doi/abs/10.1139/a11-010 |
| [2] | 施致雄. 食品中六溴环十二烷和四溴双酚A的检测技术与暴露评估[D]. 北京: 中国疾病预防控制中心营养与食品安全所, 2009. http://www.cnki.com.cn/Article/CJFDTotal-SPAJ201504046.htm |
| [3] | Tada Y, Fujitani T, Yano N, et al. Effects of tetrabromobisphenol A, brominated flame retardant, in ICR mice after prenatal and postnatal exposure[J]. Food and Chemical Toxicology, 2006, 44(8): 1408–1413. doi: 10.1016/j.fct.2006.03.006 |
| [4] | Tada Y, Fujitani T, Ogata A, et al. Flame retardant tetrabromobisphenol A induced hepatic Changes in ICR mice[J]. Environmental Toxicology and Pharmacology, 2007, 23(2): 174–178. doi: 10.1016/j.etap.2006.08.007 |
| [5] | Van der Ven L, Van de Kuil T, Verhoef A, et al. Endocrine effects of tetrabromobisphenol-A (TBBPA) in Wistar rats as tested in a one-generation reproduction study and a subacute toxicity study[J]. Toxicology, 2008, 245(1-2): 76–89. doi: 10.1016/j.tox.2007.12.009 |
| [6] | Lilienthal H, Verwer CM, van der Ven L, et al. Exposure to tetrabromobisphenol A (TBBPA) in Wistar rats:Neurobehavioral effects in offspring from a one-generation reproduction study[J]. Toxicology, 2008, 246(1): 45–54. doi: 10.1016/j.tox.2008.01.007 |
| [7] | Boecker RH, Schwind B, Kraus V, et al. Cellular disturbances by various brominated flame retardants[C]. Presented at the second international workshop on brominated flame retardants in Stockholm, Abstract 2001, Part 3:Effects and metabolism, 138-139. http://www.sciencedirect.com/science/article/pii/B9780444538086000032 |
| [8] | Nakagawa Y, Suzuki T, Ishii H, et al. Biotransformation and cytotoxicity of a brominated flame retardant, tetrabromobisphenol A, and its analogues in rat hepatocytes[J]. Xenobiotica, 2007, 37(7): 693–708. doi: 10.1080/00498250701397697 |
| [9] | Kitamura S, Jinno N, Ohta S, et al. Thyroid hormonal activity of the flame retardants tetrabromobisphenol A and tetrachlorobisphenol A[J]. Biochemical and Biophysical Research Communications, 2002, 293(1): 554–559. doi: 10.1016/S0006-291X(02)00262-0 |
| [10] | Reistad T, Mariussen E, Ring A, et al. In vitro toxicity of tetrabromobisphenol-A on cerebellar granule cells:cell death, free radical formation, calcium influx and extracellular glutamate[J]. Toxicological Sciences, 2007, 96(2): 268–278. |
| [11] | Tagliaferri S, Caglieri A, Goldoni M, et al. Low concentrations of the brominated flame retardants BDE-47 and BDE-99 induce synergistic oxidative stress-mediated neurotoxicity in human neuroblastoma cells[J]. Toxicology in Vitro, 2010, 24(1): 116–122. doi: 10.1016/j.tiv.2009.08.020 |
| [12] | 梁永钜, 符立梧. MTS法细胞毒试验的非线性关系研究[J]. 中国药理学通报, 2004, 20(6): 623–627. |
| [13] | 周一平. 用SPSS软件计算新药的LD50[J]. 药学进展, 2003, 27(5): 314–316. |
| [14] | Franco R, Sánchez-Olea R, Reyes-Reyes EM, et al. Environmental toxicity, oxidative stress and apoptosis:Ménage ā Trois[J]. Mutation Research/Genetic Toxicology and Environmental Mutagenesis, 2009, 674(1-2): 3–22. doi: 10.1016/j.mrgentox.2008.11.012 |
| [15] | 吴雪, 义虎, 姜春阳, 等. PBDE-47对人神经母细胞瘤细胞凋亡和线粒体膜电位及细胞色素C蛋白表达的影响[J]. 环境与健康杂志, 2012, 29(8): 675–678. |
| [16] | 阮晓倩, 何平, 谢静, 等. PBDE-47对INS-1细胞氧化应激和凋亡影响[J]. 中国公共卫生, 2013, 29(4): 536–538. doi: 10.11847/zgggws2013-29-04-23 |
| [17] | 常青, 赵泽文, 李泽桂, 等. PCB153诱导小鼠胚胎细胞凋亡对胚胎生长发育的影响[J]. 第三军医大学学报, 2007, 29(19): 1838–1840. doi: 10.3321/j.issn:1000-5404.2007.19.003 |
| [18] | 代志军, 王西京, 薛茜, 等. 半枝莲含药血清对肝癌H22细胞凋亡及线粒体膜电位的影响[J]. 中西医结合学报, 2008, 6(8): 821–826. |
| [19] | Lucken-Ardjomande S, Matinou JC. Newcomers in the process of mitochondrial permeabilization[J]. Journal of Cell Science, 2005, 118(3): 473–483. doi: 10.1242/jcs.01654 |



