2. 河北石家庄中心医院
随着信息爆炸时代的来临,手机已成为人们必不可少的通讯工具,人们使用手机通话频率和时长逐渐增高。手机给人类带来方便的同时,手机辐射是否会给人们造成健康危害一直备受关注。近来电离辐射对于雄性生殖系统不良影响的报道逐渐增多[1-4]。而手机辐射属于非电离辐射,是否对睾丸有不良影响,目前研究相对较少。睾丸是产生生殖细胞和雄性激素的场所,是雄性生殖器官,研究手机辐射对睾丸的影响有重要意义。Nrf2蛋白是细胞最重要的抗氧化应激蛋白,有报道称Nrf2蛋白的表达情况可以影响电磁辐射对机体的损伤程度。本实验模仿手机通话时的发射频率和平均功率密度(900 MHz,370 μW/cm2),通过观察其对睾丸组织形态和Nrf2蛋白表达的改变,探讨拟手机辐射对大鼠睾丸的影响,以期为手机辐射对雄性生殖损伤提供实验依据。
1 材料与方法 1.1 动物30只SPF级健康SD雄性大鼠,体重(230±20) g,由河北医科大学实验动物中心提供,动物合格证号SCXK(冀)2008-1003。
1.2 主要仪器、药物和试剂辐射装置[5]:实验所用辐射源由河北师范大学物理系专家采用精密度高的电子元件接稳压电源制作而成, 模拟手机常用发射频率900 MHz,平均功率密度370 μW/cm2,辐射源置自制辐射箱中央,辐射箱为一面开口的长78 cm,宽48 cm,高60 cm的长方体薄木箱,外包细铁丝网,箱盖包细铁丝网制成;辐射箱内四个方向分别置冰袋防止温度过高,辐射期间多次检测箱内各方向功率密度:辐射近中央为380 μW/cm2,鼠笼位置370 μW/cm2,最小值370 μW/cm2;暴露参数测定:北京龙震天科技发展有限公司生产的电磁辐射测定仪(型号:LZT-1150);徕卡RM2245切片机;流式细胞仪;Nrf2抗体及免疫组化试剂盒。
1.3 分组、辐射30只SPF级健康SD雄性大鼠正常饲养1周,以体重均衡为原则将其均分3组。正常组:每日将大鼠置辐射箱4 h但不辐射;12 d及30 d辐射组:将大鼠置于频率900 MHz,功率密度为370 μW/cm2 的辐射箱内,每日4 h,每次辐射完后正常饲养,分别辐射12 d,30 d。
1.4 标本的制备及测定正常组饲养2周后,12、30 d辐射组于辐射结束后次日以4%水合氯醛腹腔麻醉, 下腹部正中切开,分别取下两侧睾丸,置于4%多聚甲醛中固定,按常规步骤制成石蜡切片,行HE染色和Nrf2免疫组化染色,光学显微镜下观察。
1.5 统计学处理所有数据采用均数±标准差(x±s表示,两组之间比较采用t检验。睾丸组织免疫组化Nrf2蛋白表达采用HMIAS-2000高清晰度彩色医学图像分析系统,每组动物选择10张免疫组化切片,每张切片在放大400倍的显微镜下随机选5个视野观察分析Nrf2蛋白表达的平均光密度值,光密度值越大表达越强。应用SPSS 13.0统计软件进行统计处理,以P < 0.05为差异有统计学意义。
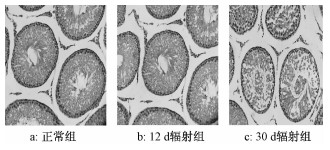
2 结果 2.1 3组大鼠睾丸组织形态比较光镜下正常组大鼠睾丸生精小管各级生精细胞排列整齐,层次清晰,管腔内充满成熟精子,12 d辐射组与正常组比较无明显变化。30 d辐射组生精小管内各级生精细胞层数减少,结构松散紊乱,有空洞形成(图 1)。
|
| 图 1 大鼠睾丸组织形态学变化(HE×100) |
2.2 3组大鼠睾丸组织Nrf2蛋白表达情况比较
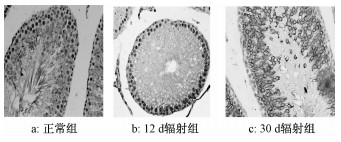
Nrf2蛋白表达部位呈棕黄色,表达越强其颜色越深。正常组大鼠睾丸Nrf2蛋白主要表达于精母细胞胞浆中,12 d辐射组大鼠Nrf2蛋白主要表达于精原细胞和精母细胞的细胞核中而其胞浆中呈弱表达,而且Nrf2蛋白表达平均光度值与正常组比较有显著差异(P < 0.05)。30 d辐射组Nrf2蛋白主要表达于精母细胞胞浆中(表 1,图 2)。
| 组别 | 精原细胞Nrf2蛋白表达平均光度值 | 精母细胞Nrf2蛋白表达平均光度值 |
| 正常组 | 0.29±0.07 | 0.34±0.06 |
| 12 d辐射组 | 1.61±0.77* | 1.75±0.76* |
| 30 d辐射组 | 0.18±0.02 | 0.44±0.07 |
| 注:*P < 0.05 | ||
|
| 图 2 大鼠睾丸细胞Nrf2蛋白的表达(×400) |
3 讨论
生活环境中电磁辐射现象普遍存在,通常将其分为电离辐射和非电离辐射。机体生命活动离不开生物电,这些生物电在器官和组织间形成稳定的微弱电磁场,一旦受到外界电磁干扰,机体电磁场平衡状态将遭到破坏,对人体造成损害。有报道称60 Coγ射线所产生的电离辐射可对小鼠多组织DNA完整性和抗氧化系统造成破坏[6]。Salama等[7]曾报道800 MHz手机频率辐射成年雄性家兔可影响其睾丸结构,使精子数量下降。微波长期辐射也可损伤雄性大鼠睾丸的生殖功能[8]。手机频率的电磁辐射是生活中普遍存在的非电离辐射,其对生殖的潜在影响不容忽视。目前手机工作频率在863~1 800 MHz,从拨号开始直到通话结束,在手机近场检测到的功率密度为300~800 μW/cm2,专业制作的模拟手机辐射装置,选用精密度高的电子元件,电路误差小,且外接稳压电源,保证了输出功率的稳定。辐射箱内置冰袋排除温度因素的影响,选用370 μW/cm2,900 MHz的辐射源模拟手机辐射,符合手机通话时的特点。本实验将观察900 MHz手机频率辐射对雄性大鼠睾丸影响,为手机频率的电磁辐射影响生殖提供实验基础。
通过大鼠睾丸组织石蜡切片-HE染色观察其形态学变化显示:正常组和12 d辐射组,睾丸生精小管排列整齐,生精细胞层次分明,结构紧凑,腔内精子丰富,30 d辐射组,睾丸生精小管空洞形成,生精细胞之间结构疏松,管腔内精子数量明显下降。这可能与12 d辐射组的电磁辐射诱发了大鼠的兴奋效应和适应性反应有关。30 d辐射组随着辐射天数增加辐射总剂量逐渐加大,睾丸组织病理变化逐渐显现,可能与手机辐射的累积效应有关[9]。
核转录因子E2相关因子2(Nrf2蛋白)是细胞最重要的抗氧化应激蛋白。Nrf2通过与胞浆蛋白Keleh样环氧氯丙烷相关蛋白-1(Keap1) 以及抗氧化反应元件ARE相互作用,诱导抗氧化蛋白和Ⅱ相解毒酶的基因表达,保持细胞内抗氧化还原环境的平衡从而发挥细胞保护作用[10]。正常生理条件下Nrf2通过Keap1与肌动蛋白结合,锚定在胞浆中并通过泛素介导的蛋白降解系统维持Nrf2的基础水平[11]。当细胞内氧化物质聚积时,Keapl感受到氧化—还原状态失衡,Nrf2与Keapl解偶联、转移到核内与解毒Ⅱ相酶的ARE结合从而编码一系列抗氧化还原酶和蛋白,如NAD(P)H、谷脱甘肽S一转移酶、谷脱甘肽等,氧化还原平衡恢复,Nrf2与ARE序列解离,输出到胞浆,泛素化后降解,维持低水平的Nrf2[12-13]。研究显示,Nrf2在多环境下(亲电物质、活性氧族、炎症)的多器官保护(肺脏、肝脏、肾脏)中起关键作用[14],Nrf2在高温对大鼠睾丸和精子形成造成的损伤中也有一定保护作用[15-17]。但电磁辐射所致大鼠睾丸损伤方面的Nrf2蛋白表达情况还未有报道。本实验中Nrf2蛋白免疫组化显示:正常组生精细胞胞浆为Nrf2蛋白主要表达部位,而细胞核无明显表达。12 d辐射组大鼠睾丸精原细胞和精母细胞细胞核出现明显表达,提示Nrf2蛋白表达出现核转位。30 d辐射组Nrf2蛋白表达主要在生精细胞胞浆。说明在辐射12 d时大鼠睾丸生殖细胞已经受到电磁辐射影响,导致生殖细胞内(尤其是精原细胞和精母细胞)氧化还原状态失衡,这种失衡使得胞浆中Nrf2-Keapl蛋白解离,Nrf2进入细胞核内启动编码一系列抗氧化还原酶和抗氧化蛋白,保护细胞免受氧化应激的损伤。30 d辐射组Nrf2蛋白表达情况与正常组无明显差异,说明持续的手机频率电磁辐射可能导致Nrf2的核定位信号和核输出序列之间的调节失衡,Nrf2不能产生核转位或Nrf2蛋白不稳定,泛素化降解加速,从而使细胞抗氧化能力减低[10]。这与睾丸组织HE染色结果相呼应:12 d辐射组由于Nrf2的核转位且高表达抗氧化还原酶和抗氧化蛋白,从而使生殖细胞的病理损伤轻微,而30 d辐射组Nrf2蛋白低,不能产生足够的抗氧化蛋白和酶类,因此细胞出现严重病理损伤。据报道,低剂量电离辐射(LDR)在一定时间范围(累积75 mGy)可有效增强糖尿病状态下Nrf2及其下游因子等抗氧化物质的表达,这可能是LDR对糖尿病小鼠肾脏起到一定保护作用的原因[17]。这与实验结果有相似之处。具体机制有待进一步研究。
本实验研究表明手机频率电磁辐射可对大鼠睾丸组织造成病理损伤,可能与影响睾丸组织Nrf2蛋白表达有关。
| [1] | 刘光伟, 董丽华, 王珍琦, 等. 低剂量电离辐射对小鼠睾丸生精细胞P53和Bcl-2蛋白表达的影响[J]. 吉林大学学报(医学版), 2004, 1(30): 85–88. |
| [2] | 工艳梅. X射线电离辐射对成年小鼠睾丸组织的损伤[J]. 中国组织工程研究与临床康复, 2009, 13(20): 3829–3832. doi: 10.3969/j.issn.1673-8225.2009.20.004 |
| [3] | Luo Q, Liu J, Yan J, et al. The effect of laminaria japonica polysaccharides on the recovery of the male rat reproductive system and mating function damaged by multiple mini-doses of ionizing radiations[J]. Environmental Toxicology and Pharmacology, 2011, 31(2): 286–294. doi: 10.1016/j.etap.2010.11.006 |
| [4] | Adaramoye OA, Adedara IA, Farombi EO. Possible ameliorative effects of kolaviron against reproductive toxicity in sub-lethally whole body gamma-irradiated rats[J]. Experimental and Toxicologic Pathology, 2012, 64(4): 379–385. doi: 10.1016/j.etp.2010.10.002 |
| [5] | 马惠荣, 栗晶晶, 赵亚楠, 等. 900MHz手机频率辐射损伤妊娠SD大鼠肝功能的实验研究[J]. 环境卫生学杂志, 2013, 3(5): 394–397. |
| [6] | 吴媚, 张遵真, 叶丛茂, 等. 60Coγ射线对小鼠组织细胞氧化损伤的研究[J]. 现代预防医学, 2005, 32(10): 1267–1269. |
| [7] | Salama N, Kishinoto T, Kanayama HO. Effects of exposure to a mobile phone on testicular function and structure in adult rabbit[J]. Int J Androl, 2010, 33(1): 88–94. doi: 10.1111/j.1365-2605.2008.00940.x |
| [8] | 陈浩宇, 王水明, 彭瑞云, 等. 微波长期辐射对雄性生殖的影响研究[J]. 中华男科学杂志, 2011, 17(3): 214–218. |
| [9] | 邢潇. 低剂量电离辐射对1型糖尿病小鼠肾脏保护作用及机制[D]. 吉林大学博士学位论文, 2013. http://cdmd.cnki.com.cn/Article/CDMD-10183-1013193736.htm |
| [10] | 李雪朋, 唐石, 许雪珠. 核转录因子Nrf2最新研究进展[J]. 中国组织上程研究, 2012, 16(24): 4530–4534. |
| [11] | 林晓萍, 李雯, 沈华浩. 抗氧化应激转录因子一Nrf2的研究进展[J]. 中国病理生理学杂志, 2011, 27(6): 1234–1239. |
| [12] | Klaassen CD, Reisman SA. Nrf2 the resue:effects of the antioxidative/eletrophilic response on the liver[J]. Toxicology and Applied Pharmacology, 2010, 244(1): 57–65. doi: 10.1016/j.taap.2010.01.013 |
| [13] | Maher J, Yamamoto M. The rise of antioxidant signaling-the evolution and hormetic actions of Nrf2[J]. Toxicology and Applied Pharmacology, 2010, 244(1): 4–15. doi: 10.1016/j.taap.2010.01.011 |
| [14] | Lee JM, Li J, Johnson DA, et al. Nrf2, a multi-organ protector[J]. FASEB J, 2005, 19(9): 1061–1066. doi: 10.1096/fj.04-2591hyp |
| [15] | Nakamura BN, Lawson G, Chan JY, et al. Knockout of the transcription factor NRF2 disrupts spermatogenesis in an age-dependent manner[J]. Free Radical Biology and Medicine, 2010, 49(9): 1368–1379. doi: 10.1016/j.freeradbiomed.2010.07.019 |
| [16] | Li Y, Huang Y, Piao Y, et al. Protective effects of nuclear factor erythroid 2-related factor 2 on whole body heat stress-induced oxidative damage in the mouse testis[J/OL]. Reproductive Biology and Endocrinology, 2013, 11.23. https://www.researchgate.net/publication/236066148_Protective_effects_of_nuclear_factor_erythroid_2-related_factor_2_on_whole_body_heat_stress-induced_oxidative_damage_in_the_mouse_testis |
| [17] | 孙景娟. 低剂量辐射对人肺上皮细胞和肺癌细胞Nrf2表达差异的研究[D]. 吉林大学硕士学位论文, 2012. http://cpfd.cnki.com.cn/Article/CPFDTOTAL-ZGDV200908001069.htm |



