常用的生活饮水中含有各种阴阳离子,不同阴离子对人体的作用各有不同。氯离子以氯化钠的形式广泛存在于人体,对调节人体内的水分、渗透压与酸碱平衡等起重要作用。人体内缺少氯会导致腹泻、缺水等症状,过多的摄取钠则会导致高血压;在天然饮用水和食物中都有低浓度的氟化物存在,地下水中的氟含量则要高一些,海水中平均为1.3 mg/L,淡水中的则为0.01~0.3 mg/L。氟离子会与血液中的钙离子结合,生成不溶的氟化钙,从而进一步造成低血钙症。同时因氟化物具有预防龋齿的作用,某些饮用水及其他口腔卫生产品中人为添加了少量氟;硝酸盐与亚硝酸盐作为环境污染物而广泛地存在于自然界中,尤其是在气态水、地表水和地下水、动植物体内以及食物中。特别是亚硝酸盐在胃液中或与肠道中细菌作用,产生致癌的亚硝酸胺,增加胃癌的发病风险,因而亚硝酸盐含量的多少近些年一直是社会上关注的指标。硝酸盐在还原菌的作用下亦可被还原为亚硝酸盐;硫酸盐经常存在于饮用水中,其主要来源是地层矿物质的硫酸盐,在大量摄入硫酸盐后出现的最主要生理反应是腹泻、脱水和胃肠道混乱。
现在家庭中,除了传统的柴火铁锅烧水、煤气茶壶烧水外,电热水壶因其省时、节能、快速、美观、便捷、安全的特点,在进入市场后,迅速受到广大消费者青睐。而电热水壶也因其方便、便捷等特点而使很多人不将煮完的开水倒入热水瓶,而是直接放于电热水壶中,需要时继续加热从而导致反复煮水,或将电热水壶当做储水用具。市场上现有的电热水壶的材质主要有塑料、不锈钢和陶瓷,为了解多次煮沸后水质中阴离子含量的变化以及不同材质电热水壶在反复煮沸后各阴离子含量的差别,现对这3种不同材质的电热水壶进行多次煮沸,检测其水中阴离子含量变化情况。
1 材料与方法 1.1 仪器与试剂IS 900离子色谱仪 (美国戴安)、Cary 60 UV-vis紫外可见分光光度计 (美国安捷伦)、50 mL比色管;对氨基苯磺酰胺溶液 (AR)、盐酸N-(1-萘) 乙二胺溶液 (AR)、碳酸氢钠、碳酸钠 (AR),由环保部标准样品研究所生产的氯化物标准溶液 (500 mg/L)、硫酸盐标准溶液 (500 mg/L)、硝酸盐氮标准溶液 (500 mg/L)、亚硝酸盐氮标准溶液 (1 000 mg/L),中国计量科学研究院生产的氟化物标准溶液 (1 000 mg/L)。
1.2 检测与评价方法氟化物、氯化物、硝酸盐、硫酸盐、亚硝酸盐氮均按照《生活饮用水标准检验方法》(GB/T 5750-2006) [2]进行检测,其中氟化物、氯化物、硝酸盐、硫酸盐选择离子色谱法,亚硝酸盐氮选择重氮偶合分光光度法。评价标准依据《生活饮用水卫生标准》(GB 5749-2006)[1]规定,氟化物<1.0 mg/L,硝酸盐 (以N计)<10 mg/L,亚硝酸盐<1 mg/L,氯化物<250 mg/L,硫酸盐<250 mg/L。
1.3 标准曲线的制备氟化物、氯化物、硝酸盐、硫酸盐标准曲线的配制,首先配制氟化物1.00 mg/L、氯化物50.0 mg/L、硝酸盐氮5.00 mg/L、硫酸盐125 mg/L的混合标准使用液。取10.00 mL氟化物标准溶液于100 mL容量瓶中用水稀释至标线,配置成质量浓度为100 mg/L的氟化物标准中间溶液。取5.00 mL氯化物标准溶液、12.5 mL硫酸盐标准溶液、0.50 mL硝酸盐氮标准溶液及0.50 mL氟化物标准中间溶液于50mL容量瓶中用水稀释至标线配得混合标准使用液。取50 mL比色管6支,分别加入0、2.00、4.00、6.00、8.00、10.00 mL混合使用液,用水稀释至50 mL。配制成6个梯度的质量浓度系列 (表 1)。色谱条件:色谱柱为AS23(4 × 250 mm)、检测器为电导检测器、淋洗液为67.2 mg/L碳酸氢钠—477 mg/L碳酸钠溶液、淋洗使用液流速为1.0 mL/min、进样量为250 μL。将水样注入色谱仪进样系统,记录峰面积,以质量浓度为横坐标峰面积为纵坐标制作标准曲线。亚硝酸盐氮则配制标准使用液1.00 mg/L,取1.00 mL亚硝酸盐氮标准溶液于1 000 mL容量瓶中用水稀释至标线。取50 mL比色管6支,分别加入0、0.25、0.5、1.0、2.0、3.0 mL亚硝酸盐氮标准使用液,用水稀释至50 mL,配制成6个梯度的质量浓度系列 (表 1)。以质量浓度对应吸光度制作标准曲线。
| 项目 | 1 | 2 | 3 | 4 | 5 | 6 | 线性方程 | 相关系数 |
| 氟化物 | 0.000 | 0.040 | 0.080 | 0.120 | 0.160 | 0.200 | y=2.346x + 0.0272 | 0.9995 |
| 氯化物 | 0.000 | 2.00 | 4.00 | 6.00 | 8.00 | 10.0 | y=2.322x-0.281 | 0.9997 |
| 硝酸盐氮 | 0.000 | 0.200 | 0.400 | 0.600 | 0.800 | 1.00 | y=4.729x + 0.0811 | 0.9992 |
| 硫酸盐 | 0.000 | 5.00 | 10.0 | 15.0 | 20.0 | 25.0 | y=1.155x + 0.1960 | 0.9999 |
| 亚硝酸盐氮 | 0.000 | 0.005 | 0.010 | 0.020 | 0.040 | 0.060 | y=3.301x + 0.0001 | 0.9999 |
1.4 水样的测定
取饮用水 (自来水) 置于3种不同材质的电热水壶中,加入量分别为各材质电热水壶的最大水位处,容量均为1.2 L,测定该饮用水中阴离子含量。将电热水壶中的水煮沸后冷却,壶中水量均会随煮沸稍有减少,减少量约为10 mL,测定各电热水壶中水质的阴离子含量。按上述方法将电热水壶中的水每天煮沸4次,每次煮沸后取出10 mL用于分析,不加入新的饮用水,分两天,共煮沸8次,测定不同材质电热水壶煮沸后水中的阴离子含量。每个水样测定3次,取其平均值作为测定结果。
1.5 质量控制实验室所用仪器、器皿均经过检定,标准物质均在有效期范围内;在样品检测的同时抽取10%平行样,10%的样品进行加标回收;每次检测均测定质控样品。
2 结果对于不同材质的电热水壶,其阴离子含量随其煮沸次数的增加,有含量基本不变和随着次数增加而不同程度的增加两种表现形式。其中氟化物变化不大,其余阴离子含量均有不同程度的增加,特别对于人们所关注的亚硝酸盐,增加比较明显。对于材质为塑料和陶瓷的电热水壶,两者的阴离子含量增加程度相差不大,通常家庭中较多使用的不锈钢材质的电热水壶则较其他两种材质的电热水壶阴离子增加程度相对偏大。
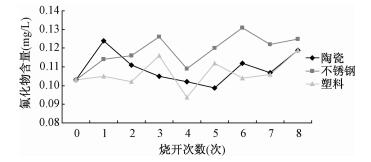
2.1 氟化物氟化物在3种不同材质的电热水壶中反复煮沸后质量浓度变动范围在0.09~0.13 mg/L之间波动,几乎无较为明显的变化 (图 1)。未煮开前氟化物测定结果为0.103 mg/L。其中8次煮沸后因蒸发过程使体积缩小而引起的浓度增加量约为0.007 mg/L。
|
| 图 1 氟化物相对煮沸次数的含量变化情况 |
2.2 氯化物
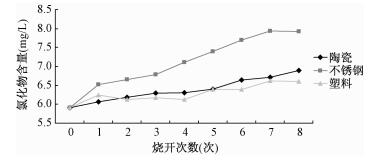
氯化物在塑料和陶瓷两种材质的电热水壶中反复煮沸后波动上升,但上升幅度不大,从6 mg/L上升至7 mg/L,而不锈钢材质的电热水壶在经过反复煮沸后,其质量浓度由6 mg/L增加至8 mg/L,增加幅度较另外两种材质的电热水壶偏高 (图 2)。未煮开前氯化物测定结果为5.91 mg/L。其中8次煮沸后因蒸发过程使体积缩小而引起的浓度增加量约为0.45 mg/L。
|
| 图 2 氯化物相对煮沸次数的含量变化情况 |
2.3 亚硝酸盐
亚硝酸盐在陶瓷材质中反复煮沸后,其含量从0.003 mg/L波动增加至0.042 mg/L,在塑料材质中反复煮沸后其含量从0.003 mg/L波动增加至0.072 mg/L,在不锈钢材质中反复煮沸后其含量从0.003 mg/L波动增加至0.183 mg/L。由此看出亚硝酸盐在3种材质的电热水壶反复煮沸后,其含量陶瓷低于塑料,塑料低于不锈钢 (图 3)。未煮开前亚硝酸盐测定结果为0.0033 mg/L。其中8次煮沸后因蒸发过程使体积缩小而引起的浓度增加量约为0.0002 mg/L。

|
| 图 3 亚硝酸盐相对煮沸次数的含量变化情况 |
2.4 硝酸盐
硝酸盐 (以N计) 在塑料和陶瓷两种材质的电热水壶中一直波动上升,但上升幅度不大,从0.712 mg/L增加至0.812 mg/L,而不锈钢材质的电热水壶在经过反复煮沸后,其质量浓度由0.712 mg/L增加至0.965 mg/L,增加幅度较另外两种材质的电热水壶偏高 (图 4)。未煮开前硝酸盐 (以N计) 测定结果为0.712 mg/L。其中8次煮沸后因蒸发过程使体积缩小而引起的浓度增加量约为0.05 mg/L。

|
| 图 4 硝酸盐相对煮沸次数的含量变化情况 |
2.5 硫酸盐
硫酸盐在塑料和陶瓷两种材质的电热水壶中一直波动上升,但上升幅度不大,从14.05 mg/L波动增加至16.47 mg/L,而不锈钢材质的电热水壶在经过反复煮沸后,其质量浓度由14.05 mg/L增加至19.01 mg/L,增加幅度较另外两种材质的电热水壶偏高 (图 5)。未煮开前硫酸盐测定结果为14.1 mg/L。其中8次煮沸后因蒸发过程使体积缩小而引起的浓度增加量约为1.00 mg/L。

|
| 图 5 硫酸盐相对煮沸次数的含量变化情况 |
3 讨论
不同的阴离子随着水的反复煮沸除氟化物变化不大以外,其他各阴离子均随煮沸次数的增加而增加。反复煮沸使水蒸发浓缩[6],是所有离子增加的一个因素,其煮沸8次后增加量为7%左右,但实际各离子增加的含量除氟外均大于10%,增加量大于浓缩因素的影响。硝酸盐增加的因素可能为:①加热过程中发生的化学反应将氨氮直接氧化成硝态氮;②有机氮转化为硝态氮[3]。亚硝酸盐增加的因素可能为:①开水放置较长时间并被细菌污染,细菌使硝酸盐还原为亚硝酸盐;②硝酸盐受热分解成亚硝酸盐[7]。同时高温煮沸过程也促进氨氮氧化成亚硝酸盐[4]。氯离子增加的因素可能为:二氧化氯是目前国际公认的一种安全、高效、低毒、快速的新型强氧化灭菌消毒剂[5]。在正常的水处理过程中二氧化氯通过氧化还原反应被转化成亚氯酸根离子、氯酸根离子和氯离子。目前关于加热容器材质对水中亚硝酸盐氮的影响还未见报道[7],有待进一步实验,探讨不同容器引起部分阴离子增加的发生机制。
4 结论根据《生活饮用水卫生标准》(GB 5749-2006)[1],水在8次煮沸后仍符合卫生要求,说明反复煮沸的水是安全的。但随着煮沸次数的增加,水中各阴离子含量有增加趋势的。
对3种不同材质的电热水壶中的水反复煮沸后的结果分析,3种电热水壶在反复煮沸后均能符合《生活饮用水卫生标准》(GB 5749-2006)[1],但所引起的变化却有所不同。从结果可以看出,不锈钢材质的电热水壶总体引起的阴离子增加量较其他两种材质的稍大,其他两种材质的电热水壶中水质的阴离子变化量基本相同。因此平常选购电热水壶时可适当的参考。本实验仅仅随机选购了3个不同材质的电热水壶,并只探讨了阴离子的变化情况,其他材质的电热水壶及指标的变化还有待于进一步探讨。
| [1] | 中华人民共和国卫生部, 中国国家标准化管理委员会. GB 5749-2006生活饮用水卫生标准[S]. 北京: 中国标准出版社, 2007. |
| [2] | 中华人民共和国卫生部, 中国国家标准化管理委员会. GB/T 5750-2006生活饮用水标准检测方法[S]. 北京: 中国标准出版社, 2007. |
| [3] | 沈倩倩, 张光明. 饮用水反复烧开对水质的影响[J]. 环境科学与技术, 2011, 34(5): 128–130. |
| [4] | 崔宇, 杨志国. 饮用水三氮变化分析[J]. 中国医药导报, 2009, 6(25): 119–122. doi: 10.3969/j.issn.1673-7210.2009.25.071 |
| [5] | 林勇. 饮用水加氯消毒副产物的危害及去除[J]. 济南职业学院学报, 2007(2): 86–88. |
| [6] | 王兴国. "千滚水"与亚硝酸盐[J]. 大众健康, 2013(2): 73. |
| [7] | 王九龙, 张明明, 王金叶. 青岛农业大学生活饮用水亚硝态氮检测与情况分析[J]. 青岛农业大学学报 (自然科学版), 2012, 29(2): 111–114. |


