2. 遵义医学院附一院
壬基酚(nonylphenol,NP)作为典型的环境雌激素类污染物之一,是目前最常见的工业毒物和环境毒物。前期研究发现孕期暴露壬基酚可导致子代学习记忆能力下降[1-3],但有关壬基酚影响脑发育的机制目前还不十分清楚。基因芯片技术是20世纪90年代迅速发展起来的分子生物学技术,他具有快速、准确、多样性、微型化和自动化等优点[4]。本研究应用基因芯片技术筛选暴露仔鼠脑组织的差异表达基因,拟在基因水平揭示壬基酚引发仔鼠学习记忆能力降低的可能作用机制。
1 材料与方法 1.1 材料 1.1.1 实验动物分组及染毒清洁级SD大鼠60只(动物合格证号:SCXK(渝)20070005),按雌:雄2:1同笼交配,次日晨经阴道涂片检查发现精子者,当日记为妊娠0 d(GD 0),将交配成功的孕鼠根据妊娠日期分层后随机分配到2组,即对照组(溶剂花生油)和暴露组(NP 200 mg/kg·d),每组7只,于受孕第6 d到出生后21 d哺乳期(GD 6~PND 21) 空腹灌胃NP,饲养于相对湿度(60±5)%,温度(20±2)℃,自然通风,12 h光照,12 h黑暗。
1.1.2 主要试剂TRIzol试剂(美国Invitrogen life technologies公司);单色DNA标记试剂盒(瑞士Nimblegen公司);芯片杂交试剂盒(瑞士Nimblegen公司);洗涤缓冲试剂盒(瑞士Nimblegen公司)。
1.1.3 主要仪器Biopulverizer组织研磨器(biospec);Mini-Bead-Beater-16研磨珠均质器(biospec);NimbleGen芯片杂交系统(Nimblegen);GenePix 4000B (Axon);GenePix pro V6.0,RNeasy小型离心柱。
1.1.4 芯片大鼠表达谱芯片采用Roche NimbleGen(nimblegen systems, Inc, USA)的12×135 K芯片,每张芯片可检测26 419个基因,每个基因平均设置5个探针。
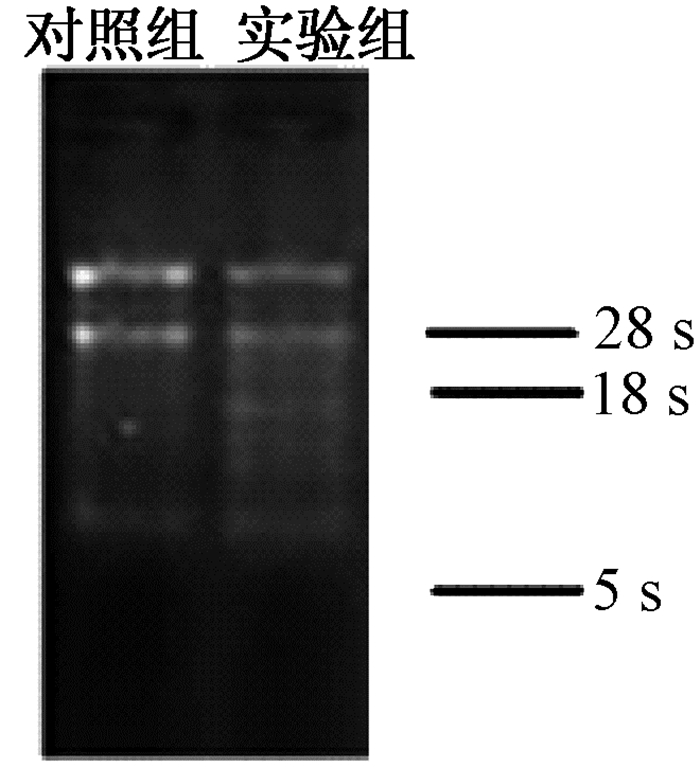
1.2 实验方法 1.2.1 样品的采集将21 d龄雄性仔鼠断头处死,并在盛有少量灭菌蒸馏水的培养皿中迅速剥离出脑组织放入冻存管中,做好标记,NP暴露组和对照组分别积累取样5个,然后在盛有液氮的金属容器内分别将各组的样品合并,放液氮罐中备用,操作全过程少于1 min。总RNA提取后质检,OD值A260 /A280比值应在1.8~2.1之间(表 1、图 1)。
| 样品 | OD260/280 | OD260/230 | 浓度(ng/μL) |
| 对照组 | 2.04 | 2.35 | 1 721.97 |
| 实验组 | 2.06 | 2.28 | 2 024.5 |
|
| 图 1 组织总RNA琼脂糖凝胶电泳检测 |
1.2.2 芯片杂交与洗涤
委托上海康成科技有限公司完成。
1.2.3 芯片扫描与分析芯片晾干后,结果采用Axon GenePix 4 000 B芯片扫描仪,在5 μm/像素的分辨率下进行扫描,用GenePix Pro V6.0软件读取原始荧光值。
2 结果 2.1 脑组织RNA提取及质量鉴定提取组织总RNA,经核酸浓度测定仪检测A260/A280比值在1.9~2.1之间,表明提取的总RNA无降解,纯度高(表 1)。经1.5%琼脂糖凝胶电泳以检测总RNA的完整性,显示总RNA的28S和18S两条带比较清晰完整(图 1)。
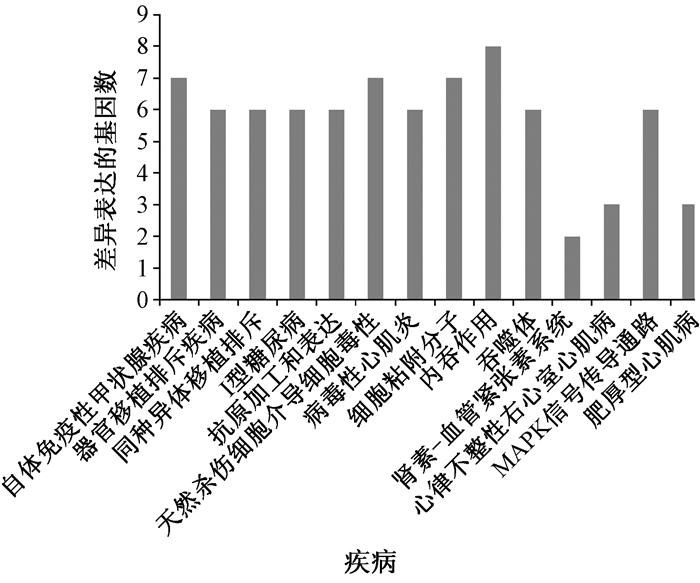
2.2 信号通路及与疾病发生 2.2.1 上调基因参与的通路及疾病DAVID软件对差异表达基因的通路分析表明差异表达基因主要参与MAPK、细胞黏附信号通路、细胞毒性,JNK等信号通路传导过程,其中MAPK信号通路在控制细胞生长与增殖、发育、分裂、死亡等方面起重要的作用。参与信号通路及疾病的上调基因(图 2)。
|
| 图 2 上调基因参与的信号通路及疾病 |
2.2.2 下调的基因参与的通路及疾病
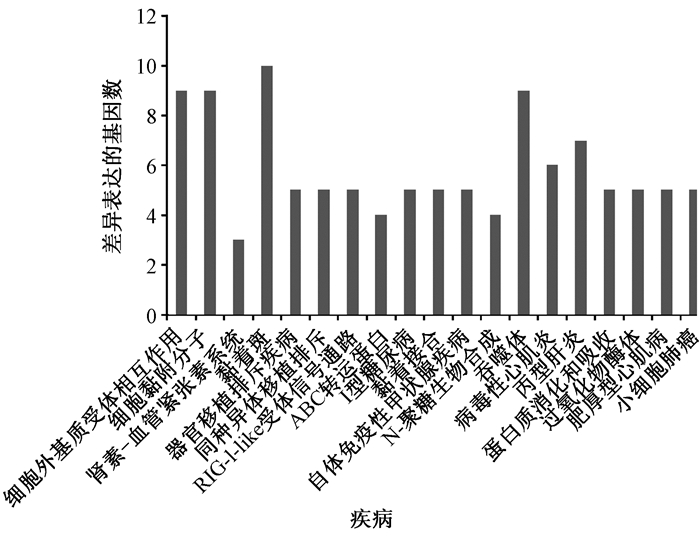
DAVID软件对差异表达下调基因的通路分析表明差异表达基因参与了NF-κB、细胞黏附信号通路、细胞毒性,JNK等信号通路传导过程,参与信号通路及疾病的上调基因见图 3。其中MAPK信号通路在控制细胞生长与增殖、发育、分裂、死亡起重要的作用参与信号通路及疾病的上调基因。
|
| 图 3 下调基因参与的信号通路及疾病 |
3 讨论
本课题组从分子生物学角度出发,在以往研究的基础上,首次采用NP暴露组和对照组出生第21 d雄性仔鼠脑组织样(注:本实验中只做了雄性仔鼠的芯片,原因是从目前已有的研究和本课题组前期的研究中发现,NP发挥的拟雌激素样作用主要针对雄性仔鼠有发育毒性和神经毒性,而对雌性仔鼠的影响不大,所以整个实验只做了雄性仔鼠)。通过提取组织总RNA,应用基因芯片技术检测两组差异基因,基因芯片技术可了解NP等环境污染物与导致神经毒性相关基因的相互关系。目前NP的神经毒作用机制尚不清楚,通过神经毒作用相关基因的差异表达,找出可供更进一步研究的方向和思路。
为了能更清楚的阐明NP对成熟期仔鼠神经系统发育影响的机制,现将差异表达的基因按功能进行分类,重点关注与神经营养相关的基因和细胞凋亡基因的变化,进行分类讨论。
3.1 NP对神经营养相关基因的影响 3.1.1 甘丙肽(galanin,Gal)基因下调Gal是一种在哺乳动物脑中有广泛分布的神经肽,通过几种Gal受体亚型介导参与了体内广泛的生理过程和病理反应。Gal和Gal受体mRNA表达在发育中的和成熟的大鼠脑内神经细胞新生部位包括脑室下带,海马的齿状回和吻端迁移途径都有发现。在功能上,Gal除了在成体脑中起快速传导的调制作用外,其还在神经生成和神经损伤修复中能起到营养因子的作用。将脑源性神经营养因子Gal基因敲除后,观察到小鼠空间记忆缺损[5];冯思明等[6]综述国内外的四十多项研究表明Gal等脑源性神经营养因子与学习记忆有密切的关系。因此,孕期及哺乳期暴露NP,导致海马组织神经营养因子Gal基因下调,可能会影响子代神经生成和损伤修复。
3.1.2 神经生长因子(nerve growth factor,NGF)基因下调NGF是第一个被发现的神经营养因子,他具有维持和促进神经元的发育和分化,发挥修复和再生的生理功能[7]。有研究发现,中枢NGF与学习记忆密切相关,NGF缺乏可引起动物学习记忆的缺陷,反之,提高NGF的水平,能改善认知功能障碍[8]。国外有关于NP作用于体外分离培养的胚胎爪蟾脊髓神经元对NGF影响的研究,结果显示NP不会直接改变神经细胞的生存或突起生长,但可抑制NGF诱导突起生长,同时NP可增加神经生长因子蛋白激酶A在此细胞株的活性[9]。
3.2 NP对细胞凋亡相关基因的影响 3.2.1 凋亡蛋白酶活化因子-1 (apoptotic protease activating factor-1,Apaf-1) 基因上调Apaf-1是一种分子量为130 kD的蛋白质,其存在于细胞质中。人Apaf-1基因位于染色体12q23,是细胞增殖与凋亡的核心调控因子[10]。目前已有很多研究表明NP可导致细胞凋亡,Aoki等[11]研究发现NP可促进体外培养精子的凋亡,体内外实验表明NP引起的免疫毒性可能是由于NP通过调节Fas/Fas-L mRNA的表达量,诱导胸腺细胞凋亡而引起的[12]。Kim等[13]将NP和辛基酚联合暴露于人胚胎干细胞,结果发现NP通过调节Fas/Fas-L的表达,从而诱导人胚胎干细胞的凋亡途径导致凋亡。而另一研究发现NP可以使线粒体膜电位的丢失从而导致细胞凋亡[14]。本实验结果发现NP染毒组海马组织中凋亡蛋白酶活化因子-1基因上调,表明NP可能通过上调Apaf-1等凋亡基因从而使神经细胞增殖失调,影响子代的神经系统功能的正常发挥。
3.2.2 凋亡抑制基因-1(defender ageinst apoptotic death-1,DAD1) 基因下调DAD1是哺孔动物高度保守的凋亡抑制基因,定位于细胞内质网,且广泛表达,最初是在BHK21细胞系的体外培养中,据Kelleher等[15]报道,DAD1具有下调细胞内Bcl-2蛋白的作用,Bcl-2家族蛋白在调节神经系统细胞凋亡中起到重要作用。Bcl-2基因产物Bcl-2蛋白是一种抑制凋亡蛋白,他通过与促凋亡Bax蛋白竞争性结合,形成异源二聚体来抑制细胞的凋亡[16],目前已有研究发现200 mg/kg剂量的NP能够抑制脑组织中Bcl-2 mRNA的表达[17]。本次芯片同时检测出NP导致Caspase7基因上调,结合毛缜研究结果,即NP导致Bcl-2 mRNA低表达,推测的原因可能是通过调控caspase家族蛋白或者通过DAD1下调来抑制细胞内Bcl-2蛋白或RNA表达,从而诱发凋亡。
本实验同时检测出与神经生长相关的基因有AGT、POU3F1、POU3F2、NKX6等,检测出与细胞凋亡相关的差异表达基因有PROK2、LHX4、PCSK6、SERPINE1、PIM1、PHB、CD38、BCL11B、AGT、NTRK1,因此,表达谱芯片结果推测NP可通过降低NGF等神经营养因子的表达,或上下调细胞凋亡相关基因影响神经元的发育、轴突的生长、递质的合成,这可能是NP引起子代学习记忆障碍的可能原因和机制之一,需对部分差异表达基因和通路进行进一步验证。
| [1] | Jie X, Yang W, Jie Y, et al. Toxic effect of gestational exposure to nonylphenol on F1 male rats[J]. Birth Defects Research (Part B), 2010, 89(5): 418–429. doi: 10.1002/bdrb.v89:5 |
| [2] | Yu J, Fan QY, Binli H, et al. Joint neurodevelopmental and behavioral effects of nonylphenol and estradiol on F(1) male rats[J]. International Journal of Environmental Health Research, 2013, 23(4): 321–330. doi: 10.1080/09603123.2012.733936 |
| [3] | Xu Jie, Li JM, Feng Z, et al. Neurotoxic effects of nonylphenol:a review[J]. Wien Klin Wochenschr, 2013, 125(3-4): 61–70. doi: 10.1007/s00508-012-0221-2 |
| [4] | Simunovic F, Yi M, Wang Y, et al. Evidence for gender specific transcriptional profiles of nigral dopamine neurons in Parkinson disease[J]. PLoS ONE, 2010, 5(1): 8856. doi: 10.1371/journal.pone.0008856 |
| [5] | 戴薇薇, 金国琴, 张学礼, 等. 补肾方药对衰老大鼠海马学习记忆相关基因BDNF及其受体TrkB mRNA表达的影响[J]. 中华中医药杂志, 2008, 23(4): 296–299. |
| [6] | 冯思明. 补肾益智方对AD大鼠学习记忆能力及神经生长因子表达的影响[D]. 广州中医药大学硕士论文, 2009. http://cdmd.cnki.com.cn/Article/CDMD-10572-2009120639.htm |
| [7] | Tang XQ, Cai J, Nelson KD. Functional repair after dorsal root and neurotrophic molecules[J]. Eur Neurosci, 2004, 20(5): 1211–1218. doi: 10.1111/ejn.2004.20.issue-5 |
| [8] | Yin M. The summarize of nerve growth factor[J]. Navy Military Affairs J Med, 1998, 19(1): 44–46. |
| [9] | Tessarollo L. Pleiotropic functions of neurotrophins in development[J]. Cytokin Growth Factor Reviews, 1998, 9(2): 125–129. doi: 10.1016/S1359-6101(98)00003-3 |
| [10] | Bevan CL, Porter DM, Schumann CR. The endocrine-disrupting compound, nonylphenol, inhibits neurotrophin-dependent neurite outgrowth[J]. Endocrinology, 2006, 147(9): 4192–4204. doi: 10.1210/en.2006-0581 |
| [11] | Aoki M, Kurasaki M, Saito T, et al. Nonylphenol enhances apoptosis induced by serum deprivation in PC12 cells[J]. Life Sci, 2004, 74: 2301–2312. doi: 10.1016/j.lfs.2003.09.066 |
| [12] | Yao G, Hu Y, Liang J, et al. Nonylphenol-induced thymocyte apoptosis is related to Fas/FasL pathway[J]. Life Sci, 2005, 77(26): 3306–3320. doi: 10.1016/j.lfs.2005.05.035 |
| [13] | Kim DK, Kim BK, Shim JH, et al. Nonylphenol and octylphenol-induced apoptosis in human embryonic stem cells is related to Fas-Fas ligand pathway[J]. Toxicol Sci, 2006, 94(2): 310–321. doi: 10.1093/toxsci/kfl114 |
| [14] | Yao G, Ling L, Luan J, et al. Nonylphenol induces apoptosis of jurkat cells by a caspase-8 dependent mechanism[J]. International Immuno pharmacology, 2007(4): 444–453. |
| [15] | Kelleher DJ, Gilmore R. DAD1, the defender against apoptotic cell death, is a subunit of the mammalian oligosaccharyltransferase[J]. Proc Natl Acad Sci, 1997, 94(10): 4994–4999. doi: 10.1073/pnas.94.10.4994 |
| [16] | Akhtar RS, Ness JM, Roth KA. Bcl-2 family regulation of neuronal development andneurodegeneration[J]. Biochimica et Biophysica Acta, 2004, 1644(2-3): 189–203. doi: 10.1016/j.bbamcr.2003.10.013 |
| [17] | Nicolas K, Emily JC, Emmanuel S. Developmental and metabolic brain alterations in rats exposed to bisphenol A during gestation and lactation[J]. International Journal of Developmental Neuroscience, 2011, 29(1): 37–43. doi: 10.1016/j.ijdevneu.2010.09.009 |


