草甘膦(glyphosate),是由美国孟山都公司开发的除草剂。25℃时在水中的溶解度为1.2%,不溶于一般有机溶剂。是一种非选择性、低残留灭生性除草剂,对多年生根杂草非常有效,是全世界用量最大的一种除草剂。2,4-滴,化学名:2,4-二氯苯氧乙酸。纯品为白色结晶,水中溶解度很小,易溶于乙醇、苯等有机溶剂,但其钠盐、胺盐则极易溶于水。因其用量多、成本低,一直是世界主要除草剂品种之一,也是我国目前使用量最大的几种除草剂中的两种。
《生活饮用水卫生标准》(GB 5749-2006)[1]中,有19项农药卫生指标,其中草甘膦和2,4-D的最大残留限量分别是0.7 g/mL和0.03 g/mL。原生活饮用水标准检验方法中给出的方法,需要浓缩,复杂的前处理和衍生化[2]。草甘膦在传统的反相液相色谱柱,保留时间很短,难以得到好的分离,色谱峰拖尾严重[3],也有用离子色谱法[4-7]测定水中的草甘膦,该方法与液相色谱质谱法相比,由于抗干扰能力弱,容易出现假阳性,在2013年的水源水农药残留建监测中发现可能有多例假阳性样品。本方法采样正相色谱柱,进一步优化了色谱条件,不但峰型对称,灵敏度大为提高,前处理无需进行预浓缩,草甘膦的灵敏度能够达到4 ng/mL,2,4-滴到0.4 ng/mL,完全可以满足饮用水卫生指标的分析,对保护我国的水体安全有重要的意义。
1 实验部分 1.1 仪器高效液相色谱质谱仪:液相色谱是Waters公司的Acquity UPLC,自动进样器是Waters公司的2777C,所配置的质谱是Waters公司的XEVO TQ串联质谱。
1.2 试剂草甘膦(99.9%),2,4-滴(99.8%)从SIGMA公司所购。称取10.0 mg标样草甘膦和2,4-滴,用纯水定容50 mL,得草甘膦和2,4-滴储备液200.0 μg/mL。
乙腈(Fisher公司,色谱纯);乙酸铵(天津光伏精细化工研究所,色谱纯);氨水(北京化工厂,分析纯);超纯水,由TTL-10B纯化制备,电阻18.2 MΩ。
1.3 标准溶液的配制分别取适量的草甘膦和2,4-滴储备液至1个100 mL的容量瓶中,用经0.22 μm滤膜过滤的自来水稀释,配制的草甘膦系列标准溶液的质量浓度分别为20.0、40.0、100.0、400.0和800.0 ng/mL;2,4-滴系列标准溶液的浓度分别为2.0、4.0、10.0、40.0和80.0 ng/mL,以自来水作空白对照。
1.4 色谱质谱条件 1.4.1 质谱条件电喷雾三重四极杆串联质谱,负离子ESI模式,去溶剂温度450℃;去溶剂气流量:800 L/h;毛细管电压:2.5 kV;锥孔电压:25 V;碰撞气(氩气)流量:0.16 mL/min。MRM参数如下:草甘膦检测的定量离子对:168.0/149.9,碰撞电压:10V,定性离子对168.0/123.9,碰撞电压:12V,这两对离子对的锥孔电压都为:25 V,驻留时间都为(Dwell)0.1s;2,4-滴检测的定量离子对:219.1/160.9,碰撞电压:14 V,定性离子对219.1/124.9,碰撞电压:16V,这两对离子对的锥孔电压都为:18 V,驻留时间都为(Dwell)0.1 s。
1.4.2 色谱条件色谱柱:资生堂CAPCELL PAK ST柱(2.1 mm×150 mm);柱温:30℃。流动相为:A:10 mmol/L乙酸铵水溶液(用氨水调pH至10.10),B:乙腈,A/B=72/ 28,流速:0.4 mL/min;进样量:10 μL。
1.5 样品的制备直接过0.22 μm滤膜,装样品瓶,待分析。
2 结果与分析 2.1 液相色谱条件的优化色谱柱的选择:草甘膦和2,4-滴具有较强的极性,试用了Waters公司的UPLC BHC C18柱,Atlantis C18柱,和Agilent公司的ZORBAX Eclipse Plus C18柱,发现草甘膦或者不能够出峰,或者拖尾现象严重。参考了曾经分析测定水中强极性除草剂百草枯的分析方法,采用正相色谱柱CAPCELL PAK ST柱(2.1 mm× 150 mm),无需添加离子对试剂,就能够得到有效的分离,且峰型对称,灵敏度高。
优化流动相:流动相A配置为10 mmol/L乙酸铵水溶液,用氨水调节流动相A的pH值,设置流动相A/B=7/3,经试验发现,在pH在10.0以下时,草甘膦和2,4-滴的灵敏度有明显的下降,在pH值大于10.2时,虽然随pH的变大,草甘膦的灵敏度能有部分增加,但由于溶液中添加的氨水有一定的挥发性,氨水浓度越高,pH越不易稳定,易造成草甘膦和2,4-滴出峰强度和保留时间不稳。因此经过多次优化流动相试验,发现流动相A的pH调至10.10,水相和有机相的比例为72/28,草甘膦和2,4-滴有较好的灵敏度和合适的稳定性。
在柱温的选择上,柱温设为40℃时,30℃和室温时,对出峰的峰型,分离度,灵敏度等影响不大。选择柱温30℃,保留时间重复性好,受室内环境稳定影响小。
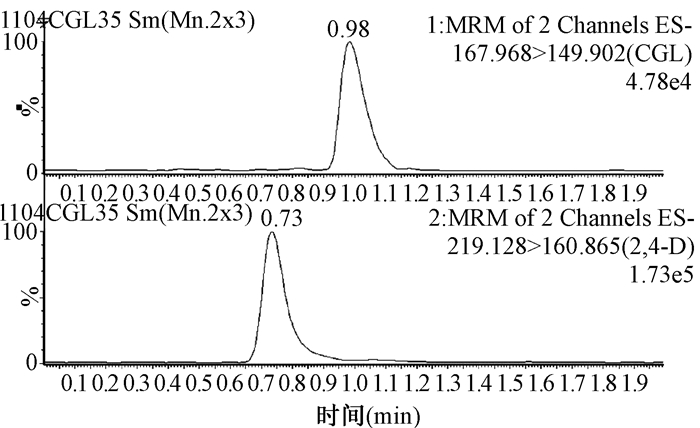
优化后的色谱条件:流速0.4 mL/min,柱温30℃,流动相为A:10 mmol/L乙酸铵水溶液(用氨水调pH至10.10),B:乙腈,A/B=72/28,在此色谱条件下,草甘膦的保留时间0.98 min,2,4-滴的保留时间0.73 min。图 1显示的是草甘膦和2,4-滴在自来水中添加4.0 ng/mL的样品色谱图
|
| 图 1 草甘膦和2,4-滴在自来水中的添加样品色谱图 |
2.2 质谱条件的优化
根据草甘膦和2,4-滴的分子结构的特征,实验选择了负离子ESI电离模式。考虑到在液相中,流动相中乙腈的比例较大,设置去溶剂温度450℃;去溶剂气流量:800 L/hr,最佳的毛细管电压2.5 kV,锥孔电压25 V。然后通过质谱仪进行MRM参数自动优化:草甘膦强度最好的两个离子对168.0/149.9和168.0/123.9,最佳碰撞电压分别为10V和12V,锥孔电压均为25 V,驻留时间均为(Dwell)0.1s。以离子对168.0/149.9强度最大,故以此离子对为定量离子对,而以168.0/123.9作为定性离子对;2,4-滴强度最好的两个离子对219.1/160.9和219.1/124.9,最佳碰撞电压分别为14 V和16 V,锥孔电压都为:18V,驻留时间都为(Dwell)0.1 s。以离子对219.1/160.9强度最大,故以此离子对为定量离子对,而以219.1/124.9作为定性离子对。
2.3 工作曲线,最低检出限,加标回收率和精密度在设定的色谱和质谱条件下,分别取10 μL在1.3中配制的系列标准溶液,进样LC-MS-MS分析,以草甘膦和2,4-滴在水中的质量浓度为横坐标,以草甘膦和2,4-滴的响应值为纵坐标,做工作曲线。得到草甘膦在水中浓度范围20.0~800.0 ng/mL时,线性相关系数为0.9992;2,4-滴在水中浓度范围2.0~80.0 ng/mL时,线性相关系数为0.9996。
在自来水中添加草甘膦和2,4-滴,以10倍信噪比(S/N)计算,在进样量10 μL时,得到的本方法草甘膦和2,4-滴最低检测质量浓度分别为4.0 ng/mL和0.4 ng/mL。
另外,草甘膦(100.0 ng/mL,400.0 ng/mL)和2,4-滴(10.0 ng/mL,40.0 ng/mL)在水中进行了两个水平的加标,每个水平6个重复。通过测定和工作曲线的计算,得到草甘膦测定的结果为:95.3±3.8ng/mL和402.7±20.8 ng/mL,即平均回收率分别为95.3%和100.7%,精密度RSD(n=6) 分别为4.0%和5.2%;2,4-滴测定的结果为:9.7±0.2 ng/mL和38.6±1.0 ng/mL,即平均回收率分别为97.0%和96.5%,精密度RSD(n=6) 分别为2.1%和2.6%。
3 讨论草甘膦的强离子特性使得他在传统的反相C18或C8色谱柱上,保留很弱,难以得到良好的分离,而且易与固定液上的硅羟基发生作用,产生严重拖尾。采用正相色谱柱,进行分离,草甘膦的分离和出峰峰型得到了极大的改善,使分离效果和灵敏度都得到了提高,在国内外草甘膦相关的文献中,很少见到这方面的报道。
在我国饮用水标准中草甘膦和2,4-滴的最大残留限量分别是700 ng/mL和30 ng/mL[1]。原生活饮用水标准检验方法中给出的方法,需要浓缩,前处理复杂和需要衍生化。根据现代检验技术的最新发展,采用灵敏度更高,准确性更好的液相色谱质谱技术。根据饮用水基质比较干净的特点,通过过滤,直接进样分析,快速,准确地测定这两种农药。建立的方法对草甘膦和2,4-滴的最低检测质量浓度分别为4 ng/mL和0.4 ng/mL。完全可以满足测定日常饮用水中这两种农药检测项目的需要。另外,如果结合其它合适的样品前处理方法,该检测方法也可以应用在食品和环境样品的分析检测方面。
| [1] | 中华人民共和国卫生部, 中国国家标准化管理委员会. GB/T 5750-2006生活饮用水标准检验方法[S]. 北京: 中国标准出版社, 2007. |
| [2] | 郭忠, 段江平, 王妍妍, 等. 高压液相色谱串联质谱法直接进样测定生活饮用水中的草甘膦[J]. 中国卫生检验杂志, 2013, 23(7): 1683–1685. |
| [3] | 郑和辉, 李洁, 魏建荣, 等. 液相色谱串联质谱法直接进样测定水中呋喃丹、草甘膦、灭草松和2,4-滴[J]. 卫生研究, 2009, 38(3): 302–303. |
| [4] | 王勇, 吴波, 连厚彬, 等. 离子色谱法检验尸体心血中草甘膦[J]. 色谱, 2012, 30(4): 419–422. |
| [5] | 胡忠阳, 叶明立, 潘广文, 等. 离子色谱-抑制电导检测法同时测定草甘膦母液中的含磷副产物及无机阴离子[J]. 色谱, 2012, 30(4): 391–394. |
| [6] | 王莹, 魏慧珠, 马颖. 离子色谱法测定水源水和生活饮用水中的草甘膦[J]. 供水技术, 2012, 6(1): 53–55. |
| [7] | 宋耀英, 李霞, 唐建春. 离子色谱法测定生活饮用水中的草甘膦含量[J]. 实用预防医学, 2009, 16(4): 1267–1269. |



