2. 遵义医学院公共卫生学院;
3. 遵义市第一人民医院检验科
壬基酚(nonylphenol,NP)是一类能改变内分泌系统的功能、干扰机体内分泌代谢、导致代谢紊乱的环境内分泌干扰物(environmental endocrine disrupters,EEDs)。既往的研究表明围产期NP暴露可对包括子代内分泌系统在内的多个系统造成影响[1]。但其与影响机制相关的研究较少。TNF-α是一种多功能的炎症介质,既与肾上腺皮质功能状态联系紧密[2],又是肾上腺皮质功能损伤的重要因素[3]。IL-1β是炎症反应中的重要启动因子,与TNF-α有协同作用,加重炎性反应和组织损伤[4]。本研究通过建立孕哺期暴露NP的仔鼠模型,观察幼年期仔鼠(21 d),成熟期(60 d)仔鼠肾上腺TNF-α和IL-1β表达,检测血清中激素水平的变化,初步探讨NP导致肾上腺损伤和功能异常的作用机制。
1 材料与方法 1.1 材料 1.1.1 实验分组清洁级SD大鼠60只(动物合格证号:SCXK(渝)20070005),雌鼠和雄鼠按2:1比例合笼交配,阴道涂片检查以标定妊娠天数。据妊娠日期将32只成功受孕的孕鼠随机分配到对照组、低、中、高剂量暴露组,每组8只;消化道暴露,暴露剂量分别为0、25、50、100 mg/(kg ·d),对照组由10 mg/(kg ·d)花生油代替;暴露时间为受孕第6 d到出生后21 d(仔鼠哺乳结束)。仔鼠21 d后按8 g/100 g干饲料喂食,饲养于温度(25±1)℃,相对湿度45%±5%,通风良好,昼夜交替(12 h/12 h)。
1.1.2 试剂一抗为兔抗鼠TNF-α、IL-1β多克隆抗体(北京中山生物试剂制品有限公司);二抗为羊抗兔IgG抗体(北京中杉金桥生物科技有限公司);DAB显色试剂盒(DAKO公司);精制花生油(中粮集团有限公司);睾酮-19位测试盒(北京北方生物技术研究所);NP纯度99%(东京化成株试会社)。
1.1.3 实验仪器γ放射免疫计数器(GC-2010)(中科大中佳公司);普通光学/荧光显微成像系统(德国徕卡公司);电热鼓风干燥箱(北京市永光明医疗仪器厂);艾克超纯水机(成都康宁实验专用纯水设备厂);三用电热恒温水浴箱(天津市泰斯特仪器有限公司);FC104电子天平(上海精科天平)。
1.2 方法 1.2.1 免疫组化步骤4%多聚甲醛固定组织12 h,经常规石蜡包埋、制片;二甲苯脱蜡2×10 min;梯度乙醇涮洗30 s(无水乙醇—95%乙醇—75%乙醇);蒸馏水冲洗1 min;3%H2O2侵泡10 min;0.01 mol/L PBS震荡冲洗3×3 min;柠檬酸盐高压修复5 min,保温30 min,自然冷却;0.01 mol/L PBS震荡冲洗3×3 min;滴加30 μL动物封闭血清液,37℃封闭30 min;滴加兔抗鼠TNF-α、IL-1β一抗(1:100)30 μL,4℃孵育过夜;0.01 mol/L PBS震荡冲洗3×3 min;滴加生物素标记羊抗兔IgG,37℃孵育60 min;0.01 mol/L PBS震荡冲洗3×3 min;DAB显色液显色,在显微镜下观察显色颜色深浅,自来水冲洗以终止显色;苏木素复染,0.5%盐酸乙醇分化;自来水冲洗10~15 min;梯度乙醇涮洗30 s(75%乙醇—95%乙醇—无水乙醇);中性树脂胶封片。
1.2.2 免疫组化图象分析每张肾上腺切片随机挑选5个400倍视野进行拍照。Image-Pro Plus6.0和LAS V43.OB600(G)软件测量每张照片的累积光密度值(integral optical density,IOD)。IOD值越大,提示染色强度越强。
1.2.3 放免法实验步骤取仔鼠出生后60 d全血,经2 000 rpm、4℃离心10 min分离血清,按放免法检测试剂盒说明书操作步骤如下:先将圆底聚苯乙烯试管编号,分别编为标准S0-S6管,质控管,样品管;S0-S6分别加入试剂盒配备的标准品,各100 μL,质控管加入试剂盒中质控血清100 μL,样品管加入待测样品100 μL;以上每管加入125I-T 200 μL,抗体200 μL;充分混匀,37℃水浴60 min;加入分离剂500 μL,充分混匀,3 500 rpm离心25 min,立即吸弃上清液,在γ放射免疫计数器检测各管的放射性。
1.3 统计学分析用SPSS 13.0统计软件录入及分析。采用单因素方差分析做差异比较,对于有差异者再进行LSD两两比较,检验水准为α=0.05。
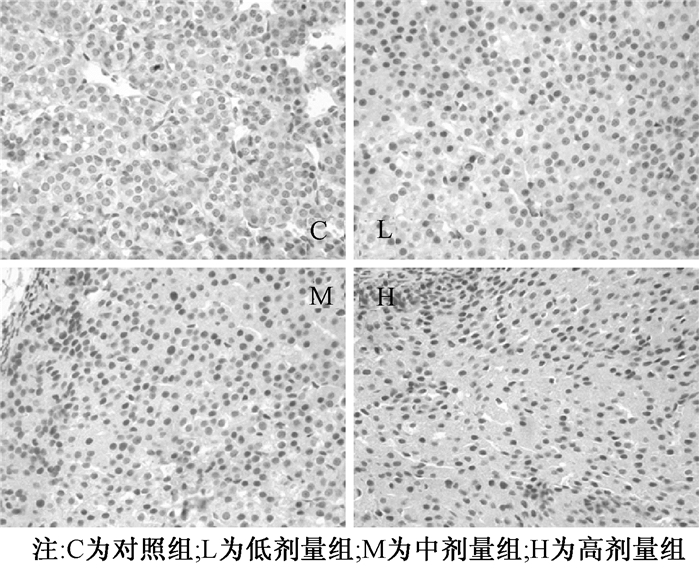
2 结果 2.1 TNF-α和IL-1β的表达各暴露组与对照组比较,仔鼠21、60 d肾上腺TNF-α和IL-1β染色强度较强。高剂量组与中、低剂量组比较,TNF-α和IL-1β染色强度较强。随着给药剂量和给药时间的增加,TNF-α和IL-1β染色强度逐渐增强。60 d各剂量组与21 d比较,TNF-α和IL-1β染色强度增加。结果见图 1—图 4。
|
| 图 1 NP各剂量组仔鼠肾上腺TNF-α表达(21 d,400×) |
|
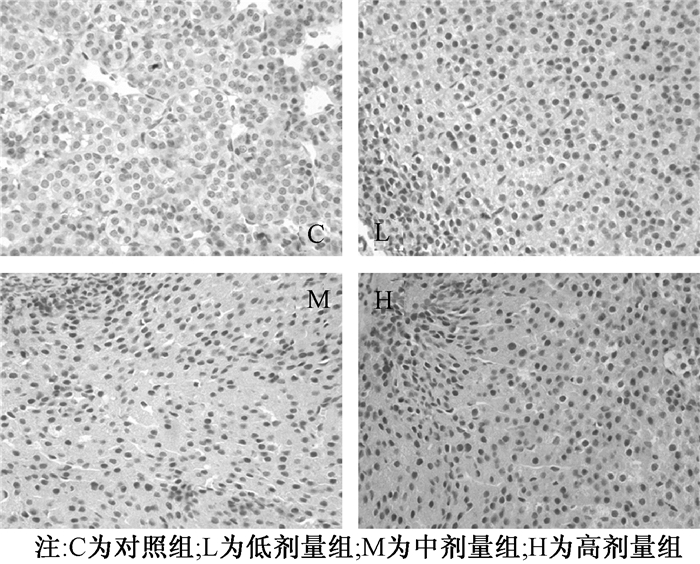
| 图 2 NP各剂量组仔鼠肾上腺TNF-α表达(60 d,400×) |
|
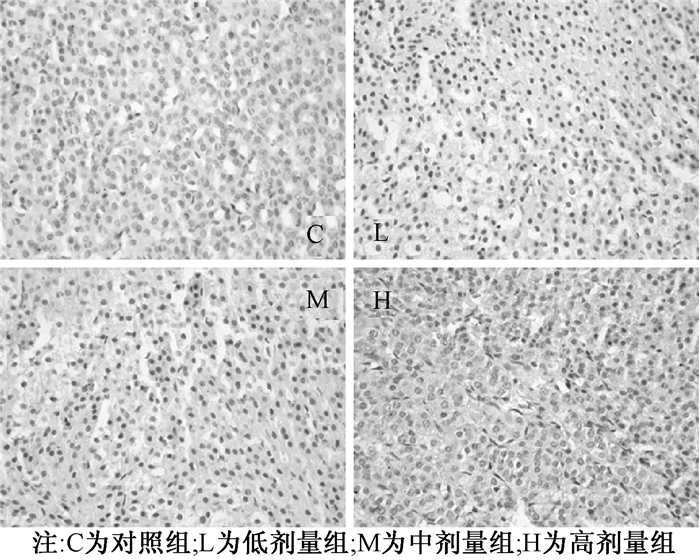
| 图 3 NP各剂量组仔鼠肾上腺IL-1β表达(21 d,400×) |
|
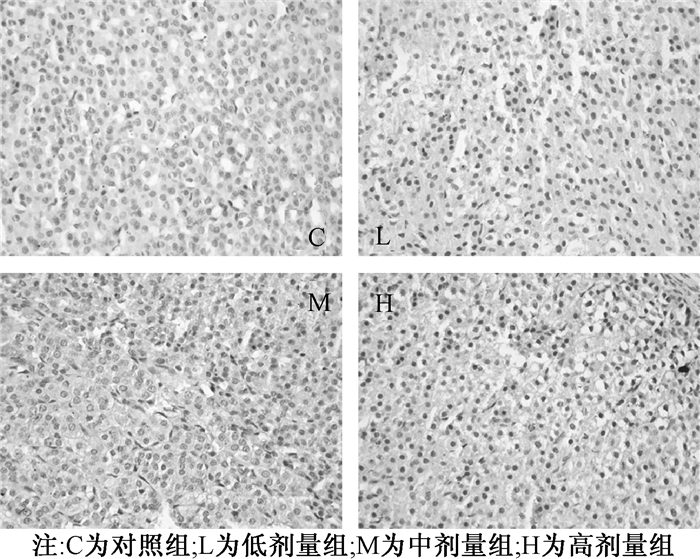
| 图 4 NP各剂量组仔鼠肾上腺IL-1β表达(60 d,400×) |
图像分析数据显示,孕鼠NP暴露后,TNF-α和IL-1β与对照组比较,低、中、高剂量组光密度增高(F=4265.85、96.191,P < 0.05) 和(F=428.759、1519.815,P < 0.05,表 1,2)
| 分组 | 累积光密度值 | |
| 21 d | 60 d | |
| C | 369 160±4 916 | 394 764±6 775 |
| L | 540 180±1 181* | 664 629±15 699* |
| M | 547 573±5 621* | 708 787±12 537* |
| H | 727 529±10 174* | 1 040 760±151 338* |
| F值 | 4 265.850 | 96.191 |
| P值 | 0.000 | 0.000 |
| 注:*与对照组比较,P < 0.05 | ||
| 分组 | 累积光密度值 | |
| 21 d | 60 d | |
| C | 414 938±19 865 | 445 232±20 392 |
| L | 520 938±16 963* | 612 177±5 289* |
| M | 635 861±11 632* | 768 210±7 068* |
| H | 639 362±6 198* | 772 053±3 623* |
| F值 | 428.759 | 1 519.815 |
| P值 | 0.000 | 0.000 |
| 注:*与对照组比较,P < 0.05 | ||
2.2 血清放免结果
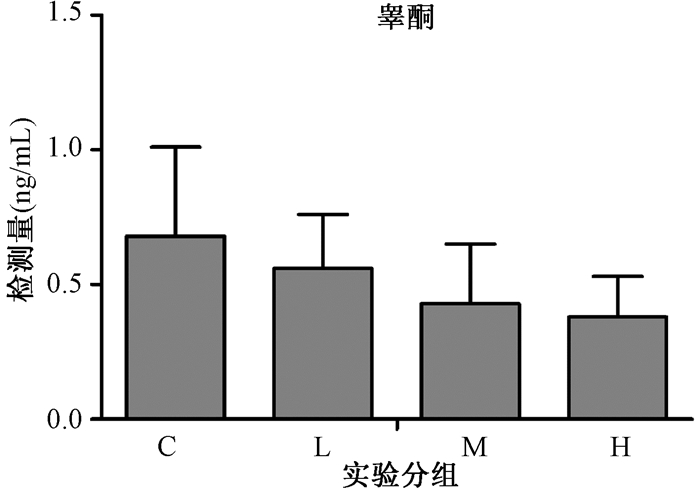
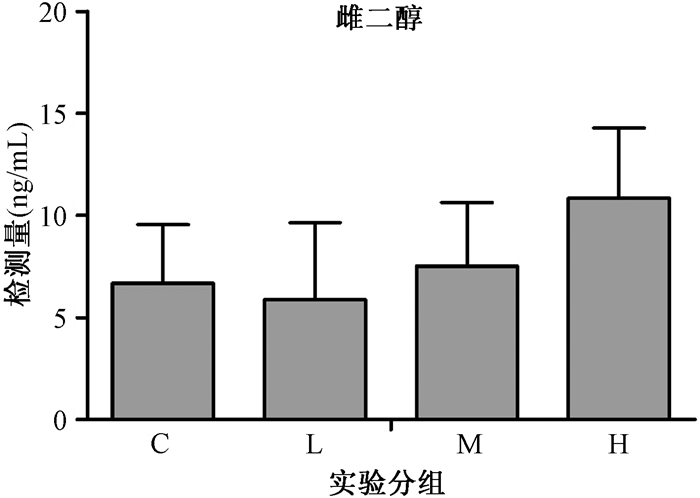
仔鼠出生后60 d血清放免结果示:血清睾酮水平与NP暴露剂量呈负相关(r=-0.417,P < 0.05),中、高剂量组睾酮低于对照组,差异有统计学意义(P < 0.01)。血清雌二醇水平与NP暴露剂量呈正相关(r=-0.462,P < 0.01),高剂量组血清雌二醇水平高于对照组,差异有统计学意义(P < 0.05;图 5、6)。
|
| 图 5 各组血清睾酮水平比较 |
|
| 图 6 各组血清雌二醇水平比较 |
3 讨论
壬基酚(nonylphenol,NP)是一类环境内分泌干扰物[5]。既往的研究表明围产期暴露NP对成年子代多种器官有毒性作用[6-8]。目前对NP能否影响肾上腺以及怎样影响肾上腺的研究较少。
TNF-α是一种多功能的细胞因子[9],TNF-α可通过提高caspase 8/3的活性而促进小鼠肾上腺皮质细胞的凋亡[10],又可作用于下丘脑,对肾上腺皮质功能的调节有重要影响。同时在炎症反应、内毒素休克等病理生理过程中,TNF-α作为一种重要的炎症介质,对于肾上腺皮质功能的损伤发挥着重要作用。IL-1β和TNF-α有协同作用,两者生物活性也非常相似,都是有多效性作用的促炎细胞因子,可刺激抗原递呈细胞和T细胞活化,促进B细胞增殖和分泌抗体,大量产生内分泌效应,引起炎症介质释放,刺激多种间质细胞释放蛋白分解酶并产生一些效应,以及促进抗原递呈细胞的抗原递呈能力,并且两者可协同诱导黏附分子的表达、自由基的产生,增加血管通透性,引起微循环障碍,促发炎性因子的一系列级联连锁反应[11];共同加重和扩大了组织的损伤。
本实验结果证实NP暴露后仔鼠肾上腺出现了对肾上腺皮质功能损伤有重要联系的两种炎性介质的表达,且与暴露剂量和暴露时间呈正相关,可推测仔鼠的肾上腺可能存在炎性反应,并导致炎性损伤。该病理生理过程中可能有TNF-α、IL-1β协同作用的肾上腺损伤,并可能损伤了肾上腺皮质束状带细胞,影响其正常生理状态下主要分泌雄激素并分泌少量的雌激素的功能,从而引起血清学激素水平的变化。血清放免结果也显示了这种变化:血清中睾酮水平降低、雌二醇水平增加。本实验结果表明NP可损伤仔鼠肾上腺细胞,而炎性反应可能是致其细胞损伤及功能异常的重要机制。
| [1] | 俞捷, 吴芹, 张镖, 等. 壬基酚对机体的毒性影响及其机制[J]. 环境卫生学杂志, 2013, 3(3): 268–272. |
| [2] | Harman E, Karadeniz M, Biray C, et al. The relation of adiponectin and tumor necrosis factor alpha levels between endothelial nitric oxide synthase angiotensin-converting enzyme, transforming growth factor beta and tumor necrosis factor alpha gene polymorphism in adrenal incidentalomas[J]. Endocrinol Invest, 2009, 32(11): 881–888. doi: 10.1007/BF03345766 |
| [3] | 夏海鸣, 方媛, 黄培林. TNF-α通过TNF-R1促进小鼠肾上腺皮质细胞系Y1凋亡[J]. 南京医科大学学报, 2011, 3(31): 364–373. |
| [4] | 武永胜, 李得溪, 赵海平, 等. 银杏叶提取物对重症急性胰腺炎大鼠脑组织中IL-1β、IL-6和TNF-α表达水平的影响[J]. 中国普外基础及临床杂志, 2012, 6(19): 616–621. |
| [5] | William Z, Mary ML. Male pubertal development:are endocrine-disrupting compounds shifting the norms:a review[J]. Endocrinol, 2013, 218: R1–R12. doi: 10.1530/JOE-12-0449 |
| [6] | 许洁, 俞捷, 刘晓云, 等. 壬基酚对胎鼠发育的毒性作用研究[J]. 卫生工业与职业病, 2009, 3(35): 132–134. |
| [7] | Ling LC, Wan S, Paulus SW. Effects and mechanisms of nonylphenol on corticosterone release in rat zona fasciculata-reticularis cells[J]. Toxicol Sci, 2010, 118: 411–419. doi: 10.1093/toxsci/kfq274 |
| [8] | Jubendradass R, D'Cruz SC, Mathur PP. Long-term exposure to nonylphenolaffects insulin signaling in the liver of adult male rats[J]. Human and Experimental Toxicology, 2012, 31: 868–876. doi: 10.1177/0960327111426587 |
| [9] | Bharat BA, Subash CG, Ji HK. Historical perspectives on tumor necrosis factor and its superfamily:25 years later, a golden journey:a review[J]. Blood, 2012, 119: 651–665. doi: 10.1182/blood-2011-04-325225 |
| [10] | 方媛, 夏海鸣, 孙佳, 等. TNF-α对小鼠肾上腺皮质细胞系Y1增殖、凋亡的影响[J]. 东南大学学报(医学版), 2010, 29(1): 81–85. |
| [11] | Annika T, Raphaela S, Henrike S, et al. Inflammation and metabolic dysfunction:links to cardiovascular diseases:a review[J]. Physiol Heart Circ Physiol, 2012, 302: H2148–H2165. doi: 10.1152/ajpheart.00907.2011 |



