2. 广东省肇庆市质量计量监督检测所
生产加工过程中包装容器的污染是食品中甲醛的来源之一。目前,食品包装材料中甲醛的分析方法有变色酸法[1]、盐酸苯肼比色法[2]、示波极谱电化学法[3]等。这些成熟的方法分析时间长、方法稳定性差、灵敏度低;同时由于甲醛的分子量较小,造成气相色谱法不能直接检测甲醛。有文献报道采用2,4-二硝基苯肼(DNPH)柱前衍生、GC-ECD检测包装材料中甲醛,与用DNPH柱前衍生、液相色谱仪定量分析相比,后者具有灵敏度高、选择性好等优点[4-6]。
1 实验部分 1.1 仪器与试剂岛津LC-2010AHT液相色谱仪(具紫外检测器);甲醛标准溶液(9.91 mg/mL, 国家标准物质中心);DNPH(广州化学试剂厂经重晶纯化处理或按文献[5]配制和提纯)乙腈溶液2.0 mg/mL;乙腈(天津科密欧化学有限公司,色谱纯);环己烷(天津化学有限公司,色谱纯);磷酸氢二钠溶液(180 g/L);盐酸—氯化钠溶液(氯化钠2 g加少许纯水溶解,再加入37%盐酸6 mL,最后用纯水定容至100 mL)。
1.2 液相色谱条件XDB C18不锈钢柱(250 mm×4.6 mm,5 μm)流动相;乙腈:水=62:38;柱流量1.0 mL/min;波长365 nm;柱温40℃;进样量10 μL。
1.3 标准曲线的制备吸取1.00 mL甲醛标准溶液于100 mL容量瓶中,纯水定容至刻度,作为甲醛标准储备溶液,临用前用纯水配制成20.00 μg/mL甲醛标准使用溶液。准确吸取0.00、0.10、0.20、0.40、0.80、1.50、2.00 mL甲醛标准使用溶液于50 mL比色管中,加纯水至5.00 mL,再加入盐酸—氯化钠溶液2.00 mL、磷酸氢二钠溶液1.00 mL、衍生物(DNPH乙腈溶液)0.50 mL,摇匀,于60℃水浴中衍生20 min,最后准确加入环乙烷5.00 mL,再用迷你振荡器(MS2 Mini Shaker)以2 000转/min振摇1 min,静止分层后将环乙烷层吸出,过滤,取0.01 mL滤液进样,每个浓度进样3次,以标准物质的峰面积对应标准浓度绘制标准曲线[6]。
1.4 样品的处理及测定样品的预处理按《食品罐头内壁环氧酚醛涂料卫生标准的分析方法》(GB/T 5009.69-2008)[1]进行样品的预处理。按每平方厘米的样品用95℃的纯净水2.00 mL进行浸泡30 min,浸泡液再按《食品罐头内壁环氧酚醛涂料卫生标准的分析方法》(GB/T 5009.69-2008)[1]之7.2.4.2处理后取蒸馏液或上清液5.00 mL于50 mL比色管中,衍生操作方法同标准曲线,最后进样0.01 mL,于液相色谱仪分析定量,以保留时间定性,峰面积定量。
1.5 空白测定取空白蒸馏液或纯净水5.00 mL于10 mL离心管中,衍生操作方法同标准曲线,最后进样0.01 mL,于液相色谱仪分析定量,衍生化后样品、衍生化后标样必须扣除空白样品中衍生产物。
1.6 质量控制本方法做了工作曲线、空白试验、平行样的测定及加标回收等试验,工作曲线的线性范围为0~8.00 μg/mL,相关系数r=0.9998,最低检出限0.01 μg,加标回收率为91.0%~101.5%, 精密度为0.9%~2.6%,质量控制均符合《全国疾病控制机构工作规范》(2001版)[7]的要求。
2 结果与讨论 2.1 衍生化时间和温度的影响分别在40℃、50℃、60℃的水浴条件下衍生20、40、60 min后测定标准曲线的峰面积(表 1)。40℃的水浴60 min内衍生化反应一直在进行,反应不完全;50℃的水浴40 min及在60℃水浴20 min的衍生化反应均已基本完全。本文采用在60℃的水浴衍生20 min的条件来加快检测速度、提高工作效率。
2.2 衍生物的稳定性
在衍生反应完成后,将各标准点衍生液和样品衍生液在25℃室温放置5 min、30 min、1 h、2 h、6 h,以评价衍生物的稳定性。实验结果表明,各标准点和样品的峰面积在6 h内的变异系数<5%(表 2), 说明衍生物在室温下就能保持良好的稳定性。
| 样品 | 5 (min) (峰面积) |
30 (min) (峰面积) |
1 (h) (峰面积) |
2 (h) (峰面积) |
6 (h) (峰面积) |
变异系数RSD(%) |
| 标准衍生液 | 215 941 | 216 007 | 213 894 | 214 865 | 215 113 | 0.40 |
| 样品衍生液 | 89 561 | 90 171 | 91 236 | 86 963 | 88 169 | 1.88 |
2.3 提取液的选择
甲醛在酸性条件下与衍生剂在水浴中衍生成脂溶性苯腙类化合物[8]。根据其化学特性,可以采用石油醚、正己烷、环己烷等非极性有机溶剂进行提取,其中环己烷是毒性相对较小的试剂,所以本文用环己烷作为提取液。
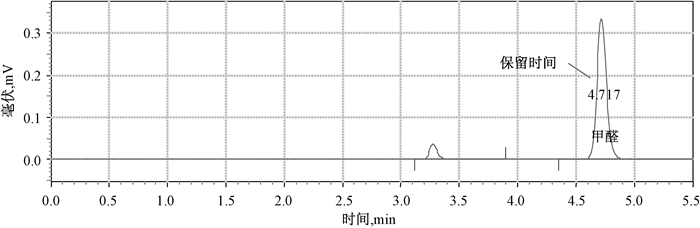
2.4 色谱条件的选择实验证明,在采用XDB C18不锈钢柱(250 mm× 4.6 mm,5 μm)作为固定相,乙腈:水=62:38作为流动相的条件下甲醛的衍生物能达到很好的基线分离,峰型良好,保留时间适中,标准色谱图见图 1。
|
| 图 1 甲醛标准衍生物色谱图 |
2.5 线性范围与检出限
本实验甲醛在0~8.00 μg/mL浓度范围内,各标准点的进样浓度与衍生产物的峰面积显良好的线性关系,相关系数r=0.999 8。以噪声的3倍计算,甲醛最低检出限0.01 μg,取5.00 mL甲醛标准使用溶液(20.00 μg/mL)衍生后测定计算,最低检出浓度为0.002 mg/L, 最低检测浓度时0.006 mg/L。
2.6 精密度、准确度和回收率实验按本文方法随机检测99份包装材料中的甲醛,每份浸泡液进行6次平行样品测定,计算RSD值,结果表明甲醛的RSD为0.9%~2.6%。另随机抽取有代表性样品各3份分别加入高浓度和低浓度的甲醛标准,将每份样品中加标量与本底值相近的数据统计并计算加标回收率,试验结果表明甲醛回收率为91.0%~101.5%(表 3)。
| 样品 (号) |
本底值 (μg) |
加标量 (μg) |
测定值 (μg) |
回收率 (%) |
| 1 | 0.103 | 0.20 | 0.297 | 97.0 |
| 2 | 0.248 | 0.20 | 0.436 | 94.0 |
| 3 | 0.810 | 1.00 | 1.788 | 97.8 |
| 4 | 0.367 | 0.20 | 0.549 | 91.0 |
| 5 | 0.191 | 0.20 | 0.386 | 97.5 |
| 6 | 0.685 | 1.00 | 1.688 | 100.3 |
| 7 | 0.554 | 0.20 | 0.750 | 98.0 |
| 8 | 0.416 | 0.20 | 0.607 | 95.5 |
| 9 | 0.490 | 0.20 | 0.693 | 101.5 |
| 10 | 0.871 | 1.00 | 1.874 | 100.3 |
2.7 干扰试验
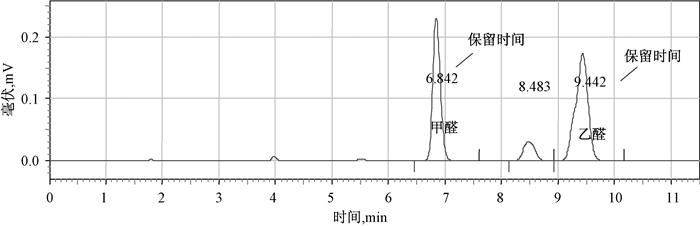
本实验将甲醛、乙醛配成混和的标准溶液,按本方法操作,未发现乙醛对甲醛有干扰(图 2)。
|
| 图 2 甲醛、乙醛标准衍生物色谱图 |
3 小结
本方法采用DNPH柱前衍生法,液相色谱仪分析定量,不但具有灵敏度高、选择性好、精密度和准确度好等优点,而且简便、快捷,适合分析大批量的检测工作。
| [1] | 中华人民共和国卫生部. GB/T 5009. 69-2008食品罐头内壁环氧酚醛涂料卫生标准的分析方法[S]. 北京: 中国标准出版社, 2008. |
| [2] | 中华人民共和国卫生部. GB/T 5009. 61-2003食品包装用三聚氰胺成型品卫生标准的分析方法[S]. 北京: 中国标准出版社, 2003. |
| [3] | 中华人民共和国卫生部GB/T 5009. 178-2003食品包装材料中甲醛的测定[S]. 北京: 中国标准出版社, 2003. |
| [4] | 黄惠玲, 何莺, 王玉健, 等. 气相色谱测定食品包装材料中微量甲醛[J]. 分析实验室, 2009, 28(5): 203–205. |
| [5] | 吕春华, 陈梅, 陈笑梅, 等. 衍生液提取-高效液相色谱法测定食品中甲醛[J]. 理化检验-化学分册, 2011, 47(5): 1005–1008. |
| [6] | 陈笑梅, 施旭霞, 朱卫健, 等. 高效液相色谱直接测定甲醛衍生物反应条件的研究[J]. 分析化学, 2004, 32(11): 1489–1491. doi: 10.3321/j.issn:0253-3820.2004.11.017 |
| [7] | 卫生部办公厅, 全国疾病预防控制机构工作规范(2001版)[M]. 2002, 248. |
| [8] | 武耐英, 高伟, 马淮凌. 衍生气相色谱法测定水产品中的甲醛含量[J]. 商丘师范学院学报, 2010, 26(9): 69–72. |

