2. 华侨大学土木工程学院, 厦门 361021
2. College of Civil Engineering, Huaqiao University, Xiamen 361021
双金属氧化物作为催化剂时,由于双金属之间协同作用可提高催化剂的活性(Cheng et al,2012;Wang et al,2015),同时可减少金属离子溶出(Deng et al.,2013). Strlič等(2003)以过渡金属作为类Fenton试剂,发现Cu(Ⅱ)/H2O2体系比其它过渡金属体系更容易产生羟基自由基(·OH).Gao等(2014)合成了Cu掺杂的Bi2WO6,发现Cu掺杂不仅增强了Bi2WO6对可见光的吸收性能,而且有效抑制了电子-空穴对的复合,使得可见光下对苯酚的去除效率显著提高. Bian等(2014)研究发现,Cu掺杂使BiVO4的能带带隙变窄,重复使用过程中具有良好的稳定性. Shen等(2012)采用水热法合成了α-(Fe,Cu)OOH纳米线,但水热法对设备要求高,规模化应用受限,若能在常压下一步回流合成α-(Fe,Cu)OOH,则容易实现批量制备,为材料推广应用提供便利.
环丙沙星(CIP)是第三代喹诺酮类广谱抗菌药物,被广泛用于人、畜疾病的治疗,这可能诱致细菌产生耐药性;同时,CIP对非目标生物具有一定的环境毒性,在环境中残留的低浓度CIP扩散可对人类健康和生态系统安全构成威胁(De Bel et al.,2009).研究发现,CIP具有难生物降解性(Adjei et al,2006),常规的水处理工艺对CIP去除能力有限,它在不同水体中被频繁检出,如饮用水源、地下水体、地表水体.因此,去除水环境中的CIP已成为亟待解决的问题.目前,人们多采用高级氧化技术中的臭氧氧化、光催化、光解、光助Fenton等方法处理含CIP废水.其中,光助异相类Fenton体系能够产生以羟基自由基为主的活性氧化物种,能够有效降解水体中的有机物(Mackuíak et al,2015).
本文采用一步回流法在常压下成功合成Cu掺杂α-FeOOH,并以卤钨灯为可见光光源,以该双金属氧化物为类Fenton试剂催化过氧化氢去除难生物降解的CIP,研究溶液初始pH值、催化剂投加量和过氧化氢投加量等对CIP去除率的影响及催化剂的重复使用性能.
2 材料与方法(Materials and methods) 2.1 实验仪器X′Pert Pro型X射线粉末衍射仪(XRD)(荷兰帕纳科公司);S4800型场发射扫描电子显微镜(SEM),并配备Genesis XM2型X射线探测能谱仪(EDX)(日本日立公司);Nicolet Is10型傅里叶红外光谱仪(FT-IR)(美国热电公司);1260型高效液相色谱仪(HPLC)(美国Ailigent公司);UV-2450型紫外光谱仪(UV-vis DRS)(日本岛津公司); ESCALAB 250型的X射线光电子能谱仪(XPS)(美国赛默飞世尔科技公司);F-4600型的荧光光谱仪(日本日立公司).
2.2 催化剂制备先称取5.56 g FeSO4·7H2O溶于水/乙醇中,然后加入1.20 g尿素持续搅拌10 min,再加入0.15 g CuSO4·5H2O溶解均匀,倒入三口烧瓶置于集热式恒温加热磁力搅拌器中,反应温度缓慢升温至90 ℃持续反应6 h,自然冷却至室温,离心洗涤烘干后制得α-(Fe,Cu)OOH.
2.3 催化降解CIP实验量取浓度为30 mg·L-1的CIP标准溶液于锥形瓶中,称取一定量的催化剂放入标准溶液中,吸附达到平衡后将溶液转入石英烧杯,置于装有500 W卤钨灯的光反应器中(组合滤光片过滤得到波长为420 nm < λ <800 nm的可见光),开启光照的同时加入过氧化氢,一定时间间隔取样. 采用HPLC测定CIP的浓度,计算其去除率. CIP的HPLC测定条件:L-2455二极管阵列检测器,反相C18液相色谱柱(XB C185 μm×4.6 mm×250 mm);流动相为20%乙腈+80%磷酸盐溶液,进样量20 μL;流速1.0 mL·min-1,柱温30 ℃,紫外检测波长278 nm.
2.4 羟基自由基的测定称取一定量的催化剂放入含有0.01 mol·L-1氢氧化钠的3 mmol·L-1对苯二甲酸溶液中,吸附平衡后取样. 水样置于荧光光谱仪中,以波长为313 nm的光进行激发,测定2-羟基对苯二甲酸的荧光光谱信号.
3 结果与讨论(Results and discussion) 3.1 α-(Fe,Cu)OOH的表征分析α-(Fe,Cu)OOH的XRD图谱见图 1,图中2θ=17.80°、21.22°、26.32°、33.24°、34.70°、36.65°、41.19°等处的衍射峰分别与α-FeOOH衍射峰位置一致,没有其它明显杂质峰,也没有出现Cu 物种的衍射峰,表明Cu掺入α-FeOOH晶格中形成α-(Fe,Cu)OOH或呈高度分散状态(Wu et al,2004;Shi et al,2009). Fe2+和Cu2+所带电荷相同,它们的离子半径相差不大(分别为0.074和0.073 nm),Cu2+在结晶阶段容易取代α-FeOOH中的Fe3+形成α-(Fe,Cu)OOH(Shen et al,2012;Tian et al,2014). α-(Fe,Cu)OOH的微观形貌如图 2a所示,催化剂呈纳米棒自组装形成三维花状结构,纳米棒的长度在200~300 nm范围内,直径在30~50 nm范围内;通过EDX(图 2b)分析可知,α-(Fe,Cu)OOH中Cu的质量分数为5.25%.红外光谱进一步分析了催化剂组成元素的键合状态,结果如图 3所示.由图 3可知,波数为619、796、895 cm-1处为Fe—O、Fe—OH—Fe的特征吸收峰(Li et al,2012;Chen et al,2011),波数为1348、637 cm-1处为Cu—O特征吸收峰(Nie et al.,2009).比表面积测试表明,α-(Fe,Cu)OOH的比表面积为75.03 m2·g-1.
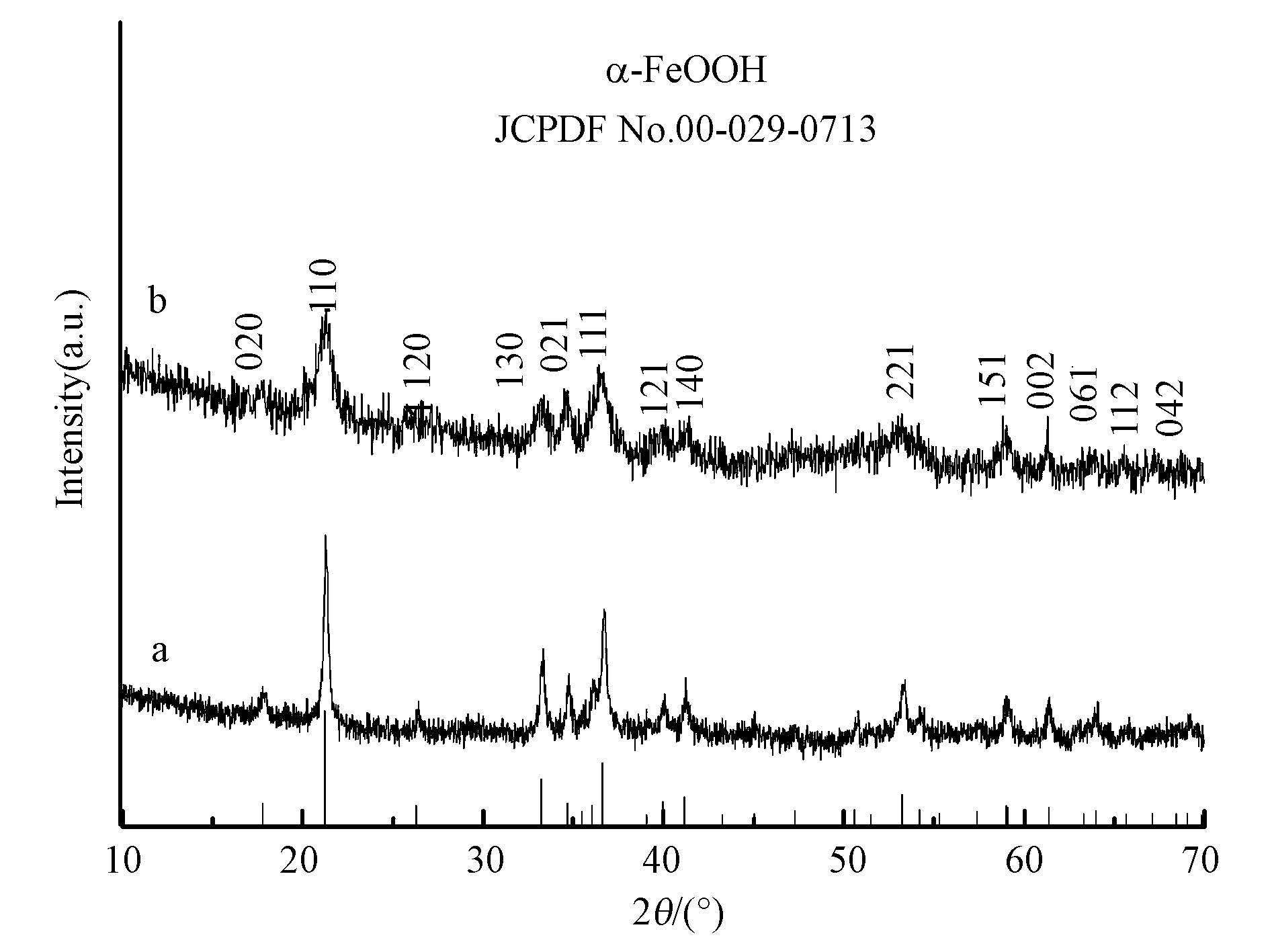 |
| 图 1 催化剂α-FeOOH(a)和α-(Fe,Cu)OOH(b)的XRD图 Fig. 1 XRD patterns of α-FeOOH(a)and α-(Fe,Cu)OOH(b) |
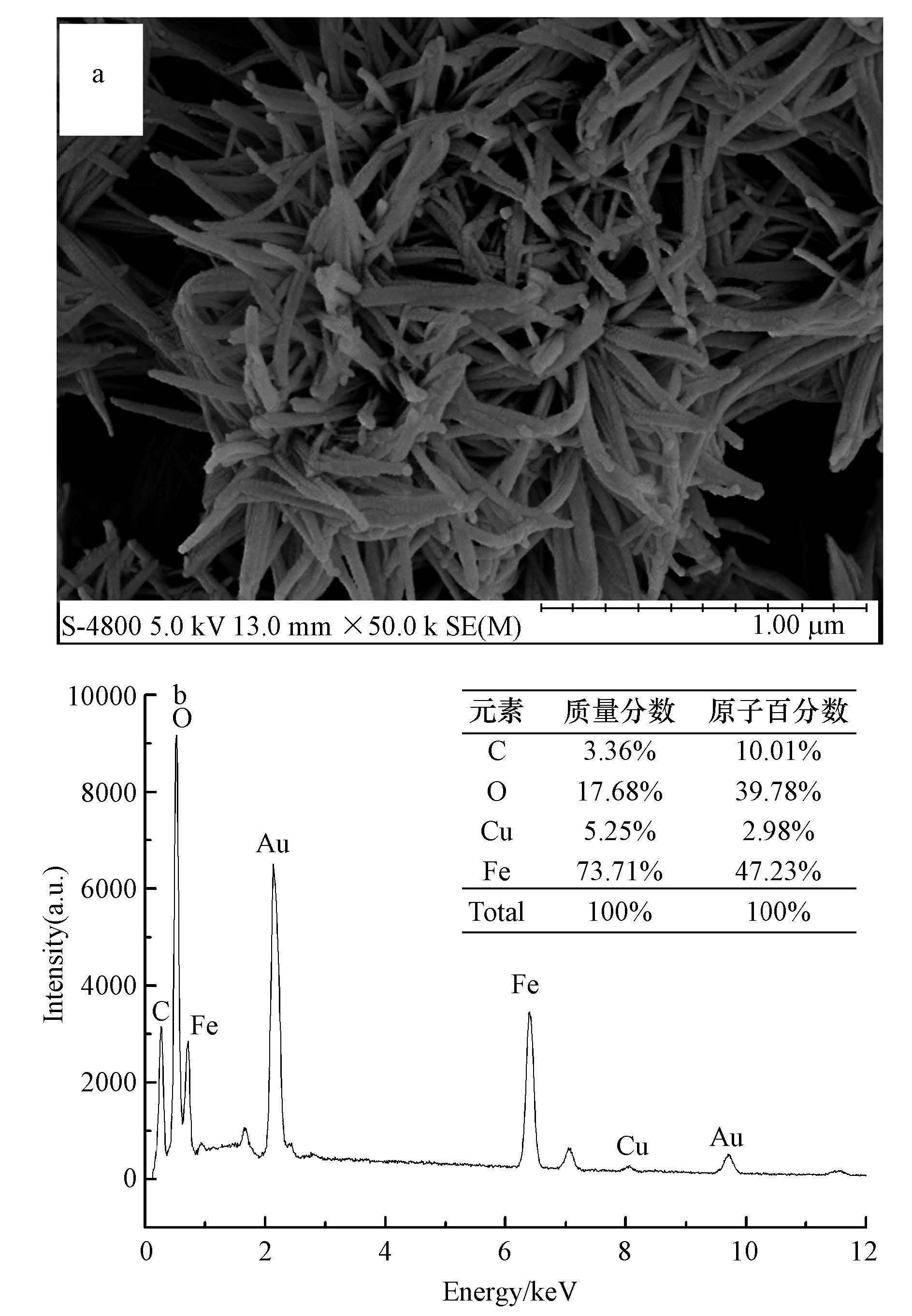 |
| 图 2 催化剂α-(Fe,Cu)OOH的SEM图(a)和EDX图(b) Fig. 2 SEM image(a)and EDX spectrum(b)of α-(Fe,Cu)OOH |
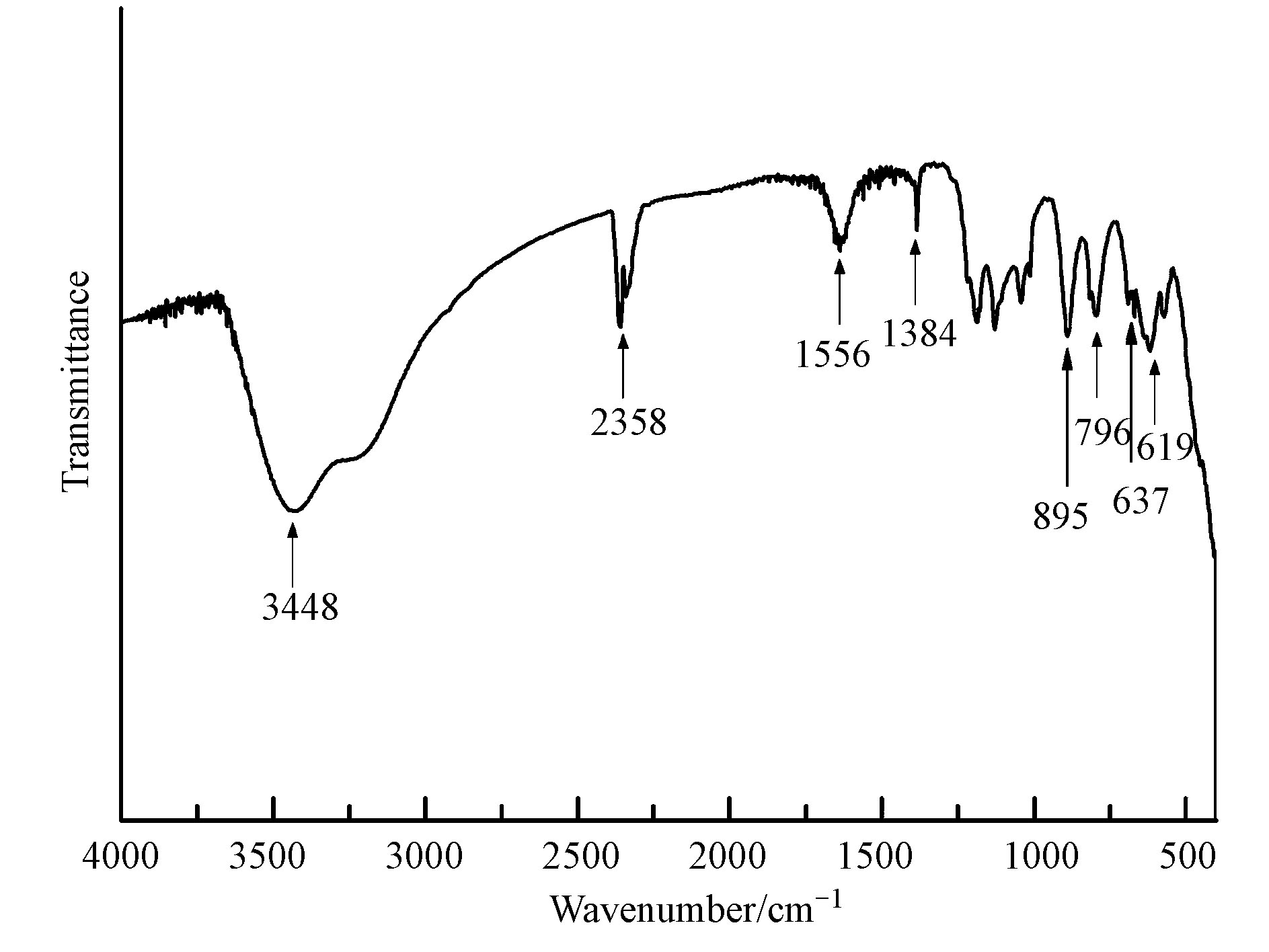 |
| 图 3 α-(Fe,Cu)OOH的红外光谱图 Fig. 3 FT-IR spectrum of α-(Fe,Cu)OOH |
为考察催化剂 α-(Fe,Cu)OOH的光学性质,在200~800 nm波长范围内进行UV-Vis DRS分析,结果如图 4所示.由图可知,Cu掺杂后催化剂对可见光的吸收能力比掺杂前增强,这归结为Fe3+的eα g→eβ g和tα 2g→tα 2g存在“自旋反转”配位场转换,α-(Fe,Cu)OOH在270~450 nm范围内有较强的吸收(Krehula et al,2013);Cu2+的d-d跃迁能量比Fe3+低(Yang et al,2014),Cu替代Fe进入α-FeOOH内部时,α-(Fe,Cu)OOH的配位场向较低能量区转换,即在可见光区域光吸收边向长波长移动. 因此,Cu掺杂利于提高α-FeOOH对可见光的吸收.
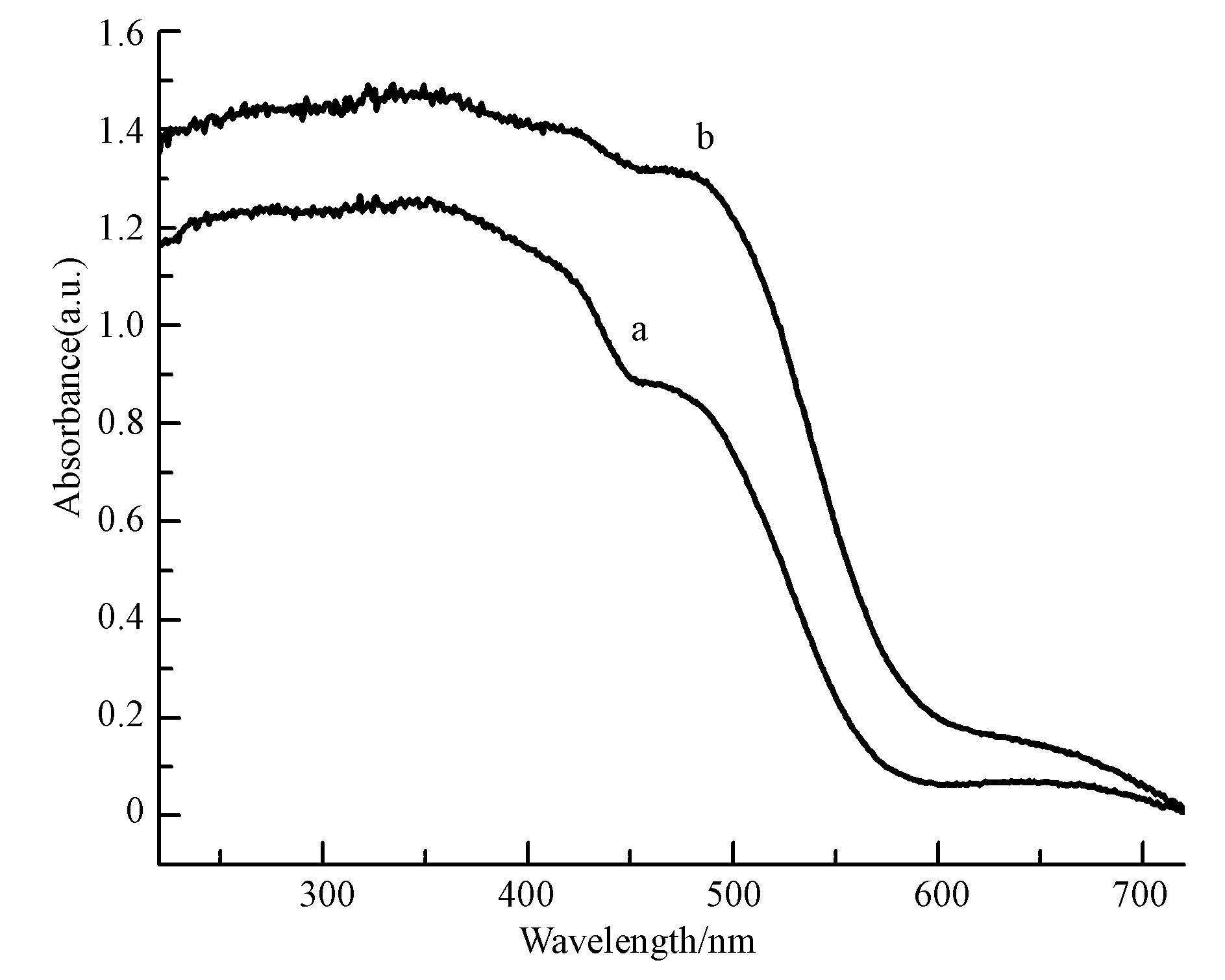 |
| 图 4 α-FeOOH(a)和α-(Fe,Cu)OOH(b)的紫外-可见漫反射图 Fig. 4 UV-Vis DRS spectra of α-FeOOH(a)and α-(Fe,Cu)OOH(b) |
α-(Fe,Cu)OOH的XPS谱图如图 5所示,Cu 2p3/2的XPS光谱中,935.2 eV处的峰对应于Cu2+物种,而出现在933.4 eV处的峰对应于Cu+物种,表明催化剂中同时存在Cu+和Cu2+物种(Nie et al,2009;Yang et al,2006). Fe 2p的XPS光谱中,Fe 2p3/2的XPS光谱拟合结果中可清楚地观察到位于711.2和713.0 eV处的峰,表明催化剂中的Fe以Fe2+和Fe3+呈现;Fe 2p1/2的峰分别对应于724.0和726.3 eV处的Fe2+和Fe3+;位于717.8 eV处的峰表示Fe 2p3/2振动峰的出现(Zhang et al,2014;Bukhtiyarova et al,2009).
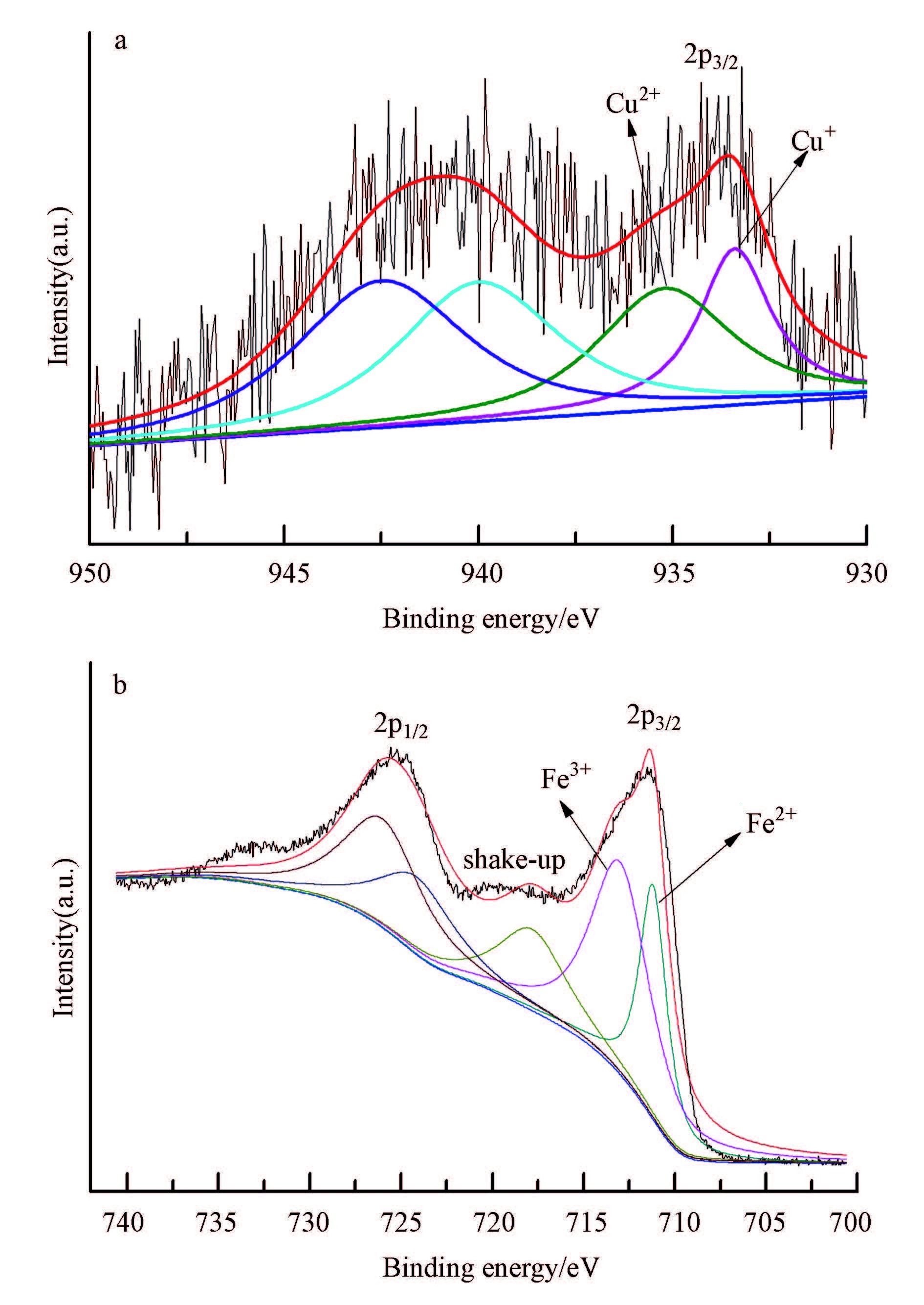 |
| 图 5 催化剂α-(Fe,Cu)OOH的XPS图谱(a.Cu 2p,b.Fe 2p) Fig. 5 XPS spectra of α-(Fe,Cu)OOH(a.Cu 2p,b.Fe 2p) |
α-(Fe,Cu)OOH用于光助异相Fenton体系中去除CIP实验中,氧化剂H2O2是在吸附饱和后进行的. 先加入α-(Fe,Cu)OOH吸附平衡后,再加氧化剂H2O2进行降解. 催化剂α-(Fe,Cu)OOH对CIP的吸附性能如图 6所示,吸附3 h时基本达到平衡,即溶液中CIP的浓度随时间不再发生明显变化,此时α-(Fe,Cu)OOH对CIP的吸附去除率约11.9%.
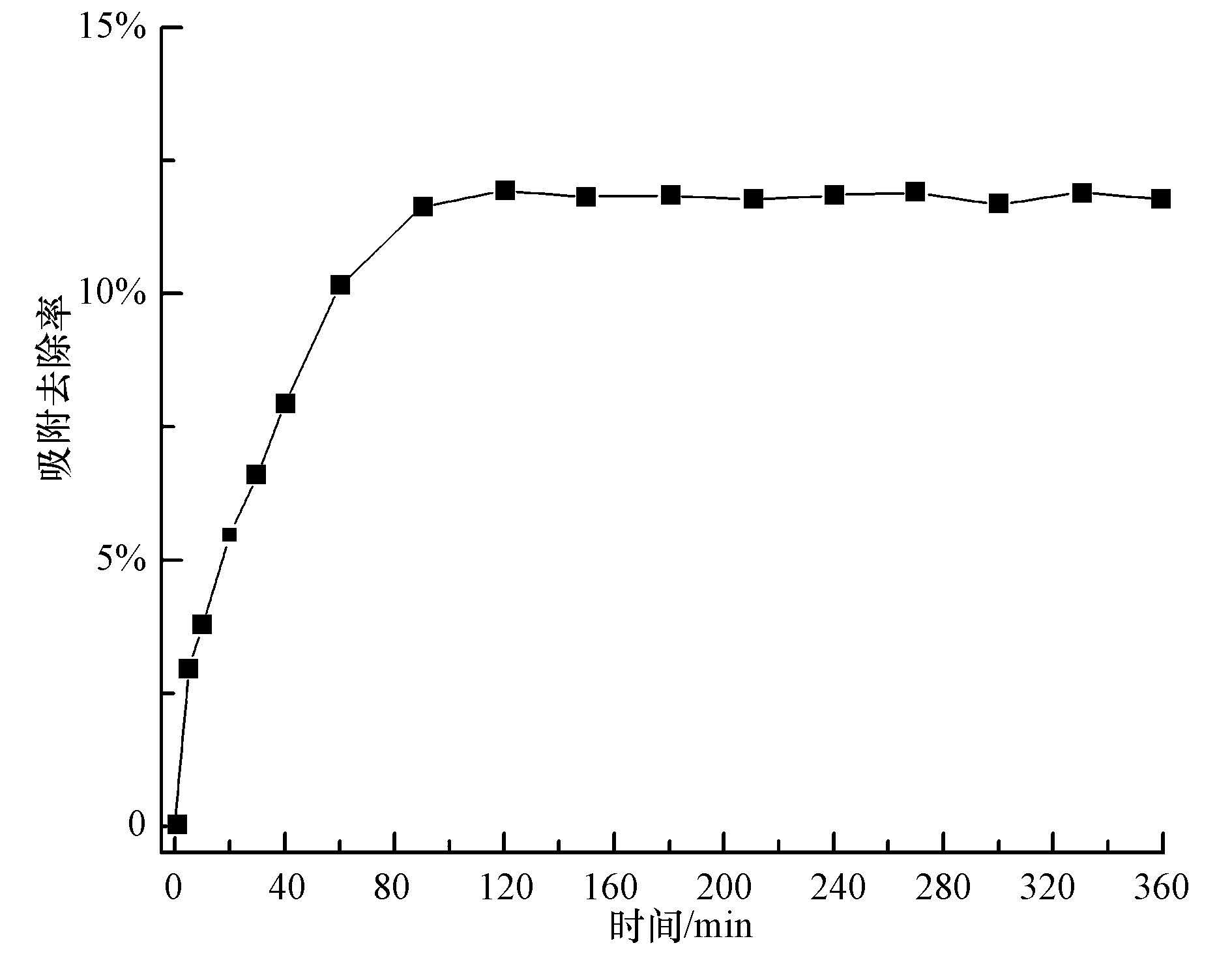 |
| 图 6 α-(Fe,Cu)OOH对CIP的吸附曲线 Fig. 6 Adsorption curve of CIP over α-(Fe,Cu)OOH under darkness |
为考察α-(Fe,Cu)OOH在光助异相Fenton体系中的催化效能,在催化剂投加量为0.40 g·L-1,H2O2浓度为0.10 mol·L-1时,对比不同反应体系对CIP的去除效果,结果如图 7所示.由图 7可知,α-FeOOH/H2O2体系对CIP的去除效率仅为30%,α-(Fe,Cu)OOH/H2O2体系对CIP的去除效率为60%,光助α-FeOOH/H2O2体系对CIP的去除效率为58%;光助α-(Fe,Cu)OOH/H2O2体系对CIP的去除率可达90%以上.结果表明,Cu掺杂提高了α-FeOOH的催化活性,使得α-(Fe,Cu)OOH/H2O2和光助α-(Fe,Cu)OOH/H2O2体系对CIP去除效率分别明显高于α-FeOOH/H2O2和光助α-FeOOH/H2O2体系.
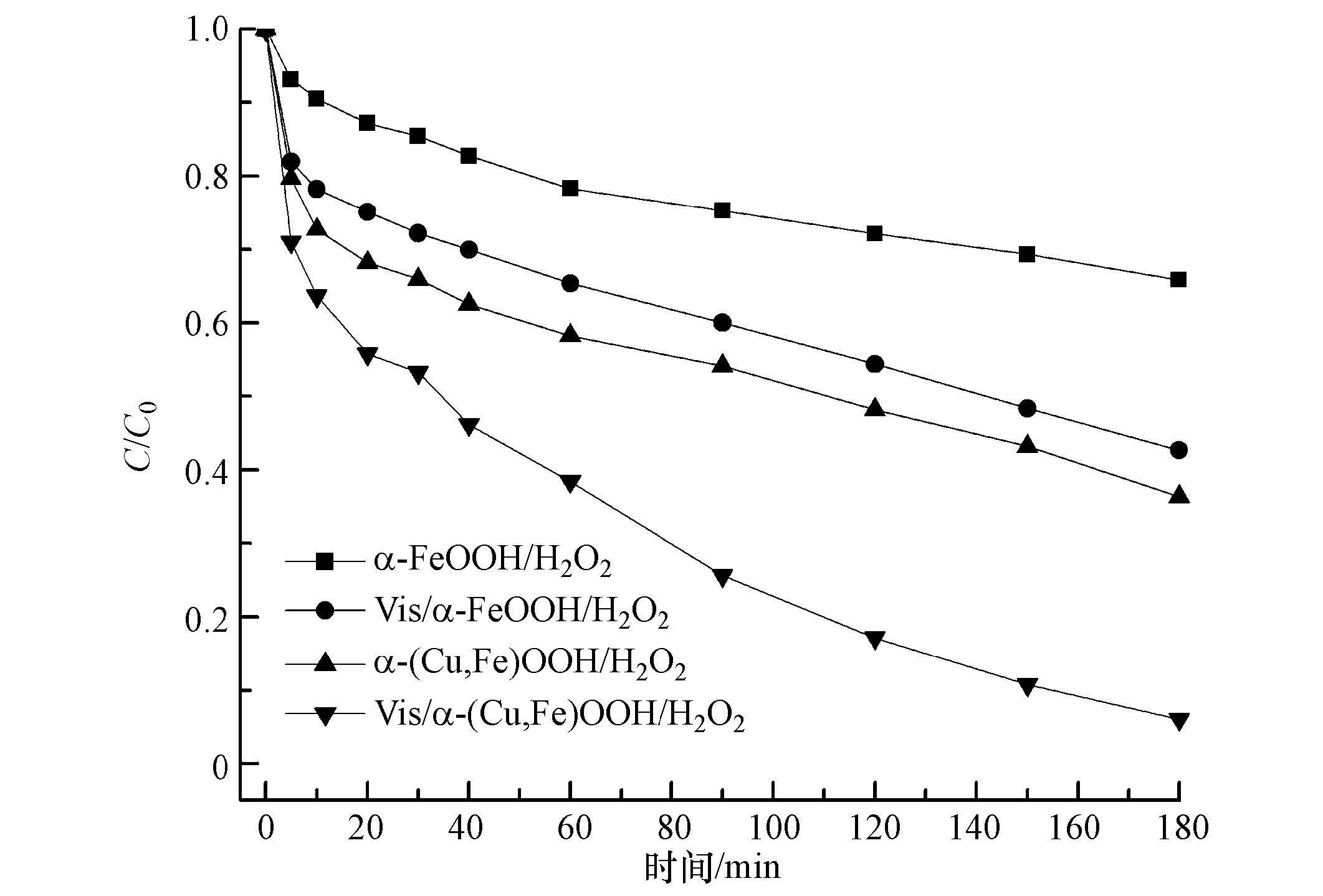 |
| 图 7 不同反应体系对CIP的去除效率 Fig. 7 Removal efficiency of CIP in different reaction systems |
溶液初始pH值是影响目标污染物去除率的重要因素,而污染物的去除率包括吸附去除率和降解去除率. 研究发现,CIP存在几个酸碱点,CIP在不同的溶液pH值下电离常数也不同,存在阳离子、中性分子和阴离子3种形态(Van Doorslaer et al,2011).
溶液初始pH值对CIP吸附去除率的影响如图 8a所示,可见,CIP的吸附去除率随溶液pH值的升高呈现先升高后降低的趋势. 溶液pH值通过质子化和去质子化作用影响CIP的表面电荷性质,不同pH值下催化剂表面所带电荷不同,进而影响CIP的吸附去除率. 溶液初始pH值对CIP降解去除率的影响如图 8b所示,pH=5时CIP降解去除速率最高,CIP质子化带正电与催化剂表面带的正电荷之间电性相斥,难以被吸附在催化剂表面,但较高的H+浓度仍促使·OH的生成(Zhang et al,2015);pH=6~8时催化剂和CIP之间保持电中性,CIP与催化剂表面所交互过程温和,CIP的降解速率变化不大;pH=9时哌嗪环基团去质子化,CIP阴离子与催化剂表面带负电荷之间虽电性相斥,但CIP分子中哌嗪环的活性部位的电离使pH=9时的降解速率大于pH=8时,这与文献报道中的结果相一致(De Bel et al,2009;Zhang et al,2015).结果表明,溶液pH值通过影响CIP官能团的电离常数和催化剂表面所带电荷,进而影响催化剂对CIP的降解去除率.
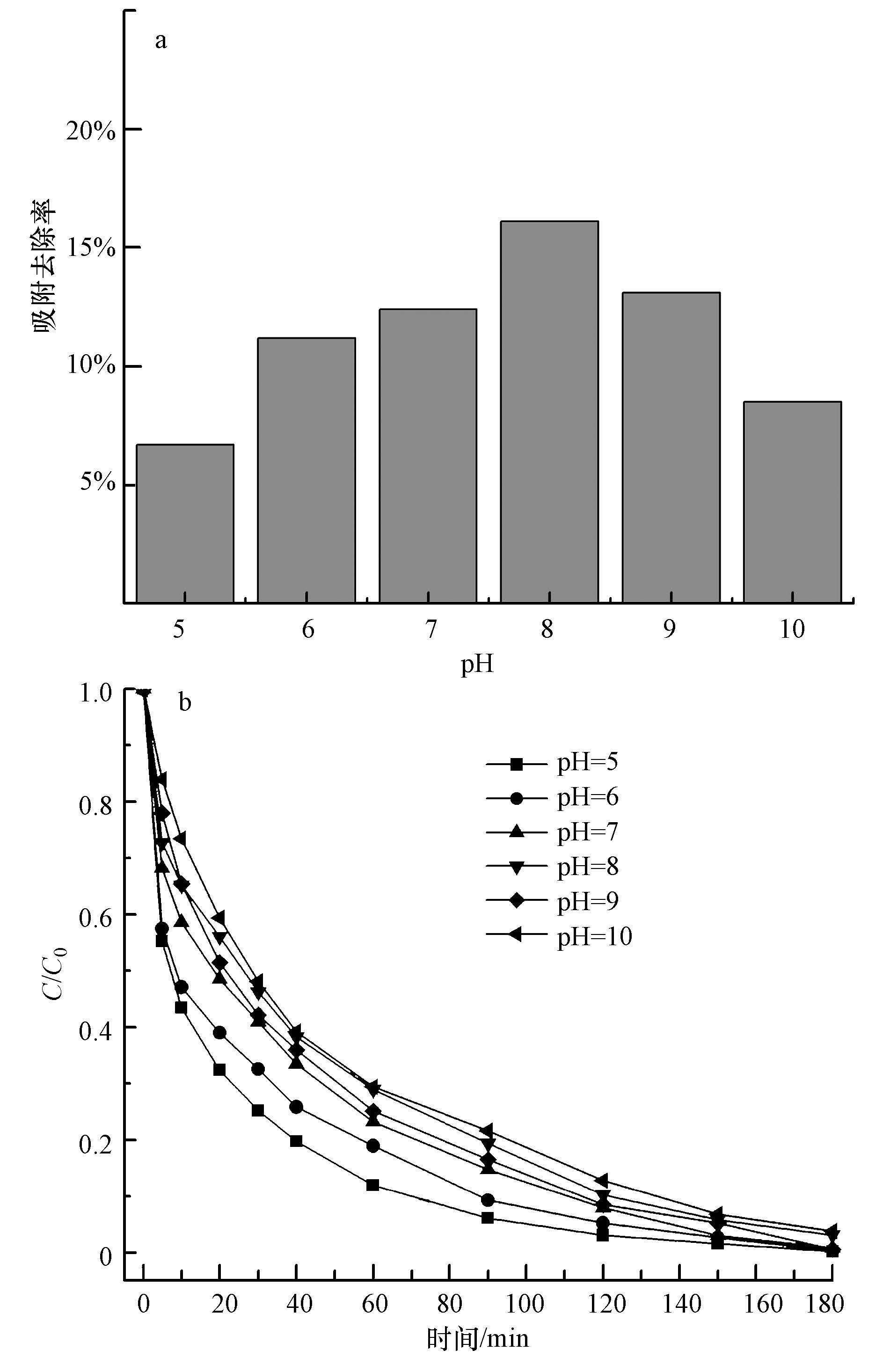 |
| 图 8 pH值对CIP吸附(a)和降解(b)的影响 Fig. 8 Effects on CIP adsorption(a)and catalytic degradation(b)at different initial pH of solution |
催化剂投加量是影响CIP去除效率的一个主要因素.在催化剂投加量分别为0.20、0.40、0.60、0.80 g·L-1时,可见光下催化0.10 mol·L-1的H2O2对CIP去除率的影响如图 9a所示. 由图可知,CIP去除率随催化剂投加量的增大而升高,这主要是因为催化活性物种的生成概率和数量随催化剂投加量升高而增多,CIP与催化剂总接触表面积几率增大,容易被吸附在催化剂表面,进而被活性物种降解.投加量为0.60和0.80 g·L-1时,CIP初始反应速率和去除率相差不大,这主要是因为CIP的浓度是固定的,当催化剂投加增大到一定程度时,其表面不能吸附足够的污染物,将影响体系初始反应速率的进一步提高.故综合考虑催化剂成本和CIP去除率因素,最佳投加量选定为0.60 g·L-1.
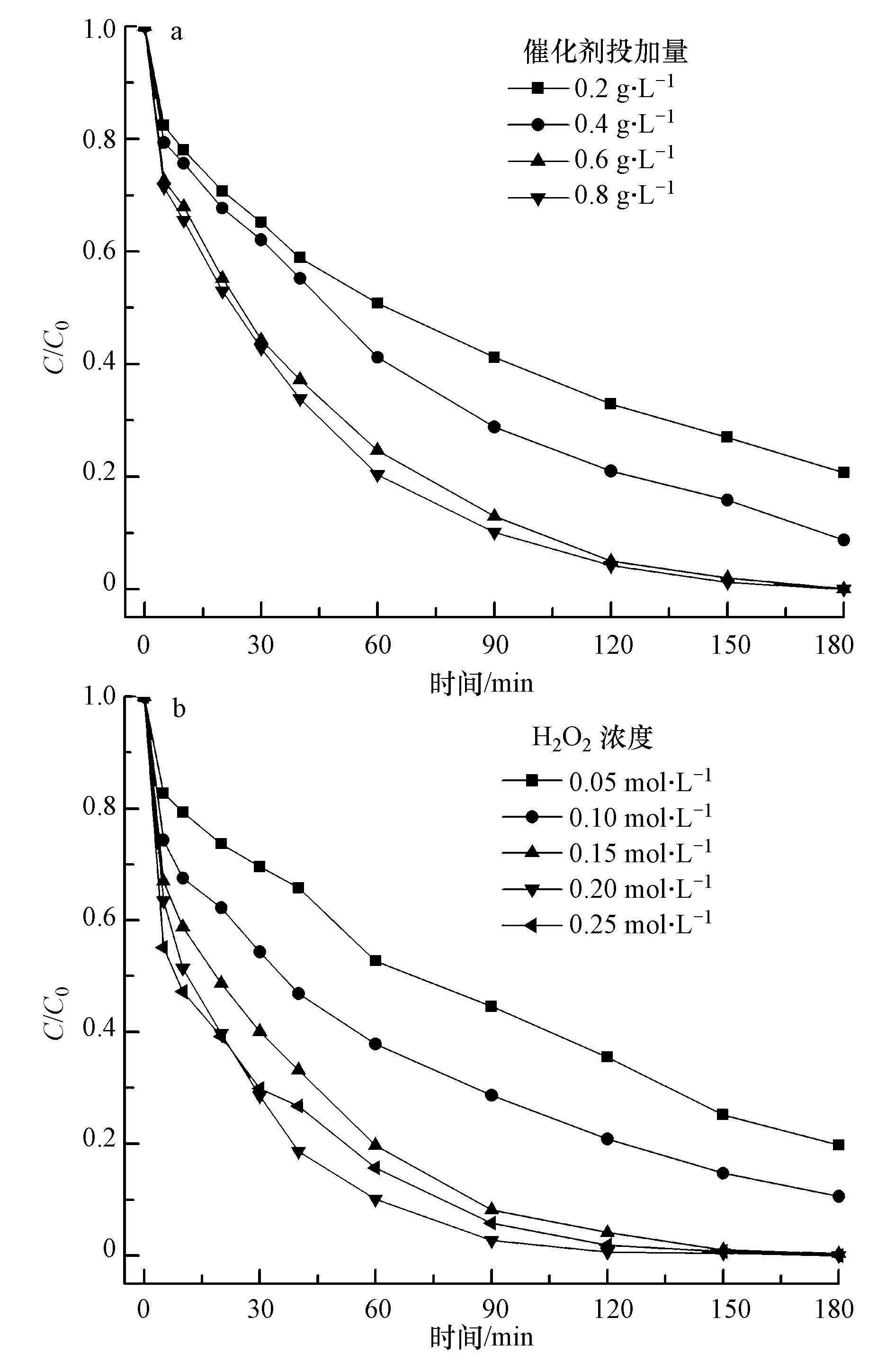 |
| 图 9 催化剂加量(a)和H2O2浓度(b)对CIP去除率的影响 Fig. 9 Effects on the removal of CIP at different catalyst dosages(a)and different H2O2 concentrations(b) |
催化剂投加量固定为0.60 g·L-1,H2O2浓度对CIP去除率的影响如图 9b所示.可见,当H2O2浓度为0.05 mol·L-1时,CIP去除率约为80%;当H2O2浓度为0.10 mol·L-1时,CIP的去除率为90%;当H2O2浓度为0.15 mol·L-1时,CIP的去除率可达99%以上;当H2O2浓度增至0.25 mol·L-1时,反应初始速率增大,反应150 min时CIP就被全部去除.从实际应用成本角度考虑,H2O2的最佳浓度选定为0.15 mol·L-1.
3.5 催化剂的重复使用性能为进一步考察α-(Fe,Cu)OOH的循环使用性能,设定催化剂投加量为0.60 g·L-1,过氧化氢浓度为0.15 mol·L-1,反应180 min后对催化剂进行离心、洗涤、烘干回收,5次重复试验结果如图 10所示.由图可知,随着循环次数的增多,催化剂对CIP去除率仍保持在90%左右.测定光助α-FeOOH/H2O2和α-(Fe,Cu)OOH/H2O2体系反应过程的铁溶出情况,前者铁溶出的最大浓度为0.40 mg·L-1,后者最大浓度为0.19 mg·L-1,表明Cu掺杂抑制铁溶出.因此,Cu掺杂提高了α-FeOOH的稳定性(Wang et al,2013).
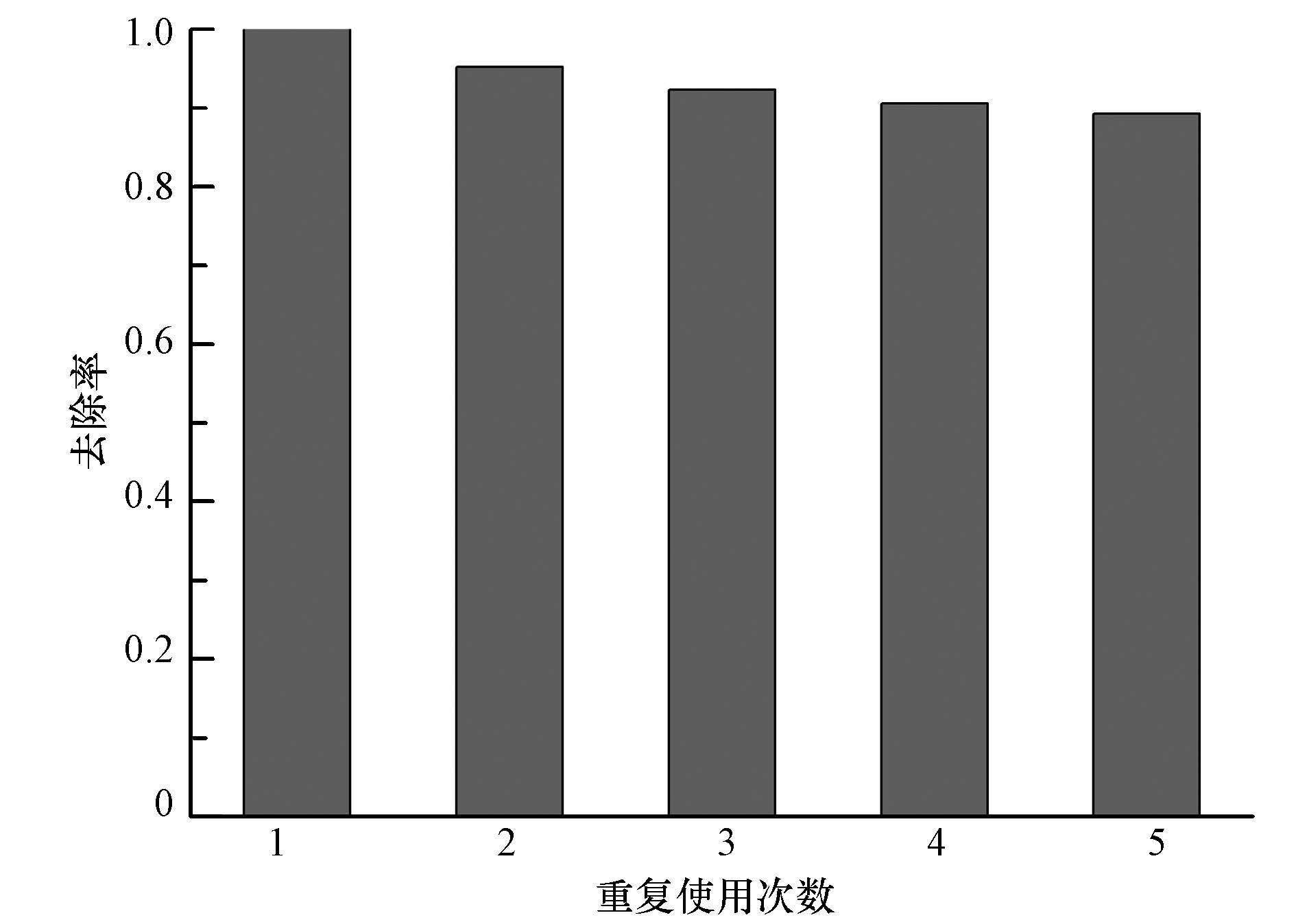 |
| 图 10 催化剂α-(Fe,Cu)OOH的重复使用效果 Fig. 10 Reusability of α-FeOOH as catalyst for degradation of CIP |
通过向可见光助α-(Fe,Cu)OOH/H2O2体系中加入·OH捕获剂-叔丁醇,推测光助异相类Fenton降解CIP过程中的重要活性氧化物种是否为·OH.由图 11可知,CIP去除率随着叔丁醇浓度的升高而降低,当叔丁醇浓度为0.15 mol·L-1时,CIP去除率降低了23%左右;当叔丁醇浓度增至0.30 mol·L-1时,CIP去除率降低了36%左右.结果表明,可见光助α-(Fe,Cu)OOH/H2O2体系中是以·OH作为重要的氧化活性基团参与反应.
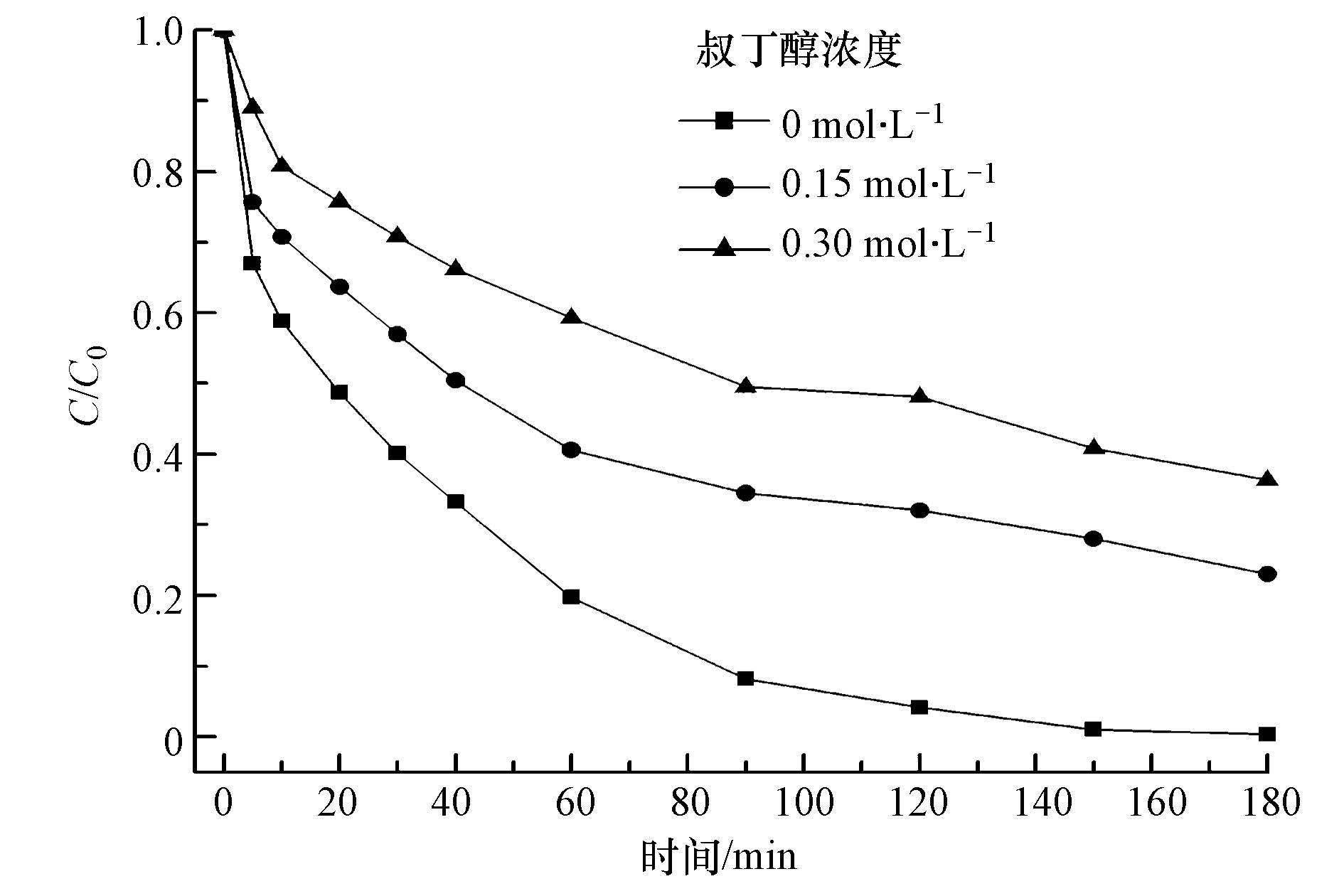 |
| 图 11 叔丁醇对CIP去除效果的影响 Fig. 11 Effects on the removal of CIP at different tertiary butanol concentrations |
采用分子荧光光度法测定各反应体系中·OH产生量的变化,结果如图 12所示.反应体系中生成产物的荧光强度均随反应时间延长而逐渐增强,表明·OH总量随反应时间延长而增加(Sheydaei et al,2014;Liu et al,2013),光助异相类Fenton体系遵从·OH反应机理.光助α-FeOOH/H2O2体系中·OH的生成量较少,光助α-(Fe,Cu)OOH/H2O2体系中·OH生成速率快,且生成量较多,表明Cu(Ⅱ)/Cu(I)不仅影响·OH的生成速率,而且影响·OH的生成量. 随着反应进行到慢反应阶段,光助α-(Fe,Cu)OOH/H2O2体系中·OH的生成速率仍高于α-FeOOH/H2O2反应体系,表明慢反应阶段Cu(I)与H2O2反应直接促进·OH生成;同时,Cu(I)还原Fe(Ⅲ)生成Fe(Ⅱ),改变体系中Fe(Ⅱ)的浓度,间接促进·OH的生成,这两方面协同提高了光助α-(Fe,Cu)OOH/H2O2体系中·OH的生成效率.
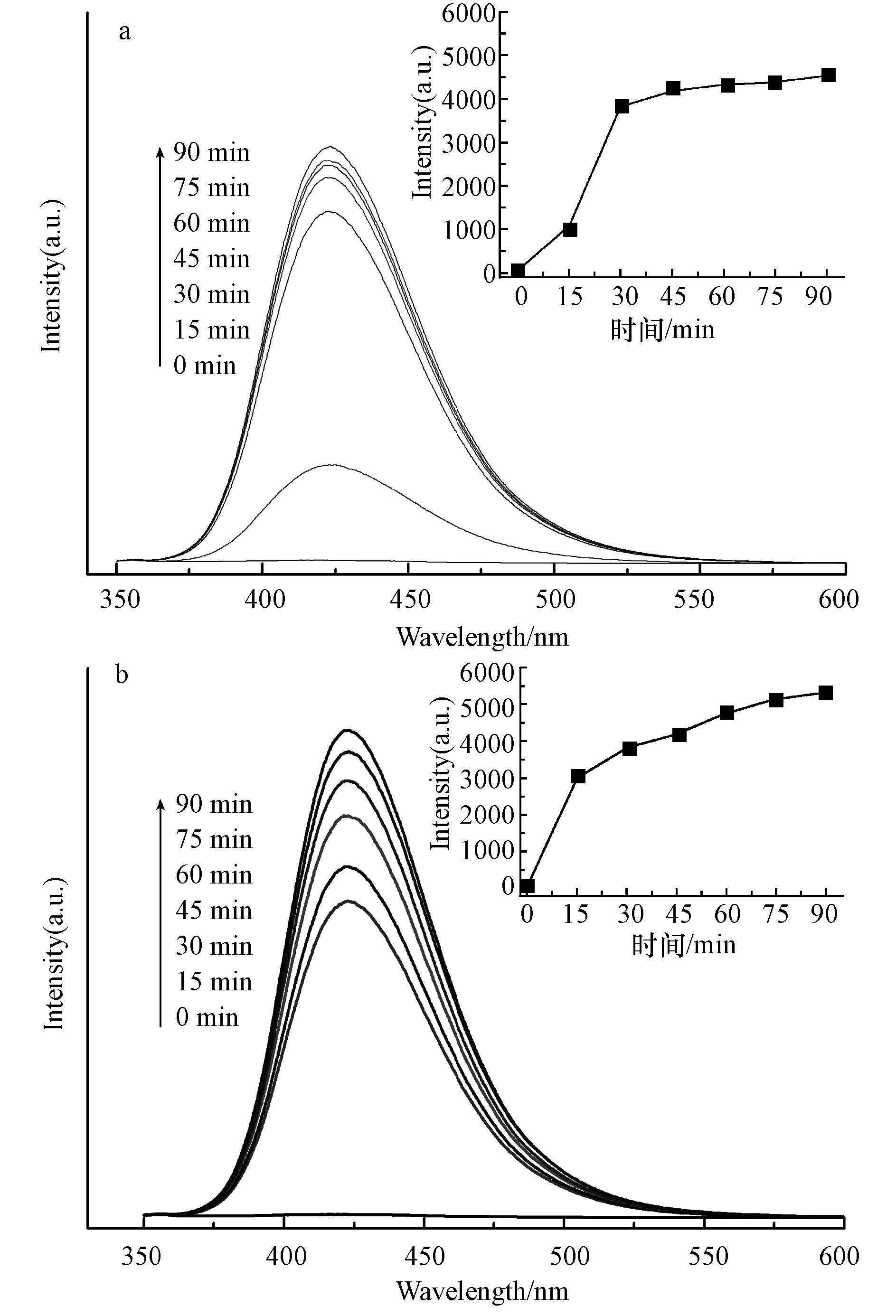 |
| 图 12 可见光助α-FeOOH/H2O2(a)和可见光助α-(Fe,Cu)OOH/H2O2(b)的·OH荧光光谱图和荧光信号强度变化图 Fig. 12 Fluorescence spectra of ·OH and fluorescence signal intensity variation ofvisible light/α-FeOOH/H2O2(a)and visible light/α-(Fe,Cu)OOH/H2O2(b)(the insets are the dependence of the fluorescence signal intensities(425 nm)against light illumination time for 2-hydroxy terephthalic acid) |
1) 通过一步回流法制得花状结构的α-(Fe,Cu)OOH,Cu掺杂未改变α-FeOOH的晶体结构,使α-FeOOH在可见光区域的光吸收边发生红移,具有良好的可见光响应效果.
2) 光助α-(Fe,Cu)OOH/H2O2降解CIP反应过程遵从·OH反应机理,其最佳反应条件为:α-(Fe,Cu)OOH投加量为0.60 g·L-1,H2O2投加浓度为0.15 mol·L-1,反应180 min,该条件下CIP被全部去除. Cu掺杂可有效抑制α-FeOOH的铁溶出;经5次循环后催化剂对CIP的去除率仍保持在90%左右,表明催化剂α-(Fe,Cu)OOH具有良好的稳定性.
| [1] | Adjei M D, Heinze T M, Deck J, et al. 2006. Transformation of the antibacterial agent norfloxacin by environmental mycobacteria[J]. Applied and Environmental Microbiology , 72 (9) : 5790–5793. DOI:10.1128/AEM.03032-05 |
| [2] | Bian Z Y, Zhu Y Q, Zhang J X, et al. 2014. Visible-light driven degradation of ibuprofen using abundant metal-loaded BiVO4 photocatalysts[J]. Chemosphere , 117 : 527–531. DOI:10.1016/j.chemosphere.2014.09.017 |
| [3] | Bukhtiyarova M V, Ivanova A S, Plyasova L M, et al. 2009. Selective catalytic reduction of nitrogen oxide by ammonia on Mn(Fe)-substituted Sr(La) aluminates[J]. Applied Catalysis A: General , 357 (2) : 193–205. DOI:10.1016/j.apcata.2009.01.028 |
| [4] | Cheng W, He J, Sun Z, et al. 2012. Ni-Doped overlayer hematite nanotube: A highly photoactive architecture for utilization of visible light[J]. The Journal of Physical Chemistry C , 116 (45) : 24060–24067. DOI:10.1021/jp306738e |
| [5] | Chen H F, Wei G D, Han X, et al. 2011. Large-scale synthesis of hierarchical α-FeOOH flowers by ultrasonic-assisted hydrothermal route[J]. Journal of Materials Science-Materials in Electronics , 22 (3) : 252–259. DOI:10.1007/s10854-010-0124-9 |
| [6] | Deng J, Shao Y, Gao N, et al. 2013. CoFe2O4 magnetic nanoparticles as a highly active heterogeneous catalyst of oxone for the degradation of diclofenac in water[J]. Journal of Hazardous Materials , 262 : 836–844. DOI:10.1016/j.jhazmat.2013.09.049 |
| [7] | De Bel E, Dewulf J, De Witte B, et al. 2009. Influence of pH on the sonolysis of ciprofloxacin: biodegradability,ecotoxicity and antibiotic activity of its degradation products[J]. Chemosphere , 77 (2) : 291–295. DOI:10.1016/j.chemosphere.2009.07.033 |
| [8] | Gao X M, Fu F, Li W H. 2014. 3D Hierarchical microspheres of Cu-doped Bi2WO6: Synthesis,characterization,and enhanced photocatalytic activity[J]. Journal of Materials Engineering and Performance , 23 (12) : 4342–4349. DOI:10.1007/s11665-014-1241-z |
| [9] | Krehula S, Krehula L K, Musić S. 2013. Synthesis and microstructural properties of α-Fe1-xGaxOOH solid solutions[J]. Journal of Alloys and Compounds , 581 : 335–343. DOI:10.1016/j.jallcom.2013.07.076 |
| [10] | Liu Z, Chen F, Fang P, et al. 2013. Study of adsorption-assisted photocatalytic oxidation of benzene with TiO2/SiO2 nanocomposites[J]. Applied Catalysis A: General , 451 : 120–126. DOI:10.1016/j.apcata.2012.11.020 |
| [11] | Li Z C, Guan M Y, Lou Z S, et al. 2012. Facile hydrothermal synthesis and electrochemical properties of flowerlike α-FeOOH[J]. Micro & Nano Letters , 7 (1) : 33–36. |
| [12] | Mackuíak T, Nagyová K, Faberová M, et al. 2015. Utilization of Fenton-like reaction for antibiotics and resistant bacteria elimination in different parts of WWTP[J]. Environmental Toxicology and Pharmacology , 40 (2) : 492–497. DOI:10.1016/j.etap.2015.07.002 |
| [13] | Nie Y, Hu C, Qu J, et al. 2009. Photoassisted degradation of endocrine disruptors over CuOx-FeOOH with H2O2 at neutral pH[J]. Applied Catalysis B: Environmental , 87 (1/2) : 30–36. |
| [14] | Shen N, Xiang X, She X, et al. 2012. Hydrothermal synthesis and characterization of single crystalline Cu-doped α-FeOOH nanowires[J]. Applied Surface Science , 259 : 306–310. DOI:10.1016/j.apsusc.2012.07.038 |
| [15] | Shi J W, Zheng J T, Wu P. 2009. Preparation,characterization and photocatalytic activities of holmium-doped titanium dioxide nanoparticles[J]. Journal of Hazardous Materials , 161 (1) : 416–422. DOI:10.1016/j.jhazmat.2008.03.114 |
| [16] | Sheydaei M, Aber S, Khataee A. 2014. Preparation of a novel γ-FeOOH-GAC nano composite for decolorization of textile wastewater by photo Fenton-like process in a continuous reactor[J]. Journal of Molecular Catalysis A: Chemical , 392 : 229–234. DOI:10.1016/j.molcata.2014.05.019 |
| [17] | Strlič M, Kolar J, Šelih V S, et al. 2003. A comparative study of several transition metals in Fenton-like reaction systems at circum-neutral pH[J]. Acta Chim Slov , 50 (4) : 619–632. |
| [18] | Tian J J, Na W, Wang H, et al. 2014. Preparation and characterization of Cu-doped mesoporous CeO2 for CO oxidation[J]. Journal of Central South University , 21 : 482–486. DOI:10.1007/s11771-014-1964-x |
| [19] | Van Doorslaer X, Demeestere K, Heynderickx P M, et al. 2011. UV-A and UV-C induced photolytic and photocatalytic degradation of aqueous ciprofloxacin and moxifloxacin: reaction kinetics and role of adsorption[J]. Applied Catalysis B: Environmental , 101 (3) : 540–547. |
| [20] | Wu J C S, Chen C H. 2004. A visible-light response vanadium-doped titania nanocatalyst by sol-gel method[J]. Journal of Photochemistry and Photobiology A: Chemistry , 163 (3) : 509–515. DOI:10.1016/j.jphotochem.2004.02.007 |
| [21] | Wang L Q, Pang Q, Song Q Q, et al. 2015. Novel microbial synthesis of Cu doped LaCoO3 photocatalyst and its high efficient hydrogen production from formaldehyde solution under visible light irradiation[J]. Fuel , 140 : 267–274. DOI:10.1016/j.fuel.2014.09.107 |
| [22] | Wang B W, Zhao H B, Zheng Y, et al. 2013. Chemical looping combustion of petroleum coke with CuFe2O4 as oxygen carrier[J]. Chemical Engineering & Technology , 36 (9) : 1488–1495. |
| [23] | Yang Y, Ratner M A, Schatz G C. Multireference Ab lnitio study of ligand field d-d transitions in octahedral transition-metal oxide clusters[J]. Journal of Physical Chemistry C , 118 (50) : 29296–29208. |
| [24] | Yang H M, Ouyang J, Tang A D, et al. 2006. Electrochemical synthesis and photocatalytic property of cuprous oxide nanoparticles[J]. Materials Research Bulletin , 41 (7) : 1310–1318. DOI:10.1016/j.materresbull.2006.01.004 |
| [25] | Zhang T, Liu J, Wang D, et al. 2014. Selective catalytic reduction of NO with NH3 over HZSM-5-supported Fe-Cu nanocomposite catalysts: The Fe-Cu bimetallic effect[J]. Applied Catalysis B-Environmental , 148 : 520–531. |
| [26] | Zhang X, Li R, Jia M, et al. 2015. Degradation of ciprofloxacin in aqueous bismuth oxybromide (BiOBr) suspensions under visible light irradiation: A direct hole oxidation pathway[J]. Chemical Engineering Journal , 274 : 290–297. DOI:10.1016/j.cej.2015.03.077 |
 2016, Vol. 36
2016, Vol. 36


