由于自身引发的诸多水环境问题, 溶解性有机物(Dissolved Organic Matter, DOM)受到越来越多的关注.DOM实际上是一操作定义, 它是指能通过0.45 μm滤膜, 具有不同结构及分子量大小的有机物的连续体或混合体(Fu et al., 2007).DOM既可引起色、嗅、浊等表观水质问题, 又可成为微污染物如重金属、持久性有机污染物的载体, 在水体微污染物的迁移、转化中起着重要作用.更重要的是, 在加氯消毒过程中DOM会和氯反应生成三卤甲烷(Trihalomethanes, THMs)、卤乙酸(Haloacetic acids, HAAs)等消毒副产物(Disinfection by-products, DBPs)(杨海红等, 2007), 对人体健康构成威胁.
我国北方广大地区, 冬季长而寒冷, 积雪较厚.到春季融雪期, 气候转暖, 冬季积累在流域地表的积雪逐渐融化补给河流, 形成融雪径流.已有研究表明, 土壤有机质是水体中DOM的重要来源, 并随地表径流以面源污染负荷的形式进入水体(Zhang et al., 2009).由于冬春季节转换间土壤的冻融过程发生强烈, 在融雪径流的冲刷作用下, 大量土壤有机质进入水体, 融雪期水体中DOM的含量往往较高(Shiller et al., 2010).融雪径流中DOM的含量、性质和迁移转化直接关系到饮用水处理工艺的处理效率和饮用水中DBPs的浓度水平, 进而影响到人类健康.因此, 迫切需要对融雪径流中DOM的产生、分布特征和迁移转化进行系统研究.
由于具有疏松多孔的物理特性, 积雪对近地面空气中的悬浮颗粒、有毒化学物质、杂质、重金属等污染物有较强的吸附作用(Meyer et al., 2008;严登华等, 2001).污染物在雪中通过冬季较长时间的积累, 在春季融雪时短期内全部释放出来(Meyer et al., 2008).研究发现, 积雪初始融水中的离子含量远高于原始积雪的离子含量, 这种由于积雪融水作用而导致雪层中化学成分发生迁移的现象即被称作离子的“淋溶作用”(Meyer et al., 2008).积雪淋溶作用不仅能够影响雪层化学记录的原始状况, 而且能够影响融雪径流的化学成分, 产生所谓的“离子脉冲”现象(侯书贵, 2000).“离子脉冲”指的是季节积雪开始消融的几日时间内, 少量(一般少于全部积雪雪水当量的10%)的融雪水, 在短至数小时长至数日内, 集中将积雪中80%之多的化学物质排出, 并可使径流化学成分产生一瞬时高峰(Meyer et al., 2008).据报道, 天山乌鲁木齐河融雪径流的离子浓度一般能达到全水文年离子浓度的几倍(刘风景等, 1997).然而, 关于积雪淋溶作用对进入融雪径流的土壤DOM含量和性质的研究未见文献报道.因此, 本研究主要考察化学离子的种类与浓度对进入融雪径流的土壤DOM的影响, 以及积雪融化条件下土壤DOM的释放规律.
2 材料与方法(Meterials and methods) 2.1 样品采集辽宁省沈阳市位于中国东北地区, 辽宁中部, 以平原为主, 属温带半湿润地区, 全年气温在-35~36 ℃之间, 受季风影响, 温差较大, 四季分明, 冬季长而寒冷, 降雪较多.土壤类型以棕壤、暗棕壤为主.采样点位于辽宁大学(崇山校区)校园内, 坐标为41°50′1″N, 123°30′12″E.采样时间为2015年1月, 在校园各绿化区内用铁铲采集0~15 cm的表层土壤充分混合均匀后, 用塑料袋收集带回.自降雪之日算起至第7 d后, 在校园内多个地点随机采集积雪, 充分混合均匀后, 用塑料袋带回置于冰箱中待用.土壤性质见表 1, 土壤颗粒级配见表 2, 积雪融水性质见表 3.
| 表 1 土壤性质 Table 1 Soil characteristics |
| 表 2 土壤颗粒级配 Table 2 Mechanical composition of soil for soil columns |
| 表 3 积雪融水性质 Table 3 Characteristics of snowmelt water |
在辽宁大学校园内多个地点随机采集适量积雪充分混合均匀, 取其中少量完全融化后, 测定该雪水中Cl-、NO3-、SO42-、Na+、K+、Mg2+、Ca2+浓度后, 分别配制0.5、1、2及5倍的积雪中离子浓度的KCl、KNO3、K2SO4、NaCl、KCl、MgCl2、CaCl2溶液来浸提土壤.实验所用土壤采自辽宁大学校园各绿化区, 将各个地点土壤风干、除杂、混合均匀后, 过2 mm筛.将筛下土样以40 g土/300 mL浸取剂的比例进行稀释溶解, 恒温磁力搅拌0.5 h, 静置24 h后将上清液过0.45 μm滤膜.本部分实验研究的是单离子浓度变化对土壤中DOM光谱学特性的影响, 为了保证实验结果不受过多离子干扰, 当研究阳离子对土壤中DOM的影响时, 阴离子统一引入氯离子;当研究阴离子对其影响时, 阳离子统一引入钾离子.浸提液中的离子浓度与雪水中离子浓度的比值及命名如表 4所示.
| 表 4 浸提液中离子浓度与雪水中离子浓度的比值及命名 Table 4 The ratios of ion concentrtion in the extracts to the snow water and their names |
积雪在融化时会发生离子脉冲现象, 并且随着积雪在地表积累的时间不同, 其离子含量是不同的.刚落到地面的新雪融水中离子含量明显低于在地面积累数日的积雪融水中离子的含量.北方地区冬季长达数月, 降雪后, 积雪在地表积累时间较长并且当积雪融化时, 离子从雪中释放是一个缓慢的动态变化过程.该变化过程在自然界不易被及时捕捉到, 因而设计了用不同浓度的离子淋溶土壤, 来模拟自然界的积雪淋溶作用, 给人以直观的感受.自降雪之日起, 第1 d (新雪)及第7 d (旧雪)积雪融水中所含各离子浓度如表 5所示.为了具有更好的代表性, 本次实验中各不同的浓度倍数均以降雪日为7 d的积雪为标准.
| 表 5 新、旧积雪全融水性质 Table 5 Characteristics of new and old snowmelted water |
实验装置由3个土壤柱及一个蠕动泵组成.土壤柱高1.5 m, 直径0.2 m, 由不锈钢制成, 内装有400 g风干土壤, 底部有溢流口及控制开关, 溢流口处塞有脱脂棉, 防止土壤溢出, 柱外壁包裹1.5 cm的保温层, 以缓冲外界温度变化对土壤的影响.3个土壤柱分别命名为A柱、B柱及C柱, 实验装置如图 1所示.在A柱土壤上方放置1.7 kg超纯水冷冻而成的冰柱, B柱土壤上方放置1.7 kg积雪, C柱顶端与蠕动泵出水口连接, 蠕动泵进水口与装有1.7 L融雪水(即取1.7 kg积雪置于室内, 待完全融化成雪水后, 装入塑料瓶中)的容器连接.A柱及B柱白天早7:00至17:00置于室内, 室内温度约为15 ℃, 其余时间置于-15 ℃的冰箱内.C柱置于室内, 早7:00打开蠕动泵, 17:00关闭, 设置蠕动泵流速为25 mL·h-1.在溢流口处接取滤液, 每300 mL收集一次, 每柱收集5次, 分别命名为A1~A5、B1~B5、C1~C5.将收集好的淋滤液过0.45 μm滤膜后, 置于4 ℃冰箱保存.实验装置如图 1所示.
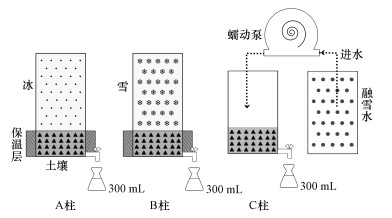 |
| 图 1 土柱装置示意图 Fig. 1 Scheme of the soil columns |
离子浓度采用Dionex ICS-90离子色谱仪(美国戴安公司)测定.溶解性有机碳(Dissolved Organic Carbon, DOC)采用Shimadou TOC-5000型(日本岛津公司)总有机碳分析仪测定.调节水样pH=7, 然后将水样置于1 cm石英比色皿中, 用紫外-可见分光光度计(Cary 50, 美国Varian公司)进行紫外-可见扫描, 扫描范围为190~900 nm, 用高纯水作空白.
三维荧光光谱用CARY Eclipse EL0507-3920型分光荧光计(美国Varian公司)测定.测定荧光光谱时, 将各个水样调节pH=7, 以消除DOM的pH对荧光光谱的影响.用光程为1 cm的石英荧光比色皿盛装样品.三维荧光光谱图的激发波长扫描范围为220~400 nm, 发射波长扫描范围为280~550 nm, 激发和发射狭缝宽度均为5 nm, 扫描速度为1200 nm·min-1, 扫描间隔为1 nm.同步荧光光谱的波长扫描范围为190~600 nm, 所采用的扫描间隔为60 nm.
3 结果与讨论(Results and discussion) 3.1 化学离子的种类与浓度对进入融雪径流中土壤DOM的影响 3.1.1 化学离子的种类与浓度对进入融雪径流中的土壤DOM含量的影响图 2所示为不同离子在不同浓度下, 即单离子浓度变化单因素影响条件下, 对土壤提取液中DOC含量变化的影响.由于土壤淋滤液胶体有机质的稳定性是受胶体表面双电层结构中扩散层的厚度及有机质颗粒零电位点值所影响的(Ritvo et al., 2003).双电层结构包括了稳定层和扩散层, 扩散层中的离子可以自由地从此层脱离开.当两颗粒在扩散层相遇时, 它们因为表面静电斥力而相互排斥, 所以使得彼此能够分离, 保持稳定的悬液状态.但如果溶液离子强度增加, 扩散层被压缩, 两胶体颗粒表面得以更近距离的接触.若颗粒表面间的距离持续减小, 以至于静电斥力已经无法抵挡范德华吸引力的时候, 此时, 两胶体颗粒便彻底地相互吸附结合, 悬浊液由此不稳定, 并导致絮凝现象的出现.由于DOC是带有负电荷的胶体, 因而与阴离子首先能产生静电斥力, 与金属阳离子能够产生絮凝作用.从图 2中可以看出, Cl-浓度的变化与DOC含量的变化并无显著关联性.NO3-浓度对土壤提取液中DOC含量具有显著的影响, DOC含量随NO3-浓度的增加而增大, 由20.51 mg·L-1逐渐增大至64.30 mg·L-1.DOC含量随Na+、Mg2+及Ca2+浓度的增大而逐渐减小, 当Na+、Mg2+及Ca2+的浓度为雪中浓度的5倍时, 即(Na+)4、(Mg2+)4和(Ca2+)4中的DOC含量最低, 分别达到18.73、9.84和9.42 mg·L-1, 与(Na+)1、(Mg2+)1和(Ca2+)1相比, 分别降低了35.3%、55.7%及41.2%, 降低幅度明显大于其他离子.而Na+、Mg2+及Ca2+的浓度为积雪中浓度的0.5、1、2倍时, 土壤提取液中DOC含量变化不显著, Cl-、K+浓度由0.5倍变化至5倍过程中对土壤提取液中DOC含量的变化影响都不大.SO42-在1倍浓度时, 提取液中的DOC含量显著高于其他浓度溶液, 可能是由于该浓度下离子与DOC分子之间产生的静电斥力刚好能使水溶液中的DOC释放量达到最大值, 而过低浓度或过高浓度的硫酸根离子都抑制了DOC从土壤中的释放.导致上述结果可能是由于DOC中含有很大一部分酸性组分, 钙和镁盐是土壤中最普遍存在的游离盐矿物, 作为土壤的贮备碱, 它们能对土壤中的各种酸, 包括有机酸(如DOC)起中和作用, 形成溶解度低的配合物(李学垣等, 2001).土壤溶液中阳离子与有机分子中的阴离子官能团的化学反应会降低有机酸的表面张力, 并且改变其自身结构, 进而降低其溶解度.此外, 阳离子可以通过与有机分子发生配合作用, 絮凝形成稳定的溶解度较低的金属-有机配合物(毕冉等, 2013), 从而降低有机分子的溶解度(Kalbitz et al., 2000), 故较高离子浓度下, 其浸提液中DOC含量较低.阳离子会导致溶解性有机质胶体絮凝, 因此, 阳离子浓度增加一般会导致土壤淋滤液溶解性有机质降低.
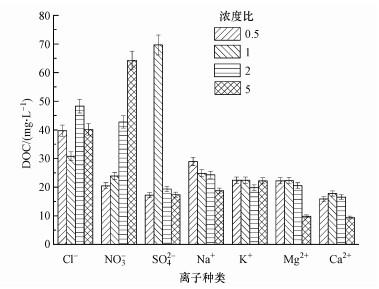 |
| 图 2 土壤浸提液中DOM的含量 Fig. 2 The contents of DOM in soil extracts |
UV-254是指在波长为254 nm处的单位比色皿光程下的紫外吸光度, 其值能够反映所测样品中腐殖质类大分子有机物及含C=C和C=O双键的芳香族化合物的多少(Leenheer et al., 2003).UV-254/DOC, 即单位溶解性有机碳的紫外吸收值SUVA (L·m-1·mg-1), 它可以反映水中有机物的芳香构造化程度, 简称芳香度(Reckhow et al., 1990).SUVA还可以反映出水中有机物的某些特性, 如芳香性及不饱和双键或芳香环有机物相对含量的多少等(Leenheer et al., 2003).Nishijima等(2004)认为, 有机物在254 nm下的紫外吸收主要代表包括芳香族化合物在内的具有不饱和碳碳键的化合物, 相同DOC浓度的有机质在该波长下吸光值的增加意味着非腐殖质向腐殖质的转化.不同离子在不同浓度下浸提土壤, 浸提液中UV-254及SUVA值如图 3所示.随着Cl-、SO42-、Mg2+、Ca2+浓度的升高, 土壤浸提液中的UV-254值逐渐降低, 说明这几种离子对土壤中芳香性化合物的解吸具有抑制作用.随着NO3-浓度的升高, 土壤浸提液中的UV-254逐渐增高, SUVA值逐渐降低, 说明高浓度的NO3-更容易将土壤中非芳香性化合物解吸出来, 因而导致浸提液中芳香性化合物相对含量的降低.随着Na+浓度的升高, SUVA值逐渐升高, 由1.05 L·m-1·mg-1升高至1.48 L·m-1·mg-1, 而DOC含量逐渐降低(图 2), 说明高浓度的钠盐能抑制DOM从土壤中的释放, 并且对非芳香性化合物的抑制作用更强, 导致浸提液中芳香性化合物相对含量的升高.其他离子浓度变化对芳香性物质从土壤中的释放影响不明显.
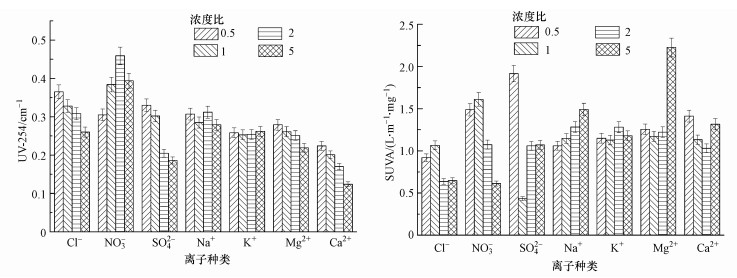 |
| 图 3 土壤浸提液中DOM的UV-254及SUVA Fig. 3 UV-254 and SUVA of DOM in soil extracts |
由图 4可以看出, 随着Cl-、Mg2+、Ca2+浓度的升高, 类腐殖酸和类富里酸荧光峰强度均表现为降低趋势.类腐殖酸荧光峰强度分别降低了10.5%、16%、46.6%;类富里酸荧光峰强度分别降低了30.7%、12.5%及37%.K+浓度的变化对土壤中DOM各荧光峰的影响不显著, NO3-、SO42-及Na+浓度变化对类腐殖酸及类富里酸荧光峰强度影响相似, 均表现为过高及过低浓度时, 其荧光峰强度较低.这说明低离子强度下DOM的扩散双电层较厚, 颗粒间排斥力高, 有利于溶液保持稳定, 随着离子强度的增加, 使得DOM扩散双电层厚度变小, 颗粒间双电层排斥力降低, 这种变化有利于有机质的絮凝沉淀(徐端平等, 2014).随着土壤有机质发生聚沉, 土柱中的孔隙被胶体堵截, 使得有机质滞留在土柱当中.同时可以看出, 当硝酸盐浓度增高时, 产生新峰类溶解性微生物代谢产物荧光峰.
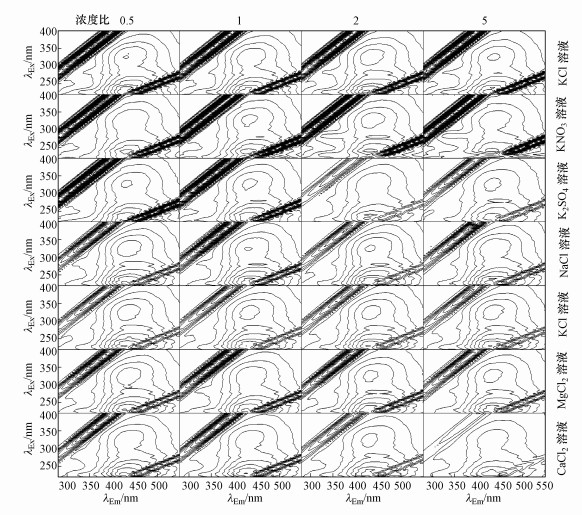 |
| 图 4 土壤浸提液中DOM的三维荧光谱图 Fig. 4 Three-dimensional fluorescence spectra of DOM in soil extracts |
从图 5可以看出, 各样品同步荧光谱图中有两个显著荧光峰Ⅰ(λsyn=280~300 nm)和峰Ⅱ(λsyn=330~350 nm), 与三维荧光谱图对比可知, 峰Ⅰ位于类溶解性微生物代谢产物荧光区, Alberts等(2004)认为该峰表示的是芳香性氨基酸(色氨酸、酪氨酸和苯丙氨酸)类物质及含有芳香性氨基酸的蛋白质.峰Ⅱ位于类腐殖酸荧光区, 从图 5可以看出, 各样品同步荧光谱图中该峰为主要荧光峰, 这与三维荧光谱图中所反映的类腐殖酸荧光物质为主要荧光物质一致.随着Cl-、Mg2+、Ca2+浓度的升高, 类腐殖酸荧光峰强度逐渐降低.硝酸根浓度升高至2倍, 类溶解性微生物代谢产物荧光峰突然增高, 当硝酸根浓度升至5倍时, 达到最高, 这说明高浓度的硝酸根离子能促进微生物的代谢活性, 从而导致类溶解性微生物代谢产物的增多, 其荧光峰强度的增大.这与上述三维荧光分析中所得氮沉降能促使有机质分解的结论相一致.
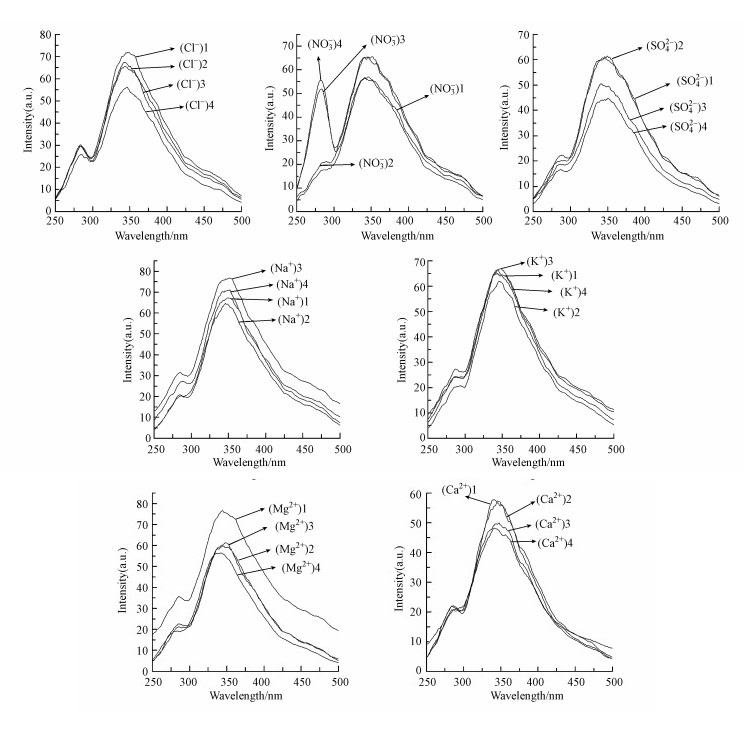 |
| 图 5 土壤浸提液中DOM的同步荧光谱图 Fig. 5 Synchronous fluorescence spectra of DOM in soil extracts |
在不同化学特征的积雪融化条件下土壤淋滤液中化学离子的浓度变化如图 6所示.可以看出, 在3个土柱接口处依次接取的5个淋滤液中, Na+浓度最平稳, 其浓度变化幅度不大;K+和Mg2+浓度略微有降低的趋势;Ca2+降低幅度最大, 与A5相比, B5、C5中Ca2+浓度较高, 这是由于雪中含有浓度相对较高的Ca2+, 而A柱进水为超纯水(不含Ca2+), 导致土壤淋滤液中Ca2+相差较大.A柱中各样品中各离子浓度与B、C柱相比均较低.3个土壤柱中, 阴离子浓度降低幅度较为明显, 总体来看, B、C柱中SO42-浓度明显高于A柱.同时可以发现, A柱与B、C柱相比, 第2次接取淋滤液的离子浓度与第1次相比降低较为明显, 如图所示, 从A1至A2 Ca2+浓度由54 mg·L-1降低至14 mg·L-1, 降低了74.1%.在第2次接取淋滤液中离子浓度出现了骤减现象, 之后几次的接取液中离子浓度变化不大.而B、C柱离子浓度降低幅度相对较平缓, B1至B2 Ca2+浓度由68 mg·L-1降低至47 mg·L-1, 降低幅度为30.8%;C1至C2 Ca2+浓度由95 mg·L-1降低至69 mg·L-1, 降低幅度为27.3%.以Ca2+、Cl-、NO3-和SO42-浓度变化趋势表现较为显著.
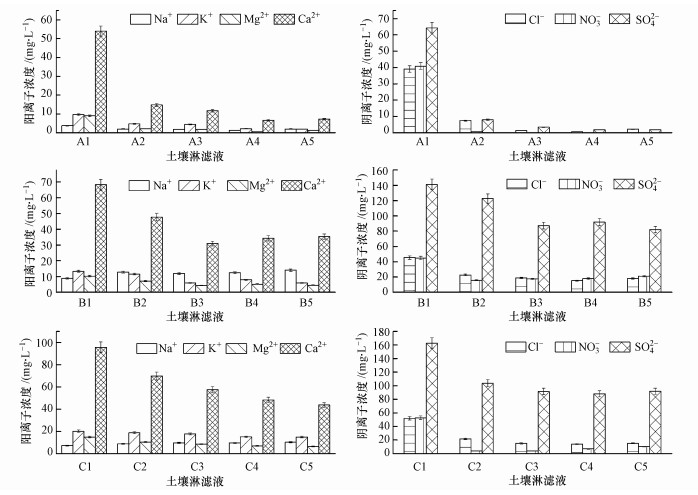 |
| 图 6 不同化学特征的积雪融化过程中土壤淋滤液中离子的浓度变化 Fig. 6 Changes in ion concentrations in soil leachates during the melting of snow with different chemical characteristics |
图 7表示的是土壤分别在A冰柱、B雪柱及C雪水的淋溶下, 土壤DOC含量的变化规律.3个土柱所接取滤液分别依次由1标记至5.可以看出, 各柱淋溶液中DOC含量逐渐减少, 这是由于DOC含量与降水量呈负相关关系, 降水不断稀释土壤中的DOC造成的(黄黎英等, 2007).A5、B5和C5中DOC含量分别为13.3、16.31、13.99 mg·L-1, 其含量大体一致, 然而A1、B1及C1中DOC含量分别为45.56、31.2、52.84 mg·L-1, 其含量相差甚远.将雪柱B白天置于室内时, 上层积雪逐渐融化, 由于淋溶作用导致积雪初始淋溶液中离子浓度较高, 阳离子浓度相应也较高, 因而B1中阳离子浓度明显高于A1及C1, 由于DOC中很大一部分为酸性组分, 因而很容易与其他物质如钙镁化合物发生絮凝沉淀, 所以, 较高离子强度的溶液浸提下土壤中DOC含量低于低离子强度的土壤浸提液中DOC的含量.C1中DOC含量高于A1、B1, 这可能是由于C雪水柱中含有适量阴阳离子, 当雪水流经土壤时, 土壤表面与DOC之间的静电斥力降低, DOC颗粒间相互吸引团聚的机会减弱, 稳定性增强, 从而导致适量的离子浓度下, DOC含量高于不含离子的A柱淋溶液.根据胡俊栋等(2009)的研究, 离子强度的减小会促进土壤胶体的稳定和释放;相反地, 离子强度增大会抑制土壤胶体的稳定和释放, 这一理论与本实验结果相符.随着B柱积雪不断融化, 积雪融水中的离子浓度显著减少, 故在第4、5次接取的淋滤液中DOC含量与A柱和C柱DOC含量相接近.
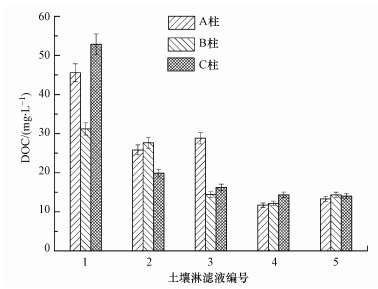 |
| 图 7 不同化学特征的积雪融化过程中土壤淋滤液中DOM的含量变化 Fig. 7 Changes in DOM contents in soil leachates during the melting of snow with different chemical characteristics |
由图 8可以看出, 3个土柱淋滤液UV-254值变化趋势一致, 都表现为逐渐减少的趋势;SUVA值并未随之减少, C柱的SUVA值明显高于A柱及B柱.B柱为雪柱, 积雪初融水中离子浓度最高, 积雪融水流经土壤, 所得淋滤液B1的UV-254值与A1、C1相比最低, 同时发生土壤冻融作用, 说明土壤经高浓度的离子溶液淋滤后其淋滤液中难分解的芳香族化合物含量最少, 冻融交替抑制了DOM自土壤解吸进入淋滤液.C柱淋溶液雪水在淋溶过程中, 前后离子浓度保持一致, 经过与土壤中一系列物理化学微生物反应后, C柱各淋滤液的UV-254值普遍高于A柱与B柱, 说明适宜的离子浓度能够促进土壤中难分解的芳香族化合物的释放, 溶液中离子浓度较高则抑制土壤中难分解的芳香族化合物的释放, 冻融交替抑制DOM自土壤解吸进入淋滤液, 并且导致土壤淋滤液中芳香族化合物相对含量的降低.同时可以看出, 单纯的增多降水量能够导致芳香性物质的含量减少, 但并不能使土壤淋滤液DOM中所含有机物的芳香性明显降低, 因而难分解的芳香性物质在此淋溶过程中不断被消耗并转化为非芳香性物质, 而导致富含非芳香结构的腐殖质物质占有机物的比例升高.
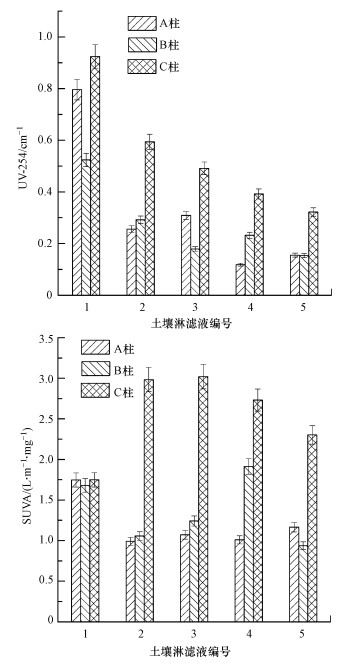 |
| 图 8 不同化学特征的积雪融化过程中土壤淋滤液中DOM的UV-254及SUVA的变化 Fig. 8 Changes in UV-254 and SUVA of DOM in soil leachates during the melting of snow with different chemical characteristics |
三维荧光光谱是表征滤液DOM的重要参数, 它能有效反映多组分复杂体系的物质组成(席北斗等, 2009).三维荧光光谱比起普通的荧光光谱能够获得激发波长和发射波长同时变化时的荧光强度信息, 可对多组分复杂体系中荧光光谱重叠的对象进行光谱表征(傅平青等, 2005).图 9各样品三维荧光谱图的4个区域中各有3个显著荧光峰和一片“肩峰”.第1个峰在激发波长/发射波长(λEx/λEm)=295~330 nm/411~434 nm区域内, 是类腐殖酸荧光峰;第2个荧光峰在λEx/λEm=245~260 nm/405~440 nm区域内, 是类富里酸荧光峰;第3个峰分布在λEx/λEm=280 nm/316~348 nm区域内, 是类溶解性微生物代谢产物荧光峰.第4个峰分布在λEx<240 nm的区域内, 是类芳香族蛋白质荧光峰.本次实验中类溶解性微生物代谢产物荧光峰及类芳香族蛋白质荧光峰均以“肩峰”形式存在.
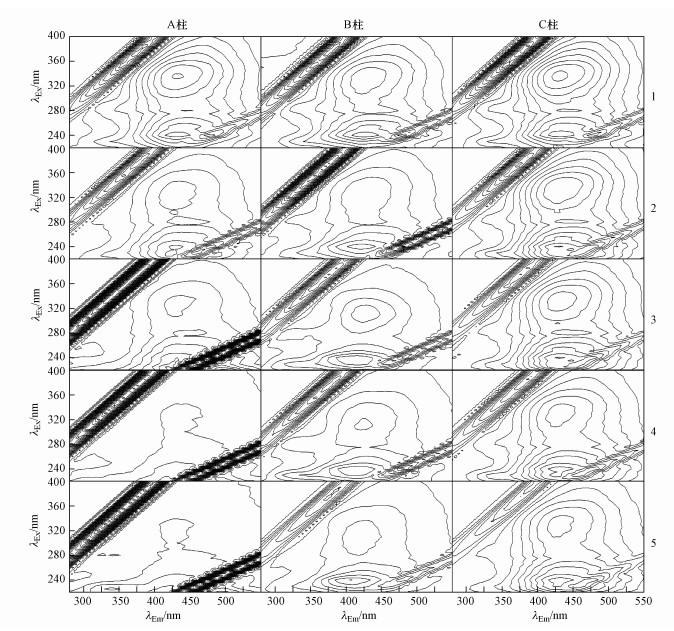 |
| 图 9 不同化学特征的积雪融化过程中土壤淋滤液中DOM的三维荧光谱图的变化 Fig. 9 Changes in three-dimensional fluorescence spectra of DOM in soil leachates during the melting of snow with different chemical characteristics |
从图 9的三维荧光谱图中可以看到有两个显著的吸收峰, 分别为类腐殖酸荧光峰和类富里酸荧光峰.A1与A5相比, 类腐殖酸荧光峰强度由222.8降低为103.6, 降低幅度为53.5%, 类富里酸荧光峰强度由231.8降低为159.1, 降低幅度为31.3%;B1与B5相比, 类腐殖酸荧光峰强度由197.0降低为114.7, 降低幅度为41.8%, 类富里酸荧光峰强度由233.6降低为177.2, 降低幅度为24.1%;C1与C5相比, 类腐殖酸荧光峰强度由222.8降低为103.6, 降低幅度为53.5%, 类富里酸荧光峰强度由231.8降低为159.1, 降低幅度为31.4%.A柱、B柱及C柱3柱相比, B柱中两个荧光峰强度降低幅度最小, 分别为41.8%及24.1%, A柱与C柱两个荧光峰强度降低幅度接近, 由此可见, B柱中高离子浓度溶液对土壤中类腐殖酸及类富里酸的流失起到抑制作用;与A柱相比, B柱以融雪水作为淋洗液导致土壤淋滤液DOM中类微生物代谢产物荧光峰强度的增高, 冻融交替抑制DOM自土壤解吸进入淋滤液.A柱、B柱及C柱均表现为类富里酸荧光峰强度降幅较类腐殖酸荧光峰强度降幅小, 这说明与类腐殖酸荧光峰相比, 较高的离子浓度溶液更容易与土壤中类富里酸发生吸附, 从而使类富里酸荧光峰强度降幅较小.
三维荧光光谱包含了DOM的全部指纹, 但由于DOM的组成非常复杂, 多种组分的荧光光谱发生重叠, 对三维荧光光谱中包含的DOM结构的潜在信息进行识别比较困难.而同步荧光法具有选择性好、干扰少、谱图简化、灵敏度高等特点, 尤其适合对多组分混合物的分析(陈女等, 2006).
同步荧光法在扫描过程中使激发波长和发射波长彼此间保持固定的波长间隔(Δλ=λEm-λEx=常数), 在同步荧光法中, Δλ的选择十分重要, 这将直接影响到同步荧光光谱的形状、带宽和信号强度.准确选择某种成分的Δλ能够极大地提高同步荧光光谱对多组分复杂体系中的该成分的选择性(Chen et al., 2003; Alberts et al., 2004).本次试验选择Δλ=60 nm.
由图 10可以看出, 各样品DOM同步荧光谱图中均显示两个显著的特征峰Ⅰ(λsyn=280~300 nm)和峰Ⅱ(λsyn=330~350 nm).与三维荧光谱图比较可知, 峰Ⅰ位于类溶解性微生物代谢产物荧光区, Alberts和Takacs (2004)认为该峰表示的是芳香性氨基酸(色氨酸、酪氨酸和苯丙氨酸)类物质及含有芳香性氨基酸的蛋白质.峰Ⅱ位于类腐殖酸荧光区, 各样品同步荧光谱图中该峰为主要荧光峰, 这与三维荧光谱图中所反映的类腐殖酸荧光物质为主要荧光物质一致.与A柱相比, B柱与C柱淋滤液中DOM的类微生物代谢产物荧光峰强度相对较高, 这可能是由于源源不断融雪水中所含的硝酸根离子刺激了微生物的代谢活性, 从而导致其类溶解性微生物代谢产物增多, 其荧光峰强度较高.与A、C柱相比, B柱淋滤液DOM中类腐植酸荧光峰强度较低, 说明B柱中类腐殖酸荧光物质相对较少, 这与三维荧光谱图中得到的结论相一致.
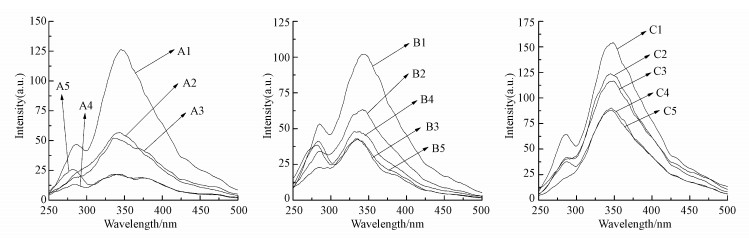 |
| 图 10 不同化学特征的积雪融化过程中土壤淋滤液中DOM的同步荧光谱图的变化 Fig. 10 Changes in synchronous fluorescence spectra of DOM in soil leachates during the melting of snow with different chemical characteristics |
1) 随着Na+、Mg2+和Ca2+溶液浓度的升高, 土壤浸提液中DOC浓度显著降低;随着Cl-、SO42-、Mg2+、Ca2+溶液浓度的升高, UV-254值逐渐减小;随着Na+、Mg2+浓度的升高, SUVA值逐渐升高.NO3-、SO42-及Na+的浓度过高或过低时, 土壤浸提液中DOM的类腐殖酸及类富里酸荧光峰强度较低;随着Cl-、Mg2+和Ca2+浓度的升高, 土壤浸提液中DOM类腐殖酸荧光峰强度逐渐降低.
2) 类腐殖酸及类富里酸荧光物质是土壤淋滤液中的主要荧光物质.与纯水相比, 以融雪水作为淋洗液导致土壤淋滤液中DOC含量的降低, 以及类微生物代谢产物荧光峰强度的增高.冻融交替抑制DOM自土壤解吸进入淋滤液, 并且导致土壤淋滤液中芳香族化合物相对含量的降低.
| [${referVo.labelOrder}] | Alberts J J, Takacs M. 2004. Comparison of the natural fluorescence distribution among size fractions of terrestrial fulvic and humic acids and aquatic natural organic matter[J]. Organic Geochemistry, 35(10) : 1141–1149. DOI:10.1016/j.orggeochem.2004.06.010 |
| [${referVo.labelOrder}] | 毕冉, 周顺桂, 袁田, 等. 2013. 水溶性有机物电子转移能力及其生态效应[J]. 生态学报, 2013, 33(1) : 45–52. |
| [${referVo.labelOrder}] | Chen J, LeBoeuf E J, Dai S, et al. 2003. Fluorescence spectroscopic studies of natural organic matter fractions[J]. Chemosphere, 50(5) : 639–647. DOI:10.1016/S0045-6535(02)00616-1 |
| [${referVo.labelOrder}] | 陈女, 吴倩, 李佟茗. 2006. 几种椰壳活性炭材料的孔结构分析[J]. 上海化工, 2006, 31(11) : 13–16. |
| [${referVo.labelOrder}] | 傅平青, 刘丛强, 吴丰昌. 2005. 溶解有机质的三维荧光光谱特性研究[J]. 光谱学与光谱分析, 2005, 25(12) : 2024–2028. |
| [${referVo.labelOrder}] | Fu P Q, Wu F C, Liu C Q, et al. 2007. Fluorescence characterization of dissolved organic matter in an urban river and its complexation with Hg (Ⅱ)[J]. Applied Geochemistry, 22(8) : 1668–1679. DOI:10.1016/j.apgeochem.2007.03.041 |
| [${referVo.labelOrder}] | 侯书贵. 2000. 乌鲁木齐河源冬季积雪淋溶作用的实验结果[J]. 冰川冻土, 2000, 22(4) : 362–365. |
| [${referVo.labelOrder}] | 黄黎英, 曹建华, 周莉, 等. 2007. 不同地质背景下土壤溶解有机碳含量的季节动态及其影响因子[J]. 生态环境, 2007, 16(4) : 1282–1288. |
| [${referVo.labelOrder}] | 胡俊栋, 沈亚婷, 王学军. 2009. 离子强度、pH对土壤胶体释放、分配沉积行为的影响[J]. 生态环境学报, 2009, 18(2) : 629–637. |
| [${referVo.labelOrder}] | Kalbitz K, Solinger S, Park J H, et al. 2000. Controls on the dynamics of dissolved organic matter in soil:A review[J]. Soil Science, 165(4) : 277–304. DOI:10.1097/00010694-200004000-00001 |
| [${referVo.labelOrder}] | 李学垣. 2001. 土壤化学[M]. 北京: 高等教育出版社 . |
| [${referVo.labelOrder}] | Leenheer J A, Croue P. 2003. Characterizing dissolved aquatic organic matter[J]. Environmental Science Technology, 37(1) : 19–26. |
| [${referVo.labelOrder}] | 刘德燕, 宋长春, 王丽, 等. 2008. 外源氮输入对湿地土壤有机碳矿化及可溶性有机碳的影响[J]. 环境科学, 2008, 29(12) : 3525–3530. |
| [${referVo.labelOrder}] | 刘风景, WilliamsM, 杨大庆. 1997. 天山乌鲁木齐河融雪径流的"离子脉冲"现象初探[J]. 科学通报, 1997, 42(4) : 417–419. |
| [${referVo.labelOrder}] | Meyer T, Wania F. 2008. Organic contaminant amplification during snowmelt[J]. Water Research, 42(8/9) : 1847–1865. |
| [${referVo.labelOrder}] | Ritvo G, Dassa O, Kochba M. 2003. Salinity and pH effect on the colloidal properties of suspended particles in super intensive aquaculture systems[J]. Aquaculture, 218(1) : 379–386. |
| [${referVo.labelOrder}] | Reckhow D A, Singer P C, Malcolm R L. 1990. Chlorination of humic materials:byproduct formation and chemical interpretations[J]. Environmental Science and Technology, 24(11) : 1655–1664. DOI:10.1021/es00081a005 |
| [${referVo.labelOrder}] | Shiller A M. 2010. Dissolved rare earth elements in a seasonally snow-covered, alpine/subalpine watershed, Loch Vale, Colorado[J]. Geochimica et Cosmochimica Acta, 74(7) : 2040–2052. DOI:10.1016/j.gca.2010.01.019 |
| [${referVo.labelOrder}] | 席北斗, 何小松, 赵越. 2009. 填埋垃圾稳定化进程的光谱学特性表征[J]. 光谱学与光谱分析, 2009, 29(9) : 2475–2479. |
| [${referVo.labelOrder}] | 许端平, 刘渚白, 谷长建, 等. 2014. 不同离子对黑土胶体在土壤中运移的影响[J]. 地球与环境, 2014, 42(3) : 333–339. |
| [${referVo.labelOrder}] | 严登华, 邓伟, 何岩. 2001. 融水对流域水环境系统影响研究进展[J]. 水文, 2001, 21(1) : 5–9. |
| [${referVo.labelOrder}] | 杨海红, 魏群山, 王东升, 等. 2007. 不同水体溶解性有机物的混凝去除特性[J]. 环境科学学报, 2007, 27(12) : 1951–1956. |
| [${referVo.labelOrder}] | Zhang Q, Kuang W, Liu L, et al. 2009. Trihalomethane, haloacetonitrile, and chloral hydrate formation potentials of organic carbon fractions from sub-tropical forest soils[J]. Journal of Hazardous Materials, 172(2/3) : 880–887. |
 2016, Vol. 36
2016, Vol. 36


