2. 暨南大学环境学院, 广州 510632
2. School of Environment, Jinan University, Guangzhou 510632
水体富营养化造成的蓝藻水华污染日趋严重, 并向水体中释放各类藻毒素, 其中, 微囊藻毒素(Microcystins, MCs)分布最广、毒性最大(Hernández et al., 2009;Gurbuz et al., 2009;Dörr et al., 2010;Xu et al., 2010), 是公认的肝毒素和促癌剂(Dawson et al., 1998;Lee et al., 1998;Wirsing et al., 1998).目前, 我国河流、湖泊、水库内均普遍检出MCs, 含量可高达数百甚至上千μg·L-1(Cook et al., 2004;Zhang et al., 2006).值得注意的是, MCs可通过灌溉、溢流等途径进入农田土壤.前人在蓝藻水华频发的太湖及滇池周边农田土壤中均普遍检出MCs, 含量达数个μg·kg-1(Chen et al., 2012;詹晓静等, 2015).与多环芳烃、多氯联苯等有机污染物不同, MCs水溶性高, 进入土壤后易被农作物吸收积累, 进而影响农作物生长, 并通过食物链威胁人类健康(Li et al., 2014).课题组前期调查发现, 滇池农田蔬菜普遍检出MCs, 以MC-RR检出最多, 其含量达36.4~2352.2 μg·kg-1 (以干重计) (Li et al., 2014).然而, 以往有关MCs环境问题的研究主要集中于其在水环境中的污染特征、毒性效应等方面, 有关土壤中MCs环境问题的研究还较为薄弱, 尤其缺乏其土壤环境行为的研究.
吸附行为是评价污染物在土壤中迁移性、生物有效性及环境行为的重要参数, 对于客观评价污染物的生态和健康风险具有重要意义(张旭等, 2014), 但目前有关MCs土壤吸附行为的研究还鲜见报道(Chen et al., 2006;詹晓静等, 2015).基于此, 本文以典型微囊藻毒素MC-RR为研究对象, 通过吸附批处理实验, 研究其在农田土壤(水稻土、赤红壤和咸田土)中的吸附动力学和热力学特征, 并探讨土壤理化性质对其吸附行为的影响, 以期为MCs生态风险评价及土壤环境污染控制提供基础数据.
2 材料与方法(Materials and methods) 2.1 实验材料与仪器 2.1.1 实验材料微囊藻毒素MC-RR (Algal Science Inc., 中国台湾), 分子量为1038.2, 分子式为C49H75N13O12(图 1), 纯度>95%, 溶解度>1 g·L-1, logKOW值为-1.09;甲醇、乙腈均为色谱纯, 购自美国Sigma;Sep-Pak C18固相萃取柱(500 mg/6 mL, Waters, 美国);其余试剂包括氯化钙、叠氮化钠、盐酸均为分析纯, 购自广州化学试剂厂;实验用水为高纯水.
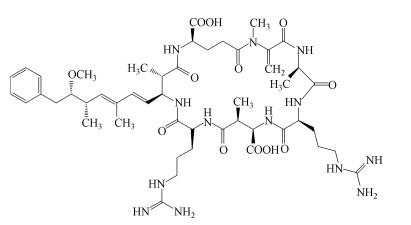 |
| 图 1 MC-RR的化学结构 Fig. 1 Structure of MC-RR |
供试土壤(水稻土、赤红壤、咸田土)均为未受微囊藻毒素污染的表层农田土壤(0~20 cm), 其中, 水稻土、赤红壤采自华南农业大学种植基地, 咸田土采自广州南沙区种植基地.所采土壤经风干、粉碎、过60目筛后于4 ℃保存备用.土壤理化性质根据文献(鲁如坤, 2000)方法进行测定, 结果列于表 1.
| 表 1 供试农田土壤理化性质 Table 1 Physicochemical properties of the tested agricultural soils |
API 4000Q-TRAP串联四极杆线性离子阱质谱仪配电喷雾离子源(ESI)(Applied Biosystems, 美国);1100液相色谱系统(Agilent, 美国);VERTEX70傅里叶转换红外光谱仪(Bruker, 德国);高速冷冻离心机(HC-3081R, 中国);固相萃取装置(VisiprepTM-DL, 美国);数控恒温水浴氮吹仪(KL512J, 中国).
2.2 实验方法 2.2.1 吸附实验根据OECD guideline 106进行批平衡吸附实验(OECD, 2000), 研究MC-RR在土壤中的吸附动力学和热力学特征.称取供试土样2.000 g置于50 mL的聚丙烯离心管中, 加入10 mL一定浓度的MC-RR溶液, 溶液含0.01 mol·L-1的CaCl3(平衡溶液离子浓度)和0.01 mol·L-1的NaN3(抑制微生物), 进行恒温((25±1) ℃)振荡(200 r·min-1), 以8000 r·min-1离心10 min, 取上清液, 测定其MC-RR浓度.研究吸附动力学特征时, MC-RR初始浓度设定为400 μg·L-1, 温度为25 ℃, 分别于0.5、1、4、6、8、12、16、24 h采样, 测定其上清液中MC-RR浓度, 并根据吸附前后上清液MC-RR浓度差计算土壤MC-RR吸附量.研究热力学特征时, MC-RR初始浓度分别为10、25、50、200、400 μg·L-1, 振荡时间为24 h (根据动力学研究, 该振荡时间可达到土壤对MC-RR的吸附平衡), 分别研究不同温度条件下(15、25、35 ℃)供试土壤对MC-RR的吸附等温线.以上各浓度处理均设置3个平行.
2.2.2 MC-RR的测定方法取上清液过C18固相萃取小柱富集(控制流速为1 mL·min-1), 用10 mL高纯水洗脱小柱, 弃去洗脱液, 真空干燥后, 用5 mL酸化甲醇再次洗脱小柱后, 收集洗脱液, 以氮气浓缩至近干, 用色谱纯甲醇定容为1 mL, 过0.22 μm滤膜, 于4 ℃下保存备测.采用API 4000Q-TRAP串联四极杆线性离子阱质谱仪测定MC-RR浓度, 测定过程中用Agilent Eclipse Plus C18柱(150 mm×2.1 mm, 5 μm)进行色谱分离, 进样量为5 μL.质谱分析采用正离子扫描, 多离子反应检测(MRM)模式.上述条件下, MC-RR的保留时间为5.22 min.为控制实验质量, 每测定6个样品间隔设置空白样、样品平行样、样品加标样, 空白样中均未检出MC-RR, 平行样标准偏差低于10%, 样品加标回收率为85%~90%.实验过程中MC-RR的检出限量(LOQ)为0.25 μg·L-1, 质量平衡率为90%~95%, 吸附率为30%~99%.
2.2.3 傅立叶转换红外光谱分析采用KBr压片技术制片(土样与KBr的质量比为1.5:300), 设定扫描波数范围为400~4000 cm-1, 扫描分辨率为4 cm-1, 进行傅立叶转换红外光谱扫描.
2.3 数据分析分别采用Excel2007进行数据统计, Origin8.0进行图形绘制和数据拟合, SPSS16.0进行相关性分析.
3 结果与讨论(Results and discussion) 3.1 吸附动力学研究3种供试土壤对MC-RR (400 μg·L-1, 25 ℃)的吸附在4 h内达到平衡, 其吸附过程均满足拟二级动力学方程(式(1))(R2>0.994).
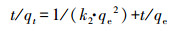
|
(1) |
式中, t为反应时间(h), qt为t时刻吸附量(μg·g-1), qe为平衡吸附量(μg·g-1), k2为二级动力学吸附速率常数(min·μg·g-1).根据拟二级动力学方程拟合结果, 由图 2a可知, 3种土壤对MC-RR吸附平衡量大小顺序为:咸田土(1.15 μg·g-1)>赤红壤(0.99 μg·g-1)>水稻土(0.66 μg·g-1).
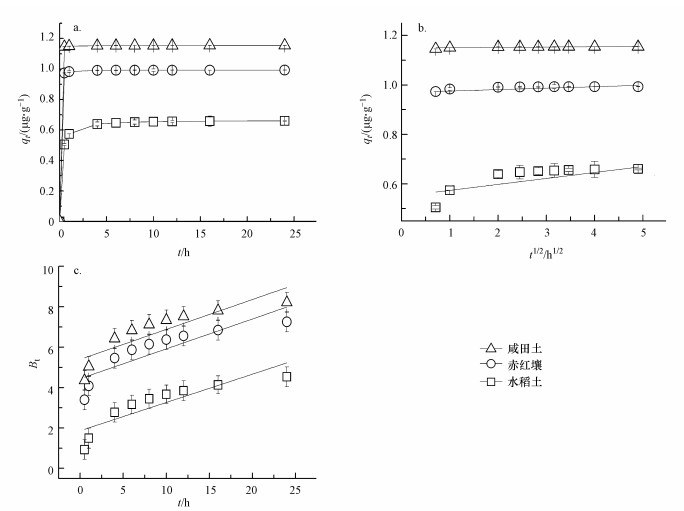 |
| 图 2 MC-RR在3种土壤中的吸附动力学特征(a.土壤吸附量随时间的变化曲线b.颗粒内扩散方程拟合曲线c.Boyd方程拟合曲线) Fig. 2 Sorption kinetics of MC-RR in the agricultral soils (a. sorption amounts with time b. the fitting curves based on the intraparticle diffusion model c. the fitting curves based on the Boyd model) |
为进一步研究MC-RR在3种土壤中的吸附动力学机理, 分别采用颗粒内扩散方程(式(2))及Boyd方程(式(3))进行拟合分析.
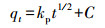
|
(2) |
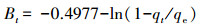
|
(3) |
式中, kp为颗粒内扩散速率常数(μg·g-1·h-1/2), C为常数(μg·g-1), Bt为qt/qe(文中该比值均大于0.85)的函数;若式(2)拟合方程为线性且过原点, 则颗粒内扩散过程是吸附的唯一速率控制过程, 若不过原点, 则吸附涉及颗粒内扩散过程但该过程并非唯一控速过程(Lian et al., 2014);若式(3)拟合方程为线性且过原点, 则颗粒扩散过程是吸附的主要控速过程, 若不过原点, 则液膜扩散过程是吸附的主要控速过程(Lizethly et al., 2013).拟合结果显示, MC-RR在3种土壤中的颗粒内扩散方程和Boyd方程的拟合曲线均呈线性且不过原点(图 2b, 2c), 表明MC-RR的吸附过程同时涉及颗粒内扩散和液膜扩散过程, 且后者为主要控速过程.
3.2 吸附热力学研究不同温度下(15、25、35 ℃)3种土壤对MC-RR的吸附等温线(图 3)均满足Langmuir方程(式(4))(R2>0.827), 表明MC-RR在3种土壤中的吸附过程可能为单分子层吸附(Shao et al., 2014).
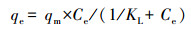
|
(4) |
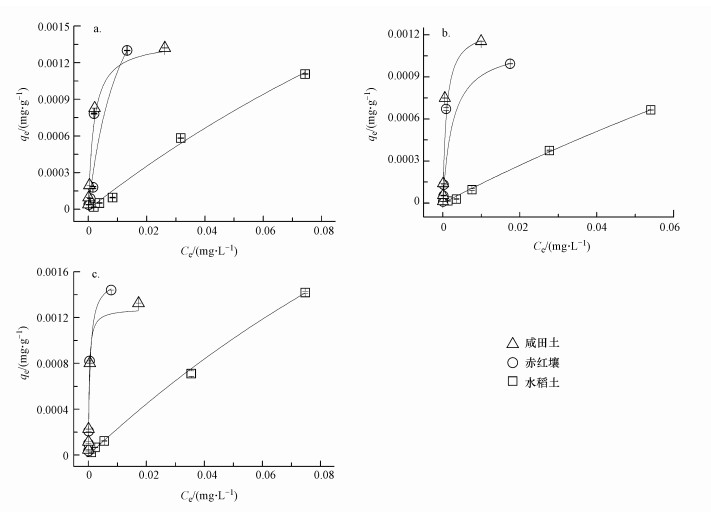 |
| 图 3 MC-RR在3种土壤中Langmuir方程拟合等温线(a.15 ℃, b.25 ℃, c.35 ℃) Fig. 3 Langmuir sorption isotherm of MC-RR in the soils under different temperature (a.15 ℃, b.25 ℃, c.35 ℃) |
式中, Ce为溶液中MC-RR的吸附平衡浓度(mg·L-1), qm为最大吸附量(mg·g-1), KL为表面吸附强度系数(L·mg-1).在Ce较低时, 可用最大吸附量与吸附强度系数之积(KL·qm, μL·g-1)评价土壤对MC-RR的吸附性能, 该值越大, 越有利于MC-RR吸附(Wu et al., 2011).对水稻土而言, 其吸附MC-RR的KL·qm值随温度升高而减小, 而对于赤红壤和咸田土而言, 其KL·qm值随温度升高而增大, 指示温度降低有利于MC-RR在水稻土中的吸附, 而温度升高有利于MC-RR在赤红壤和咸田土中的吸附.根据Langmuir拟合方程并由式(5)、(6)、(7)计算吉布斯自由能变(Δ G)、焓变(Δ H)及熵变(Δ S).
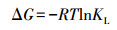
|
(5) |
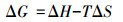
|
(6) |
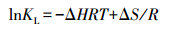
|
(7) |
式中, R为摩尔气体常数(8.314 J·mol-1·k-1), T为绝对温度(K).计算结果如表 2所示, 不同温度下3种土壤吸附MC-RR的ΔG值均小于零, 且ΔS均大于零, 指示MC-RR在3种土壤中的吸附均为熵增的自发过程(Lei et al., 2013).不同的是, 水稻土吸附MC-RR的ΔH值小于零, 而赤红壤和咸田土吸附MC-RR的ΔH值大于零, 表明MC-RR在水稻土中的吸附过程为放热反应, 而在赤红壤和咸田土中的吸附过程为吸热反应(Wu et al., 2011), 这就解释了水稻土对MC-RR的吸附能力随温度增加而降低, 而赤红壤和咸田土对MC-RR的吸附能力随温度增加而升高.同时, 由于水稻土吸附MC-RR的ΔH绝对值小于40.00 kJ·mol-1, 而赤红壤和咸田土吸附MC-RR的ΔH绝对值大于40.00 kJ·mol-1, 表明MC-RR在水稻土中的吸附为氢键作用力介导的物理吸附过程, 而MC-RR在赤红壤和咸田土中的吸附为官能团相互作用介导的化学吸附过程(DiVincenzo et al., 2001).
| 表 2 三种土壤中MC-RR的吸附热力学参数 Table 2 Sorption thermodynamic parameters of MC-RR in three agricultural soils |
为进一步查明吸附过程中土壤表面官能团与MC-RR的相互作用, 研究了3种土壤吸附MC-RR (400 μg·L-1, 25 ℃)的红外光谱图(图 4), 结果表明, 吸附MC-RR后, 赤红壤红外光谱图中烷烃类化合物-CH3不对称伸缩振动峰(2976 cm-1)和CH2对称伸缩振动峰(2880 cm-1)显著增强, 而咸田土红外光谱图中-CH3不对称伸缩振动峰(2976 cm-1)与-NO2不对称伸缩振动峰(1530 cm-1)显著减弱, 表明吸附过程中MC-RR可能与赤红壤和咸田土中的烷烃类化合物及硝基化合物发生反应, 形成化学吸附(张超群等, 2007).与此不同的是, 吸附MC-RR后, 水稻土红外光谱图无明显变化, 这进一步说明水稻土对MC-RR的吸附主要为物理吸附.
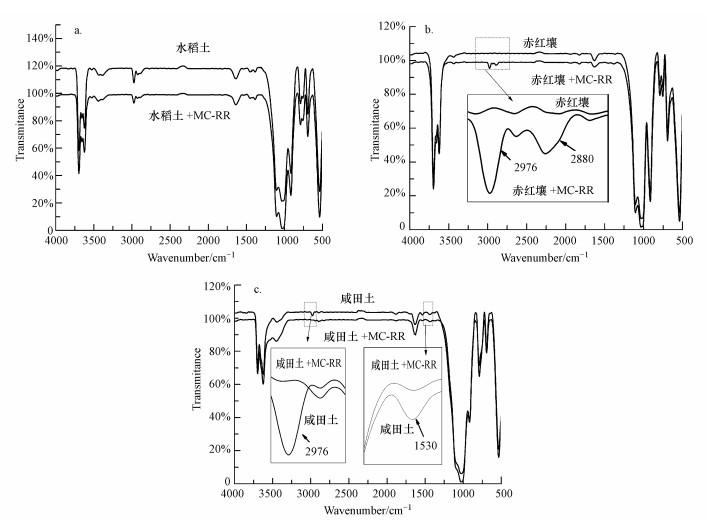 |
| 图 4 三种土壤吸附MC-RR的傅立叶变换红外光谱(a.水稻土, b.赤红壤, c.咸田土) Fig. 4 The FTIR spectra of the three agricultural soils with and without MC-RR (a. paddy soil, b. latosolic red soil, c.salted paddy soil) |
土壤有机碳分配系数(Koc)是评价土壤吸附污染物的重要参数(王雄科等, 2015), 其值可由式(8)计算, 该值越大, 表明土壤对污染物的吸附能力越强.
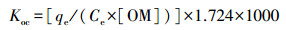
|
(8) |
式中, Koc为土壤有机碳分配系数(mL·g-1), [OM]为有机质含量(g·g-1), 1.724为土壤有机碳与其有机质的转换系数, 1000为体积单位转换系数.
不同温度条件下, 赤红壤和咸田土吸附MC-RR的Koc值均大于水稻土的Koc值.其中, 水稻土、赤红壤咸田土在15 ℃时其吸附MC-RR的Koc值分别为325~611、14034~57580、5768~202641 mL·g-1;在25 ℃时, 其吸附MC-RR的Koc值分别为266~448、8160~113828、13343~174327 mL·g-1;在35 ℃时, 其吸附MC-RR的Koc值分别为629~933、26274~286837、8806~474618 mL·g-1.由于目前缺乏MCs的评价标准, 本文依据《化学农药环境安全评价试验准则》(GB31270.4-2014)方法评价MC-RR在农田土壤中吸附能力.该准则按Koc值(mL·g-1)的大小将污染物吸附性能分为5个等级, 即易吸附型(Koc>20000), 较易吸附型(5000 < Koc≤20000), 中等吸附型(1000 < Koc≤5000), 较难吸附型(200 < Koc≤1000)和难吸附型(Koc≤200).可见, MC-RR在赤红壤和咸田土中为易吸附型污染物, 在水稻土中为难吸附型污染物.
3.4 土壤理化性质对MC-RR吸附的影响相关性分析显示, 不同温度(15、25、35 ℃)条件下, 3种土壤吸附MC-RR的KL·qm值和Koc值(以10、50、200 μg·L-1为例)总体与土壤粘粒含量呈显著正相关关系, 而与土壤有机质含量呈显著负相关关系(表 3、4), 即土壤粘粒含量越高, 有机质含量越低, 对MC-RR的吸附能力越强.粘粒矿物表面积较大, 其含量越高, 吸附活性位点越多, 从而有利于土壤吸附MC-RR (Chen et al., 2006), 因此, 土壤粘粒含量与其吸附MC-RR能力呈正相关.对于有机质而言, 由于MC-RR溶解度较高(1 g·L-1), 而辛醇水分配系数较低(logKOW=-1.09), 土壤有机质较高不利于其吸附.同时, Wu等(2011)研究发现, 当土壤或沉积物有机质含量小于8.0%时, 其与MC-RR发生竞争吸附, 从而抑制MC-RR的吸附, 且有机质含量越高抑制作用越强;而当土壤或沉积物含量大于8.0%时, 其与MC-RR发生共吸附, 有机质含量越高, MC-RR的吸附越强.本文供试土壤有机质含量(1.2%~5.2%)均小于8.0%, MC-RR可与土壤有机质发生竞争吸附, 其吸附能力随有机质增多而减弱.因此,土壤有机质含量与其吸附MC-RR的能力呈负相关.
| 表 3 KL·qm与供试土壤理化性质的相关性 Table 3 Correlations between KL·qm and soil physicochemical properties |
| 表 4 Koc与供试土壤理化性质的相关性 Table 4 Correlations between Kocand soil physicochemical properties |
1) 3种农田土壤对MC-RR的吸附均在4 h内达到平衡, 吸附动力学均符合拟二级动力学方程, 液膜扩散是主要控速过程.
2) 水稻土吸附MC-RR主要为自发放热的物理吸附过程, 温度升高不利于其吸附;赤红壤和咸田土吸附MC-RR主要为自发吸热的化学吸附过程, 温度升高有利于其吸附.
3) 土壤理化性质显著影响其对MC-RR的吸附能力, 粘粒矿物含量越高, 有机质含量越低, MC-RR吸附能力越强.因此, MC-RR在有机质含量较高的水稻土中难吸附, 而在有机质含量较低的赤红壤和粘粒含量较高的咸田土中易吸附.
| [${referVo.labelOrder}] | Cook C M, Vardaka E, Lanaras T. 2004. Toxic cyanobacteria in Greek freshwaters, 1987-2000: Occurrence, toxicity, and impacts in the Mediterranean region[J]. Acta Hydrochimica et Hydrobiologica, 32(2) : 107–124. DOI:10.1002/(ISSN)1521-401X |
| [${referVo.labelOrder}] | Chen W, Jia Y L, Li E H, et al. 2012. Soil-based treatments of mechanically collected cyanobacterial blooms from Lake Taihu: Efficiencies and potential risks[J]. Environmental Science and Technology, 46 : 13370–13376. DOI:10.1021/es3027902 |
| [${referVo.labelOrder}] | Chen W, Song L R, Gan N Q, et al. 2006. Sorption, degradation and mobility of microcystins in Chinese agriculture soils: Risk assessment for groundwater protection[J]. Environmental Pollution, 144(3) : 752–758. DOI:10.1016/j.envpol.2006.02.023 |
| [${referVo.labelOrder}] | Dörr F A, Pinto E, Soares R M, et al. 2010. Microcystins in South American aquatic ecosystems: Occurrence, toxicity and toxicological assays[J]. Toxicon, 56(7) : 1247–1256. DOI:10.1016/j.toxicon.2010.03.018 |
| [${referVo.labelOrder}] | DiVincenzo J, Sparks D L. 2001. Sorption of the neutral and charged forms of penthachlorophenol on soil: evidence for different mechanisms[J]. Archives of Environmental Contamination and Toxicology, 40 : 445–450. DOI:10.1007/s002440010196 |
| [${referVo.labelOrder}] | Dawson R M. 1998. The toxicology of microcystins[J]. Toxicon, 36(4) : 953–962. |
| [${referVo.labelOrder}] | Gurbuz F, Metcalf J S, Karahan A G, et al. 2009. Analysis of dissolved microcystins in surface water samples from Kovada Lake, Turkey[J]. Science of the Total Environment, 407(13) : 4038–4046. DOI:10.1016/j.scitotenv.2009.02.039 |
| [${referVo.labelOrder}] | 国家农业部农药检定所.2014.GB/T 31270.4-2014化学农药环境安全评价试验准则:第4部分:土壤吸附/解吸试验[S].北京:国家质量监督检验检疫总局 |
| [${referVo.labelOrder}] | Hernández J M, López-Rodas V, Costas E, et al. 2009. Microcystins from tap water could be a risk factor for liver and colorectal cancer: A risk intensified by global change[J]. Medical Hypotheses, 72(5) : 539–540. DOI:10.1016/j.mehy.2008.11.041 |
| [${referVo.labelOrder}] | Lei C, Hu Y Y, He M Z. 2013. Adsorption characteristics of triclosan from aqueous solution onto cetylpyridinium bromide (CPB) modified zeolites[J]. Chemical Engineering Journal, 219 : 361–370. DOI:10.1016/j.cej.2012.12.099 |
| [${referVo.labelOrder}] | Lizethly C J, Jorge R B, Joselyn P R, et al. 2013. Sorption kinetics of diuron on volcanic ash derived soils[J]. Journal of Hazardous Materials, 261 : 602–613. DOI:10.1016/j.jhazmat.2013.07.073 |
| [${referVo.labelOrder}] | Lian L L, Cao X L, Wu Y Q, et al. 2014. A green synthesis of magnetic bentonite material and its application for removal of microcystin-LR in water[J]. Applied Surface Science, 289 : 245–151. DOI:10.1016/j.apsusc.2013.10.144 |
| [${referVo.labelOrder}] | 鲁如坤. 2000. 土壤农业化学分析方法[M]. 北京: 中国农业科技出版社 . |
| [${referVo.labelOrder}] | Lee T, Chen Y, Chou H, et al. 1998. First report of microcystins in Taiwan[J]. Toxicon, 36(2) : 247–255. DOI:10.1016/S0041-0101(97)00128-1 |
| [${referVo.labelOrder}] | Li Y W, Zhan X J, Xiang L, et al. 2014. Analysis of trace microcystins in vegetables using solid-phase extraction followed by high performance liquid chromatography triple-quadrupole mass spectrometry[J]. Agricultural and Food Chemisty, 62 : 11831–11839. DOI:10.1021/jf5033075 |
| [${referVo.labelOrder}] | OECD. 2000. OECD Guidelines for Testing of Chemicals, Test Guideline 106: Adsorption/Desorption Using a Batch Equilibrium Method[M]. Paris: Revised Draft Document OECD : 1–45. |
| [${referVo.labelOrder}] | Shao J H, Gu J D, Peng L, et al. 2014. Modification of cyanobacterial bloom-derived biomass using potassium permanganate enhanced the removal of microcystins and adsorption capacity toward cadmium (Ⅱ)[J]. Journal of Hazardous Materials, 272 : 83–88. DOI:10.1016/j.jhazmat.2014.03.013 |
| [${referVo.labelOrder}] | Song L R, Chen W, Peng L, et al. 2007. Distribution and bioaccumulation of microcystins in water columns: A systematic investigation into the environmental fate and the risks associated with microcystins in Meiliang Bay, Lake Taihu[J]. Water Research, 41(13) : 2853–2864. DOI:10.1016/j.watres.2007.02.013 |
| [${referVo.labelOrder}] | Wirsing B, Hoffmann L. 1998. First report on the identification of microcystin in a water bloom collected in Belglum[J]. Systematic & Applied Microbiology, 21(1) : 23–27. |
| [${referVo.labelOrder}] | 王雄科, 向垒, 郑美洁, 等. 2015. 季胺盐化合物在水稻土中的吸附与淋溶行为[J]. 农业环境科学学报, 2015, 34(6) : 1115–1120. |
| [${referVo.labelOrder}] | Wu X Q, Xiao B D, Li R H, et al. 2011. Mechanisms and factors affecting sorption of microcystins onto natural sediments[J]. Environmental Science and Technology, 45 : 2641–2647. DOI:10.1021/es103729m |
| [${referVo.labelOrder}] | Xu C, Chen J A, Huang Y J, et al. 2010. Identification of microcystins contamination in surface water samples from the Three Gorges Reservoir, China[J]. Environmental Monitoring and Assessment, 180(1/4) : 77–86. |
| [${referVo.labelOrder}] | 张超群, 姜秀民, 黄庠永, 等. 2007. 煤焦吸附NO特性与红外光谱分析[J]. 化工学报, 2007, 58(3) : 581–586. |
| [${referVo.labelOrder}] | 张旭, 向垒, 莫测辉, 等. 2014. 喹诺酮类抗生素在土壤中的迁移行为及影响因素研究[J]. 农业环境科学学报, 2014, 33(7) : 1345–1350. |
| [${referVo.labelOrder}] | Zhang X, Xie P, Hao L, et al. 2006. Effects of the phytoplanktivorous silver carp (Hypophthalmichthys molitrixon) on plankton and the hepatotoxic microcystins in an enclosure experiment in a eutrophic lake, Lake Shichahai in Beijing[J]. Aquaculture, 257(1/4) : 173–186. |
| [${referVo.labelOrder}] | 詹晓静, 向垒, 邓哲深, 等. 2015. 农田土壤中微囊藻毒素污染特征及风险评价[J]. 中国环境科学, 2015, 35(7) : 2129–2136. |
 2016, Vol. 36
2016, Vol. 36


