2. 中国科学院大学, 北京 100049;
3. 辽宁欧科环境监测技术有限公司, 锦州 121000
2. University of Chinese Academy of Sciences, Beijing 100049;
3. Oke Environmental Monitoring Technology Co. Ltd, Jinzhou 121000
沼渣是厌氧发酵生产沼气过程中产生的固体废弃物, 由于发酵原料(多是生活垃圾和畜禽粪便)成分复杂, 沼渣不仅含有大量有机质和矿质养分, 通常还含有一定量的重金属等有害物质(董志新等, 2015).随着我国沼气应用的推广普及, 沼渣产生量不断增加, 如何适当处理沼渣的问题随之而来.诸多研究表明, 沼渣因富含养分物质可作为肥料施用, 能显著改善土壤理化性质, 提高作物产量及品质(Abubaker et al., 2012; 2013; Svoboda et al., 2013), 但同时因其可能含有重金属而使其利用存在一定的安全隐患(谢景欢等, 2010; 陈苗等, 2012; Herrmann et al., 2013).
丛枝菌根(Arbuscular mycorrhiza, AM)真菌是在自然和农业生态系统中广泛存在的一类土壤真菌, 能与绝大多数高等植物形成共生体系(Smith et al., 2008).AM真菌能够有效促进宿主植物对矿质养分的吸收, 并能增强植物对各种逆境胁迫的耐受性(孙吉庆等, 2012).在重金属污染情况下, AM真菌可以通过不同途径影响重金属在土壤-植物系统中的迁移转化过程, 从而影响植物对重金属的吸收累积, 减轻重金属对植物的毒害(伍松林等, 2013).在沼渣农业利用过程中, 接种AM真菌有可能在促进植物吸收利用沼渣中养分物质的同时降低其重金属污染风险, 但目前这方面尚罕见研究报道.
甘草(Glycyrrhiza uralensis Fisch.)为豆科(Leguminosae)甘草属多年生草本植物, 是一种广泛应用的补益中草药, 具有清热解毒、祛痰止咳、调和诸药等功效, 同时也是现代制药工业、食品保健业、轻工业等诸多行业中重要的原材料(田庆来等, 2006), 因而甘草的人工种植具有较高的社会经济效益.甘草自身耐逆性较强, 对环境条件需求不是很严格, 但在集约化种植体系中仍需要适当的水肥管理才能保障甘草的产量和品质.沼渣作为一种来源广泛、成本低廉的肥料, 应用于作物生产和生态恢复有明显的优势, 但有关沼渣在甘草栽培中的应用及风险管理却少有试验研究.基于此, 本研究采用甘草为供试植物开展盆栽试验, 设置不同沼渣添加量及AM接种剂量, 考察沼渣和AM真菌对甘草生长和矿质营养, 以及土壤理化性质的影响, 以期为沼渣在甘草种植体系中的安全利用提供技术支撑.
2 材料与方法(Materials and methods) 2.1 试验材料供试植物:甘草(Glycyrrhiza uralensisFisch.)种子从新疆康隆农业科技发展有限公司购得.种子用10%(V/V)过氧化氢表面消毒10 min, 而后用去离子水冲洗, 均匀地铺在覆有湿润吸水纸的托盘中, 28 ℃催芽2 d, 种子露白后备播种.
菌剂:AM真菌(Rhizophagus intraradices Błaszk., Wubet, Renker, and Buscot BGC AH01)原始菌剂由北京市农林科学院植物营养与资源研究所提供.试验用菌剂通过盆栽苜蓿扩繁获得, 接种剂为含有菌根真菌孢子、宿主植物根段及培养基质的混合物, 每克菌剂大约含有80个孢子.
供试基质:供试土壤取自内蒙古多伦(42°02′N, 116°17′E), 其基本理化性质如下:pH为7.02(土水比1:2.5), 有机质含量1.78%, 最大田间持水量24.24%, 速效磷6.73 mg·kg-1, 总氮0.85 g·kg-1.测定方法参考文献(鲍士旦, 2000).土壤过2 mm筛后, 送至中国农业科学院原子能所辐照中心进行辐照灭菌(60Co, γ射线25 kGy).培养基质为土壤和石英砂(过2 mm筛)按质量比1:1混合而成.除非特别注明, 文中“土壤”即指此混合培养基质.
沼渣来源:沼渣是由内蒙古自治区鄂尔多斯市东胜区工业垃圾和生活垃圾分选出的有机物料经过厌氧发酵得到的固体残余物.沼渣经风干敲碎后过2 mm筛, 送至中国农业科学院原子能所辐照中心进行辐照灭菌(60Co, γ射线25 kGy).参照《土壤农化分析》测得沼渣pH为8.05, 有机质含量21.1%, 速效磷171.5 mg·kg-1, 总氮915 mg·kg-1, 铬354.70 mg·kg-1, 铜660.14 mg·kg-1, 铅607.21 mg·kg-1, 锌63.52 mg·kg-1, 铬0.463 mg·kg-1, 砷0.023 mg·kg-1, 其中, 铬、铜和铅含量超出城镇垃圾农用标准GB8172-87(铬≤300 mg·kg-1, 铜≤300 mg·kg-1, 铅≤100 mg·kg-1), 因而本试验考虑将这3种重金属的含量作为评判施用沼渣环境污染风险的分析指标.
2.2 试验设计采用塑料盆(上口直径8 cm, 下底直径6 cm, 高8 cm)作为培养容器.AM真菌接种剂量和沼渣施加量均设置3个水平:0、10、20 g·盆-1.每盆装土400 g, 接种剂和沼渣与土壤充分混匀后装盆.试验为2因素3水平完全随机区组设计, 共9个处理, 每个处理重复5次.
2.3 试验管理每盆播种3颗经催芽处理的甘草种子, 出苗后2周每盆间留1株幼苗.试验在人工气候室中开展, 昼夜温度为25 ℃/20 ℃, 相对湿度60%, 光强约700 μmol·m-2·s-1, 每天光照时间16 h.每日称重浇水, 保持15%的土壤含水量.试验过程中盆钵完全随机排列且每周定期重排.
2.4 试验收获与样品分析甘草生长60 d后进行收获, 自土表将植物剪断, 界面以上为地上部.将地上部和根系分别用去离子水清洗干净, 取新鲜根系0.5 g左右用于测定菌根侵染率, 另取新鲜叶片0.5 g用于测定叶绿素含量, 其余植物样品于105 ℃杀青30 min, 然后于70 ℃烘干48 h至恒重后称取干重.采用Trypan blue染色-镜检法观测菌根侵染状况(Phillips et al., 1970), 计算菌根侵染率(Biermann et al., 1981).采用比色法测定叶片叶绿素含量.植物磷和重金属(Cr、Cu、Pb)含量测定时采用微波消解进行样品前处理, ICP-MS (7500a Agilent Technologies, Palo Alto, CA, USA)进行样品分析, 同时采用国家一级标准物质灌木枝叶(GBW07603)进行分析质控.
土壤有机质含量采用重铬酸钾氧化法测定.土壤全磷和重金属(Cr、Cu、Pb)含量采用微波消解进行样品前处理, ICP-MS进行样品分析, 同时, 采用中国地质科学院地球物理化学勘探研究所的土壤标准样品(GBW07406)进行分析质控.
2.5 数据分析采用SPSS (SPSS 18.0 for Windows, SPSS Inc, Chicago, USA)和Microsoft Excel®对数据进行统计分析和作图.采用双因素方差分析检验接种处理、沼渣处理及二者交互作用的显著性.当交互作用显著时, 采用最小显著性差异法(LSD)将全部处理统一进行多重比较.当接种处理与沼渣处理交互作用不显著时, 则将试验数据按试验因素分组进行多重比较.
3 结果与分析(Results and analysis) 3.1 菌根侵染状况试验条件下, 接种处理甘草根系均检测到一定程度的菌根侵染, 在较高接种剂量下菌根侵染率也较高, 而未接种处理(接种剂量0 g·盆-1)无菌根侵染迹象(表 1).总体上, 沼渣对菌根侵染表现出明显抑制作用, 随沼渣施加量提高, 菌根侵染率显著下降(表 1).
| 表 1 不同处理下甘草菌根侵染率 Table 1 Mycorrhizal colonization rates of licorice plants under different experimental treatments |
与不施加沼渣对照(0 g·盆-1)相比, 施用沼渣显著促进了植物生长, 提高了植物生物量、磷含量和叶片叶绿素含量, 但总体上10和20 g·盆-1两个沼渣施加水平之间差异不显著(图 1).总体上, 接种AM真菌也显著提高了植物生物量、根系磷含量及叶片叶绿素含量, 但接种和沼渣处理对甘草地上部生物量及植株磷含量的影响存在显著交互作用(表 2):在不施加沼渣情况下, 接种处理的促生作用显著, 而在20 g·盆-1沼渣添加量下, 接种处理作用不明显, 甚至反而降低了地上部磷含量(图 1).
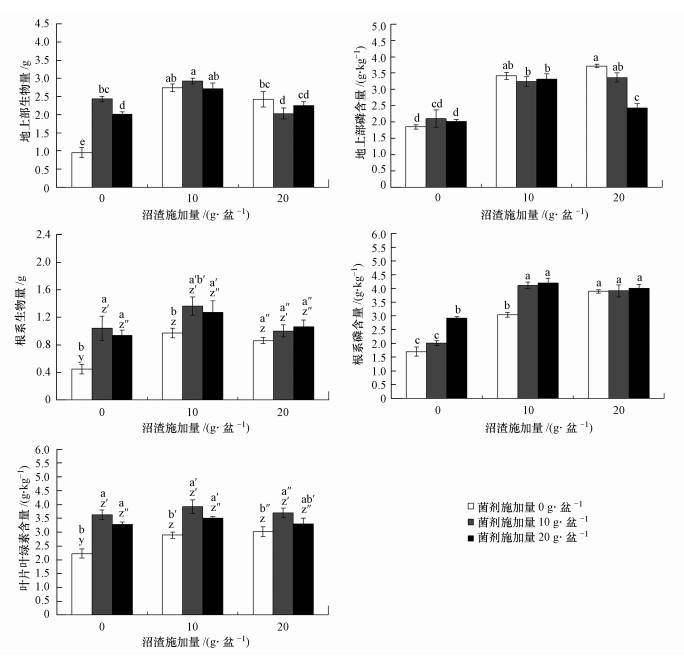 |
| 图 1 不同处理下甘草生物量、磷含量及叶片叶绿素含量(柱形上方不同字母表示相应处理之间差异显著(p < 0.05);当接种处理与沼渣处理交互作用显著(p < 0.05)时, 所有处理统一进行多重比较, 以不同小写字母(a, b, c…)标示处理之间的差异显著性;当交互作用不显著时, 以小写字母(z, y, x…)、(z′, y′, x′…)和(z″, y″, x″…)分别标示0、10和20 g·盆-1接种水平下不同沼渣施加水平之间的差异显著性;以小写字母(a, b, c…)、(a′, b′, c′…)和(a″, b″, c″…)分别标示0、10和20 g·盆-1沼渣施加水平下不同接种水平之间的差异显著性) Fig. 1 Plant dry weights, P concentrations and leaf chlorophyll contents under different experimental treatments |
| 表 2 甘草植株生物量、磷含量及叶片叶绿素含量方差分析结果 Table 2 Two-way ANOVA outputs of dry weights, P concentrations and leaf chlorophyll contents of licorice plants |
施用沼渣显著提高了甘草植株Cr、Cu、Pb含量, 接种处理显著降低了地上部Cu、Pb含量和根系Cr、Cu、Pb含量(表 3、表 4).沼渣处理和接种处理对根系Pb含量存在显著交互作用, 添加20 g·盆-1沼渣和10 g ·盆-1菌剂处理下根系Pb含量最低.
| 表 3 不同处理下甘草地上部Cr、Cu和Pb含量 Table 3 Shoot Cr, Cu and Pb concentrations under different experimental treatments |
| 表 4 不同处理下甘草根系Cr、Cu和Pb含量 Table 4 Root Cr, Cu and Pb concentrations under different experimental treatments |
施加沼渣使土壤磷含量提高了30%~140%, 而接种处理对土壤磷含量无显著影响(表 5).接种处理和施加沼渣均显著增加了土壤有机质含量, 且两因素之间存在显著交互作用:添加20 g·盆-1沼渣和10 g·盆-1菌剂处理下土壤有机质含量最高, 达到对照处理(沼渣施加量和接种剂量均为0 g·盆-1)的1.5倍.
| 表 5 不同处理下土壤有机质及磷含量 Table 5 Soil organic matter contents and P concentrations under different experimental treatments |
添加沼渣显著提高了土壤重金属含量(表 6).与不施加沼渣对照处理(0 g·盆-1)相比, 沼渣施加量为10 g·盆-1情况下土壤Cr、Cu和Pb含量分别增加了5.4%~6.2%, 9.6%~12.8%和6.5%~7.4%;沼渣施加量为20 g·盆-1情况下, 土壤Cr、Cu和Pb含量分别增加了10.9%~11.4%, 22.4%~24.2%和15.1%~16.5%.总体上, 接种处理对土壤重金属含量无显著影响.
| 表 6 不同处理下土壤重金属含量 Table 6 Soil heavy metal concentrations under different experimental treatments |
沼渣作为厌氧发酵的副产物, 含有植物生长所需的多种养分, 而且成本十分低廉.诸多试验已表明, 沼渣作为肥料施于土壤, 可提高土壤中有机质和矿质养分含量, 从而促进农作物增产, 但因为厌氧发酵原料来源较为复杂, 沼渣中可能含有一定量的重金属等有毒有害物质, 在施用过程中有二次污染风险, 进而可能引起农产品质量安全问题.本文正是在该研究背景下开展试验, 选用具有代表性的含有重金属的沼渣, 且在保证添加沼渣后的土壤重金属含量未超出GB15618-2010土壤污染三级标准的前提下, 探讨接种菌根真菌与施用沼渣对甘草生长和重金属吸收的交互影响, 期望通过菌根技术控制沼渣中重金属的污染风险, 为沼渣安全利用提供可能的技术支持.
植物生长所需的矿质养分主要来源于土壤, 而土壤理化性质在很大程度上决定了养分有效性, 对植物的生长有至关重要的影响.本试验中, 添加沼渣使土壤有机质和磷含量分别提高了23%~40%和30%~140%(表 5), 也印证了前人施用沼渣能够提高土壤肥力的试验结果(杨彦等, 2010; Herrmann et al., 2013; 董志新等, 2015).在本试验中, 接种AM真菌也显著增加了土壤有机质含量.已有研究证明, AM共生体能够通过影响根际有机质积淀及土壤团聚结构而影响土壤有机质含量(Wilson et al., 2009; Hoeksema et al., 2010).值得注意的是, 接种AM真菌和施加沼渣对土壤有机质含量存在显著的交互作用, 很可能是由于AM真菌和沼渣通过不同作用机制促进甘草生长和影响土壤有机质含量, 同时因为沼渣中富含矿质养分而对菌根发育会产生直接影响.另一方面, 由于发酵原料来源和成分复杂, 沼渣在提高土壤肥力的同时也可能将一定量的重金属带到土壤中(Duan et al., 2012;Ma et al., 2013).本试验条件下, 添加沼渣提高了土壤Cr、Cu和Pb含量(表 6), 但因为沼渣添加量有限, 因而土壤重金属含量并未超出GB15618-2010土壤污染3级标准(Cr≤400 mg·kg-1, Cu≤400 mg·kg-1, Pb≤500 mg·kg-1).
值得注意的是, 添加沼渣显著抑制了菌根侵染, 使菌根侵染率下降了23%~59%(表 1), 这可能与沼渣富含养分及含有一定量重金属有关.有研究表明, 在养分(尤其是磷)含量较高的土壤中, 植物直接从土壤中吸收的养分能够满足自身生长所需, 因而对AM真菌的依赖性降低(Osorio et al., 2015; Saia et al., 2015);另一方面, 在重金属污染土壤中, 由于重金属的植物毒性和对AM真菌的直接生理毒害, 菌根侵染也会受到抑制(Chen et al., 2005; Liu et al., 2015).尽管如此, 本试验中添加沼渣并未完全抑制AM真菌侵染, 表明AM真菌具有较强的耐逆能力.
沼渣提高土壤肥力最终可反映为对植物生长的促进作用(杨彦等, 2010).在本试验中, 施用沼渣显著提高了植物生物量、磷含量及叶片叶绿素含量(图 1).另一方面, 总体上接种AM真菌也显著促进了甘草生长, 这与众多有关AM真菌促生效应的报道相一致.业已证明, AM真菌主要是通过改善宿主植物矿质营养(尤其磷营养)促进植物生长(Bagyaraj et al., 2015).AM根外菌丝能够直接从土壤中吸收无机磷, 还能分泌磷酸酶和有机酸等分泌物来矿化有机磷, 帮助植物获取生长所需的磷素(童琳等, 2015).本试验中接种处理显著提高了甘草根系磷含量(图 1), 可在一定程度上解释AM接种效应.此外, 很多研究表明, AM共生体系还能通过提高叶片叶绿素含量而促进光合作用(Wu et al., 2010; 张中峰等, 2013; 冉琼等, 2015).本试验中, 接种处理也显著提高了叶片叶绿素含量(图 1), 从另一角度解释了AM共生体对植物的促生作用.
不能忽视的是, AM真菌对植物生长和矿质营养的影响受到沼渣施加量的显著影响:在沼渣施加量较高情况下(特别是20 g·盆-1添加水平), 接种处理对植物生长没有明显影响, 甚至还降低了植物地上部磷含量(图 1).这主要是因为添加沼渣大幅度提高了土壤磷含量(表 5), 使得土壤磷素供应充分(植株磷含量可很好映证), 因而植物对菌根的依赖程度显著降低(表现为菌根侵染率显著下降), 从另一角度来看, 即表现为菌根对植物生长没有显著积极作用.尽管表观上AM真菌对植物生长和磷营养没有积极作用, 但并不意味着AM真菌对宿主没有实质贡献(Grace et al., 2009; Smith et al., 2012), 毕竟在较高沼渣施加量下, 仍有一定程度的菌根侵染.不管怎样, 本试验结果表明, 沼渣施用量和菌根真菌接种剂量对于二者交互作用有重要影响, 在实际应用中需要考虑最合适的配比以最大限度发挥沼渣和AM真菌的积极作用.
施加沼渣显著提高了植株Cr、Cu、Pb含量, 且在添加10 g·盆-1沼渣处理下, 未接种甘草根系Cr和Pb含量超出安全标准(2010年版《中国药典》甘草重金属含量安全标准, Cr≤10 mg·kg-1, Cu≤20 mg·kg-1, Pb≤20 mg·kg-1)46%和18%;添加20 g·盆-1沼渣处理下, 未接种甘草地上部Cu、根系Cr、Cu和Pb含量各超出标准10%、64%、65%和47%(表 3、表 4);沼渣的添加对未接种甘草地上部Cr和Pb含量无显著影响, 这可能是由于本试验周期较短(60 d), 同时Cr和Pb在植物体内的转移和再分配比较有限.另一方面, 接种处理显著降低了植株地上部Cu、Pb含量和根系Cr、Cu、Pb含量, 降低幅度分别达到21%~71%、9%~27%、13%~43%、22%~58%和25%~40%(表 3、表 4).AM共生体系不仅有效缓解了沼渣中重金属的对植物的潜在毒害, 更重要的是使植物重金属含量均降低至安全阈值以内.目前有关AM真菌对宿主植物吸收累积重金属的影响仍有一定争议(Hassan et al., 2011; Saraswat et al., 2011), 多数研究表明, AM共生体系能够降低植物体内重金属含量(Chen et al., 2007; Wu et al., 2014; Zhang et al., 2015; Wu et al., 2016), 而在一些试验条件下, AM真菌通过直接吸收和传输重金属而使植物体内重金属含量增高(Alguacil et al., 2011; Aghababaei et al., 2014; Arias et al., 2015).不管怎样, 本试验证实AM真菌能有效降低甘草重金属含量, 从而消除或降低施用沼渣可能带来的重金属污染风险.因此, 施用沼渣和接种AM真菌相结合在很大程度上有利于建立经济安全高效的甘草人工种植体系.
5 结论(Conclusions)本试验表明, 施用沼渣能够提高土壤肥力、促进植物生长, 而AM真菌在促进植物有效利用土壤养分的同时, 有效控制了沼渣中重金属的污染风险, 因此, 施用沼渣结合接种AM真菌为沼渣安全利用提供了一种可能的技术途径.考虑到沼渣和AM真菌对植物生长和矿质营养的复杂交互作用, 仍需要进一步试验探索二者最佳配施条件.此外, 甘草是多年生植物, 而本试验周期较短(60 d)且在控制环境条件下完成, 因此, 有必要开展长期田间试验, 系统考察沼渣和AM真菌应用于甘草种植体系的安全性和综合效益.
责任作者简介:陈保冬(1975-), 男, 中国科学院生态环境研究中心城市与区域生态国家重点实验室研究员, 博士生导师, 主要研究方向为土壤生态过程与生态重建.E-mail: bdchen@rcees.ac.cn.
| [${referVo.labelOrder}] | Abubaker J, Cederlund H, Arthurson V, et al. 2013. Bacterial community structure and microbial activity in different soils amended with biogas residues and cattle slurry[J]. Applied Soil Ecology, 72 : 171–180. DOI:10.1016/j.apsoil.2013.07.002 |
| [${referVo.labelOrder}] | Aghababaei F, Raiesi F, Fiosseinpur A. 2014. The influence of earthworm and mycorrhizal co-inoculation on Cd speciation in a contaminated soil[J]. Soil Biology & Biochemistry, 78 : 21–29. |
| [${referVo.labelOrder}] | Alguacil M M, Torrecillas E, Caravaca F, et al. 2011. The application of an organic amendment modifies the arbuscular mycorrhizal fungal communities colonizing native seedlings grown in a heavy-metal-polluted soil[J]. Soil Biology & Biochemistry, 43(7) : 1498–1508. |
| [${referVo.labelOrder}] | Arias M S, Peña Cabriales J J, Alarcón A, et al. 2015. Enhanced Pb absorption by Hordeum vulgare L.and Helianthus annuus L.plants inoculated with an arbuscular mycorrhizal fungi consortium[J]. International Journal of Phytoremediation, 17(5) : 405–413. DOI:10.1080/15226514.2014.898023 |
| [${referVo.labelOrder}] | Abubaker J, Risberg K, Pell M. 2012. Biogas residues as fertilisers-effects on wheat growth and soil microbial activities[J]. Applied Energy, 99 : 126–134. DOI:10.1016/j.apenergy.2012.04.050 |
| [${referVo.labelOrder}] | Bagyaraj D J, Sharma M P, Maiti D. 2015. Phosphorus nutrition of crops through arbuscular mycorrhizal fungi[J]. Current Science, 108(7) : 1288–1293. |
| [${referVo.labelOrder}] | Biermann B, Linderman R G. 1981. Quantifying vesicular-arbuscular mycorrhizae: a proposed method towards standardization[J]. New Phytologist, 87(1) : 63–67. DOI:10.1111/nph.1981.87.issue-1 |
| [${referVo.labelOrder}] | Chen B D, Xiao X Y, Zhu Y G, et al. 2007. The arbuscular mycorrhizal fungus Glomus mosseae gives contrary effects on phosphorus and arsenic acquisition by Medicago sativa Linn.[J]. Science of the Total Environment, 379(2/3) : 226–234. |
| [${referVo.labelOrder}] | Chen B D, Zhu Y G, Zhang X H, et al. 2005. The influence of mycorrhiza on uranium and phosphorus uptake by barley plants from a field-contaminated soil[J]. Environmental Science and Pollution Research, 12(6) : 325–331. DOI:10.1065/espr2005.06.267 |
| [${referVo.labelOrder}] | 陈苗, 白帆, 崔岩山. 2012. 几种沼渣中Cu和Zn的含量及其形态分布[J]. 环境化学, 2012, 31(2) : 175–181. |
| [${referVo.labelOrder}] | 董志新, 李筱梅, 续珍, 等. 2015. 沼渣有机无机复混肥对土壤养分含量和酶活性的影响[J]. 土壤通报, 2015, 46(2) : 398–404. |
| [${referVo.labelOrder}] | Duan G, Zhang H, Liu Y, et al. 2012. Long-term fertilization with pig-biogas residues results in heavy metal accumulation in paddy field and rice grains in Jiaxing of China[J]. Soil Science and Plant Nutrition, 58(5) : 637–646. DOI:10.1080/00380768.2012.726597 |
| [${referVo.labelOrder}] | Grace E J, Cotsaftis O, Tester M, et al. 2009. Arbuscular mycorrhizal inhibition of growth in barley cannot be attributed to extent of colonization, fungal phosphorus uptake or effects on expression of plant phosphate transporter genes[J]. New Phytologist, 181 : 938–949. DOI:10.1111/j.1469-8137.2008.02720.x |
| [${referVo.labelOrder}] | Hassan S E D, Boon E, St Arnaud M, et al. 2011. Molecular biodiversity of arbuscular mycorrhizal fungi in trace metal-polluted soils[J]. Molecular Ecology, 20(16) : 3469–3483. DOI:10.1111/mec.2011.20.issue-16 |
| [${referVo.labelOrder}] | Hoeksema J D, Chaudhary V B, Gehring C A, et al. 2010. A meta-analysis of context-dependency in plant response to inoculation with mycorrhizal fungi[J]. Ecology Letters, 13(3) : 394–407. DOI:10.1111/ele.2010.13.issue-3 |
| [${referVo.labelOrder}] | Herrmann A, Sieling K, Wienforth B, et al. 2013. Short-term effects of biogas residue application on yield performance and N balance parameters of maize in different cropping systems[J]. Journal of Agricultural Science, 151(4) : 449–462. DOI:10.1017/S0021859612000548 |
| [${referVo.labelOrder}] | Liu H, Yuan M, Tan S Y, et al. 2015. Enhancement of arbuscular mycorrhizal fungus (Glomus versiforme) on the growth and Cd uptake by Cd-hyperaccumulator Solanum nigrum[J]. Applied Soil Ecology, 89 : 44–49. DOI:10.1016/j.apsoil.2015.01.006 |
| [${referVo.labelOrder}] | Ma J, Zhu H, Fan M. 2013. Distribution of heavy metals in pig farm biogas residues and the safety and feasibility assessment of biogas fertilizer[J]. International Journal of Agricultural and Biological Engineering, 6(4) : 35–43. |
| [${referVo.labelOrder}] | Osorio N W, Habte M. 2015. Effect of a phosphate-solubilizing fungus and an arbuscular mycorrhizal fungus on leucaena seedlings in tropical soils with contrasting phosphate sorption capacity[J]. Plant and Soil, 389(1/2) : 375–385. |
| [${referVo.labelOrder}] | Phillips J M, Hayman D S. 1970. Improved procedure of clearing roots and staining parasitic and vesicular-arbuscular mycorrhizal fungi for rapid assessment of infection[J]. Transactions of the British Mycological Society, 55(1) : 159–161. |
| [${referVo.labelOrder}] | 冉琼, 钟章成. 2015. 模拟岩溶旱钙土壤基质中AM真菌对玉米幼苗光合生长的影响[J]. 生态学报, 2015, 35(2) : 460–467. |
| [${referVo.labelOrder}] | Saia S, Ruisi P, Fileccia V, et al. 2015. Metabolomics suggests that soil inoculation with arbuscular mycorrhizal fungi decreased free amino acid content in roots of durum wheat grown under N-limited, P-rich field conditions[J]. Plos One, 10(6) : e0129591. DOI:10.1371/journal.pone.0129591 |
| [${referVo.labelOrder}] | Saraswat S, Rai J P N. 2011. Mechanism of metal tolerance and detoxification in mycorrhizal fungi[J]. Biomanagement of Metal-Contaminated Soils, 20 : 225–240. DOI:10.1007/978-94-007-1914-9 |
| [${referVo.labelOrder}] | Smith S E, Read D. 2008. Mycorrhizal Symbiosis[M]. San Diego: Academic Press 148-158, 174-175, 182-186. |
| [${referVo.labelOrder}] | Smith S E, Smith F A. 2012. Fresh perspectives on the roles of arbuscular mycorrhizal fungi in plant nutrition and growth[J]. Mycologia, 104 : 1–13. DOI:10.3852/11-229 |
| [${referVo.labelOrder}] | 孙吉庆, 刘润进, 李敏. 2012. 丛枝菌根真菌提高植物抗逆性的效应及其机制研究进展[J]. 植物生理学报, 2012, 48(9) : 845–852. |
| [${referVo.labelOrder}] | Svoboda N, Taube F, Wienforth B, et al. 2013. Nitrogen leaching losses after biogas residue application to maize[J]. Soil and Tillage Research, 130 : 69–80. DOI:10.1016/j.still.2013.02.006 |
| [${referVo.labelOrder}] | 田庆来, 官月平, 张波, 等. 2006. 甘草有效成分的药理作用研究进展[J]. 天然产物研究与开发, 2006, 18(2) : 343–347. |
| [${referVo.labelOrder}] | 童琳, 唐旭利, 张静, 等. 2015. 菌根形成对不同成熟度的森林优势树种磷吸收的影响[J]. 生态科学, 2015, 34(4) : 93–98. |
| [${referVo.labelOrder}] | Wu Q S, Zou Y N, He X H. 2010. Contributions of arbuscular mycorrhizal fungi to growth, photosynthesis, root morphology and ionic balance of citrus seedlings under salt stress[J]. Acta Physiologiae Plantarum, 32(2) : 297–304. DOI:10.1007/s11738-009-0407-z |
| [${referVo.labelOrder}] | Wu S L, Chen B D, Sun Y, et al. 2014. Chromium resistance of dandelion (Taraxacum platypecidum Diels[J]. ) and bermudagrass (Cynodon dactylon [Linn.] Pers.) is enhanced by arbuscular mycorrhiza in Cr (VI)-contaminated soils[J].Environmental Toxicology & Chemistry, 33(9) : 2105–2113. |
| [${referVo.labelOrder}] | Wu S L, Zhang X, Chen B D, et al. 2016. Chromium immobilization by extraradical mycelium of arbuscular mycorrhiza contributes to plant chromium tolerance[J]. Environmental and Experimental Botany, 122 : 10–18. DOI:10.1016/j.envexpbot.2015.08.006 |
| [${referVo.labelOrder}] | Wilson G W T, Rice C W, Rillig M C, et al. 2009. Soil aggregation and carbon sequestration are tightly correlated with the abundance of arbuscular mycorrhizal fungi: results from long-term field experiments[J]. Ecology Letters, 12(5) : 452–461. DOI:10.1111/ele.2009.12.issue-5 |
| [${referVo.labelOrder}] | 伍松林, 张莘, 陈保冬. 2013. 丛枝菌根对土壤-植物系统中重金属迁移转化的影响[J]. 生态毒理学报, 2013, 8(6) : 847–856. |
| [${referVo.labelOrder}] | 谢景欢, 陈钢, 袁巧霞, 等. 2010. 沼渣与化肥配合施用对温室番茄生长发育、产量及品质的影响[J]. 应用生态学报, 2010, 21(9) : 2353–2357. |
| [${referVo.labelOrder}] | 杨彦, 裴宇, 洪坚平. 2010. 菌肥沼渣配施对采煤塌陷复垦土壤养分与油菜品质的影响[J]. 山西农业科学, 2010, 38(1) : 68–72. |
| [${referVo.labelOrder}] | Zhang X, Ren B H, Wu S L, et al. 2015. Arbuscular mycorrhizal symbiosis influences arsenic accumulation and speciation in Medicago truncatula L.in arsenic-contaminated soil[J]. Chemosphere, 119 : 224–230. DOI:10.1016/j.chemosphere.2014.06.042 |
| [${referVo.labelOrder}] | 张中峰, 张金池, 黄玉清, 等. 2013. 接种丛枝菌根真菌对青冈栎幼苗生长和光合作用的影响[J]. 广西植物, 2013, 33(3) : 319–323. |
 2016, Vol. 36
2016, Vol. 36


