2. 农业部农村可再生能源开发利用重点实验室, 成都 610041
2. Key Laboratoary of Development and Application of Rural Renewable Energy of Ministry of Agriculture, Chengdu 610041
餐厨垃圾废弃物含有丰富的脂类,是很好的厌氧发酵原料.由于脂类的产甲烷潜力高于相同质量的碳水化合物(Angelidaki and Sanders, 2004),所以在厌氧发酵过程中有助于甲烷产量的提升(Li et al.,2002) .但是,当脂类降解和转化的产物长链脂肪酸(LCFA)累积到一定浓度的时候,将会导致厌氧发酵受到抑制,甲烷产量明显下降(Silva et al.,2014; 任连海等,2015; Meng et al.,2015) .
针对长链脂肪酸对厌氧发酵抑制浓度和抑制机理的研究尚未形成统一的观点.周洪波等的研究表明,油酸(C18:1) 半抑制浓度(IC50) 值为1.8 g · L-1(周洪波等,2002).根据Chen等的报道,油酸(C18 ∶ 1) 的IC50值为1.2 g · L-1(Chen et al.,2008) .由于油酸在水中难溶,Palatsi等采用LCFA的钠盐(油酸钠、硬脂酸钠、棕榈酸钠混合物)进行了猪粪的高温厌氧发酵的抑制实验,发现当LCFA混合物的浓度大于1.0 g · L-1时,会对厌氧发酵造成抑制(Palatsi et al.,2009) .Hwu等研究了LCFA对UASB反应器中颗粒污泥的抑制机理研究,发现在LCFA的作用下可以造成反应器中微生物的细胞膜或细胞壁的溶解(Hwu et al.,1998) .也有学者研究了不同类型反应器中LCFA对厌氧污泥的影响,认为是LCFA包裹在微生物上,限制了营养物质的传输,从而抑制了微生物的生长(Pereira et al.,2005; MmAlves,2001).
目前,餐厨垃圾多采用两相厌氧发酵工艺处理(陈雪等,2015),餐厨垃圾油脂中的长链脂肪酸对利用乙酸产甲烷过程的抑制作用是两相厌氧发酵工艺的难点之一,但是相关研究报道并不多.因此本文采用批式实验,在中温(35±1) ℃条件下,研究了油酸钠对累积甲烷产量、产甲烷古菌数量以及发酵过程中乙酸代谢和氢分压的影响,以期为提高餐厨垃圾厌氧消化中油脂的转化效率提供参考.
2 材料与方法(Materials and methods) 2.1 实验材料选用连续运行1年的餐厨垃圾两相厌氧发酵装置中的产甲烷相反应器出水作为接种液(性质见表 1),将取得的接种液放置在(35±1) ℃培养箱中,培养至产气不再增加后使用,目的是消除接种液中原有底物对实验造成的误差.油酸钠采用分析纯油酸钠试剂.乙酸溶液由分析纯冰醋酸配置而成.
| 表 1 接种液的性质 Table 1 The Characteristics of inoculated solution |
实验采用批式发酵法,500 mL的血清瓶作为发酵容器,采用丁基橡胶塞及铝封密封,有效发酵体积为300 mL.
2.3 实验设计实验设置6个处理组,每组设置3个平行实验,分别加入0.27 mol · L-1乙酸溶液50 mL作为底物,加入250 mL浓度为10 g · L-1的餐厨垃圾厌氧发酵产甲烷相出水作为接种液,而后分别加入浓度为0.0、2.0、4.0、6.0、8.0、10.0 g · L-1的油酸钠作为抑制物质(见表 2).最后,各处理组通入氮气5 min,并用丁基橡胶瓶塞和铝封封口,放入恒温培养箱中进行厌氧发酵.每日检测产气量、甲烷含量、氢分压、VFA含量.待发酵30 d结束后,测定各个处理组中发酵液的脂肪酸成分,并对微生物总量和产甲烷古菌数量进行微生物计数.
| 表 2 实验设计 Table 2 Experimental set-up |
日产气量采用排水集气法每日收集并记录体积;甲烷含量、二氧化碳含量和氢气压力测定通过气相色谱法,仪器型号为:岛津GC-2010,色谱条件为:60 m Parapak-QX色谱柱,柱箱温度:50 ℃,进样器温度150 ℃,检测器温度:200 ℃;挥发性脂肪酸(VFA)含量测定采用气相色谱法,仪器型号为:上分GC112A,色谱条件为:1.5 m GDX103+5%磷酸色谱柱,柱温160 ℃,进样器温度210 ℃,检测器温度230 ℃(赵兴涛等,2013);pH值采用雷磁PHS-25型pH计测定;长链脂肪酸(LCFA)含量测定采用气相色谱与质谱联用法,取第30 d各处理组发酵液,离心、过滤后取上清液,将上清液以乙酸乙酯为溶剂,通过萃取、旋转蒸发、氮吹等步骤获得LCFA,向所获得的LCFA样品中添加BSTFA试剂衍生化后上机分析.GC-MS型号为:安捷伦7890A-5975C,质谱库采用NIST11版(Sparkman et al.,2013) .LCFA采用“中文名称(C碳原子个数:不饱和键个数)”的方式表示,例如:油酸(C18 ∶ 1) ,即油酸有18个碳原子,一个不饱和键;微生物计数采用文献(张云飞等,2011)中提供的方法,其原理是利用产甲烷古菌特有的F420酶可以在紫外光激发下发出荧光的特点(吴唯民,蒋青,1984),分别在可见光下和在紫外光下计出总微生物数量与产甲烷古菌数量;实验所得数据应用SPSS软件进行分析,应用Origin9.0做图;
2.5 油酸钠的甲烷转化率(CR)的计算油酸钠的理论甲烷产量(式3) ,可以通过Buswall公式(式 1) 得出(Li et al.,2013; Meng et al.,2015) .油酸钠的甲烷转化率(CR)公式(式4) ,可由实际油酸钠产甲烷量(EMY)和理论产甲烷量(TMY)(式3) 相比得出.
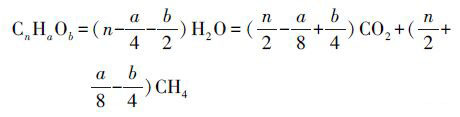
|
(1) |
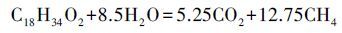
|
(2) |
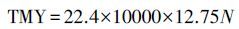
|
(3) |
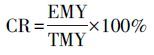
|
(4) |
式中: n、a、b为C、H、O原子个数; TMY为油酸钠理论产甲烷量(mL); N为各处理组油酸钠总摩尔数(mol); EMY为油酸钠实际产甲烷量(等于各处理组累积甲烷产量减去CK组累积甲烷产量)(mL); CR为油酸钠降解率.
3 结果与分析(Results and discussion) 3.1 油酸钠对产甲烷过程的影响图 1为油酸钠对厌氧发酵产甲烷过程的影响.从图中可看出,CK组产气延滞期为0 d,而其余处理组随着油酸钠浓度升高,各实验组产气延滞期依次延长.油酸钠浓度为2.0、4.0、6.0 g · L-1处理组分别经历了5 d、12 d和19 d的产甲烷延滞期,经过延滞期后可正常产气;油酸钠浓度为8.0 g · L-1和10.0 g · L-1处理组的产气延滞期达到了30 d以上,厌氧发酵被完全抑制.该现象与Cavaleiro等观察到产甲烷延滞期随油酸钠浓度的增加而延长的结果相似(Cavaleiro et al.,2008) .
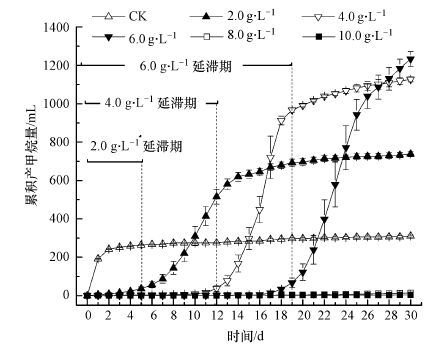 |
| 图 1 不同浓度油酸钠对累积甲烷产量的影响 Fig. 1 Variation of cumulative methane yields at different sodium oleate concentration |
从图 1中还可以发现,不同浓度的油酸钠对累积甲烷产量也有着重要的影响.截至第30 d时,CK组累积产甲烷量为310 mL;油酸钠浓度为2.0~6.0 g · L-1处理组的累积产甲烷量为738 mL、1126 mL和1233 mL,分别是CK组第30 d累积产甲烷量的238%、367%和397%;8.0 g · L-1和10.0 g · L-1处理组(图 1中累积产甲烷曲线重叠)到第30 d累积产甲烷量较低,分别仅为14 mL和4 mL.任连海等在油脂厌氧发酵实验中也发现,当油脂的负荷超过一定范围时,会对厌氧发酵产生抑制作用,导致累计产甲烷量下降(任连海等,2015).
上述结果显示,油酸钠浓度为2.0~6.0 g · L-1处理组累积产气量远高于CK组,说明除了加入的乙酸可以被转化为甲烷外,油酸钠也可以被转化为甲烷.采用Buswall公式对油酸钠的甲烷转化率(CR)进行计算,结果见表 3.由表 3可以看出,油酸钠浓度为2.0~6.0 g · L-1处理组CR值分别为76%、72%和55%;油酸钠浓度为8.0 g · L-1和10.0 g · L-1处理组CR值为0,说明这两组的厌氧发酵产甲烷过程受到了严重的抑制.王静等通过研究也发现,当厌氧发酵受到油脂抑制时,油脂无法正常转化为甲烷(王静,杨殿海,2012).
| 表 3 油酸钠的甲烷转化率(CR) Table 3 Conversion rate of sodium oleate |
本研究采用荧光显微镜计数的方法对各处理组的产甲烷古菌数量进行统计,来评价油酸钠对微生物的影响(结果见表 4).发酵第30 d时微生物计数结果显示,各处理之间总微生物数量差异不显著(p=0.241>0.01) ,而各处理之间产甲烷古菌数量差异显著(p=0.00<0.01) ,说明油酸钠的加入对产甲烷古菌造成了严重抑制.产甲烷古菌数量占总微生物数量比例(A/M)最高的处理组为CK组,所占比例为23.88%.添加了油酸钠的各实验组中A/M值均低于CK组,且A/M值随着油酸钠浓度的升高而逐渐下降,分别为6.31%、7.49%、6.72%、2.18%和1.38%.
| 表 4 微生物计数结果 Table 4 Result of microorganism count |
上述结果结合3.1节结果说明,油酸钠使厌氧发酵中产甲烷古菌数量大幅度减少是产甲烷过程受到抑制的主要原因.该现象与Angelidaki等在研究中观察到,油酸钠的加入对产甲烷古菌产生了抑制作用,使产甲烷古菌数量大幅度减少的现象一致(Angelidaki and Ahring, 1992).
3.3 油酸钠中间代谢产物分析3.1节的结果显示,高浓度的油酸钠会抑制厌氧发酵产甲烷过程,而低浓度的油酸钠可以作为厌氧发酵底物被微生物利用.油酸钠在发酵过程中可以通过β氧化途径生成不同种类的脂肪酸(Long et al.,2012) ,因此本研究检测了油酸钠在厌氧发酵中的中间代谢产物.图 2结果显示,所有实验组中均未检测到油酸(C18 ∶ 1) ,说明油酸(C18 ∶ 1) 可以被微生物分解;所有实验组中均检测出棕榈酸(C16 ∶ 0) 和硬脂酸(C18 ∶ 0) ,这是由于实验采用含油脂的餐厨垃圾厌氧发酵液作为接种液,其中残留少量棕榈酸(C16 ∶ 0) 和硬脂酸(C18 ∶ 0) ,且这两种脂肪酸难以在厌氧消化过程中被利用(Rasit et al.,2015) .
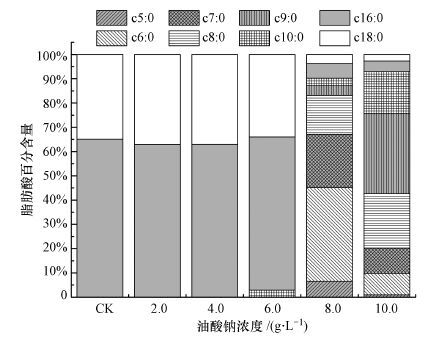 |
| 图 2 中间代谢产物分析 Fig. 2 Intermediate metabolite analysis |
结合图 1、图 2和表 3可以看出,油酸钠浓度为2.0 g · L-1和4.0 g · L-1处理组,受到抑制较轻,经过延滞期后可正常产甲烷,且未检测到油酸钠的其他中间代谢产物,故这两组油酸钠在厌氧发酵过程中甲烷转化率较高;而在油酸钠浓度为6.0 g · L-1处理组中,受到部分抑制,经过较长的延滞期后可正常产甲烷,并且检测到含量为3%的癸酸(C10 ∶ 0) ,因此该组中油酸钠的甲烷转化率低于前两组;油酸钠浓度为8.0 g · L-1和10.0 g · L-1处理组被油酸钠完全抑制,截至第30 d仍未正常产甲烷,且检测到多种脂肪酸.其中8.0 g · L-1处理组的脂肪酸以己酸(C6 ∶ 0) 和庚酸(C7 ∶ 0) 为主,约占总含量的60%,而10.0 g · L-1处理组中的脂肪酸以辛酸(C8 ∶ 0) 和壬酸(C9 ∶ 0) 为主,约占总含量的56%,这两组中油酸的甲烷转化率为0.Cirne等利用不同种类脂肪酸模拟含油废水进行厌氧发酵也观察到(Cirne et al.,2007) 反应初期加入过多的油酸钠会抑制产甲烷过程,生成的脂肪酸不能够进一步被微生物利用,从而累积在发酵液中.
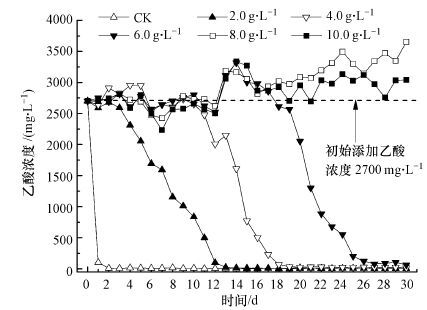 |
| 图 3 油酸钠对乙酸代谢的影响 Fig. 3 Variation of acetate content at different sodium oleate concentration |
在两相厌氧消化中,餐厨垃圾在水解相被分解成挥发性有机酸(主要是乙酸),而在厌氧发酵产甲烷过程中大约70%的甲烷由乙酸代谢途径生成(贺延龄,1998),因此本实验研究了在油酸钠作用下乙酸的代谢过程.图 3为油酸钠对乙酸代谢的影响,虚线所示为乙酸的起始添加浓度.CK组由于只添加了乙酸,在第1 d乙酸很快被降解,2 d后基本被完全转化为甲烷.而其他的处理组由于厌氧发酵受到抑制,乙酸在实验初期未降解,其浓度均为2700 mg · L-1左右.油酸钠浓度为2.0~6.0 g · L-1的处理组经过产甲烷延滞期后(图 1),乙酸开始被降解,分别经过13 d、19 d和28 d后基本被完全转化为甲烷.油酸钠浓度为8.0 g · L-1、10.0 g · L-1的处理组,乙酸代谢和产甲烷(3.1节)被完全抑制,乙酸浓度呈缓慢增加的趋势,且不能被转化为甲烷.Lalman等通过向厌氧发酵液中添加油酸后也证实油酸的加入会对利用乙酸代谢产生抑制作用(Lalman and Bagley, 2001).
乙酸浓度的变化会影响发酵液的pH值.结合图 3、图 4可以看出油酸钠浓度为2.0~6.0 g · L-1的处理组经过产甲烷延滞期(图 1)后,乙酸浓度出现明显下降,pH值逐渐恢复到正常水平(6.8~7.2) ,与Kabouris等观察到的将油脂加入厌氧发酵液中会引起发酵液pH值改变的现象一致(Kabouris et al.,2009) ;油酸钠浓度为8.0 g · L-1和10.0 g · L-1的处理组,乙酸代谢和产甲烷(3.1节)被完全抑制,乙酸浓度呈缓慢增加的趋势,经过30 d后pH值未达到正常水平.
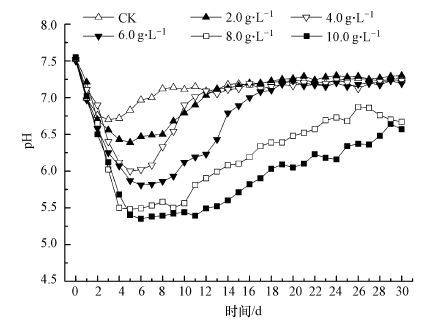 |
| 图 4 油酸钠对pH值的影响 Fig. 4 Variation of pH at different sodium oleate concentration |
根据相关报道,氢分压越低越有利于厌氧发酵进行(薛旭东,彭党聪,2012),因此本研究也对发酵过程中氢分压的变化做了检测,图 5为氢分压的变化规律.从图 5a中可以看出,在30 d的实验周期内,CK组的氢分压保持在很低的水平,且未产生明显变化;油酸钠浓度为2.0、4.0 g · L-1组氢分也压保持在较低的水平且波动幅度不大,仅4.0 g · L-1组在实验初始阶段,短时间内氢分压达到29Pa,说明利用H2/CO2产甲烷途径并未受到抑制;从图 5b中可以看出,油酸钠浓度为6.0 g · L-1的处理组在实验前期氢分压大幅度波动,最高氢分压达到了117 Pa,说明利用H2/CO2产甲烷途径受到影响.在实验后期氢分压下降,甲烷产出(图 1),说明利用H2/CO2产甲烷途径抑制解除;油酸钠浓度为8.0 g · L-1和10.0 g · L-1的处理组,实验前期氢分压大幅度上升,最高氢分压分别达到了71 Pa和105 Pa,无甲烷生成,说明利用H2/CO2产甲烷途径受到严重抑制.实验后期氢分压下降,仅少量甲烷产出(图 1),其原因不明,有待进一步研究.上述实验结果说明,随着油酸钠浓度的增加,对H2/CO2代谢途径抑制作用逐渐增强;当油酸钠浓度超过8.0 g · L-1时,利用H2/CO2产甲烷途径被完全抑制.Lokshina等在含油废水抑制厌氧发酵的实验中也观察到了氢分压升高的现象(Lokshina et al.,2003) .
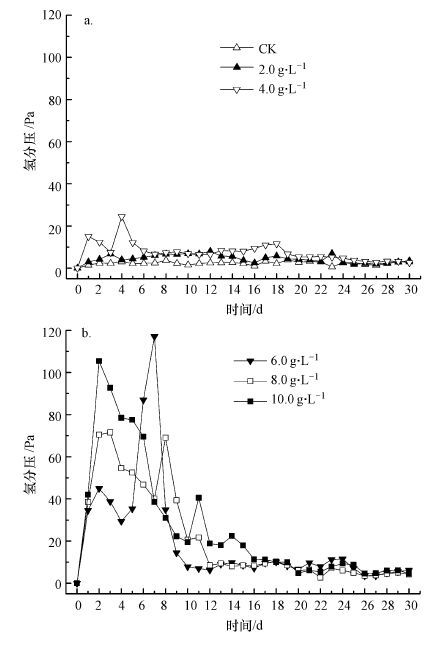 |
| 图 5 油酸钠对氢分压的影响 Fig. 5 Variation of hydrogen partial pressure at different sodium oleate concentration |
1) 油酸钠会对产甲烷过程产生抑制作用,延滞期随油酸钠浓度增加而延长;油酸钠浓度低于6.0 g · L-1的处理组,经过延滞期后乙酸代谢恢复正常,可以完全被转化为甲烷;油酸钠浓度高于8.0 g · L-1的处理组乙酸代谢受到严重抑制,只有少量甲烷生成.
2) 油酸钠浓度低于6.0 g · L-1时,部分油酸可被转化为甲烷;油酸钠浓度高于8.0 g · L-1时,油酸分解形成长链脂肪酸和乙酸等中间代谢产物,油酸钠的转化率为0.
3) 油酸钠对厌氧发酵中微生物总量影响不明显,但对产甲烷古菌有严重的抑制作用.产甲烷古菌数量大幅度减少是乙酸代谢过程受到抑制的主要原因.
4) 油酸钠的添加量超过6.0 g · L-1时,在实验初期会引起产甲烷相中氢分压的升高,也证实了油酸钠对厌氧发酵的抑制作用.
| [1] | Angelidaki I, Ahring B K. 1992. Effects of free long-chain fatty acids on thermophilic anaerobic digestion[J]. Applied Microbiology and Biotechnology , 37 (6) : 808–812. |
| [2] | Angelidaki I, Sanders W. 2004. Assessment of the anaerobic biodegradability of macropollutants[J]. Re/Views in Environmental Science & Bio/Technology , 3 (2) : 117–129. |
| [3] | Cavaleiro A J, Pereira M A, Alves M. 2008. Enhancement of methane production from long chain fatty acid based effluents[J]. Bioresource Technology , 99 (10) : 4086–4095. DOI:10.1016/j.biortech.2007.09.005 |
| [4] | Chen Y, Cheng J J, Creamer K S. 2008. Inhibition of anaerobic digestion process: A review[J]. Bioresource Technology , 99 (10) : 4044–4064. DOI:10.1016/j.biortech.2007.01.057 |
| [5] | Cirne D G, Paloumet X, Björnsson L, et al. 2007. Anaerobic digestion of lipid-rich waste-Effects of lipid concentration[J]. Renewable Energy , 32 (6) : 965–975. DOI:10.1016/j.renene.2006.04.003 |
| [6] | Hwu C, Tseng S, Yuan C, et al. 1998. Biosorption of long-chain fatty acids in UASB treatment process[J]. Water Research , 32 (5) : 1571–1579. DOI:10.1016/S0043-1354(97)00352-7 |
| [7] | Kabouris J C, Ulas T, Pavlostathis S G, et al. 2009. Mesophilic and thermophilic anaerobic digestion of municipal sludge and fat, oil, and grease.[J]. Water Environment Research A Research Publication of the Water Environment Federation, 81(5): 476-485 |
| [8] | Lalman J A, Bagley D M. 2001. Anaerobic degradation and methanogenic inhibitory effects of oleic and stearic acids[J]. Water Research , 35 (12) : 2975–2983. DOI:10.1016/S0043-1354(00)00593-5 |
| [9] | Li Y Y, Sasaki H, Yamashita K, et al. 2002. High-rate methane fermentation of lipid-rich food wastes by a high-solids co-digestion process[J]. Water Sci Technol , 45 (12) : 143–150. |
| [10] | Li Y, Zhang R, Liu G, et al. 2013. Comparison of methane production potential, biodegradability, and kinetics of different organic substrates[J]. Bioresource Technology , 149 : 565–569. DOI:10.1016/j.biortech.2013.09.063 |
| [11] | Long J H, Aziz T N, Francis L, et al. 2012. Anaerobic co-digestion of fat, oil, and grease (FOG): a review of gas production and process limitations[J]. Process Safety and Environmental Protection , 90 (3) : 231–245. DOI:10.1016/j.psep.2011.10.001 |
| [12] | Meng Y, Li S, Yuan H, et al. 2015. Evaluating biomethane production from anaerobic mono- and co-digestion of food waste and floatable oil (FO) skimmed from food waste[J]. Bioresource Technology , 185 : 7–13. DOI:10.1016/j.biortech.2015.02.036 |
| [13] | Meng Y, Li S, Yuan H, et al. 2015. Effect of lipase addition on hydrolysis and biomethane production of Chinese food waste[J]. Bioresource Technology , 179 : 452–459. DOI:10.1016/j.biortech.2014.12.015 |
| [14] | Mm Alves J V R P. 2001. Effects of lipids and oleic acid on biomass development in anaerobic fixed-bed reactors. Part II: Oleic acid toxicity and biodegradability[J]. Water Research , 35 (1) : 260–270. |
| [15] | Palatsi J, Laureni M, Andrés M V, et al. 2009. Strategies for recovering inhibition caused by long chain fatty acids on anaerobic thermophilic biogas reactors[J]. Bioresource Technology , 100 (20) : 4588–4596. DOI:10.1016/j.biortech.2009.04.046 |
| [16] | Pereira M A, Pires O C, Mota M, et al. 2005. Anaerobic biodegradation of oleic and palmitic acids: evidence of mass transfer limitations caused by long chain fatty acid accumulation onto the anaerobic sludge[J]. Biotechnology & Bioengineering , 92 (1) : 15–23. |
| [17] | Rasit N, Idris A, Harun R, et al. 2015. Effects of lipid inhibition on biogas production of anaerobic digestion from oily effluents and sludges: An overview[J]. Renewable and Sustainable Energy Reviews , 45 (0) : 351–358. |
| [18] | Silva S A, Cavaleiro A J, Pereira M A, et al. 2014. Long-term acclimation of anaerobic sludges for high-rate methanogenesis from LCFA[J]. Biomass and Bioenergy , 67 : 297–303. DOI:10.1016/j.biombioe.2014.05.012 |
| [19] | Sparkman O D, Penton Z E, Kitson F G. 2013. Gas Chromatography and Mass Spectrometry: A Practical Guide[M]. 北京: 科学出版社: 221 -229. |
| [20] | 贺延龄. 1998. 废水的厌氧生物处理[M]. 北京: 中国轻工业出版社: 17 -18. |
| [21] | 任连海, 黄燕冰, 王攀, 等.2015. 含油率对餐厨垃圾干式厌氧发酵的影响[J]. 环境科学学报 , 2015, 35 (8) : 2534–2539. |
| [22] | 王静, 杨殿海.2012. 剩余污泥与废弃油脂混合厌氧消化产气缓滞因素研究[J]. 环境科学学报 , 2012, 32 (5) : 1088–1094. |
| [23] | 汪善全, 原媛, 孔云华, 等.2008. 好氧颗粒污泥处理高含盐废水研究[J]. 环境科学 , 2008 (1) : 145–151. |
| [24] | 吴唯民, 蒋青.1984. 辅酶F_(420)及其在厌氧处理中的作用[J]. 中国沼气 , 1984 (2) : 3–11. |
| [25] | 张云飞, 曲浩丽, 李强, 等.2011. 沼气发酵过程中产甲烷菌快速计数方法的研究[J]. 中国沼气 , 2011 (2) : 24–25. |
| [26] | 赵兴涛, 徐桂转, 刘杰博, 等.2013. 气相色谱法测定厌氧发酵液中挥发性脂肪酸的研究[J]. 河南农业大学学报 , 2013 (5) : 584–586. |
| [27] | 周洪波, 陈坚, 赵由才, 等.2002. 长链脂肪酸对厌氧颗粒污泥产甲烷毒性研究[J]. 水处理技术 , 2002, 28 (2) : 93–97. |
 2016, Vol. 36
2016, Vol. 36


