2. 中国科学院陆地表层格局与模拟重点实验室, 北京 100101;
3. 中国科学院大学, 北京 100049;
4. 广东省环境科学研究院, 广州 510045
2. Key Laboratory of Land Surface Pattern and Simulation, Chinese Academy of Sciences, Beijing 100101;
3. University of Chinese Academy of Sciences, Beijing 100049;
4. Guangdong Provincial Academy of Environmental Science, Guangzhou 510045
我国砷矿资源储量丰富,约占全球砷探明储量的70%,但由于历史上不规范的采选冶状况,致使我国砷矿区附近通常存在大面积的土壤和水体砷污染问题,在广西、云南和湖南等地这些问题更加严重.然而,自然界中的砷大多以硫化物形式夹杂在锡、铅、铜、锌、金等金属矿中,据调查,我国共生、伴生砷矿占总量的比例高达87.1%(肖细元等,2008).每年有大量的砷随其它矿种而开采出来,由于历史上选矿和冶炼技术的相对落后,无法达到对矿产资源的充分利用,暴露于地表的废石、尾砂及冶炼废渣在地表经风化、淋滤等作用,其中所含的砷和重金属被活化,扩散到周围环境中,因此,我国矿区附近通常存在As、Pb、Zn、Cu等重金属复合污染问题.在我国有“有色金属之乡”之称的湖南省,重金属污染土壤面积达2.8万km2,超过全省土地总面积的1/10,部分矿区土壤中As、Pb、Cd、Cu含量超标达数百倍(郭朝晖等,2004),严重威胁着当地居民的生产和生活.
采用稳定化技术对重金属污染土壤进行修复是见效快、效率高且经济可行的修复措施,该技术运用化学的方法将污染物转化成化学性质不活泼的形态,阻止其在环境中迁移、扩散等过程,从而降低污染物的毒害程度(USEPA,2013).由于AsO43-、AsO33-等阴离子基团与Pb2+、Cd2+、Zn2+、Cu2+等重金属阳离子化学性质不同,稳定化的机理也不相同,砷和其他重金属复合污染土壤的稳定化治理一直是个难题.如使用石灰、粉煤灰等pH控制剂或磷酸盐等沉淀剂能很好地固定土壤中的Pb、Zn、Cd等元素,但由于使土壤pH升高及与As竞争吸附位点,会活化土壤中的As元素(Kumpiene et al.,2008; 钟倩云等,2012; Miretzky et al.,2010);使用铁盐/亚铁盐能够对污染土壤中的As产生很好的稳定化作用,但Fe(Ⅱ/Ⅲ)离子水解会导致土壤酸化(Kim et al.,2003; Moore et al.,2000),使Pb、Cd、Zn等重金属阳离子浸出浓度增加.
课题组前期研究发现,将铁氧化物和锰氧化物进行复合,合成的铁锰双金属材料(Fe-Mn Binary Oxides,FMBO)结构疏松,比表面积大,表面羟基基团(-OH)丰富,具有氧化和吸附的双重作用,对土壤中的As(Ⅲ)和As(V)均有很好的稳定化效果(费杨等,2015).有研究发现,FMBO作为吸附材料对水体中的AsO43-、AsO33-、SbO3-等阴离子基团和Pb2+、Cr6+、Cd2+等重金属阳离子均有较好的吸附作用(Zhang et al.,2007a;许可等,2011; 宋娇艳等,2014;刘峰等,2013).但目前关于该材料对复合污染土壤中砷和重金属的稳定化效果鲜有研究.因此,本文拟通过室内模拟培养实验,按不同添加量向As和重金属复合污染土壤中添加人工合成的FMBO,研究其对As及Pb、Cd、Zn、Cu等复合污染土壤的稳定化作用,并通过形态提取、微观分析等手段对其稳定化机制进行探讨,以期对实际As和重金属复合污染场地进行稳定化修复提供科学指导.
2 材料与方法(Materials and methods) 2.1 供试材料和土壤 2.1.1 FMBO材料的制备铁锰双金属材料(FMBO)具体合成步骤参照文献(费杨等,2015).FMBO材料是一种无定形态的棕褐色粉末状材料,体积平均粒径D[4,3]为33.7 μm,采用BET方法(Tristar 3020 Ⅱ型,脱气温度100 ℃)测得材料比表面积为155.7 m2·g-1,Fe、Mn含量分别为37.9%、12.7%,Fe和Mn分别以Fe(Ⅲ)和Mn(Ⅳ)氧化态存在.
2.1.2 供试土壤污染土壤分别采自湖南株洲某冶炼厂(27°52′38″N,113°04′24″E)、湖南郴州某尾矿库(25°35′49″N,112°32′25″E)、辽宁大连某化工厂(38°58′6″N,121°38′1″E)附近,均为矿产采选冶过程造成的重金属复合污染土壤,采样深度0~20 cm,采集的土壤经过自然风干后,研磨过2 mm筛,均匀混合后储存备用.供试土壤基本理化性质见表 1,分析方法参照《土壤农化分析(第3版)》(鲍士旦,1999).
| 表 1 供试土壤基本理化性质 Table 1 Basic physical and chemical properties of soils |
称量供试土壤200.0 g于250 mL三角瓶中,分别按质量百分比0(未添加)、1%、2.5%、5%加入FMBO材料,充分搅拌使其混匀,调节土壤含水率为25%左右.水分调节好后用封瓶膜封好瓶口,以减少水分的散失,置于人工气候箱(温度(25±2)℃,相对湿度96%)中进行培养,每个处理3次重复.培养30 d后取样,进行TCLP毒性浸出实验(Toxicity Characteristic Leaching Procedure,USEPA Method 1311),采用1#浸提剂(醋酸/醋酸钠缓冲液,pH=4.93±0.05)浸提,按液固比20∶1(L·kg-1)加入浸提剂,翻转振荡器振荡,调节转速为30 r·min-1,振荡18 h,过滤并收集浸出液,于4 ℃下保存待测.稳定化效率W(即TCLP浸提液中重金属浓度降低百分比)按照下式进行计算:
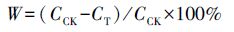
|
(1) |
式中,CCK、CT分别表示对照、不同处理TCLP毒性浸出液中重金属元素浓度.
培养30 d后取样进行土壤重金属结合态及pH测定,重金属结合态采用文献中(Rauret et al.,1999)改进的BCR连续提取方法,pH测定参考农业行业标准《土壤pH的测定 NY/T 1377-2007》,水土比2.5∶1.
2.3 静态吸附试验分别称量约0.015 mol Na3AsO4·12H2O、Pb(NO3)2、CdCl2、CuSO4·5H2O、ZnCl2(分析纯,购于国药集团化学试剂有限公司),将其固体试剂溶于约100 mL去离子水后,加入10.0 g FMBO,搅拌混匀,封好瓶口,置于人工气候箱(温度25 ℃,相对湿度96%)中进行培养,培养7 d后进行取样,用去离子水清洗掉未结合的AsO43-、Pb2+、Cd2+、Zn2+、Cu2+等离子,40 ℃低温烘干后,通过XRD、FTIR分析FMBO、FMBO-M(M=As、Pb、Cd、Zn、Cu)的结构特性及表面基团的变化.具体为:通过X射线衍射仪(Rigaku D/Max-rA)扫描产物的晶体结构,激发源Cu Kα,电流100 mA,电压40 kV,扫描范围为3°~70°;通过傅里叶变换红外光谱仪(FTIR-650)分析产物表面官能团类型,分辨率为4 cm-1,波数范围为4000~400 cm-1,动镜速度为6.25 mm·s-1.
2.4 化学分析土壤中砷和重金属元素总量及BCR连续提取残渣态含量(表 2)测定采用微波消解的方法(USEPA Method 3052),称量0.200 g过100目筛的样品于聚四氟乙烯消解罐中,加入9 mL浓硝酸和3 mL氢氟酸,浸泡30 min,再放入微波消解仪(XH-800B,北京祥鹄科技)中消解.溶液中的重金属浓度使用ICP-OES(Agilent 5100)进行测定.土壤样品分析过程中采用国家标准参比物质(土壤GBW 07404和GBW07402)进行分析质量控制,标样测定结果均在参比物质允许误差范围内.本研究所用试剂均为分析纯,实验用水为超纯水(PALL Cascada AN MK2).BCR连续提取实验的总回收率(各结合态重金属提取含量之和与土壤重金属总量之比)为95.4%~103.2%.
| 表 2 BCR形态分析法提取步骤 Table 2 BCR sequential extraction procedure |
数据采用Microsoft Excel 2010、SAS 8.0、Origin 8.5软件进行统计分析并作图.
3 结果(Results) 3.1 FMBO材料对复合污染土壤的稳定化效果从图 1可以看出,FMBO材料对复合污染土壤中As和重金属均能起到一定的稳定化作用,其中,对As和Pb的稳定化效果显著,对Cd、Zn、Cu的稳定化效果相对较低.由图 1可知,FMBO材料对复合污染土壤中As有较好的稳定化作用,且在0~5%范围内随着材料添加量的增加,As的浸出浓度逐渐降低.培养30 d后,与不添加稳定化材料的对照处理相比,以1%、2.5%、5%质量百分比添加FMBO的土
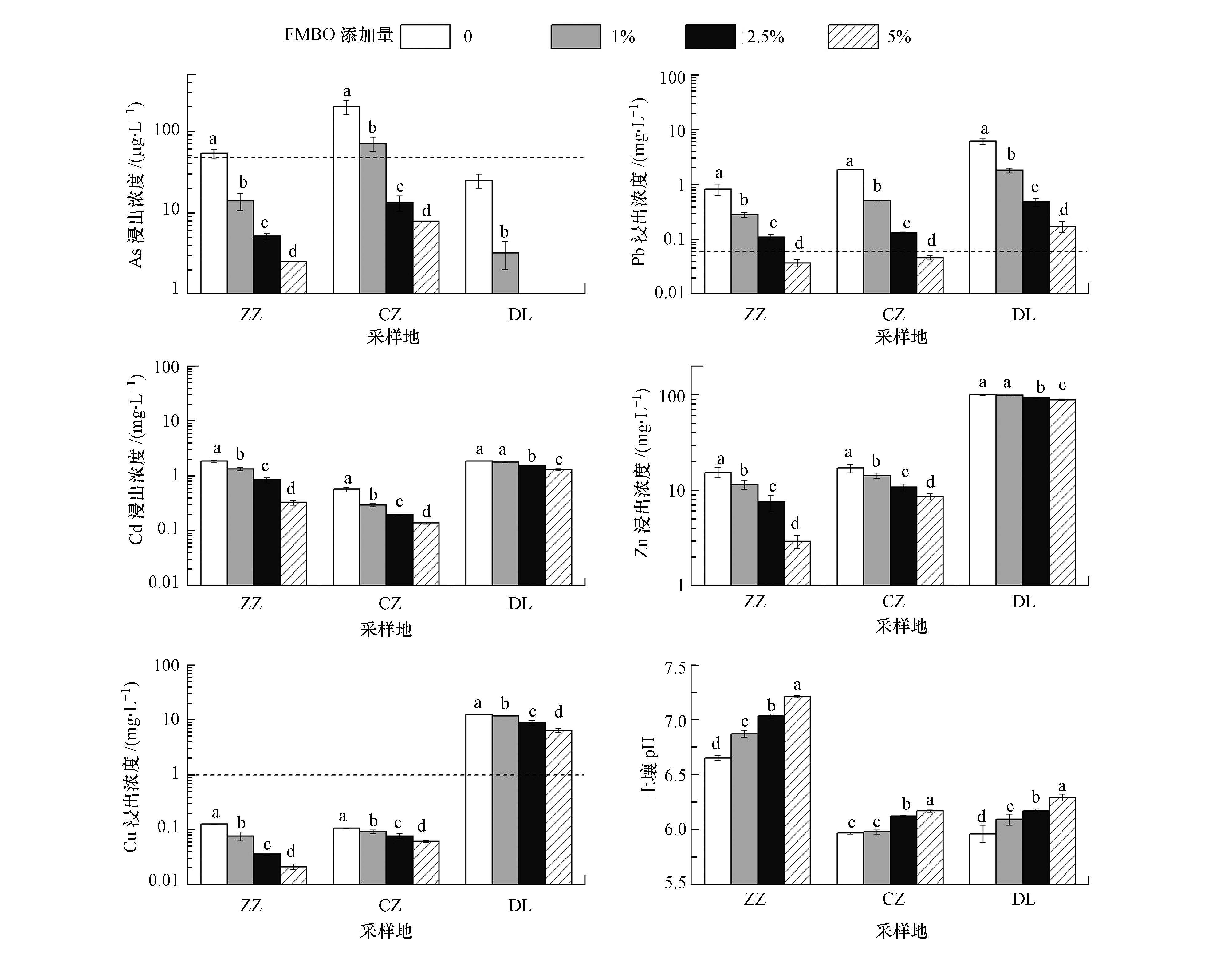 |
| 图 1 不同添加量FMBO处理后复合污染土壤TCLP浸出液中重金属浓度及土壤pH变化(图中虚线表示我国Ⅲ类地下水质量标准(GB/T 14848-93,标准值As≤0.05 mg·L-1,Pb≤0.05 mg·L-1,Cd≤0.01 mg·L-1,Cu≤ 1.0 mg·L-1,Zn≤1.0 mg·L-1),以人体健康基准值为依据,主要适用于集中式生活饮用水水源及工、农业用水) Fig. 1 As and heavy metal concentrations in TCLP leachate and soil pH change after adding FMBO in different soils |
壤浸提液中,ZZ土壤中As元素的浸出浓度由52.9 μg·L-1分别降低至13.9、5.13、2.55 μg·L-1,CZ土壤中As的浸出浓度由201.0 μg·L-1分别降低至70.9、13.3、7.80 μg·L-1,DL土壤中As的浸出浓度由25.0 μg·L-1分别降低至3.22 μg·L-1、未检出、未检出.在FMBO材料添加量达到2.5%以上时,3种类型的复合污染土壤中As的稳定化效率均达到90%以上,浸出浓度可以达到我国Ⅲ类地下水环境质量标准(≤50 μg·L-1,GB/T 14848-93).
FMBO材料除对As有较好的稳定化作用外,也能够大大降低复合污染土壤中Pb元素的浸出浓度.相比于不添加稳定化材料的对照处理,以1%、2.5%、5%质量百分比添加FMBO的土壤浸提液中,ZZ土壤中Pb元素的浸出浓度由0.82 mg·L-1分别降低至0.28、0.11、0.037 mg·L-1,CZ土壤中Pb的浸出浓度由1.85 mg·L-1分别降低至0.51、0.13、0.046 mg·L-1,DL土壤中Pb的浸出浓度由6.00 mg·L-1分别降低至1.78、0.48、0.17 mg·L-1.在材料添加量为5%时,ZZ和CZ土壤Pb的浸出浓度可以达到我国Ⅲ类地下水环境质量标准(≤50 μg·L-1,GB/T 14848-93).FMBO材料对Cd、Zn、Cu的稳定化效果在ZZ和CZ土壤中较为显著,当FMBO材料添加量为5%时,ZZ土壤中Cd、Zn、Cu的浸出浓度分别下降了82.9%、81.2%、83.4%,CZ土壤中Cd、Zn、Cu的浸出浓度分别下降了75.6%、50.2%、42.1%,而DL土壤中Cd、Zn、Cu浸出浓度下降的比例均低于50%.
结合图 1的数据,根据公式(1),计算FMBO对3种土壤中As和重金属的稳定化效率,结果表明,在5%的最大添加量下,FMBO对As、Pb、Cd、Zn、Cu的稳定化效率分别能够达到95.2%~100%、95.5%~97.5%、30.7%~82.9%、11.4%~81.2%、42.1%~83.4%.
从图 1中可以看出,随FMBO材料添加量的增加,3种复合污染土壤的pH均呈现升高的趋势,但pH变化幅度相对较小,均在6.0~7.5中性范围内,FMBO材料并没有明显的致酸致碱作用.其中,ZZ土壤pH变化最大,当FMBO添加量为1%、2.5%、5%时,pH分别升高了0.22、0.38、0.56,DL和CZ土壤pH变化较小,当材料添加量为5%时,pH分别升高了0.33、0.20.
3.2 FMBO材料对土壤重金属结合态的影响通过BCR连续提取,将土壤中重金属分为酸可提取态(F1)、可还原态(F2)、可氧化态(F3)和残渣态(F4)4种结合态,F1至F4稳定性依次增高.从图 2中可以看出,FMBO材料对土壤中As和Pb的结合态影响较大,添加FMBO会使土壤中酸可提取态As、Pb向可还原态转化.由图 2可知,As在ZZ、CZ、DL3种复合污染土壤中均以残渣态比例最高,其次是可还原态.添加FMBO材料能够使土壤中酸可提取态As比例降低,可还原态As比例升高,尤其在CZ土壤中,相比于对照,当FMBO添加量为1%、2.5%、5%时,土壤中酸可提取态As比例分别减少了0.23%、0.49%、0.54%,可还原态As比例分别增加了3.5%、11.2%、12.8%.结合态(F3和F4)As的比例在ZZ和DL土壤中无显著变化.
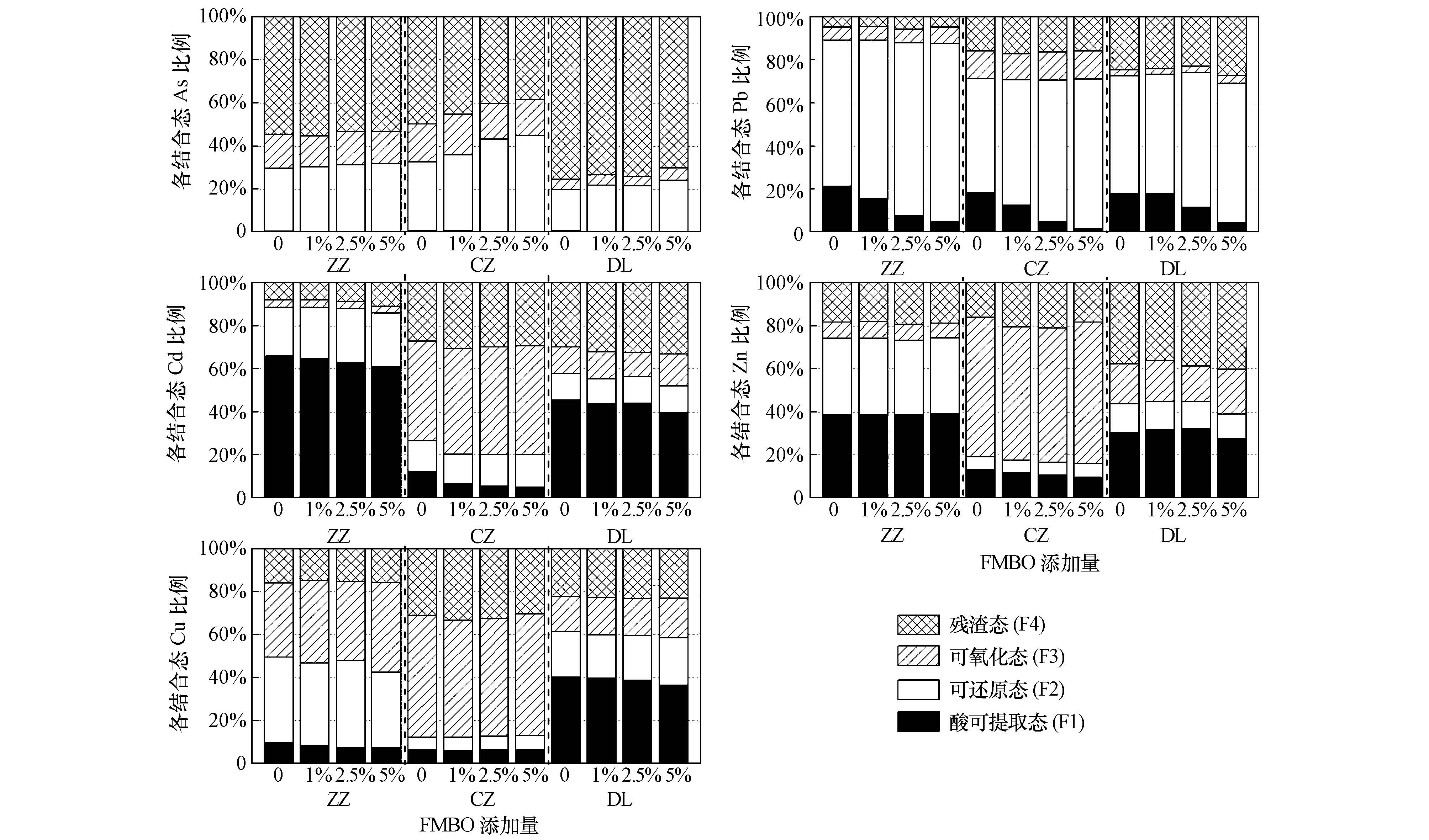 |
| 图 2 不同添加量的FMBO处理后复合污染土壤中各结合态重金属百分比含量 Fig. 2 Percentage of BCR sequential extraction speciations of arsenic and heavy metals in soils after adding FMBO |
从图 2中还可以看出,Pb在3种土壤中均以可还原态所占比例最高,添加FMBO材料后3种土壤中酸可提取态Pb含量均降低,且在0~5%范围内,随FMBO添加量增加,酸可提取态Pb含量逐渐减少,可还原态Pb含量逐渐增加,可氧化态及残渣态Pb比例变化较小.相比于对照,FMBO添加量为2.5%时,ZZ、CZ、DL土壤中酸可提取态Pb的比例分别减少了13.6%、13.3%、6.1%,可还原态Pb的比例分别增加了12.4%、12.5%、7.7%.
添加FMBO材料后3种土壤酸可提取态Cd的比例稍有降低,结合态(F2~F4)Cd比例变化不大.相比于对照,FMBO添加量为2.5%时,ZZ、CZ、DL土壤酸可提取态Cd比例分别下降了3.0%、6%、1.5%.而添加FMBO材料对土壤中的Zn、Cu无明显的形态转化作用.
3.3 FMBO与重金属的微观吸附特征 3.3.1 FMBO与重金属吸附前后XRD分析从FMBO吸附As、Pb、Cd、Zn、Cu前后XRD谱图中可以看出,吸附后FMBO-As、FMBO-Pb、FMBO-Cd复合体仍为无定形或弱结晶态,并没有明显的特征衍射峰出现(图 3),这说明在FMBO与As、Pb、Cd反应过程中,并无大量结晶态矿物生成.FMBO-Zn、FMBO-Cu反应产物也基本为无定形或弱结晶态,但出现了少量不规则的衍射峰,结晶度有所增加,说明反应过程中有沉淀物质生成,除了吸附反应外,还有沉淀反应发生.
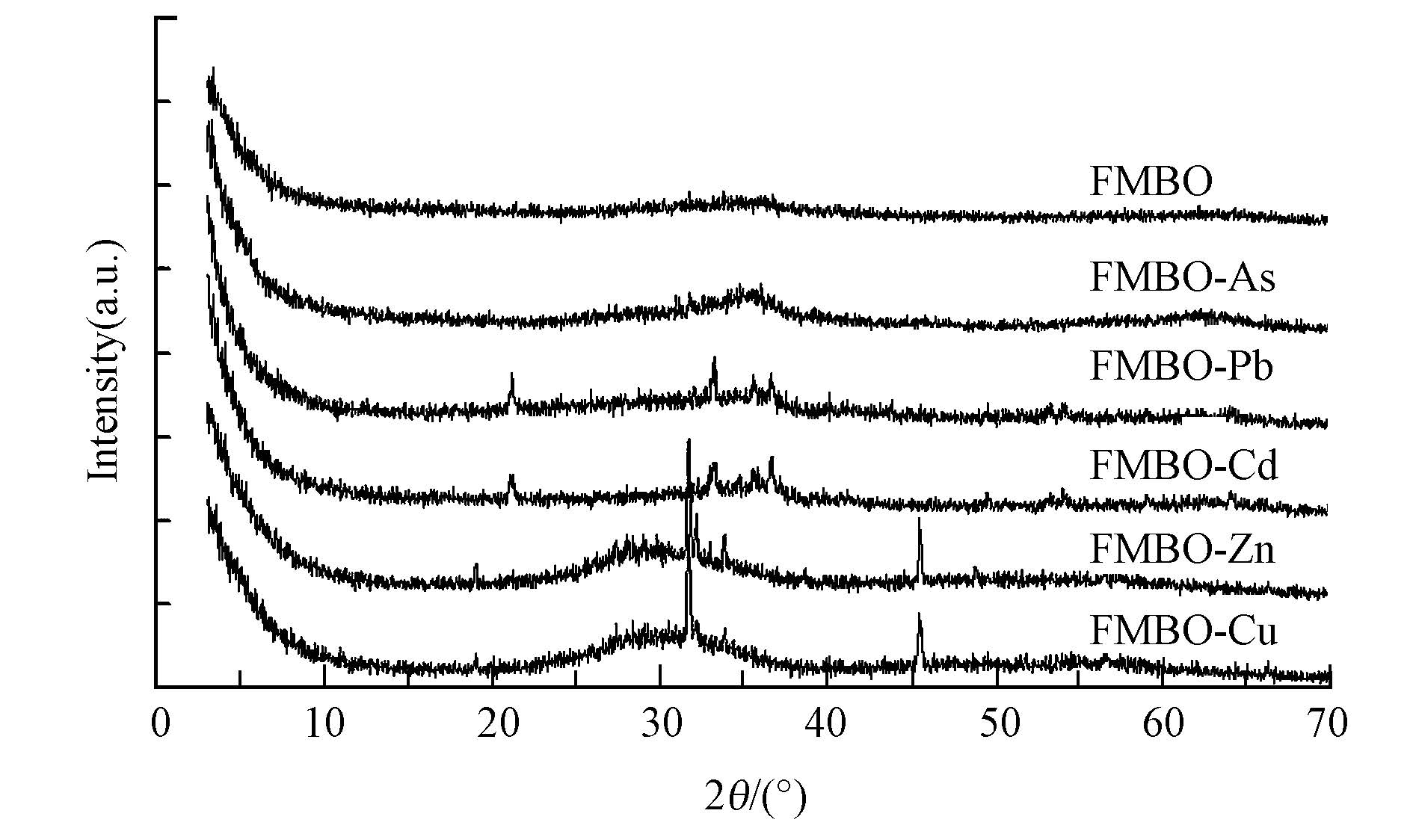 |
| 图 3 FMBO吸附不同重金属前后XRD谱图 Fig. 3 XRD graphs of FMBO after reacting with As and heavy metals |
作为一种水合金属氧化物,FMBO表面含有丰富的羟基位点(M-OH,M代表表面金属离子Fe和Mn).根据Russell(1979)对水铁矿表面羟基基团的表征,羟基氧化铁FeOOH中水的吸收谱表现为3550~3200 cm-1处的O-H(结晶水)伸缩振动和1630 cm-1处H-O-H(吸附水)的弯曲振动,而M-OH 的摇摆振动峰通常出现在1200 cm-1以下.由FMBO吸附重金属前后FTIR谱图(图 4)可以看出,FMBO-As的FTIR谱图与其他金属元素差别较大,在1128.15 cm-1处FMBO表面羟基位点(Fe-OH)的振动吸收峰减弱,说明有吸附反应发生,As与FMBO表面羟基基团结合形成新的表面螯合物.在802.24 cm-1处形成新的吸收峰,该位置是As-O键的伸缩振动峰(Zhang et al.,2009),图中并未出现Fe-As-O的特征吸收峰,说明Fe元素并未与As元素直接键合,形成诸如FeAsO4等铁砷矿物.该结果表明,FMBO对As的稳定化主要是通过专性吸附,而不是以形成沉淀的方式起作用.FMBO与Pb、Cd、Zn、Cu等重金属阳离子反应后的FTIR谱线相似,在1128.15 cm-1处的振动峰说明其反应后仍存在大量表面羟基(-OH)位点,而在1052.94、892.88 cm-1处形成新的吸收峰,说明有新的化学键生成,该过程也有吸附反应发生.
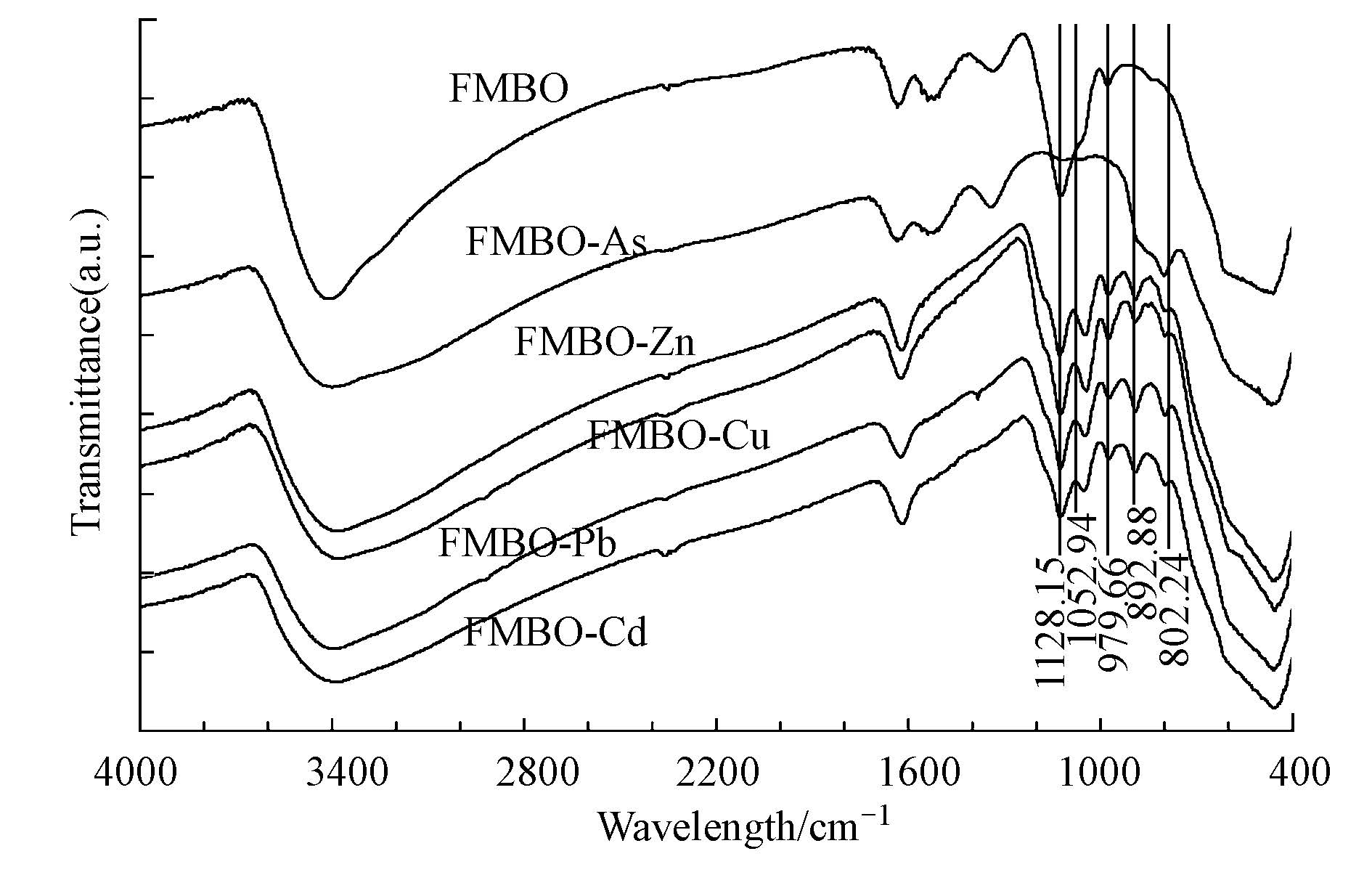 |
| 图 4 FMBO吸附不同重金属前后FTIR谱图 Fig. 4 FTIR graphs of FMBO after reacting with As and heavy metals |
本文研究了FMBO材料对3种复合污染土壤中As和重金属的稳定化效果,结果发现,FMBO材料对As、Pb的稳定化作用最为显著,稳定化效率分别能达到95.2%~100%和95.5%~97.5%,而对Cd、Zn、Cu的稳定化效果相对较低,且在0~5%范围内,随着FMBO添加量的增加,其对As和重金属的稳定化效率均逐渐升高.从本研究TCLP结果可知,对于ZZ、CZ、DL 3种土壤,FMBO在对复合污染土壤中As进行有效稳定化的同时,对Pb也能够起到较好的稳定化作用,且没有使Cd、Zn、Cu等其他重金属产生活化.因此,FMBO材料对于含As、Pb等重金属复合污染土壤而言,是一种良好的稳定化材料.
通过改变污染土壤中重金属形态进行风险控制是稳定化修复的核心思想.根据与土壤不同组分结合,重金属一般分为酸可提取态、可还原态、可氧化态和残渣态4种形态,其中,酸可提取态金属对环境条件特别是pH最为敏感,当pH下降容易重新释放出来,可还原态是指金属元素与土壤中铁、锰氧化物结合的部分(宋照亮等,2004).在对稳定化前后土壤中砷和重金属结合态变化的研究中发现,添加FMBO材料会使酸可提取态的As、Pb向稳定性更高的可还原态转化,说明土壤中活性较高的As、Pb会与FMBO材料结合,以更稳定的铁、锰氧化物复合体形式存在,因而浸出浓度降低,起到显著的稳定化作用.而添加FMBO材料后,土壤中可还原态Cd、Zn、Cu的比例并无显著增加,其浸出浓度降低可能是由于土壤pH的变化引起的.添加FMBO材料后土壤pH升高,使土壤表面负电荷增加,进而增加了土壤对重金属的吸附,同时有利于羟基化金属离子([MOH]n+)的形成,并能促使土壤中的Pb、Cd、Zn、Cu等重金属阳离子形成氢氧化物或碳酸盐沉淀,对其稳定化过程产生促进作用(Friesl et al.,2006; Lombi et al.,2003).
由本文XRD、FTIR微观分析结果及前人研究可知,As和重金属与FMBO的相互作用方式主要包括吸附、氧化和沉淀3种,3种方式共同作用从而起到稳定化的目的,使As和重金属的环境风险降低.表面羟基-OH在FMBO材料的稳定化过程中起到很大作用.表面络合理论认为,以羟基化的氧化物为主的吸附材料,其表面羟基参与各种氧化物-水界面的配体交换和络合反应,是决定材料对重金属离子吸附和离子交换能力的主要因素之一(张昱等,2006).由FTIR分析结果可知,FMBO材料与As反应后,表面活性吸附位点-OH数量减少,且有新的化学键生成,说明发生了表面吸附反应.大量研究表明,铁基氧化物能够通过表面的-OH或-OH2+与砷酸根或亚砷酸根离子结合,形成双齿双核、双齿单核、单齿单核3种类型的内表面螯合物(Sherman et al.,2003;Carabante et al.,2009;Miretzky et al.,2010),其稳定性远大于通过静电吸附、氢键结合等方式形成的外表面螯合物(Cundy et al.,2008;Catalano et al.,2008;Wang et al.,2008).FMBO材料通过Fe、Mn氧化物复合改变了材料的物理化学特性,破坏了铁氧化物的晶体结构,使材料比表面积增大,表面活性吸附位点-OH增多,从而增加了其对污染物的吸附容量.FMBO对As(Ⅲ)和As(V)的饱和吸附容量可分别达到129.9、80.6 mg·g-1(费杨等,2015),在吸附过程中,Mn(Ⅳ)对As(Ⅲ)的氧化会释放Mn2+,暴露新的吸附位点,进一步提高了FMBO材料的吸附性能(Zhang et al.,2007b).FTIR结果中FMBO与Pb、Cd、Zn、Cu反应后也有新的化学键生成,说明FMBO也能通过表面吸附的方式对重金属阳离子起到稳定化作用.已有研究表明,Pb、Cd等二价金属阳离子(Me2+)也可以通过表面-OH吸附到Fe、Mn氧化物表面,形成共齿共角多面体(Komárek et al.,2013; 宋娇艳等,2014),如Pb可形成双齿单核和单齿单核螯合物形式,Cd可形成单齿、双齿、三齿3种螯合物形式(Trivedi et al.,2003; Venema et al.,1996).此外,吸附后新形成的次级氧化物与重金属离子发生表面共沉淀反应(如FeAsO4·2H2O、MnPbO3等),是另一重要的稳定化机制(Martinez et al.,1998; Tournassat et al.,2002; Kumpiene et al.,2008),XRD结果中反应产物的结晶度增加说明了该问题.相比于吸附反应,共沉淀产物具有更低的溶解性.有研究表明,在As污染土壤的稳定化过程中,难溶性的Fe(Ⅱ/Ⅲ)-As矿物(如FeAsO4·H2O、FeAsO4·2H2O、Fe3(AsO4)2·8H2O)的形成降低了As的移动性和生物有效性(Kim et al.,2003;Drahota et al.,2009;Miretzky et al.,2010).
5 结论(Conclusions)针对As和重金属复合污染土壤,FMBO材料可以作为一种经济、高效、绿色安全的稳定化修复材料.FMBO除对As有较高的稳定化效率外,对Pb也有较高的稳定化效率,而对Cd、Zn、Cu的稳定化效率相对较低,在稳定化修复时不会引起某种重金属的活化.FMBO能够使土壤中As和Pb由酸可提取态向可还原态转变,稳定性增加,从而使其环境风险降低.FMBO材料对As的稳定化主要通过表面羟基-OH基团的吸附作用,而对Pb、Cd等金属离子则通过吸附、沉淀等多种方式起作用.此外,FMBO材料的添加会使土壤pH值升高,对稳定化过程起到一定的促进作用.
| [1] | 鲍士旦. 1999. 土壤农化分析(第3版)[M]. 北京: 中国农业出版社 . |
| [2] | Carabante I, Grahn M, Holmgren A, et al. 2009. Adsorption of As (V) on iron oxide nanoparticle films studied by in situ ATR-FTIR spectroscopy[J]. Colloids and Surfaces A-Physicochemical and Engineering Aspects , 346 (1/3) : 106–113. |
| [3] | Catalano J G, Park C, Fenter P, et al. 2008. Simultaneous inner-and outer-sphere arsenate adsorption on corundum and hematite[J]. Geochimica et Cosmochimica Acta , 72 (8) : 1986–2004. DOI:10.1016/j.gca.2008.02.013 |
| [4] | Cundy A B, Hopkinson L, Whitby R L D. 2008. Use of iron-based technologies in contaminated land and groundwater remediation: A review[J]. Science of the Total Environment , 400 (1/3) : 42–51. |
| [5] | Drahota P, Filippi M. 2009. Secondary arsenic minerals in the environment: A review[J]. Environment International , 35 (8) : 1243–1255. DOI:10.1016/j.envint.2009.07.004 |
| [6] | 费杨, 阎秀兰, 廖晓勇, 等.2015. 不同水分条件下铁基氧化物对土壤砷的稳定化效应研究[J]. 环境科学学报 , 2015, 35 (10) : 3252–3260. |
| [7] | Friesl W, Friedl J, Platzer K, et al. 2006. Remediation of contaminated agricultural soils near a former Pb/Zn smelter in Austria: Batch,pot and field experiments[J]. EnvironmentalPollution , 144 (1) : 40–50. |
| [8] | 郭朝晖, 朱永官.2004. 典型矿冶周边地区土壤重金属污染及有效性含量[J]. 生态环境 , 2004, 13 (4) : 553–555. |
| [9] | Kim J Y, Davis A P, Kim K W. 2003. Stabilization of available arsenic in highly contaminated mine tailings using iron[J]. Environmental Science & Technology , 37 (1) : 189–195. |
| [10] | Komárek M, Vaněk A, Ettler V. 2013. Chemical stabilization of metals and arsenic in contaminated soils using oxides-A review[J]. Environmental Pollution , 172 : 9–22. DOI:10.1016/j.envpol.2012.07.045 |
| [11] | Kumpiene J, Lagerkvist A, Maurice C. 2008. Stabilization of As,Cr,Cu,Pb and Zn in soil using amendments-A review[J]. Waste Management , 28 (1) : 215–225. DOI:10.1016/j.wasman.2006.12.012 |
| [12] | 刘峰, 刘锐平, 刘会娟, 等.2013. 铁锰复合氧化物同时吸附锑镉性能研究[J]. 环境科学学报 , 2013, 33 (12) : 3189–3196. |
| [13] | Lombi E, Hamon R E, McGrath S P, et al. 2003. Lability of Cd,Cu,and Zn in polluted soils treated with lime,beringite,and red mud and identification of a non-labile colloidal fraction of metals using isotopic techniques[J]. Environmental Science and Technology , 37 (5) : 979–984. DOI:10.1021/es026083w |
| [14] | Martinez C E, Mcbride M B. 1998. Coprecipitates of Cd,Cu,Pb and Zn in iron oxides: Solid phase transformation and metal solubility after aging and thermal treatment[J]. Clays and Clay Minerals , 46 (5) : 537–545. DOI:10.1346/CCMN |
| [15] | Miretzky P, Fernandez Cirelli A. 2010. Remediation of arsenic-contaminated soils by iron amendments: A review[J]. Critical Reviews in Environmental Science and Technology , 40 (2) : 93–115. DOI:10.1080/10643380802202059 |
| [16] | Moore T J, Rightmire C M, Vempati R K. 2000. Ferrous iron treatment of soils contaminated with arsenic-containing wood-preserving solution[J]. Soil & Sediment Contamination , 9 (4) : 375–405. |
| [17] | Rauret G, Lopez-Sanchez J F, Sahuquillo A, et al. 1999. Improvement of the BCR three step sequential extraction procedure prior to the certification of new sediment and soil reference materials[J]. Journal of Environmental Monitoring , 1 (1) : 57–61. DOI:10.1039/a807854h |
| [18] | Russell J D. 1979. Infrared spectroscopy of ferrihydrite: evidence for the presence of structural hydroxyl groups[J]. Clay Miner , 14 : 109–114. DOI:10.1180/claymin |
| [19] | Sherman D M, Randall S R. 2003. Surface complexation of arsenie(V) to iron(Ⅲ) (hydr)oxides: Structural mechanism from ab initio molecular geometries and EXAFS spectroscopy[J]. Geochimica et Cosmochimica Acta , 67 (22) : 4223–4230. DOI:10.1016/S0016-7037(03)00237-0 |
| [20] | 宋娇艳, 袁林, 杨志丹, 等.2014. 铁锰复合氧化物对铅离子的吸附特征及影响因素研究[J]. 西南大学学报(自然科学版) , 2014 (7) : 135–142. |
| [21] | 宋照亮, 刘丛强, 彭渤, 等.2004. 逐级提取(SEE)技术及其在沉积物和土壤元素形态研究中的应用[J]. 地球与环境 , 2004, 32 (2) : 70–77. |
| [22] | Tournassat C, Charlet L, Bosbach D, et al. 2002. Arsenic(Ⅲ) oxidation by birnessite and precipitation of manganese(Ⅱ) arsenate[J]. Environmental Science & Technology , 36 (3) : 493–500. |
| [23] | Trivedi P, Dyer J A, Sparks D L. 2003. Lead sorption onto ferrihydrite[J]. 1. A macroscopic and spectroscopic assessment[J]. Environmental Science & Technology , 37 (5) : 908–914. |
| [24] | USEPA. 1992. SW-846 Test Method 1311: Toxicity characteristic leaching procedure[EB/OL]. 2016-10-25. https://www.epa.gov/sites/production/files/2015-12/documents/1311.pdf |
| [25] | USEPA. 1996. SW-846 Test Method 3052: Microwave assisted acid digestion of siliceous and organically based matrices[EB/OL]. 2016-10-25. https://www.epa.gov/sites/production/files/2015-12/documents/3052.pdf |
| [26] | USEPA. 2013. Superfund remedy report(Fourteenth Edition)[OL]. 2016-10-25. http://www.epa.gov/superfund/remedytech/srr/ |
| [27] | Venema P, Hiemstra T, Vanriemsdijk W H. 1996. Multisite adsorption of cadmium on goethite[J]. Journal of Colloid and Interface Science , 183 (2) : 515–527. DOI:10.1006/jcis.1996.0575 |
| [28] | Wang S, Mulligan C N. 2008. Speciation and surface structure of inorganic arsenic in solid phases: A review[J]. Environment International , 34 (6) : 867–879. DOI:10.1016/j.envint.2007.11.005 |
| [29] | 肖细元, 陈同斌, 廖晓勇, 等.2008. 中国主要含砷矿产资源的区域分布与砷污染问题[J]. 地理研究 , 2008, 27 (1) : 201–212. |
| [30] | 许可, 刘军坛, 彭伟功, 等.2011. 铁锰复合氧化物处理含铬废水的研究[J]. 水处理技术 , 2011, 37 (12) : 20–23. |
| [31] | Zhang G, Liu H, Liu R, et al. 2009. Adsorption behavior and mechanism of arsenate at Fe-Mn binary oxide/water interface[J]. Journal of Hazardous Materials , 168 (2/3) : 820–825. |
| [32] | Zhang G, Qu J, Liu H, et al. 2007a. Preparation and evaluation of a novel Fe-Mn binary oxide adsorbent for effective arsenite removal[J]. Water Research , 41 (9) : 1921–1928. DOI:10.1016/j.watres.2007.02.009 |
| [33] | Zhang G, Qu J, Liu H, et al. 2007b. Removal mechanism of As(Ⅲ) by a novel Fe-Mn binary oxide adsorbent: Oxidation and sorption[J]. Environmental Science & Technology , 41 (13) : 4613–4619. |
| [34] | 张昱, 豆小敏, 杨敏, 等.2006. 砷在金属氧化物/水界面上的吸附机制I[J]. 金属表面羟基的表征和作用[J].环境科学学报 , 2006, 26 (10) : 1586–1591. |
| [35] | 钟倩云, 曾敏, 廖柏寒, 等.2012. 2种固化剂对重金属和砷复合污染底泥的稳定化处理效果[J]. 水土保持学报 , 2012, 26 (6) : 190–193. |
 2016, Vol. 36
2016, Vol. 36


