三氯生(Triclosan,TCS)是一种广谱抗菌剂,广泛使用于个人护理品及医药等行业中.近年来TCS在地表水、土壤/底泥,甚至生物体中频繁检出(Wang et al., 2014; Dann and Hontela, 2011)而成为一种新型环境物质.TCS较高的疏水特性(logKow=4.76)(Andrea et al., 2012)使其更易吸附在底泥、土壤等固相介质上(Zhao et al., 2010).处于底泥的厌氧环境中,TCS的生物降解被抑制(McAvoy et al., 2002);而将TCS从底泥相迁移到含氧量较高的水相,则可通过生物降解、活性炭吸附、膜分离等方法进行去除(Aranami and Readman, 2007; Ying et al., 2007; Behera et al., 2010).
生物表面活性剂可有效调控疏水性有机化合物(Hydrophobic Organic Compounds, HOCs)在底泥/土壤-水体系中的分配,一方面,胶束增溶作用能促进HOCs向水相的迁移(Zhou and Zhu, 2007; Cao et al., 2008);另一方面生物表面活性剂在底泥/土壤上的吸附导致HOCs绑定在底泥/土壤上(Paria and Yuet, 2007; Wu et al., 2015).生物表面活性剂的典型代表鼠李糖脂(Rhamnolipid, RL)由于具有良好的表面活性,低细胞毒性及极好的生物降解性而广泛应用于污染修复领域(林晖等,2011).目前关于RL修复HOCs的典型代表TCS污染底泥的研究主要集中在pH、底泥/土壤组成、RL投加量、RL结构以及TCS溶解度等方面(Zhang et al., 2013; Yu et al., 2011; ElSayed and Prasher, 2014; Wu et al., 2015).
人们也注意到,水体中大量存在的阳离子对表面活性剂的胶束聚集形态有很大影响(Alargova et al., 2003; Arutchelvi et al., 2014; Sammalkorpi et al., 2009).Helvacı等(2004)发现Na+能降低RL溶液的临界胶束浓度(CMC)和表面张力.二价阳离子能与阴离子表面活性剂产生强烈绑定作用而导致沉淀(Alargova et al., 2003; Yu et al., 2008),然而Chen等(2013)发现Ca2+对单/双鼠李糖脂的胶束形态没有影响却对RL/十二烷基苯磺酸钠的胶束形态有强烈影响.此外,阳离子强度对RL作用下碳氢化合物溶解度的影响也差异很大(Bai et al., 1998).但因RL和阳离子之间的相互作用至今仍不清楚,以至于阳离子强度对RL作用下TCS在底泥-水相中分配的影响亦无答案.
为此,本文选取水体中常见的Na+/Ca2+两种阳离子,首先从RL胶束粒径分布及zeta电位的角度考察了阳离子强度对RL胶束聚集形态的影响,然后采用批式实验探讨了阳离子强度对RL作用下TCS表观溶解度的影响,进而分析了阳离子强度对TCS在底泥-水-RL体系中分配的影响,以期为不同盐度/硬度水体中RL对TCS分配的调控提供指导.
2 材料与方法(Materialsandmethods) 2.1 试剂与材料三氯生(2, 4, 4′-三氯-2′-羟基二苯醚)(99%)和鼠李糖脂(90%)分别购自美国Alfa Aesar公司和湖州紫金生物科技有限公司.其他试剂均为分析纯级试剂.用去离子水配制成不同浓度的NaCl和CaCl2,并加入微生物抑制剂100 mg·L-1 NaN3,制备成不同阳离子强度的背景溶液.Na+浓度梯度为0、5、10、20、30、40、50、100、200 mmol·L-1(不包含抑菌剂中的Na+),Ca2+浓度梯度为0、0.2、0.5、1、2、3、5、10、30 mmol·L-1(Bai et al., 1998).用背景溶液配制成浓度为1250 mg·L-1的RL溶液.预实验显示阴离子对TCS在底泥-水-RL体系中分布作用基本没有影响.用甲醇配制成浓度为100 mg·L-1的三氯生储备液,4 ℃条件下避光冷藏保存.
2.2 底泥样品的制备底泥样品采自于广州珠江支流瀛洲生态公园的冲积入海口处,在室温下自然风干,去除杂质后捣碎过筛(2 mm),随后储存在棕色玻璃瓶中备用.底泥样品的有机碳含量为0.41%,粘土、淤泥和沙含量分别为15%、36%和49%,pH为7.31.预实验显示底泥样品的TCS背景值低于检测限.
2.3 RL的胶束粒径分布及zeta电位测量以不同阳离子强度为背景溶液配制的RL溶液的胶束粒径分布及zeta电位通过Malvern NANO-ZS90 (UK)型电位粒度仪测量.RL溶液的胶束粒径分布是用动力学光散射法测试,温度为25 ℃,散射光角度为90°.Zeta电位是基于应用电场中悬浮颗粒的速度(电泳迁移率),使用电泳光散射法来测量的(Arutchelvi et al., 2014).
2.4 TCS在RL溶液中表观溶解度的测定不同阳离子强度下TCS在RL溶液中表观溶解度的测定通过批式实验(重复3次)来完成.向锥形瓶内加入32 mg TCS固体(预实验显示能使溶液达到溶解平衡)和160 mL不同阳离子强度的RL溶液,于摇床中,(20±0.1)℃,100 r·min-1(模拟自然水体的低扰度条件),在黑暗中(抑制光降解)反应96 h.预实验结果显示96 h能够达到溶解平衡,且吸附在锥形瓶内壁的TCS可以忽略.最后,用玻璃注射器取1 mL上清液过玻璃纤维滤膜,用超高效液相色谱(UPLC)测量TCS的浓度.此外,另取1 mL上清液用苔黑酚比色法测定RL的浓度(Lin et al., 2011).
2.5 RL作用下TCS在底泥-水体系中分配的测定在锥形瓶内加入16 g底泥和特定体积(5、8、10、12、16、20 mL)TCS储备液,使得TCS的最终浓度达到31.25、50、62.5、75、100、125 μg·g-1底泥,待甲醇挥发后用蠕动泵缓慢加入(避免大的扰动)160 mL不同阳离子强度的RL溶液.于摇床中,(20±0.1)℃,100 r·min-1,在黑暗中反应96 h(预实验显示能达到分配平衡),检测水相中的TCS浓度,并对添加有16 mL TCS甲醇储备液样品水相中的RL浓度进行检测,测定方法如上所示,重复3次(Wu et al., 2015).
2.6 TCS浓度的检测样品中TCS的浓度通过超高效液相色谱(UPLC, Waters ACQUITY UPLC system, USA),配置光-二极管矩阵检测器和三乙胺流动相体系色谱柱(2.1 mm×50 mm),在230 nm处测量.流动相为V(甲醇)/V(水)=60:40,流速为0.3 mL·min-1,进样量为2 μL.仪器检测限为5 μg·L-1.
3 结果与讨论(Resultsanddiscussion) 3.1 阳离子强度对RL胶束聚集形态的影响 3.1.1 阳离子强度对RL胶束粒径分布的影响采用动力学光散射(DLS)测量不同阳离子强度下RL的胶束粒径分布,如图 1a所示.未添加阳离子时,RL胶束粒径分布较为分散;加入阳离子后RL胶束的粒径分布更为集中.图 1b所示为对不同的阳离子浓度下Na+、Ca2+溶液中RL的平均胶束粒径作点线图.由图可见,阳离子的加入能改变RL胶束粒径,RL的平均胶束粒径随Na+离子强度的增大先减小后增大,在Na+离子浓度为30 mmol·L-1时达到最小值;但却随着Ca2+离子强度的增大持续减小.
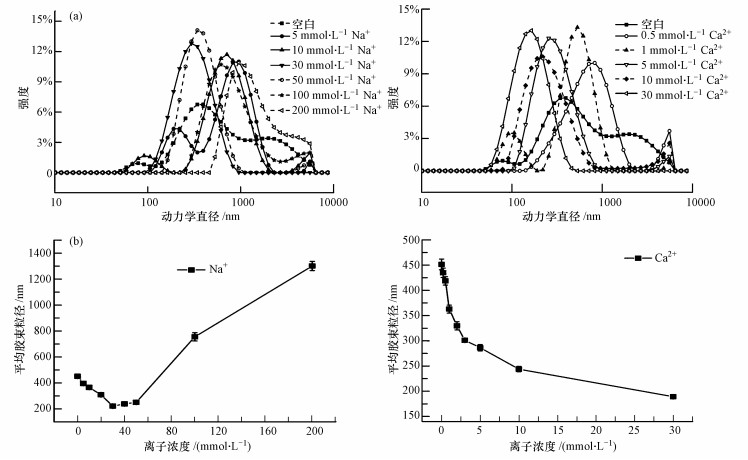 |
| 图 1 不同阳离子强度条件下RL的(a)胶束粒径分布图,(b)平均粒径点线图 Fig. 1 (a) micellar size distribution and (b) plot of average micellar size of RL with different cationic strength |
在Na+溶液中,RL的平均胶束粒径从415.4 nm(0 mmol·L-1)逐渐降低到221.8 nm(30 mmol·L-1),随后增加到1301 nm(200 mmol·L-1).而在Ca2+溶液中,RL的平均胶束粒径从415.4 nm(0 mmol·L-1)逐渐降低到189.1 nm(30 mmol·L-1).理论上,加入的阳离子与RL分子间将产生盐桥作用(Sammalkorpi et al., 2009),降低RL分子头部间的静电斥力,从而促进RL胶束的形成和聚集(Arutchelvi et al., 2014).离子强度的增强,先使得胶束的聚集更为紧密,导致胶束平均粒径减小;当离子强度增加到一定程度后,较强的相互作用力使得RL胶束聚集形态发生变化,从球状胶束转变为层状胶束,并可能导致沉淀(Penfold et al., 2007; 林晖等,2011).对于Na+溶液,较弱的作用力使一些粒径较大的胶束依然保留于溶液中,从而导致平均胶束粒径的增大.相比Na+,Ca2+与RL分子之间的作用力要强的多,Ca2+在很低的浓度下(1 mmol·L-1)就能使得胶束聚集体沉淀,缩小平均胶束粒径(Jia et al., 2015).
3.1.2 阳离子强度对RL溶液zeta电位的影响Zeta电位表征胶体溶液的稳定性,较高的zeta电位(-30~-85 mV)下,胶体较为稳定.如图 2所示,RL溶液的zeta电位随着Na+/Ca2+离子强度的增大而减小,即溶液的稳定性逐渐降低.其中,在Na+溶液中,在离子浓度大于50 mmol·L-1后,系统趋于不稳定状态;而在Ca2+溶液中,在离子浓度大于1 mmol·L-1时,系统就已处于不稳定状态,甚至沉淀.这是由于阳离子与RL分子间的盐桥作用(Sammalkorpi et al., 2009),RL单体所带的负电荷被阳离子所中和,形成更加紧密的胶束聚集体而使溶液的稳定性降低.相比Na+,Ca2+中和负电荷的能力更强,形成的胶束聚集体也更加密实,因而在较低浓度时(1 mmol·L-1)就能大大降低RL溶液的稳定性(Jia et al., 2015).
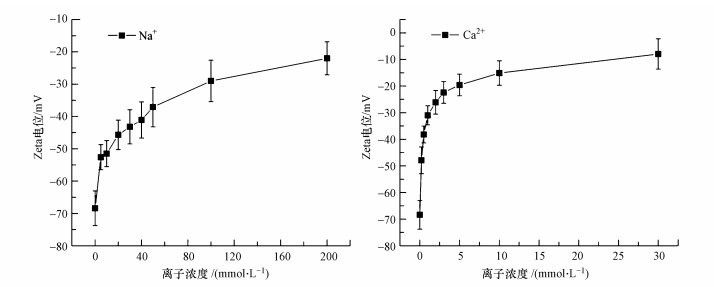 |
| 图 2 不同阳离子强度下RL溶液的zeta电位 Fig. 2 Zeta potential of RL solutions with different cationic strength |
综合阳离子强度对RL胶束粒径分布及zeta电位的影响,可以得出阳离子通过与RL分子间的盐桥作用而促进了RL胶束的聚集,从而降低了溶液的稳定性,其影响随着离子强度的增大而增大.与Na+相比,Ca2+在较低浓度(1 mmol·L-1)下就对RL胶束的聚集产生很大的影响,其与RL分子间的盐桥作用更为强烈,聚集体更为密集,更易产生沉淀.
3.2 阳离子强度对RL溶液中TCS表观溶解度的影响如图 3所示,在Na+溶液中,TCS的表观溶解度随着离子强度的增大先增大后减小,在浓度为30 mmol·L-1时达到最大值,并在浓度高于50 mmol·L-1后表观溶解度急剧下降;在Ca2+溶液中,TCS的表观溶解度随着离子强度的增大而减小,在浓度高于1 mmol·L-1后表观溶解度便急剧下降.无RL时,TCS在各不同阳离子强度溶液中的表观溶解度均约为5 mg·L-1.在RL作用下,在无阳离子时,TCS表观溶解度为143.8 mg·L-1.在加入Na+后,随着离子强度的增大,TCS的表观溶解度逐渐增加到187.1 mg·L-1(30 mmol·L-1),随后又迅速下降到51.6 mg·L-1(200 mmol·L-1).在Ca2+溶液中,当离子浓度小于1 mmol·L-1时,TCS的表观溶解度基本无变化,但当Ca2+离子强度超过此值后TCS的表观溶解度迅速降低到0.52 mg·L-1(30 mmol·L-1).
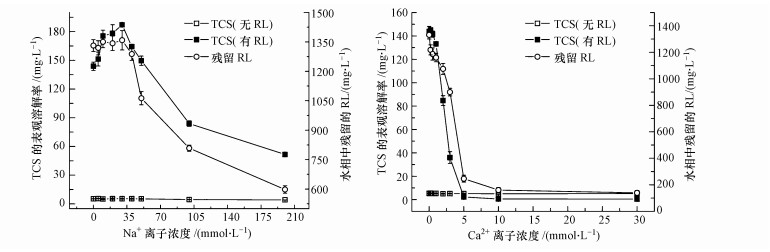 |
| 图 3 不同阳离子强度下TCS在RL中的表观溶解度及残留的RL浓度 Fig. 3 The apparent solubility of TCS in RL solutions and the residual RL concentration with different cationic strength |
检测水溶液中的RL浓度,发现Na+浓度小于50 mmol·L-1时RL浓度无明显变化,而Na+浓度大于50 mmol·L-1后水溶液中的RL浓度便开始降低;而在Ca2+溶液中的RL浓度仅在Ca2+离子浓度高于1 mmol·L-1后便迅速下降.在Na+、Ca2+浓度分别为200 mmol·L-1和30 mmol·L-1时,水相中的RL浓度从1250 mg·L-1分别降低到597.7 mg·L-1和139.1 mg·L-1.
结合阳离子强度对RL胶束聚集形态的影响可以看出,Na+在低浓度时(<50 mmol·L-1)促进了RL胶束的形成,提供足够的RL胶束促进其对TCS的增溶作用;但当Na+浓度大于50 mmol·L-1后,TCS会因“盐析”作用而导致表观溶解度的降低(Yang et al., 2011).这与Abouseoud等(2010)的结论类似,他们发现在高盐度条件下萘在生物表面活性剂溶液中的表观溶解度会降低50%以上.
而Ca2+促进RL胶束形成的作用强烈,其在很低浓度(1 mmol·L-1)下就能与RL胶束产生强烈的盐桥作用而生成沉淀,这一方面是因降低了RL的稳定胶束浓度而大大降低了其对TCS的增溶性能,另一方面却又将包裹在RL中的TCS从水相中沉淀下来.
3.3 阳离子强度对RL作用下TCS在底泥-水中分配的影响不同阳离子强度条件下,RL作用下TCS在底泥-水相中的吸附等温线如图 4所示.线性拟合得到的模型参数列于表 1,R2值均在0.97以上,说明该吸附过程较好的符合Linear模型.线性吸附方程的斜率Kd*代表TCS在底泥-水-RL体系中的分配系数.Kd*值越大,说明TCS在底泥中的分配越多.从表 1可知,在Na+溶液中,Kd*值先减小后增大,从64.16 L·kg-1 (0 mmol·L-1)减小到40.81 L·kg-1 (30 mmol·L-1),然后增大到178.76 L·kg-1 (200 mmol·L-1),说明在Na+存在条件下,随着离子强度的增大,RL作用下TCS在底泥上的分配先减小后增大.在Ca2+溶液中,Kd*值在Ca2+小于1 mmol·L-1时无明显变化,在Ca2+大于1 mmol·L-1后迅速增大,当Ca2+浓度为30 mmol·L-1时达到4987.76 L·kg-1,说明在Ca2+存在条件下,在离子强度大于1 mmol·L-1后,随着离子强度的增大,RL作用下TCS在底泥上的分配逐渐增大.这是因为Ca2+离子强度越大,其与RL胶束间的盐桥作用使得RL沉淀越强,这不仅降低了RL对TCS的增溶作用,同时又将包裹在RL中的TCS沉淀下来,增强其在底泥相的分配.
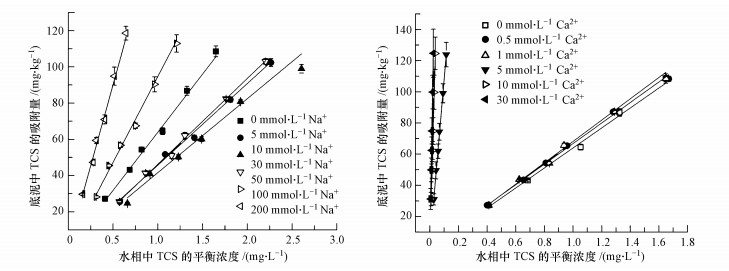 |
| 图 4 不同阳离子强度下鼠李糖脂作用下TCS在底泥上的吸附等温线 Fig. 4 Linear isotherm for the sorption of TCS onto sediment in the presence of rhamnolipid under various cationic strength |
| 表 1 不同阳离子强度下鼠李糖脂作用下TCS在底泥上吸附的线性吸附等温线参数 |
检测平衡后不同阳离子强度下水相中的TCS浓度(图 5),在有无阳离子存在下,TCS的浓度均约为0.14 mg·L-1,说明阳离子对TCS的在底泥-水相的分配并无影响.在添加RL但无阳离子条件下,TCS的浓度增加到1.33 mg·L-1,说明RL能有效的将TCS从底泥相转移到水相,提高了TCS在水相的分配比例.在有RL下再添加Na+,TCS的浓度随着Na+离子强度的增加先增加后降低,在Na+浓度为30 mmol·L-1时达到最大值(1.92 mg·L-1),而在浓度大于50 mmol·L-1后迅速下降,在Na+离子浓度为200 mmol·L-1时TCS的浓度下降到0.51 mg·L-1.在有RL下再添加Ca2+,在Ca2+离子浓度小于1 mmol·L-1时,水相中TCS的浓度无明显变化,而当Ca2+离子浓度仅仅大于1 mmol·L-1后,TCS浓度随离子强度的增大而快速降低,在30 mmol·L-1时降低到0.02 mg·L-1.这说明在RL作用下,低浓度Na+( < 50 mmol·L-1)能促进TCS向水相中迁移,提高了TCS在水相的分配比例;但很低浓度Ca2+(>1 mmol·L-1)和较高浓度Na+(>50 mmol·L-1)会抑制RL对TCS的增溶作用,甚至反过来增强TCS在底泥相的分配.
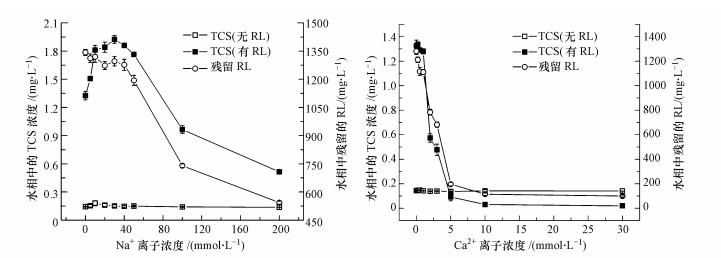 |
| 图 5 不同阳离子强度下TCS在底泥-水-RL体系中的分配及水相中残留的RL浓度 Fig. 5 The distribution of TCS in sediment-water-RL system and the residue RL concentration in water |
检测平衡后水相中残留的RL浓度(图 5),发现Na+浓度小于50 mmol·L-1时,RL浓度无明显变化,但大于该浓度后RL浓度显著下降;而Ca2+离子浓度仅仅在大于1 mmol·L-1后RL浓度就已显著下降.在Na+浓度为200 mmol·L-1,Ca2+浓度为30 mmol·L-1时,水相中的RL浓度从1250 mg·L-1分别降低到543.2 mg·L-1和99.1 mg·L-1.这与表观溶解度实验的结果一致.且添加底泥后水相中的RL浓度会更低,这说明此时存在RL因胶束聚集沉淀与底泥吸附作用.阴离子表面活性剂能通过静电吸附作用而绑定在底泥上(Rao and He, 2006).底泥对RL的吸附一方面降低了水相中RL的浓度,另一方面能增加底泥的有机质含量,从而增强底泥对TCS的吸附作用.与未添加阳离子的溶液相比,阳离子的添加增强了RL在底泥上的吸附,这是由于阳离子与RL分子间的盐桥作用降低了RL胶束与带负电荷的底泥间的静电斥力.
综合阳离子强度对RL胶束聚集及TCS表观溶解度的影响,可以得出阳离子强度通过阳离子与RL分子间的盐桥作用的强弱而影响RL的胶束聚集过程,使得水相中的RL浓度发生了明显的变化,从而影响了RL对TCS的增溶作用,改变TCS的表观溶解度,进而改变TCS在底泥-水中的分配.这为不同盐度和硬度水体中采用RL增溶TCS的修复提供了指导:在低盐度的软水中适合使用RL将TCS从底泥相转移到水相,强化其在好氧水相的生物降解过程以降低环境风险;但该方法不适用于高盐度或高硬度的水体.
4 结论(Conclusions)1) 阳离子对TCS的表观溶解度及其在底泥-水中的分配无明显作用,但能与RL分子形成盐桥作用而改变RL的胶束聚集形态及溶液的稳定性.相比Na+,Ca2+与RL分子间的盐桥作用要强得多.
2) 不同阳离子强度下RL胶束聚集行为的差异改变了水相中RL的浓度,进而导致了RL作用下TCS表观溶解度以及其在底泥-水中分配的不同.
3) RL胶束粒径随着Na+离子强度的增加先降低后增加,但随着Ca2+离子强度的增加逐渐降低.RL溶液的zeta电位随着Na+/Ca2+离子强度的增加而降低,即RL溶液的稳定度降低.Na+在浓度小于50 mmol·L-1下会促进RL胶束的形成,提高RL对TCS的增溶能力,促进TCS从底泥相向水相迁移,提高了TCS在水相的分配比例,吸附等温Kd*值从64.16 L·kg-1减小到40.81 L·kg-1(30 mmol·L-1 Na+);但Na+离子浓度大于50 mmol·L-1后会因“盐析”作用降低TCS的表观溶解度并抑制其向水相的迁移.Ca2+在浓度大于1 mmol·L-1后就能与RL胶束间产生强的盐桥作用而生成沉淀,大幅度降低RL的浓度以及其对TCS的增溶能力,反而提高了TCS在底泥的分配比例,Kd*值从64.16 L·kg-1增加到4987.76 L·kg-1(30 mmol·L-1 Ca2+).
| [${referVo.labelOrder}] | Abouseoud M, Yataghene A, Amrane A, et al. 2010. Effect of pH and salinity on the emulsifying capacity and naphthalene solubility of a biosurfactant produced by Pseudomonas fluorescens[J]. Journal of Hazardous Materials , 180 (1/3) : 131–136. |
| [${referVo.labelOrder}] | Alargova R G, Petkov J T, Petsev D N. 2003. Micellization and interfacial properties of alkyloxyethylene sulfate surfactants in the presence of multivalent counterions[J]. Journal of Colloid and Interface Science , 261 (1) : 1–11. DOI:10.1016/S0021-9797(03)00027-4 |
| [${referVo.labelOrder}] | Aranami K, Readman J W. 2007. Photolytic degradation of triclosan in freshwater and seawater[J]. Chemosphere , 66 (6) : 1052–1056. DOI:10.1016/j.chemosphere.2006.07.010 |
| [${referVo.labelOrder}] | Arutchelvi J, Sangeetha J, Philip J, et al. 2014. Self-assembly of surfactin in aqueous solution: Role of divalent counterions[J]. Colloids and Surfaces B: Biointerfaces) , 116 : 396–402. DOI:10.1016/j.colsurfb.2013.12.034 |
| [${referVo.labelOrder}] | Bai G Y, Brusseau M L, Miller R M. 1998. Influence of cation type, ionic strength, and pH on solubilization and mobilization of residual hydrocarbon by a biosurfactant[J]. Journal of Contaminant Hydrology , 30 (3/4) : 265–279. |
| [${referVo.labelOrder}] | Behera S K, Oh S Y, Park H S. 2010. Sorption of triclosan onto activated carbon, kaolinite and montmorillonite: Effects of pH, ionic strength, and humic acid[J]. Journal of Hazardous Materials , 179 (1/3) : 684–691. |
| [${referVo.labelOrder}] | Cao J, Guo H, Zhu H M, et al. 2008. Effects of SOM, surfactant and pH on the sorption-desorption and mobility of prometryne in soils[J]. Chemosphere , 70 (11) : 2127–2134. DOI:10.1016/j.chemosphere.2007.08.062 |
| [${referVo.labelOrder}] | Chen M L, Dong C C, Penfold J, et al. 2013. Influence of calcium ions on rhamnolipid and rhamnolipid/anionic surfactant adsorption and self-assembly[J]. Langmuir , 29 (12) : 3912–3923. DOI:10.1021/la400432v |
| [${referVo.labelOrder}] | Dann A B, Hontela A. 2011. Triclosan: environmental exposure, toxicity and mechanisms of action[J]. Journal of Applied Toxicology , 31 (4) : 285–311. DOI:10.1002/jat.1660 |
| [${referVo.labelOrder}] | ElSayed E M, Prasher S O. 2014. Sorption/desorption behavior of oxytetracycline and sulfachloropyridazine in the soil water surfactant system[J]. Environmental Science and Pollution Research , 21 (5) : 3339–3350. DOI:10.1007/s11356-013-2273-x |
| [${referVo.labelOrder}] | Helvacı Ş Ş, Peker S, Özdemir G. 2004. Effect of electrolytes on the surface behavior of rhamnolipids R1 and R2[J]. Colloids and Surfaces B: Biointerfaces) , 35 (3/4) : 225–233. |
| [${referVo.labelOrder}] | Jia D, You J, Hu Y, et al. 2015. Effect of CaCl2 on denaturation and aggregation of silver carp myosin during setting[J]. Food Chemistry , 185 : 212–218. DOI:10.1016/j.foodchem.2015.03.130 |
| [${referVo.labelOrder}] | Lin H, Hu Y Y, Zhang X Y, et al. 2011. Sorption of triclosan onto sediments and its distribution behavior in sediment-water-rhamnolipid systems[J]. Environmental Toxicology and Chemistry , 30 (11) : 2416–2422. DOI:10.1002/etc.v30.11 |
| [${referVo.labelOrder}] | 林晖, 胡勇有, 张潇予, 等.2011. 不同组分鼠李糖脂的胶束性质及其对三氯生的增溶作用[J]. 环境科学学报 , 2011, 31 (12) : 2609–2615. |
| [${referVo.labelOrder}] | McAvoy D C, Schatowitz B, Jacob M, et al. 2002. Measurement of triclosan in wastewater treatment systems[J]. Environmental Toxicology and Chemistry , 21 (7) : 1323–1329. DOI:10.1002/etc.v21:7 |
| [${referVo.labelOrder}] | Paria S, Yuet P K. 2007. Adsorption of non-ionic surfactants onto sand and its importance in naphthalene removal[J]. Industrial & Engineering Chemistry Research , 46 (1) : 108–113. |
| [${referVo.labelOrder}] | Penfold J, Thomas R K, Dong C C, et al. 2007. Equilibrium surface adsorption behavior in complex anionic/nonionic surfactant mixtures[J]. Langmuir , 23 (20) : 10140–10149. DOI:10.1021/la701151m |
| [${referVo.labelOrder}] | Rao P H, He M. 2006. Adsorption of anionic and nonionic surfactant mixtures from synthetic detergents on soils[J]. Chemosphere , 63 (7) : 1214–1221. DOI:10.1016/j.chemosphere.2005.08.067 |
| [${referVo.labelOrder}] | Sammalkorpi M, Karttunen M, Haataja M. 2009. Ionic surfactant aggregates in saline solutions: Sodium Dodecyl Sulfate (SDS) in the presence of excess sodium chloride (NaCl) or calcium chloride (CaCl2)[J]. The Journal of Physical Chemistry B , 113 (17) : 5863–5870. DOI:10.1021/jp901228v |
| [${referVo.labelOrder}] | Wang X K, Jiang X J, Wang Y N, et al. 2014. Occurrence, distribution, and multi-phase partitioning of triclocarban and triclosan in an urban river receiving wastewater treatment plants effluent in China[J]. Environmental Science and Pollution Research , 21 (11) : 7065–7074. DOI:10.1007/s11356-014-2617-1 |
| [${referVo.labelOrder}] | Wu W J, Hu Y Y, Guo Q, et al. 2015. Sorption/desorption behavior of triclosan in sediment-water-rhamnolipid systems: Effects of pH, ionic strength, and DOM[J]. Journal of Hazardous Materials , 297 : 59–65. DOI:10.1016/j.jhazmat.2015.04.078 |
| [${referVo.labelOrder}] | Yang G P, Ding H Y, Cao X Y, et al. 2011. Sorption behavior of nonylphenol on marine sediments: Effect of temperature, medium, sediment organic carbon and surfactant[J]. Marine Pollution Bulletin , 62 (11) : 2362–2369. DOI:10.1016/j.marpolbul.2011.08.036 |
| [${referVo.labelOrder}] | Ying G G, Yu X Y, Kookana R S. 2007. Biological degradation of triclocarban and triclosan in a soil under aerobic and anaerobic conditions and comparison with environmental fate modelling[J]. Environmental Pollution , 150 (3) : 300–305. DOI:10.1016/j.envpol.2007.02.013 |
| [${referVo.labelOrder}] | Yu H, Huang G H, An C J, et al. 2011. Combined effects of DOM extracted from site soil/compost and biosurfactant on the sorption and desorption of PAHs in a soil-water system[J]. Journal of Hazardous Materials , 190 (1/3) : 883–890. |
| [${referVo.labelOrder}] | Yu Y X, Zhao X, Bayly A E. 2008. Development of surfactants and builders in detergent formulations[J]. Chinese Journal of Chemical Engineering , 16 (4) : 517–527. DOI:10.1016/S1004-9541(08)60115-9 |
| [${referVo.labelOrder}] | Zhang X Y, Guo Q, Hu Y Y, et al. 2013. Effects of monorhamnolipid and dirhamnolipid on sorption and desorption of triclosan in sediment-water system[J]. Chemosphere , 90 (2) : 581–587. DOI:10.1016/j.chemosphere.2012.08.036 |
| [${referVo.labelOrder}] | Zhao J L, Ying G G, Liu Y S, et al. 2010. Occurrence and risks of triclosan and triclocarban in the Pearl River system, South China: From source to the receiving environment[J]. Journal of Hazardous Materials , 179 (1/3) : 215–222. |
| [${referVo.labelOrder}] | Zhou W J, Zhu L Z. 2007. Enhanced desorption of phenanthrene from contaminated soil using anionic/nonionic mixed surfactant[J]. Environmental Pollution , 147 (2) : 350–357. DOI:10.1016/j.envpol.2006.05.025 |
 2016, Vol. 36
2016, Vol. 36


