2. 重庆长安汽车股份有限公司动力研究院, 重庆 401120
2. Powertrain Engineering R & D Center, Chongqing Chang'an Automobile Company Limited, Chongqing 401120
缸内直喷(Gasoline Direct Injection,GDI)汽油机由于具有良好的动力性和经济性而成为汽油机发展的主要趋势之一.但由于燃油直接在缸内喷射造成油气混合不均和燃油湿壁现象增多,从而导致GDI汽油机的颗粒物(PM)排放浓度远高于传统的PFI汽油机的颗粒物排放浓度(Braisher et al .,2010;魏群等,2015).日益严格排放法规对GDI汽油机颗粒物排放提出了更高的限制要求(Myung et al .,2012).
GDI汽油机尾气中主要有碳氢化合物(HC)、颗粒物等常规污染物,还存在少量的非常规污染物,如醛类、多环芳烃(Polycyclic Aromatic Hydrocarbons,PAHs)、金属粒子等.其中,多环芳烃是最早发现的具有致癌、致畸、致突变作用的有机污染物之一,对人体健康和生态环境危害较大(Menzie et al.,1992),世界上许多国家都已将PAHs列为优先控制的环境污染物.近年来,中国汽车保有量迅速增加,有研究表明,汽车尾气已经成为多环芳烃污染物的主要来源之一(李军等,2004).此外,PAHs通常被认为是发动机生成碳烟颗粒的前驱物,对碳烟颗粒的形成与演化有重要影响(Leermakers et al .,2015).所以,为了减少汽车尾气中的有害气体和碳烟颗粒排放,有必要对发动机的PAHs排放开展相关研究.
当前,对于发动机PAHs排放的相关研究主要集中于柴油机(Karavalakis et al.,2011;Guarieiro et al.,2014;Huang et al.,2015;Vojtisek-Lom et al.,2015;王忠等,2011),国内外研究人员对汽油机,尤其是GDI汽油机PAHs排放的相关研究较少(Elghawi et al.,2010;An et al.,2015).基于此,本文在一台缸内直喷汽油机上对尾气中的气相和颗粒相PAHs进行采集,利用气相色谱-质谱(GC-MS)化学分析方法进行定性与定量分析,研究不同点火时刻和废气再循环(EGR)率对GDI汽油机尾气中PAHs排放的影响,以期为发展汽油燃料燃烧生成PAHs的化学反应机理提供数据支持,同时为深入认识GDI汽油机碳烟生成机理及探寻降低GDI汽油机有害气体和颗粒物排放的措施提供参考.
2 试验装置和方法(Experiment and methods) 2.1 PAHs采集试验试验使用的发动机是一款直列四缸涡轮增压四冲程气流引导型缸内直喷汽油机,其主要的技术参数见表 1.试验用燃油为壳牌公司销售的满足国Ⅴ标准的95#汽油,参考国标《GB 17930-2013 车用汽油》,其主要特性参见表 2. 试验采用自行设计的采样装置对汽油机尾气中颗粒相和气相PAHs进行采集,PAHs采集试验台架如图 1所示.利用开放式ECU控制点火时刻等参数;空燃比仪实时监测过量空气系数,始终保持过量空气系数为1.0;AVL415烟度计测量尾气中的碳烟浓度;Horiba MEXA-7100 DEGR排放分析仪结合EGR阀进行EGR率的测量和调节.GDI汽油机尾气由真空泵将其从排气管中抽出,经稀释(稀释气体为N2)后,通过串联在同一管路上的采样装置进行PAHs的采集.用涂有碳氟化合物的耐热型硼硅玻璃纤维标准滤膜采集尾气中颗粒相PAHs,用聚氨基甲酸乙酯泡沫(PUF)+XAD-2采集尾气中的气相PAHs.采样流量控制在5 L·min-1,为保证采集到足量的样品,每个工况平均采集时间为45 min.
| 表 1 发动机技术参数 Table 1 Engine technical parameter |
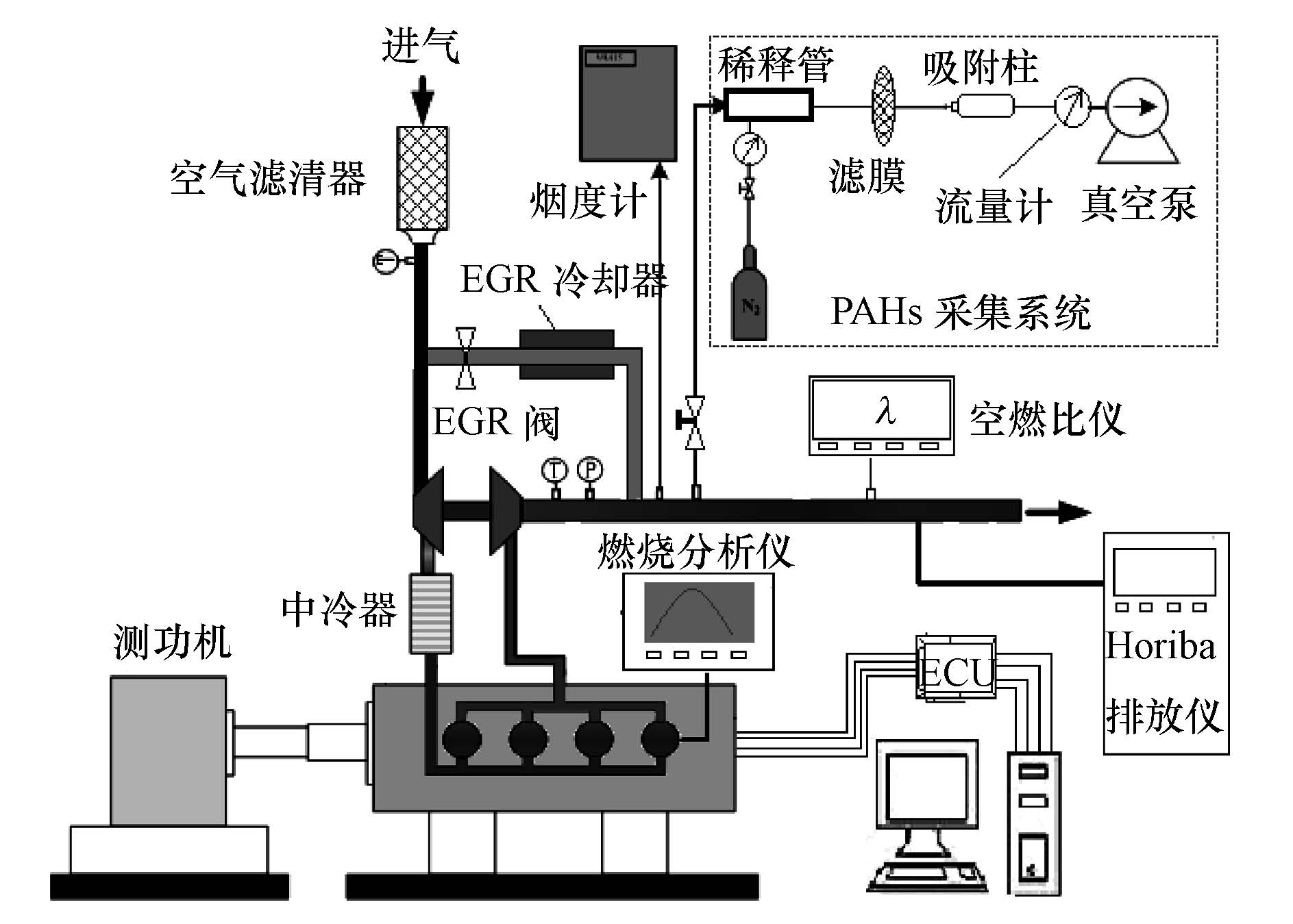 |
| 图 1 试验台架布置示意图 Fig. 1 Schematic diagram of test bench |
| 表 2 燃料特性 Table 2 Fuel properties |
为了研究不同点火时刻和EGR率对GDI汽油机尾气中PAHs排放的影响,试验时保持发动机在转速2000 r·min-1和转矩120 N·m的工况下,分别设置点火时刻为压缩上止点前10°CA、14°CA、18°CA、23°CA和25°CA;EGR率分别设置为0、2.5%、5.0%、8.0%和10%.在每个试验点下,待发动机稳定运行2 min后开始测量和记录数据,对每个试验点都进行了3次试验,试验结果均为3次试验数据的平均值以减小误差.此外,为了尽可能减小边界条件因素的影响,进气温度、冷却液温度、机油温度分别保持在(35±2)、(85±2)、(90±2)℃.
2.2 采集样品前处理将采样后的玻璃纤维滤膜用纯净的 60 mL CH2Cl2加热萃取12 h,将采样后的PUF/XAD-2/PUF多环吸附柱用120 mL纯净的 CH2Cl2索氏萃取24 h.萃取后的溶液用旋转蒸发仪蒸发浓缩至约1 mL,浓缩过程中用氮气保护,以防止样品成分被空气污染或氧化变质.
2.3 PAHs样品分析由于PAHs成分复杂,试验选择了被美国国家环保局(USEPA)优先列为监测污染物的16种PAHs进行定性定量分析,分别是萘(Nap)、苊(Acp)、苊烯(Acpy)、芴(Flu)、菲(PA)、蒽(Ant)、荧蒽(FL)、芘(Pyr)、苯并[a]蒽(BaA)、䓛(CHR)、苯并[b]荧蒽(BbF)、苯并[k]荧蒽(BkF)、苯并[a]芘(BaP)、茚并[1,2,3-cd]芘(IND)、二苯并[a,h]蒽(DBA)、苯并[g,h,i]苝(BghiP).
GC-MS分析仪器为美国安捷伦公司生产的Agilent 7890A-5975C MSD型气相色谱-质谱联用仪和G1030-90201-MSD型化学工作站.GC-MS分析条件(何浩然,2012)为:进样方式为不分流进样,进样量为1 μL;高纯氦气作为载气,恒流量1.0 mL·min-1;色谱柱采用Agilent HP-5型(30 m×250 μm×0.25 μm);色谱柱升温程序为30 ℃保持7.5 min,以30 ℃·min-1升温到 280 ℃,保持8 min,再以60 ℃·min-1升温到 300 ℃,保持6 min;质谱离子源为电子轰击源(EI),离子源温度为280 ℃;四极杆温度为150 ℃;质谱调谐标准物质为全氟三丁胺(BFTBA);全扫描+选择离子(SIM)扫描方式,扫描质量范围为30~310 amu;质谱检索谱库为美国国家标准局NIST05数据库.
采用保留时间及气相色谱/质谱总离子流谱图(TIC)对PAHs进行定性,图 2为标准样品中16种PAHs色谱图;采用外标法定量.试验中选取浓度为 0.1 μg·mL-1的标准样品,平行重复进样6次,由实验数据计算出16种PAHs每种物质的平均相对标准偏差(RSD)值在1.12%~6.07%之间,符合检测要求.
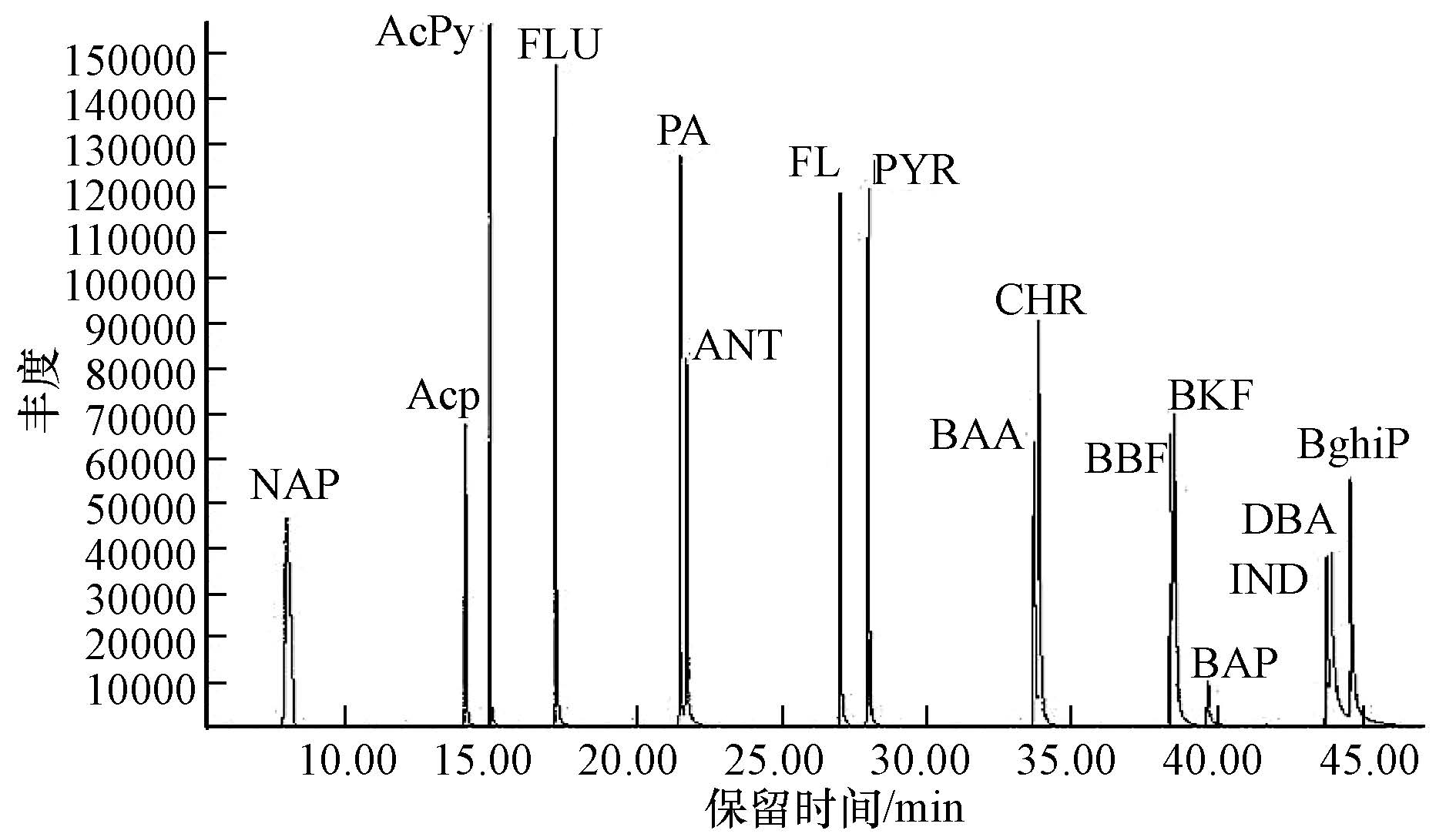 |
| 图 2 标准样品中16种PAHs色谱图 Fig. 2 Chromatogram of 16 kinds of PAHs in standard sample |
图 3是GDI汽油机尾气中碳烟和总PAHs排放随点火时刻的变化关系.由图 3可知,随着点火时刻的提前,尾气中PAHs总浓度呈现先减小后增加再减小的变化趋势,碳烟浓度也呈现相似变化,表明尾气中PAHs的浓度变化可以作为碳烟排放的表征之一.
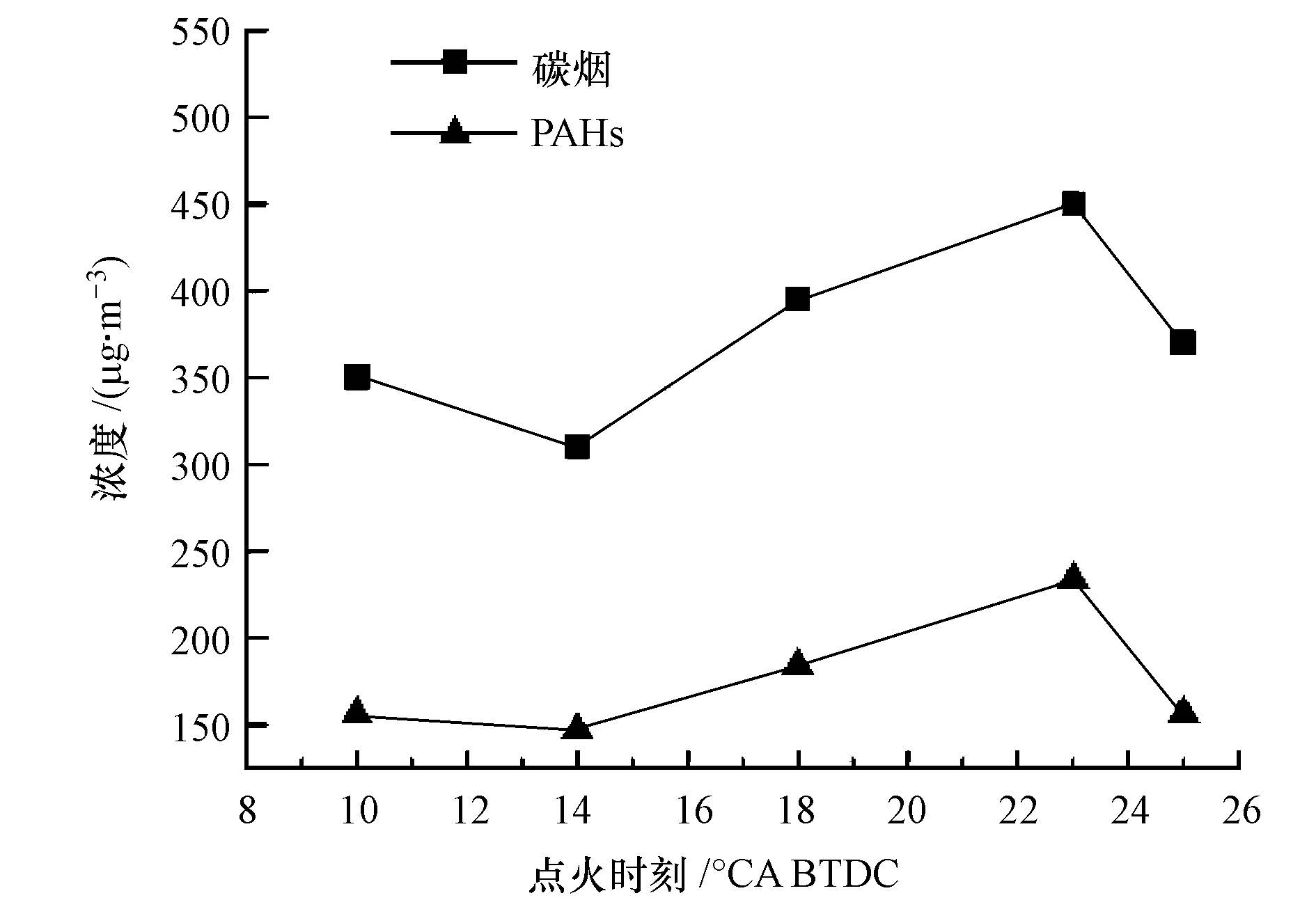 |
| 图 3 点火时刻对碳烟和总PAHs排放的影响 Fig. 3 Effect of spark timing on soot and total PAHs emissions |
如图 4所示,在不同点火时刻的GDI汽油机PAHs排放中,气相PAHs浓度大于140 μg·m-3,所占比例也均在96.9%以上;颗粒相PAHs浓度均在8 μg·m-3以下,所占比例均小于3.1%.随着点火时刻的提前,气相和颗粒相PAHs的浓度呈现相似的变化趋势,都是先略微减小然后逐渐增大最后有所减小,而二者所占比例变化趋势相反,气相PAHs所占比例先增大后减小,颗粒相PAHs所占比例先减小后增大.
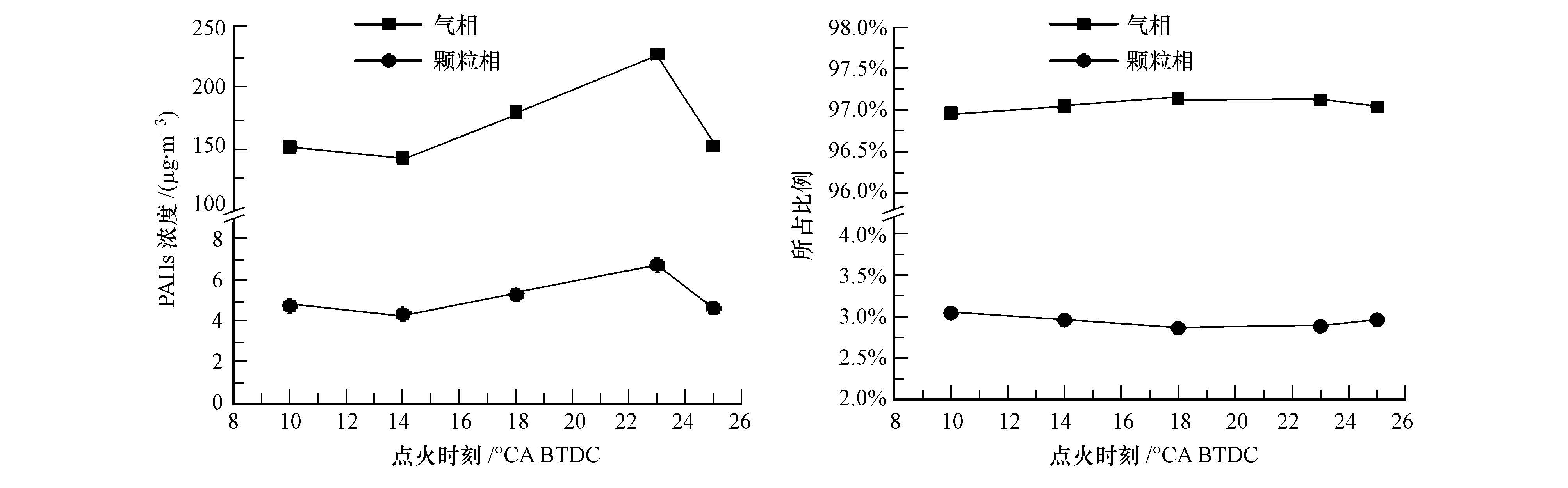 |
| 图 4 点火时刻对气相和颗粒相PAHs排放的影响 Fig. 4 Effect of spark timing on particulate-phase and vapour-phase PAHs emissions |
各环PAHs在气相中的分布如图 5所示,在气相PAHs中,2环PAHs浓度最高,所占比例均在82%以上且随着点火时刻的提前而增大;3环PAHs所占比例在5%~15%之间且随着点火时刻的提前而减小;其他各环PAHs浓度较低,所占比例较小,变化趋势不明显.
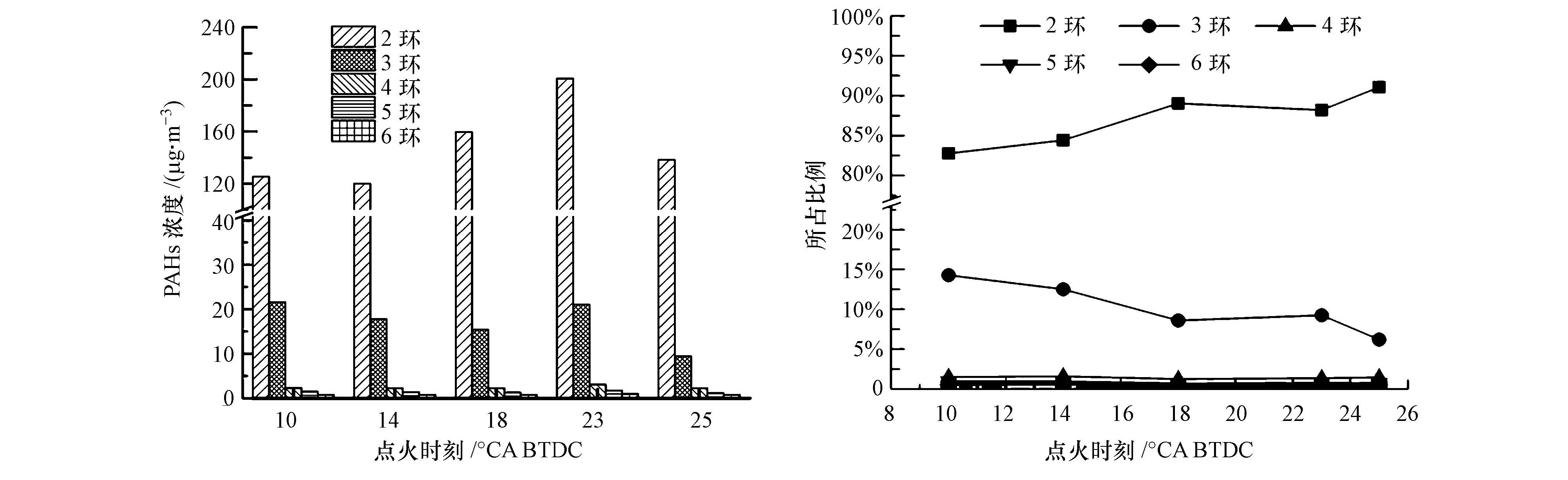 |
| 图 5 点火时刻对气相PAHs中不同环数PAHs的影响 Fig. 5 Effect of spark timing on vapour-phase PAHs with different rings |
如图 6所示,在颗粒相PAHs中,4环PAHs浓度最高,所占比例最大,均在40%左右;5环PAHs所占比例在22%~25%之间;3环和6环PAHs所占比例均在17%左右;2环PAHs在颗粒相中浓度最低,所占比例在4%以下.当点火时刻为23°CA BTDC时,颗粒相PAHs中,2环PAHs浓度减小,所占比例达到最小值,其他各环PAHs浓度均有所增加;在其他点火时刻,各环PAHs浓度变化不明显.
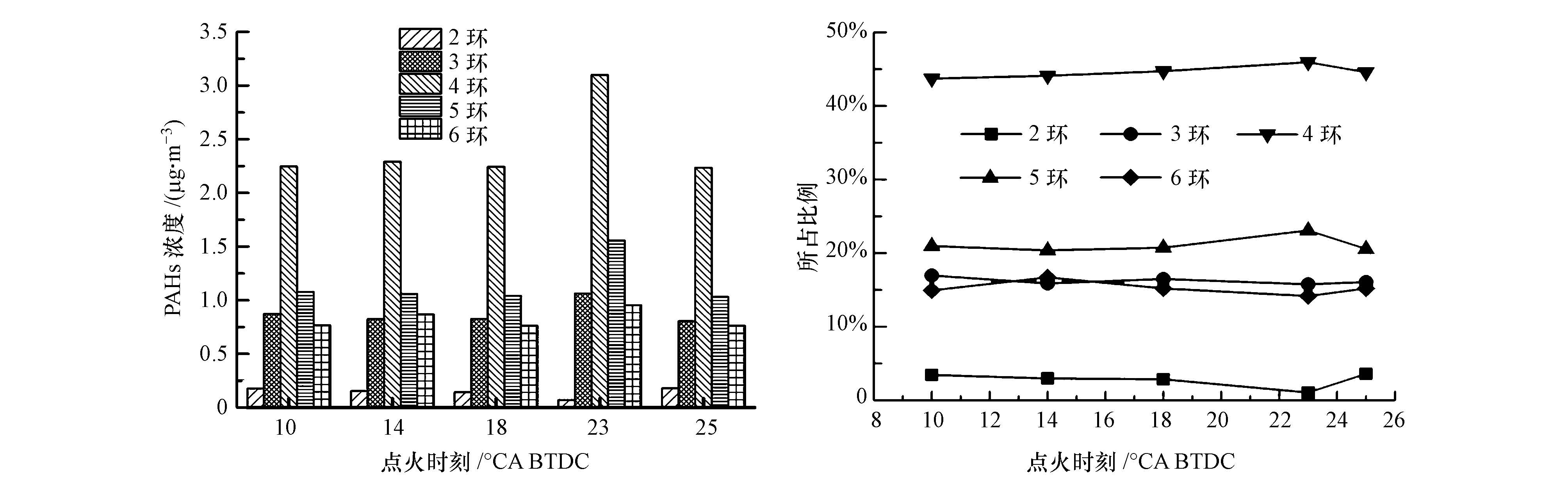 |
| 图 6 点火时刻对颗粒相PAHs中不同环数PAHs的影响 Fig. 6 Effect of spark timing on particulate-phase PAHs with different rings |
温度是影响PAHs生成的重要因素.如图 7所示,当点火时刻由压缩上止点前10°CA提前到14°CA后,由于燃烧速度加快,等容度提高,发动机的热效率升高,缸内燃烧峰值温度升高,峰值温度出现时刻提前,燃烧持续期增加,表明缸内燃烧有所改善,未完全燃烧的燃油比例有所减小,同时较高温度有利于小环PAHs分子通过脱氢加乙炔反应(HACA)生长为大环PAHs(Jones et al.,2004),所占比例较大的气相中的2环和3环PAHs浓度均有所减小,而颗粒相的5环和6环PAHs浓度略微增大,从而使得总的PAHs浓度减小.在点火时刻从压缩上止点前14°CA提前到23°CA的过程中,虽然缸内峰值温度逐渐升高,但由于点火时刻的提前使得大部分燃料在上止点附近的急燃期内迅速燃烧,等容度和理论热效率升高,废气带走的能量减少,后燃期内燃烧的燃料也相应减少,膨胀冲程的缸内温度和排气温度明显下降,PAHs后期氧化减少,从而导致PAHs排放浓度增大.而在点火时刻为25°CA BTDC时,缸内燃烧峰值温度最高,高温持续时间较长,排气温度有所升高,有利于PAHs的后期氧化,同时在该工况下试验中出现了轻微爆震,在一定程度上改善了缸内燃烧状况,从而导致了点火时刻为25°CA BTDC时PAHs和碳烟排放浓度的降低.
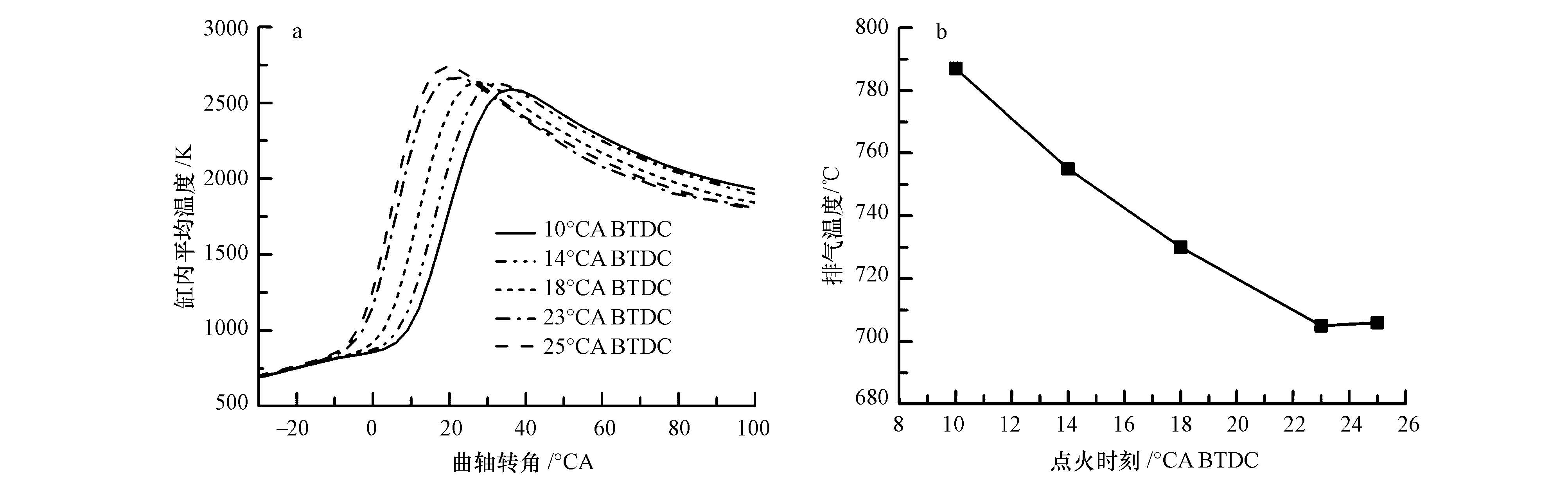 |
| 图 7 缸内平均温度(a)和排气温度(b)随点火时刻的变化 Fig. 7 Variation of average in-cylinder temperature(a)and exhaust temperature(b)with time |
GDI汽油机尾气中的碳烟和PAHs浓度随EGR率的变化关系如图 8所示.随着EGR率的不断增大,尾气中的碳烟浓度整体上呈现逐渐减小的趋势,PAHs浓度也在整体上呈现逐渐减小的趋势,两者的变化趋势同样具有一定的相似性.进气添加EGR后,尾气中PAHs的排放明显减小,最大降幅达到83%,与改变点火提前角相比,添加EGR能够更有效地降低尾气中PAHs排放.
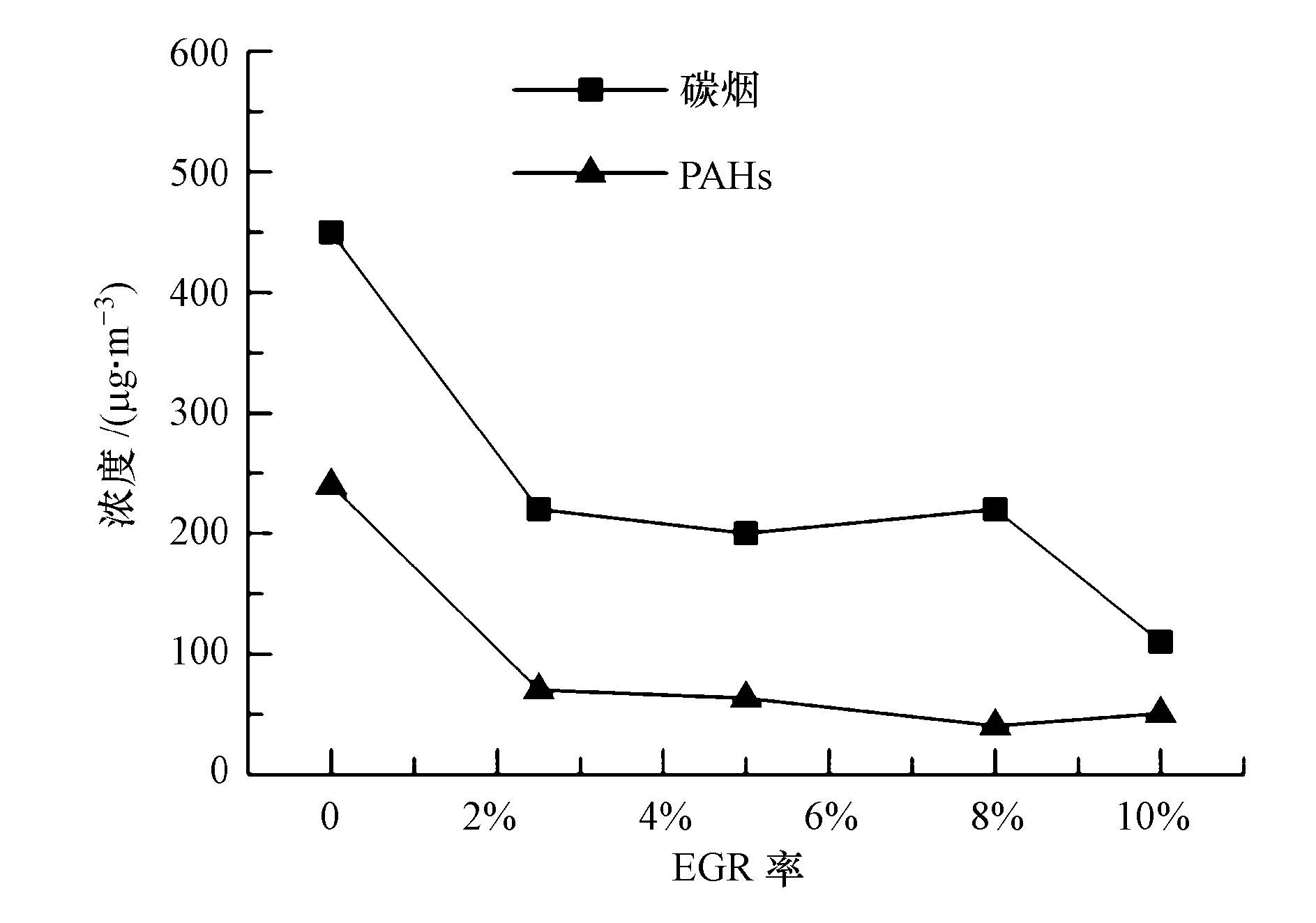 |
| 图 8 EGR率对碳烟和总PAHs排放的影响 Fig. 8 Effect of EGR rate on soot and total PAHs emissions |
通过EGR将一部分废气加入到进气的新鲜充量中,由于废气具有稀释作用和热容作用,稀释作用降低了发动机缸内氧浓度,热容效应增大了工质的热容,两者的共同作用抑制了工质的燃烧,降低了缸内最高燃烧温度,使放热过程变的迟缓.如图 9所示,随着EGR率的增大,缸内最高燃烧温度逐渐下降,峰值出现时刻逐渐后移.废气对缸内工质有一定的加热作用,有利于燃油的蒸发雾化,改善了缸内工质燃烧质量;燃烧温度的降低抑制了缸内燃油的热裂解和脱氢反应,减少了初级碳烟粒子的形成;缸内局部过浓区温度的降低也抑制了碳烟颗粒的生成;此外,燃烧后期温度下降不明显,碳烟后期氧化没有明显减少,在这几种因素的共同作用下,导致随着EGR率的不断增大,尾气中的碳烟浓度整体上逐渐减小.燃烧温度的降低可以有效抑制燃油在高温条件下热解成小分子的碳氢物质(如乙烯、乙炔等),从而减弱了这些小分子物质的聚合、重组和环化反应,抑制了苯环的形成和苯环成长为大环PAHs的倾向,最终使得PAHs的生成量减小(Wang et al.,1997; An et al.,2015).另外,燃烧后期温度和排气温度下降不明显,保证了PAHs的后期氧化,两者共同作用使得PAHs的排放逐渐减少.
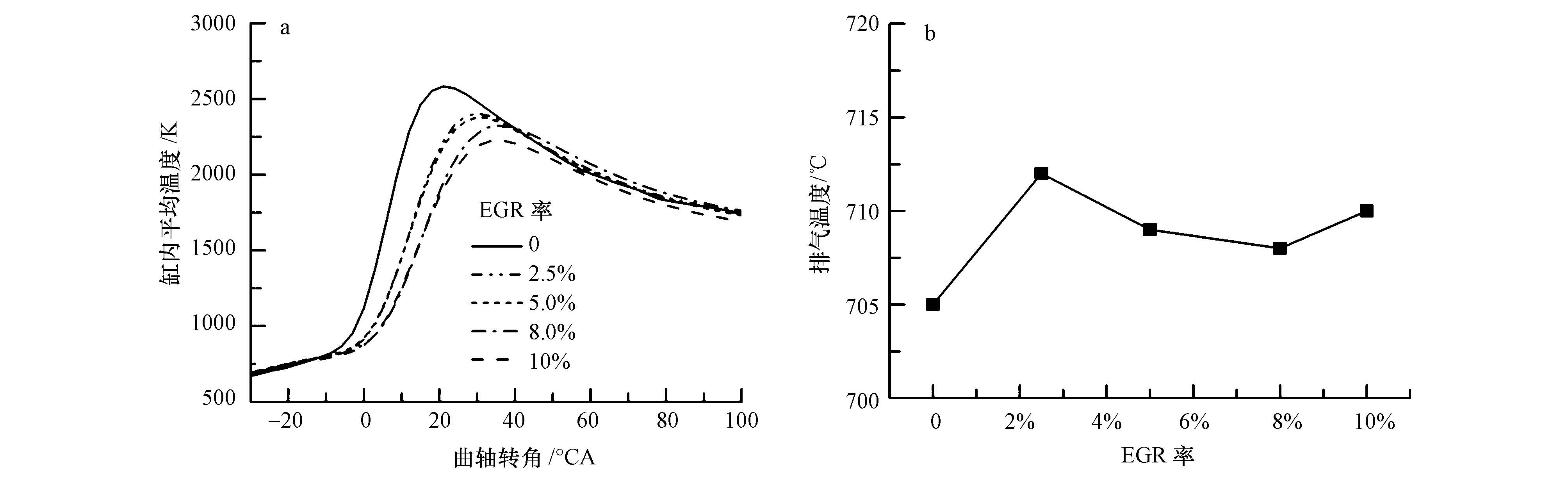 |
| 图 9 缸内平均温度(a)和排气温度(b)随EGR率的变化 Fig. 9 Average in-cylinder temperature(a)and the exhaust temperature(b)with the EGR rate changes |
图 10展示了EGR率对气相和颗粒相PAHs的影响.随着EGR率的不断增大,尾气中气相PAHs的浓度呈现逐渐降低的变化趋势,最大降幅达到90.9%,且平均浓度远高于颗粒相PAHs浓度.EGR率为2.5%时,颗粒相PAHs降低比较明显,继续增加EGR率,颗粒相PAHs降低不明显.EGR率的增大使得缸内燃烧温度逐渐降低,抑制了燃油在高温条件下热解而产生的小分子碳氢物质的生成及聚合、重组和环化反应,从而减少了小环PAHs的生成,使得以小环PAHs为主的气相PAHs排放逐渐减少;小分子碳氢物质及小环PAHs的减少,不利于小环PAHs通过脱氢加乙炔的反应(HACA反应机理)成长为大环PAHs,从而导致了以大环PAHs为主的颗粒相PAHs的减少.随着EGR率的增大,尾气中的气相PAHs所占比例均在87%以上,且呈现先减小后增大的变化趋势;尾气中颗粒相PAHs所占比例均小于12.5%,最低达到2.81%,且随着EGR率的增大,呈现先增大后减小的变化趋势.
 |
| 图 10 EGR率对气相和颗粒相PAHs排放的影响 Fig. 10 Effect of EGR rate on particulate-phase and vapour-phase PAHs emissions |
图 11展示了EGR率对气相PAHs中各环PAHs的影响.在气相PAHs中,2环PAHs的浓度仍然最高,所占比例最大,均在63%以上,最高达到86%;其次是3环PAHs,所占比例在11%~25%之间;其余各环PAHs浓度较低,所占比例较小.随着EGR率的增大,在气相PAHs中,2环PAHs的浓度和所占比例先不断减小,当EGR率大于8%时又有所增大;3环PAHs浓度整体上呈现逐渐减小的趋势,但所占比例呈现先增加后减小的趋势;其余各环PAHs由于浓度较低,变化趋势不明显.
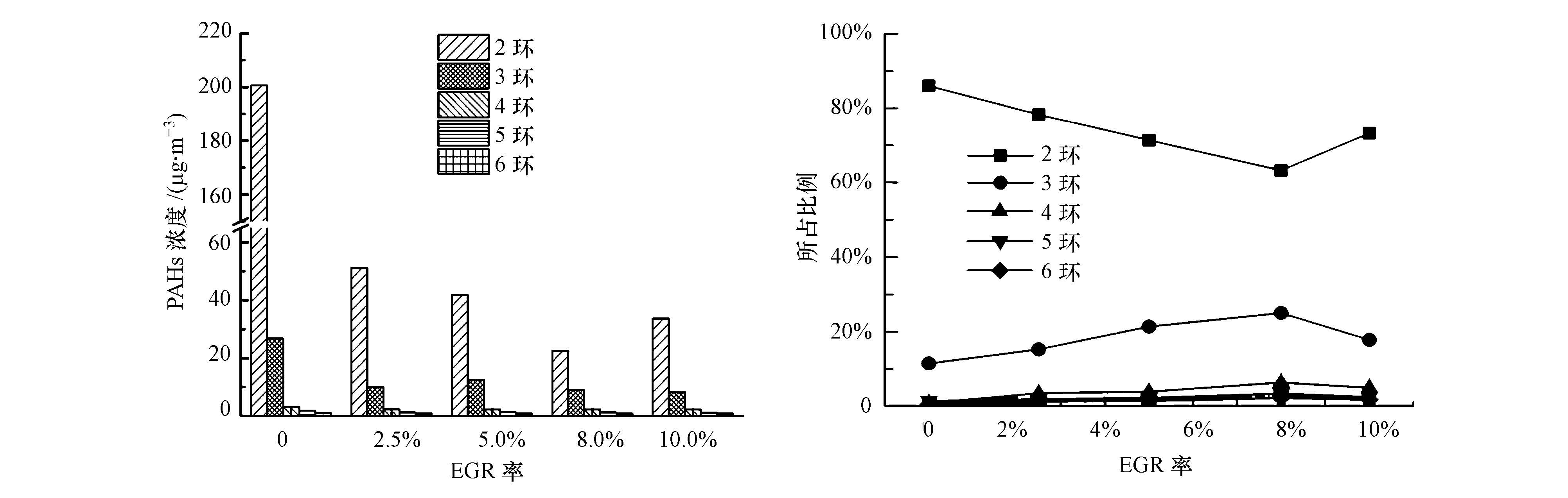 |
| 图 11 EGR率对气相PAHs中不同环数PAHs的影响 Fig. 11 Effect of EGR rate on vapour-phase PAHs with different rings |
EGR率对颗粒相PAHs中各环PAHs的影响如图 12所示.在颗粒相PAHs中,4环PAHs的浓度最高,所占比例最大,均在45%左右;其次是5环PAHs,所占比例在20%~23%之间;3环和6环PAHs浓度相近,所占比例均在15%左右;2环PAHs浓度最低,所占比例在4%以下.随着EGR率的增大,2环PAHs浓度先增加后减小,其余各环PAHs的浓度整体上均呈现逐渐减小的变化趋势.4环和5环PAHs所占比例整体上均呈现不断减小的变化趋势;2环PAHs所占比例则先增大然后有所减小.
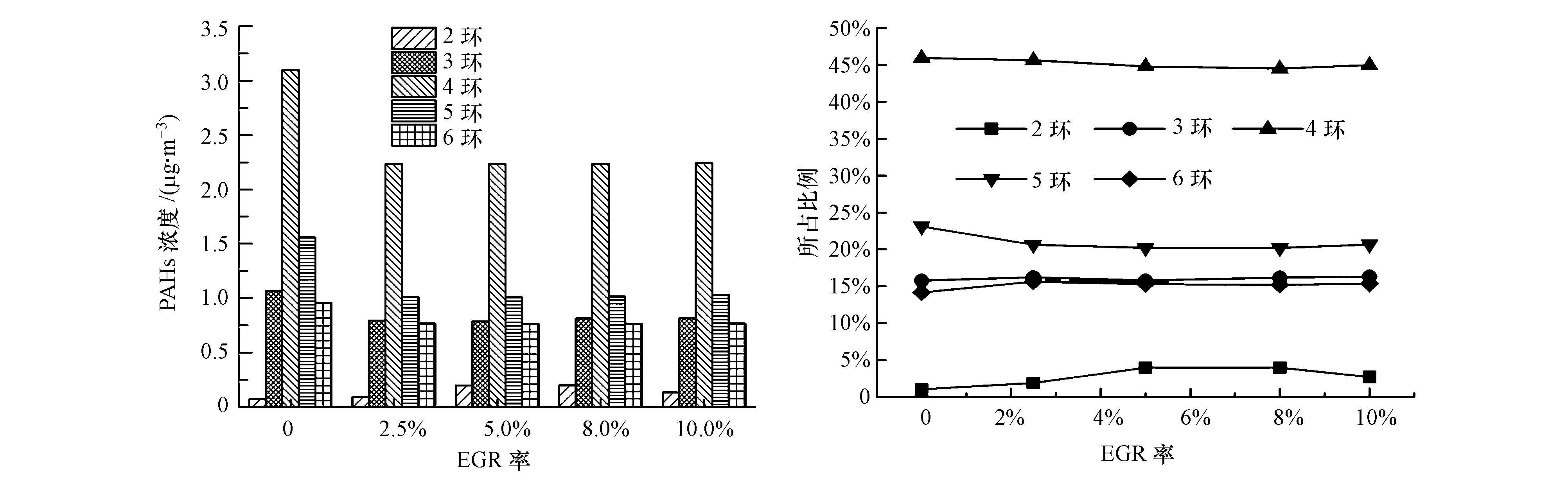 |
| 图 12 EGR率对颗粒相PAHs中不同环数PAHs的影响 Fig. 12 Effect of EGR rate on particulate-phase PAHs with different rings |
PAHs作为一类有毒的污染物,会对人体健康造成严重危害.然而,各种PAHs的毒性差异很大,Nisbet和LaGoy(1992)以BaP为标准,提出了不同PAHs的毒性相当因子(Toxicology Equivalent Factor,TEF),通过计算可得PAHs的毒性当量,可以作为发动机尾气毒性的可比性指标.一般而言,毒性当量越高代表致癌风险越大.毒性当量的计算公式为:
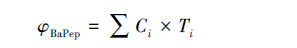
|
式中,Ci 为各种PAHs的浓度百分比; Ti 为各种PAHs的毒性相当因子(TEF),具体如表 3所示.
| 表 3 16种PAHs的毒性当量因子 Table 3 TEF for 16 kinds of PAHs |
图 13为不同点火时刻和EGR率下GDI汽油机尾气排放的PAHs毒性当量.由图 13a可知,在不同的点火时刻下,尾气中PAHs的毒性当量在0.0098~0.0124之间,在点火时刻为18°CA BTDC时,尾气的毒性当量最小.如图 13b所示,随着EGR率的增加,尾气中的PAHs毒性当量先增大然后有所减小,在EGR率为8%时达到最大值,整体上呈增大趋势.与改变点火时刻相比,GDI汽油机加入EGR后,尾气中的PAHs毒性当量增加更明显.
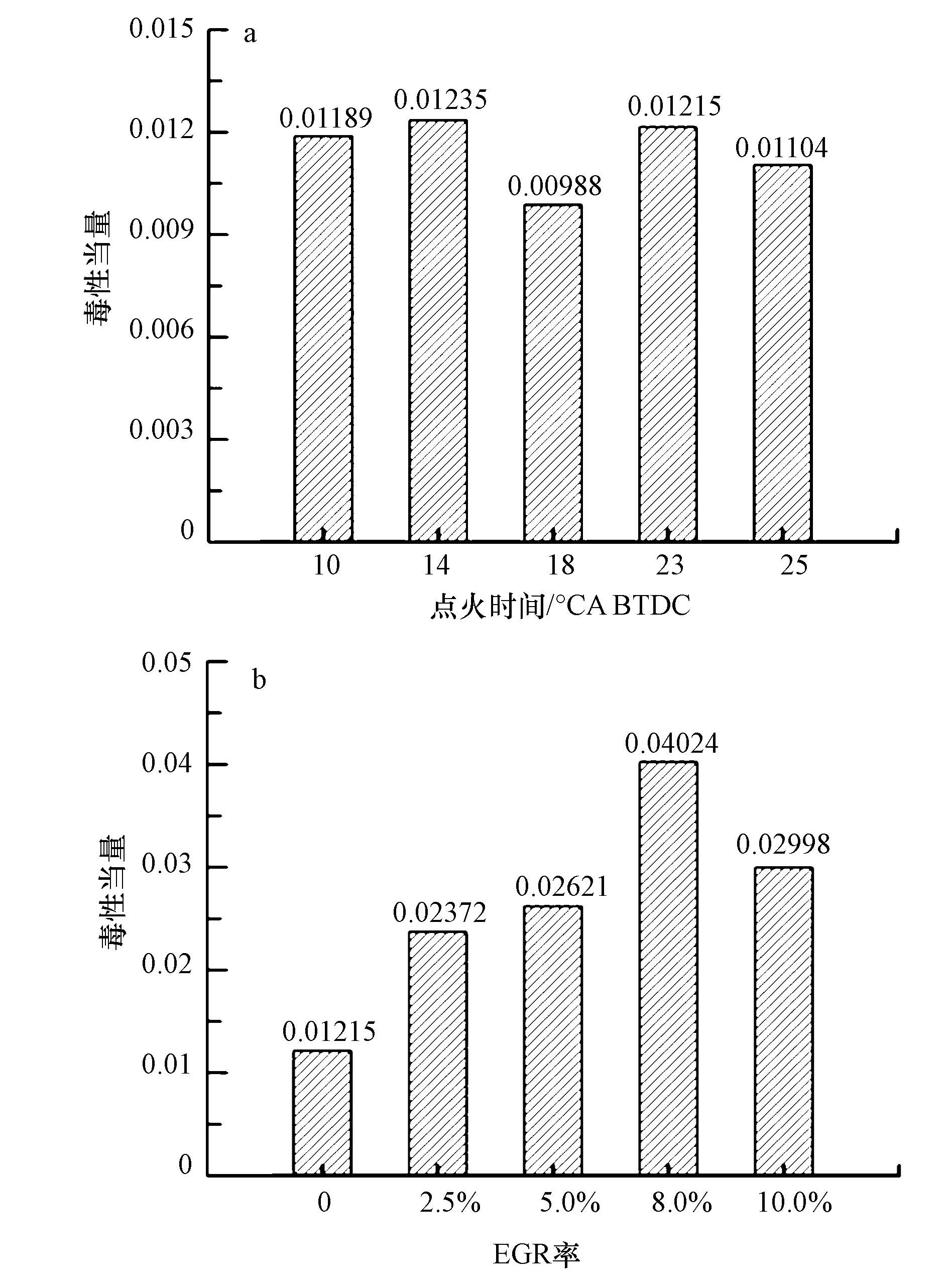 |
| 图 13 不同点火时刻(a)和不同EGR率(b)的PAHs毒性当量 Fig. 13 Toxicity equivalent of PAHs under different spark timings(a)and different EGR rates(b) |
1) 中速中负荷时,在边界条件和其他运行参数基本稳定的前提下,改变点火时刻和EGR率后,GDI汽油机尾气中的碳烟浓度和PAHs浓度的变化趋势具有相似性,表明尾气中PAHs的浓度变化可以作为碳烟排放的表征之一.
2) GDI汽油机的PAHs排放以气相为主,气相PAHs浓度远高于颗粒相PAHs浓度,在气相PAHs中主要是2环和3环等小环PAHs,而在颗粒相PAHs中则是以4环及以上的大环PAHs为主.
3) 随着点火时刻的提前,尾气中总的PAHs浓度及气相和颗粒相PAHs浓度均先减小后增加,当点火时刻超过23°CA BTDC后,由于出现了轻微爆震,PAHs浓度又有所减小.随着EGR率的增大,PAHs排放整体上呈现逐渐减小的变化趋势,其中,气相PAHs所占比例先减小后增大,颗粒相PAHs所占比例的变化趋势与之相反.点火时刻和EGR率的变化对气相中的2环、3环PAHs所占比例影响较大,而对颗粒相中的各环PAHs所占比例影响较小.
4) 以BaP为标准,与改变点火时刻相比,GDI汽油机加入EGR后会显著增大尾气毒性.
| [1] | An Y Z, Pei Y Q, Qin J, et al. 2015. Kinetic modeling of polycyclic aromatic hydrocarbons formation process for gasoline surrogate fuels[J]. Energy Conversion and Management , 100 : 249–261. DOI:10.1016/j.enconman.2015.05.013 |
| [2] | An Y Z, Teng S P, Pei Y Q, et al. 2016. An experimental study of polycyclic aromatic hydrocarbons and soot emissions from a GDI engine fueled with commercial gasoline[J]. Fuel , 164 (1) : 160–171. |
| [3] | Braisher M, Stone R, Price P.2010.Particle number emissions from a range of European vehicles[R]. 2010-01-0786. Detroit, Michigan, USA: Society of Automotive Engineers(SAE) |
| [4] | Elghawi U M, Mayouf A, Tsolakis A, et al. 2010. Vapour-phase and particulate-bound PAHs profile generated by a (SI/HCCI) engine from a winter grade commercial gasoline fuel[J]. Fuel , 89 (8) : 2019–2025. DOI:10.1016/j.fuel.2010.01.002 |
| [5] | Guarieiro A L N, Santos J V S, Eiguren-Fernandez A, et al. 2014. Redox activity and PAH content in size-classified nanoparticles emitted by a diesel engine fuelled with biodiesel and diesel blends[J]. Fuel , 116 (3) : 490–497. |
| [6] | 国家环境保护总局. 2003. 空气和废气监测分析方法[M]. 北京: 中国环境科学出版社 . |
| [7] | 国家质量监督检验检疫总局.2013.GB 17930-2013 车用汽油[S].北京:中国标准出版社 http://www.cnki.com.cn/Article/CJFDTotal-LYSZ201401018.htm |
| [8] | 何浩然.2012.不同燃料在柴油机燃烧过程中多环芳香烃演化的实验研究[D].天津:天津大学 http://cdmd.cnki.com.cn/article/cdmd-10056-1012022957.htm |
| [9] | Huang L, Bohac S V, Chernyak S M, et al. 2015. Effects of fuels, engine load and exhaust after-treatment on diesel engine SVOC emissions and development of SVOC profiles for receptor modelng[J]. Atmospheric Environment , 102 : 228–238. DOI:10.1016/j.atmosenv.2014.11.046 |
| [10] | Jones C C, Chughtai A R, Murugaverl B, et al. 2004. Effects of air/fuel combustion ratio on the polycyclic aromatic hydrocarbon content of carbonaceous soots from selected fuels[J]. Carbon , 42 (12) : 2471–2484. |
| [11] | Karavalakis G, Bakeas E, Fontaras G, et al. 2011. Effect of biodiesel origin on regulated and particle-bound PAH (polycyclic aromatic hydrocarbon) emissions from a Euro 4 passenger car[J]. Energy , 36 (8) : 5328–5337. DOI:10.1016/j.energy.2011.06.041 |
| [12] | Leermakers C A J, Musculus M P B. 2015. In-cylinder soot precursor growth in a low-temperature combustion diesel engine: Laser-induced fluorescence of polycyclic aromatic hydrocarbons[J]. Proceedings of the Combustion Institute , 35 (3) : 3079–3086. DOI:10.1016/j.proci.2014.06.101 |
| [13] | 李军, 张干, 祁士华, 等.2004. 广州市大气中颗粒态多环芳烃 (PAHs) 的主要污染源[J]. 环境科学学报 , 2004, 24 (4) : 661–666. |
| [14] | Myung C L, Park S. 2012. Exhaust nanoparticle emissions from internal combustion engines: A review[J]. International Journal of Automotive Technology , 13 (1) : 9–22. DOI:10.1007/s12239-012-0002-y |
| [15] | Menzie C A, Potoki B B, Santodonato J. 1992. Exposure to carcinogenic PAHs in the environment[J]. Environmental Science and Technology , 26 (7) : 1278–1284. DOI:10.1021/es00031a002 |
| [16] | Nisbet I C T, LaGoy P K. 1992. Toxic equivalency factors (TEFs) for polycyclic aromatic hydrocarbons (PAHs)[J]. Regulatory Toxicology and Pharmacology , 16 (3) : 290–300. DOI:10.1016/0273-2300(92)90009-X |
| [17] | Vojtisek-Lom M, Pechout M, Dittrich L, et al. 2015. Polycyclic aromatic hydrocarbons (PAH) and their genotoxicity in exhaust emissions from a diesel engine during extended low-load operation on diesel and biodiesel fuels[J]. Atmospheric Environment , 109 : 9–18. DOI:10.1016/j.atmosenv.2015.02.077 |
| [18] | Wang H, Frenklach M. 1997. A detailed kinetic modeling study of aromatics formation in laminar premixed acetylene and ethylene flames[J]. Combustion and Flame , 110 (1) : 173–221. |
| [19] | 王忠, 安玉光, 许广举, 等.2011. 不同燃料柴油机多环芳烃排放特征的试验研究[J]. 环境科学 , 2011, 32 (7) : 1888–1893. |
| [20] | 魏群, 王天友, 张志进, 等.2015. 醇类汽油混合燃料 EGR 氛围下颗粒物排放特性研究[J]. 环境科学学报 , 2015, 35 (6) : 1690–1696. |
 2016, Vol. 36
2016, Vol. 36


