砷作为一种公认的剧毒元素, 由于各种自然和人为的原因, 目前已广泛地出现在人类生存的环境中, 对人类的健康造成了巨大威胁(Smedley et al., 2002;Kanel et al., 2006;Choong et al., 2007).近年来, 世界各地砷污染事件时有发生, 例如, 孟加拉国和西孟加拉州受砷污染水域超过75%, 最高浓度达到1000 μg·L-1;土耳其西部地表水砷最高浓度达到7754 μg·L-1;中国甘肃徽县作为饮用水的冷泉水最高砷浓度达到482 μg·L-1(Ross, 1998; Ng et al., 2005; Zheng et al., 2010).为了解决慢性砷中毒问题, 我国于2007年7月1日实施了《生活饮用水卫生标准》(GB 5749—2006), 新国标中将砷的标准浓度值由原来的50 μg·L-1降低至10 μg·L-1, 这也给除砷技术带来了新的挑战.
砷按照存在形态可以分为有机砷和无机砷, 在自然水体中主要以无机砷的形式存在, 其中又以As(V)、As(Ⅲ)为主体.虽然As(Ⅲ)的毒性是As(V)的60倍, 且比As(V)更难以去除(Zhang et al., 2011), 但As(Ⅲ)易于氧化变成As(V), 因此, 去除As(V)才是除砷的主要研究方向.
目前除砷的方法可以分为物理化学方法和生物法, 其中, 物理化学法包括混凝沉淀、吸附、离子交换、膜过滤和渗透反应等;生物法包括植物修复和活性污泥/生物滤池技术(Mondal et al., 2006).吸附法由于其经济可行性而成为目前广泛研究和使用的方法.除砷的吸附剂种类繁多, 从人工合成的树脂、矿物(吴萍萍等, 2011)到自然存在的各种矿物都有相关研究与应用, 而吸附剂的效率和成本是制约吸附法应用的重要因素, 也是除砷研究的重点.
磁黄铁矿是地球上最常见的硫铁矿物之一, 广泛存在于各种内生矿床之中, 主要用于提取硫和生产硫酸, 在氧气和水同时存在时容易被氧化产生大量H+, 这也是矿山废水(AMD)的主要来源之一(Bednar et al., 2005).相关研究证明, 硫铁矿能够用来去除水中的砷和其他重金属(Ozverdi et al., 2006;Gallegos et al., 2007), 这说明磁黄铁矿也很可能用来除砷, 同时作为一种广泛分布的天然矿物相比人工合成的吸附剂要简单易得、成本低廉, 因此, 磁黄铁矿很有可能成为一种极具应用前景的除砷材料.因此, 本文利用天然磁黄铁矿作为除砷材料, 研究其对As(V)的吸附特性与相关机理, 以期为利用天然磁黄铁矿去除水中的砷污染提供科学指导和技术基础.
2 材料与方法(Materials and methods) 2.1 实验材料实验所用砷为Na2HAsO4·12H2O(分析纯, 南京化学试剂有限公司), 天然磁黄铁矿来自安徽铜陵.矿物粒度采用8~100目(150~180 μm), 使用前置于10%的盐酸浸泡2 h, 再用蒸馏水反复洗涤至中性, 最后在30 ℃真空干燥箱中烘干.
2.2 实验方法 2.2.1 天然磁黄铁矿对砷的静态吸附实验于42 mL棕色螺纹瓶中加入所需浓度的砷溶液40 mL, pH用1 mol·L-1的HCl和1 mol·L-1的NaOH调整, 加入一定量的天然磁黄铁矿后置于垂直旋转转盘上, 在10 r·min-1、一定温度下反应.实验设3组平行样, 每间隔一段时间取样.
时间对吸附的影响实验:砷初始浓度为30 mg·L-1, 温度为303 K, 加入矿量0.5 g, 每隔2 h取一次样, 考察时间对天然磁黄铁矿吸附砷的影响.
温度对吸附的影响实验:砷初始浓度为30 mg·L-1, 加入矿量0.5 g, 分别在不同温度下(283~323 K, 每5 K一个区段)反应24 h后取样, 考察温度对天然磁黄铁矿吸附砷的影响.
pH对吸附的影响实验:砷初始浓度为30 mg·L-1, 温度为303 K, 加入矿量0.5 g, 调节不同pH(3~11), 每隔24 h取样, 考察pH对天然磁黄铁矿吸附砷的影响.
投加量对吸附的影响实验:砷初始浓度为30 mg·L-1, 温度为303 K, 加入不同矿量(0.2、0.5、1.5、2.0、4.0 g), 每隔24 h取样, 考察投加量对天然磁黄铁矿吸附砷的影响.
阴离子对吸附的影响实验:砷初始浓度为30 mg·L-1, 温度为303 K, 加入矿量0.5 g, 设置PO43-、SiO32-、CO32-、F-、NO3-、SO42-、Cl-浓度分别为砷浓度的1、2、8倍, 每隔24 h取样, 考察阴离子对天然磁黄铁矿吸附砷的影响.
吸附动力学和等温线实验:吸附动力学实验中, 砷初始浓度为30 mg·L-1, 温度为303 K, 加入矿量0.5 g, 每隔2 h取一次样;吸附等温线实验中, 初始砷浓度分别为10、20、30、40、50 mg·L-1, 温度分别为288、303、318 K, 吸附时间为24 h, 加入矿量0.5 g.
2.2.2 动态吸附实验利用玻璃砂芯层析柱进行动态小柱(Φ1 cm×30 cm)吸附研究, 矿物填充高度10 cm, 用去离子水冲洗两次赶去气泡, 然后在室温293 K、As(V)浓度为2 mg·L-1时, 以恒定流速自上而下通过吸附床进行动态吸附实验.每隔2 h取样并测定砷浓度, 设定流出浓度大于10 μg·L-1时达到吸附穿透点.
2.3 分析方法 2.3.1 样品分析方法反应后的水样先经过0.22 μm的滤膜过滤, 其中, 磷酸盐采用钼酸盐分光光度法(GB-11893-89)测定, 硝酸盐利用紫外分光光度法(HJ/T 346-2007)测定, 其他阴离子利用离子色谱分析测定, pH利用实验室pH计测定, 砷利用色谱-原子荧光联用测定.实验所用仪器见表 1.
| 表 1 实验所用仪器表 Table 1 Experimental instrument used in table |
动力学数据分别利用准一级动力学方程(1)和准二级动力学方程(2) 拟合(Demiral et al., 2010).吸附等温线数据分别采用Langmuir方程(3)(Deng et al., 2005)和Freundlich方程(4)(Ho et al., 2002)进行拟合.
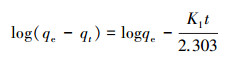
|
(1) |
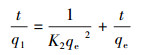
|
(2) |
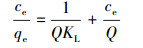
|
(3) |
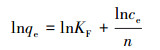
|
(4) |
式中, t为吸附作用时间(h);qt为t时刻矿物对砷的吸附量(mg·g-1);qe为理论平衡吸附容量(mg·g-1);K1、K2分别为准一级和准二级吸附动力学常数;ce为吸附平衡浓度(mg·L-1);Q为理论最大饱和吸附容量(mg·g-1);KF、KL为方程特征参数;n为常数.
3 结果与讨论(Results and discussion) 3.1 磁黄铁矿分析实验所用磁黄铁矿粒径为150~170 μm, 密度为4.63 g·cm-3, 比表面积为8.315 cm2·g-1(BET, N2, 77 K).通过X射线荧光光谱(XRF)分析可得矿物元素组成为:Fe 58.46%、S 38.87%、Si 0.74%、Cu 0.46%、Ca 0.18%、Mg 0.12%、Al 0.11%、Cl 0.05%、W 0.02%、K 0.02%、Zn 0.01%、Mn 0.02%、Cr 0.005%, 剩下的是O及其他微量金属.通过化学计算可得此磁黄铁矿理论分子式Fe0.86S, 其中, 矿物中硫和铁的质量占97.33%.
3.2 各因素对磁黄铁矿除砷的影响 3.2.1 时间对磁黄铁矿除砷的影响图 1为在不同吸附时间下磁黄铁矿吸附As(V)的变化过程.由图可知, 去除过程分为两个阶段:第一阶段(0~20 h)去除速度增长较快, 第二阶段(20 h后)去除速度逐渐平缓, 大约在24 h后基本达到稳定, 最大去除率达到98%, 出水浓度(0.56 mg·L-1)接近污水综合排放标准(GB 8978-1996) 中的总砷值0.5 mg·L-1, 因此, 本实验采用24 h作为实验时间.4 d以后出水砷浓度为0.0055 mg·L-1(图中未显示), 达到国家饮用水标准, 而3周以后砷浓度为0.0061 mg·L-1, 基本保持不变, 说明磁黄铁矿去除砷的效果比较彻底.
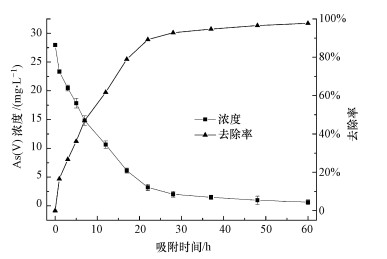 |
| 图 1 吸附时间对磁黄铁矿除As(V)的影响 Fig. 1 Effect of time for removal of As(V) on pyrrhotite |
图 2所示为温度对磁黄铁矿去除As(V)的影响, 可知温度对磁黄铁矿去除As(V)的影响较大, 首先在较广泛的温度范围内都有较高的去除效率;在283 K时就有75%的去除率, 随着温度的升高去除率不断上升, 到323 K时接近100%.这说明较高的温度有利于磁黄铁矿对As(V)的去除.
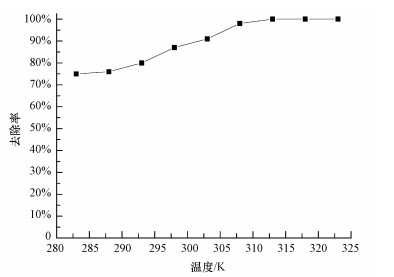 |
| 图 2 温度对磁黄铁矿除As(V)的影响 Fig. 2 Effect of temperature on removal of As(V) by pyrrhotite |
由图 3可知, 随着pH值的不断升高, As(V)的去除率呈现先升高后逐渐下降的过程, 在pH为3~4时去除率都在98%以上, pH小于3时去除率急剧下降, pH大于4时去除率缓慢减低.磁黄铁矿的ξ电位随着pH的增大逐渐减小, 等电点为3.83(由于表面存在部分氧化使得等电点偏小);磁黄铁矿在pH小于3.83时带正电, 有利于对H2AsO4-的吸附去除, 但随着pH的降低磁黄铁矿开始溶解(Li et al., 2013), 以及H2AsO4-逐渐转变成电中性的H3AsO4(Mamindy et al., 2009), 使得磁黄铁矿对As(V)去除率反而越来越小;当pH大于3.83时磁黄铁矿带负电, 由于静电相斥不利于吸附去除进行, 随着pH增大, OH-的竞争吸附效果逐渐变大, 造成As(V)去除率缓慢变小.因此, 磁黄铁矿在静电作用最弱的3.83左右有最高吸附效率.
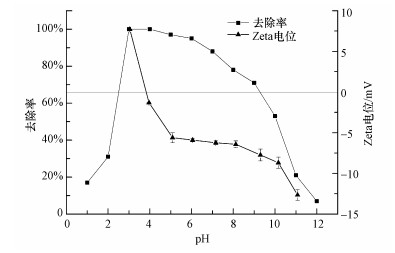 |
| 图 3 pH对磁黄铁矿的ξ电位和除As(V)效果的影响 Fig. 3 Effect of solution pH onξpotential of pyrrhotite and theAs(V)removal |
从图 4可以看出, 随着磁黄铁矿投加量的增加, As(V)的去除效果会有明显的增加, 投加量为0.2 g时去除率为58%, 投加量大于2 g时, 去除率接近100%, 出水可以达到10 μg·L-1的国家饮用水标准.随着磁黄铁矿投加量的增加, 单位磁黄铁矿的吸附量下降, 在4 g时只有0.28 mg·g-1.当As(V)浓度为30 mg·L-1时, 磁黄铁矿投加量从0.2 g增至1.5 g时, 其去除率提高了43%;当投加量继续增加时, As(V)去除效果提升趋势趋于平缓.因此, 在实际应用中磁黄铁矿的投加量应该根据所需出水浓度来进行适当调整, 以节约成本.
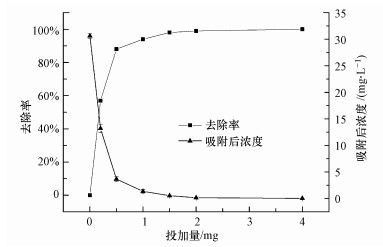 |
| 图 4 吸附剂投加量对磁黄铁矿吸附As(V)的影响 Fig. 4 Effect of mass on the As(V) adsorption by pyrrhotite |
图 5结果显示, 阴离子NO3-、SO42-、Cl-、F-对磁黄铁矿除砷的影响不大;而PO43-、SiO32-、CO32-对吸附有较强的抑制作用, 表明这些无阴离子与As(V)之间可能存在较强的竞争吸附作用, 其对磁黄铁矿除As(V)影响的大小顺序为:PO43-> CO32->SiO32-, 在摩尔比为8时, 磁黄铁矿对As(V)的去除率分别下降了80%、28%和21%, 这是因为这些阴离子都能与铁形成难溶性化合物, 故PO43-、CO32-、SiO32-能对磁黄铁矿除As(V)产生影响, 且铁盐溶度积Ksp的大小顺序为:Fe3(AsO4)2<Fe3(PO4)2<FeCO3<FeSiO3, 说明其与铁离子成键的能力为AsO43-> PO4->CO32->SiO32-, 因此, 它们对磁黄铁矿除砷影响的大小顺序为PO43-> CO32->SiO32-, 这已经在许多研究中得到证实(Zhao et al., 2001;Violante et al., 2002;Meng et al., 2000;Hussain et al., 2011).天然水体中的无机阴离子浓度通常为10~250 mg·L-1, 在这个范围内一些阴离子可能会对吸附产生影响, 故建议把吸附过程放在合适的前处理之后, 以有利于吸附的有效进行.
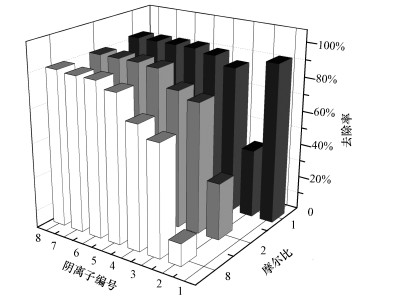 |
| 图 5 阴离子对磁黄铁矿除As(V)的影响(1~8分别代表H2AsO4-、PO43-、SiO32-、CO32-、F-、NO3-、SO42-、Cl-) Fig. 5 Effect of anions on the As(V)adsorption by pyrrhotite |
图 6为磁黄铁矿吸附As(V)及溶液pH的变化过程.由图 6可知, 随着反应时间的增加, 被磁黄铁矿吸附的砷逐渐增加, 大约在24 h后基本达到其平衡吸附量(1.88 mg·g-1);溶液的pH从初始的7.02迅速下降到5.82, 再逐渐回升稳定在6.60左右.由于矿物表面的部分氧化形成的三价铁离子水解和砷酸铁沉淀造成了溶液pH的急剧下降, 具体反应方程如式(5)~(6) 所示.监测到实验溶液中总铁(TFe)的浓度增加, 说明上述反应确实存在.同时, 吸附后溶液变浑浊, EDS分析得到过滤后的悬浮物中含有砷也说明了反应(6)的存在;铁氧化物和羟基氧化铁吸附砷是一种配位体交换吸附的反应, 反应中Fe—O(H)键断裂, 形成Fe—O—As键(Sherman et al., 2003;Dixit et al., 2003;Manning et al., 1998).因此, 有理由推测在磁黄铁矿除砷的过程中有Fe—S键断裂, Fe—O—As键形成, 反应方程见式(7).
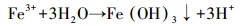
|
(5) |
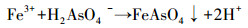
|
(6) |
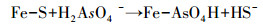
|
(7) |
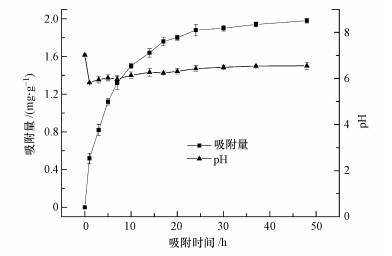 |
| 图 6 磁黄铁矿吸附砷(V)动力学 Fig. 6 Kinetics of arsenic(V)adsorption by pyrrhotite |
同时, Han等(2000)的研究也证明了这一过程的存在, 此过程产生的HS-水解方程如式(8)所示.HS-水解造成了溶液pH的上升, 这也可以解释溶液pH随着砷吸附量的增加而上升, 当吸附平衡时溶液pH同样趋于稳定.
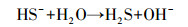
|
(8) |
利用伪一、二级动力学方程对反应进行拟合, 结果见表 2.由表 2可知, 伪二级动力学方程有更好的契合度, 说明在整个吸附过程不是简单地由单一的外部质量扩散因素所控制(Raven et al., 1998), 还存在化学吸附或者内部基质扩散(Anawar et al., 2004), 而较小的矿物颗粒比表面积说明颗粒表面孔隙率很低.因此, 本反应是一个化学吸附过程, 同时反应(6)说明也存在着部分混凝共沉淀的作用.
| 表 2 磁黄铁矿除As(V)动力学参数 Table 2 The parameters of As(V) removal Kinetics on pyrrhotite |
图 7为在288、303、318 K下分别利用Langmuir和Freundlich吸附等温线的拟合结果.可知, 随着砷浓度的增加吸附量也相应增加, 这是因为反应物浓度的增加自然推动吸附反应进行.由拟合结果还可知, Langmuir和Freundlich模型都能模拟吸附的过程, 但Langmuir模型的效果更好, 这说明As(V)在磁黄铁矿表面的吸附过程更符合单层吸附理论.
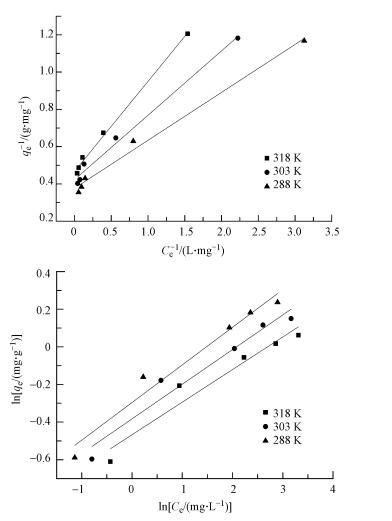 |
| 图 7 Langmuir(a)和Freundlich(b)吸附等温线 Fig. 7 Langmuir(a) and Freundlich(b) adsorption isotherm |
由表 3可知, 随着温度的增加吸附量也随之增加, 这是因为砷吸附的实质不仅仅是As(V)吸附在矿物表面, 而是一个H2AsO4-取代矿物上S2-的配位离子交换过程, 而这样的一个离子交换过程是一个吸热过程(Han et al., 2000).磁黄铁矿吸附As(V)的理论饱和吸附量在15~45 ℃时为2.1~2.8 mg·g-1.KL是与吸附剂、吸附质和温度有关的量, 反映了吸附剂与吸附质之间的吸附亲和力, KL越大表示亲和力越强.由表 3可知, 随温度增加磁黄铁矿对As(V)的亲和力越强.n与吸附强度有关, n大于1表示吸附容易进行, n小于0.5表示吸附很难进行.由表 3可知, n在各个温度下均远大于1, 说明磁黄铁矿对砷的吸附反应很容易进行.
| 表 3 各温度下Langmuir和Freundlich吸附等温常数 Table 3 constant values of Langmuir and Freundlich model for fitting the adsorption data under different temperature |
利用吸附实验前后的磁黄铁矿物进行扫描电镜-电子能谱仪(SEM-EDS)和X射线电子能谱分析(XPS), 以观察矿物表面吸附前后元素的变化来研究磁黄铁矿吸附砷(V)的机理.由图 8可知, 反应前附着在矿物表面上的细小颗粒和氧化物在反应后消失了, 说明反应过程中这些颗粒可能脱离固相转移到溶液之中.而表 4中EDS的数据显示, 矿物中铁相对含量减少, 说明部分铁转移进入水相, 这也证实了上面的说法和反应(5)、(6)的存在;但EDS中没有显示As的存在, 这可能是由于吸附量太小低于检测限所致.因此, 对矿物反应前后的表面元素含量做XPS分析, 结果见表 5.由表 5可知, 矿物表面在反应后出现了As, 说明As确实吸附到了矿物表面.通过之前XRF测得数据可知, 碳氧元素可能是XPS刻蚀时间过长受到空气中CO2和氧气的污染.表 5中显示在吸附后出现砷, 说明As(V)确实吸附在矿物表面上;反应前Fe:S为0.82, 反应后变成0.98, 说明磁黄铁矿表面的部分硫被砷取代, 这也证实了之前配位离子交换吸附的结论.
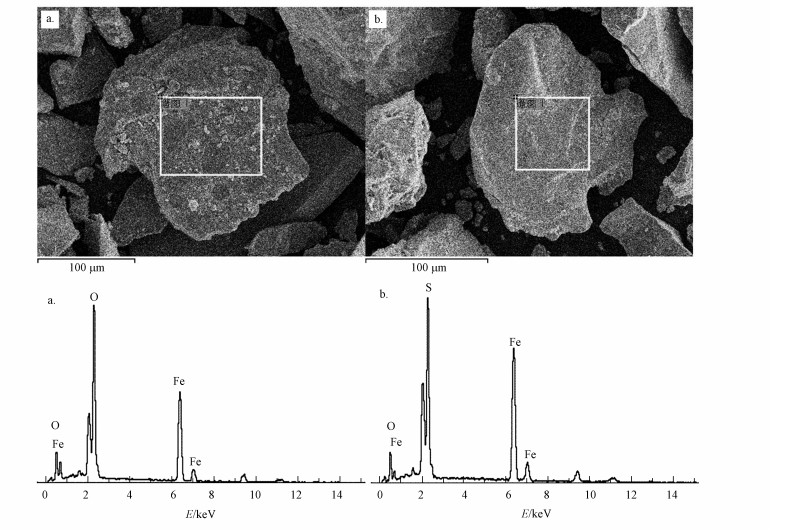 |
| 图 8 吸附前(a)、后(b)磁黄铁矿SEM-EDS图 Fig. 8 SEM-EDS photos of the surface of pyrrhotite before and after adsorption |
| 表 4 吸附前后磁黄铁矿除As(V)的EDS结果 Table 4 EDS results of pyrrhotite before and after removal |
| 表 5 吸附前、后磁黄铁矿除砷(V)的XPS结果 Table 5 XPS results of pyrrhotite before and after As (V) removal |
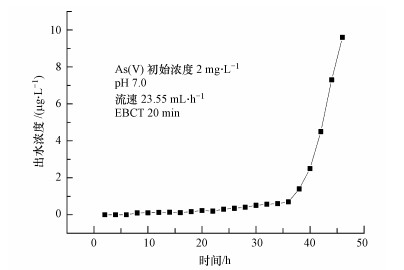 |
| 图 9 As(V)动态吸附穿透曲线 Fig. 9 Breakthrough curves of As(V) through the column bed |
利用磁黄铁矿为吸附剂的固定床动态吸附处理含砷溶液.由图 7可知, 在动态吸附情况下, 前45 h即(150个BV)出水砷浓度小于10 μg·L-1, 达到国家饮用水标准.在前324个BV出水砷浓度小于0.5 mg·L-1, 达到污水综合排放标准.出水达标的单位BV所需成本远低于其他人工合成吸附剂, 这说明价格低廉的磁黄铁矿在处理含砷废水方面具有相当好的应用前景.
4 结论(Conclusions)1) 采用磁黄铁矿对As(V)进行吸附去除具有良好的效果, 在30 ℃、As(V)初始浓度为30 mg·L-1的条件下, 24 h就可以达到90%以上的去除效果.温度对去除过程的影响显著, 在283 K时有75%的去除率, 313 K以上时去除率达到99%.在pH=2~11的范围内磁黄铁矿对As(V)的去除率先增后减, 在pH=3~9之间去除率都在80%以上, 在pH为4左右时吸附效果最好, 此时磁黄铁矿对As(V)的去除率达到99%.投加量对磁黄铁矿除砷的影响显著, 投加量为0.2时As(V)去除率为58%, 投加量大于2 g时, As(V)去除率接近100%, 实际应用时应根据出水浓度调节投料比.NO3-、SO42-、Cl-、F-对磁黄铁矿除砷的影响不大, 而PO43-、SiO32-、CO32-对砷吸附有较强的抑制作用, 表明这些无机阴离子与As(V)之间可能存在较强的竞争吸附作用, 工业应用时应注意预先脱盐处置.在2 mg·L-1砷初始浓度下的动态吸附结果显示, 在前150个BV的As(V)出水浓度能达到国家饮用水标准.
2) Langmuir和Freundlich吸附等温线方程都可以模拟磁黄铁矿吸附As(V)的过程, 而Langmuir方程的拟合效果更好, 说明磁黄铁矿吸附As(V)的过程可以用单层吸附模型进行描述.伪一级动力学和伪二级动力学方程都能对磁黄铁矿吸附As(V)的动力学过程进行模拟, 但伪二级动力学方程的模拟效果更佳, 说明吸附是一个吸热的化学吸附过程.
3) 磁黄铁矿除砷是一个吸热的配位离子交换过程, 同时伴随一些化学沉淀反应, 其吸附砷之后的较长时间内没有检测到砷的释放, 表明磁黄铁矿吸附是一种有效的除砷手段, 磁黄铁矿作为除砷吸附剂极具应用前景.
| [${referVo.labelOrder}] | Anawar H, Akai M, Sakugawa J. 2004. Mobilization of arsenic from subsurface sediments by effect of bicarbonate ions in groundwater[J]. Chemosphere , 54 (6) : 753–762. DOI:10.1016/j.chemosphere.2003.08.030 |
| [${referVo.labelOrder}] | Bednar A J, GarbarinoJ R, Ranville J F, et al. 2005. Effects of iron on arsenic speciation and redox chemistry in acid mine water[J]. Journal of Geochemical Exploration , 85 (2) : 55–62. DOI:10.1016/j.gexplo.2004.10.001 |
| [${referVo.labelOrder}] | Choong T S Y, Chuah T G, Robiah Y, et al. 2007. Arsenic toxicity, health hazards and removal techniques from water: an overview[J]. Desalination , 217 (1/3) : 139–166. |
| [${referVo.labelOrder}] | Demiral H, Gunduzoglu G. 2010. Removal of nitrate from aqueous solutions by activated carbon prepared from sugar beet bagasse[J]. Bioresour Technol , 101 (6) : 1675–1680. DOI:10.1016/j.biortech.2009.09.087 |
| [${referVo.labelOrder}] | Deng S B, Ting Y P. 2005. Fungal biomass with grafted poly(acrylic acid) for enhancement of Cu(II) and Cd(II) biosorption[J]. Langmuir , 21 (13) : 5940–5948. DOI:10.1021/la047349a |
| [${referVo.labelOrder}] | Dixit S, Hering J G. 2003. Comparison of arsenic(V) and arsenic(III) sorption onto iron oxide minerals: Implications for arsenic mobility[J]. Environmental Science & Technology , 37 (18) : 4182–4189. |
| [${referVo.labelOrder}] | Gallegos T J, Hyun S P, Hayes K F. 2007. Spectroscopic investigation of the uptake of arsenite from solution by synthetic mackinawite[J]. Environmental Science & Technology , 41 (22) : 7781–7786. |
| [${referVo.labelOrder}] | Han J T, Fyfe W S. 2000. Arsenic removal from water by iron-sulphide minerals[J]. Chinese Science Bulletin , 45 (15) : 1430–1434. DOI:10.1007/BF02886253 |
| [${referVo.labelOrder}] | Ho Y S, Huang C T, Huang H W. 2002. Equilibrium sorption isotherm for metal ions on tree fern[J]. Process Biochemistry , 37 (12) : 1421–1430. DOI:10.1016/S0032-9592(02)00036-5 |
| [${referVo.labelOrder}] | Hussain S, Aziz H A, Isa M H, et al. 2011. Orthophosphate removal from domestic wastewater using limestone and granular activated carbon[J]. Desalination , 271 (1/3) : 265–272. |
| [${referVo.labelOrder}] | Kanel S R, Grenèche J, Choi H. 2006. Arsenic(V) removal from groundwater using nano scale zero-valent iron as a colloidal reactive barrier material[J]. Environmental Science & Technology , 40 (6) : 2045–2050. |
| [${referVo.labelOrder}] | Li R, KellyC, Keegan R, et al. 2013. Phosphorus removal from wastewater using natural pyrrhotite[J]. Colloids and Surfaces A: Physicochemical and Engineering Aspects , 427 : 13–18. |
| [${referVo.labelOrder}] | Mamindy-Pajany Y, Hurel C, Marmier N, et al. 2009. Arsenic adsorption onto hematite and goethite[J]. Comptes Rendus Chimie , 12 (8) : 876–881. DOI:10.1016/j.crci.2008.10.012 |
| [${referVo.labelOrder}] | Meng X G, Bang S, Korfiatis G P. 2000. Effects of silicate, sulfate, and carbonate on arsenic removal by ferric chloride[J]. Water Research , 34 (4) : 1255–1261. DOI:10.1016/S0043-1354(99)00272-9 |
| [${referVo.labelOrder}] | Manning B A, Fendorf S E, Goldberg S. 1998. Surface structures and stability of arsenic(III) on goethite: Spectroscopic evidence for inner-sphere complexes[J]. Environmental Science & Technology , 32 (16) : 2383–2388. |
| [${referVo.labelOrder}] | Mondal P, Majumder C B, Mohanty B. 2006. Laboratory based approaches for arsenic remediation from contaminated water: recent developments[J]. J Hazard Mater , 137 (1) : 464–479. DOI:10.1016/j.jhazmat.2006.02.023 |
| [${referVo.labelOrder}] | Ng J C, Wang J B, Zhai C, et al. 2005. Urinary porphyrins as biomarkers for arsenic exposure among susceptible populations in Guizhou province, China[J]. Toxicol Appl Pharmacol , 206 (2) : 176–184. DOI:10.1016/j.taap.2004.09.021 |
| [${referVo.labelOrder}] | Ozverdi A, Erdem M. 2006. Cu2+, Cd2+ and Pb2+ adsorption from aqueous solutions by pyrite and synthetic iron sulphide[J]. J Hazard Mater , 137 (1) : 626–632. DOI:10.1016/j.jhazmat.2006.02.051 |
| [${referVo.labelOrder}] | Ross Nickson J M. 1998. Arsenic poisoning of Bangadesh groundwater[J]. Nature , 395 (6700) : 338. DOI:10.1038/26387 |
| [${referVo.labelOrder}] | Raven K P, Jain A R H. 1998. Loeppert, Arsenite and arsenate adsorption on ferrihydrite: Kinetics, equilibrium, and adsorption envelopes[J]. Environmental Science & Technology , 32 (3) : 344–349. |
| [${referVo.labelOrder}] | Smedley P L, Kinniburgh D G. 2002. A review of the source, behaviour and distribution of arsenic in natural waters[J]. Applied Geochemistry , 17 (5) : 517–568. DOI:10.1016/S0883-2927(02)00018-5 |
| [${referVo.labelOrder}] | Sherman D M, Randall S R. 2003. Surface complexation of arsenic(V) to iron(III) (hydr)oxides: structural mechanism from ab initio molecular geometries and EXAFS spectroscopy[J]. Geochimica et Cosmochimica Acta , 67 (22) : 4223–4230. DOI:10.1016/S0016-7037(03)00237-0 |
| [${referVo.labelOrder}] | Violante A, Pigna M. 2002. Competitive sorption of arsenate and phosphate on different clay minerals and soils[J]. Soil Science Society of America Journal , 66 (6) : 1788–1796. DOI:10.2136/sssaj2002.1788 |
| [${referVo.labelOrder}] | 吴萍萍, 曾希柏.2011. 人工合成铁、铝矿对As(V)吸附的研究[J]. 中国环境科学 , 2011, 3 (4) : 603–610. |
| [${referVo.labelOrder}] | Zheng Y. 2010. Mobilization of natural arsenic in groundwater_ targeting low arsenic aquifers in high arsenic occurrence areas[J]. Geology in China , 37 (3) : 323–329. |
| [${referVo.labelOrder}] | Zhang Q, Zheng Q, Sun G. 2011. Arsenic-contaminated cold-spring water in mountainous areas of Hui County, Northwest China: a new source of arsenic exposure[J]. Sci Total Environ , 409 (24) : 5513–5516. DOI:10.1016/j.scitotenv.2011.08.055 |
| [${referVo.labelOrder}] | Zhao H S, Stanforth R. 2001. Competitive adsorption of phosphate and arsenate on goethite[J]. Environmental Science & Technology , 35 (24) : 4753–4757. |
 2016, Vol. 36
2016, Vol. 36


