随着不可再生能源的日益枯竭,节能减排、保护环境的呼声日益高涨,各国纷纷采取有效措施鼓励生物质能产业的发展(Lin and Tanaka, 2006).生物乙醇的生产与使用能够降低全球变暖和缓解能源危机,受到全球的关注(Asgher et al., 2014). 第一代生物乙醇的主要原料是淀粉类作物和糖类作物,如:玉米和甘蔗等,大面积种植这些作物,会出现“与人争粮,与粮争地”的现象(张文彬等,2014).纤维素乙醇是第二代生物乙醇,主要原料为木质纤维素类生物质,这类木质纤维素储量大,价格低,不仅不会影响农业生产资源,还可以降低生产成本.而当前这些农业废弃物绝大部分被烧掉或废弃,其利用率极低,不仅造成大量资源的浪费,而且对环境造成很大的污染,若能将其转化为生物燃料,使这些废弃物得到综合利用,也将大量取代交通燃料对石油、煤炭的依赖,改善自然环境.但是,由于木质纤维素材料具有复杂的结构,使其影响酶解效果,降低还原糖转化率(Nasirpour et al., 2014).
预处理是生物乙醇生产过程中最关键的环节,因为它能破坏木质纤维素材料复杂的高分子结构.预处理方法有物理方法(如蒸汽爆破、辐射、冷冻等)和化学方法(如酸、碱、有机溶剂等)(Sun and Cheng, 2002)都能提高木质纤维材料的酶解效果,但是它们分别存在着耗能高、效率低且过程污染较严重等问题,难以工业化推广.因此,需要寻求一种成本低、效果好、对下一步影响小的方法.离子液体是具有潜力的预处理木质纤维材料的溶剂,因为它具有优良溶解性、强极性 、不挥发 、不氧化 、对水和空气稳定等特点,不仅有效克服了传统溶剂的缺陷,而且大大拓展了纤维素工业的应用前景,将纤维素工业应用提升到一个新平台.
先前的研究主要使用离子液体预处理木质纤维材料(Qiu and Aita, 2013;Shafiei et al., 2013),但是将表面活性剂联合离子液体作为预处理方法鲜有报道(Qing et al., 2013).表面活性剂具有亲水性和疏水性结构,通过提高疏水基团的转移来降低两液相间表面张力.由于这种特性,表面活性剂广泛应用于造纸工业,阴离子与阳离子表面活性剂混合提高纸浆产量,主要原因是提高浆液的可湿性(Zhao et al., 2004),也使表面活性剂在木质纤维素预处理方面具有很好的前景.本研究的主要目的为研究[AMIM]Cl联合不同表面活性剂预处理木质纤维提高酶解的效果,并通过成分分析、FTIR、XRD等分析,了解预处理前后木质纤维材料的物理化学变化.
2 试验材料与方法(Materials and methods) 2.1 材料本实验的木质纤维素原料为稻草秸秆.稻草秸秆样品是生长期为5个月的日本稻米,这些样品采收于台湾省台北市中央研究院的实验农场(北纬25°020′32.79″,西经121°360′47.40″,海拔高度为18 m).稻草秸秆收集之后进行风干处理,研磨成粉即为本次实验的样品.将稻草秸秆储存在密封的塑料袋中,于干燥处室温保存.用网筛对稻草秸秆进行筛分,得到实验稻草秸秆粉末的粒径范围及其含量分别为:粒径大于300 mm的占3.39%;粒径为300~150 mm的占47.95%;粒径为150~106 mm的占15.52%;粒径为106~75 mm的占20.57%;粒径小于75 mm的占2.63%.
2.2 实验药品与仪器氯化-1-烯丙基-3-甲基咪唑([AMIM]Cl)(上海默尼化工有限公司)99%;十二烷基硫酸钠(SDS)(上海泰坦科技股份有限公司)65%;十六烷基三甲基溴化铵(CTAB)(sigma-Aldrich)98%;吐温80(Tween80) (阿拉丁)98%;曲拉通100(TritonX-100) (阿拉丁)98%;鼠李糖脂(阿拉丁)98%; 3,5-二硝基水杨酸(成都市科龙化工试剂厂)98%;酶(NS22086、NS22118) (Novozymes公司).
MS-100型恒温混匀仪(杭州奥盛仪器有有限公司);UV756CRT型紫外可见分光光度计(上海佑科仪器仪表有限公司);Nicolet6700傅立叶红外光谱仪(美国赛默飞世尔科技公司);UItima X-射线衍射仪(日本理学).
2.3 [AMIMC]Cl联合表面活性剂预处理木质纤维材料称取0.5 g 稻秆加入到带螺旋塞的瓶子中,加入5 g 离子液体及1%的表面活性剂,离子液体预处理稻秆前,将离子液体在120 ℃下加热30 min,并不断搅拌,目的是去除离子液体中的水分(Muhammad et al., 2013).置于磁力搅拌器上,在 110 ℃条件下搅拌 1 h 后,加入45 mL去离子水,将混合液置于50 mL的离心管中,以 7000 r · min-1 高速离心15 min后分离.移出上层清液,储存.
取下层沉淀物,用去离子水反复清洗,去除离子液体,在60 ℃真空干燥至少18 h,取出称重,留至下一步的酶解.
2.4 木质纤维材料的物化特性1) 预处理前后木质纤维材料的成分分析
秸秆中纤维素、半纤维素及木质素的测定方法(石淑兰和何福望,2006).
硝酸乙醇法和亚氯酸钠法测定纤维素和综纤维素(注: 半纤维素=综纤维素-纤维素),72%浓硫酸法测定木质素.
2) 预处理前后木质纤维素材料的FTIR分析
取1 mg预处理前后的稻秆样品研磨,然后与300 ~ 400 mg干燥的KBr粉末充分混合,然后再次研磨至符合压片要求为止,将其压成透明薄片,以KBr空白片作为参比扫描红外光谱.扫描范围4000~400 cm-1.
3) 预处理前后木质纤维素材料的XRD分析
采用Cu 靶产生X射线,管压40 kV,管流20 mA,扫描步长0.02(°)· s-1.样品的结晶度指数利用下面的方程(Nasirpour et al., 2014)进行计算:
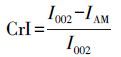
|
(1) |
式中,CrI表示结晶度指数,I002是晶体衍射最大强度,IAM是在2θ时16.6°的衍射强度.
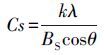
|
(2) |
式中,Cs 表示晶粒大小,k表示谢乐常数,λ表示X-射线波长(Å),θ是衍射角度,BS是最大半宽高.
2.5 预处理前后的木质纤维素样品糖化准确称取0.1 g预处理前后稻秆试样分别置于25 mL锥形瓶中,加入4 mL 0.1 mol · L-1 pH4.8 的柠檬酸缓冲溶液和100 μL 0.02%叠氮化钠溶液,摇匀,再添加 50 FPU · g-1稻秆(实际酶活250 FPU · g-1纤维素酶)及40 CBU · g-1稻秆(实际酶活 320 CBU · g-1 葡萄糖苷酶),置于(50±0.5) ℃恒温水浴振荡器中,转速为150 r · min-1下糖化0、3、6、12、24、48、72 h.反应完毕,在7000 r · min-1离心,得酶水解液,取样用DNS测定法分析还原糖量,计算纤维转化率(Worasuwannarak et al., 2007).

|
(3) |
式中,c表示72 h反应生成还原糖浓度(mg · mL-1),V表示反应液总体积(mL),η表示纤维素、半纤维素的占比(%),m表示使用原始稻秆量(mg).
3 结果与分析(Results and analysis) 3.1 不同种类表面活性剂联合离子液体对稻秆酶解的影响图 1是未处理、单独离子液体([AMIM]Cl、阴离子型表面活性剂-离子液体([AMIM]Cl+1%SDS)、阳离子型表面活性剂-离子液体([AMIM]Cl+1%CTAB)、非离子型表面活性剂-离子液体([AMIM]Cl+1%Tween80、[AMIM]Cl+1%Triton-X100) 、生物表面活性剂-离子液体([AMIM]Cl+1%鼠李糖脂)对稻秆酶解的影响.由图 1可知,所有的样品从0 h到24 h纤维转化率明显升高,延长酶解时间至72 h 纤维转化率基本保持不变,其主要原因可能是随着酶解时间的增加,体系中基质或酶已经消耗尽;预处理后的稻秆纤维转化率明显高于未处理稻秆的纤维转化率.在酶解72 h时,未处理的稻秆、[AMIM]Cl、[AMIM]Cl+1%CTAB、[AMIM]Cl+1%SDS、[AMIM]Cl+1%Tween80、[AMIM]Cl+1%Triton-X100、[AMIM]Cl+1%鼠李糖脂处理的稻秆纤维转化率分别为:16.16%、28.24%、33.80%、31.56%、34.76%、33.22%、36.22%.其中,生物表面活性剂-离子液体处理稻秆的纤维转化率最高,与未处理及单独离子液体处理稻秆分别高55.38%和22.03%;非离子型表面活性剂-离子液体处理稻秆的纤维转化率次之,阳离子型表表面剂-离子液体处理稻秆的纤维转化率最低.表 1为不同种类表面活性剂联合离子液体处理稻秆的酶解初速度.结果表明,生物表面活性剂-离子液体处理稻秆的酶解初速度最高,比未处理的酶解初速度高1.6倍.由此可见,生物表面活性剂-离子液体处理稻秆更有利于稻秆与酶的结合,提高酶解效果.
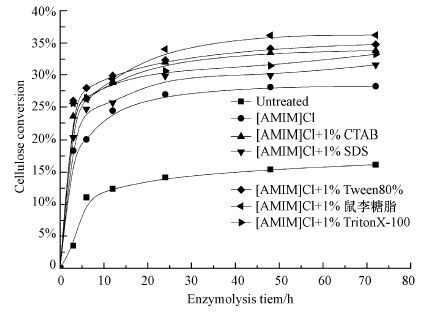 |
| 图 1 不同种类表面活性剂联合离子液体对稻秆酶解效果的影响 Fig. 1 Effect of different surfactant-assisted ionic liquid on enzymatic hydrolysis of rice straw |
| 表 1 不同预处理方法的稻秆酶解初速度 Table 1 Enzymatic hydrolysis velocity of rice straw at different pretreatment |
从表 2可知,未处理、离子液体、表面活性剂-离子液体预处理稻秆的化学成分分析.其中未处理稻秆的纤维素含量35.36%、半纤维素含量24.15%和木质素含量25.98%,与Zhu等(2015) 研究的结果(纤维素含量38.4%、半纤维素含量21.8%、和木质素含量16.2%)有差异.可能是由于稻秆原料和含量检测方法的差异造成的.经过[AMIM]Cl、[AMIM]Cl+1%SDS、[AMIM]Cl+1%CTAB、[AMIM]Cl+1%Tween80、[AMIM]Cl+ 1%TritonX-100、[AMIM]Cl+1%鼠李糖脂处理后稻秆生物质分别损失:15.92%、16.09%、15.59%、20.00%、16.99%、18.94%;这些生物质损失的主要原因可能是表面活性剂联合离子液体预处理稻秆后,部分半纤维素和木质素遭到破坏,在水洗过程中,部分物质溶于滤液中或随水流被冲掉而造成的损失(Nasirpour et al., 2014).与未处理的稻秆相比,预处理后的稻秆木质素比例皆有明显下降,而添加不同种类表面活性剂后大都能更进一步降低木质素含量(除CTAB持平),说明表面活性剂与离子液体的协同作用,能降低表面张力与提高木质素去除率,增加纤维素与酶的结合效率.
| 表 2 预处理前后的稻秆的化学成分分析 Table 2 Chemical composition of untreated and pretreated rice straw |
利用红外光谱(FTIR)分析预处理前后稻秆的结构特征,由此推测出表面活性剂联合离子液体预处理稻秆提高酶解效果的机理.由(da Costa Lopes et al., 2013)知,3400 cm-1 、1430 cm-1、1160 cm-1 处的吸收峰为纤维素分子的—OH键的伸缩振动,2900 cm-1和1060 cm-1处为纤维素的—CH键伸缩振动和C—O变形振动峰;在1375 cm-1附近属于C—H的弯曲振动.由图 2可知,预处理后的稻秆纤维素各特征峰出现的位置与未处理稻秆红外光谱图保持一致,但预处理后纤维素各基团的吸收峰明显增强,表明预处理后纤维素的结晶度下降,基团结构一致,纤维素并没有发生衍生化,也没有新的官能团产生.根据红外光谱图,可以计算出两条红外透过率的比率(Nasirpour et al., 2014):① α1437cm-1/α899 cm-1,表示结晶指数或者侧枝结构指数(LOI),② α1378 cm-1/α2900 cm-1,表示总结晶指数(TCI).较高的指数说明材料有较高的结晶度和结构指数.由表 3可知,与未处理及单独离子液体处理后稻秆的LOI和TCI相比,经过表面活性剂联合离子液体处理稻秆后的LOI和TCI均明显下降.这表明溶解后的稻秆重新析出时,材料的结晶结构遭到破坏,变得比较松散.其原因推测为析出过程中,由于水使得被溶解稻秆快速沉淀析出,而阻止它形成原来的结晶结构.因此结构不完整的稻秆更易被酶解.而X-射线衍射分析可知,未处理稻秆的晶粒大小为48 Å,通过离子液体、表面活性剂-离子液体处理的稻秆结晶指数和晶粒大小都有所下降,与红外光谱图计算得出的结论一致.根据纤维素预处理前后结晶指数和晶粒尺寸的变化,可以推测出在预处理过程中,原料中半纤维素和木质素可能部分被去除,以及纤维素结晶区域发生变化,从而导致纤维素结晶指数和晶粒尺寸下降.由于预处理后纤维素结晶度下降,增大了纤维素与酶的接触表面积,有利于酶解反应.
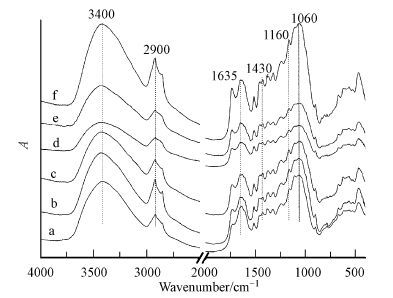 |
| 图 2 不同预处理方式得到的稻秆的 FTIR 图(a.Untreated,b.[AMIM]Cl,c.[AMIM]Cl+1%SDS,d.[AMIM]Cl+1%CTAB,e.[AMIM]Cl+1%Tween80,f.[AMIM]Cl+1% TritonX-100,g.[AMIM]Cl+1%鼠李糖脂) Fig. 2 FTIR of rice straw after diffident pretreatment technology |
| 表 3 预处理前后稻秆XRD结晶指数和红外比率 Table 3 The crystallinity index of XRD and the infrared ratios of Fourier transform spectroscopy for various untreated and pretreated and pretreated rice straw |
在纤维乙醇研究领域中,由于稻秆结构复杂,降低了纤维素酶与纤维素的有效接触,不利于酶解的进行,为改变天然的纤维素结构,降低结晶度,脱去木质素和半纤维素,从而使纤维素更容易被酶解.目前预处理的方法有理化处理和生物降解,理化处理有蒸汽爆破、酸、碱等,虽然效果好,可去除50%的木质素,但成本高,易造成二次污染,生物降解周期长,酶制剂成本高(李红艳等,2009).因此,对预处理技术的研究是实现木质纤维原料的高效化利用的重要途径.
有研究报道显示,离子液体([MEIM][DMP])处理后纤维素产糖率均明显高于未处理的纤维素,而离子液体联合表面活性剂处理比单独离子液体处理产糖率高,其中未处理的纤维素及[MEIM][DMP]、[MEIM][DMP]/PEG4000、[MEIM][DMP]/TritonX-100、[MEIM][DMP]/AOP、[MEIM][DMP]/SDS处理的纤维素产糖浓度分别2.20、3.68、3.92、3.72、3.56、3.06 mg · mL-1(冯圆圆等,2014).利用非离子型表面活性剂Tween80辅助NaOH 溶液预处理稻秆,结果表明预处理过程中添加Tween80明显提高预处理效果,进一步降低木质素的含量,提高有机质得率,有助于强化糖化效率(黄涛等,2011).从图 1实验结果与上述研究结果比较可见,虽然联合作用的木质纤维材料不同,但是都说明表面活性剂在一定程度上促进稻秆与酶解结合,提高纤维转化率,而且试验结果与前人研究的规律一致.
通过探讨预处理前后稻秆的化学成分、结晶度等理化特性,能够更清楚的了解离子液体联合表面活性剂对稻秆酶解的影响.Qing等(2010) 认为表面活性剂能够提高木质素的去除率是因为木质素与表面活性剂之间的憎水作用.Nasirpour等(2014) 发表一种新型的表面活性剂耦合离子液体预处理甘蔗渣提高酶解研究,结果表明,与单纯离子液体处理甘蔗渣相比,添加表面活性剂木质素去除率增加12.5%,同时也提高酶解效率.本研究中预处理前后稻秆的化学成分分析(图 4)也发现添加表面活性剂木质素有明显下降.因此,在某种程度上印证以上研究结果.利用红外光谱(FTIR)分析预处理前后稻秆的结构特征(图 2),可以清楚的看出纤维素、半纤维素及木质纤维素的特征吸收峰,并且预处理后的稻秆纤维素各特征峰出现的位置与未处理稻秆红外光谱图保持一致,纤维素并没有发生衍生化,也没有新的官能团产生.根据红外光谱图和X-射线衍射分析(表 3)分别计算出LOI、TCI、CrI和Crystallite size,则充分证明预处理后的稻秆结晶度下降.这一试验结果与Nasirpour等(2014) 的研究结果一致.
5 结论(Conclusions)1) 与单独离子液体处理相比,表面活性剂联合离子液体处理稻秆纤维转化率为:生物表面活性剂-离子液体 > 非离子型表面活性剂-离子液体 > 阴离子型表面活性剂-离子液体 > 阳离子型表面活性剂-离子液体.
2) 生物表面活性剂-离子液体处理稻秆的纤维转化率最高,与未处理及单独离子液体处理稻秆分别高55.38%和22.03%.通过稻秆酶解初速度分析,生物表面活性剂-离子液体处理稻秆酶解初速度最大.由此可见,生物表面活性剂-离子液体处理稻秆更有利于稻秆与酶的结合,提高酶解效果.
3) 通过稻秆成分分析表明稻秆在110 ℃条件下,处理 60 min,半纤维素和木质素有明显下降,纤维素损失不大;红外分光光谱图(FTIR)表明处理后的稻秆基团结构没发生衍生化;X-射线衍射(XRD)分析表明经处理后稻秆结晶指数下降,晶体尺寸也变小,说明预处理后能有效降低结晶度,提高纤维素与酶的结合效果.
| [1] | Asgher M, Bashir F, Iqbal H M N. 2014. A comprehensive ligninolytic pre-treatment approach from lignocellulose green biotechnology to produce bio-ethanol[J]. Chemical Engineering Research and Design , 92 (8) : 1571–1578. DOI:10.1016/j.cherd.2013.09.003 |
| [2] | da Costa Lopes A M, João H G, Rubik D F, et al. 2013. Pre-treatment of lignocellulosic biomass using ionic liquids: wheat straw fractionation[J]. Bioresource Technology , 142 : 198–208. DOI:10.1016/j.biortech.2013.05.032 |
| [3] | 黄涛, 程康华, 王传槐.2011. 吐温-80及碱预处理对饲用稻草木质纤维素含量和纤维素酶解产糖的影响[J]. 纤维素科学与技术 , 2011, 19 (2) : 52–58. |
| [4] | 李红艳, 张增强, 李荣华, 等.2009. 微波辅助酸预处理玉米秸秆水解条件研究[J]. 环境科学学报 , 2009, 29 (12) : 2557–2566. |
| [5] | Lin Y, Tanaka S. 2006. Ethanol fermentation from biomass resources: current state and prospects[J]. Applied Microbiology and Biotechnology , 69 (6) : 627–642. DOI:10.1007/s00253-005-0229-x |
| [6] | Muhammad N, Man Z, Bustam M A, et al. 2013. Investigations of novel nitrile based ionic liquids as pre-treatment solvent for extraction of lignin from bamboo biomass[J]. Journal of Industrial and Engineering Chemistry , 19 (1) : 207–214. DOI:10.1016/j.jiec.2012.08.003 |
| [7] | Nasirpour N, Mousavi S M, Shojaosadati S A, et al. 2014. A novel surfactant-assisted ionic liquid pretreatment of sugarcane bagasse for enhanced enzymatic hydrolysis[J]. Bioresource Technology , 169 : 33–37. DOI:10.1016/j.biortech.2014.06.023 |
| [8] | Qing Q, Yang B, Wyman C E. 2010. Impact of surfactants on pretreatment of corn stover[J]. Bioresource Technology , 101 (15) : 5941–5951. DOI:10.1016/j.biortech.2010.03.003 |
| [9] | Qiu Z H, Aita G M. 2013. Pretreatment of energy cane bagasse with recycled ionic liquid for enzymatic hydrolysis[J]. Bioresource Technology , 129 : 532–537. DOI:10.1016/j.biortech.2012.11.062 |
| [10] | Shafiei M, Zilouei H, Zamani A, et al. 2013. Enhancement of ethanol production from spruce wood chips by ionic liquid pretreatment[J]. Applied Energy , 102 : 163–169. DOI:10.1016/j.apenergy.2012.05.060 |
| [11] | Sun Y, Cheng J Y. 2002. Hydrolysis of lignocellulosic materials for ethanol production: a review[J]. Bioresource Technology , 83 (1) : 1–11. DOI:10.1016/S0960-8524(01)00212-7 |
| [12] | 石淑兰, 何福望. 2006. 纸浆造纸分析与检测[M]. 北京: 中国轻工业出版社: 1 -380. |
| [13] | Worasuwannarak N, Sonobe T, Tanthapanichakoon W. 2007. Pyrolysis behaviors of rice straw, rice husk, and corncob by TG-MS technique[J]. Journal of Analytical and Applied Pyrolysis , 78 (2) : 265–271. DOI:10.1016/j.jaap.2006.08.002 |
| [14] | 张文彬, 蔡葆, 徐艳丽. 2010. 我国生物燃料乙醇产业的发展[J]. 中国糖料, (3): 58-62; 67 |
| [15] | Zhao Y L, Deng Y L, Zhu J Y. 2004. Roles of surfactants in flotation deinking[J]. Progress in Paper Recycling , 14 (1) : 41–45. |
| [16] | Zhu S D, Huang W J, Huang W X, et al. 2015. Pretreatment of rice straw for ethanol production by a two-step process using dilute sulfuric acid and sulfomethylation reagent[J]. Applied Energy , 154 : 190–196. DOI:10.1016/j.apenergy.2015.05.008 |
 2016, Vol. 36
2016, Vol. 36


