挥发性有机物(VOCs)是形成雾霾、导致光化学烟雾、破坏臭氧层的主要原因之一.甲苯具有强刺激性和毒性,对人体皮肤、粘膜、神经系统及内脏具有一定的危害性,且甲苯性质稳定,苯环不易被破坏,在环境中难以去除.因此,如何有效地降解和去除环境中的甲苯已成为国内外研究的热点及难点问题.
以TiO2为催化剂的光催化氧化技术是一种环保、高效的污染治理技术,具有氧化能力强、降解速率快、反应效率高、无二次污染等优点.但由于TiO2的禁带宽(Eg=3.2 eV),只能吸收短波长的紫外光(λ<387 nm),光生电子和空穴对容易复合,光能利用率低(Linsebigler et al.,1995),使其应用受到很大的限制.通过对TiO2沉积贵金属或其他金属氧化物、硫化物,掺杂非金属元素、无机离子、光敏化剂及表面还原处理等方法,能降低TiO2禁带能隙,拓宽TiO2的吸收光范围,提高稳态光降解量子效率及光催化性能(盛国栋等,2009).其中,非金属N掺杂TiO2自2001年被报道(Asahi et al.,2001)以来便广受关注,例如,Irokawa等(2006)采用氮掺杂二氧化钛进行可见光催化降解甲苯气体研究;Aoki等(2006)采用氮掺杂二氧化钛光催化降解甲醛和甲苯气体;Chen等(2007)采用常压等离子体法制备氮掺杂二氧化钛催化剂,在紫外光和可见光条件下光催化降解异丙醇;Morikawa等(2006)采用湿浸渍法制备Cu加载的N-TiO2混合催化剂,在可见光条件下催化降解乙醛气体;Ozaki等(2007)采用N和Si共掺杂TiO2催化剂光催化降解乙醛气体;WaN-Kuen等(2012)以LED灯为光源,利用N-TiO2光催化降解甲苯、乙苯、间二甲苯、对二甲苯和邻二甲苯,其降解率分别达到35%、68%、94%和93%;Sun等(2011)采用溶胶-凝胶法制备Pt/N-TiO2催化剂,自然光催化降解乙醇、丙酮、2-丙醇、正-己烷、甲苯和三氯乙烯.已有研究表明,以膨润土、丝沸石、活性炭、陶瓷等(金苏君等,2008;杨瑞等,2005;黄雯等,2007;王建宏等,2008)具有高比表面积的多孔材料为TiO2的载体,能增大光催化反应的面积,从而提高光催化反应的效率.研究发现,疏水性中空纤维膜比表面积大,利于纳米N-TiO2的表面分散,且相对化学惰性,不溶于有机物,分离透过通量大,能提高甲苯传质效果,高效分离甲苯/空气二元混合气体(Liu et al.,2011).已有学者开展了将聚偏氟乙烯(PVDF)中空纤维膜作为TiO2载体的PVDF/TiO2光催化降解水中壬基苯酚的研究(Dzinun et al.,2015),但还未见到以聚丙烯(PP)中空纤维膜为载体负载N-TiO2催化降解甲苯气体的研究报道.
因此,本研究采用溶胶-凝胶法制备N-TiO2复合溶胶,采用聚丙烯(PP)中空纤维微滤膜作为支撑底膜,N-TiO2复合溶胶作为催化层,制备N-TiO2/PP复合催化膜,分别以自然光、可见光、紫外光为光催化反应的光源,研究气体停留时间、光照时间、光照强度、进气浓度等因素对甲苯去除效率的影响.同时,采用紫外-可见光谱(UV-Vis)表征分析TiO2及N-TiO2催化剂,用X-射线光电子能谱(XPS)、傅立叶变换红外光谱(FT-IR)分析手段表征分析光催化反应前后膜催化剂,用GC-MS分析甲苯降解过程的中间产物并推测反应过程机理,以期为N-TiO2/PP复合膜光催化降解甲苯工业化应用奠定基础.
2 材料与方法(Materials and methods) 2.1 N-TiO2/PP复合膜的制备采用溶胶-凝胶法制备N-TiO2,具体操作为:以钛酸丁酯(Ti(OC4H9)4)为基本原料,先将25 mL钛酸丁酯溶解在350 mL无水乙醇溶剂中,逐渐加入10 mL冰乙酸,并磁力搅拌45 min得到胶体A;将1.5 g尿素(含氮化合物,改性剂)溶解在15 mL去离子水中,并加入150 mL无水乙醇和10 mL冰乙酸,形成混合溶液B;在磁力搅拌2 h内,用蠕动泵向以每2 s 1滴的速度将溶液B滴入溶胶A中,使胶体粒子形成一种开放的骨架结构,溶胶逐渐失去流动性而形成凝胶C,继续搅拌凝胶24 h后,将凝胶C放在暗处静置陈化24 h而得到N-TiO2催化剂.
以聚丙烯(PP)中空纤维膜为载体,采用浸渍法制备N-TiO2/PP复合催化膜.具体操作为:在密封的模具内放置聚丙烯中空纤维膜,用蠕动泵以每2 s 1滴的速度慢慢地将N-TiO2催化剂滴到中空纤维膜表面上,然后让聚丙烯中空纤维膜在N-TiO2催化剂中浸泡24 h;将浸渍好的聚丙烯中空纤维膜取出自然风干后而得到N-TiO2/PP复合催化膜.
2.2 实验装置N-TiO2/PP复合催化膜降解甲苯废气的实验流程如图 1所示.挥发性有机废气采用动态配置法,甲苯气体经过混合缓冲瓶与空气充分混合后,从底部进入复合催化膜反应器,甲苯/空气混合气体在上升的过程中由膜内扩散传质到膜外的N-TiO2催化层,经光催化降解后从复合膜反应器顶部排出.其中,复合膜的主体构件为定制的中空纤维膜组件,其材料为聚丙烯(PP).膜组件由2400根中空纤维膜组成,纤维内径为0.38 mm,纤维外径为0.50 mm,微孔孔径为0.01~0.1 μm,有效膜长为300 mm,膜腔内的容积为54 mL,膜的有效传质面积为2.2608 m2,整个复合膜反应器外壳的内径为4 cm,高度为41 cm.
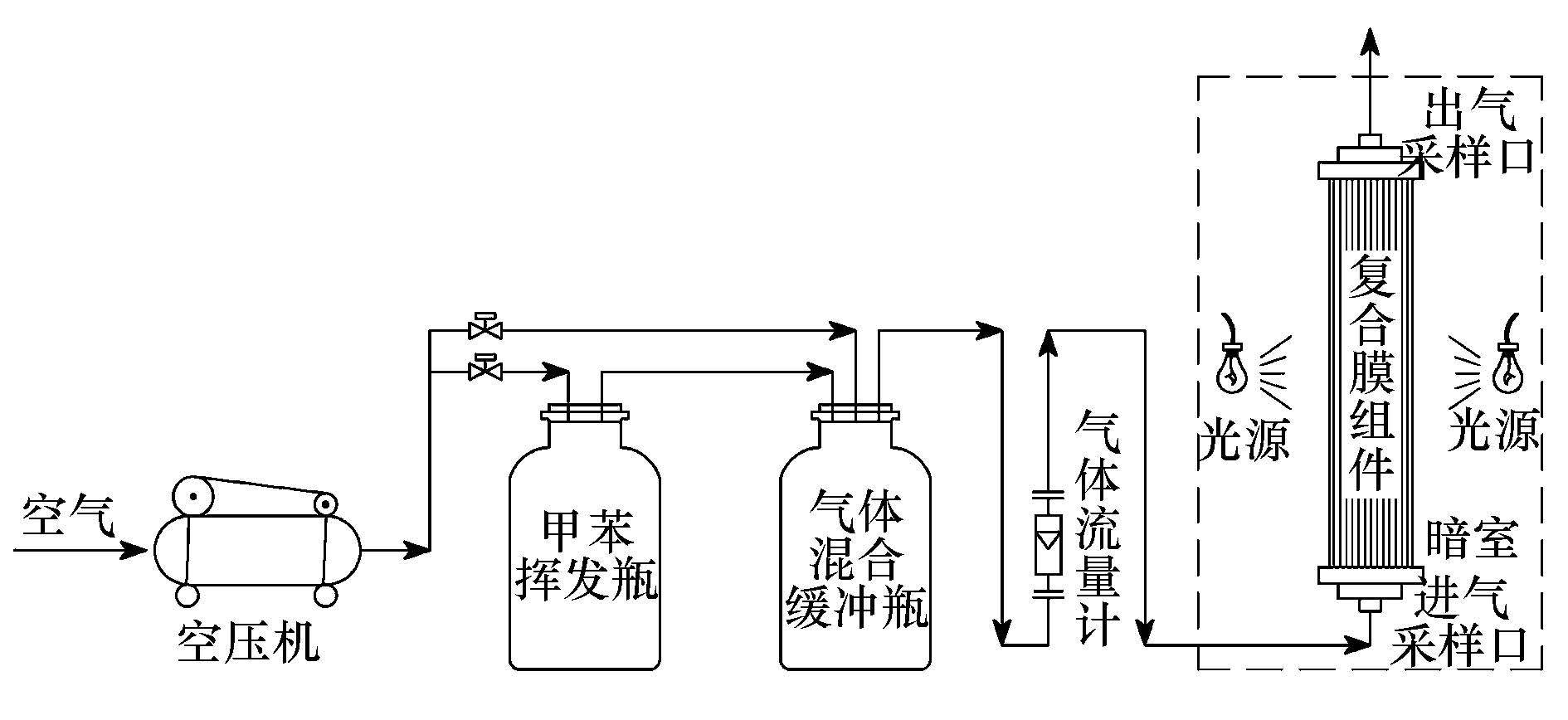 |
| 图 1 N-TiO2/PP复合膜处理甲苯气体实验装置图 Fig. 1 Schematic diagram of the N-TiO2/ PP composite film for toluene removal |
甲苯气体浓度采用美国RAE systems的PGM-7600型挥发性有机物(VOCs)检测仪检测;CO2采用德国德图testo535CO2二氧化碳检测仪进行测定;气体流量采用玻璃转子流量计测定,测量范围为0.15~1.5 L·min-1;光照强度由香港希玛AR823型分体式照度计测量,测量范围为1~100000 lx;XPS采用Thermo Fisher Scientific 生产的ESCALAB250型X-射线光电子能谱进行测试;FT-IR采用美国Thermo scientific 公司生产的Nicolet6700-Contiuμm型傅里叶变换红外光谱-显微镜联用仪进行测试.
3 结果与分析(Results and analysis) 3.1 气体停留时间对膜反应器催化处理甲苯的影响中空纤维复合膜气体停留时间以膜的容积和气体流量计算,进气流量为0.3~1.5 L·min-1,相应的气体停留时间为10.8~2.16 s.在甲苯初始浓度为130 mg·m-3,温度为25 ℃,以光照强度为1000 lx的自然光、可见光、紫外光为光源的条件下,考察气体停留时间对N-TiO2/PP复合膜光催化甲苯去除效果的影响,结果如图 2所示.由图 2可知,以紫外光为光源时,甲苯的降解效果最佳,可见光次之.随着气体停留时间的延长,甲苯的降解率逐渐增大后趋于稳定.当气体停留时间为2.16 s时,紫外光、可见光和自然光催化的甲苯降解率分别为65.8%、64.0%、52.7%;延长气体停留时间至3.24 s时,甲苯降解率分别上升至70.1%、68.0%、59.2%;继续延长气体停留时间至4.32 s时,甲苯降解率已分别达到77.0%、72.0%、60.0%以上.延长气体停留时间,单位体积气体获得的能量增多,活性物种(·OH、·O等)量增多,甲苯光催化降解效率增大.但气体停留时间的增长将增大反应器体积,增大设备投资,因此,工程应用中应选择适宜的气体停留时间.综合考虑实验结果及运营成本等因素,认为4.32 s为本实验最适宜的气体停留时间.
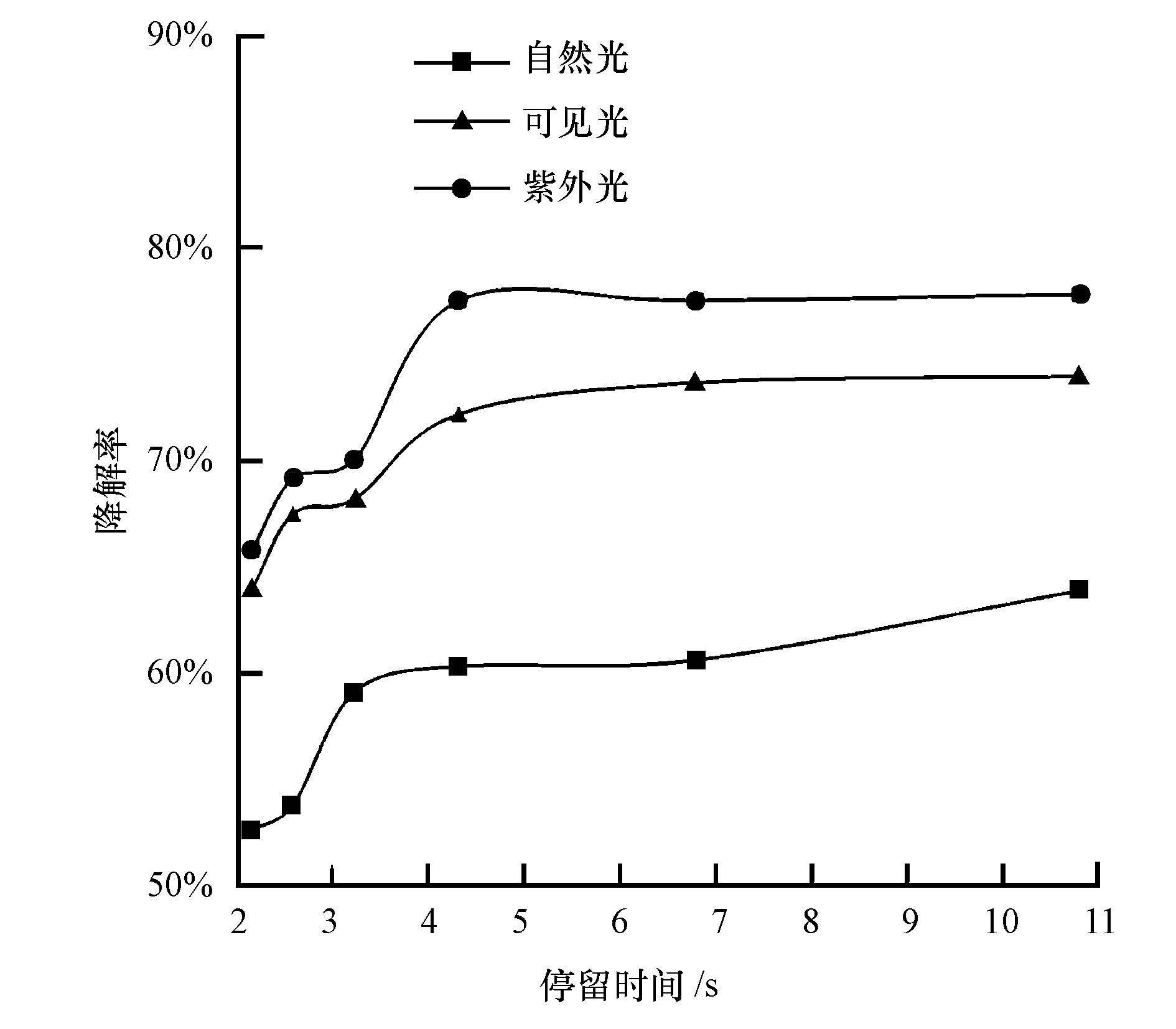 |
| 图 2 气体停留时间对甲苯去除效果的影响 Fig. 2 Influence of resistance time on toluene removal |
在甲苯初始浓度为130 mg·m-3,温度为25 ℃,气体停留时间为4.32 s的条件下,分别以光照强度为1000 lx的自然光、可见光、紫外光为光源,考察光照时间对N-TiO2/PP复合膜光催化甲苯去除效果的影响,结果如图 3所示.由图 3可知,甲苯的降解率随光照时间的增加而逐渐减小后趋于稳定.当光照时间为5 min时,紫外光、可见光和自然光催化的甲苯降解率分别可达83.0%、77.0%和76.0%;继续延长光照时间甲苯降解率逐渐下降,30 min时可见光催化的甲苯降解率下降至70.7%;40 min时自然光催化的甲苯降解率下降至67.4%;光照时间延长至60 min时,紫外光催化的甲苯降解率下降至72.7%.继续延长光照时间,甲苯降解率变化不大,光照时间为30~100 min时,可见光催化的甲苯降解率基本稳定在70.0%左右;光照时间为40~60 min时,自然光催化的甲苯降解率基本稳定在67.0%左右,光照时间延长至80 min时,自然光催化的甲苯降解率下降至60.3%,80~100 min内自然光催化的甲苯降解率基本稳定在60.0%;光照时间为60~100 min时,紫外光催化的甲苯降解率基本稳定在72.0%左右.反应起始阶段N-TiO2催化剂对甲苯的吸附与甲苯的光催化降解未达到平衡,甲苯的吸附速率小于降解速率,光照产生的·OH将甲苯迅速氧化分解,随着光照时间的延长吸附速率与降解速率的比值逐渐减小,于是甲苯降解率逐渐减小.当达到一定光照时间后,甲苯的吸附与降解达到平衡,甲苯降解率可保持稳定,这有利于甲苯的长时间净化.
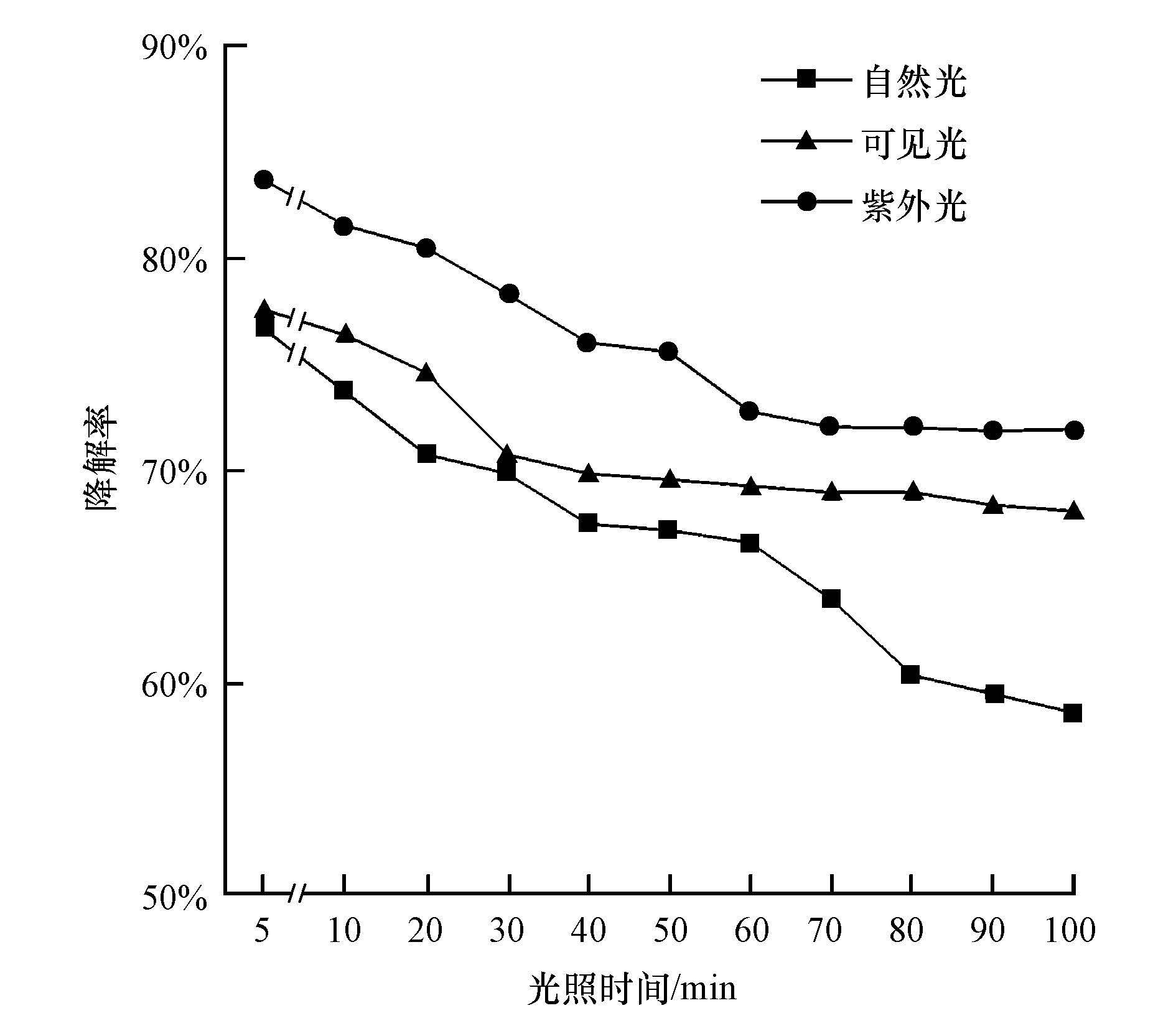 |
| 图 3 光照时间对甲苯去除效果的影响 Fig. 3 Influence of illumination time on toluene removal |
在甲苯进气浓度为130 mg·m-3,温度为25 ℃,气体停留时间为4.32 s的条件下,分别以可见光、紫外光为光源,考察光照强度对N-TiO2/PP复合膜催化甲苯去除效果的影响,结果如图 4所示.由图 4可知,随着光照强度的增加,甲苯降解率逐渐增大后趋于稳定.在光照强度为50~800 lx的范围内,甲苯降解率与光照强度成正比,相应的紫外光催化的甲苯降解率为70.7%~78.4%,可见光催化的甲苯降解率也由67.8%逐渐增大至76.3%.光照强度增强光子量增多,光子提供能量,在N-TiO2催化剂表面形成电子-空穴对,光照强度越强则产生的电子-空穴对越多(Ma et al.,2009),电子e-和空穴h+将O2和H2O氧化成具有强氧化性的羟基自由基·OH,·OH将甲苯氧化为CO2和H2O,因此,甲苯降解率逐渐增大.在光照强度为800~1000 lx的范围内,紫外光和可见光催化的甲苯降解率分别基本稳定在80.0%和76.0%.当光照强度增大至一定值时,由于受催化剂表面活性位的限制,催化剂表面吸附的光子数达到饱和,部分电子-空穴对直接复合,反应速率趋于缓慢并逐渐达到定值(丁华等,2006).此时,光催化降解甲苯的速率受制于中空纤维膜对甲苯的吸附传质速率,而与光照强度无关(陈洲洋等,2015).
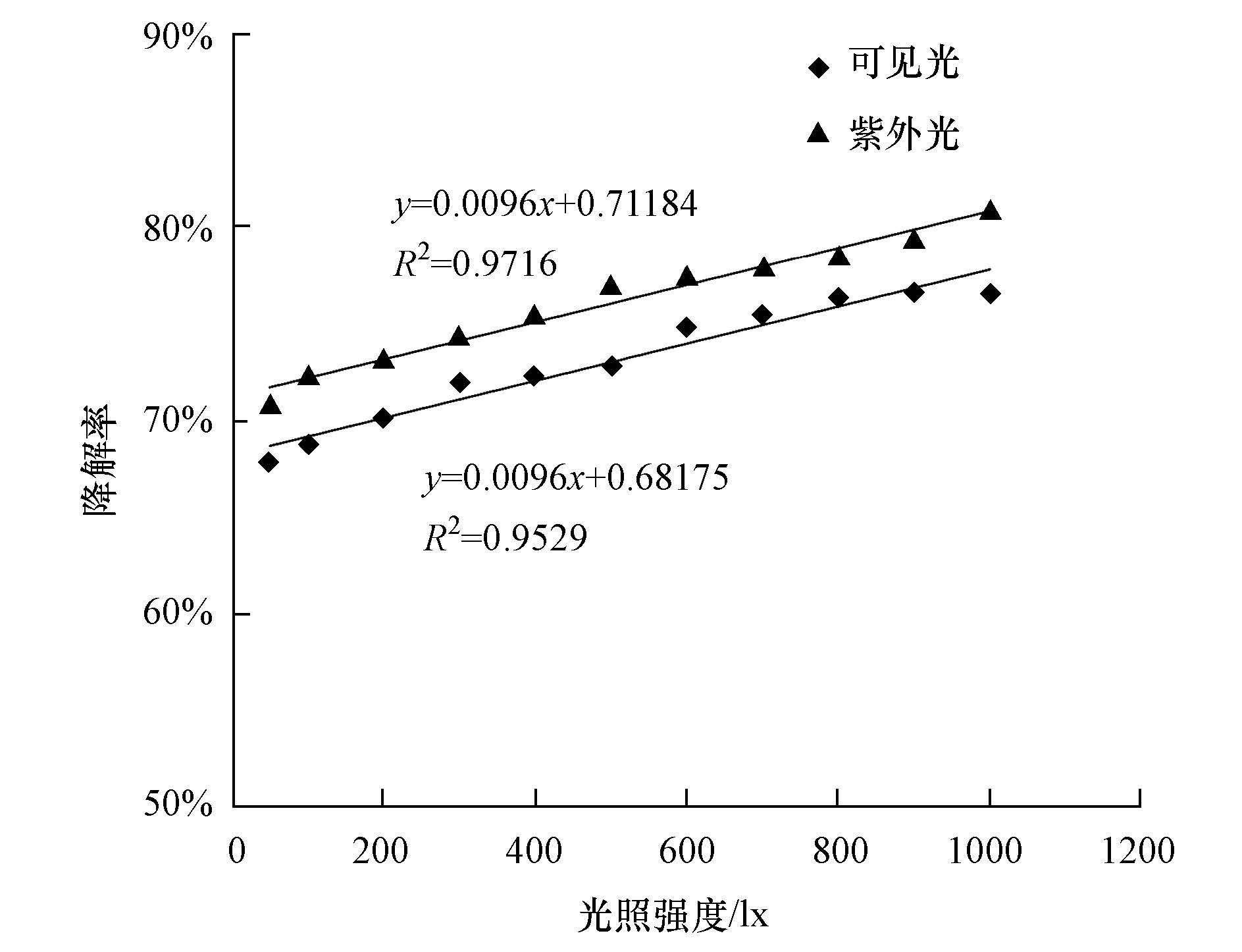 |
| 图 4 光照强度对甲苯去除效果的影响 Fig. 4 Influence of illumination intensity on toluene removal |
在温度为25 ℃,气体停留时间为4.32 s,分别在无光和以光照强度为1000 lx的自然光、可见光、紫外光为光源的实验条件下,改变甲苯的进气浓度,考察进气浓度对N-TiO2/PP复合膜催化甲苯去除效果的影响,结果如图 5所示.由图 5可知,无光照时,在进气浓度为80~140 mg·m-3的范围内,甲苯的去除率基本维持在30%左右,说明PP中空纤维膜作为疏水性气体分离膜,具有一定的甲苯/空气分离能力.有光的条件下,甲苯的降解率随着进气浓度的升高而先逐渐增大后逐渐减少.当甲苯进气浓度为80 mg·m-3时,紫外光、可见光和自然光催化的甲苯降解率分别为61.5%、55.9%和48.0%;甲苯进气浓度为80~140 mg·m-3时,随着进气浓度的升高甲苯降解率逐渐增大,当甲苯进气浓度升高至130 mg·m-3时,可见光和自然光催化的甲苯降解率达到最大值,分别为72.6%和63.9%;甲苯进气浓度升高至140 mg·m-3时,紫外光催化的甲苯降解率达到最大值为84.0%.此时,光催化降解率只与催化剂表面对甲苯的吸附速率相关,甲苯进气浓度较低时,催化剂表面吸附的甲苯量少,催化剂表面的活性位过量,甲苯迅速被氧化分解.增大进气浓度,催化剂表面对甲苯的吸附速率加快,光量子效率提高,故降解率逐渐增大.当达到吸附平衡点时,光量子效率最高,甲苯降解率最大(张一兵等,2012).逐渐增加甲苯进气浓度为130~200 mg·m-3时,甲苯的降解率随着进气浓度的升高而逐渐减小,当甲苯进气浓度为200 mg·m-3时,紫外光、可见光和自然光催化的甲苯降解率分别下降至66.7%、63.8%和43.5%.达到吸附平衡点后,催化剂表面的吸附量已达到饱和,继续增大甲苯浓度时,催化剂表面活性位迅速被大量甲苯和中间产物占据,导致光催化氧化反应速率常数减小(杨访等,2015),甲苯和中间产物及其聚合物将催化剂覆盖,导致催化剂一定程度的失活(邱作志等,2008);同时,光照强度也因甲苯气体的吸收、屏蔽作用而不断削弱(张一兵等,2012),因此,甲苯降解率下降.
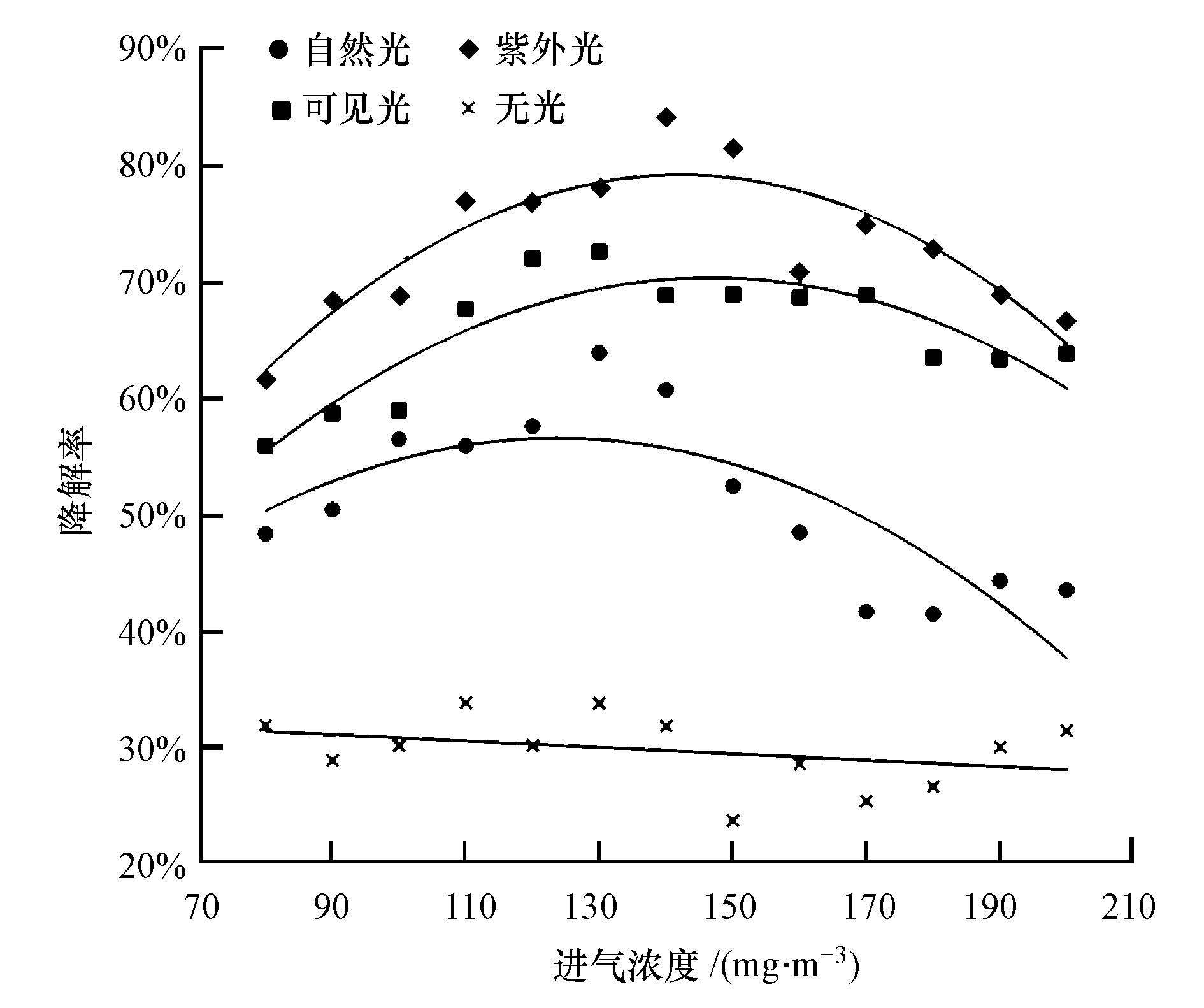 |
| 图 5 进气浓度对甲苯去除效果的影响 Fig. 5 Influence of inlet concentration on toluene removal |
N-TiO2/PP复合膜光催化降解甲苯废气的理想产物为CO2和H2O,CO2的生成量和甲苯的直接矿化率是表征复合催化膜系统性能的一个重要指标.甲苯的矿化率(MR)以C原子为计算对象,即:
MR=N1/N2×100%
式中,N1为二氧化碳中C原子的物质的量,N2为甲苯中C原子的物质的量.
在气体停留时间为4.32 s,以可见光为光源的条件下,考察甲苯去除量与CO2生成量、甲苯矿化率之间的关系,结果如图 6所示.CO2生成量随甲苯去除量的增大而逐渐增大,甲苯矿化率随甲苯去除量的增大而呈下降的趋势.在甲苯去除量为4.21~15.1 μmol·h-1的范围内时,甲苯的矿化率维持在91%以上.当甲苯去除量为4.21 μmol·h-1时,CO2生成量为28.13 μmol·h-1,矿化率最大为95.2%;当甲苯去除量增大到15.1 μmol·h-1时,CO2生成量增大至105.5 μmol·h-1,而矿化率下降至91.4%.当甲苯去除量在20~30 μmol·h-1的范围内,甲苯的矿化率维持在82%以上;而当甲苯去除量继续增大至46.8 μmol·h-1时,CO2生成量增大至最大值为229 μmol·h-1,矿化率为70%.CO2的生成量随甲苯去除量的增大而逐渐增大,且矿化率维持在70%以上,说明N-TiO2催化剂具有较高的活性,其光催化降解低浓度甲苯的主要产物为CO2和H2O,只有少部分甲苯被氧化为其它的中间产物.
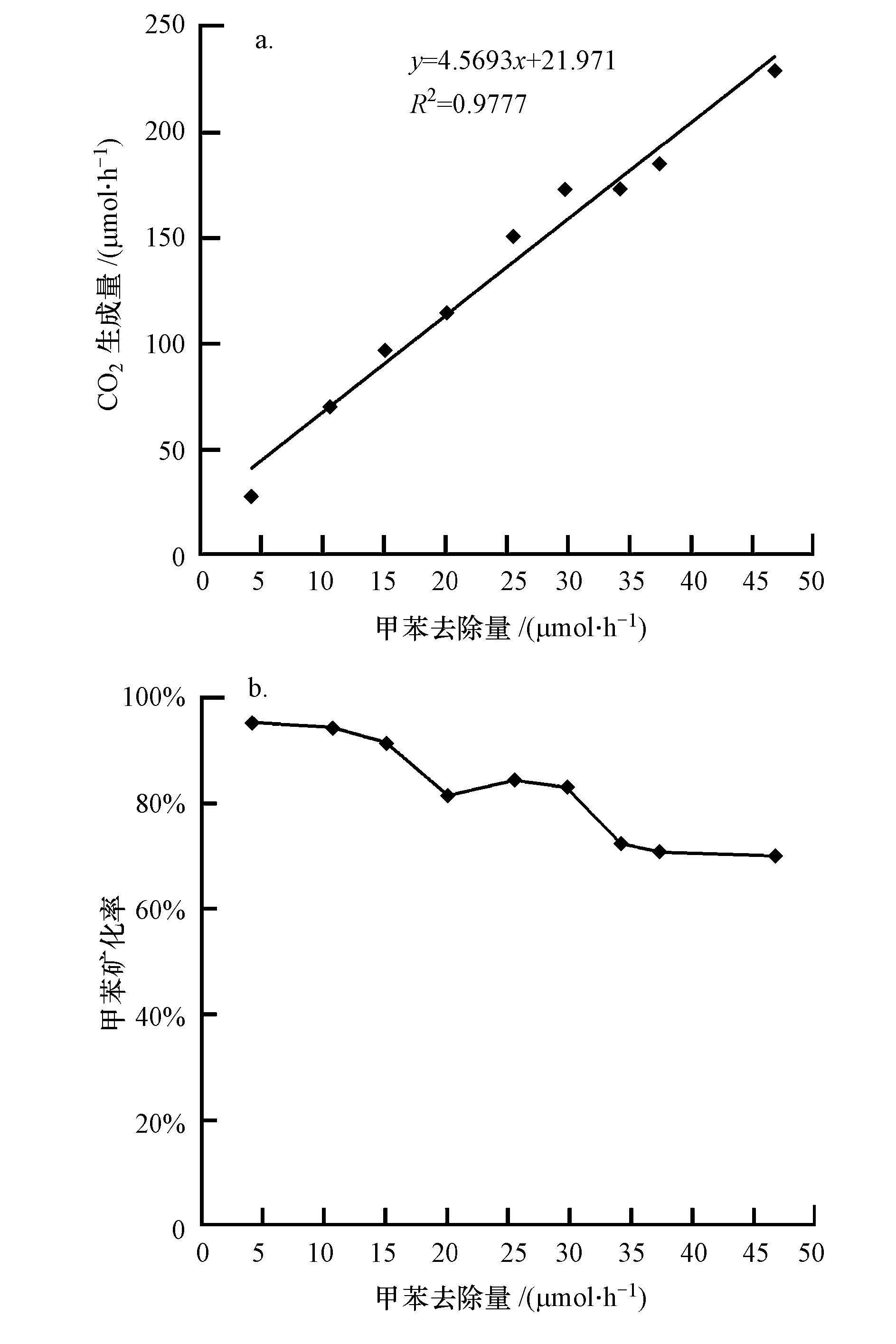 |
| 图 6 CO2生成量(a)及甲苯矿化率(b)与甲苯去除量的关系 Fig. 6 Relationship between CO2 generation rate(a),mineralization rate(b)and toluene removal rate |
图 7为TiO2及N-TiO2催化剂的紫外-可见(UV-Vis)光谱图,其中,a为TiO2催化剂,b为掺杂了N的N-TiO2催化剂.从图中可以看出,单一的TiO2光响应范围为λ <387 nm,而掺入N后的N-TiO2催化剂响应范围明显强于单一的TiO2催化剂,在λ为400~800 nm范围内均有很强的吸收值.这说明N的掺杂拓宽了催化剂的光响应范围,增强可见光下的吸光率,提高光催化剂的可见光光催化活性.在λ<400 nm的光吸收是由TiO2的固定禁带跃迁引起的(董帆等,2010).而N掺杂TiO2表现出的可见光吸收,是由于价带之上存在N掺杂引起的额外电子状态(Asahi et al.,2001).
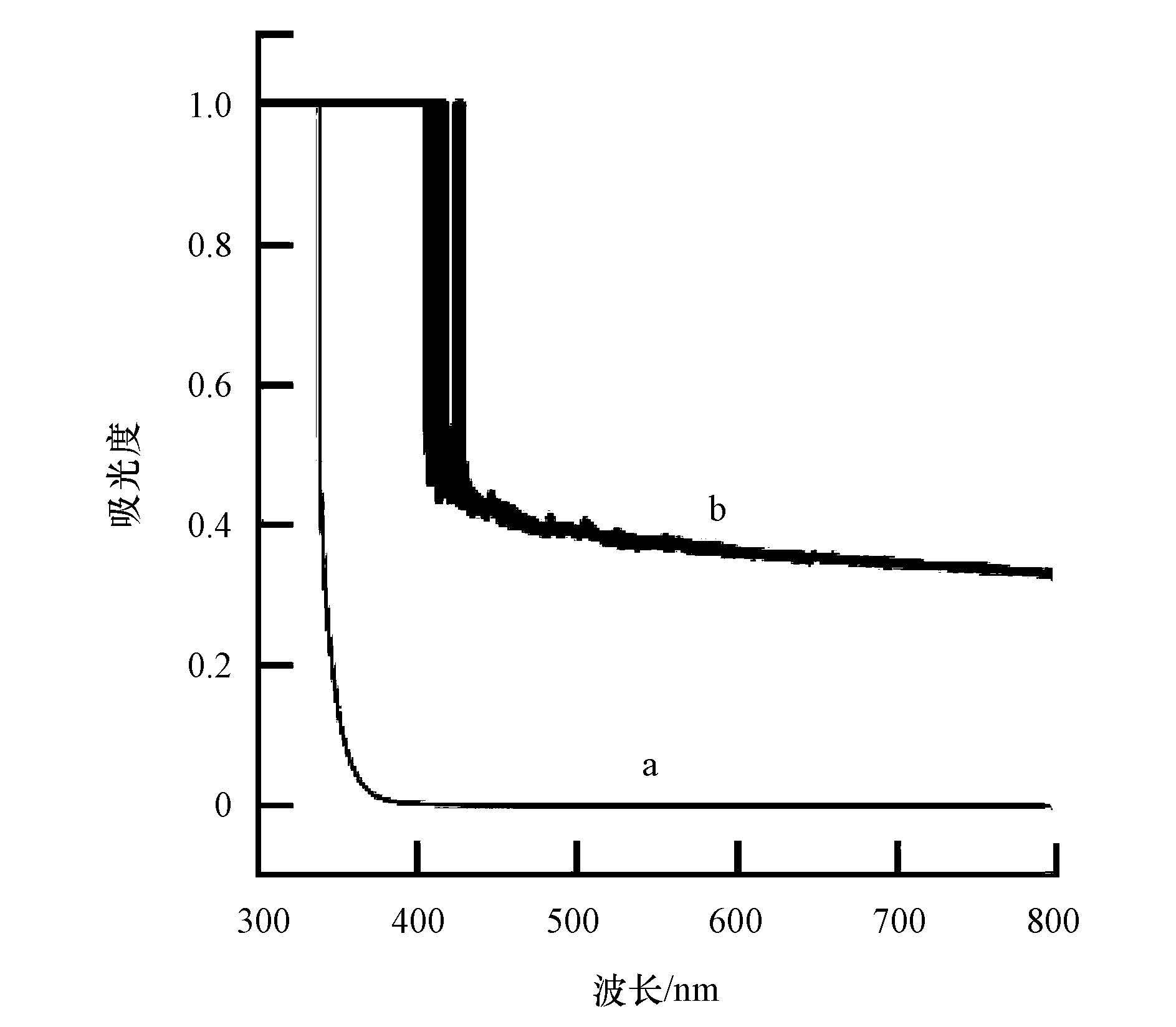 |
| 图 7 TiO2及N-TiO2催化剂的UV-Vis吸收光谱 Fig. 7 UV-vis of TiO2 and N-TiO2 |
图 8a为N-TiO2/PP复合膜的XPS全谱图,由图 8a可知,复合膜由C、N、Ti、O组成,C的存在是由于空气中存在大量的C所致.图 8b为Ti2p的XPS图,在结合能为458.64 eV和464.5 eV处出现的特征峰分别对应于Ti2p3/2和Ti2p1/2,两峰的带间能量差为5.86 eV,表明Ti主要以Ti4+形式存在(Xiao et al.,2009).图 8c为N-TiO2/PP复合膜中N1s的XPS谱图,在结合能为399.72 eV处出现了特征峰.据文献报道(Sathish et al.,2005),N—Ti—O中的N的结合能为400 eV左右,因此,推断399.72 eV处的N以N—Ti—O的形式存在,即N取代O—Ti—O中的O而生成N—Ti—O.图 8d为光催化前后O1s的XPS谱图,其峰比较宽(约为528~535 eV)说明至少存在3种不同形态的氧,结合能为530.1 eV归属于Ti—O—Ti;结合能为530.3 eV归属于Ti4+—O键(Zhou et al.,2006);光催化前,在结合能为532.4 eV处出现了一特征峰,其归属于表面·OH;经过光催化反应后,在531.7 eV和532.07 eV处分别出现了特征峰,其均为羟基氧(Zhan et al.,2013),且峰值较光催化反应前明显升高,因此,推断经过光催化反应后,电子、空穴与空气中的O2和H2O发生氧化反应生成了·OH.
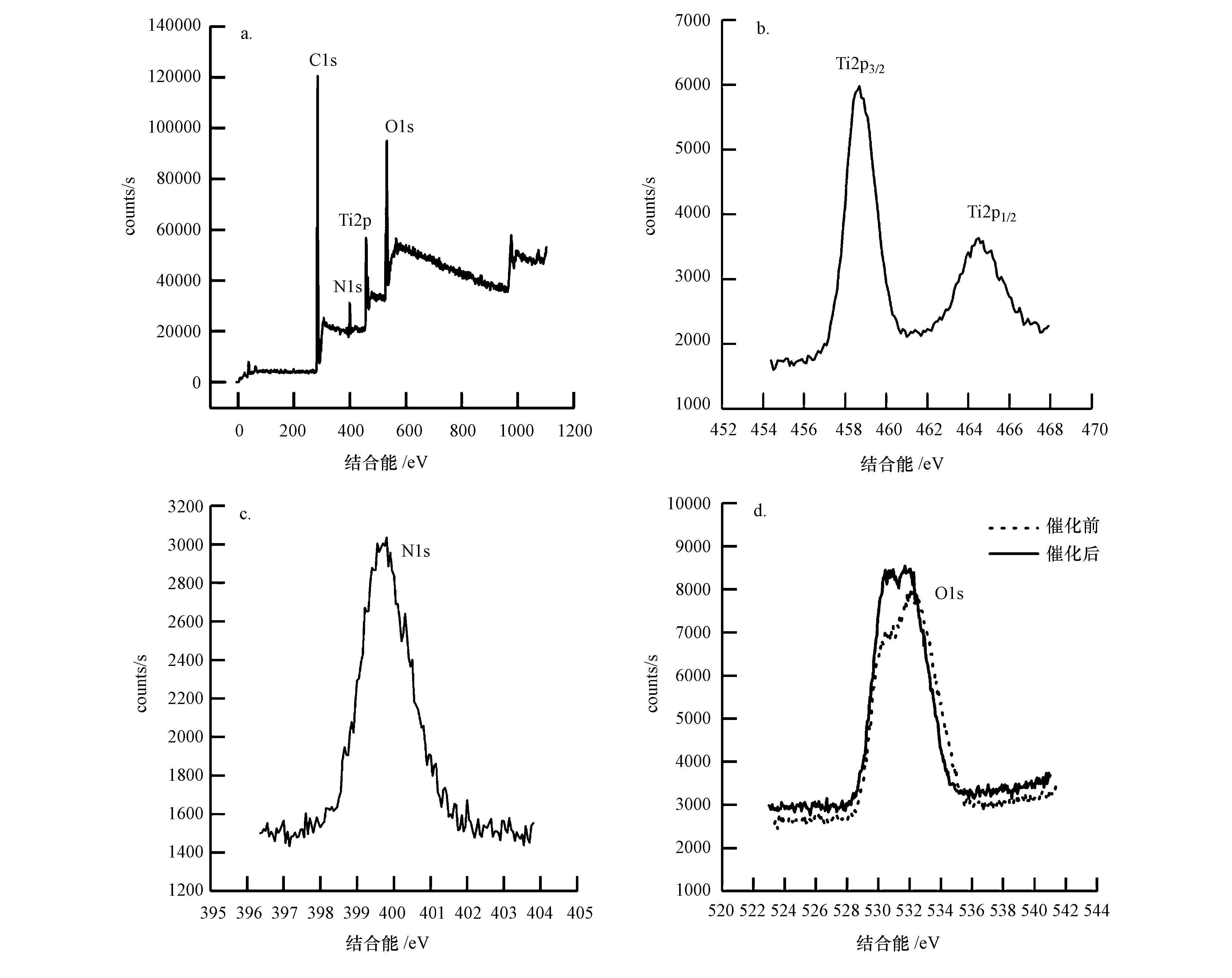 |
| 图 8 复合膜的XPS谱图(a.N-TiO2/PP复合膜,b.Ti2p,c.N1s,d.O1s) Fig. 8 XPS spectra of composite film |
图 9为光催化前后N-TiO2/PP复合膜光催化前后的红外特征光谱图.由图可知,光催化前后复合膜均在670、1167、1377、1454、2839、2873、2920、2953、3000~3600 cm-1处出现了吸收峰,光催化前复合膜在1549、1639 cm-1处出现了吸收峰,而光催化后复合膜在1556、1646 cm-1处出现了吸收峰.一般认为500~800 cm-1范围出现的峰为TiO2的晶格振动造成,据文献报道(Xie et al.,2001),670 cm-1处为CO2的特征峰,因此,可认为670 cm-1处的峰在光催化反应前为TiO2的晶格振动峰,光催化反应后甲苯氧化生成CO2,因此峰值升高. 1167 cm-1归属于C—O—C伸缩振动酯吸收峰,TiO2的前驱为钛酸丁酯,因而此处有峰.1377 cm-1处为甲基(—CH3)的对称面内弯曲振动吸收峰,1454 cm-1处为O—H的面内弯曲和甲苯的芳环的面内骨架振动峰(Zhu et al.,2013).光催化前复合膜在1549 cm-1和1639 cm-1处出现的峰为Ti—O键的伸缩振动峰,而光催化反应后复合膜在1556 cm-1和1646 cm-1处的出现的峰为CO(Zou et al.,2012),说明甲苯光催化过程中有醛类或酸类物质生成.光催化前1700~2800 cm-1范围内吸收值几乎为0,而经过光催化反应后吸收值逐渐增大,为光催化反应过程中产生的CO2所致.2839、2873、2920、2953 cm-1处为甲基组的对称和反对称C—H伸缩振动及芳环的C—H伸缩振动峰(邹学军等,2011).3000~3600 cm-1处为复合膜催化剂表面吸附水分子或表面羟基O—H键的伸缩振动峰(Maira et al.,2001),光催化反应后峰值明显升高,表明甲苯光催化过程中产生了羟基组和H2O.
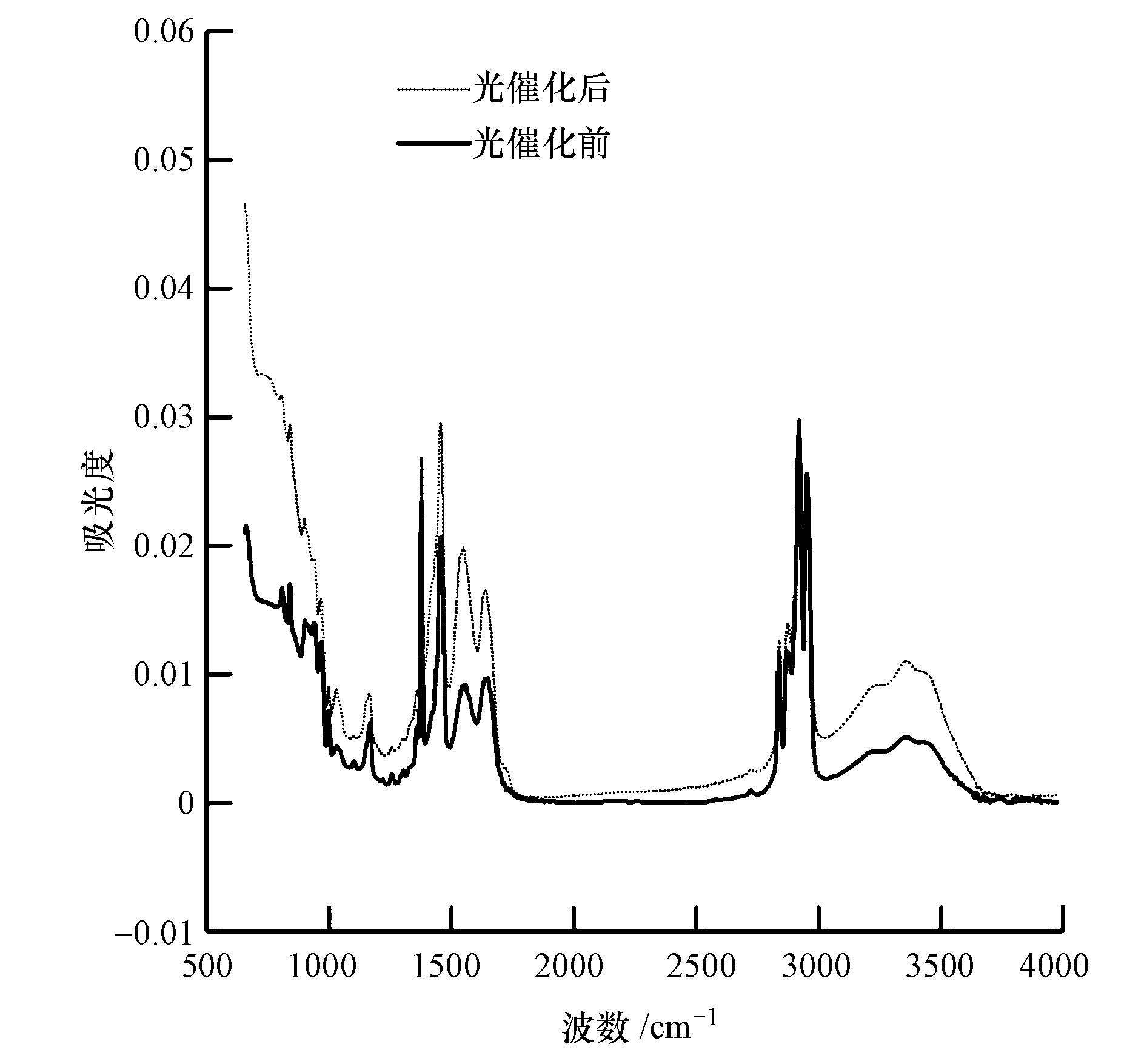 |
| 图 9 复合膜红外特征光谱图 Fig. 9 FT-IR spectra of composite film |
在光催化反应过程中,采集反应器出口气体样品,用气相色谱-质谱联用仪(GC-MS)进行样品分析.分析结果显示,甲苯光催化降解产生的中间产物主要有苯(C6H6,m/z=78)、苯甲醛(C7H6O, m/z=106)、苯乙酸(C8H8O2, m/z=136)和一系列开环产物如丙烯醛(C3H4O, m/z=56)、乙烯(C2H4, m/z=28)等,以及化合物甲酸甲酯(C2H4O2, m/z=60),质谱结构如图 10所示,并最终被氧化生成CO2和H2O.
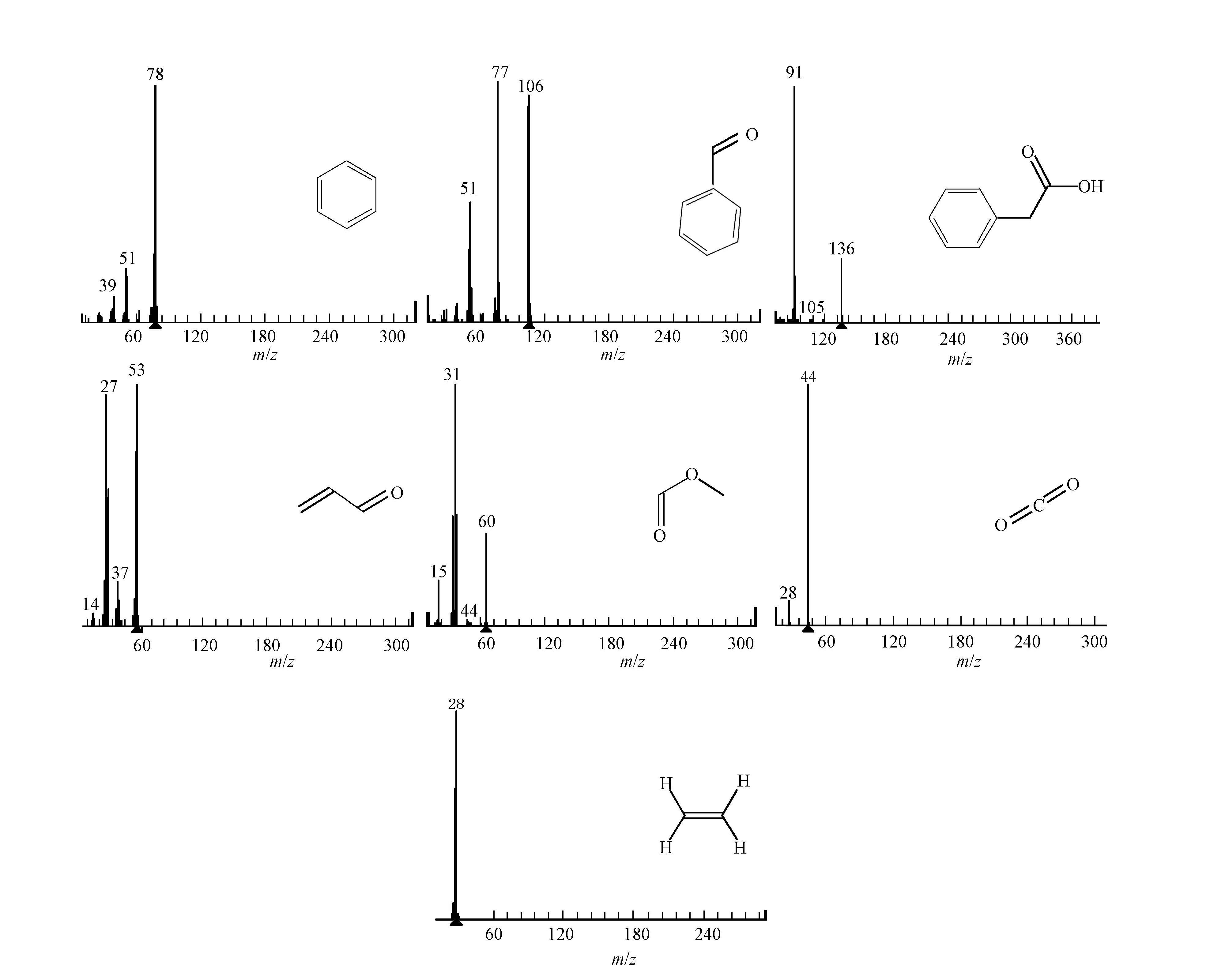 |
| 图 10 甲苯光催化降解出口气体组分GC-MS分析 Fig. 10 Outlet gas component from toluene photo catalytic degradation by GC-MS analysis |
在光的照射下,TiO2中的光生电子吸收能量后由价带跃迁到导带,形成带负电子e-;同时,在TiO2的价带上产生具有强氧化性的空穴h+.带负电子e-与吸附在复合膜上的O2反应生成氧自由基(·O2-),·O2-进一步与H+发生反应生成过氧氢根自由基(·HO-2),最终·HO-2与电子e-反应生成强氧化性的羟基自由基(·OH);同时,在TiO2价带上的空穴h+与吸附在复合膜上的OH-和H2O发生氧化反应生成氧化性更强的羟基自由基(·OH).
根据甲苯光催化降解的中间产物,结合相关文献报道(武江波等,2007)推测出甲苯光催化降解过程机理如图 11所示.首先被吸附到复合膜上的甲苯气体,在光的作用下发生脱氢反应生成氢自由基(·H)和苄基自由基(phCH2·),之后甲苯降解过程可能有以下4个途径:一是苄基自由基(phCH2·)与羰基自由基(·CO·)及羟基自由基(·OH)发生加成反应生成苯乙酸(phCH2COOH),苯乙酸发生分解反应后在氢自由基(·H)的还原及羟基自由基(·OH)的氧化下生成苯和羟基乙酸(C2H4O3),苯和羟基乙酸(C2H4O3)最后氧化生成CO2和H2O;二是苄基自由基(phCH2·)与羟基自由基(·OH)发生加成反应生成苯乙醇(phCH2OH),苯乙醇脱羟甲基(—CH2OH)后生成的苯基自由基(C6H5·)和羟甲基自由基(·CH2OH)分别与氢自由基(·H)发生加和反应生成苯和甲醇;三是苄基自由基(phCH2·)与空气中的O2发生反应生成苄过氧自由基(phCH2OO·),苄过氧自由基(phCH2OO·)在电子e-的还原下生成苯甲醛(phCHO)和羟基,苯甲醛受羟基自由基(·OH)攻击发生摘氢反应后又继续被羟基氧化生成苯甲酸(phCOOH),苯环与羧基之间的C—C键发生断裂与氢自由基相加合生成苯环和甲酸,甲酸继续与步骤三中的甲醇发生反应生成甲酸甲酯(C2H4O2),甲酸甲酯(C2H4O2)最后氧化生成CO2和H2O;四是苯甲醛在氧气的攻击下苯环上的C—C键发生断裂并在氢自由基(·H)的作用下生成丙烯醛(C3H4O)和乙烯(C2H4),丙烯醛(C3H4O)和乙烯(C2H4)最后氧化生成CO2和H2O.
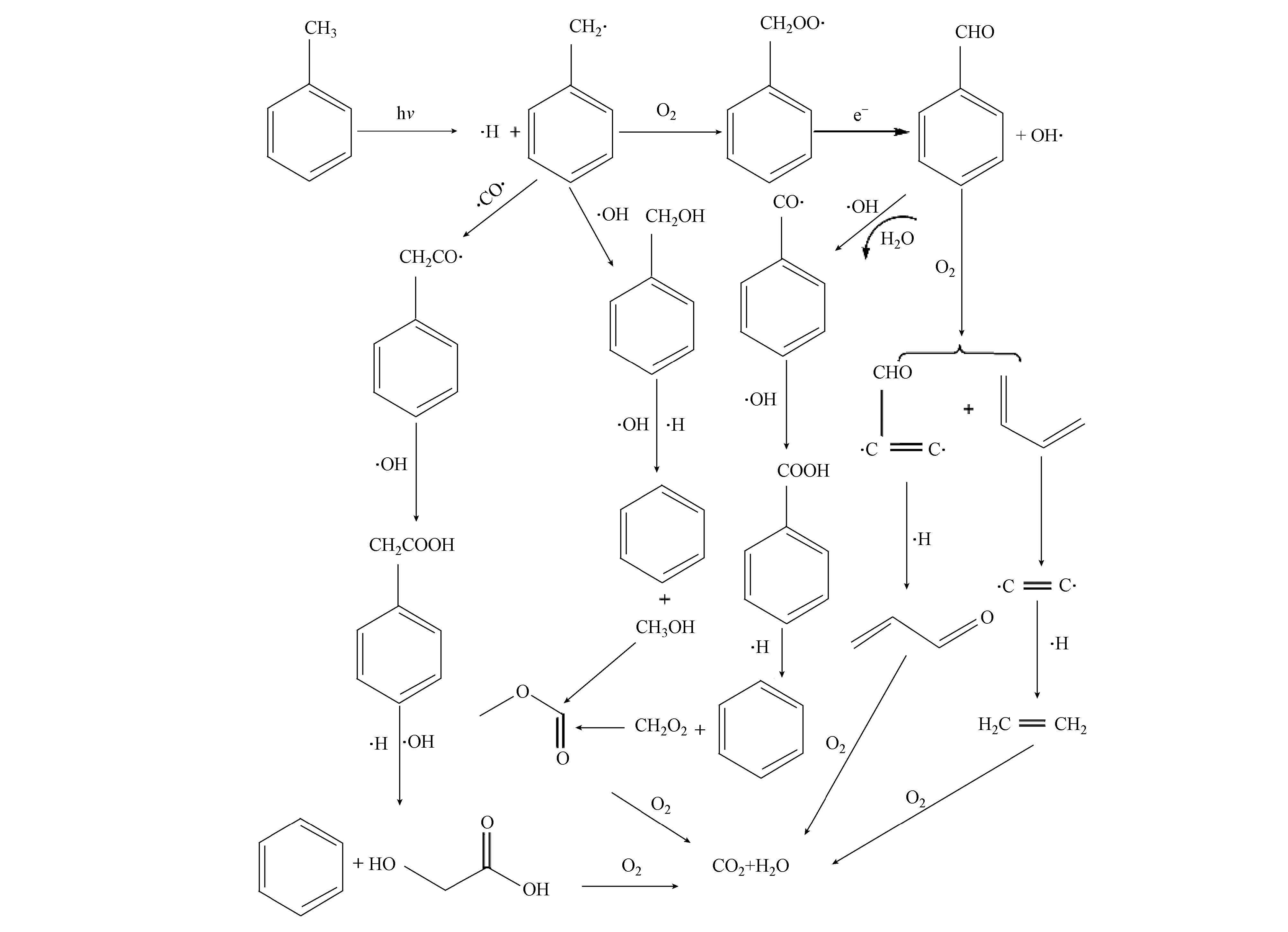 |
| 图 11 甲苯光催化降解反应途径 Fig. 11 Toluene photocatalytic degradation pathway |
1) 采用N-TiO2/PP复合催化膜能有效降解甲苯气体,在紫外光照射下,甲苯降解率可达84%,去除负荷可达89.8 g·m-3·h-1;其次为可见光,甲苯降解率可达77%,去除负荷可达76.5 g·m-3·h-1;最后为自然光,甲苯降解率可达63.9%,去除负荷可达69.25g·m-3·h-1;适宜气体停留时间为4.32 s.
2) 采用紫外-可见光谱(UV-Vis)表征分析了TiO2和N-TiO2催化剂,结果表明,掺杂N改性的TiO2复合膜光催化层在紫外和可见光波段的吸收性能都有极大的改善.采用X-射线光电子能谱(XPS)和傅里叶变换红外光谱(FT-IR)表征了N-TiO2/PP复合催化膜,XPS表明存在N—Ti—O和Ti4+—O键,FT-IR表明甲苯光催化降解过程中有羟基、CO生成.GC-MS分析结果表明,甲苯光催化降解的中间产物有苯(C6H6)、苯甲醛(C7H6O)、苯乙酸(C8H8O2)和丙烯醛(C3H4O)、乙烯(C2H4)等开环产物,以及化合物甲酸甲酯(C2H4O2)等.
3) N-TiO2/PP复合催化膜降解甲苯机制为甲苯气体通过中空纤维膜传质到N-TiO2/PP复合催化膜,光催化产生羟基自由基,甲苯气体被羟基自由基氧化成中间产物,然后继续降解为最终产物二氧化碳和水.
| [1] | Aoki K, Morikawa T, Ohwaki T, et al. 2006. Photocatalytic degradation of formaldehyde and toluene mixtures in air with a nitrogeN-doped TiO2 photocatalyst[J]. Chemistry Letters , 35 (6) : 616–617. DOI:10.1246/cl.2006.616 |
| [2] | Asahi R, Morikawa T, Ohwaki T, et al. 2001. Visible-light photocatalysis in nitrogeN-doped titanium oxides[J]. Science , 293 (5528) : 269–271. DOI:10.1126/science.1061051 |
| [3] | Chen C, Bai H, Chang S, et al. 2007. Preparation of N-doped TiO2 photocatalyst by atmospheric pressure plasma process for VOCs decomposition under UV and visible light sources[J]. Journal of Nanoparticle Research , 9 (3) : 365–375. DOI:10.1007/s11051-006-9141-2 |
| [4] | 丁华.2006. Ce(0.5)Zr(0.5)O2固溶体的制备与其催化甲苯燃烧的性能[J]. 辽宁化工 , 2006 (3) : 145-146–172. |
| [5] | 董帆,2010.非金属掺杂TiO2基纳米材料的制备新方法、结构表征及可见光催化降解气相甲苯性能[D].杭州:浙江大学 http://cdmd.cnki.com.cn/Article/CDMD-10335-2010166357.htm |
| [6] | Dzinun H, Othman M H D, Ismail A F, et al. 2015. Photocatalytic degradation of nonylphenol by immobilized TiO2 in dual layer hollow fibre membranes[J]. Chemical Engineering Journal , 269 : 255–261. DOI:10.1016/j.cej.2015.01.114 |
| [7] | 黄雯, 杨家宽, 范双艳.2007. 活性炭负载TiO2的甲苯光催化降解性能研究[J]. 工业催化 , 2007 (10) : 55–59. |
| [8] | Irokawa Y, Morikawa T, Aoki K, et al. 2006. 2006.Photodegradation of toluene over TiO2-xNx under visible light irradiation[J]. Physical Chemistry Chemical Physics , 8 (9) : 1116–1121. DOI:10.1039/b517653k |
| [9] | 金苏君, 陈侠胜, 李爽, 等.2008. TiO2柱撑膨润土光催化气相甲苯的活性研究:湿度对活性的影响与催化剂结构的关系[J]. 环境科学 , 2008, 29 (12) : 3331–3336. |
| [10] | Linsebigler A L, Lu G, Yates Jr J T. 1995. Photocatalysis on TiO2 surfaces: principles,mechanisms,and selected results[J]. Chemical Reviews , 95 (3) : 735–758. DOI:10.1021/cr00035a013 |
| [11] | Liu F, Hashim N A, Liu Y, et al. 2011. Progress in the production and modification of PVDF membranes[J]. Journal of Membrane Science , 375 (1) : 1–27. |
| [12] | Ma C M, Ku Y, Kuo Y L, et al. 2009. Effects of silver on the photocatalytic degradation of gaseous isopropanol[J]. Water,air,and soil pollution , 197 (1/4) : 313–321. |
| [13] | Maira A J, Coronado J M, Augugliaro V, et al. 2001. Fourier transform infrared study of the performance of nanostructured TiO2 particles for the photocatalytic oxidation of gaseous toluene[J]. Journal of Catalysis , 202 (2) : 413–420. DOI:10.1006/jcat.2001.3301 |
| [14] | Morikawa T, Irokawa Y, Ohwaki T. 2006. 006.Enhanced photocatalytic activity of TiO2-xNx loaded with copper ions under visible light irradiation[J]. Applied Catalysis A: General , 314 (1) : 123–127. DOI:10.1016/j.apcata.2006.08.011 |
| [15] | Ozaki H, Iwamoto S, Marked I M. 2007. Promotive effect of iron on visible-light-induced photocatalytic activities of nitrogeN-and silicoN-codoped titanias[J]. The Journal of Physical Chemistry C , 111 (45) : 17061–17066. DOI:10.1021/jp0751211 |
| [16] | 邱作志, 叶代启.2008. 放电等离子体驱动光催化降解甲苯研究[J]. 工业催化 , 2008, 16 (6) : 69–74. |
| [17] | Sathish M, Viswanathan B, Viswanath R P, et al. 2005. Synthesis,characterization,electronic structure,and photocatalytic activity of nitrogeN-doped TiO2 nanocatalyst[J]. Chemistry of Materials , 17 (25) : 6349–6353. DOI:10.1021/cm052047v |
| [18] | 盛国栋, 李家星, 王所伟, 等.2009. 提高TiO2可见光催化性能的改性方法[J]. 化学进展 , 2009, 21 (12) : 2492–2504. |
| [19] | Sun H, Ullah R, Chong S, et al. 2011. Room-light-induced indoor air purification using an efficient Pt/N-TiO2 photocatalyst[J]. Applied Catalysis B: Environmental , 108 : 127–133. |
| [20] | 王建宏, 高宁, 高仲芳.2008. 陶瓷填料上TiO2薄膜光催化降解甲苯的研究[J]. 能源环境保护 , 2008, 34 (1) : 26-29–34. |
| [21] | WaN-Kuen J O, HyuN-Jung K. 2012. LED irradiation of a photocatalyst for benzene,toluene,ethyl benzene,and xylene decomposition[J]. Chinese Journal of Catalysis , 33 (9) : 1672–1680. |
| [22] | 武江波.2007.甲苯光降解及光催化降解的初步研究[D].广州:中国科学院广州地球化学研究所 http://cdmd.cnki.com.cn/Article/CDMD-80165-2007101536.htm |
| [23] | Xiao Q, Ouyang L L. 2009. Photocatalytic activity and hydroxyl radical formation of carboN-doped TiO2 nanocrystalline:Effect of calcinations temperature[J]. Chemical Engineering Journal , 148 : 248–253. DOI:10.1016/j.cej.2008.08.024 |
| [24] | Xie W, Pan W P. 2001. Thermal characterization of materials using evolved gas analysis[J]. Journal of Thermal Analysis and Calorimetry , 65 (3) : 669–685. DOI:10.1023/A:1011946707342 |
| [25] | 杨访, 宣绍峰, 马新胜.2015. 纳米光催化网 ACH/TiO2 动态降解甲苯气体[J]. 过程工程学报 , 2015 (1) : 28. |
| [26] | 杨瑞, 张寅平, 赵荣义.2005. TiO2/丝光沸石光催化降解甲苯特性研究[J]. 自然科学进展 , 2005 (8) : 981–986. |
| [27] | Zhan R, Dong C, Yang B R, et al. 2013. 2013.Modulation of interface and bulk states in amorphous InGaZnO thiN-film transistors with double stacked channel layers[J]. Japanese Journal of Applied Physics , 52 (9R) : 090205. DOI:10.7567/JJAP.52.090205 |
| [28] | 张一兵, 黄明俊.2012. 甲苯的光催化降解及其动力学研究[J]. 化学试剂 , 2012 (12) : 10. |
| [29] | Zhou J, Zhang Y, Zhao X S, et al. 2006. Photodegradation of benzoic acid over metal-doped TiO2[J]. Industrial &Engineering Chemistry Research , 45 (10) : 3503–3511. |
| [30] | 邹学军.2011.TiO2基纳米材料制备及光催化降解气相甲苯的研究[D].大连:大连理工大学 http://cdmd.cnki.com.cn/Article/CDMD-10141-1012171756.htm |
| [31] | Zou X, Li X, Qu Z, et al. 2012. Photocatalytic degradation of gaseous toluene over TiO2-SiO2 composite nanotubes synthesized by sol-gel with template technique[J]. Materials Research Bulletin , 47 (2) : 279–284. DOI:10.1016/j.materresbull.2011.11.024 |
| [32] | Zhu Z, Zhao Q, Li X, et al. 2013. Photocatalytic performances and activities in Ag-doped ZnAl2O4 nanorods studied by FTIR spectroscopy[J]. Catalysis Science &Technology , 3 (3) : 788–796. |
 2016, Vol. 36
2016, Vol. 36


