2. 华南理工大学环境与能源学院, 广州 510006
2. College of Environment and Energy, South China University of Technology, Guangzhou 510006
由于抗生素药物长期且广泛应用于人与动物疾病治疗和预防及动物饲料添加剂,导致其在生态环境中持续存在,从而具有“假持久性”.这些药物不仅给人体健康和生态环境带来一定的危害,而且能诱发微生物产生一定的耐药性,从而受到了国内外学者的广泛关注(Lian et al.,2015).泰乐菌素作为一种广泛使用的兽药添加剂,其进入动物体之后,不能完全被吸收和转化,有超过85%的泰乐菌素药物会以代谢物和母体的形式被排出体外,再通过不同的途径进入到生态环境中(Guo et al.,2015).因此,了解泰乐菌素在环境中的迁移转化特性,明确其与环境介质之间的交互特性,可以科学合理地为抗生素生态环境风险评价提供一定的理论依据.
吸附是环境中抗生素迁移的重要过程,通过研究抗生素在环境介质上的吸附,可以明确抗生素在环境中的迁移特性(Mutavdžic′ Pavlovic′ et al.,2014).之前的研究者报道了泰乐菌素在土壤上的吸附特性,研究发现,土壤有机质及土壤矿物是影响抗生素在土壤上吸附的主要因素(Zhang et al.,2011).Zhang等(2013)和Guo等(2013;2014)报道了泰乐菌素在粘土矿物和铁氧化物上的吸附特性,发现离子交换、表面络合、静电作用和氢键作用是抗生素在矿物上吸附的主要因素.而对于抗生素在土壤有机质上的吸附,目前已有大量报道,Zhang等(2012)报道了诺氟沙星在腐殖酸上的吸附,发现离子交换是主导抗生素在腐殖酸上吸附的主要机制.Ahmed等(2015)报道了腐殖酸对抗生素在环境介质上的吸附,发现有机质的存在可以明显增强抗生素在环境介质上的吸附特性.Peng等(2015)研究发现,腐殖酸的存在能明显提高铁氧化物对氧氟沙星的吸附,吸附机制主要以疏水性作用和离子交换为主.Zhao等(2014)研究了灭蝇胺在腐殖酸上的吸附,发现pH值、离子强度和外来离子对吸附的影响最大,吸附机制主要以离子交换为主.以上研究中所用的腐殖酸都是直接购买或者经化学提纯的,而对于实际环境体系中大量存在的杂质较多的腐殖酸,其对抗生素的吸附特性和机制还尚不明确,且腐殖酸经提纯前后其对抗生素的吸附有何影响,目前还不得而知.因此,本文以泰乐菌素和工业腐殖酸为研究对象,系统考察工业腐殖酸提纯前后对泰乐菌素的吸附动力学、吸附等温线及pH值和离子强度对吸附的影响,以期为科学评价有机质对抗生素在环境中迁移的影响提供理论依据.
2 材料与方法(Materials and methods) 2.1 实验材料泰乐菌素(TYL,纯度>95%)和工业腐殖酸分别购于美国Sigma公司和贵州世华日升遵义县腐殖酸工业分公司;乙腈和甲酸均为色谱纯,购于美国Sigma公司;其他试剂均为分析纯,购于国药试剂有限公司;实验用水为超纯水,由Milli-Q超纯水制备(Merck Millipore Advantage A10).泰乐菌素的分子结构及其在不同pH水溶液中呈现的不同形态见图 1,在溶液pH值小于7.1时其带正电荷,在pH值大于7.1时,其以不带电荷的分子态形式存在(Guo et al.,2014).
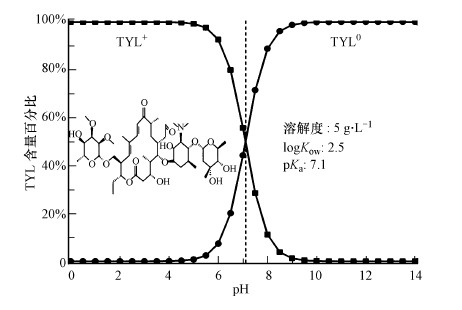 |
| 图 1 泰乐菌素的分子结构及其在不同pH水溶液中呈现的不同形态 Fig. 1 Structure of tylosin and pH-dependent speciation of tylosin molecular |
工业腐殖酸的提纯参照稀碱法(郭凌等,2014),在腐殖酸样品中加入1 mol·L-1 HCl直至pH值达到1.0,用0.1 mol·L-1 HCl调节溶液体积使最终固液比达到1:10(1 g样品:10 mL 溶液),连续搅拌2 h后离心分离沉淀物;在沉淀物中加入1 mol·L-1 NaOH直至pH值达到7.0,用0.1 mol·L-1 NaOH调节溶液体积使最终固液比达到1:10,搅拌24 h后离心;倾倒上层溶液后在沉淀物中加入6 mol·L-1 HCl不断搅拌直至pH值达到1.0,静置24 h后离心弃去上清液将沉淀物冷冻干燥,研磨过100目筛备用.具体流程图见图 2.
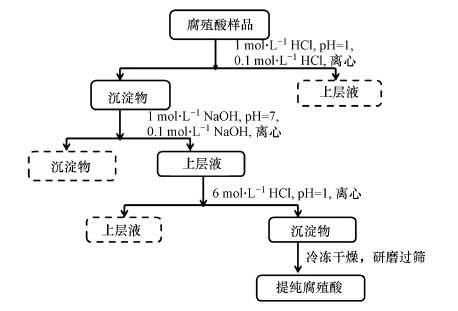 |
| 图 2 提纯腐殖酸的流程示意图 Fig. 2 Sketch of the humic acid purification procession |
称取一定量腐殖酸样品于离心管中,加入用0.01 mol·L-1 KNO3溶液配制的泰乐菌素的吸附液,并加入微量的叠氮化钠(NaN3),使其浓度为0.001 mol·L-1,以抑制土壤中微生物的影响,恒温(25±2)℃振荡,分别在相应的时间点取样.于3000 r·min-1离心10 min,取上清液分析检测.
2.3.2 吸附等温线试验配置一系列初始浓度范围为0.5~50 mg·L-1 的泰乐菌素吸附液.分别加入一定量的腐殖酸样品,用35 mL的玻璃离心管作为反应容器,放入恒温(25±2)℃、150 r·min-1的摇床中振荡达到平衡.每个样品重复3个平行样,每个浓度设置空白样品对照.平衡后,所有样品于3000 r·min-1条件下离心10 min,然后静置12 h取上清液,使腐殖酸颗粒完全沉淀.用玻璃滴管吸取1.5 mL的上清液于棕色色谱瓶中待测,在吸附背景溶液中加入0.001 mol·L-1 NaN3以抑制微生物的作用.
离子强度影响实验设置泰乐菌素的初始浓度为10 mg·L-1,用 KNO3将体系离子强度分别调节至0~0.1 mol·L-1,pH值为3.0.pH值的影响实验中,泰乐菌素的初始浓度为10 mg·L-1,用HNO3或KOH把体系pH值调为2.0~12.0,离子强度为0.01 mol·L-1的KNO3.
2.3.3 泰乐菌素的检测泰乐菌素的浓度用高效液相色谱(Agilent1200)检测,配二极管阵列检测器和反相色谱分离柱Luna(美国,Phenomenex公司),C18(2)型色谱柱(250 mm×4.6 mm,5 μm),流动相V(KH2PO4):V(乙腈)=65:35,检测波长290 nm.
2.4 吸附模型吸附动力学分别用拉格朗日一级动力学方程、拉格朗日二级动力学方程和颗粒间扩散模型进行拟合,其表达式分别如公式(1)、(2)和(3)所示(Guo et al.,2015).
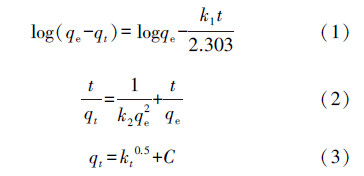
吸附等温线分别用线性吸附模型(Linear)((式(4))、Freundlich吸附模型(式(5))、Langmuir吸附模型(式(6))进行拟合(Guo et al.,2015).
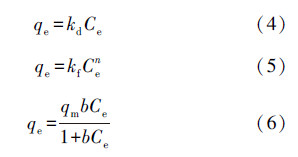
工业腐殖酸和提纯腐殖酸样品分别用VARIO III型元素分析仪和傅里叶变换红外光谱仪(FTIR Bruker)进行表征.元素组成分析是判断有机质结构和性质最简单、最重要的方法之一.腐殖酸的元素组成见表 1.从表 1可以看出,工业腐殖酸经提纯后,C、H、O、N、S的含量明显增加,灰分含量显著减小.为了表征腐殖酸结构的差异性,通过O/C、H/C和C/N原子比来进行说明.O/C原子比反映出腐殖酸的腐化程度,O/C原子比从0.801降低到0.793,表示腐殖质芳香度有所提高,因此,可以认为提纯后的腐殖酸具有更深的腐化程度.C/N原子比指示自然体系中腐殖酸的来源,来源于非维管水生植物的腐殖酸的C/N原子比为2.0~10,而来源于维管植物的腐殖酸的C/N原子比为20或更高.工业腐殖酸和提纯腐殖酸的C/N原子比分别为22.37和26.73,说明腐殖酸的来源为陆生维管植物.提纯腐殖酸的灰分含量从44.53%降到32.73%,说明纯化过程中酸处理降低样品灰分的效果较好(Zhang et al.,2014,Zhao et al.,2014).
| 表 1 腐殖酸的元素组成分析 Table 1 Elemental composition analysis of humic acid |
通过图 3可知,提纯腐殖酸和工业腐殖酸显示出相似的红外光谱特征:在3434 cm-1处的缔合—OH伸缩振动吸收宽峰;在1714 cm-1处的羧基和羰基官能团的—C=O伸缩振动吸收峰;在1615 cm-1处包括芳环的骨架振动C=C吸收峰,H键缔合C=O吸收峰和酰胺键等相互叠加吸收峰;在1375 cm-1处的羧酸类O—H弯曲振动吸收峰;在1029 cm-1处的醇类或酚类C—O伸缩振动吸收峰;以及在529 cm-1处和在474 cm-1处的C—Cl和C—Br伸缩振动吸收峰(Li et al.,2014,Peng et al.,2015).表明提纯前后的腐殖酸都有类似的结构组成.
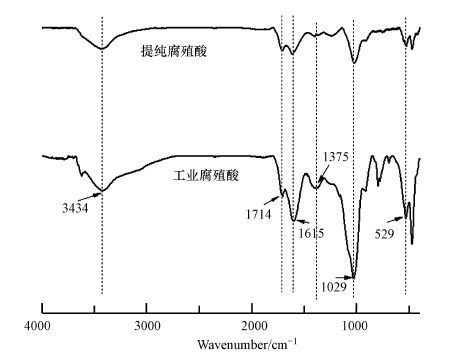 |
| 图 3 工业腐殖酸提纯前后的红外光谱图 Fig. 3 FTIR spectrum of industrial humic acid before and after purification |
两个不同浓度的泰乐菌素在工业腐殖酸和提纯腐殖酸上的吸附动力学见图 4,吸附的pH值为3.0.从图中可见,0.5、10 mg·L-1泰乐菌素在两种腐殖酸上表现出了相近的动力学行为:吸附达到完全动态平衡的时间均为24 h,吸附试验初始的0~3 h是一个快速吸附的过程,泰乐菌素的吸附量迅速上升达到总吸附量的60%;之后吸附速率逐渐减慢,在12 h时已基本达到平衡,此后吸附量随着时间的继续增加而略微增加直至达到吸附平衡.
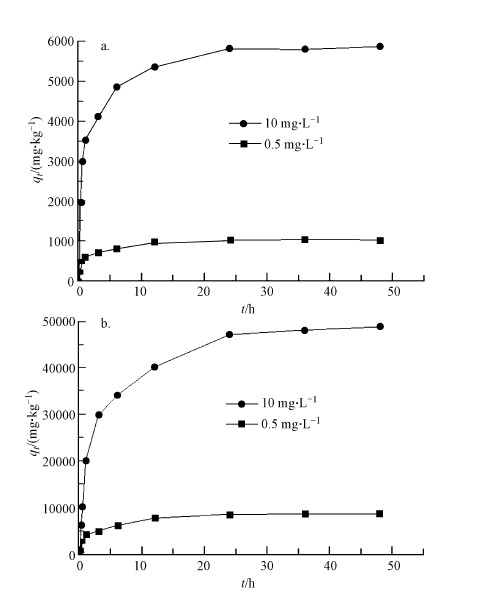 |
| 图 4 工业腐殖酸(a)和提纯腐殖酸(b)对泰乐菌素的吸附动力学 Fig. 4 Effect of initial concentration on the sorption kinetics of tylosin on industrial humic acid (a) and purification humic acid (b) |
分别用拉格朗日一级和二级动力学模型对泰乐菌素在工业腐殖酸和提纯腐殖酸上吸附的动力学数据进行拟合,拟合参数见表 2.结果表明:拉格朗日一级动力学方程的R2在0.776~0.972之间,拟合效果较差.而拉格朗日二级动力学模型拟合效果较好, R2均在0.998以上.且泰乐菌素浓度越高,吸附速率k2越小,可能的原因是:当泰乐菌素初始浓度很高时增大了分子间的碰撞几率,从而延长了泰乐菌素与吸附剂活性位点结合的时间(Chakraborty et al.,2014).
| 表 2 泰乐菌素在工业腐殖酸和提纯腐殖酸上吸附动力学的模型拟合 Table 2 The pseudo-first-order and pseudo-second-order sorption models constants of tylosin |
为了深入了解泰乐菌素在两种腐殖酸上的吸附过程,用颗粒扩散模型对吸附动力学进行拟合,拟合结果如图 5所示.从图中可以看出,颗粒扩散主要分为3个阶段(Li et al.,2013):外部扩散、界面层扩散和孔内扩散,外部扩散和界面层扩散进行迅速,提高泰乐菌素溶液的浓度有利于进行外部扩散和界面层扩散.这可能是与固液两相的浓度差及腐殖酸的结构有关,固液两相之间污染物的浓度在溶液与腐殖酸刚开始接触时相差较大,从而导致污染物从液相(高浓度)向固相(低浓度)迅速转移,短暂时间内污染物在固相吸附剂表面的孔隙结构上大量聚集,但吸附平衡没有到达.在相对稳定的平衡阶段之前,溶质会在弥散作用下重新分配(Zhao et al.,2012).
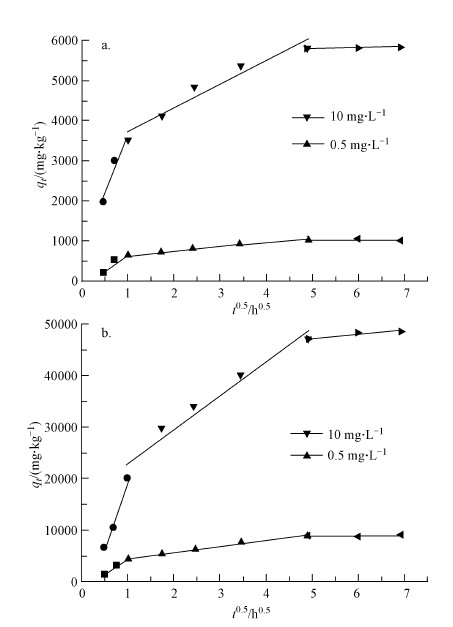 |
| 图 5 颗粒扩散模型对工业腐殖酸(a)和提纯腐殖酸(b)吸附泰乐菌素的拟合 Fig. 5 Intraparticle diffusion model with different initial concentrations of tylosin on industrial humic acid(a) and purification humic acid(b) |
吸附等温线可以描述一定温度下吸附过程达到平衡时溶质分子在两相中浓度之间的关系.提纯腐殖酸和工业腐殖酸样品对泰乐菌素的吸附等温线如图 6所示,吸附的pH值为3.0.吸附等温线分别用线性吸附模型、Freundlich吸附模型及Langmuir吸附模型进行拟合,拟合结果见表 3.
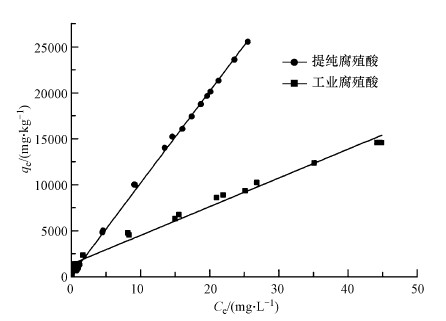 |
| 图 6 提纯腐殖酸和工业腐殖酸对泰乐菌素的吸附等温线 Fig. 6 Sorption isotherms of tylosin on purification humic acid and industrial humic acid |
| 表 3 提纯腐殖酸和工业腐殖酸对泰乐菌素的吸附等温线的拟合参数 Table 3 Sorption isotherm parameters of tylosin on purification humic acid and industrial humic acid |
从图 6中可以看出,提纯腐殖酸和工业腐殖酸在吸附平衡时的吸附量与溶液平衡浓度呈线性关系,且提纯腐殖酸的平衡吸附量比工业腐殖酸的平衡吸附量高70%,吸附明显增强.从表 3中吸附等温线的拟合参数可以看出,线性吸附模型和Freundlich吸附模型能够较好的拟合泰乐菌素在两种腐殖酸上的吸附,拟合的R2均在0.98以上.泰乐菌素在提纯腐殖酸和工业腐殖酸上的分配系数Kd分别是999.20 L·kg-1和302.56 L·kg-1,且工业腐殖酸吸附泰乐菌素的分配系数值远远小于提纯腐殖酸吸附泰乐菌素的分配系数.因此,腐殖酸对泰乐菌素的吸附可能与腐殖酸中的有机质含量有关,有机质含量越高,其对污染物的分配作用越强.Zhang等(2012)报道了诺氟沙星在风化煤提取腐殖酸上的吸附,发现诺氟沙星在腐殖酸上的吸附也可以用线性吸附模型和Freundlich吸附模型较好地拟合,拟合的R2都在0.98以上,且吸附的Kd为4949.5 L·kg-1.
在Freundlich吸附模型中,n值用来表征吸附的非线性程度.从表 3可知,工业腐殖酸提纯后其对泰乐菌素的吸附的n值从0.55上升到1.01,因此,工业腐殖酸提纯之后其对泰乐菌素的线性分配明显增强.因此,腐殖酸对泰乐菌素的吸附主要以线性分配为主(Lin et al.,2012).且两种腐殖酸对泰乐菌素的吸附等温线用Freundlich吸附模型拟合的R2均在0.98以上,可知两种腐殖酸吸附泰乐菌素是一个非均质的多分子层吸附过程.吸附过程中泰乐菌素首先占据腐殖酸上的高能吸附位点,当这些高能吸附位点被完全占据后,再由低能吸附位点进行吸附(Zhou et al.,2014).
3.4 pH值和离子强度对工业腐殖酸和提纯腐殖酸吸附泰乐菌素的影响泰乐菌素是一种离子型的有机物,在不同pH值下会以不同的形态存在,因此,溶液的pH值和离子强度会对其在腐殖酸上的吸附产生一定的影响.图 7为不同的pH值和离子强度对腐殖酸提纯前后吸附泰乐菌素的影响.从图 7可以看出,腐殖酸提纯前后对泰乐菌素的吸附随着pH值和离子强度的增加而逐渐减弱.
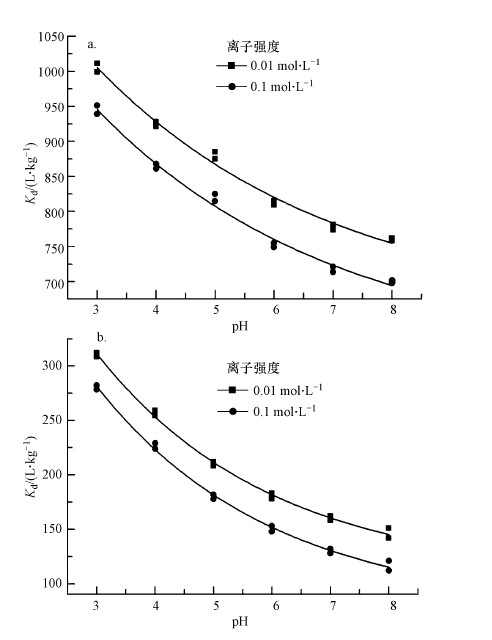 |
| 图 7 pH和离子强度对提纯腐殖酸(a)和工业腐殖酸(b)吸附泰乐菌素的影响 Fig. 7 Effects of ionic strength and pH on the sorption of tylosin on purification humic acid (a) and industrial humic acid (b) |
吸附随着pH的增加而降低可能与泰乐菌素在不同pH条件下的存在形态有关.当pH<7.1时,泰乐菌素主要以离子态TYL+形式存在,在酸性条件下,腐殖酸带有的官能团包括大量羧基、羟基和磺酸基等,这些基团往往会发生电离,从而和泰乐菌素通过氢键作用进行结合,而且带正电的腐殖酸和离子态的泰乐菌素之间也可能通过离子交换的形式进行结合(Li et al.,2014;Zhao et al.,2014).当pH>7.1,泰乐菌素主要以分子态TYL0形式存在,泰乐菌素在腐殖酸上的吸附可能通过疏水性作用(Ahmed et al.,2015).两种腐殖酸对泰乐菌素的吸附都随离子强度的增加而减小,主要是因为增加的离子会和泰乐菌素竞争腐殖酸表面上的活性吸附位点,从而不利于泰乐菌素的吸附(Doretto et al.,2014).
4 结论(Conclusions)1)工业腐殖酸经提纯后,其C、H、O、N、S的含量明显增加,灰分含量显著减小,且提纯腐殖酸和工业腐殖酸显示出相似的红外光谱特征.
2)工业腐殖酸提纯前后对泰乐菌素的吸附在24 h均可完全达到吸附平衡,吸附动力学可以用拉格朗日二级动力学和扩散模型较好的拟合.吸附等温线可以用线性吸附模型和Freundlich模型较好的拟合,两种腐殖酸对泰乐菌素的吸附存在明显的分配作用.
3)工业腐殖酸提纯后对泰乐菌素的吸附明显增强,吸附受溶液pH值和离子强的影响较大.泰乐菌素在两种腐殖酸上的吸附主要以分配作用、氢键作用和离子交换为主.
| [1] | Ahmed A A, Thiele-Bruhn S, Aziz S G, et al.2015.Interaction of polar and nonpolar organic pollutants with soil organic matter:Sorption experiments and molecular dynamics simulation[J].Science of the Total Environment, 508:276-287 |
| [2] | Chakraborty R, Karmakar S, Mukherjee S, et al.2014.Kinetic evaluation of chromium(VI) sorption by water lettuce (Pistia)[J].Water Science and Technology, 69:195-201 |
| [3] | Doretto K M, Peruchi L M, Rath S.2014.Sorption and desorption of sulfadimethoxine, sulfaquinoxaline and sulfamethazine antimicrobials in Brazilian soils[J].Science of the Total Environment, 476-477:406-414 |
| [4] | 郭凌, 卜玉山, 张曼, 等.2014.煤基腐殖酸对外源砷胁迫下玉米生长及生理性状的影响[J].环境工程学报, 8(2):758-766 |
| [5] | Guo X, Yang C, Dang Z, et al.2013.Sorption thermodynamics and kinetics properties of tylosin and sulfamethazine on goethite[J].Chemical Engineering Journal, 223:59-67 |
| [6] | Guo X, Yang C, Wu Y, et al.2014.The influences of pH and ionic strength on the sorption of tylosin on goethite[J].Environ Sci Pollut Res, 21:2572-2580 |
| [7] | Guo X, Ge J, Yang C, et al.2015.Sorption behavior of tylosin and sulfamethazine on humic acid:kinetic and thermodynamic studies[J].RSC Adv, 5:58865-58872 |
| [8] | Li J, Fu J, Xiang X, et al.2013.Kinetics, equilibrium, and mechanisms of sorption and desorption of 17 alpha-ethinyl estradiol in two natural soils and their organic fractions[J].Science of the Total Environment, 452:404-410 |
| [9] | Li Y, Niu J, Shang E, et al.2014.Effects of nitrate and humic acid on enrofloxacin photolysis in an aqueous system under three light conditions:kinetics and mechanism[J].Environmental Chemistry, 11:333-340 |
| [10] | Lian F, Sun B, Chen X, et al.2015.Effect of humic acid (HA) on sulfonamide sorption by biochars[J].Environmental Pollution (Barking, Essex:1987), 204:306-12 |
| [11] | Lin D, Tian X, Li T, et al.2012.Surface-bound humic acid increased Pb2+ sorption on carbon nanotubes[J].Environmental Pollution, 167:138-147 |
| [12] | Mutavdžic' Pavlovic' D, C'urkovic' L, Blažek D, et al.2014.The sorption of sulfamethazine on soil samples:Isotherms and error analysis[J].Science of the Total Environment, 497-498:543-552 |
| [13] | Peng H, Liang N, Li H, et al.2015.Contribution of coated humic acids calculated through their surface coverage on nano iron oxides for ofloxacin and norfloxacin sorption[J].Environmental pollution (Barking, Essex:1987), 204:191-198 |
| [14] | Zhang Q, Yang C, Dang Z, et al.2011.Sorption of tylosin on agricultural soils[J].Soil Science, 176:407-412 |
| [15] | Zhang Q, Zhao L, Dong Y H, et al.2012.Sorption of norfloxacin onto humic acid extracted from weathered coal[J].Journal of Environmental Management, 102:165-172 |
| [16] | Zhang Q, Yang C, Huang W, et al.2013.Sorption of tylosin on clay minerals[J].Chemosphere, 93:2180-2186 |
| [17] | Zhang Y, Ma X, Ran Y.2014.Sorption of phenanthrene and benzene on differently structural kerogen:Important role of micropore-filling[J].Environmental Pollution, 185:213-218 |
| [18] | Zhao L, Lin Z R, Dong Y H.2014.Sorption of cyromazine on humic acid:Effects of pH, ionic strength and foreign ions[J].Environ Sci Pollut Res, 21:2688-2696 |
| [19] | Zhao Y, Gu X, Gao S, et al.2012.Adsorption of tetracycline (TC) onto montmorillonite:Cations and humic acid effects[J].Geoderma, 183:12-18 |
| [20] | Zhou D, Chen B, Wu M, et al.2014.Ofloxacin sorption in soils after long-term tillage:The contribution of organic and mineral compositions[J].Science of the Total Environment, 497:665-670 |
 2016, Vol. 36
2016, Vol. 36


