2. 长春工程学院水利与环境工程学院, 长春 130012
2. School of Water Conservancy and Environment Engineering, Changchun Institute of Technology, Changchun 130012
随着厌氧氨氧化反应的发现,自然生态系统的氮循环过程被重新认识.长久以来,人们一直认为反硝化是自然界产生N2的唯一途径,直到厌氧氨氧化的发现打破了这个观念.厌氧氨氧化细菌首次在生物反应器中被发现(Mulder et al., 1995).在自然界中,厌氧氨氧化首次被发现于海洋沉积物中(Thamdrup et al., 2002),随后学者发现在加勒比海(Dalsgaard et al., 2003)和黑海(Kuypers et al., 2003)中广泛存在厌氧氨氧化细菌,海洋生态系统中存在大规模的厌氧氨氧化反应且该反应在全球海洋生态系统的氮损失中贡献率高达50%(Kuypers et al., 2005).厌氧氨氧化反应主要过程包括:NO2-被转化为中间产物NO,NO作为电子受体被还原为联胺(N2H4),N2H4被氧化成N2,NO2-被氧化成NO3-,避免N2O的产生并完成封闭的产N2循环(Strous et al., 2006;Kartal et al., 2011).N2O是强力的温室气体,其增温潜势在100年时间尺度上是CO2的298倍(Change IPOC,2007;Dalsgaard et al., 2003).大量研究表明,厌氧氨氧化在海洋生态系统广泛、规模性的发生.目前对厌氧氨氧化细菌的研究主要集中在海洋生态系统中,陆地和淡水生态系统中关于厌氧氨氧化细菌的报道还很少,且很少有关外源污染物较少的陆地和淡水生态系统厌氧氨氧化的报道.
青藏高原作为世界“第三级”,具有高海拔的显著特性,而且青藏高原人烟稀少,平均每平方公里不及4人,在高原自然环境发展演变的历史过程中,人为因素对自然环境的作用和影响较弱,有些地方还保留着天然的原始状况.青藏高原是我国开发程度较低的地区,自然资源的利用仍处于初期阶段.在这种外源污染物较少,氮污染负荷较低的情况下,是否仍然存在着广泛性的厌氧氨氧化反应还未知,因此,研究青藏高原表层不同类型土壤及沉积物厌氧氨氧化反应沿海拔梯度的分布特征和环境效应,将更加具有普遍性意义.研究结果将修正和完善氮循环过程理论体系,为全球性厌氧氨氧化反应的研究起到向导作用.
2 材料与方法(Materials and methods) 2.1 研究区概况青藏高原,中国最大、世界海拔最高并仍在隆升的一个高原.中国境内包括西南的西藏自治区、四川省西部及云南省部分地区,东北青海省的大部分地区、新疆维吾尔自治区南部及甘肃省部分地区.地理位置为北纬25°~40°,东经74°~104°,中国地区总面积为257万km2,平均海拔4000~5000 m,有“世界屋脊”和“第三级”之称.青藏高原是亚洲许多大河的发源地,长江、黄河、澜沧江、怒江、雅鲁藏布江等都发源于此,水力资源丰富.青藏高原受人为影响较少,其沉积物污染物较少、氮污染负荷较低.
在分析了大量背景资料和野外调查基础上,兼顾采样可行性和代表性,在青藏高原地区设置8个采样点(图 1)采集不同海拔高度(2000~5000 m)、不同深度(0~40 cm,每10 cm样品分为一层)的土壤及沉积物样品进行研究.包括海拔为2725 m的林芝波密湿地沉积物及小麦田土壤样品各4个(0~40 cm);海拔为3875 m的昌都芒康河流沉积物及草地土壤样品各4个(0~40 cm);海拔4030 m的日喀则拉孜县溪流沉积物样品4个(0~40 cm)、小麦田土壤样品3个(0~30 cm);海拔5011 m的那曲那曲县河流沉积物样品及草地土壤样品各4个(0~40 cm).共计31个样品,其中,湿地样品16个,旱地样品15个.所有样品置于无菌自封袋中,冰盒保存带回实验室.部分理化指标及实验室模拟实验使用新鲜样品,另有部分样品冷冻干燥后保存于-80 ℃冰箱中用于DNA提取和后续分子生物学实验,剩余样品存放于4 ℃冷库保存.
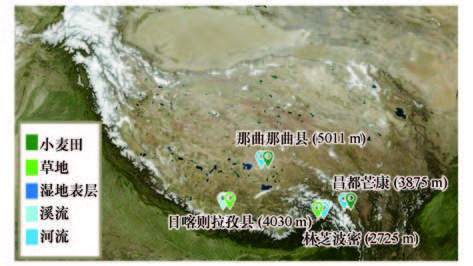 |
| 图1 采样点布设 Fig.1 Geographical distribution of sampling sites |
对土壤样品氨氮(NH4+-N)、硝氮(NO3--N)和亚硝氮(NO2--N)的测定参考《土壤农化分析》中的方法,经2 mol · L-1 KCl溶液浸提、0.45 μm微孔滤膜过滤后,用连续流动分析仪(SAN plus,Skalar Analytical B.V.,Breda,the Netherl and s)测定(鲍士旦,2000).向土壤中加入超纯水使土壤与水的质量比为1 ∶ 5后测定土壤的pH值.测定样品550 ℃的烧失量(LOI550)代表土壤总有机质(张文河等,2007).样品的所有理化指标都进行3次重复测定.
2.3 DNA提取和聚合酶链式反应(PCR)称取0.33 g左右经冷冻干燥处理的沉积物和土壤样品,使用FastDNA Spin Kit for Soil DNA提取试剂盒(MP Biomedicals,USA)提取样品中的总DNA,具体提取方法参照试剂盒使用说明.使用1%的凝胶电泳检测总DNA的质量,同时用NanoDrop 2000 UV-Vis Spectrophotometer(Thermo Fisher Scientific,USA)测定总DNA的浓度.
在厌氧氨氧化细菌研究中,分别对厌氧氨氧化细菌的16S rRNA基因和hzsB功能基因扩增.针对厌氧氨氧化细菌16S rRNA基因的扩增采用巢式 PCR 途径:首先使用引物pla46f(5′-GGATTAGGCATGCAAGTC-3′)和通用引物630r(5′-CAKAAAGGAGGTGATCC-3′)对浮霉菌属(Planctomycetes)进行PCR扩增(Juretschko et al., 1998;Neef et al., 1998);第二步则以第一步PCR产物作为模板,选用厌氧氨氧化细菌特异性引物Amx368f(5′- TTCGCAATGCCCGAAAGG-3′)和Amx820r(5′- AAAACCCCTCTACTTAGTGCCC -3′)对厌氧氨氧化菌16S rRNA进行全长PCR 扩增(Schmid et al., 2005).PCR反应体系为50 μL,其中,10×buffer 5 μL,2.5 mol · L-1 dNTP 4 μL,10 mmol · L-1正反向引物各1 μL(生工生物工程(上海)股份有限公司,上海),牛血清蛋白(BSA,20 mg · mL-1)0.5 μL,Taq酶0.5 μL,DNA模板2 μL,用无核酸酶纯水补足至50 μL.PCR反应扩增程序见文献(Zhu et al., 2011).针对厌氧氨氧化菌hzsB功能基因的扩增PCR方法:采用了新设计的针对羟铵合成酶hzsB功能基因的引物HSBeta396f/HSBeta742r进行扩增,PCR扩增的体系和程序见文献(Wang et al., 2012;Kartal et al., 2011;Harhangi et al., 2012).
2.4 克隆、测序和系统发育分析PCR扩增产物用Promega Agarose Gel DNA纯化试剂盒(Promega Corporation,USA)切胶纯化回收,将回收的PCR扩增产物与pGEM-Teasy载体(Promega Corporation,USA)连接后,转入JM109感受态细胞(Takara Bio Company,大连).涂布于Luria-Bertani(LB)固体培养基上于37 ℃培养12 h,然后进行蓝白斑筛选.随机选取合适数量的白色克隆子,采用菌落PCR扩增的方法鉴定阳性克隆,所用引物为pGEM-T Easy Vector通用引物T7(5′-TAATAC GACTCACTATAGGG-3′)和SP6(5′-ATTTAGGTGA CACTATAGAA-3′)(生工生物工程股份有限公司,上海).应用DNASTAR软件对测序结果进行编辑,去除载体序列后得到的基因序列在GenBank数据库中进行BLAST比对,并选取相关参比序列,使用Clustal_X程序进行序列对齐,应用MEGA5软件以邻接法(Neighbor-Joining)构建系统发育树.操作分类单元(OTU)利用DOTUR软件进行划分.
2.5 定量PCR分析采用实时荧光定量PCR方法对土壤样品中厌氧氨氧化细菌进行定量分析,使用ABI 7300 Real-Time PCR System扩增仪(Applied Biosystems,CA,USA)进行定量扩增,定量方法为SYBR Green法.选择HSBeta396F/HSBeta742R引物对厌氧氨氧化细菌的hzsB基因进行特异性定量扩增(Wang et al., 2012;Kartal et al., 2011).定量PCR扩增体系为20 μL,其中SYBR Premix Ex Taq酶(Takara Bio Company,大连)10 μL,ROX 50(Takara Bio Company,大连)0.4 μL,牛血清蛋白BSA(Takara Bio Company,大连)0.4 μL,浓度为10 mmol · L-1的正反向引物(生工生物工程(上海)股份有限公司,上海)各1 μL,稀释10倍的土壤总DNA模板2 μL,用无核酸酶纯水补足至20 μL.使用ABI 7300 Real-Time PCR System扩增仪(Applied Biosystems,CA,USA)进行定量,并将拷贝数已知的质粒DNA按10倍梯度稀释,得到7个标准样品同时进行定量扩增,得到标准曲线.定量PCR结果用7300 SDS System 配套软件进行分析运算,得出厌氧氨氧化菌功能基因hzsB的丰度值.每个样品做3次平行,要求结果扩增效率在90%~110%之间,可决系数R2>0.98,溶解曲线为单一峰.
2.6 数据分析利用SPSS 19软件(Statistical Product and Service Solutions)进行相关性分析;利用Origin 8.0软件做图.
3 结果(Results) 3.1 青藏高原采样点基本理化指标青藏高原采样点土壤样品基本理化指标见图 2.从结果可以看出,青藏高原土壤样品理化性质相似,均为偏碱性土,除昌都芒康和那曲两地的河流样品,氨氮含量可达到20 mg · kg-1以上,其他地点氨氮含量较低,为0.581~4.265 mg · kg-1,说明青藏高原土壤样品受人为扰动较少,氮污染负荷较低,这也是选择青藏高原作为研究地点的主要原因.
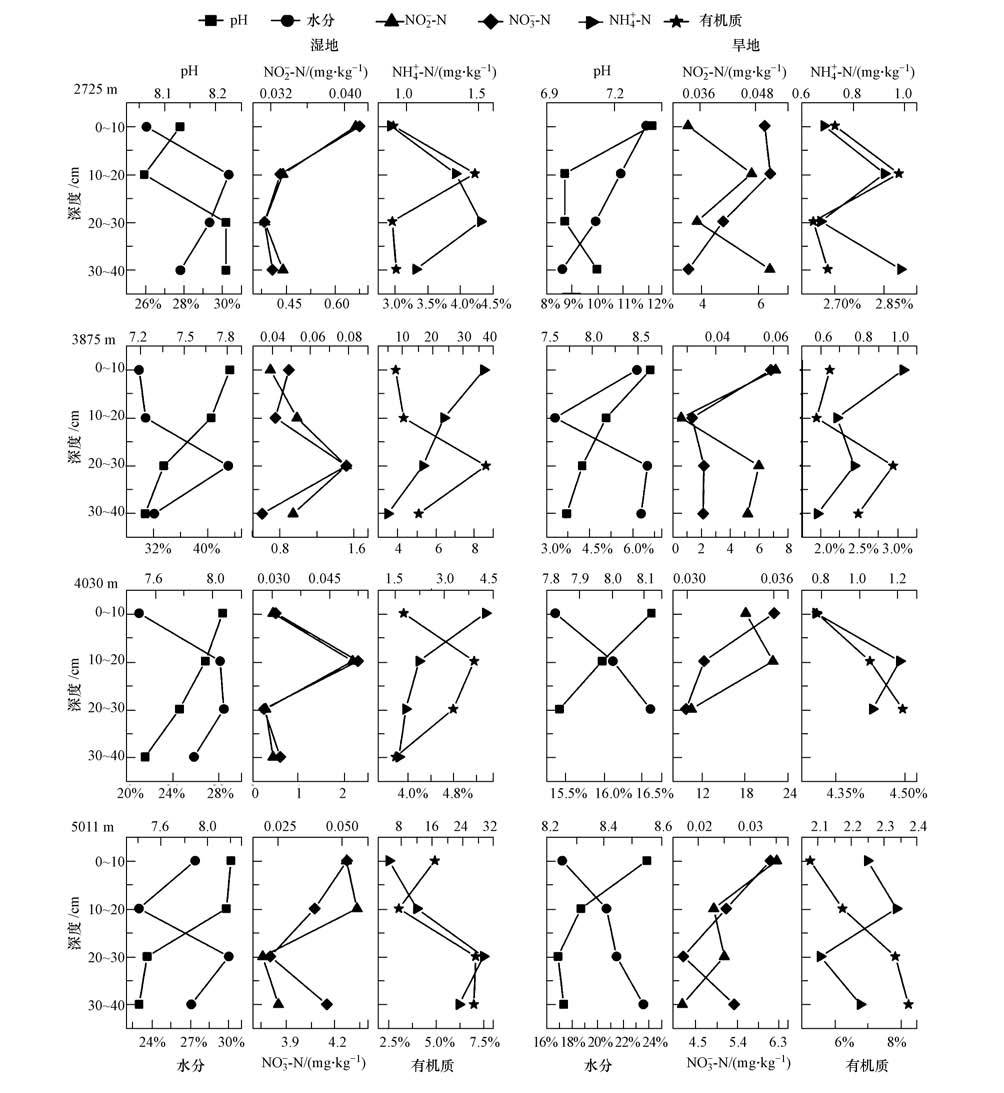 |
| 图2 青藏高原不同海拔梯度土壤样品基本理化指标 Fig.2 Chemical characteristics of the soil samples along altitude gradient in Qinghai-Tibet Plateau |
采用实时荧光定量PCR技术,对青藏高原8个采样点垂向样品的16个湿地沉积物、15个旱地土壤样品进行厌氧氨氧化细菌功能基因hzsB的定量分析,结果见图 3.在16个湿地沉积物样品中,海拔为4030 m的日喀则拉孜溪流4个样品和海拔为3875 m的昌都芒康河流第3层样品(20~30 cm)未检测到厌氧氨氧化细菌丰度,其余11个样品均能检测到厌氧氨氧化细菌丰度,说明厌氧氨氧化细菌在湿地系统中具有广泛存在性;在15个旱地土壤样品中,只有海拔为5011 m的那曲那曲草地的3个样品能够检测到厌氧氨氧化细菌丰度,说明在旱地系统中,也存在厌氧氨氧化细菌,只是其含量较低,可能低于仪器的检测限(2.28×103 copies · g-1,以干土计)而检测不到丰度.
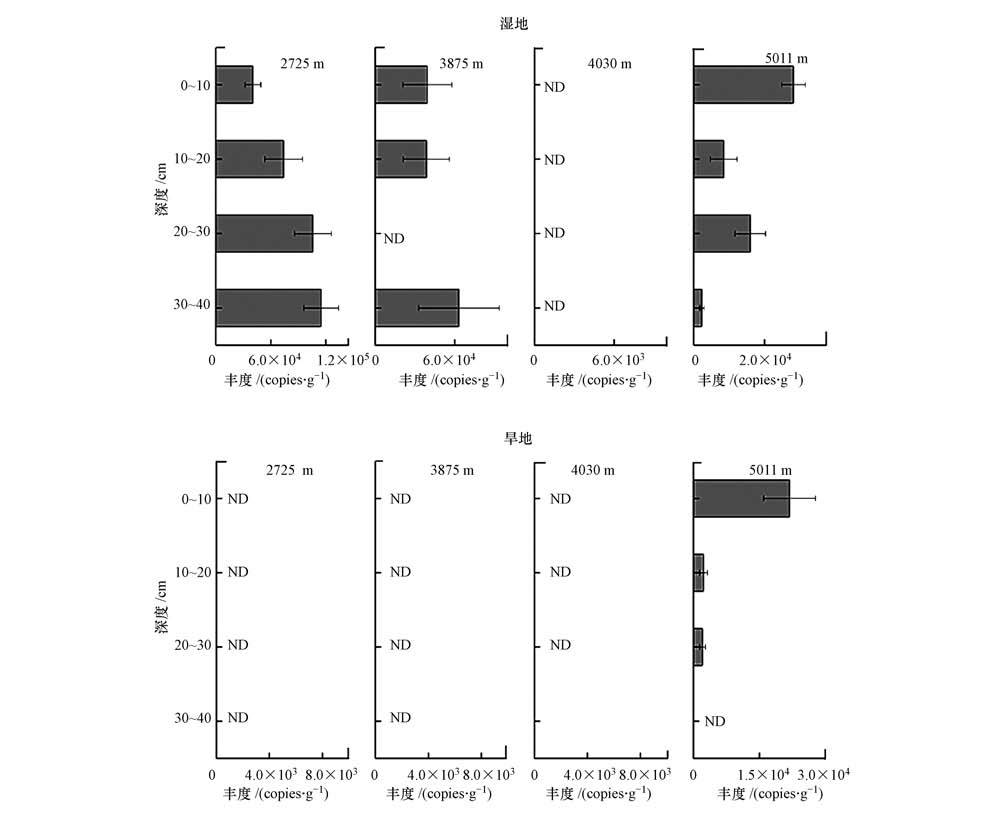 |
| 图3 青藏高原不同海拔梯度样品厌氧氨氧化细菌丰度(ND表示未检测到的样品) Fig.3 Abundance of anammox bacteria along altitude gradient in Qinghai-Tibet Plateau(Undetected samples are showed with ND) |
由青藏高原不同海拔的定量结果可以看出(图 3),海拔较低的2725 m的湿地样品厌氧氨氧化细菌丰度较高,可达105 copies · g-1(以干土计);而海拔较高的点厌氧氨氧化细菌丰度相对较低(2.06×103~6.31×104 copies · g-1,以干土计).在垂向尺度上,海拔为2725 m和3875 m的垂向样品,表层样品厌氧氨氧化细菌丰度低于底层;海拔为5011 m的垂向样品,表层样品厌氧氨氧化细菌丰度明显高于底层样品.
3.3 不同海拔高度厌氧氨氧化细菌生物多样性的变化在所采的4个地区16个湿地样品、15个旱地样品中,均能检测到厌氧氨氧化细菌16S rRNA.为研究青藏高原土壤样品厌氧氨氧化细菌的生物多样性,选取青藏高原不同海拔的4个地区湿地、旱地各4个表层(0~10 cm)土壤样品,通过DNA提取、定性 PCR扩增、克隆和测序等过程,获得湿地系统厌氧氨氧化细菌16S rRNA序列195个,旱地系统厌氧氨氧化菌16S rRNA序列192个.将所得序列在GenBank数据库中进行BLAST比对,结果表明其均与厌氧氨氧化菌16S rRNA序列相似.利用DOTUR软件对其进行生物多样性分析,在差异度0.03的条件下将湿地、旱地系统厌氧氨氧化菌序列相应划分为58、104个操作分类单元(OTU).另外得到湿地系统生物多样性的重要指数Shannon和Simpson值分别为3.07097和0.0137435,旱地系统Shannnon和Simpson值分别为4.34513和0.105181.数据结果表明,青藏高原土壤样品厌氧氨氧化细菌具有较高的生物多样性,且旱地系统生物多样性高于湿地系统.
为研究青藏高原土壤样品厌氧氨氧化细菌生物多样性沿海拔梯度的变化,按照海拔(2725、3875、4030、5011 m)递增的顺序依次获得47、53、47、48个湿地表层沉积物样品厌氧氨氧化细菌16S rRNA序列和51、48、46、47个旱地表层土壤样品厌氧氨氧化细菌16S rRNA序列.在差异度为0.03的条件下划分OTU,结果表明(图 4),海拔为2725 m的湿地样品生物多样性高于旱地系统;海拔为3875 m和5011 m处旱地系统生物多样性明显高于湿地系统;海拔为4030 m处旱地系统生物多样性略高于湿地系统.海拔为3875 m和5011 m的湿地样品厌氧氨氧化细菌生物多样性较低,而海拔为2725 m和4030 m的湿地样品厌氧氨氧化细菌生物多样性较高,表明青藏高原湿地系统厌氧氨氧化细菌的生物多样性与海拔的变化无明显关系;旱地系统厌氧氨氧化菌的生物多样性随着海拔高度的增高有上升趋势.
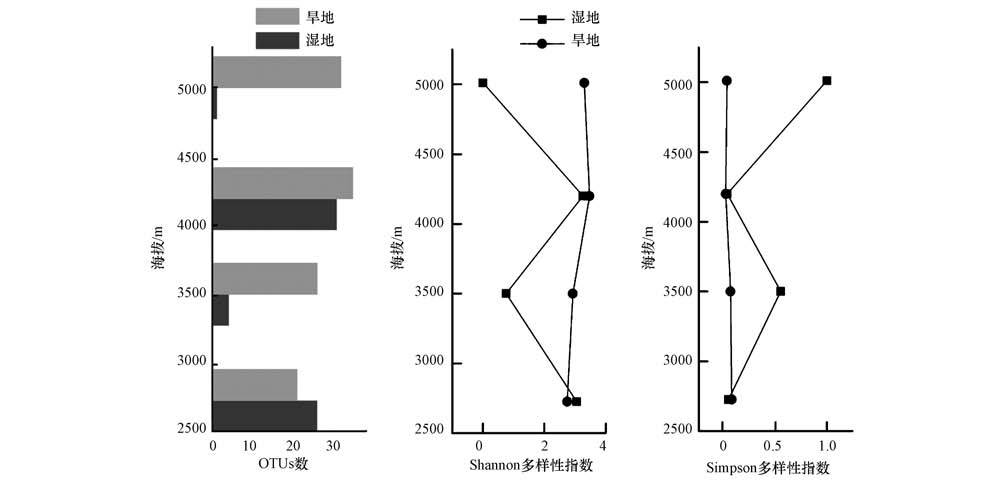 |
| 图4 不同海拔高度土壤样品中厌氧氨氧化细菌16S rRNA基因序列的生物多样性指数 Fig.4 Biodiversity indexes of anammox bacterial 16S rRNA gene sequences from soil samples of different altitude |
选取海拔高度为5011 m的那曲那曲湿地、旱地底层(30~40 cm)沉积物土壤样品研究不同深度样品厌氧氨氧化细菌生物多样性的分布,通过DNA提取、定性 PCR扩增、克隆和测序等过程,获得湿地沉积物样品厌氧氨氧化细菌16S rRNA序列53个,在差异度为0.03的条件下划分为2个OTU,Shannon、Simpson指数分别为0.562335和0.617647;获得旱地土壤样品厌氧氨氧化细菌16S rRNA序列50个,在差异度为0.03的条件下划分为33个OTU,Shannon、Simpson指数分别为3.26699和0.0367347.与表层样品比较可知(表 1),底层样品厌氧氨氧化细菌生物多样性略高于表层样品.
| 表1 不同深度土壤样品厌氧氨氧化细菌16S rRNA基因序列生物多样性指数 Table 1 Biodiversity indexes of anammox bacterial 16S rRNA gene sequences from soil samples of different depth |
对青藏高原湿地样品中厌氧氨氧化细菌16S rRNA基因序列的OTU代表序列和GenBank数据库中的相关序列进行系统发育树分析,结果见图 5.在差异度为3%的条件下划分OTU.由图 5可知,海拔为5011 m的那曲河流(cz29)厌氧氨氧化序列均包含在OTU8#中,分析得OTU8#与厌氧氨氧化菌 C and idatus Brocadia anammoxidans的同源性达到95%;对海拔为3875 m的昌都芒康河流(cz23)厌氧氨氧化序列分析发现,有73%的厌氧氨氧化序列与C and idatus Kuenenia stuttgartiensis同源性较高,有27%的厌氧氨氧化序列与C and idatus Brocadia anammoxidans的同源性较高;而对海拔为2725 m(cz19)和4030 m(cz34)的厌氧氨氧化序列分析发现,该采样点序列多数聚集在系统发育树第一、二个分支中,与我国南方稻田及大型根际土壤沉积物中厌氧氨氧化细菌相似度较高,与已知菌属的厌氧氨氧化细菌相似度较低,多数在85%~95%之间,猜想可能是新型的厌氧氨氧化细菌.
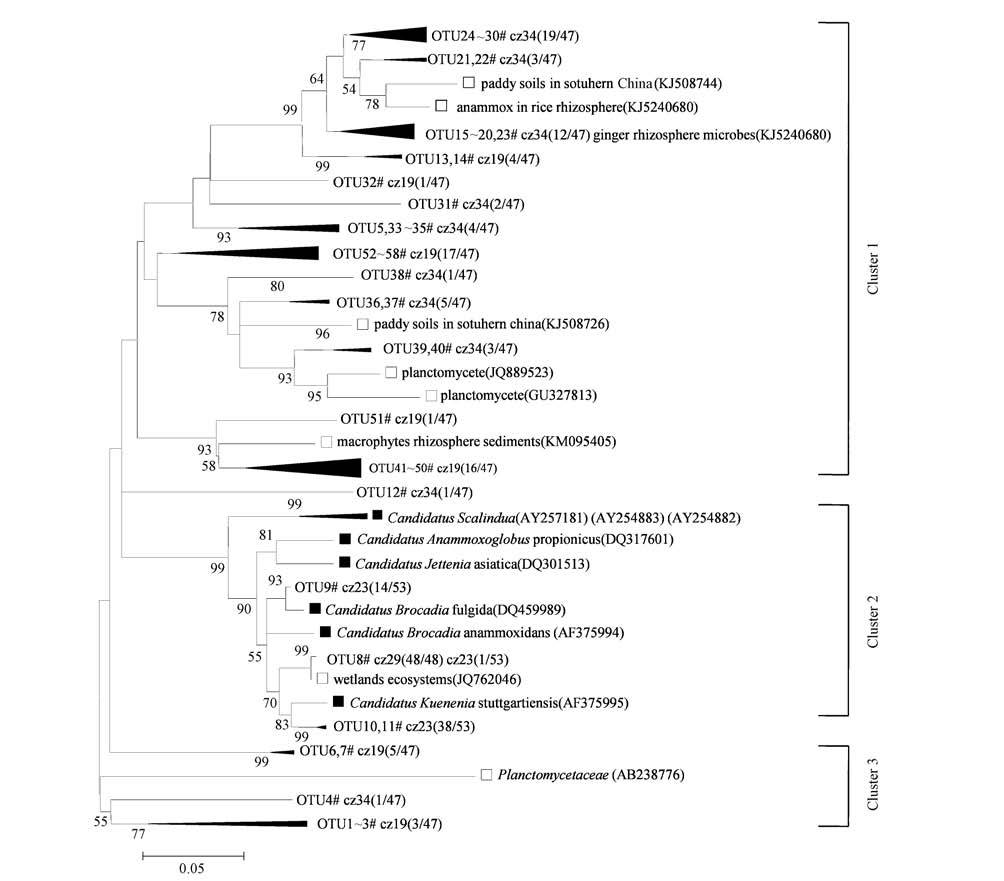 |
| 图5 湿地样品厌氧氨氧化菌16S rRNA系统发育树(青藏高原湿地样品中厌氧氨氧化细菌16S rRNA序列的分类操作单元以OTU开头表示,参比序列来自GenBank数据库,括号中字母和数字为序列提交序号,分支节点上的数字为每1000次Bootstrap分析所支持的概率,发育树左下方标尺表示5%序列差异的分支长度) Fig.5 Phylogenetic tree ofanammox bacteria16S rRNA sequences from wetl and soil samples(Anammox bacteria 16S rRNA sequences from wetl and soil samples of Qinghai-Tibet Plateauare begining with OTU,The reference sequences in this study were gained from GenBank; letters and numbers in brackets represent the sequences accession number; the numbers next to the nodes represent the bootstrap values of 1000 replications;the values less than 50 were not listed; the scale barat the bottom-left of phylogenetic tree represents 5 nucleotide substitutions per 100 nucleotides) |
对青藏高原旱地样品中厌氧氨氧化细菌16S rRNA基因序列的OTU代表序列和GenBank数据库中的相关序列进行系统发育树分析,结果见图 6.由图 6可知,旱地系统厌氧氨氧化细菌序列均属于浮霉菌属且多数序列(128个)聚集在第一个分支中,与我国南方稻田、水稻根际土壤等厌氧氨氧化细菌亲缘关系较近;以海拔为2725 m的林芝波密小麦田(cz41)为主的33条序列分布在第二个分支中,与已知菌种亲缘关系相对较近,但相似度仍低于95%,可能属于未分离或培养的区别于已知菌种的新型厌氧氨氧化细菌.研究发现不同海拔的序列大多数聚集在一起,但少数较为分散,说明青藏高原旱地生态系统中厌氧氨氧化菌异质性较低.
 |
| 图6 旱地样品厌氧氨氧化菌16S rRNA系统发育树(青藏高原旱地样品中厌氧氨氧化细菌16S rRNA序列的分类操作单元以OTU开头表示,参比序列来自GenBank数据库,括号中字母和数字为序列提交序号,分支节点上的数字为每1000次Bootstrap分析所支持的概率,发育树左下方标尺表示2%序列差异的分支长度) Fig.6 Phylogenetic tree ofanammox bacteria16S rRNA sequences from dryl and soil samples(Anammox bacteria 16S rRNA sequences from dryl and soil samples of Qinghai-Tibet Plateauare begining with OTU,The reference sequences in this study were gained from GenBank; letters and numbers in brackets represent the sequences accession number; the numbers next to the nodes represent the bootstrap values of 1000 replications;the values less than 50 were not listed; the scale barat the bottom-left of phylogenetic tree represents 2 nucleotide substitutions per 100 nucleotides) |
为了进一步验证青藏高原地区湿地、旱地生态系统厌氧氨氧化细菌为新型厌氧氨氧化细菌,选用特异性引物HSBeta396f和HSBeta742r对厌氧氨氧化细菌的功能基因hzsB进 行PCR扩增.发现所选8个采样点的表层样品均能检测到厌氧氨氧化细菌功能基因的存在.经分子生物学克隆检验,每个采样点选取5个阳性克隆子进行测序.返回序列进行BLAST比对,全部与厌氧氨氧化序列相似度较高(89%~99%).对所得到序列构建系统发育树(图 7).分析发现,青藏高原表层土壤样品厌氧氨氧化细菌序列多数(27个)聚集在第一个小分支中,与厌氧氨氧化细菌Brocadia属的同源性较高,说明该区域厌氧氨氧化细菌多数可能隶属于Brocadia属;有12个序列分布于第二个分支中,与厌氧氨氧化细菌Jetteia属同源性较高,进而证明了所监测到的青藏高原地区16S rRNA序列属于厌氧氨氧化细菌.从树图可以看出,青藏高原地区厌氧氨氧化细菌生物多样性较高,异质性相对较低,与16S rRNA序列分析结果相同.
 |
| 图7 青藏高原地区样品厌氧氨氧化菌hzsB系统发育树(青藏高原样品中厌氧氨氧化菌hzsB序列以CZ开头表示,参比序列来自GenBank数据库,括号中字母和数字为序列提交序号,分支节点上的数字为每1000次Bootstrap分析所支持的概率,发育树左下方标尺表示2%序列差异的分支长度) Fig.7 Phylogenetic tree ofanammox bacteria hzsB gene sequences from Qinghai-Tibet Plateau(Anammox bacteria hzsB gene sequences from Qinghai-Tibet Plateauare begining with CZ,The reference sequences in this study were gained from GenBank; letters and numbers in brackets represent the sequences accession number; the numbers next to the nodes represent the bootstrap values of 1000 replications;the values less than 50 were not listed; the scale barat the bottom-left of phylogenetic tree represents 2 nucleotide substitutions per 100 nucleotides) |
本研究为第一次报道在人为因素对自然环境影响较少的青藏高原湿地系统普遍存在厌氧氨氧化菌.对于重新认识陆地系统氮循环过程具有重要意义.
采用分子生物学方法对厌氧氨氧化菌生物多样性进行考察,全世界范围内已有很多报道.在海洋生态系统中,已有的厌氧氨氧化菌都严格隶属于Scalindus属(Schmid et al., 2005).在淡水系统中厌氧氨氧化菌的生物多样性也很低,例如,在坦噶尼喀湖中发现的厌氧氨氧化菌种C and idatus Scalindus brodae,在河流湿地沉积物中发现的厌氧氨氧化细菌多数隶属于Brocadia(Zhang et al., 2007).在本研究中发现,青藏高原地区厌氧氨氧化细菌的生物多样性较高,所监测到的厌氧氨氧化细菌部分隶属于Brocadia属,其余可能为未分离或培养的区别于已知菌种的新型厌氧氨氧化细菌,与Nie等(2015)研究结果相似,他们采用CARD-FISH证明了所监测到的16S rRNA序列属于厌氧氨氧化菌.
本研究通过探讨不同海拔厌氧氨氧化细菌生物多样性的变化规律,发现青藏高原地区旱地系统生物多样性高于湿地系统,可能是因为湿地系统厌氧氨氧化细菌丰度较高,优势菌种较为明显,生物多样性较低,与以往的研究中发现自然界中功能较强的生态系统中物种多样性往往很低相一致(Loreau et al., 2001);不同海拔高度厌氧氨氧化细菌生物多样性也有所不同,湿地系统中厌氧氨氧化细菌的生物多样性与海拔高度的变化无明显关系,但旱地系统厌氧氨氧化细菌的生物多样性随着海拔的递增呈上升趋势,与贺兰山不同海拔土壤微生物多样性变化趋势一致(刘秉儒等,2013);在垂向尺度上,厌氧氨氧化细菌生物多样性在不同深度也表现出差异且随着土壤深度的增加呈递增趋势.
本文通过定量PCR技术考察了厌氧氨氧化细菌在青藏高原的空间分布,结果表明,青藏高原沉积物土壤样品中厌氧氨氧化细菌丰度均低于1.05×1025 copies · g-1(以干土计),这与珠江河口沉积物(Wang et al., 2012a)、白洋淀沉积物(Zhu et al., 2013)和水稻田(Wang et al., 2012b)等淡水生态系统8.6×105~2.0×109 copies · g-1(以干土计)的厌氧氨氧化细菌丰度相比处于较低的水平.在湿地系统中,厌氧氨氧化细菌的丰度随着海拔的升高而降低,人类活动较多的地方厌氧氨氧化细菌丰度相对较高,这可能是由于近年来人类活动对自然氮循环的影响已经远远超过了其他因素(Vitousek et al., 1997;Canfield et al., 2010),所以人类活动对厌氧氨氧化细菌丰度存在一定的影响.以往研究发现,厌氧氨氧化细菌更喜好在有着高浓度并且稳定氮营养盐的沉积物中生存(Rysgaard et al., 2004),但在青藏高原低氨氮和硝氮的环境下仍然能够检测到厌氧氨氧化细菌,可能是因为厌氧氨氧化细菌有特殊的转运蛋白来调节NH4+和NO-的运输(van Niftrik et al., 2012).厌氧氨氧化细菌的NH42+转运蛋白(AmtB)和NO-转运蛋白(FocA、NarK)的特殊作用(Strous et al., 2006;Kartal et al., 2012; van Niftrik et al., 2012),可能使得厌氧氨氧化细菌在NH42+和NO-浓度较低的环境中也可以正常生存.垂向尺度上,海拔为2725 m的林芝波密湿地表层和海拔为3875 m的昌都芒康溪流样品,厌氧氨氧化细菌丰度为表层样品低于底层样品,其余样品厌氧氨氧化细菌丰度随着深度加深而降低,与前人研究结果一致(时玉等,2014).在海拔5000 m以上人类活动较少的地区湿地和旱地样品均能够检测到厌氧氨氧化细菌丰度,说明旱地系统也存在厌氧氨氧化细菌且厌氧氨氧化可能是地球固有的反应.
在厌氧氨氧化细菌丰度与环境变量相关性研究中,发现厌氧氨氧化细菌丰度与样品含水率和氨氮浓度呈正相关关系,与硝氮呈负相关关系,这可能与青藏高原土壤沉积物样品的特殊环境有关.另外需要考虑更多的环境和气候因素来研究影响厌氧氨氧化细菌丰度变化的机制,从而揭示厌氧氨氧化菌在青藏高原的群落多样性及分布规律.
| [1] | 鲍士旦. 2000.土壤农化分析[M].北京:中国农业出版社 |
| [2] | Canfield D E,Glazer A N,Falkowski P G. 2010. The evolution and future of earth's nitrogen cycle[J].Science,330(6001): 192-196 |
| [3] | Change IPOC.2007.Climate Change 2007: the Physical Science Basis[M].New York:Cambridge University Press |
| [4] | Dalsgaard T,Canfield D E,Petersen J,et al.2003.N2 production by the anammox reaction in the anoxic water column of Golfo Dulce,Costa Rica[J].Nature,422(6932): 606-608 |
| [5] | Harhangi H R,Le Roy M,Van Alen T,et al.2012.Hydrazine synthase,a unique phylomarker with which to study the presence and biodiversity of anammox bacteria[J].Applied and Environmental Microbiology,78(3): 752-758 |
| [6] | Juretschko S,Timmermann G,Schmid M,et al.1998.Combined molecular and conventional analyses of nitrifying bacterium diversity in activated sludge: Nitrosococcusmobilis and Nitrospira-like bacteria as dominant[J].Applied and Environment Microbiology,64(8): 3042-3051 |
| [7] | Kartal B,Maalcke W J,De Almeida N M,et al.2011.Molecular mechanism of anaerobic ammonium oxidation[J].Nature,479(7371): 127-130 |
| [8] | Kartal B,van Niftrik L,Keltjens J T,et al.2012.Anammox-Growth Physiology,Cell Biology,and Metabolism[M].Burlington:Academic Press.211-262 |
| [9] | Kuypers M M,Sliekers A O,Lavik G,et al.2003.Anaerobic ammonium oxidation by anammox bacteria in the Black Sea[J].Nature,422(6932): 608-611 |
| [10] | Kuypers M M,Lavik G,Woebken D,et al.2005.Massive nitrogen loss from the Benguela upwelling system through anaerobic ammonium oxidation[J].Proceedings of the National Academy of Sciences of the United States of America,102(18): 6478-6483 |
| [11] | 刘秉儒,张秀珍,胡天华,等.2013.贺兰山不同海拔典型植被带土壤微生物多样性[J].生态学报,33(22): 7211-7220 |
| [12] | Loreau M,Naeem S,Inchausti P,et al.2001.Biodiversity and ecosystem functioning: current knowledge and future challenges[J].science,294(5543):804-808 |
| [13] | Mulder A,Graaf A,Robertson L,et al.1995.Anaerobic ammonium oxidation discovered in a denitrifying fluidized bed reactor[J].FEMS Microbiology Ecology,16(3):177-184 |
| [14] | Neef A,Amann R,Schlesner H,et al.1998.Monitoring a widespread bacterial group: in situ detection of planctomycetes with 16S rRNA-targeted probes[J].Microbiology,144(12): 3257-3266 |
| [15] | Nie S A,Li H,Yang X R,et al.2015.Nitrogen loss by anaerobic oxidation of ammoniumin rice rhizosphere[J].The ISME Journal,3: 1-9 |
| [16] | Rysgaard S,Glud R N,Risgaard-Petersen N,et al.2004.Denitrification and anammox activity in Arctic marine sediments[J].Limnology and Oceanography,49(5): 1493-1502 |
| [17] | Schmid M C,Maas B,Dapena A,et al.2005.Biomarkers for in situ detection of anaerobic ammonium-oxidizing (anammox) bacteria[J].Applied and Environmental Microbiology,71(4): 1677-1684 |
| [18] | Schubert C J,Durisch-Kaiser E,Wehrli B,et al.2006.Anaerobic ammonium oxidation in a tropical freshwater system (Lake Tanganyika)[J].Environmental Microbiology,8(10): 1857-1863 |
| [19] | 时玉,孙怀博,刘勇勤,等.2014.青藏高原淡水湖普莫雍错和盐水湖阿翁错湖底沉积物中细菌群落的垂直分布[J].微生物学通报,41(11): 2379-2387 |
| [20] | Strous M,Pelletier E,Mangenot S,et al.2006.Deciphering the evolution and metabolism of an anammox bacterium from a community genome[J].Nature,440(7085): 790-794 |
| [21] | Thamdrup B,Dalsgaard T.2002.Production of N2 through anaerobic ammonium oxidation coupled to nitrate reduction in marine sediments[J].Applied and Environmental Microbiology,68(3): 1312-1318 |
| [22] | Van Niftrik L,Jetten M S.2012.Anaerobic ammonium-oxidizing bacteria: unique microorganisms with exceptional properties[J].Microbiology and Molecular Biology Reviews,76(3): 585-596 |
| [23] | Vitousek P M,Aber J D,Howarth R W,et al.1997.Human alteration of the global nitrogen cycle: sources and consequences[J].Ecological Applications,7: 737-750 |
| [24] | Wang S,Zhu G,Peng Y,et al.2012a.Anammox bacterial abundance,activity,and contribution in riparian sediments of the Pearl River estuary[J].Environmental Science & Technology,46(16): 8834-8842 |
| [25] | Wang Y,Zhu G B,Harhangi H R,et al.2012b.Co-occurrence and distribution of nitrite-dependent anaerobic ammonium and methane-oxidizing bacteria in a paddy soil[J].Fems Microbiology Letters,336(2): 79-88 |
| [26] | 张文河,穆桂金.2007.烧失法测定有机质和碳酸盐的精度控制[J].干旱区地理,(3): 455-459 |
| [27] | Zhang Y,Ruan X H,Op den Camp H J M,et al.2007.Diversity and abundance of aerobic and anaerobicammonium-oxidizing bacteria in freshwater sedimentsof the Xinyi River (China)[J]. Environmental Microbiology.9(9): 2375-2382 |
| [28] | Zhu G B,Wang S Y,Wang Y,et al.2011.Araerobic ammonia oxidation in a fertilized paddy soil[J].The ISME Journal,5(12): 1905-1912 |
| [29] | Zhu G B,Wang S Y,Wang W D,et al.2013.Hotspots of anaerobic ammonium oxidation at land-freshwater interfaces[J].Nature Geoscience,6(2): 103-107 |
 2016, Vol. 36
2016, Vol. 36


