2. 广平大学, 越南 广平 45000;
3. 华南农业大学资源环境学院, 广州 510006
2. QuangBinh University, QuangBinh, Vietnam 45000;
3. The College of Natural Resources and Environment of South China Agricultural University, Guangzhou 510006
近年来,随着抗生素的广泛使用,导致大量抗生素进入水体环境中(Richardson et al.,2005;武庭瑄等,2009).抗生素类药物水体环境污染问题已在国际上引起普遍的关注.其中四环素作为一种典型的抗生素,被广泛应用于动物的疾病预防与治疗、促进动物生长和提高畜禽生产效率(Sarmah et al.,2006).研究表明,只有少部分四环素在动物体内被吸附和代谢,50%~80% 的四环素以原药或母体化合物形式通过动物粪便排放到环境中(Kim et al.,2005;武庭瑄等,2008).四环素的积累对环境有一定的毒性,同时可能诱导病原菌产生抗药性以及新的抗药病原菌的出现(Schmitt et al.,2006;陈昦等,2008;焦少俊等,2008).
重金属污染作为另外一个严重的环境问题,一直备受关注(Zhong et al.,2010;李荣华等,2011;Hua et al.,2013),环境中重金属含量过高,对人类的身体健康和生存环境都将造成一定的威胁(毕士川等,2009).镉作为一种毒性较大的重金属,主要来源于农药、电镀废水的排放以及印染和纺织操作等(Xiong et al.,2009;周建兵等,2010).在镉污染区域,镉可以通过食物链的积累传递到人体中,长期接触镉对人体的肾、肺和骨骼都有不可恢复的伤害,甚至会导致癌症(Jouad et al.,2005).然而,四环素与镉的污染并不只是单一的污染问题,由于动物粪便的再利用、污水灌溉和工业废尘沉降等(Wan et al.,2010),四环素与重金属污染区域的重叠是不可避免的.因此,制备出一种对四环素和镉都具有较好的去除效果的材料变得尤为重要.
粘土矿物在自然界中分布广泛,具有价格低廉、比表面积大和稳定性高等特点,是一种应用广泛的吸附材料.如周建兵等(2010)利用十二烷基磺酸钠(SDS)修饰蒙脱石,研究了其对Cu2+和Cd2+的吸附性能,结果表明有机改性蒙脱石对重金属的吸附能力增强,对Cu2+和Cd2+的最大吸附量分别增加15.7%和15.5%.Liu等(2012)用3种不同烷基链长的季铵盐表面活性剂对蒙脱石进行修饰,探讨了其对四环素的吸附性能,研究表明有机蒙脱石的吸附效果较天然蒙脱石有较大的提高,在较低的pH环境下吸附效果最好.然而以往的研究主要是针对单一的重金属或有机物污染物,两性表面活性剂由于其独特的结构特点使其能够同时吸附重金属和有机污染物,在化学修饰剂的应用方面具有良好的发展前景.因此,本文拟以蒙脱石为基础,利用十二烷基二甲基甜菜碱(BS-12)作为改性剂,制得两性修饰蒙脱石;以批处理法研究两性修饰蒙脱石对四环素和Cd2+的吸附性能,同时考察pH、初始浓度和时间对四环素和Cd2+吸附的影响.利用XRD、FTIR、TG-DSC和Zeta potentials等表征手段研究改性蒙脱石的结构特征,结合结构特征和吸附性能分析其吸附机理.
2 实验部分(Experiments) 2.1 实验试剂蒙脱石原土(Mt)购买于广东省南海飞来峰非金属矿物有限公司,其阳离子交换容量(CEC)为0.8 meq·g-1;十二烷基二甲基甜菜碱(BS-12)、硝酸镉(Cd(NO3)2)购于上海阿拉丁试剂有限公司;氢氧化钠(NaOH)、盐酸(HCl)、氯化钠(NaCl)、氯化钾(KCl)、氯化钙(CaCl2)均为分析纯,购于广州化学试剂厂;去离子水为实验室自制.
2.2 材料制备用去离子水将蒙脱石洗涤干净,干燥磨碎后过200目筛,密封保存.取3 g提纯蒙脱石加入到60 mL去离子水中,配置成5%的悬浮液,然后超声10 min,向悬浮液中加入BS-12,直至nBS-12/mMt=2.28 mmol·g-1,在40 ℃的水浴条件下匀速搅拌24 h后,以7500 r·min-1的速度离心8 min,用蒸馏水洗涤3次;得到的材料在60 ℃烘箱内烘干,研磨过200目筛,密封保存;最终产品命名为BS-Mt.
2.3 材料表征XRD分析采用德国Bruker公司的D8 ADVANCE型号衍射仪,实验条件为:铜靶Kα射线源(λ=0.15418 nm),Lynx Exe阵列探测器,电压40 kV,电流40 mA,扫描步长0.02°,扫描速度17.7 s·步-1,扫描范围4~70°.测试样品为粉末状.红外光谱(FTIR)分析采用PerkinElmer公司的1725X红外光谱仪,扫描区间为4000~400 cm-1,采用KBr压片法制样.热重分析(TG-DSC)过程利用SDT Q600型号同步热分析仪,差热量程为100 μV,仪器分辨率为2 ℃,测量范围为室温至800 ℃,升温速率为5 ℃·min-1.Zeta 电位采用Nano ZS90型号Zeta电位分析仪测量,通过配备一定浓度的悬浮液在不同pH条件下测得.
2.4 实验设计与方法 2.4.1 对Cd2+的吸附试验准确称取0.0500 g Mt和BS-Mt分别加入至一系列含25 mL 浓度分别为10、20、50、80、100、120、150 mg·L-1 Cd 2+溶液的离心管中,充分混合,用0.01 mol·L-1的NaOH和HCl 溶液调节溶液pH为5.5,25 ℃恒温水浴震荡6 h至吸附平衡,4800 r·min-1离心8 min,取上清液用XGY-1011A型原子荧光光谱仪测定上清液中Cd2+残余浓度.同时测定不同反应时间(3、8、15、30、40、60、120、180、240、360 min,混合液pH为5.5,Cd2+浓度为50 mg·L-1,实验温度25 ℃)和不同实验温度(25、35、45、55 ℃,混合液pH为5.5,Cd2+浓度为50 mg·L-1,反应时间为6 h)下溶液中Cd2+残余浓度.
2.4.2 对四环素的吸附试验分别称取Mt和BS-Mt 各0.0050 g至一系列含25 mL 浓度分别为2、5、10、15、20、30、40、60 mg·L-1四环素溶液的离心管中,混合充分,用0.01 mol·L-1的NaOH和HCl溶液调节溶液pH为5.5.在避光条件下25 ℃恒温水浴反应6 h,4800 r·min-1离心8 min,取上清液用紫外分光光度计测定溶液中四环素残余浓度.同时测定不同反应时间(3、8、15、30、40、60、120、180、240、360 min,混合液pH为5.5,TC浓度为20 mg·L-1,实验温度25 ℃)、和不同实验温度(25、35、45、55 ℃,混合液pH为5.5,四环素浓度为20 mg·L-1,反应时间为6 h)下溶液中四环素残余浓度.
2.4.3 Cd2+与四环素共存试验将一定量的100 mg·L-1的Cd2+和50 mg·L-1的四环素溶液分别加入至一系列含0.0050 g Mt和BS-Mt的离心管中,用0.01 mol·L-1NaCl溶液定容至25 mL,使离心管中Cd2+和四环素的浓度分别为50 mg·L-1和20 mg·L-1.同时用0.01 mol·L-1的NaOH和HCl 溶液调节溶液pH为2、3、4、5、6、7、8、9.在避光条件下25 ℃恒温水浴反应6 h,4800 r·min-1离心8 min,取上清液分别测定不同pH条件下溶液中Cd2+和四环素的残余浓度.
3 结果与讨论(Results and dicussion) 3.1 材料表征 3.1.1 X射线衍射分析(XRD)如图 1所示为BS-Mt和Mt的X射线衍射分析图,Mt的001衍射峰尖锐而且对称,说明原始蒙脱石较为纯净,结构有序且结晶度较好.经过BS-12改性之后,其峰型变弱,衍射峰变宽,这可能是由于经BS-12修饰后材料的有序化降低,结晶度变差所导致.BS-12的d001为1.50 nm,与原始蒙脱石相比有略微降低,这可能由两方面的因素所导致:一是BS-12是一种有机表面活性剂,当其进入蒙脱石层间时因引力的减少容易导致层间结构发生轻微的坍塌和剥离现象(代亚平等,2012);二是BS-12分子可能是以平卧的方式进入蒙脱石层间,因为蒙脱石的层间电荷密度较低,且绝大部分是分布在八面体结构中,BS-12分子进入层间就有可能以all-trans 构型平行于蒙脱石片层排列(覃宗华等,2010;陈理想等,2015).另外,BS-Mt的主要衍射峰峰型并没有发生太大的变化,这说明经BS-12改性后蒙脱石的基本骨架并没有遭受到太大的破坏.
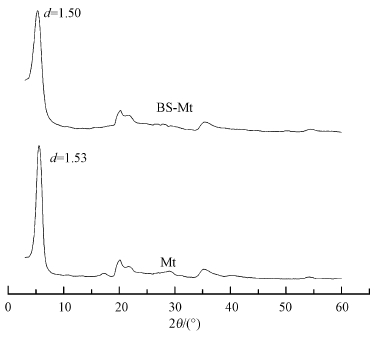 |
| 图 1 Mt和BS-Mt的XRD图 Fig. 1 X-ray diffraction of Mt and BS-Mt |
图 2所示为Mt和BS-Mt的红外光谱分析结果.在Mt的红外吸收光谱中,3620 cm-1和914 cm-1处分别为Al—OH的伸缩振动峰和弯曲振动峰;3426 cm-1和1641 cm-1处分别为水分子中—OH的伸缩振动峰和弯曲振动峰;1111 cm-1和1034 cm-1处的吸收峰为Si—O的伸缩振动;841 cm-1、518 cm-1和463 cm-1的吸收峰分别为Mg(Al)—OH、Si—O—Mg和Si—O—Fe的弯曲振动(Yu et al.,2012;龙航,2014).对比两个红外光谱图发现,经BS-Mt改性后,材料中关于蒙脱石的特征峰仍然存在,这说明BS-12的修饰并没有破坏蒙脱石的基本骨架;但材料中出现了新的吸收峰,2928 cm-1和2855 cm-1处的吸收峰为—CH2的伸缩振动;1407 cm-1处为—CH2 的弯曲振动峰;1327 cm-1 处为C—N 的伸缩振动峰;726 cm-1处为—CH2的变形振动峰(Zhaohui et al.,2008;Wu et al.,2012);以上这些吸收峰都表明,含有烷基链的BS-12成功负载到了蒙脱石上.
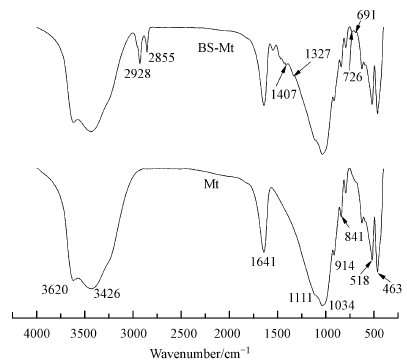 |
| 图 2 Mt和BS-Mt的红外光谱图 Fig. 2 Infrared spectra of Mt and BS-Mt |
热稳定性是评价材料实际应用的一个重要指标.图 3为Mt和BS-Mt的热重分析图,蒙脱石的失重过程主要为两个阶段,分别对应于差热曲线在120 ℃处的吸收峰,这是层间水逸出的过程,这一过程大概有12%的失重;在640 ℃处一个较强的吸收峰,这是粘土结构的内部脱羟过程,这一区间大概有3%的失重.总失重约为16%.改性蒙脱石的热分析结果与原始蒙脱石具有完全不同的特征,其层间水逸出引起的吸热峰偏移到了105 ℃附近,且其失重比例降为6%左右,这表明经改性后因BS-12进入蒙脱石层间导致其层间水减少;在355 ℃和480 ℃附近出现了原始蒙脱石的DSC图谱中不存在的吸热峰,说明此吸热峰属于一种新的成分或物相,这可能是层间BS-12分解逸出过程所导致;有机蒙脱石结构水脱羟过程的吸收峰从640 ℃降到了608 ℃附近,这说明BS-12进入了蒙脱石层间,导致蒙脱石结构发生了一些变化;其总失重约为18%,较原始蒙脱石失重较多,这可能是因为有机物进入蒙脱石层间,对粘土矿物的结构和热稳定性产生了一定影响(Xie et al.,2001;刘牛,2012).
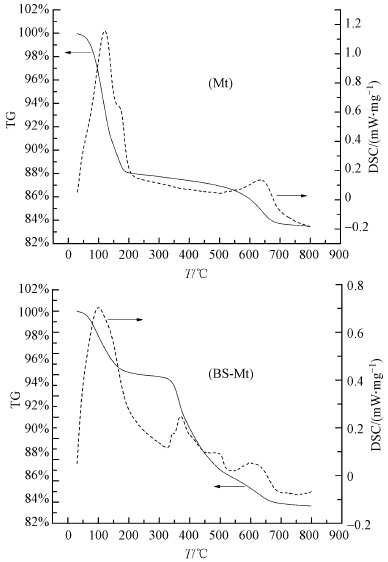 |
| 图 3 Mt和BS-Mt的TG-DSC曲线 Fig. 3 TG-DSC profiles of Mt and BS-Mt |
如图 4所示为Mt和BS-Mt在不同pH条件下的Zeta电位值.从图中我们可以观察到,Mt和BS-Mt在2~10的pH范围内都呈电负性,这说明Mt和BS-Mt表面都带有负电荷.Mt表面的负电荷主要是晶格中重金属的同类置换和表面断键水解作用所产生的(Wang et al.,2010).经过BS-12改性之后,矿物的Zeta电位在2.5~10的pH范围内较改性前有较大的降低,这可能是经改性后,BS-12分子的羧基裸露在蒙脱石表面,水解产生更多的负电荷,这为BS-Mt与目标污染物之间发生电荷吸附提供了更有利的条件(Meng et al.,2008).
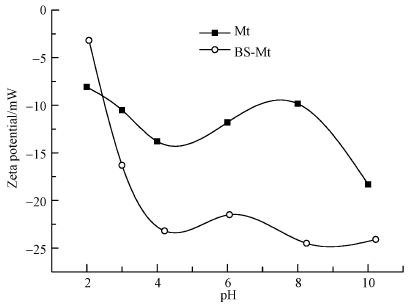 |
| 图 4 Mt和BS-Mt的Zeta电位随pH变化的曲线 Fig. 4 Influence of pH on the zeta potentials value of Mt and BS-Mt |
图 5所示为Mt和BS-Mt对Cd2+的吸附量随反应时间的变化值.Mt和BS-Mt对Cd2+的吸附行为表现出较高的相似度,吸附主要分为两个阶段,第一阶段为30 min内的快速反应阶段,这主要是因为吸附剂表面直接的电荷吸附以及孔结构引起的;随后,因为Cd2+吸附在粘土矿物表面及孔道内导致吸附位点减少和孔道堵塞,从而使吸附速率降低直至吸附达到平衡,两种吸附剂对Cd2+的吸附都在60 min左右达到了平衡.
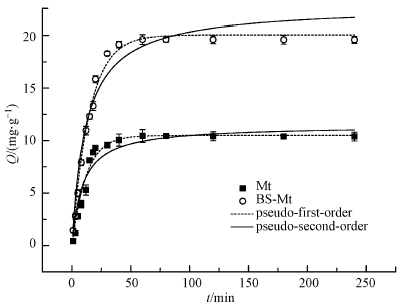 |
| 图 5 吸附时间的影响及吸附动力学 Fig. 5 Influence of adsorption time and adsorption kinetics |
利用准一级动力学方程和准二级动力学方程对实验数据进行拟合,以便更深的了解吸附剂与吸附质之间的吸附过程,拟合结果如表 2所示.准一级动力学方程对两种吸附剂的吸附数据拟合结果更好,其中可决系数分别达到0.9749和0.9921,同时经拟合的平衡吸附量与实验实际平衡吸附量很相近,所以准一级动力学方程更适合描述整个吸附过程.
| 表 1 吸附动力学拟合参数 Table 1 Adsorption kinetics fitting parameters for Cd2+ on Mt and BS-Mt |
| 表 2 等温吸附模型拟合参数 Table 2 Adsorption isotherm model fitting parameters for Cd2+ on Mt and BS-Mt |
为了探讨Cd2+与Mt和BS-Mt之间的平衡关系,研究了吸附剂对一系列不同浓度Cd2+的吸附行为,并利用Langmuir和Freundlich吸附模型对实验数据进行分析.如图 6所示为数据拟合图,从图中可以看出,随着Cd2+浓度的增大,矿物对Cd2+的吸附量逐渐增加,最后趋于平衡.这可能是因为随着Cd2+浓度的增大,矿物表面的吸附位点被占据,当达到饱和后吸附量很难再有较大的提高.
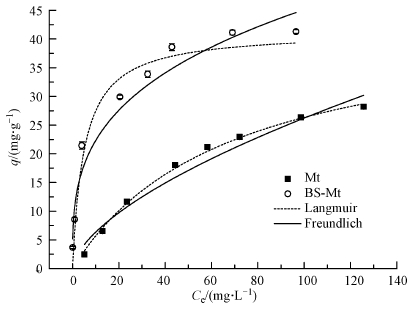 |
| 图 6 初始浓度的影响及等温吸附模型 Fig. 6 Effect of initial concentration and adsorption isotherms |
表 2所示为用Langmuir和Freundlich等温吸附模型对数据的拟合结果.根据可决系数可以知道,Langmuir吸附模型更符合Mt和BS-Mt对Cd2+的吸附.KL代表了矿物对Cd2+的亲和性,从表中可以知道,改性后蒙脱石对Cd2+的亲和性得到明显的提高,这与图 6中的实验结果一致.经过改性之后,矿物对Cd2+的最大吸附量由41.18 mg·g-1提高到了53.38 mg·g-1.这可能是经过BS-12改性后,蒙脱石表面的负电荷增多,提供了更多的吸附位点,所以吸附量增加;另外,BS-12的羧基和胺基能够与Cd2+形成五元环,通过螯合键与Cd2+相结合,从而提高了BS-Mt对Cd2+的吸附量(Meng et al.,2008).
3.2.3 温度对吸附的影响及吸附热力学为进一步研究Mt和BS-Mt对Cd2+的吸附机理,考察了温度为25 ℃、35 ℃、45 ℃、55 ℃时,Mt和BS-Mt对Cd2+的吸附行为.如图 7所示,随着温度的升高,Mt对Cd2+的吸附量呈下降趋势,而BS-Mt的吸附量基本维持不变,这表明经过BS-12改性后蒙脱石的应用范围变广,适应温度的能力变强.
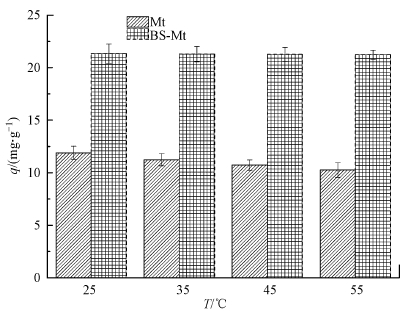 |
| 图 7 温度对Cd2+吸附的影响 Fig. 7 Effect of temperature of Cd2+ adsorption on Mt and BS-Mt |
对实验数据进行热力学拟合,如图 8所示,根据拟合结果和利用热力学公式计算出来的热力学参数如表 3所示.ΔH和ΔG值都为负值,表明Mt和BS-Mt 对Cd2+的吸附为放热反应,且吸附行为是自发进行的.ΔS值表明吸附过程中固液界面的混乱程度,其值为正,表明随着反应的进行,固液界面的混乱程度增加,BS-Mt对Cd2+吸附过程的ΔS值比Mt要大,表明BS-Mt对Cd2+的吸附过程更加剧烈(Ma et al.,2011).
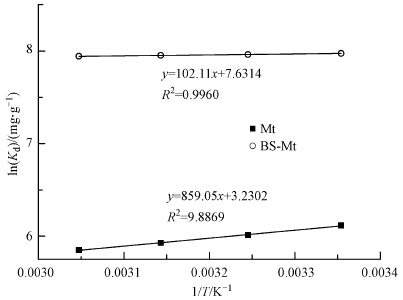 |
| 图 8 Mt和BS-Mt吸附Cd2+的热力学拟合 Fig. 8 Thermodynamic parameters for the adsorption of Cd2+ on Mt and BS-Mt |
| 表 3 Mt和BS-Mt吸附Cd2+的热力学参数 Table 3 Thermodynamic parameters for the adsorption Cd2+ on Mt and BS-Mt |
图 9所示为Mt和BS-Mt对四环素的吸附量随时间变化的数据图以及利用准一级动力学方程和准二级动力学方程对数据进行拟合的效果图.如图所示Mt和BS-Mt对四环素的吸附在2 h左右已趋于平衡;吸附过程主要分为快速吸附阶段和慢速吸附阶段,前者在60 min内达到了最大吸附量的80%,后者因为孔道的堵塞以及表面吸附位点的占据导致吸附速度变得缓慢.
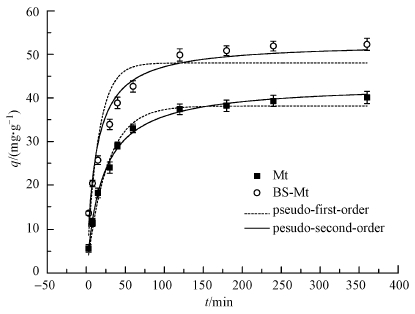 |
| 图 9 吸附时间的影响及吸附动力学 Fig. 9 Influence of adsorption time and adsorption kinetics |
表 4所示为利用动力学方程拟合所得数据,比较可决系数(R2)可知,准二级动力学方程可以很好的描述Mt和BS-Mt对四环素的吸附过程,且拟合所得的平衡吸附量与实验所得吸附量很接近.K2表示初始吸附速率,反应了四环素在矿物表面吸附的快慢,由此可知,经BS-12改性后提高了四环素的吸附速率和吸附容量.
| 表 4 吸附动力学拟合参数 Table 4 Adsorption kinetics fitting parameters for TC on Mt and BS-Mt |
图 10所示为利用Langmuir和Freundlich等温吸附模型对四环素浓度变化的实验数据进行拟合的结果.如图所示,随着四环素浓度的增加,吸附量逐渐增大,吸附剂表面的吸附位点趋于饱和,此时再增大四环素的浓度,吸附剂的吸附量不会再增加.表 5为Langmuir和Freundlich等温吸附模型的拟合参数.从表可知,Freundlich模型对Mt和BS-Mt吸附四环素的数据拟合效果较好,可决系数分别达到0.9913和0.9928.BS-Mt对四环素吸附所拟合得出的参数n和KF值都比原始蒙脱石吸附四环素所拟合的数值要高,分别从1.5501和6.5972提高到了2.1728和16.9439,这说明经BS-12改性后提高了蒙脱石内外表面对四环素的亲和力,这可能是因为BS-12结构中的疏水碳链之间形成有机相,四环素更容易被BS-Mt吸附.
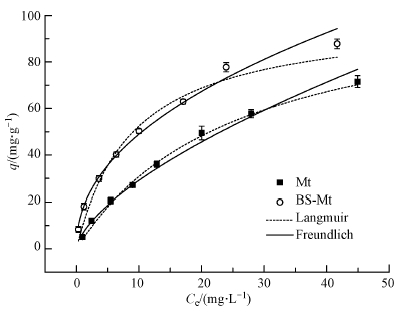 |
| 图 10 初始浓度的影响及等温吸附模型 Fig. 10 Effect of initial concentration and adsorption isotherms |
| 表 5 等温吸附模型拟合参数 Table 5 Adsorption isotherm model fitting parameters for Cd2+ on Mt and BS-Mt |
如图 11所示为分别在25 ℃、35 ℃、45 ℃、55 ℃下Mt和BS-Mt对四环素的吸附行为.由图 11可知,随着温度的升高,Mt对四环素的吸附效果缓慢的下降,而BS-Mt对四环素的吸附效果基本没什么变化.这表明改性后蒙脱石受温度的影响较小,提高了蒙脱石在较高温下的使用性能.
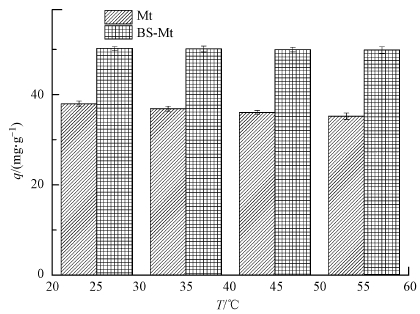 |
| 图 11 温度对四环素+吸附的影响 Fig. 11 Effect of temperature of TC adsorption on Mt and BS-Mt |
图 12所示为在不同温度下Mt和BS-Mt对四环素吸附的热力学拟合图,根据拟合数据并利用热力学方程计算得到如表 6所示的热力学参数.ΔH为负值,表明对四环素的吸附过程是放热反应,随着温度升高,吸附效果变差.ΔG为负值表明对四环素的吸附过程是自发进行的.ΔS值的大小反应了固液界面的混乱程度,两种材料对四环素吸附过程的ΔS值都为正且BS-Mt的值较大,表明随着反应的进行固液界面的混乱程度增加,且BS-Mt对四环素的吸附过程更剧烈(Ma et al.,2011).
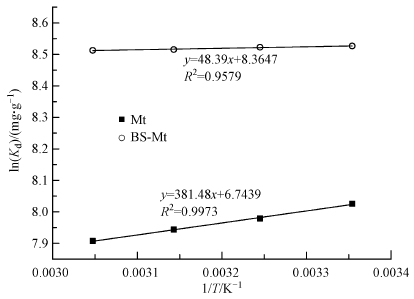 |
| 图 12 Mt和BS-Mt吸附四环素的热力学拟合 Fig. 12 Thermodynamic parameters for the adsorption of TC on Mt and BS-Mt |
| 表 6 Mt和BS-Mt吸附四环素的热力学参数 Table 6 Thermodynamic parameters for the adsorption TC on Mt and BS-Mt |
为进一步探讨有机改性蒙脱石对Cd2+和四环素的吸附机理,同时探讨其对Cd2+和四环素的共同吸附效果,进行了有机改性蒙脱石对Cd2+和TC单独存在以及Cd2++TC复合体系在不同pH条件下的吸附实验.图 13所示为Cd2+和四环素共存以及Cd2+单一体系时Mt和BS-Mt对Cd2+吸附量随pH变化的情况.由图可知,随着溶液pH值的增大,Mt和BS-Mt对Cd2+的吸附量都有所增加,如pH为2时 Mt和BS-Mt对Cd2+的吸附量仅分别为4.8 mg·g-1和12.5 mg·g-1;而当pH为5时,却分别达到了13 mg·g-1和21.8 mg·g-1,这与H+和Cd2+的竞争吸附有关,当H+浓度减少时,吸附剂中的吸附位点去质子化,增加了Cd2+与吸附位点相结合的机会,所以吸附量增加.当pH大于7时,便会出现沉淀作用而去除Cd2+.另外在Cd2++TC复合体系中,Mt和BS-Mt对Cd2+吸附量明显比Cd2+单一体系要增加,这可能是在Cd2++TC复合体系中TC的存在会改变Cd在溶液中存在的形态,特别是容易形成Cd-TC复合体,而Cd-TC复合体对蒙脱石和改性蒙脱石的亲和性要高于Cd2+,所以吸附效果增加(Wan et al.,2008).
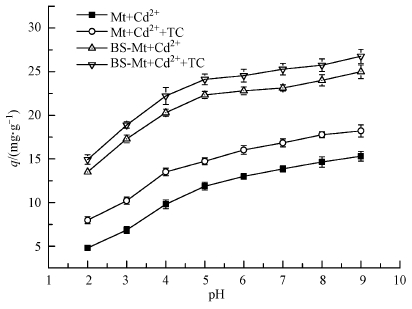 |
| 图 13 pH值对吸附Cd2+的影响(Cd2+单一体系和Cd2++TC复合体系) Fig. 13 Effect of pH on the adsorption of Cd2+ in pollutant single (Cd2+) and mixture (Cd2++TC) treatment, respectively |
图 14所示为TC单一体系和TC+Cd2+复合体系时Mt和BS-Mt对TC吸附量随pH变化的情况.由图可知,Mt和BS-Mt对四环素具有相似的吸附过程,吸附量都随着pH的升高而降低;pH在2~4范围内具有较高的吸附量;在4~5.5范围内有明显的下降趋势,在5.5~9范围内下降较为缓慢.四环素是一种四元弱酸,具有三个酸离解常数,分别为3.3、7.7和9.7,当pH<3.3时,四环素分子结构中的二甲氨基被质子化,主要以阳离子形式存在;当pH介于3.3~7.7范围内时,四环素分子中的酚二酮基团失去质子,形成两性离子,当pH为5.5时两性离子的比例达到最大;当pH>7.7时,三羧基基团和酚二酮基团失去质子,四环素主要以阴离子形式存在.当pH<3.3 时,四环素以阳离子形态存在,与Mt和BS-Mt发生强烈的静电吸附作用,因此在低pH条件下,具有较好的吸附效果;因为经改性后蒙脱石的表面电荷增多,因此BS-Mt对四环素的吸附效果较Mt有一定提高.当体系pH在5.5~7时,四环素基本不带电荷,与Mt和BS-Mt的静电作用力几乎可以忽略,因此吸附量降低.当体系pH在7~9时,四环素以阴离子形式存在,与Mt和BS-Mt有静电排斥作用,因此吸附量下降,但BS-Mt对四环素的吸附量仍大于Mt对四环素的吸附量,这是因为BS-12分子结构中含有一个C12的疏水碳链,碳链之间通过疏水键的相互作用,在BS-Mt表面形成一层有机相,使得四环素更容易被吸附,这是一种典型的物理吸附(Meng et al.,2008).同时可以发现,在TC+Cd2+复合体系中Mt和BS-Mt对四环素的吸附量要比TC单一体系要多,这是因为四环素含有氨基等基团,能与Cd2+发生反应,形成TC-Cd复合体,TC-Cd复合体与粘土矿物具有较高的亲和性;另外,在复合体系中可能存在阳离子桥联现象,即四环素可能吸附在已经吸附Cd2+的吸附位点上,Cd2+起到连接四环素和矿物颗粒的作用,因此在TC+Cd2+复合体系中对四环素的吸附效果增强(Gu et al.,2007).
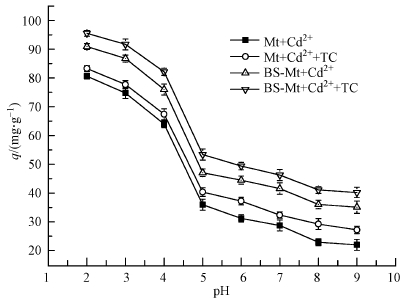 |
| 图 14 pH值对吸附四环素的影响(TC单一体系和TC+ Cd2+复合体系) Fig. 14 Effect of pH on the adsorption of TC in pollutant single (TC) and mixture (TC + Cd2+) treatment, respectively |
1) 表征结果表明,十二烷基二甲基甜菜碱(BS-12)插入了蒙脱石层间,其层间距有略微的变小,但基本结构没有太大变化,有机蒙脱石表面负电荷在pH为2.5~10范围内较原始蒙脱石增多,有利于吸附性能的提升.
2) Cd2+在Mt和BS-Mt上的吸附行为符合Langmuir等温吸附模型和准一级动力学方程,BS-Mt对Cd2+的吸附量较Mt的吸附量,有较大的提高,吸附机理主要为电荷吸附和螯合作用.
3) 四环素在Mt和BS-Mt上的吸附行为符合Freundlich等温吸附模型和准二级动力学方程,BS-Mt对四环素的吸附量和吸附速率都大于Mt,改性后BS-Mt对四环素的亲和力提高,吸附机理主要包括物理吸附和电荷吸附.
4) Cd2+在Mt和BS-Mt上的吸附量随pH的增大而升高,而四环素在Mt和BS-Mt上的吸附量受pH影响很大,随pH的升高而降低;在Cd2++TC复合体系中Cd2+与TC会形成复合体,因此对Cd2+和TC的吸附量比单一体系要大.
| [1] | 毕士川, 于慧娟, 蔡友琼, 等.2009.重金属Cd在不同水产品中的含量及污染状况评价[J].环境科学与技术, 32 (4):181–185. |
| [2] | 陈昦, 张劲强, 钟明, 等.2008.磺胺类药物在太湖地区典型水稻土上的吸附特征[J].中国环境科学, 28 (4):309–312. |
| [3] | 陈理想, 吴平霄, 杨林, 等.2015.有机改性蛭石的特性及其对Hg2+吸附性能的研究[J].环境科学学报, 35 (4):1054–1060. |
| [4] | 代亚平, 吴平霄.2012.3-氨丙基三乙氧基硅烷改性蒙脱石的表征及其对Sr(Ⅱ)的吸附研究[J].环境科学学报, 32 (10):2402–2407. |
| [5] | Gu C, Karthikeyan K, Sibley S, et al. 2007.Complexation the antibiotic tetracycline with humin acid[J]. Chemosphere, 66 : 1494–1051. |
| [6] | Hua X, Hu J, Jiang X, et al. 2013.Adsorption of Cd to natural biofilms in the presence of EDTA:effect of pH, concentration, and component addition sequence[J]. Environmental Science And Pollution Research, 20 (2): 1079–1088. |
| [7] | 焦少俊, 孙兆海, 郑寿荣, 等.2008.四环素在乌栅土中的吸附与解吸[J].农业环境科学学报, 27 (5):1732–1736. |
| [8] | Jouad E M, Jourjon F, Guillanton G L, et al. 2005.Removal of metal ions in aqueous solutions by organic polymers:use of a polydiphenylamine resin[J]. Desalination, 180 (1/3): 271–276. |
| [9] | Kim S, Eichhorn P, Jensen J N, et al. 2005.Removal of antibiotics in wastewater:Effect of hydraulic and solid retention times on the fate of tetracycline in the activated sludge process[J]. Environmental Science & Technology, 39 (15): 5816–5823. |
| [10] | 李荣华, 岳庆玲, 孟昭福, 等.2011.氨基改性SBA-15有序介孔材料对Cd(Ⅱ)的吸附热力学特征研究[J].环境科学学报, 31 (6):1241–1247. |
| [11] | 刘牛.2012. 蒙脱石的有机修饰及其对四环素的吸附[D].中国武汉:华中农业大学.34-35 |
| [12] | 龙航.2014. 乙胺改性粘土矿物对铯吸附性能的研究[D].中国广州:华南理工大学.24-25 |
| [13] | Liu N, Wang M, Liu M, et al. 2012.Sorption of tetracycline on organo-montmorillonites[J]. Journal Of Hazardous Materials, 225 : 28–35. |
| [14] | Ma B, Oh S, Shin W S, et al. 2011.Removal of Co2+, Sr2+ and Cs+ from aqueous solution by phosphate-modified montmorillonite (PMM)[J]. Desalination, 276 (1/3): 336–346. |
| [15] | Me ng, Z F, Zhang J N, Zhang Z Q. 2008.Simultaneous adsorption of phenol and cadmium on amphoteric modified soil[J]. Journal Of Hazardous Materials, 159 (2/3): 492–498. |
| [16] | Richardson B J, Larn P K S, Martin M. 2005.Emerging chemicals of concern:Pharmaceuticals and personal care products (PPCPs) in Asia, with particular reference to Southern China[J]. Marine Pollution Bulletin, 50 (9): 913–920. |
| [17] | Sarmah A K, Meyer M T, Boxal A B. 2006.A global perspective on the use, sales, exposure pathways, occurrence, fate and effects of veterinary antibiotics (VAs) in the environment[J]. Chemosphere, 65 (5): 725–759. |
| [18] | Schmitt H, Stoob K, Hamscher G, et al. 2006.Tetracyclines and tetracycline resistance in agricultural soils:Microcosm and field studies[J]. Microbial Ecology, 51 (3): 267–276. |
| [19] | 覃宗华, 袁鹏, 朱建喜, 等.2010.铝柱撑蒙脱石层间铝柱的表面硅烷功能化及其影响因素[J].矿物学报, (S1):149–150. |
| [20] | Wan Y, Bao Y, Zhou Q. 2010.Simultaneous adsorption and desorption of cadmium and tetracycline on cinnamon soil[J]. Chemosphere, 80 (7): 807–812. |
| [21] | 武庭瑄, 周敏, 郭宏栋, 等.2008.四环素在黄土中的吸附行为[J].环境科学学报, 28 (11):2311–2314. |
| [22] | 武庭瑄, 周敏, 万建新, 等.2009.膨润土和高岭土对四环素吸附的影响[J].农业环境科学学报, 28 (5):914–918. |
| [23] | Wa ng, T H, Liu T Y, Wu D C, et al. 2010.Performance of phosphoric acid activated montmorillonite as buffer materials for radioactive waste repository[J]. Journal Of Hazardous Materials, 173 (1/3): 335–342. |
| [24] | Wu P X, Dai Y, Long H, et al. 2012.Characterization of organo-montmorillonites and comparison for Sr(Ⅱ) removal:Equilibrium and kinetic studies[J]. Chemical Engineering Journal, 191 : 288–296. |
| [25] | Xie W, Gao Z, Pan W P, et al. 2001.Thermal Degradation Chemistry of Alkyl Quaternary Ammonium Montmorillonite[J]. Chemistry of Materials, 13 (9): 2979–2990. |
| [26] | Xiong C, Yao C, Wang L, et al. 2009.Adsorption behavior of Cd(Ⅱ) from aqueous solutions onto gel-type weak acid resin[J]. Hydrometallurgy, 98 (3/4): 318–324. |
| [27] | Yu X, Wei C, Ke L, et al. 2012.Preparation of trimethylchlorosilane-modified acid vermiculites for removing diethyl phthalate from water[J]. Journal Of Colloid and Interface Science, 369 : 344–351. |
| [28] | 周建兵, 吴平霄, 朱能武, 等.2010.十二烷基磺酸钠(SDS)改性蒙脱石对Cu2+、Cd2+的吸附研究[J].环境科学学报, 30 (1):88–96. |
| [29] | Zhao H L, Wei T J, Han L H. 2008.An FTIR investigation of hexadecyltrimethylammonium intercalation into rectorite[J]. Spectrochimica Acta, Part A (Molecular and Biomolecular Spectroscopy), 71 (4): 1525–1534. |
| [30] | Zhong K, Xu R K, Zhao A Z, et al. 2010.Adsorption and desorption of Cu(Ⅱ) and Cd(Ⅱ) in the tropical soils during pedogenesis in the basalt from Hainan, China[J]. Carbonates And Evaporites, 25 (1): 27–34. |
 2016, Vol. 36
2016, Vol. 36


