近年来,地下水中铁、锰、氨氮共存且严重超标的现象越来越普遍.铁、锰、氨氮共存于地下水超过限值时将引起严重的水质安全问题.当铁浓度高于0.5 mg·L-1时,水体会产生明显嗅味与颜色,影响感官;长期锰摄入过量,可能导致消化系统与骨骼疾病,锰中毒可导致神经系统缺陷,严重时会对神经系统造成永久性损害;氨氮浓度超标会导致自来水厂消毒过程消毒剂用量增加并产生令人厌恶的嗅和味.同时,被氧化的氨氮转化为硝氮、亚硝氮形态,尤其是形成的亚硝氮对人体健康造成的危害更大.因此,我国饮用水水质标准规定,饮用水中铁、锰、氨氮浓度最低限值分别为0.3、0.1和0.5 mg·L-1(陈正清等,2005;曾辉平等,2009a).因此,如何高效地实现地下水中铁、锰、氨氮的去除,已成为当前的一个研究热点.
国外有学者以改性活性炭作为吸附剂,发现吸附效果由强到弱依次为锰、铁、氨氮(Okoniewska et al., 2007).有学者尝试了用小型滴滤池同步去除铁、锰、氨氮,发现填料的颗粒大小及与之相关的填料比表面积对氨氮去除效果影响最为明显(Tekerlekopoulou et al., 2007).还有学者发现,当滤速高达24 m·h-1时,含铁、锰、氨氮的地下水经过填有附着生物膜的锰砂滤料的滤柱后出水仍能达标(Štembal et al., 2005).国内有学者在对生物过滤系统处理高铁锰、高氨氮地下水的研究中,开发了“接触氧化除铁+生物氧化除锰除氨氮”两级过滤工艺,该工艺使得地下水在10~12 m·h-1滤速下氨氮、铁、锰出水达标(曾辉平等,2009b).有学者初步研究表明,地下水中铁、锰、氨氮在去除过程中存在相互作用(汪洋等,2014).然而,NH4+-N在滤层中去除的动力学及NH4+-N氧化活化能的研究还未见报道.
因此,本文重点考察了石英砂滤料表面氧化膜去除NH4+-N的动力学方程,并研究滤层去除NH4+-N的活化能,以期为进一步增大去除NH4+-N的速率和净化含较高浓度NH4+-N的地下水提供基础依据及参考.
2 材料与方法(Materials and methods) 2.1 滤柱的启动与运行试验滤柱为直径100 mm、总高度3900 mm的有机玻璃柱.滤柱填充的滤料为化学方法挂膜成熟1年的滤料(化学方法挂膜指的是向水体中投加强氧化剂高锰酸钾将Fe2+、Mn2+分别氧化,生成溶解度较低的铁锰氧化物,铁锰氧化物被截留在石英砂的表面并逐渐形成一层具有催化氧化Fe2+、Mn2+及NH4+-N作用的铁锰氧化物膜).滤柱厚度130 cm,沿滤层高度方向设置11个取样口,取样过程先关闭滤柱底端的出水口,打开最底部的取样口,待水位上涨到从取样口溢流时,用聚乙烯塑料瓶接取溢流水样取样;之后,关闭该取样口,打开在这之上的第一个取样口,重复上述步骤,直到所有水样取完为止.滤柱在运行过程中均2天反冲洗1次,先进行气冲,气冲强度为15 L·s-1·m-2,时间2 min,接着气水同时冲洗,保持气冲强度不变,水冲强度4 L·s-1·m-2,时间4 min,最后进行8 min的强度为6 L·s-1·m-2的水冲.
滤柱启动前进水为来自西安市北郊的原水,水质指标见表 1.滤柱成熟后,配置一定浓度的Mn2+和NH4+-N溶液,通过加药泵投加进水,系统图见图 1.滤柱中水流流速为5 m·h-1.在各个水质指标测试时分别取3个平行水样测试.
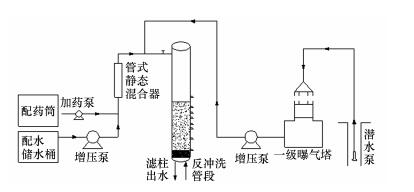 |
| 图 1 过滤工艺流程图 Fig. 1 The diagram of filter system |
| 表 1 原水水质 Table 1 Water quality of raw water |
改变进水NH4+-N浓度分别为1.6、2.1、2.5 mg·L-1,分别测试滤层厚度为7.5、15.0、22.5、30.0、37.5、45.0、52.5、67.5、97.5、127.5 cm处的NH4+-N浓度,按如下一级反应动力学方程对NH4+-N去除进行拟合:
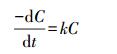
|
(1) |
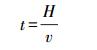
|
(3) |
对方程积分可得:
式中,C为NH4+-N浓度(mg·L-1),C0为进水NH4+-N浓度(mg·L-1),Ct为接触时间t时NH4+-N浓度(mg·L-1),H为滤层厚度(m),v为过滤速度(m·s-1),t为接触时间(s),k为速率常数(s-1).
2.3 滤层最大NH4+-N去除能力及NH4+-N氧化活化能的计算控滤速为5 m·h-1,考察滤层对NH4+-N的最大去除浓度.控制进水NH4+-N浓度为(2.1±0.2)mg·L-1,测试不同温度下NH4+-N浓度沿滤层厚度的变化,利用Arrhenius公式(4)求得反应的活化能.
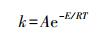
|
(4) |
式中,E为反应的活化能(kJ·mol-1),R取值为8.314472(J·mol-1·K-1),T为反应温度(K),A为频率因子(mg·L-1·s-1).
2.4 分析项目及方法试验中Fe2+、Mn2+、NH4+-N浓度、pH、DO的检测均采用标准方法(国家环境保护总局,2002).其中,Fe2+采用邻菲啰啉分光光度法测定,Mn2+采用高碘酸钾氧化光度法测定,NH4+-N采用纳氏试剂光度法测定,NO3--N采用紫外分光光度法测定,NO2--N采用N-(1-萘基)-乙二胺光度法测定,DO采用溶氧仪测定,pH值采用pH计测定.
3 结果与讨论(Results and discussion) 3.1 NH4+-N去除动力学方程的拟合地下水中NH4+-N在滤层中发生的反应如下:
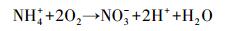
|
(5) |
相关研究表明,Mn2+、Fe2+在滤层中的去除速率分别和水中的Mn2+、Fe2+浓度呈一级反应关系,当水中的溶解氧浓度为1~10 mg·L-1,Mn2+在滤层中的去除速率与溶解氧浓度为零级反应,溶解氧在滤料表面的活性滤膜上占有的量为一定值(李圭白等,1989;Katsoyiannis et al., 2004).但NH4+-N在滤层中去除的动力学还未见报道.
通过改变不同的进水NH4+-N浓度分别为1.6、2.1、2.5 mg·L-1,进水溶解氧浓度为(8.6±0.1)mg·L-1,出水溶解氧浓度均大于2.5 mg·L-1.并且试验过程中不同温度下的实验数据均使用同滤柱测得,因此,石英砂的比表面积相差不大.对滤层中NH4+-N的去除进行一级动力学方程拟合,结果如图 2所示.可决系数R2=0.99884(可决系数越接近于1说明拟合效果越好),信概率p=1.17×10-9(置信概率越接近于0说明拟合效果越好).拟合结果表明,-log(Ct/C0)与接触时间t为线性关系,滤层中NH4+-N去除速率与水中NH4+-N浓度符合一级动力学关系;速率常数k与进水NH4+-N浓度无关.
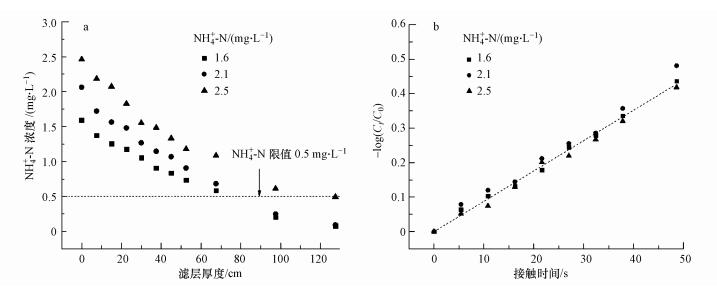 |
| 图 2 不同初始NH4+-N浓度下NH4+-N去除随滤层厚度的变化(a)及NH4+-N去除的一级动力学拟合曲线(b) Fig. 2 The changes of NH4+-N concentration with the filter depth (a) and the first-order kinetic model fitting for NH4+-N oxidation(b) under different influent ammonium concentrations |
保持进水流速为5 m·h-1,改变不同的进水NH4+-N浓度,不同进水NH4+-N浓度下各形态氮的去除情况如图 3所示.由图 3可知,进水NH4+-N浓度为1.93 mg·L-1,出水NH4+-N浓度为0 mg·L-1.当进水NH4+-N浓度为2.51 mg·L-1时,出水NH4+-N仍可达标.然而当进水NH4+-N浓度为2.63 mg·L-1时,出水NH4+-N浓度超标,滤柱对NH4+-N的最大去除能力为2.51 mg·L-1.不同进水NH4+-N浓度下,NO3--N浓度沿滤层厚度逐渐增加,NO2--N浓度沿滤层厚度先增大后减少.
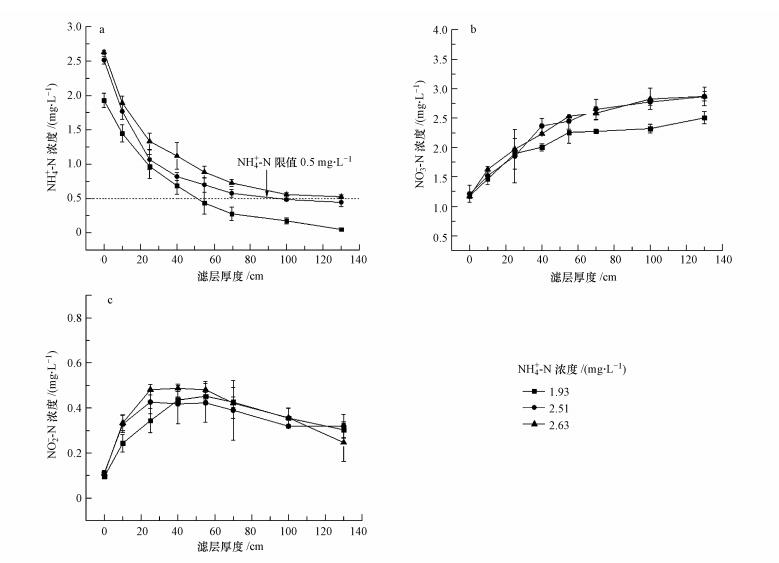 |
| 图 3 不同的进水NH4+-N浓度下NH4+-N(a)、NO3--N(b)和NO2--N(c)浓度随滤层厚度的变化 Fig. 3 The concentration profile of NH4+-N(a),NO3--N(b) and NO2--N(c) along the filter depth under different influent NH4+-N concentrations |
保持进水NH4+-N浓度在(2.1±0.2)mg·L-1,进水溶解氧浓度为(8.6±0.2)mg·L-1,出水溶解氧浓度大于2.5 mg·L-1,溶解氧浓度充足.改变不同的进水温度,NH4+-N在不同的进水温度下的去除情况如图 4所示.由图 4可知,进水NH4+-N浓度为(2.1±0.2)mg·L-1,进水温度为10.8、10.9 ℃时,出水NH4+-N浓度不达标.然而进水温度为12.4、14.0 ℃时,出水NH4+-N仍可达标.NH4+-N在滤层中的氧化为吸热反应,进水温度变低会导致出水NH4+-N浓度上升.
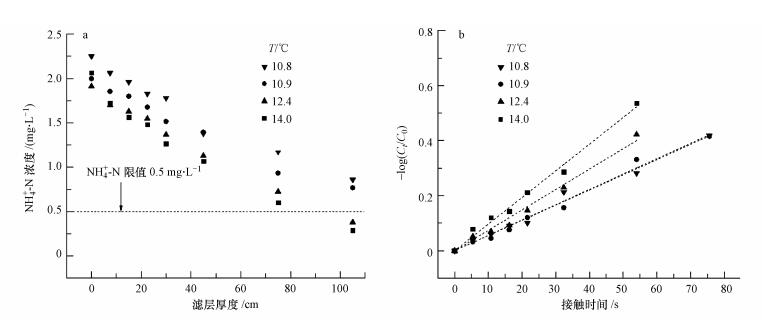 |
| 图 4 不同进水温度下NH4+-N浓度的沿层变化(a)及NH4+-N消耗与接触时间的线性回归分析(b) Fig. 4 The removal of ammonium(a) and the first-order kinetic model fitting for NH4+-N oxidation(b) under different temperature |
进一步分析不同温度下NH4+-N氧化的反应速率常数,结果如表 2所示.NH4+-N在不同进水温度中的消耗与接触时间的线性回归分析如图 4b所示.根据Arrhenius公式计算得NH4+-N氧化所需的活化能为96.8 kJ·mol-1(图 5).
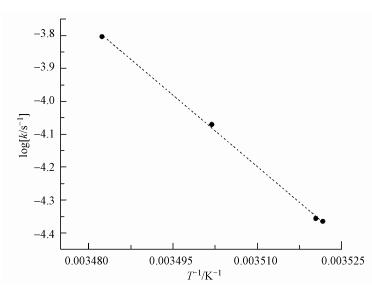 |
| 图 5 NH4+-N氧化阿伦尼乌斯方程图 Fig. 5 Arrhenius plots for the reaction rate of NH4+-N oxidation |
| 表 2 NH4+-N在不同进水Mn2+浓度、不同的进水温度的速率常数k Table 2 The rate constant k of ammonium removal with different initial manganese ion concentrations under different temperature |
从图 6中XRD峰位置的变化来判断活性滤膜中锰氧化物的组成,滤柱上层滤料和下层滤料上的滤膜主要组分为水钠锰矿(Ca、Mg)Mn14O27·xH2O,水钠锰矿可能对NH4+-N氧化具有催化作用.
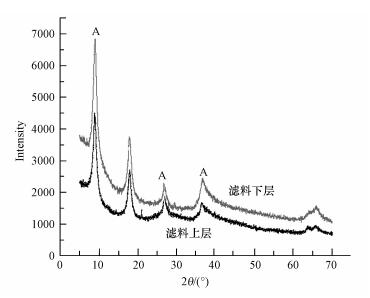 |
| 图 6 滤层滤料复合氧化膜的XRD图(A为水钠锰矿的特征峰) Fig. 6 XRD pattern of the co-oxide film from upper and lower filter layer |
NH4+-N在滤层中的氧化符合一级反应动力学方程.当进水流速为5 m·h-1时,滤层厚度为130 cm的成熟石英砂滤层对NH4+-N的最大去除浓度为2.51 mg·L-1,NH4+-N在滤层中的氧化速率常数随进水温度的降低而下降.当温度降低到10.9 ℃时,进水NH4+-N浓度为(2.1±0.2)mg·L-1,出水NH4+-N超标.NH4+-N氧化活化能的测试结果表明,NH4+-N在成熟石英砂滤层氧化所需的活化能为96.8 kJ·mol-1.XRD测试结果表明,滤柱上层滤料和下层滤料上的滤膜主要组份为水钠锰矿(Ca、Mg)Mn14O27·xH2O.
| [1] | 陈正清, 别东来, 钟俊.2005.不同滤料除铁除锰效果研究[J].环境保护科学, 31 (3):22–24. |
| [2] | 国家环境保护总局. 2002. 水和废水监测分析方法(第4版)[M]. 北京: 中国环境科学出版社 . |
| [3] | Katsoyiannis I A, Zouboulis A I. 2004.Biological treatment of Mn(Ⅱ) and Fe(Ⅱ) containing groundwater:kinetic considerations and product characterization[J]. Water Research, 38 (7): 1922–1932. |
| [4] | 李圭白, 刘超. 1989. 地下水除铁除锰(第2版)[M]. 北京: 中国建筑工业出版社 . |
| [5] | Okoniewska E, Lach J, Kacprzak M, et al. 2007.The removal of manganese,iron and ammonium nitrogen on impregnated activated carbon[J]. Desalination, 206 (1/3): 251–258. |
| [6] | Štembal T, Markic' M, Ribičic' N, et al. 2005.Removal of ammonia,iron and manganese from groundwaters of northern Croatia-pilot plant studies[J]. Process Biochemistry, 40 (1): 327–335. |
| [7] | Tekerlekopoulou A G, Vayenas D V. 2007.Ammonia,iron and manganese removal from potable water using trickling filters[J]. Desalination, 210 (1/3): 225–235. |
| [8] | 汪洋, 黄廷林, 文刚.2014.地下水中氨氮、铁、锰的同步去除及其相互作用[J].中国给水排水, 30 (19):32–35. |
| [9] | 曾辉平, 李东, 高源涛, 等.2009a.生物除铁除锰滤层的溶解氧需求及消耗规律研究[J].中国给水排水, 25 (21):37–40. |
| [10] | 曾辉平,李冬,高源涛,等.2009b.高铁高锰高氨氮地下水的两级净化流程[A]//《中国给水排水》第四届年会暨2009年给水厂污水厂升级改造及节能减排新技术新工艺研讨会论文集[C].苏州:《中国给水排水》杂志 |
 2016, Vol. 36
2016, Vol. 36


