2. 中国科学院生态环境研究中心环境水质学国家重点实验室, 北京 100085
2. Key Laboratory of Aquatic Science and Technology, Research Center for Eco-Environmental Sciences, Chinese Academy of Sciences, Beijing 100085
近年来,重金属污染日益严重,严重危害着生态安全与人类健康(罗志勇等,2009).金属开采、冶炼和电镀是造成重金属污染的重要原因.在上述行业生产过程中,通常采用氰基作为络合剂,因此,在工业生产过程中产生的废水中含有较多重金属和氰化物,而且氰化物能与重金属形成络合物(Jiraroj et al.,2006).目前处理重金属及氰化物的方法很多,诸如物化沉淀法、膜吸收法、芬顿试剂氧化法、生物法、光催化法、电化学法等(Hou et al.,2012;Gurol et al.,1985;White Daniel et al.,2000),上述方法在处理重金属及氰化物方面都具有一定的效果,但也存在相应的缺陷.例如,物化沉淀法需要添加大量化学试剂,且处理效果较差;单独光催化法中的光生空穴与光生电子容易发生复合,致使光催化效率低下;电化学氧化过程易出现电极钝化,电流效率较低.
近年来的研究表明,电化学法和光催化法的联合应用,较单独使用电化学与光催化更具优势.光电催化技术以光催化剂作为阳极,再施加一定偏压,能有效抑制光生电子与空穴的复合行为.较之单独使用光催化或电化学氧化技术,光电组合技术具有明显的协同催化降解污染物效果(陈佩仪等,2005),而且有效地省去了粉体光催化剂的繁琐分离回收过程;此外,半导体光催化剂在光解水制氢(Kudo et al.,1999)及光催化降解污染物(Kutsuna et al.,1999;Sehested et al.,2005;Zhang et al.,2006)等方面具有重要应用前景,已得到越来越多研究者的关注.
目前,常用的光催化阳极材料包括TiO2(Tada et al.,2011)、ZnO(Xu et al.,2011)等.TiO2纳米管与TiO2颗粒膜电极相比,具有较大的比表面积及量子化学效应,因而TiO2纳米管对光催化氧化去除污染物具有更高的活性.近年来,石墨烯(GO)等碳材料在纳米器件、传感器等方面受到了广泛关注.GO是一种新型的碳质薄膜材料,具有稳定结构、高比表面积及独特层状结构的特性(Peter et al.,2009).基于此,本文通过电化学方法将GO修饰到TiO2纳米管表面,用作光阳极,进行对铜氰络合物光电催化氧化去除性能的研究.
2 材料与方法(Materials and methods) 2.1 材料与主要试剂钛片购自北京恒力钛公司;氢氟酸(HF)、硝酸(HNO3)、硫酸铵((NH4)2SO4)、氟化铵(NH4F)、丙三醇(C3H8O3)、丙酮(C3H6O)、硫酸钠(Na2SO4)、氰化钠(NaCN)、氰化亚铜(CuCN)、异烟酸(C6H5NO2)、巴比妥酸(C4H4N2O3)、氯胺T(C7H7ClNNaO2S·3(H2O))、磷酸(H3PO4)、磷酸二氢钾(KH2PO4)、碘化汞(HgI2)、碘化钾(KI)、酒石酸钾钠(C4H4KNaO6·4H2O)、30%过氧化氢(H2O2)、无水乙醇(C2H6O)等均为AR级.
2.2 实验装置及主要仪器实验装置图参考文献(杨桂蓉等,2014),具体见图 1.包括石英反应器(长4.0 cm、宽4.0 cm、高7.0 cm)、150 W氙灯(Zolix instruments Co,China,波长范围190~780 nm)、电化学工作站(EG&G 263A,美国EG&G普林斯顿研究公司).工作电极为制备的光催化电极,阴极为钛片(长5.0 cm、宽3.0 cm、厚0.2 mm),参比电极为饱和甘汞电极.
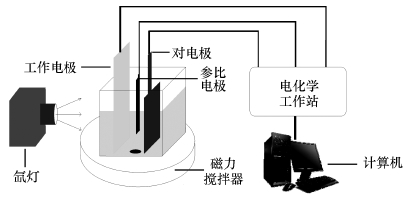 |
| 图 1 光电催化氧化实验装置示意图 Fig. 1 Schematic diagram of the photoelectrocatalytic system |
钛片预处理:钛片依次置于无水乙醇和丙酮中,经超声处理,金相砂纸打磨,去离子水清洗,清洗后,钛片在HF/HNO3/H2O体积比为1:4:5的混合溶液中浸泡1 min,使钛片化学抛光.
电解质的制备:配制100 g含氟离子电解质溶液.称取去离子水8.5 g、NH4F 0.50 g、(NH4)2SO4 1.00 g和丙三醇 90 g,经混合,充分搅拌,制成质量分数为0.5% NH4F+1%(NH4)2SO4+90%丙三醇的混合溶液.
阳极氧化法制备TiO2纳米管电极:阳极为预处理钛片,阴极为铂丝,两极间距20 mm,两极垂直插入电解质中,两极间施加20 V电压,阳极氧化10 h,在马弗炉中450 ℃(升温速率为5 ℃·min-1)煅烧2 h.
2.3.2 GO修饰TiO2纳米管电极的制备将2 mg·mL-1 GO(南京先锋纳米科技有限公司)在0.1 mol·L-1、pH=9.18的磷酸缓冲液(PBS,Na2HPO4)中超声30 min,GO电解液浓度为0.5 mg·mL-1.以TiO2纳米管电极为工作电极,铂丝为对电极,饱和甘汞电极(SEC)为参比电极,采用循环伏安法(扫描范围为-1.5~1.0 V,扫描速率为50 mV·s-1)进行还原.待 GO沉积完全,取出工作电极,去离子水冲洗并用N2吹干.
2.3.3 降解实验络合态铜氰废水的制备:配制一定体积NaOH溶液(25 mmol·L-1),按n(Cu2+):n(CN-)=1:3的比例称取一定量NaCN和CuCN,依次将NaCN、CuCN溶于NaOH溶液.以Na2SO4(1 mmol·L-1)做为电解质,初始pH为11.0.
光电催化氧化反应:取上述溶液70 mL置于反应器中,两极间施加一定电压,开启氙灯,反应总时间为120 min,取样时间依次为0、15、30、60、90、120 min.
2.3.4 表征及分析方法表征方法:TiO2纳米管、GO修饰的TiO2纳米管光电极的表面形态通过场发射扫描电镜(SEM)进行观测(JSM-6700F,JEOL,Japan).
总氰化物(对于络合态氰化物)测定方法:水样中加入磷酸和Na2EDTA,pH小于2时,加热蒸馏,NaOH溶液作为吸收液,待络合态氰化物全部变为自由态氰化物后测定,采用异烟酸-巴比妥酸紫外分光光度法测定总氰化物的量,采用纳氏试剂紫外分光光度法测定氨氮,采用电感耦合等离子体发射光谱仪(ICP-OES,P700,Agilent,USA)测定重金属含量.
3 结果与讨论(Results and discussion) 3.1 TiO2纳米管、GO修饰TiO2纳米管电极表征分析图 1为TiO2纳米管、GO修饰TiO2纳米管电极的SEM图.如图 2a所示,TiO2纳米管排列整齐;随着循环次数的增加,TiO2纳米管表面覆盖的GO逐渐增加.循环5次条件下,覆盖的GO含量较少(图 2b).循环10次后,GO薄膜均匀覆在TiO2纳米管电极表面(图 2c).循环次数增加至15次,大量的石墨烯负载在TiO2纳米管表面(图 2d).
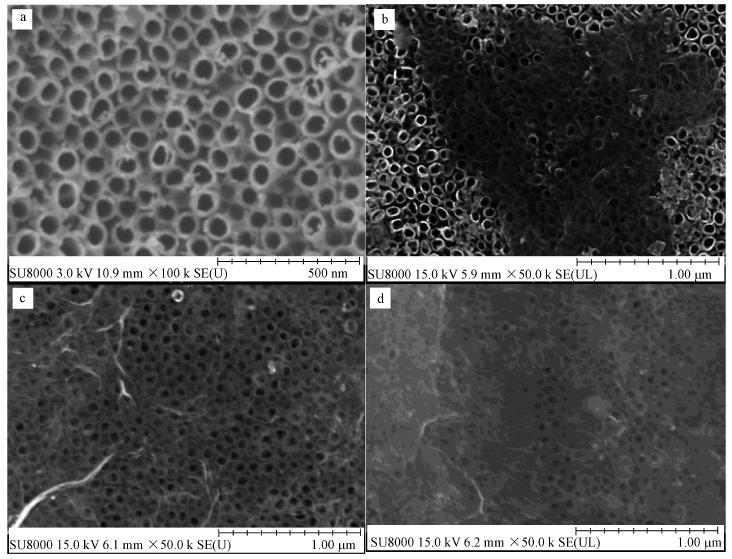 |
| 图 2 TiO2纳米管(a)、GO修饰TiO2纳米管(b.循环5次,c.循环10次,d.循环15次)的SEM图像 Fig. 2 SEM spectra of titanium dioxide nanotubes(a) and titania dioxide nanotubes modified by GO(b.5 cycles,c.10 cycles,d.15 cycles) |
光电流是衡量光催化剂光生载流子分离效率的重要指标(Liu et al.,2011).图 3为TiO2纳米管电极和GO修饰的TiO2纳米管电极在150 W氙灯辐照并加偏压条件下的光电流响应结果.如图 3所示,循环10次,GO修饰的TiO2纳米管电极光电流值最高.随着循环次数变小,石墨烯负载量减少,强化分离电荷能力变低,导致光电流响应能力减弱;循环次数增加时,TiO2纳米管电极表面负载的石墨烯量增多,遮挡辐照到TiO2表面的紫外光,从而降低了TiO2纳米管电极的光电流响应.
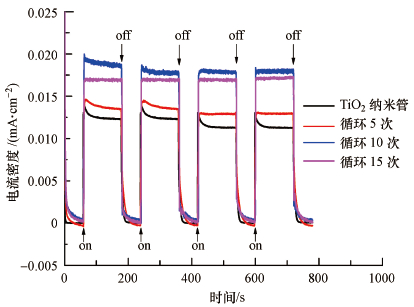 |
| 图 3 TiO2纳米管、GO修饰TiO2纳米管的光电流分析 Fig. 3 The analysis charts of photocurrent for titania nanotubes, titania nanotubes modified by GO |
采用TiO2纳米管电极,对铜氰络合物进行了光电催化去除研究.图 4为不同电压条件下,TiO2纳米管对光降解Cu(CN)32-过程中总氰的去除、Cu回收、CNO-、NH4+浓度及Cu的分布的影响结果.如图 4a所示,随着电压增大,总氰的去除及铜的回收率逐渐增大,当电压为2.0 V,反应时间为120 min时,剩余总氰含量及铜回收率分别为4.0%和96.3%.由图 4b可知,随着电压增大,CNO-含量逐渐增多,氨氮含量减少.因此,电压为2.0 V时,对光电降解Cu(CN)32-效果的影响最强,处理效果最好.图 4c分析了反应120 min后,铜元素的分布情况.随着电压增大,铜在溶液中剩余量逐渐减少,当电压为2.0 V时,处理效果最好.
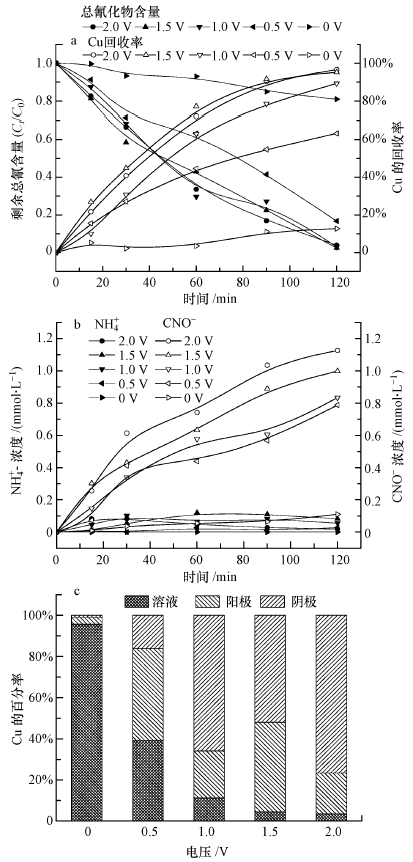 |
| 图 4 不同电压对光降解Cu(CN)32-过程中总氰的去除、Cu回收(a)、CNO-、NH4+浓度(b)及Cu的分布(c)的影响 Fig. 4 The impacts of different voltages on removal rate of total cyanide, Cu recovery(a),the concentration of of CNO-, NH4+(b) and Cu distribution(c) in the process of photodegradation Cu(CN)32- |
在电压为2.0V时,TiO2纳米管和GO修饰的TiO2纳米管对光电降解Cu(CN)32-过程中总氰的去除、Cu回收、CNO-、NH4+及Cu的分布的影响分析如图 5所示.由图 5a可知,经修饰的电极,在光电降解60 min后,污染物已经完全降解.由图 5b可知,经修饰的电极在光电降解中生成的CNO-少于未经修饰电极,生成的NH4+多于未经修饰的电极.此外,图 5c分析了反应120 min时,铜元素的分布情况,经修饰的电极在120 min时溶液中Cu的含量基本为零,回收的Cu在阴极和阳极上大量沉积,而未经修饰的电极回收的Cu主要在阴极上沉积.
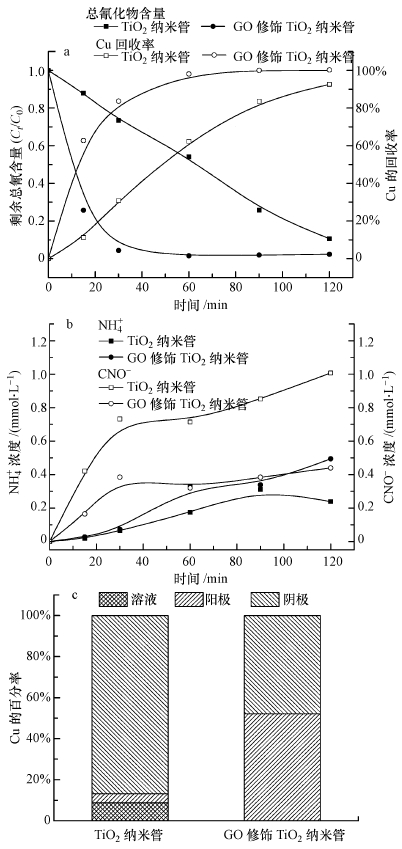 |
| 图 5 TiO2纳米管和GO修饰TiO2纳米管对光电催化降解Cu(CN)32-过程中总氰的去除、Cu回收(a)、CNO-、NH4+浓度(b)及Cu的分布(c)的影响 Fig. 5 The comparison with titania nanotubes and titania nanotubes modified by GO on the removal rate of total cyanide, Cu recovery(a), the concentration of CNO-, NH4+(b) and Cu distribution(c) in the process of photodegradation Cu(CN)32- |
一方面,GO具有较高的比表面积,经GO修饰的TiO2纳米管电极的比表面积得到了提高,吸附铜氰络合物能力增强.另一方面,GO具有较高的传递电子能力,如图 3所示,GO修饰后的TiO2纳米管电极的光电流响应得到了有效的提高.这表明光生电子和空穴得到了有效分离,提高了TiO2纳米管的光催化能力.上述原因使得GO修饰后的TiO2纳米管电极对铜氰络合物的光电催化氧化能力提高;并且在催化反应过程中,随着氰根的有效氧化,释放出来的铜离子也得到了有效回收.
3.4 电极稳定性分析为考察电极的稳定性,对GO修饰TiO2纳米管电极的光电流进行了测试分析. 采用1 mmol·L-1的Na2SO4 作为测试体系的支持电解质,施加偏压为2.0 V.在120 min内,经过GO修饰的TiO2纳米管电极的光电流几乎没有降低,初步表明该电极具有一定的稳定性和抗光腐蚀性.
4 结论(Conclusions)1) 采用阳极氧化法制备了TiO2纳米管电极,采用电化学循环伏安法将GO负载到TiO2纳米管电极表面,结果表明,经循环10次的GO修饰TiO2纳米管,其电极光电响应性能得到了提高,并且电极也表现出了较强的稳定性和较好的耐腐蚀性.
2) GO修饰的TiO2纳米管电极光电催化降解铜氰络合物的效果,明显优于未经修饰的TiO2纳米管电极.在光电催化反应60 min后,氰化物基本降解完全,铜的回收率也得到了极大提高.
| [1] | 陈佩仪, 李彦旭, 孙楹煌, 等.2005.光电催化水处理技术研究进展[J].工业水处理, 25 (12):13–17. |
| [2] | Hou Y, Li X, Zhao Q, et al. 2012.Role of hydroxyl radicals and mechanism of Escherichia coli inactivation on Ag/AgBr/TiO2 nanotube array electrode under visible light irradiation[J]. Environmental Science and Technology, 46 (7): 4042–4050. |
| [3] | Gurol M D, Bremen W M. 1985.Kinetics and mechanism of ozonation of free cyanide species in water[J]. Environmental Science and Technology, 19 : 804–809. |
| [4] | Jiraroj D, Unob F, Hagege A. 2006.Degradation of Pb-EDTA complex by a H2O2/UV process[J]. Water Research, 40 (1): 107–112. |
| [5] | Liu C B, Teng Y R, Liu R H, et al. 2011.Fabrication of graphene films on TiO2 nanotube arrays for photocatalytic application[J]. Carbon, 49 : 5312–5320. |
| [6] | 罗志勇, 张胜涛, 郑泽银, 等.2009.电化学法处理重金属废水的研究进展[J].中国给水排水, 25 (16):6–10. |
| [7] | Kudo A, Hijii S. 1999.H-2 or O-2 evolution from aqueous solutions on layered oxide photocatalysts consisting of Bi3+ with 6s(2) configuration and d(0) transition metal ions[J]. Chemistry Letters, 10 : 1103–1104. |
| [8] | Kutsuna S, Toma M, Takeuchi K, et al. 1999.Photocatalytic degradation of some methyl perfluoroalkyl ethers on TiO2 particles in air:the dependence on the dark-adsorption,the products,and the implication for a possible tropospheric sink[J]. Environmental Science & Technology, 33 (7): 1071–1076. |
| [9] | Peter S, Rainer W, Ralf T, et al. 2009.Functionalized graphenes and thermoplastic nanocomposites based upon expanded graphite oxide[J]. Macromolecular Rapid Communications, 30 : 316–327. |
| [10] | Sehested J, Dahl S, Jacobsen J, et al. 2005.Methanation of CO over nickel:mechanism and kinetics at high H2/CO ratios[J]. The Journal of Physical Chemistry B, 109 (6): 2432–2438. |
| [11] | Tada H, Jin Q, Nishijima H, et al. 2011.Titanium(Ⅳ) dioxide surface-modified with iron oxide as a visible light photocatalyst[J]. Angewandte Chemie, 123 (15): 3563–3567. |
| [12] | White Daniel M, Lilon Timothy A, Woolard Craig. 2000.Biological treatment of cyanide containing wastewater[J]. Water Research, 34 (7): 2105–2109. |
| [13] | Xu T, Zhang L, Cheng H, et al. 2011.Significantly enhanced photocatalytic performance of ZnO via graphene hybridization and the mechanism study[J]. Applied Catalysis B:Environmental, 101 (3): 382–387. |
| [14] | 杨桂蓉, 魏连雨, 李静, 等.2014.Co-BiVO4薄膜电极光电处理Pb/Cu-EDTA研究[J].环境科学学报, 34 (4):914–919. |
| [15] | Zhang S, Zhang C, Man Y, et al. 2006.Visible-light-driven photocatalyst of Bi2WO6 nanoparticles prepared via amorphous complex precursor and photocatalytic properties[J]. Journal of Solid State Chemistry, 179 (1): 62–69. |
 2016, Vol. 36
2016, Vol. 36


