2. 中国环境科学研究院环境基准与风险评估国家重点实验室, 北京 100012;
3. 兰州交通大学环境与市政工程学院, 兰州 730070;
4. 河北工程大学城市建设学院, 邯郸 056038
2. State Key Laboratory of Environmental Criteria and Risk Assessment, Chinese Research Academy of Environmental Sciences, Beijing 100012;
3. School of Environmental and Municipal Engineering, Lanzhou Jiaotong University, Lanzhou 730070;
4. School of Urban Construction, Hebei University of Engineering, Handan 056038
人工湿地是一种高效、低成本的污水处理技术,在城市暴雨径流、村镇生活污水、工业废水及农业排水处理等领域中得到了较多的应用.但是,常规人工湿地存在脱氮能力较弱的显著性缺陷(李文奇等,2009).
沸石对氨氮具有选择吸附能力,常被用作强化脱氮人工湿地填料(Liu et al., 2014; 史鹏博等,2014; Reddy et al., 2013).但沸石对氨氮的吸附容量一定,吸附饱和后需要进行再生.在人工湿地中,沸石的生物再生是一种经济可行的办法.沸石的生物再生就是沸石所吸附的氨氮通过界面发生生物硝化而解吸的过程(温东辉等,2003a),是沸石吸附的氨氮解吸及生物硝化共同作用的结果.通常,湿地中的沸石都是在吸附饱和后,再生物再生(付融冰等,2006).由于生物硝化的速率较慢,沸石吸附饱和后再生物再生所需要的时间较久.因此,以这种方式运行时,需要有轮换的湿地.
沸石对氨氮的吸附具有快速吸附缓慢平衡的特点,即氨氮被交换至沸石表层及易到达的大孔径周围的速度是非常快的,吸附的限速步骤是氨氮在沸石粒内的扩散(温东辉,2003b).在沸石再生的开始阶段,解吸先从沸石表层结构中进行,所以这个交换速度是较快的,随后交换逐渐向沸石内部通道和空腔扩散,这时交换速率逐渐变慢,最后沸石深层的孔道和空腔中氨氮与外界的交换离子的交换速率变得缓慢(付融冰等,2006).为此,根据沸石吸附-解吸前期速率较快的特点,本文构建了生物沸石快速吸附-再生动态平衡人工湿地,研究其性能和生物再生机制.
2 试验材料与方法(Materials and methods) 2.1 试验材料试验选用的天然斜发沸石产自浙江省缙云县,其矿物组成为:SiO2 69.58%,Al2O3 12.2%,Na2O 2.59%,CaO 2.59%,K2O 1.13%,Fe2O3 0.87%,MgO 0.13%,其他 10.91%,沸石粒径为3~5 mm.石灰石购自北京圣泉环保科技有限公司,粒径为1~2 mm.试验所用的氯化铵、碳酸氢钠、磷酸氢二钾试剂均为分析纯,用去离子水配制成所需浓度的溶液.接种污泥取自北京市肖家河污水处理厂浓缩后的二沉池活性污泥.
2.2 试验装置强化硝化人工湿地试验装置为长400 mm、宽200 mm、高200 mm的长方体有机玻璃,结构示意图如图 1所示.反应器左侧0~350 mm处的底层填充50 mm细沙,其上部填充经过氨氮吸附饱和的生物沸石(粒径为3~5 mm)和石灰石混合物60 mm(生物沸石和石灰石的质量比为5 ∶ 1,投加量分别为3826.2 g和765.2 g);右侧350~400 mm处填充粒径为5 mm的砾石110 mm.为避免植物根系作用的干扰,模拟湿地未种植物.
反应器浸润面变化范围为50~110 mm处(从底板上表面算起),采用虹吸方式出水,虹吸管最高处位于110 mm处,最低处位于50 mm处(60 mm高程的浸润面变化).
2.3 试验方法 2.3.1 人工湿地运行性能硝化细菌富集:取浓缩后的二沉池活性污泥2 L于5 L的烧杯中,加入1 L培养液(放置一昼夜后的自来水中加入氯化铵、碳酸氢钠、磷酸氢二钾,使氨氮、NaHCO3和K2HPO4的浓度分别为100、500和500 mg · L-1),用曝气机充分曝气(使DO大于2 mg · L-1),控制pH在5~8之间,室温24 h后静止沉降,批式换水,弃去上清液,保留硝化细菌较为集中的残渣,再加入2 L培养液继续曝气培养.连续培养18 d,每天换培养基,使其中异养菌数量大大减少、硝化细菌数量增加.
沸石接种挂膜:将富集的硝化细菌加入到一定量清洗后的沸石中,再加入一定量的培养液,进行曝气接种.接种成功的标志为体系产生的硝酸盐氮基本稳定.接种成功后的沸石称为生物沸石.
生物沸石以1000 mg · L-1的氨氮吸附饱和后(生物沸石对氨氮的饱和吸附量为12.853 mg · g-1),按图 1中的要求装填反应器.在放置1 d的自来水中加入氯化铵和磷酸氢二钾配制氨氮和磷浓度分别为100 mg · L-1和0.5 mg · L-1的配水.采用手动进水的方式,每天早9:00将2 L配水缓慢倒入反应器中,30 min后排出,每天进水1次.
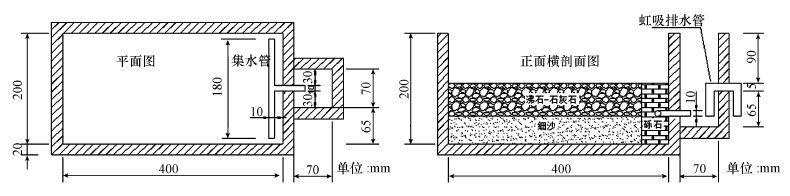 |
| 图1 强化硝化模拟人工湿地结构示意图 Fig.1 Structure diagram of enhanced nitrification constructed wetland reactor |
1)石灰石投加量的影响
将生物沸石与石灰石的混合物(组成见表 1)装入网兜,放入装有100 mL氨氮质量浓度为250 mg · L-1的氯化铵溶液(TP浓度为0.5 mg · L-1)的250 mL烧杯中.在恒温振荡培养箱中吸附30 min,温度为25 ℃,转速为100 r · min-1.吸附结束后,将网兜取出快速放入50 mL去离子水中轻晃以去除生物沸石表面的氨氮.取出的网兜放入100 mL再生液(表 1)中,曝气24 h后取样分析,随后换入100 mL再生液,每天更换再生液1次并连续曝气24 h.
| 表1 石灰石投加量 Table 1 Dosing quantities of limestone |
2)微生物对沸石再生的影响
试验系列如表 2所示.生物沸石与石灰石的混合物装入网兜,放入装有100 mL氨氮质量浓度为250 mg · L-1的氯化铵溶液(TP浓度为0.5 mg · L-1)的250 mL烧杯中.在恒温振荡培养箱中吸附30 min,温度为25 ℃,转速为100 r · min-1.吸附结束后,将网兜取出快速放入50 mL去离子水中轻晃以去除生物沸石表面的氨氮.取出的网兜放入100 mL再生液(去离子水及微生物抑制剂)中,曝气24 h后取样分析,随后换入100 mL再生液,每天更换再生液1次并连续曝气24 h.
| 表2 微生物抑制剂投加量 Table 2 Dosing quantities of microbial inhibitors |
水样分析前用0.45 μm膜过滤.氨氮采用纳氏试剂分光光度法测定,总磷采用钼锑抗分光光度法测定,硝酸盐氮采用紫外分光光度法测定,亚硝酸盐氮采用N-(1-萘基)-乙二胺分光光度法测定,金属阳离子采用火焰原子吸收法测定(国家环保总局,2002).
3 结果与讨论(Results and discussion) 3.1 人工湿地运行性能进水氨氮浓度为100 mg · L-1,TP为0.5 mg · L-1,序批进水挂膜29 d后开始取样分析,试验结果如图 2所示.从图 2a可以看出,出水中的氨氮浓度高于进水,表明生物沸石吸附氨氮饱和后,由于进水中氨氮浓度低于系统的吸附平衡浓度,氨的交换反应发生逆转,生物沸石上高浓度的氨氮在金属阳离子缓释材料所释放阳离子的作用下被逐渐释放出来.随着生物再生的持续,生物沸石内氨氮含量下降,解吸量逐渐减少,出水中氨氮浓度呈下降的趋势.出水中氧化态氮主要是硝酸盐氮,其平均浓度为106.31 mg · L-1;亚硝酸盐氮的浓度很低,其均值为0.579 mg · L-1,表明系统的复氧性能和硝化作用良好,未造成亚硝酸盐氮的积累.硝酸盐氮的产生速率略有波动,主要是由于反应器未控制温度,温度对硝化细菌和反硝化细菌的生长繁殖和活性都有较大影响.丁绍兰等(2010)以生物沸石处理制革废水,发现生物沸石对氨氮的去除在初期以离子交换作用为主,到中后期,以离子交换和硝化反应的协同作用为主.由图 2a可知,运行期内硝酸盐氮的平均产生速率为2.90×10-3 kg · m-2 · d-1,即2.30×10-3 mg · g-1 · h-1. 张曦等(2003)以生物沸石床处理村镇生活污水时表层沸石的硝化速率为6.53×10-4 mg · g-1 · h-1. 硝化速率高主要是由于生物沸石填充区域在间歇期排空的运行方式,强化了大气复氧,使得硝化细菌的生物量和活性均较好.
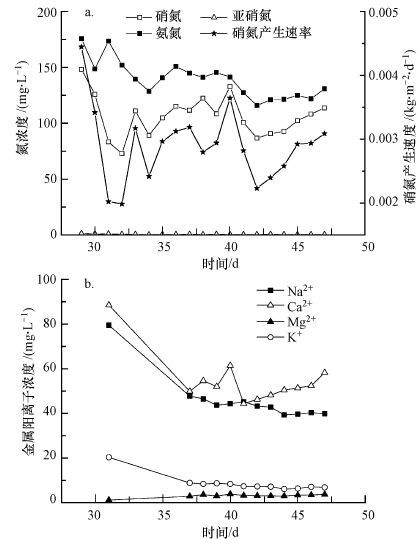 |
| 图2 强化硝化人工湿地硝化性能(a)和金属阳离子变化(b) Fig.2 Nitrification performance (a) and change of metal cation (b) in the enhanced nitrification constructed wetland |
从图 2b可以看出,出水中的金属阳离子主要为钠离子和钙离子,并且30 d后钙离子浓度大于钠离子浓度.在斜发沸石的选择性交换过程中,交换顺序为Cs+>Rb+>K+>NH4+>Pb2+>Ag+>Ba2+>Na+>Sr2+>Ca2+>Li+>Cd2+>Cu2+>Zn2+(Tsitsishvili et al., 1992).所以,试验中生物沸石内部各阳离子与溶液中的NH4+发生交换的顺序为 Ca2+>Na+>NH4+>K+.温东辉等(2003c)研究沸石对NH4+的离子交换作用时发现,Na+前期浓度高于Ca2+,但后期Ca2+的交换容量逐渐与Na+持平,并有超过的趋势.本试验中,生物沸石中的Na+在连续吸附-解吸的过程中逐渐被释放出来,空出来的位点由Ca2+(来源于石灰石)占据.因此,溶液中Na+浓度随时间逐渐降低,而Ca2+浓度则随之升高.生物沸石可交换的离子中K+的含量不低,但由于K+的活泼性比NH4+略大,所以吸附时只有少量K+与NH4+发生离子交换被释放至水中.生物沸石可交换的离子中Mg2+含量低,其活泼性也比Ca2+低,所以吸附时只有较少量的Mg2+与NH4+发生离子交换被释放至水中.
运行100 d后,人工湿地系统基本达到生物沸石快速吸附-再生动态平衡,试验结果如图 3所示.从图 3可以看出,氧化态氮的浓度要略高于吸附去除的氨氮浓度,表明系统能持续稳定地运行(即生物沸石不会达到吸附饱和),不断将进水中的氨氮通过生物沸石的快速化学吸附和离子交换作用转移至生物沸石中,随后在微生物和石灰石的协同作用下,在静置期实现缓慢再生.系统产生的氧化态氮中以硝酸盐氮为主,其浓度为85 mg · L-1左右,表明系统的复氧效果很好.出水中氨氮浓度稳定,为36.76 mg · L-1左右.人工湿地中沸石吸附饱和后,经生物再生67 d,此时湿地出水中氨氮质量浓度高达113.1 mg · L-1,亚硝氮质量浓度为3.43 mg · L-1,硝氮质量浓度为 18.53 mg · L-1,因此,需要将出水继续回流到系统中使氮在系统中转化掉(付融冰等,2006).而生物沸石快速吸附-生物再生动态平衡人工湿地可连续稳定的去除氨氮,具有操作运行简单的优势.
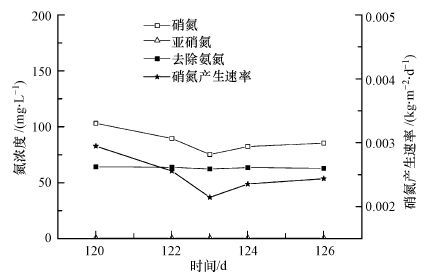 |
| 图3 生物沸石快速吸附-再生性能 Fig.3 Rapid adsorption-regeneration performance of biological zeolite |
沸石的生物再生就是沸石所吸附的氨氮通过界面发生生物硝化而解吸的过程,是沸石吸附的氨氮解吸及生物硝化共同作用的结果(温东辉等,2003a).付融冰等(2006)认为沸石生物再生首先是沸石吸附的氨氮与阳离子发生离子交换被解吸出来,随后被生物膜上的硝化细菌转化为亚硝酸盐和硝酸盐,解吸过程首先是表层结构上的孔道和空腔中的NH4+与穿过沸石表面液膜和生物膜的阳离子发生离子交换.因此,铵从沸石内部释放的速度要远远大于硝化细菌对NH4+的转化速率(McGilloway et al,2003).付融冰等(2006)发现沸石人工湿地再生67 d后,湿地出水中积累的NH4+达到113.1 mg · L-1.但是,也有研究者认为,生长在沸石表面、内部中孔及大孔附近的微生物可以直接利用沸石所吸附的氨氮,空出的吸附位点再被水中的阳离子占据.例如,在Na+等阳离子浓度低的情况下,离子交换是很困难的,但通过生物作用,沸石中的氨氮被转化为硝态氮,其内部所留空间逐步被水中其他阳离子占据(温东辉,2003b).这也与Lahav等(1998)和Dimova等(1999)的研究结论相一致,即沸石-污水体系中投加少量Na盐,生物硝化作用与离子交换作用相互促进,可更有效地实现沸石再生.鉴于沸石孔径只有0.4 nm左右,Wu等(2008)认为硝化微生物对沸石表面而非孔道内吸附的氨氮发生了直接降解.为了解析生物沸石和石灰石体系中生物沸石再生的机理,分别考察了石灰石和微生物所起的作用.
3.2.1 石灰石投加量的影响控制样、吸附样1(m(生物沸石)∶ m(石灰石)=5 ∶ 1)、吸附样2(m(生物沸石)∶ m(石灰石)=10 ∶ 1)和吸附样3(m(生物沸石)∶ m(石灰石)=15 ∶ 1)吸附过程去除的氨氮质量分别为15.992、16.266、16.211和16.677 mg.在12次的再生过程中,控制样、吸附样1、吸附样2和吸附样3的再生性能如表 3所示.
| 表3 控制样及吸附样1、吸附样2及吸附样3的多次再生性能 Table 3 The comparison of performance of bio-zeolite and control with different regeneration times |
从表 3可以看出,吸附样1、吸附样2和吸附样3的氧化态氮(硝氮+亚硝氮)的总量均比控制样的多.吸附样1的石灰石含量最高(m(生物沸石)∶ m(石灰石)=5 ∶ 1,表 1),其产生的氧化态氮的总量也最多,是控制样的5.15倍.另外,含有石灰石的吸附样1、吸附样2和吸附样3所释放出的氨氮的质量均比控制样的高.生物沸石的再生过程被认为是离子交换释放氨氮及微生物协同作用的结果.通过投加合适比例的石灰石,其可以在微生物作用下缓慢释放出Ca2+,从而强化了氨氮的离子交换释放,使生物沸石表面生物膜中的硝化微生物更易于获得氨氮,在溶解氧不受限制的情况下,使系统的硝化效果得到提升.Lahav等(1998)和Dimova等(1999)在研究沸石的再生实验中,投加了少量Na盐,发现生物硝化作用与离子交换作用相互促进,能更有效地实现沸石的再生.李云辉等(2013)在研究吸氨饱和沸石的生物再生性能中同样发现,在一定的范围内,适当添加钠离子有利于提高沸石的再生速率,可使沸石再生时间适当缩短.产生的氧化态氮中,控制样、吸附样1、吸附样2和吸附样3均以硝氮为主,亚硝氮的浓度均低于0.4 mg · L-1,表明生物沸石系统的复氧效果很好,无亚硝氮的积累.再生12次后,控制样、吸附样1、吸附样2和吸附样3所累积释放总氮(硝氮+亚硝氮+氨氮)的量占吸附去除氨氮量的比例分别为20.33%、55.68%、34.92%和22.94%.
3.2.2 微生物作用控制样(有自养微生物)、抑制氨氮氧化样和抑制亚硝氮氧化样吸附过程去除的氨氮质量分别为18.155、17.553和17.991 mg.在8次的再生过程中,控制样、抑制氨氮氧化样和抑制亚硝氮氧化样的再生性能如表 4所示.与控制样相比,抑制亚硝氮氧化样中由于叠氮化钠对硝酸细菌的抑制作用,产生了明显的亚硝酸盐氮的积累;抑制氨氮氧化样中由于丙烯基硫脲对亚硝酸细菌的抑制作用,系统中未有明显的氧化态氮积累.另外,抑制氨氮氧化样和抑制亚硝氮氧化样中均无明显的氨氮积累,表明在生物沸石与石灰石的混合体系的再生过程中,微生物起主导作用.生物反应的主体是微生物,微生物的种群结构与数量在很大程度上影响着系统的整体处理效果(陆健健等,2006).郑南等(2009)对比探讨了曝气、异养菌和硝化细菌3个因素单独或共同作用对沸石再生效果的影响,结果发现,曝气作用、异养菌代谢和硝化作用分别可将沸石的再生效率提高0.5%~1.0%、20.9%~31.1%和120%~180%.
| 表4 微生物抑制剂对生物沸石再生性能的影响 Table 5 Effect of microbial inhibitors on bio-zeolite regeneration performance |
1)基于生物沸石和石灰石的强化硝化人工湿地可实现生物沸石快速吸收-再生动态平衡,生物沸石再生所产生的氧化态氮主要为硝氮,其浓度为85 mg · L-1左右,大于吸附去除的氨氮,即生物沸石不会吸附饱和,人工湿地可持续去除氨氮.
2)生物沸石的再生是离子交换释放氨氮和微生物协同作用的结果.生物沸石与石灰石混合体系的再生过程中,石灰石缓慢释放的Ca2+可促进生物沸石再生,生物沸石与石灰石最佳质量比为5 ∶ 1.微生物在生物沸石的再生过程中起主导作用.
| [1] | 丁绍兰,雷小丽,郭洪涛.2010.生物沸石反应器处理制革废水挂膜试验研究[J].中国皮革,39(5):43-46 |
| [2] | Dimova G,Mihailov G,Tzankov T Z.1999.Combined filter for ammonia removal-part Ⅰ: Minimal zeolite contact time and requirements for desorption[J].Water Science and Technology,39(8):123-129 |
| [3] | 付融冰,杨海真,顾国维.2006.人工湿地中沸石对铵吸附能力的生物再生研究[J].生态环境,15(1):6-10 |
| [4] | 国家环保总局.2002.水和废水监测分析方法(第4版)[M].北京:中国环境科学出版社 |
| [5] | Lahav O,Green M.1998.Ammonium removal using ion exchange and biological regeneration[J].Water Research,32(7):2019-2028 |
| [6] | 李文奇,曾平,孙东亚.2009.人工湿地处理污水技术[M].北京:中国水利水电出版社 |
| [7] | 李云辉,安莹.2013.吸氨饱和沸石的生物再生性能[J].净水技术,32(1):60-63 |
| [8] | Liu M H,Wu S B,Li C,et al.2014.How substrate influences nitrogen transformations in tidal flow constructed wetlands treating high ammonium wastewater? [J].Ecological Engineering,73:478-486 |
| [9] | 陆健健,何文珊,童春福,等.2006.湿地生态学[M].北京:高等教育出版社 |
| [10] | McGilloway R L,Weaver R W,Ming D W,et al.2003.Nitrification in a zeoponic substrate[J].Plant and Soil,256:371-378 |
| [11] | Reddy G B,Forbes D A,Phillips R,et al.2013.Demonstration of technology to treat swine waste using geotextile bag,zeolite bed and constructed wetland[J].Ecological Engineering,57:353-360 |
| [12] | 史鹏博,朱洪涛,孙德智.2014.人工湿地不同填料组合去除典型污染物的研究[J].环境科学学报,34(3):704-711 |
| [13] | Tsitsishvili G V,Andronikashvili T G.1992.Natural Zeolites[M].Chichester,England: Ellis Horwood Limited. 86-91 |
| [14] | 温东辉,张曦,吴为中,等.2003a.天然沸石对铵吸附能力的生物再生试验研究[J].北京大学学报(自然科学版),39(4):494-500 |
| [15] | 温东辉.2003b.天然沸石吸附-生物再生技术及其在滇池流域暴雨径流污染控制中的试验与机理研究[M].北京:中国环境科学出版社 |
| [16] | 温东辉,唐孝炎.2003c.天然斜发沸石对溶液中NH4+的物化作用机理[J].中国环境科学,23(5):509-514 |
| [17] | Wu Z C,An Y,Wang Z W,et al.2008.Study on zeolite enhanced contact-adsorption regeneration-stabilization process for nitrogen removal[J].Journal of Hazardous Materials,156:317-326 |
| [18] | 张曦,吴为中,温东辉,等.2003.生物沸石床污水脱氮效果及机理[J].环境科学,24(5):75-80 |
| [19] | 郑南,闻岳,李剑波,等.2009.天然沸石生物再生途径机理研究[J].中国环境科学,29(5):506-511 |
 2016, Vol. 36
2016, Vol. 36


