多环芳烃(PAHs)是一类持久性有机污染物,具有较强的致癌、致畸、致突变性,普遍存在于大气(毕新慧等,2004)、土壤(Crimalt et al., 2004;孙娜等,2007)、水体(孟丽红等,2006)、沉积物(Crimalt et al., 2004;刘国卿等,2005)等环境介质中.多环芳烃具有半挥发性,它们以“全球蒸馏”和“蚱蜢跳效应”的模式,通过长距离迁移和大气干湿沉降在全球或区域范围内进行大气远距离传输,到达地球的绝大多数地区,导致全球范围的污染(Wania et al., 1996;Gouin et al., 2004).水体是PAHs迁移传输的重要介质,PAHs一般通过大气干湿沉降、地表径流、水-土、水-气界面交换或石油泄漏直接输入等方式进入到水中,在迁移过程中水体中的悬浮颗粒物对PAHs具有强烈的表面吸附作用(Schwarz et al., 2011),而且PAHs能够在沉积物中不断富集(蓝家程等,2015),造成对水体多相介质的污染.PAHs最终可通过食物链在动物和人体中发生生物蓄积,对生态系统和人类健康造成潜在的威胁(Stout et al., 2004;李新荣等,2005).
岩溶地下水是一种重要的生活饮用水源,在有的地区甚至是唯一的生产生活水源,然而研究发现岩溶区地下水正遭受到PAHs的污染(孔祥胜等,2011b;孙玉川等,2014).在岩溶区,土层浅薄,土被不连续,土层对污染物的缓冲、净化作用降低,岩溶天坑、漏斗、落水洞、裂隙等形态为污染物提供了天然通道,地表污染物可直接迁移到地下(蓝家程等,2014).毛海红(2012)在重庆雪玉洞上覆土壤、洞穴滴水和地下河中检测到有机氯农药(OCPs),发现在土壤中迁移能力较强的化合物,在地下河水和滴水中含量也较高,证明了岩溶管道或裂隙对污染物的运输成为地下河水遭受有机污染的潜在威胁.基于此,本文以重庆青木关地下河流域水体为研究对象,探讨PAHs在不同类型水中的含量、组成、来源和迁移特征,并对污染水平进行评价,以期为该区地下水资源的保护提供科学依据.
2 研究区概况(General situation of study area)青木关地下河流域位于重庆境内川东平行岭谷区华蓥山帚状褶皱束温塘峡背斜中段,构造上,下三叠统嘉陵江组(T1j)碳酸盐岩出露于背斜轴部,在裂隙发育和溶蚀作用下形成典型槽谷(图 1).两翼为中三叠统雷口坡组(T2l)碳酸盐岩和上三叠统须家河组(T3xj)长石石英砂岩、泥质粉砂岩、泥岩并夹有煤系,受轴冀转折处挤压应力作用,形成两侧的岭脊,表现为“一山二岭一槽”的典型岩溶槽谷地貌,背斜轴部经过强烈的挤压还形成了两条近似平行的复式次一级背斜.槽谷呈狭长带状,NNE向展布,南北长约12 km,青木关地下河在区内发育,流向与槽谷走向基本一致,长约7.4 km,为单一岩溶管道型地下河(杨平恒等,2008).地下河流域边界和地表分水岭一致,流域面积约13.4 km2,地下河最北端的入口为岩口落水洞,出口为位于流域最南端的姜家泉,出露后流入青木溪并最终汇入嘉陵江.研究区气候为亚热带季风性湿润气候,多年平均降水量为1250 mm,多年平均气温16.5 ℃,降雨主要集中在5—9月.降水为流域的主要补给来源,大部分降水沿坡面汇集到槽谷底部的洼地,通过表层裂隙以面状分散入渗和经落水洞集中注入等方式补给地下河.
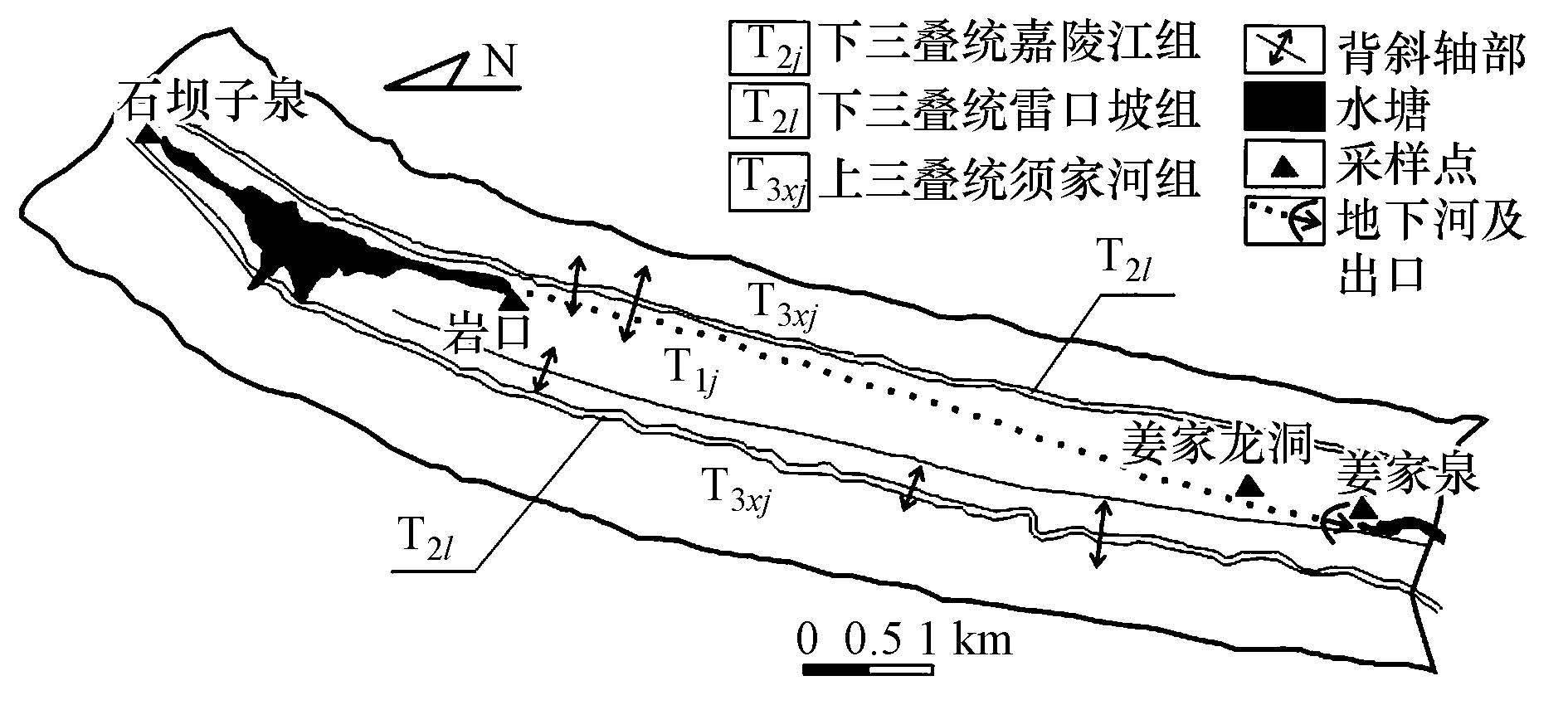 |
| 图1 采样点示意图 Fig.1 Map of sampling sites |
于2014年6—12月对流域上游的表层岩溶泉(石坝子泉)、地下河入口(岩口落水洞)地表水、下游天窗(姜家龙洞)地下河和地下河出口(姜家泉)(图 1)按月取样,共采集28个样品.取样时,用1 L带聚四氟乙烯衬垫的螺旋盖棕色玻璃瓶置于水下采集,采样过程中不能引入气泡.水样置于便携式冰箱中避光冷藏运输,尽快送达实验室,放入冰箱于4 ℃冷藏保存,并于7 d内完成样品前处理.
3.2 样品前处理水样中多环芳烃的提取采用美国EPA525.2的方法进行.水样经0.45 μm玻璃纤维膜过滤1 L,装入棕色瓶中,加入回收率指示物(氘代萘(Nap-D8)、氘代二氢苊(Ace-D10)、氘代菲(Phe-D10)、氘代(Chry-D12)、氘代苝(Per-D12),购自美国Supelco公司)和甲醇(农残级,购自美国Fisher公司)5 mL,摇匀,用铝箔封口,使用全自动固相萃取仪(美国Horizon公司,SPE-DEX 4790)萃取,提取液用50 mL鸡心瓶收集.萃取后的液体用旋转蒸发仪(德国Heidolph公司)浓缩至5 mL,过无水硫酸钠柱脱水,脱水后的液体浓缩到5 mL过硅胶氧化铝(比例为2 ∶ 1)层析柱,洗脱液浓缩至2 mL后,加入5 mL正己烷置换溶剂,再浓缩至0.8 mL,转移至细胞瓶中,用氮气吹至0.2 mL后加入内标物(六甲基苯,购自美国Supelco公司),放入-26 ℃ 冰箱中冷冻待测.
3.3 仪器分析采用气相色谱-质谱联用仪(GC-MS,美国Agilent公司,7890A/5975C)对PAHs进行测定.色谱柱为HP-5MS毛细管柱(30.0 m×0.32 mm×0.25 μm),载气为高纯氦气,流速为1 mL · min-1,进样口温度为280 ℃,升温程序为初始温度50 ℃,保持1 min后以20 ℃ · min-1升温至200 ℃,然后再以10 ℃ · min-1的速度升温至290 ℃,保持15 min.采用无分流方式进样,进样量1 μL.EI电离源70 eV,离子源温度300 ℃,同时采集全扫描数据和选择离子扫描数据,以全扫描数据定性,选择离子扫描数据定量.使用内标法和多点校正曲线对多环芳烃进行定量分析.
3.4 质量控制与质量保证参照文献(林峥等,1999),每分析10个样品同时做空白样品、加标样品、加标平行样品和样品平行样.每个样品在萃取前加入回收率指示物,用于检测实验过程中的损失情况,平行样用于确认实验结果的再现性.该方法除Nap回收率较低外(平均值为53%),其他PAHs的回收率介于78%~110% 之间,且平行样品的相对标准偏差均小于12%.以1 L水样计算的方法检出下限范围为0.2~1.5 ng · L-1.
4 结果与讨论(Results and discussion) 4.1 PAHs含量变化特征青木关地下河水体中PAHs含量和组成见表 1,水体中PAHs含量的动态变化见图 2.由表 1和图 2可知,石坝子泉水中PAHs含量变化范围为76.2~212 ng · L-1,平均值为138 ng · L-1,总体上表现出先下降后升高然后再下降的变化趋势;PAHs含量最高值出现在6月,最低值出现在9月.岩口水样中PAHs含量分别在6、8、11月出现高值,含量分别为264、272、241 ng · L-1,最低值出现在9月为81.9 ng · L-1,月动态变化较大.地下河中,姜家龙洞水
| 表1 水中多环芳烃组分及含量 Table 1 Composition and concentrations of PAHs in water samples |
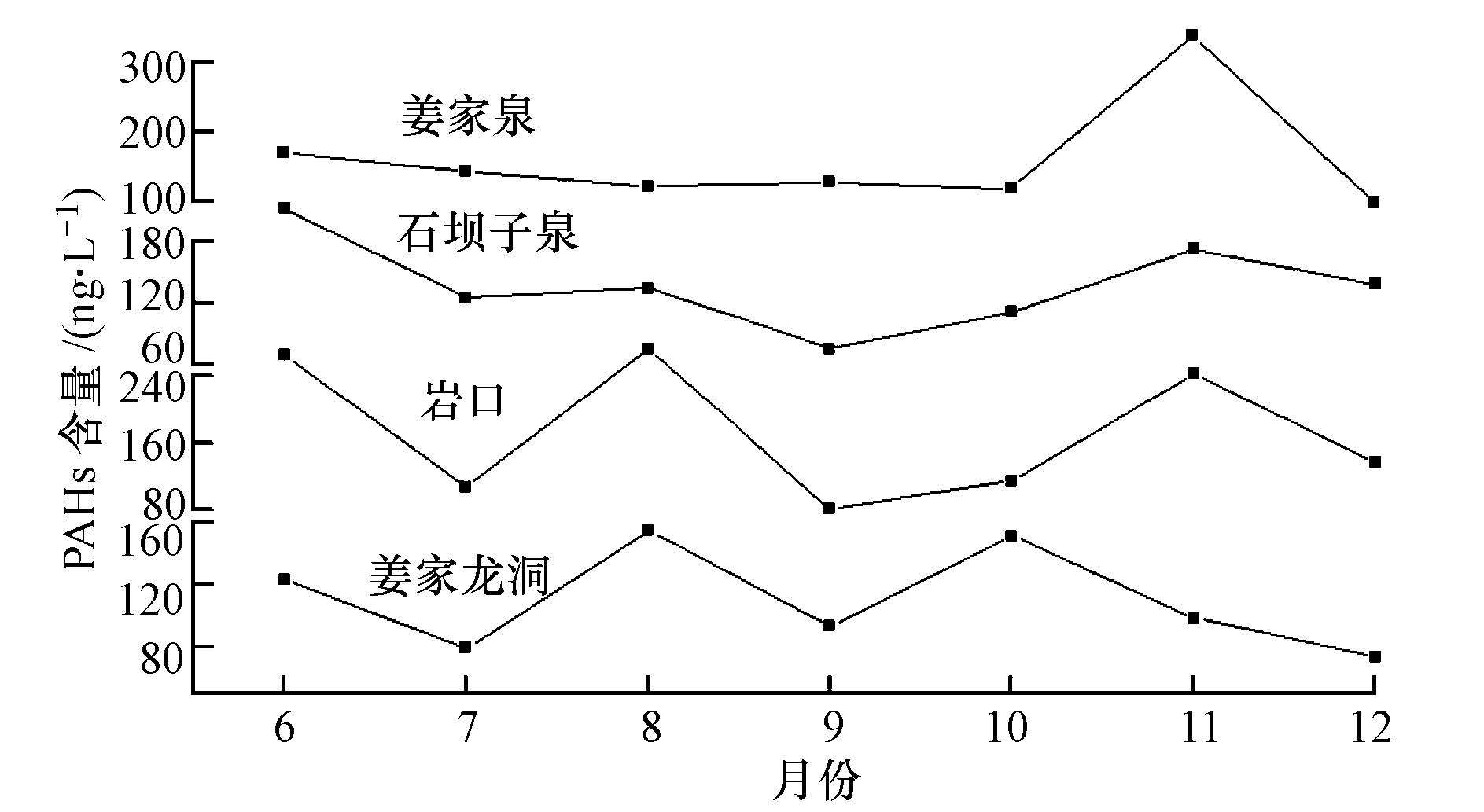 |
| 图2 水中多环芳烃含量月动态变化(2014年) Fig.2 Dynamic variations of PAHs concentrations in water samples for months(2014) |
样中PAHs的含量变化范围为73.9~154 ng · L-1,平均值为110 ng · L-1,最高值出现在8月,最低值出现在12月.姜家泉水样中PAHs的含量范围为97.5~339 ng · L-1,平均值为159 ng · L-1,最高值出现在11月,其余月份含量变化较为平稳. 总体来看,流域上游的石坝子泉和岩口及下游的姜家龙洞水样中PAHs含量的月变化趋势基本上一致,流域内水中∑PAHs平均含量对比结果为岩口>姜家泉>石坝子泉>姜家龙洞,4环及以上PAHs含量之和也表现出同样的大小特征,为进口大于出口,表层泉大于地下河.
大气干湿沉降和土壤淋滤作用对岩溶地下水中PAHs含量变化有重要影响(Perrette et al., 2013).研究区6、8月降水量分别为175、106 mm,无雨天数少,降雨集中连续,而且8月的天气午后多短时强降雨,伴随降雨过程带来的多环芳烃湿沉降会增加岩溶区地表和地下河中PAHs的含量,雨水对地表和土壤的冲刷作用还会将大量的土壤和其他地表物质带入水中,富集在这些土壤和地表物质上的不易溶解和迁移的高环PAHs也随径流进入到地表水中,增加高环PAHs的含量;而且降雨条件下土壤水达到饱和,渗透量增大,沿裂隙不断补给表层泉和地下河,造成地下水中PAHs含量升高.研究区为农业活动区,岩口取样点位于距公路大约50 m处的水塘出口,所处环境较为开放,容易受到降雨冲刷、水土流失的影响,降雨时岩口地表水较为浑浊,悬浮颗粒物较多,也表明该区域水土流失比较严重.在月降水量也超过100 mm的7、9月流域内水中PAHs含量却基本上都降低,这可能与降雨比较分散有关,而且7月高温天气多,PAHs因高温挥发的量也较多.11月除姜家龙洞外,其余样点水样中PAHs含量均出现较大升高,与雨后一天采样有很大关系.
4.2 PAHs组成特征青木关地下河流域水中PAHs主要以2~3环的低环PAHs为主,平均占到82%,4环PAHs检出率为42.8%~85.7%,5~6环PAHs仅在岩口和姜家泉中检出,水体中PAHs组成变化见图 3.低环PAHs中Nap、Flu、Phe基本上每月都能检出,总含量占低环PAHs的比重为89.0%~97.4%,占∑PAHs的比重为69.3%~87.4%;水样中Nap的平均含量最高,为59.9 ng · L-1.从组成比例来看,石坝子泉水中3环PAHs的比重稍高于2环PAHs,最高出现在2014年9月的水样中,占到54.6%;4环PAHs除在6月未检出外,其余月份均有检出,比重在8.98%~15.0%之间;5~6环PAHs在泉水中均未检出.岩口水样中PAHs的组成变化特征较为复杂,2环PAHs比重为6.24%~79.8%,3环PAHs比重为13.0%~45.9%,在8月水样中,4环PAHs含量最高,为158 ng · L-1,其比重占到58.1%;5~6环PAHs在11月检出,含量为138 ng · L-1,比重达到57.2%,这可能与采样时间在雨后有关.姜家龙洞水样在6月只有3环PAHs检出,其余月份2环PAHs比重为25.1%~61.9%,3环PAHs比重为38.0%~63.9%,8—10月均检出4环PAHs,比重为7.89%~11.5%,在整个监测期间,5~6环PAHs均未检出,在降雨较多的6—9月其组成变化幅度大于降雨较少的10—12月.姜家泉中2环PAHs的比重为16.3%~68.7%,3环PAHs比重为25.3%~42.1%,有4个月检出4环PAHs,比重为6.01%~23.1%,在11月,16种PAHs均检出,5~6环PAHs比重达到45.4%.姜家泉位于高速路旁的农村居民区,易受到汽车尾气排放和生活能源燃烧的影响,姜家泉所处位置基岩裸露,PAHs易随降雨快速下渗,并且在降雨较大的时候易随地表径流直接汇入地下河中,岩口落水洞与姜家泉一样,也易受地表环境影响,所以姜家泉和岩口水样中PAHs组成特征较为相似.
 |
| 图3 水中多环芳烃组成动态变化(2014年) Fig.3 Dynamic variations of PAHs composition in water samples(2014) |
在岩溶区,地表水可通过岩溶裂隙、漏斗、落水洞等进入地下形成地下水,而污染物也随之从地表迁移到地下(图 4).石坝子泉水的PAHs组成以2~3环为主,且变化不大,主要是因为相对于4~6环PAHs,2~3环PAHs相对易溶于水,较易随土壤水迁移,而4~6环PAHs亲脂憎水性更强,在表层土壤中迁移较难(何江涛等,2009).石坝子泉域植被覆盖良好,生态环境的调蓄能力较强,降水在泉域内保留时间较长,土壤水渗透稳定,因此,PAHs组成变化也较小,石坝子泉域内PAHs迁移主要受到降水经土壤层的淋滤和土壤水扩散迁移影响.地下河水中的PAHs能被强烈地吸附在沉积物、碳酸盐岩等地下河环境介质中,而且4~6环PAHs因辛醇-水分配系数(logKOW)较大,被沉积物等固相介质优先吸附,在地下河中表现为近距离迁移;而2~3环PAHs的logKOW较小,则主要存在于水相中,在迁移中表现为远距离迁移(孔祥胜等,2011a).岩口落水洞是青木关地下河的进口,地表水可以通过落水洞补给地下河,姜家龙洞和岩口水样的PAHs含量月变化趋势基本一致,也表明地表水对地下河存在补给关系,地表水是地下河中PAHs的主要来源.岩口地表水样2~3环PAHs比重为71.1%,而在姜家龙洞地下河水样中其比重却升高到94.6%;岩口水样中4环PAHs比重为17.5%,姜家龙洞水样中4环PAHs比重为5.40%.这说明4环PAHs在地下河迁移过程中被沉积物或悬浮颗粒物吸附,或被吸附在管道和裂隙中,而2~3环PAHs因logKOW较小,较易溶解于水中,易随水迁移,因此,呈现出地下河入口水中高环PAHs比重大于天窗内地下水中,低环PAHs比例则是天窗内大于地下河入口的现象.地下河相对于地表环境是一个低温环境,有研究认为低温有利于沉积物对PAHs的吸附作用(Joseph et al., 1996),因此,地下河水中的PAHs在长距离的地下河道内迁移时很容易被沉积物和碳酸盐岩等介质所吸附.在地下河系统中PAHs除了由上游往下游迁移外,还有自表土沿裂隙的垂向迁移过程.姜家龙洞内水中PAHs组成变化雨季(6—9月)要大于旱季(10—12月),在旱季地下河主要靠土壤渗透水补给,含水层中裂隙水补给管道水,因此,在旱季姜家龙洞水中PAHs组成变化较小;在雨季,在降雨作用下,土壤渗透性增强,PAHs易随土壤中的溶解性有机质(DOM)迁移,而且地表水的补给也会影响到姜家龙洞地下水的PAHs组成,因此,姜家龙洞水中PAHs组成在雨季变化较大.为示踪DOM在地下河中的来源及迁移,在早期于2013年7—11月对青木关地下河流域进行了水样采集,用以测试分析另一种生物标志物甾醇.结果表明,岩口、姜家龙洞、姜家泉中溶解态甾醇的平均含量分别为724、412、374 ng · L-1,表现为溶解态甾醇含量随地下河运移距离的增加而减少,表明溶解态甾醇在地下河运移的过程中容易和水中颗粒有机质结合在一起,而且地下河内的沉积物、碳酸盐岩和黏土矿物等对水中溶解态甾醇有一定的吸附.豆甾醇和β-谷甾醇在水体溶解态甾醇中占有较高比重,表明高等植物源等陆源有机质输入对水环境中DOM有较大贡献,而且这种贡献值随着地下河运移距离的增加显现出降低的趋势,这也说明了地下河上游地表环境对地下河中有机物含量的重要影响和地下环境介质对有机物的吸附作用(梁作兵等,2015).
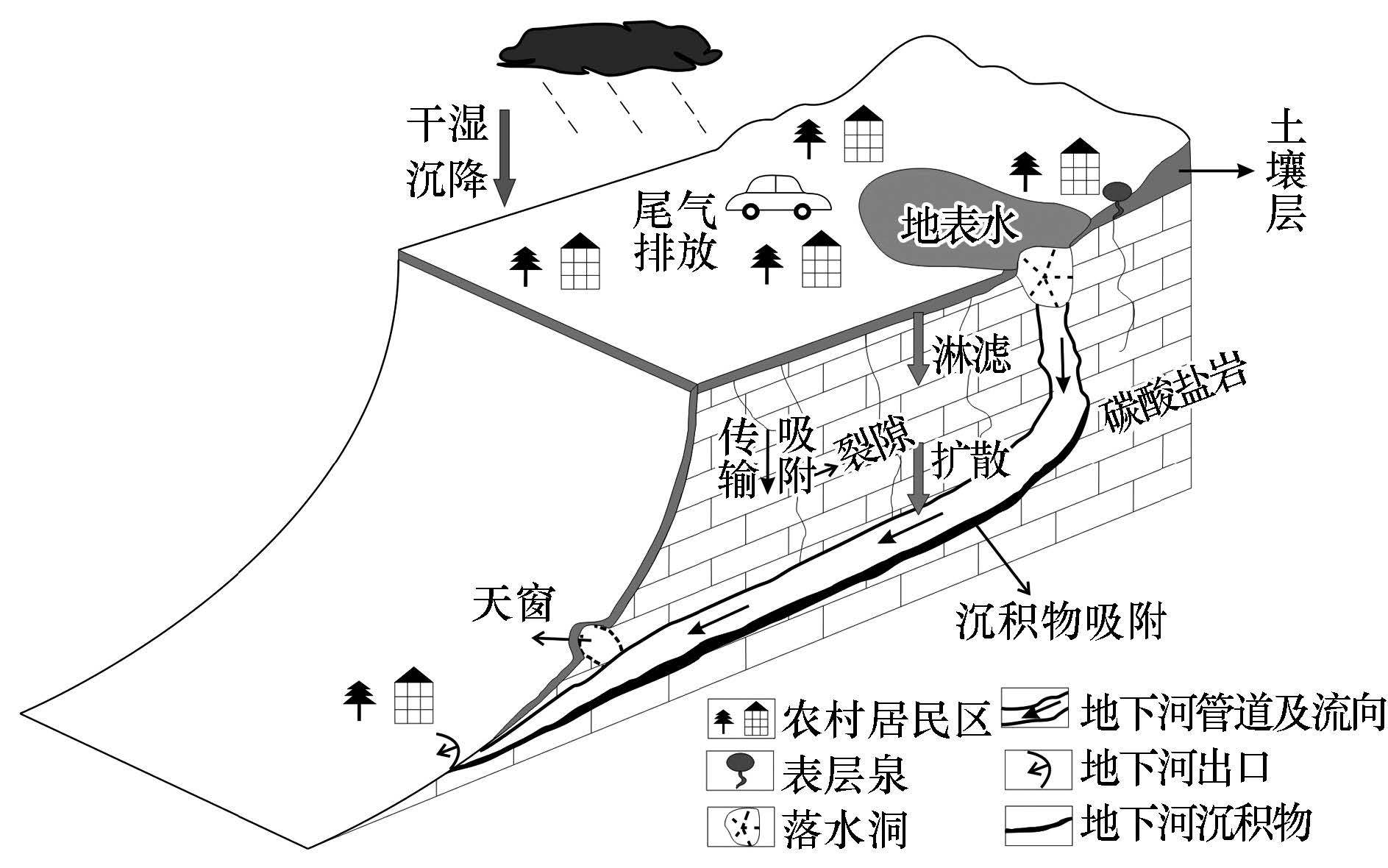 |
| 图4 地下河流域多环芳烃迁移示意图 Fig.4 Sketch map of transport of PAHs in the underground river catchment |
一般来说,环境中PAHs主要来自于燃烧源和石油源.PAHs在迁移、传输过程中存在着分馏作用,而PAHs的同分异构体具有相似的分子结构和理化性质,在传输过程中不会发生分馏作用,因此,一般可用PAHs的同分异构体比值来识别PAHs来源(Liu et al., 2005).泉水、地表水、地下河中Phe都是主要的PAHs,而Ant则基本上未检测到,根据Yunker等的同分异构体比值法,Ant/(Ant+Phe)<0.1,指示PAHs主要来自石油源,Ant/(Ant+Phe)>0.1,指示PAHs来自于燃烧源(Yunker et al., 2002),但Ant相对于Phe更易光解,导致指示来源不准确.同分异构体Fla和Pyr在环境中具有相似的降解速率(Yunker et al., 2002;Tobiszewski et al., 2012),因此,Fla/(Fla+Pyr)比值能更准确地反映PAHs的来源信息,各采样点Fla、Pyr均有检出的月份都不超过4个月,石坝子泉水中Fla/(Fla+Pyr)值范围在0.506~0.525之间,岩口水样中Fla/(Fla+Pyr)值范围为0.512~0.517,姜家龙洞水样中Fla/(Fla+Pyr)值为0.54,姜家泉为0.504~0.531,Fla/(Fla+Pyr)比值表明PAHs来源主要是木材、煤等生物质的燃烧源.整个采样期间只有11月在岩口和姜家泉中检出BaA、Chry、InP、BgP,岩口水样BaA/(BaA+Chry)值为0.48,InP/(InP+BaP)值为0.45,姜家泉水样BaA/(BaA+Chry)值为0.39,InP/(InP+BaP)值为0.43,均指示为石油燃烧源,这与岩口和姜家泉附近有较多的汽车尾气排放是相符合的,因是雨后采样所以这些高环PAHs通过沉降、径流搬运、土壤渗透等方式进入地表水和地下水,未完全被沉积物等吸附,导致水中检出较多高环PAHs.根据以上判断,研究区水体中的PAHs主要来自于燃烧源.
4.5 流域内水中PAHs污染水平表 2列出了我国生活饮用水卫生标准、荷兰地下水水质标准和加拿大水质标准中规定的PAHs含量限值(孙玉川等,2014).结合表 1可知,石坝子泉和姜家龙洞水样中均未检出BaP,岩口和姜家泉水样中只有在11月检测出BaP,含量分别为17.1、20.8 ng · L-1,超过我国生活饮用水卫生标准规定的BaP含量限值;流域内水中∑PAHs含量范围为73.8~339.0 ng · L-1,均低于国家饮用水标准.
| 表2 多环芳烃水质标准 Table 2 Stand ards for water quality of PAHs |
根据荷兰地下水水质标准,2014年6、8、10—11月姜家龙洞水样中Phe含量和8—10月水样中Fla含量超过荷兰地下水标准中规定的限值,其余月份水样中检出的PAHs均低于荷兰地下水标准;在6月石坝子泉水样中Nap含量超过荷兰地下水标准规定的限值,6—8月、11—12月Phe含量和7—12月Fla含量也超标;6月岩口和姜家泉水样中Nap含量超标,6—9月、12月岩口水样和6—11月姜家泉水样中Phe含量超标,岩口水样中Fla含量在8月、10—11月超标,其中,8月岩口样品中的Fla含量超过荷兰标准限值16倍多,姜家泉水样中Fla含量在6、8、10—11月也超过荷兰标准;11月岩口和姜家泉水样中均检出Chry、BaA、BaP、BkF、BgP、InP且含量均出现超标情况.根据加拿大水质标准可知,只有11月岩口和姜家泉水样中BaA、BaP、BbF、DaA、InP含量超过规定限值.
总体上,青木关地下河流域水中有少数低环PAHs含量超标,表层泉和天窗地下水中无高环PAHs超标;地表水和地下河出口水中在2014年11月检出高环PAHs,且含量均超过中国、荷兰和加拿大标准限值.
有研究者将水中溶解态PAHs污染水平分为4类:微污染(10~50 ng · L-1)、轻污染(50~250 ng · L-1)、中等污染(250~1000 ng · L-1)、重污染(>1000 ng · L-1)(陈宇云,2008).由表 1和图 2可知,青木关地下河流域水中PAHs污染基本上为轻污染水平.
从表 3可以看出,青木关地下河流域水中PAHs污染水平与其他地表河流相比,与西江、密西西比河相当,略高于漳卫南运河,与欧洲PAHs含量很低的多瑙河、塞纳河相比,研究区水中PAHs含量要高出很多倍,但与流经区域经济较为发达的长江、海河、大辽河、通惠河相比,研究区水中PAHs污染水平要远低于这些水体;相比于其他地区地下水,青木关表层泉水中PAHs污染水平低于南川岩溶泉、南山岩溶泉,与江汉平原地下水相当,地下河污染水平与白朗地下河相当,低于老龙洞地下河.总体上,青木关地下河流域水中PAHs污染处在较低的水平,以个别低环PAHs超标为主,基本上不存在高环PAHs超标,因此,生态风险评价中基本上不存在致癌性高环PAHs带来的负生态效应.但岩溶区代表的是一个富钙的环境,岩溶地下河显示的是富钙 条件下的地球化学特征,因溶蚀作用的发生,地下
| 表3 不同地区水中多环芳烃含量比较 Table 3 Comparison of ∑PAHs in water from different sites |
河管道发育,空间结构复杂,环境相对封闭黑暗,PAHs易于沉降进入地下系统而且不易被光降解;地下河沉积物和碳酸盐岩对PAHs具有吸附作用,这将造成PAHs在地下空间环境中不断富集,长期的积累会成为潜在的污染源使污染物向下游扩散,必然会影响整个地下生态系统(孔祥胜等,2011b).
5 结论(Conclusions)1)青木关地下河流域水中∑PAHs含量变化范围为73.9~339 ng · L-1,PAHs平均含量对比结果为:岩口>姜家泉>石坝子泉>姜家龙洞,石坝子泉、岩口、姜家龙洞水样中PAHs含量月变化趋势基本一致.PAHs组成以2~3环为主,4环检出率不高,5~6环基本上未检出.PAHs在地下河迁移过程中存在分异作用,对地下河水中PAHs组成也产生影响.
2)通过对PAHs来源解析发现,流域内水中PAHs主要来自于燃烧源.对水中PAHs的污染水平分析发现,部分单体PAHs存在超标现象,表明水体已受到PAHs污染.与其他地区地表河流和地下水相比,青木关地下水污染程度为低污染水平,但PAHs在地下空间环境中长期富集,会成为潜在的污染源,将对整个地下生态系统造成负面影响,因此,必须要引起重视.
3)为了解降雨条件下岩溶地下河流域水体中PAHs的迁移特征,在今后的研究中还要增加在不同降雨条件下的监测,而且地下河流域是一个整体系统,将在未来的工作测定土壤(水)、地下河沉积物、水体悬浮颗粒物中PAHs的含量,以探究PAHs在土壤中的迁移规律和在水体中的运移和分配规律.
致谢: 衷心感谢西南大学地理科学学院蓝家程博士、陈雪彬、徐昕、师阳等在野外采样和样品前处理过程中的大力帮助!
| [1] | 毕新慧,盛国英,谭吉华,等.2004.多环芳烃(PAHs)在大气中的相分布[J].环境科学学报,24(1):101-106 |
| [2] | 曹治国,刘静玲,王雪梅,等.2010.漳卫南运河地表水中溶解态多环芳烃的污染特征、风险评价与来源辨析[J].环境科学学报,30(2):254-260 |
| [3] | Cao Z H,Wang Y Q,Ma Y M,et al. 2005.Occurrence and distribution of polycyclic aromatic hydrocarbons in reclaimed water and surface water of Tianjin,China[J]. Journal of Hazardous Materials,122(1):51-59 |
| [4] | 陈宇云.2008.钱塘江水体中多环芳烃的时空分布、污染来源及生物有效性[D].杭州:浙江大学 |
| [5] | Crimalt,J O,Van Drooge B L,Ribes A,et al.2004. Persistent organochlorine compounds in soils and sediments of European high altitude mountain lakes[J].Chemosphere,54 (10):1549-1561 |
| [6] | 邓红梅,陈永亨,常向阳.2009.多环芳烃在西江高要段水体中的分布与分配[J].环境科学,30(11):3276-3282 |
| [7] | Fernandes M B,Sicre M A,Boireau A,et al.1997.Polyaromatic hydrocarbon (PAH) distributions in the Seine River and its estuary[J].Marine Pollution Bulletin,34(11):857-867 |
| [8] | Ford D,Williams P.2007.Karst Hydrogeology and Geomorphology[M].Hoboken,New Jersey:John Wiley & Sons Ltd. |
| [9] | 龚香宜,何炎志,孙云雷.2015.江汉平原四湖流域上区地下水中多环芳烃分布特征与源解析[J].环境科学学报,35(3):789-796 |
| [10] | Gouin T,Mackay D,Jones K C,et al.2004.Evidence for the "grasshopper" effect and fractionation during long-range atmospheric transport of organic contaminants[J].Environmental Pollution,128(1/2):139-148 |
| [11] | 郭伟,何孟常,杨志峰,等.2007.大辽河水系表层水中多环芳烃的污染特征[J].应用生态学报,18(7):1534-1538 |
| [12] | 何江涛,金爱芳,陈素暖,等.2009.北京东南郊污灌区PAHs垂向分布规律[J].环境科学,30(5):1260-1266 |
| [13] | Joseph J P,Debera A B,Paul D C,et al.1996.Temperature-dependent sorption of naphthalene phenanthrene and pyrene to low organic carbon aquifer sediments[J].Environmental Science & Technology,30(3):751-760 |
| [14] | 孔祥胜,祁士华,Oramah I T,等.2011a.大石围天坑群地下河沉积物中PAHs的污染特征[J].环境科学与技术,34(8):42-48,159 |
| [15] | 孔祥胜,祁士华,Oramah I T.2011b.广西大石围天坑群地下河水中多环芳烃的污染特征[J].环境科学,32(4):1081-1087 |
| [16] | 蓝家程,孙玉川,师阳,等.2015.岩溶地下河表层沉积物多环芳烃的污染及生态风险研究[J].环境科学,36(3):855-861 |
| [17] | 蓝家程,孙玉川,田萍,等.2014.岩溶地下河流域水中多环芳烃污染特征及生态风险评价[J].环境科学,35(10):3722-3730 |
| [18] | 李新荣,李本纲,陶澍,等.2005.天津地区人群对多环芳烃的暴露[J].环境科学学报,25(7):989-993 |
| [19] | 梁作兵,沈立成,孙玉川,等.2015.青木关地下河中溶解态甾醇来源及迁移、转化特征[J].环境科学,36(11):4074-4080 |
| [20] | 林峥,麦碧娴,张干,等.1999.沉积物中多环芳烃和有机氯农药定量分析的质量保证和质量控制[J].环境化学,18(2):115-121 |
| [21] | 刘国卿,张干,李军,等.2005.多环芳烃在珠江口的百年沉积记录[J].环境科学,26(3):141-145 |
| [22] | Liu X,Zhang G,Jones K C,et al.2005.Compositional fractionation of polycyclic aromatic hydrocarbons (PAHs) in mosses(Hypnum plumaeformae WILS.) from the northern slope of Nanling Mountains,South China[J].Atmospheric Environment,39(30):5490-5499 |
| [23] | Maldonado C,Bayona J M,Bodineau L.1999.Sources,distribution,and water column processes of aliphatic and polycyclic aromatic hydrocarbons in the Northwestern Black Sea water[J].Environmental Science & Technology,33(16):2693-2702 |
| [24] | 毛海红.2012.岩溶水文地质系统中有机氯农药的迁移机理初探[D].重庆:西南大学 |
| [25] | 孟丽红,夏星辉,余晖,等.2006.多环芳烃在黄河水体颗粒物上的表面吸附和分配作用特征[J].环境科学,27(5):892-897 |
| [26] | Mitra S,Bianchi T S.2003.A preliminary assessment of polycyclic aromatic hydrocarbon distributions in the lower Mississippi River and Gulf of Mexico[J].Marine Chemistry,82 (3):273-288 |
| [27] | 欧冬妮,刘敏,许世远,等.2009.长江口滨岸水和沉积物中多环芳烃分布特征与生态风险评价[J].环境科学,30(10):3043-3049 |
| [28] | Perrette Y,Poulenard J,Durand A,et al.2013.Atmospheric sources and soil filtering of PAH content in karst seepage waters[J].Organic Geochemistry,65:37-45 |
| [29] | Schwarz K,Goeht T,Grathwohl P.2011.Transport of polycyelic aromatic hydrocarbons in highly vulnerable karst systems[J].Environmental Pollution,159(1):133-139 |
| [30] | Stout S A,Uhler A D,EmsboMattingly S D.2004.Comparative evaluation of background anthropogenic hydrocarbons in surficial sediments from nine urban waterways[J].Environmental Science and Technology,38(11):2987-2994 |
| [31] | 孙娜,陆晨刚,高翔,等.2007.青藏高原东部土壤中多环芳烃的污染特征及来源解析[J].环境科学,28(3):664-668 |
| [32] | 孙玉川,沈立成,袁道先.2014.表层岩溶泉水中多环芳烃污染特征及来源解析[J].环境科学,35(6):2091-2098 |
| [33] | Tobiszewski M,Namies'nik J.2012.PAH diagnostic ratios for the identification of pollution emission sources[J].Environmental Pollution,162(1):110-119 |
| [34] | Wania F,Mackay D.1996.Tracking the distribution of persistent organic pollutants-control strategies for these contaminants will require a better understanding of how they around the globe[J].Environmental Science & Technology,30(9):390A-396A |
| [35] | 杨平恒,罗鉴银,彭稳,等.2008.在线技术在岩溶地下水示踪试验中的应用——以青木关地下河系统岩口落水洞至姜家泉段为例[J].中国岩溶,27(3):215-220 |
| [36] | Yunker M B,Macdonald R W,Vingarzan R,et al.2002.PAHs in the Fraser River Basin:A critical appraisal of PAH ratios as indicators of PAH source and composition[J].Organic Geochemistry,33(4):489-515 |
| [37] | Zhang Z,Huang J,Yu G,et al.2004.Occurrence of PAHs,PCBs and organochlorine pesticides in the Tonghui River of Beijing,China[J].Environmental Pollution,130(2):249-261 |
 2016, Vol. 36
2016, Vol. 36


