目前,在氯化钾等无机盐浮选中应用了阳离子胺类捕收剂.这类捕收剂的分子有1个由10~24个碳原子组成的疏水链和1个亲水氨基(—NH2),而且不溶于水,具有强碱性,故在使用前必须用盐酸中和处理,此类胺中最常用的是十八烷胺(费雯丽和李贵林,2012).
十八烷胺(ODA,C18H39N,octadecylamine)是一种具有较长烷基的高级脂肪胺,其分子结构中含有亲水端和憎水端,是阳离子表面活性剂、非离子型表面活性剂(陈进生等,2003).在钾盐的浮选中,由于长碳链的伯胺类物质在自然界中很难自然降解,长期使用会在盐湖卤水中积累,不但污染环境,而且会给高品质的氯化钾的生产带来不利影响.因此,研究浮选过程中的胺类——十八烷胺的去除方法很有意义.废水的处理方法主要有自然净化法、混凝沉降法、化学氧化法、生物处理法、吸附法等(夏洋,2007).由于吸附法具有去除水中污染物速度快、吸附容量大、无二次污染、适应性强和易操作等优点而受到了广泛的关注.
埃洛石(HNTs)是一种含水层状结构的、双层的1 ∶ 1型铝硅酸盐材料,具有典型的结晶结构(贾佩楠等,2011).相比于其他纳米材料(如碳纳米管),HNTs具有良好的离子交换性、吸附性和比表面积,在水处理领域具有广阔的应用前景.然而,当吸附剂和溶液作用后,通过离心的方法使吸附剂和溶液分离,即耗时又费力.为使吸附剂与溶液快速有效的分离,将具有磁性微粒负载到具有交换吸附性能的微孔矿物表面,使磁性复合材料在外磁场的作用下能够快速分离.
Fe3O4是一种理想的磁性粒子,特别是其超顺磁行为,容易在外磁场作用下实现定位、定向移动(袁智成等,2011).目前,有关磁性埃洛石复合材料及其在处理废水后快速回收利用的研究报道并不多见.因此,本研究是在埃洛石表面负载Fe3O4微粒得到磁性埃洛石(MHNTs),并以该材料为吸附剂,对十八烷胺的吸附性能进行研究,从吸附剂浓度、溶液pH值、温度及时间等因素进行考察,并进一步研究十八烷胺在磁性埃洛石上的吸附动力学和热力学行为.
2 实验部分(Experimental) 2.1 材料与仪器材料:六水合氯化铁、七水合硫酸亚铁、异丙醇、三氯甲烷、乙酸、乙酸钠、盐酸、氢氧化钠,均为分析纯.十八烷胺,埃洛石纳米材料(HNTs)(购买于河北省灵寿县锦川矿产品加工厂).
仪器:BSA224S-CW电子天平(赛多利斯科学仪器有限公司)、KQ-250DV型数控超声清洗器(昆山市超声仪器有限公司)、微量进样器(上海高鸽工贸有限公司)、IKAKS 4000i控温摇床(成都智诚科灵仪器仪表有限公司)、pH计(赛多利斯科学仪器有限公司)、TU-1901双光束紫外可见分光光度计(北京普析通用仪器有限公司)、透射电子显微镜(日本电子JSM)、Nexus 670 FT-IR(美国Nicolet公司)、振动样品磁强计VSM(Lake Shore 7410).
2.2 实验方法 2.2.1 磁性埃洛石复合材料的制备准确称取5.9 g FeCl3 · 6H2O和3 g FeSO4 · 7H2O放置在250 mL的烧杯中,并加入150 mL蒸馏水,然后加入3 g 埃洛石粉(200目),在N2条件下,逐滴加入0.05 mol · L-1 NaOH溶液调节pH值至11,并转入三颈圆底烧瓶中,在70 ℃ 恒温水浴条件下,机械搅拌4 h 后停止,得到的磁性埃洛石冷却至室温,利用蒸馏水洗涤至中性,最后用乙醇洗涤两次,在真空70 ℃ 条件下干燥,密封保存(Xie et al., 2011).
2.2.2 吸附实验采用静态批式法,量取一定量的磁性埃洛石和十八烷胺储备液于15 mL 的聚乙烯离心管中,并通过微量进样器添加NaOH或HCl来调节溶液的pH值,将聚乙烯离心管置于恒温振荡器上振荡24 h,然后再利用磁铁使溶液与吸附剂进行快速分离,取一定量的上层清液,采用紫外分光光度计在波长425 nm 处测定上清液中十八烷胺的含量.所有实验数据均为3次实验数据的平均值,所测数据的相对误差约为±5%.
2.2.3 数据处理十八烷胺的吸附率(Y)的计算公式见式(1).
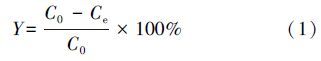
Kd 的表达式见式(2).
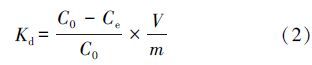
分析 图 1是 HNTs和MHNTs 在透射电子显微镜下的扫描图,从图 1a中可以看出,HNTs为形态完整的管状结构,尺寸分布均匀稳定.在图 1b中可以很明显的观察到Fe3O4 纳米粒子成功负载在埃洛石表面.
 |
| 图1 HNTs和MHNTs的TEM图谱 Fig.1 TEM images of halloysite(a) and magnetic halloysite(b) |
图 2是 HNTs和MHNTs的红外光谱图,从图 2c中可以看出埃洛石在高频区3699 cm-1、3622 cm-1和3453 cm-1处有吸收峰,三峰呈锯齿型,是埃洛石中 —OH 的伸缩振动峰(Luo et al., 2010).在中频区,912 cm-1 的吸收峰为 —OH 的弯曲振动吸收峰,1097 cm-1和1035 cm-1为Si—O—O伸缩振动吸收.在低频区,695 cm-1和751 cm-1为 —OH 的振动特征吸收带,468 cm-1 为Si—O弯曲振动吸收峰,534 cm-1为Al—O伸缩振动吸收峰(Tierrablanca et al., 2010).图 2a四氧化三铁和图 2b磁性埃洛石所对应的红外光谱图中,都在586 cm-1 处出现一个小的吸收峰,则为Fe—O—Fe伸缩振动峰(Xie et al., 2011),即表明Fe3O4微粒较好的负载到埃洛石表面.
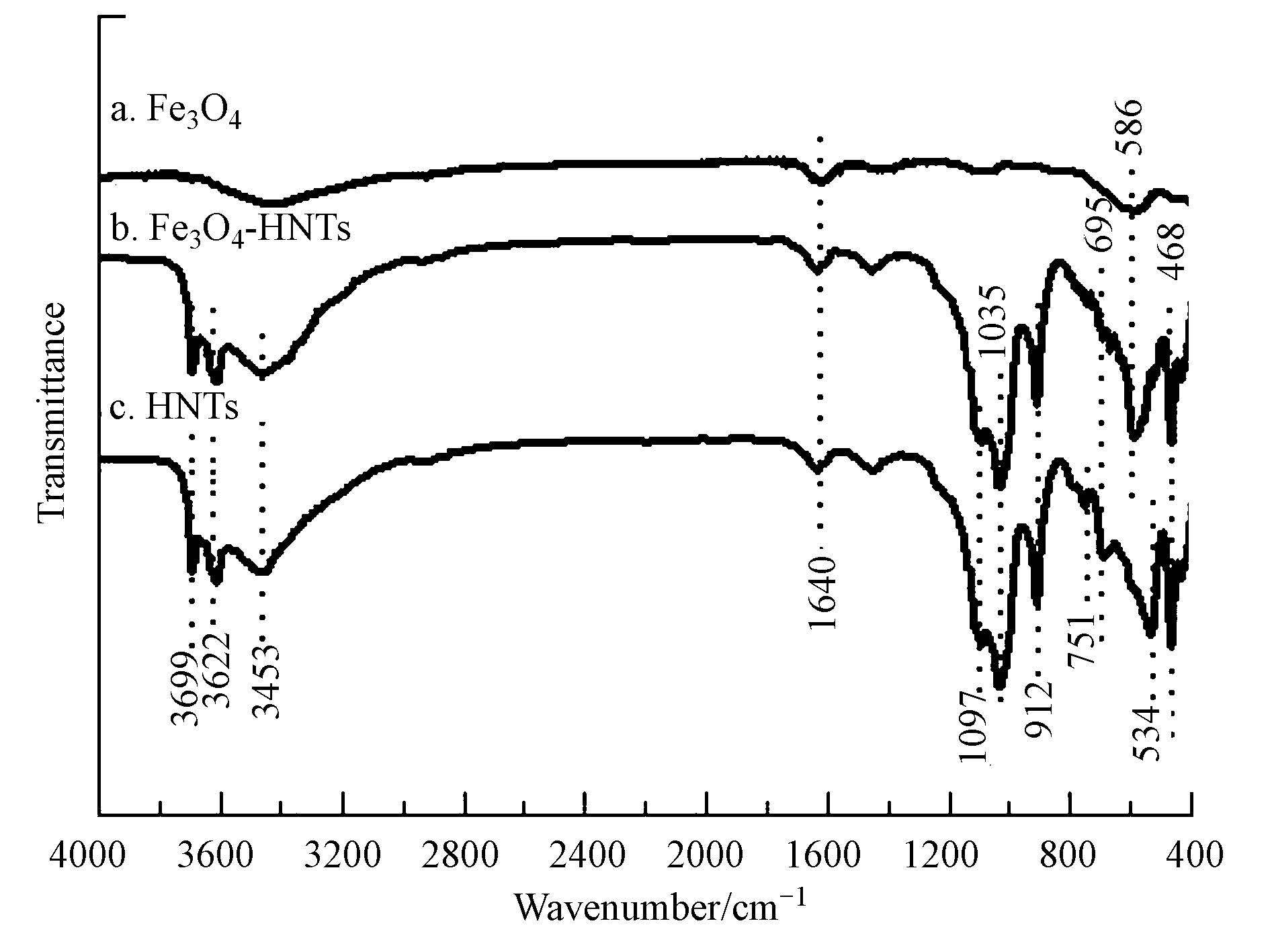 |
| 图2 Fe3O4、HNTs和MHNTs的红外光谱图 Fig.2 FTIR spectra of Fe3O4,halloysite(a) and magnetic halloysite(b) |
分析 图 3显示了MHNTs和HNTs 的X射线衍射(XRD)图谱.从图中可以看出,HNTs在2θ=12.0、20.1、21.2、24.1、26.2、35.3、39.1、55.2、 63.3处出现特征峰,而且在2θ为20°~70°的范围内,Fe3O4的4个特征峰与MHNTs相对应(2θ=30.2°、35.6°、43.3°、57.3°)(Yang et al., 2013).结果表明,Fe3O4纳米粒子成功负载到HNTs上,并没有改变其晶形结构.
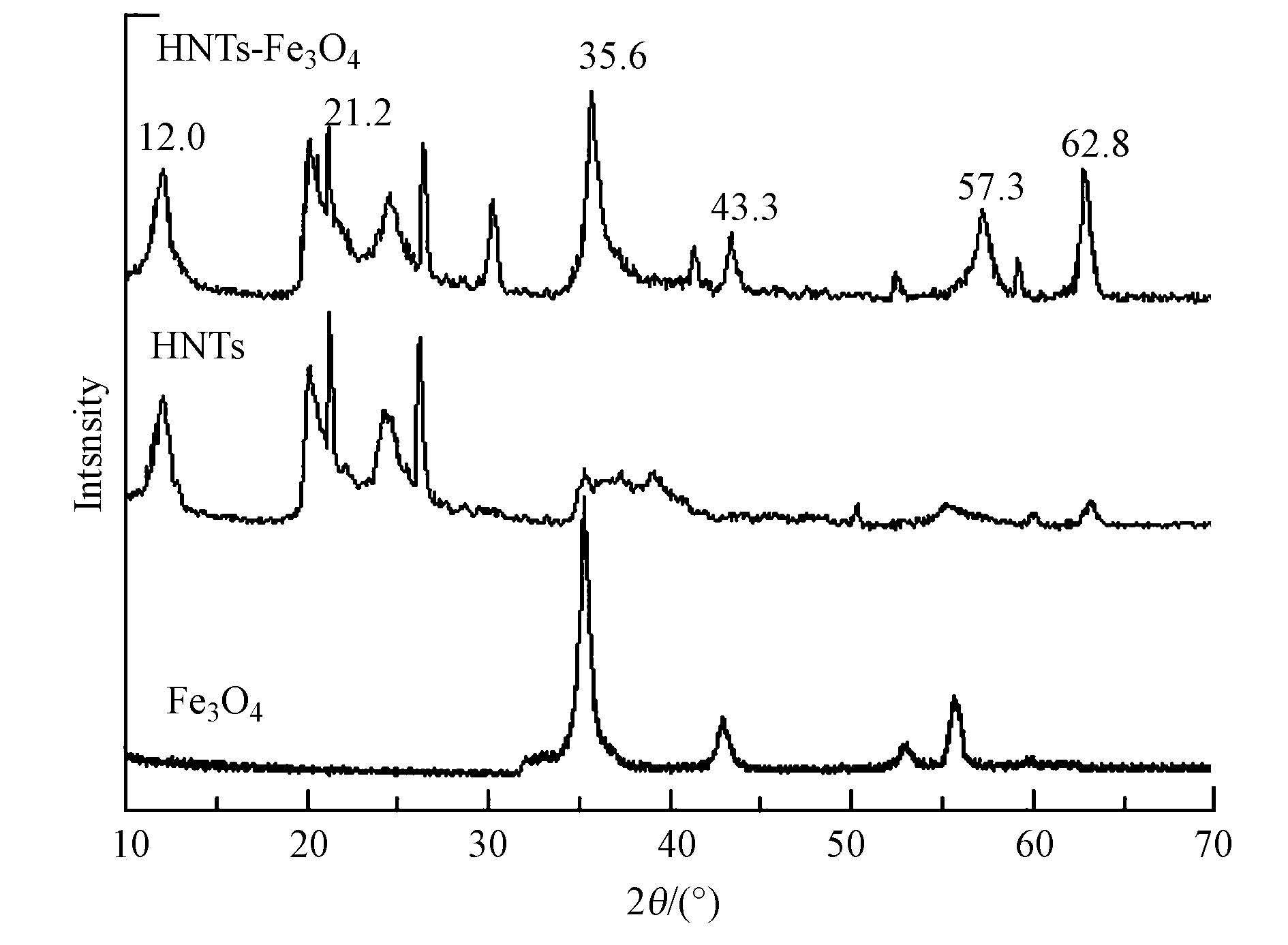 |
| 图3 HNTs、Fe3O4和MHNTs的XRD图谱 Fig.3 X-ray diffraction patterns of halloysite,Fe3O4 and magnetic halloysite |
由图 4A可知,该磁性复合材料的饱和磁化强度为28.67 emu · g-1,这意味着制备出来的磁性复合材料具有很强的磁性.磁滞回线过原点,且以原点为中心,几乎没有剩磁现象,且该粒子的矫顽力为0,表明MHNTs 具有良好的顺磁性(Duan et al., 2012; Lee et al., 2007).从图 4B中可以清楚的看到,MHNTs 能够有效的被外加磁场吸引.结果表明,磁性离子成功的负载到HNTs上,并且能够作为一个可行的磁分离载体.
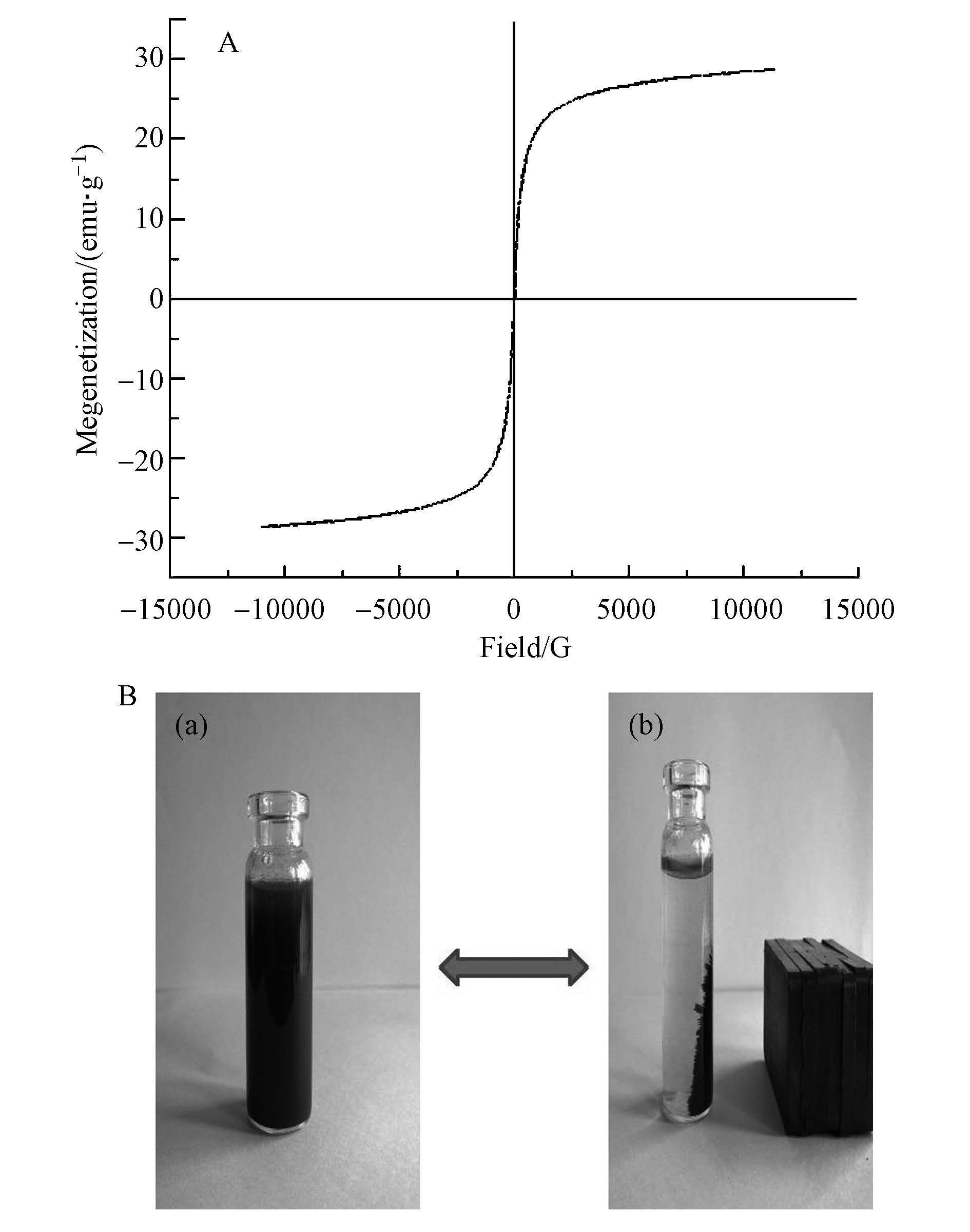 |
| 图4 (A)MHNTs的磁滞回线,(B)外磁场作用图 Fig.4 (A)VSM curve of magnetic halloysite,(B)effect of an externally magnetic field |
研究不同吸附剂初始浓度对十八烷胺吸附效果的影响,控制十八烷胺浓度为1 mg · L-1,T=293.15 K,pH=3.5,反应时间为8 h时取一定体积的十八烷胺溶液,并测定其浓度,考察不同吸附剂初始浓度对十八烷胺的吸附效果影响.由图 5可知,随着MHNTs浓度的增加,对十八烷胺的吸附率逐渐增大,这主要是因为随着吸附剂浓度的增加,对十八烷胺提供的吸附点位就越来越多,对于同一个吸附点位参与竞争的十八烷胺相对有效的减弱,故而吸附率也就越高.从图 5还可以发现分配系数Kd 随着吸附剂浓度的增加而逐渐减小.可能是由于吸附剂添加量的改变,使得吸附剂表面的官能团存在团聚或竞争.即增多的吸附点位提高了十八烷胺的吸附率,同时也增加了官能团之间的竞争,从而使吸附剂的吸附和络合能力下降,导致Kd值的下降(Liu et al., 2012; Zhang et al., 2012).
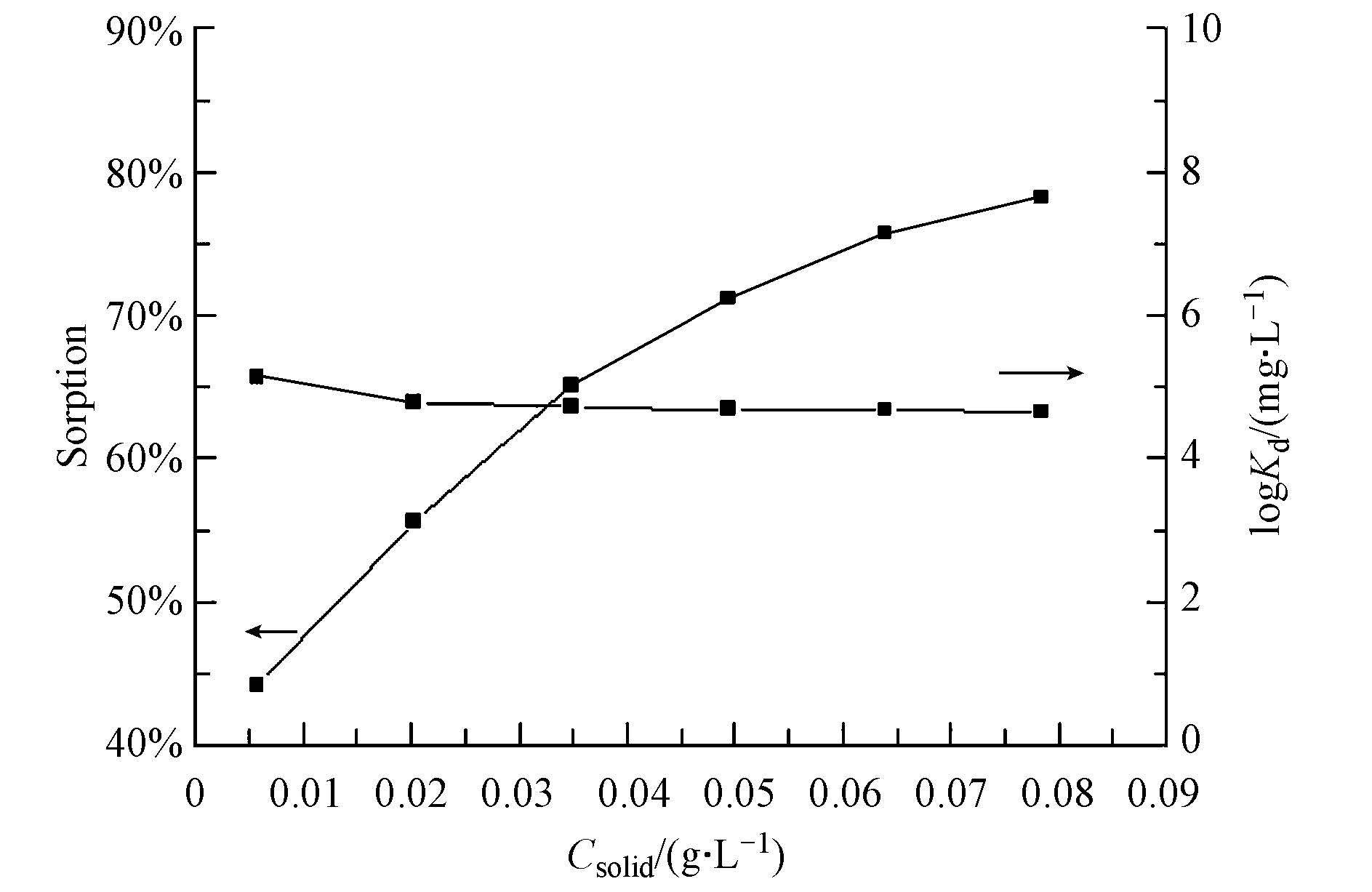 |
| 图5 MHNTs的初始浓度对十八烷胺吸附的影响(实验条件:T=293.15 K,pH=3.5±0.1,C(octadecylamine)initial=1 mg · L-1,I=0.01 mol · L-1 NaCl) Fig.5 Adsorption of octadecylamine on magnetic halloysite a function of solid content |
研究不同吸附时间对十八烷胺吸附效果的影响,控制十八烷胺浓度为1 mg · L-1,T=293.15 K,pH=3.5,吸附剂初始浓度为0.5 mg · L-1时取一定体积的十八烷胺溶液,并测定其浓度,考察不同吸附时间对十八烷胺的吸附效果影响,结果如图 6所示.从图中可以看出,十八烷胺的吸附率随着时间的增加而上升,并且逐渐趋于平衡的状态.在3 h 内吸附率达到平衡,表明了MHNTs吸附十八烷胺以化学吸附为主,物理吸附为辅(刘霞等,2012).为了更好的探索MHNTs对十八烷胺的吸附动力学机理,应用动力学准二级方程式对数据进行分析.方程式如下(卞维柏等,2014):
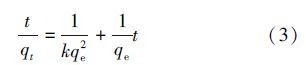
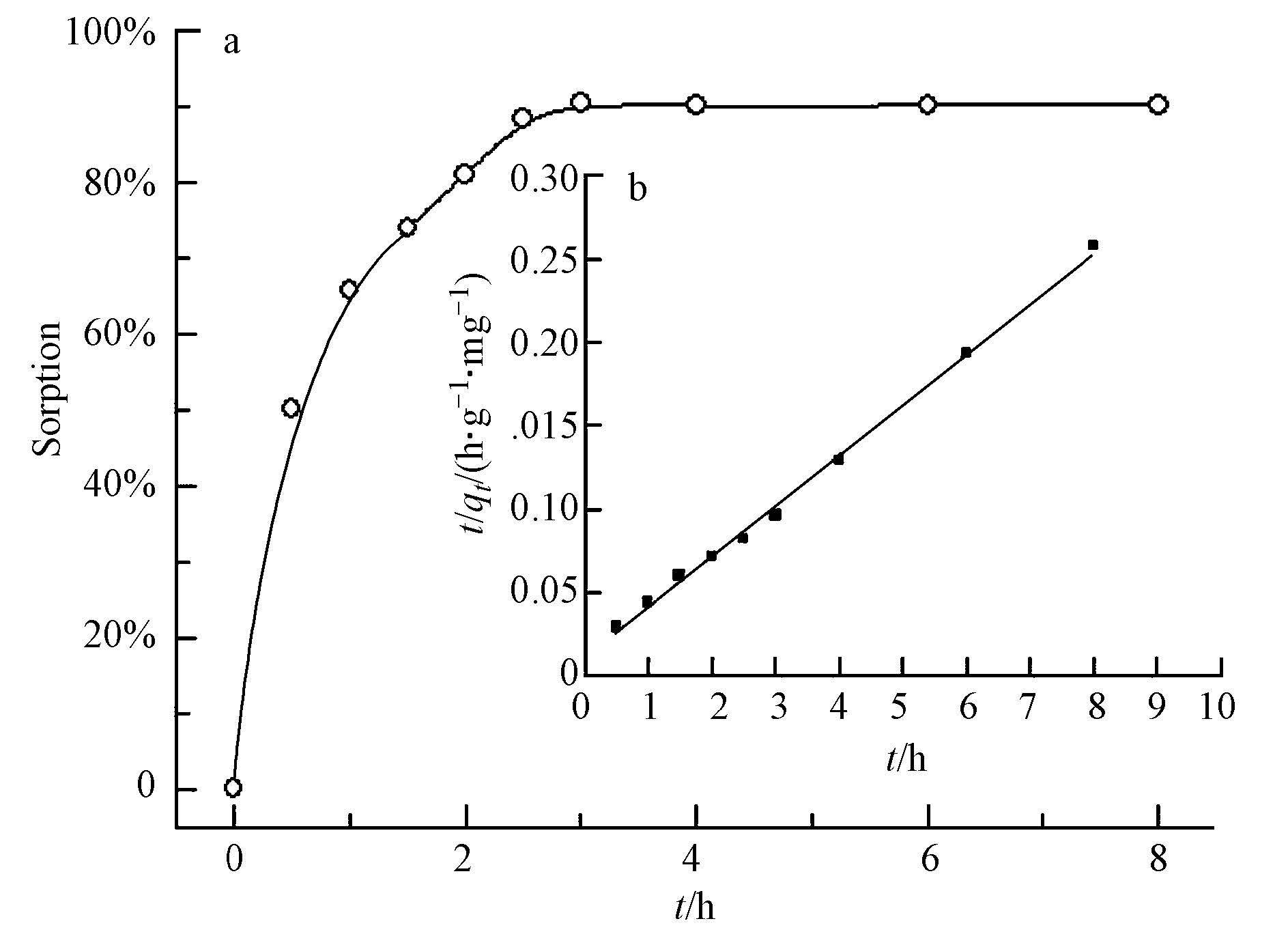 |
| 图6 吸附时间对十八烷胺吸附的影响(a)和磁性埃洛石吸附十八烷胺的准二级动力学程(b)(实验条件:T=293.15 K,pH=3.5 ± 0.1,C(octadecylamine)initial=1 mg · L-1,m/V=0.029 g · L-1,I=0.01 mol · L-1 NaCl) Fig.6 Effect of contact time on the adsorption of octadecylamine on magnetic halloysite(The inset figure is the pseudo-second-order rate equation fit of octadecylamine kinetic adsorption on magnetic halloysite) |
研究不同pH值对十八烷胺吸附效果的影响,控制十八烷胺浓度为1 mg · L-1,T=293.15 K,反应时间为8 h,吸附剂初始浓度为0.5 mg · L-1时取一定体积的十八烷胺溶液,并测定其浓度,考察不同pH值对十八烷胺的吸附效果影响,结果如图 7 所示.从图 7可以看出,溶液的pH值对十八烷胺的吸附效果有直接的影响,随着pH值的增大,吸附率也逐渐增大,pH值到10.6左右,对十八烷胺的吸附率达到最大,当pH > 10.6时,吸附率稍微降低,变化不大.这种变化可能由于埃洛石表面官能团和表面电荷所致.埃洛石的主要化学成分为二氧化硅和氧化铝,其外表面的化学性质类似于二氧化硅的性质和属性,内部圆筒状表面化学性质和氧化铝相关联.体系pH在2~12之间,埃洛石表面带负电荷,由于外层二氧化硅所带的负电荷多余内层圆筒状氧化铝表面的正电荷.随着pH的增加,埃洛石表面带有更多的负电荷,而在pH值较小时,即H+浓度较大,十八烷胺以离子态存在从而增加了埃洛石和十八烷胺之间的静电引力.在另一方面,H+对十八烷胺在磁性埃洛石上存在竞争吸附,所以随着pH值的增大,吸附率增加明显,且主要是通过外层络合或通过与占据了吸附表面点位的H+进行离子交换来实现的.当pH 增大到10.6左右时,十八烷胺以分子态存在于水溶液中,十八烷胺分子中的极性基(—NH2)的中心原子N含有未共享电子对,它可以与Fe的d电子空轨道进行配位结合,从而使得十八烷胺在MHNTs上的吸附率明显增加(严荣珍,2002).从图 7可以看出,磁性埃洛石对十八烷胺的吸附在0.001 mol · L-1 NaCl的溶液中达到最大,在0.1 mol · L-1 NaCl的溶液中最低.表明离子强度影响磁性埃洛石对十八烷胺的吸附效果,可能是由于钠离子对十八烷胺在磁性埃洛石上存在着竞争吸附,或磁性埃洛石吸附十八烷胺的吸附是通过离子交换来实现的.
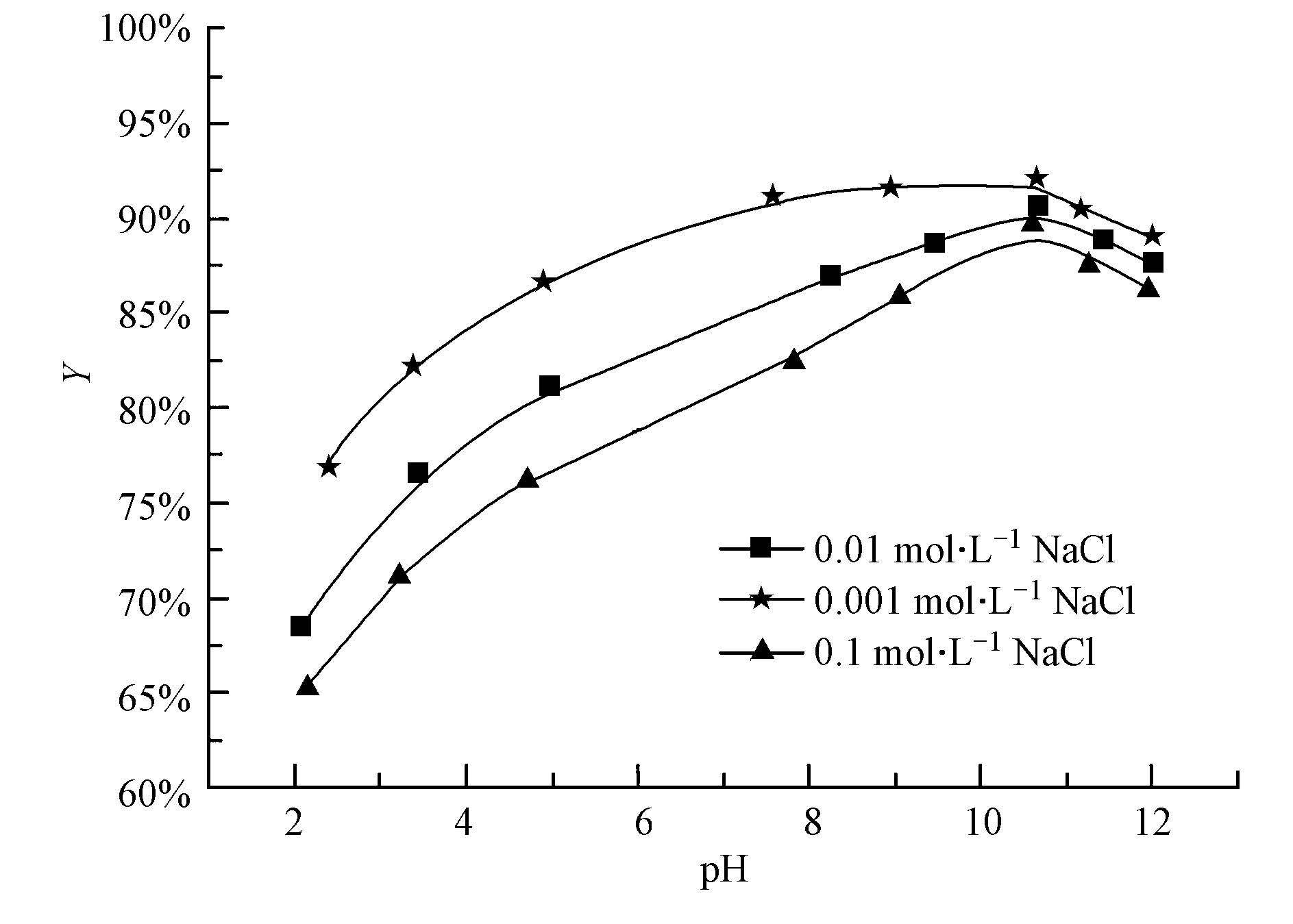 |
| 图7 pH值对磁性埃洛石吸附十八烷胺的影响(实验条件:T=293.15 K,C(octadecylamine)initial=1 mg · L-1,m/V=0.029 g · L-1) Fig.7 Effect of pH on octadecylamine adsorption to magnetic halloysite |
温度对十八烷胺吸附的影响及吸附热力学 研究不同温度对十八烷胺吸附效果的影响,控制pH=3.5,反应时间为8 h,吸附剂初始浓度为0.5 mg · L-1时取一定体积的十八烷胺溶液,并测定其浓度,考察不同温度对十八烷胺的吸附效果影响,结果如图 8 所示.通过在不同温度(T=293.15 K,308.15 K,323.15 K)下对十八烷胺在磁性埃洛石上的吸附进行了研究.由图 8可以看出,在十八烷胺浓度较低的情况下,温度对十八烷胺的吸附效果影响较小.此时,影响吸附效果的主要因素是十八烷胺的初始浓度.但是,整体趋势是随着温度的升高,十八烷胺的吸附量逐渐增大,即升高温度有利于磁性埃洛石对十八烷胺的吸附.
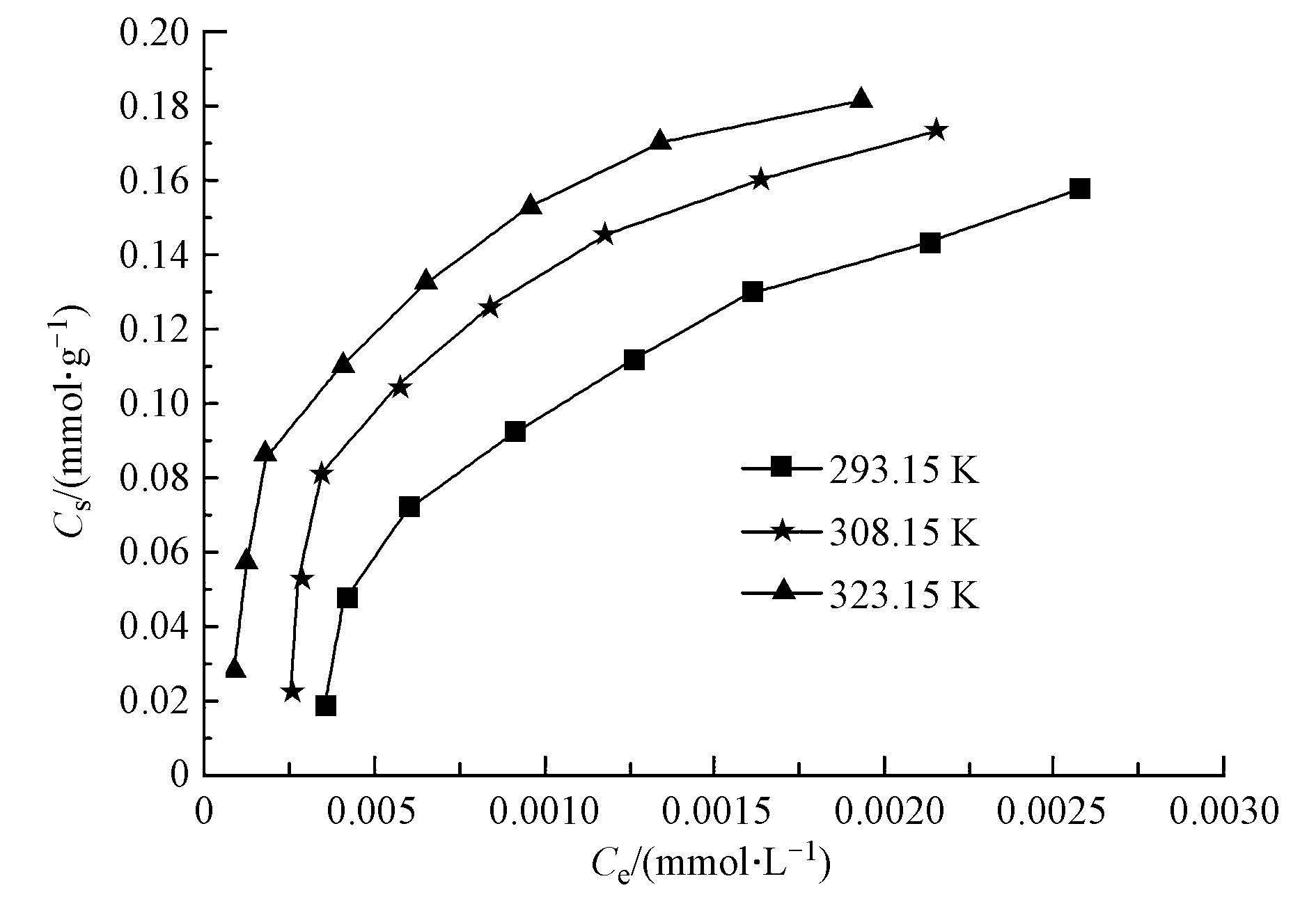 |
| 图8 十八烷胺在不同温度下的吸附等温线(实验条件:pH=3.5 ± 0.1,m/V=0.029 g · L-1,I=0.01 mol · L-1 NaCl) Fig.8 Adsorption isotherms of octadecylamine to magnetic halloysite at different temperatures |
用Langmuir和Freundlich模型对不同温度下十八烷胺在磁性埃洛石上的吸附进行拟合,结果如图 9所示,相关参数示于表 1.图 9(a)是根据Langmuir等温线方程拟合的曲线,表达式如下(田犀卓等,2015):
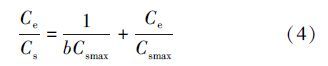
图 9(b)是根据Freundlich等温方程拟合的曲线,表达式如下:
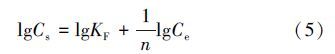
对lgCs—lgCe的线性拟合,则3种温度下的R2值分别为0.992,0.984,0.992.结果表明,十八烷胺在磁性埃洛石上的吸附符合Langmuir模型,是单层吸附.
| 表1 不同温度下Langmuir和Freundlich模拟的拟合参数 Table 1 The parameters for Langmuir and Freundlich isotherms at different temperatures |
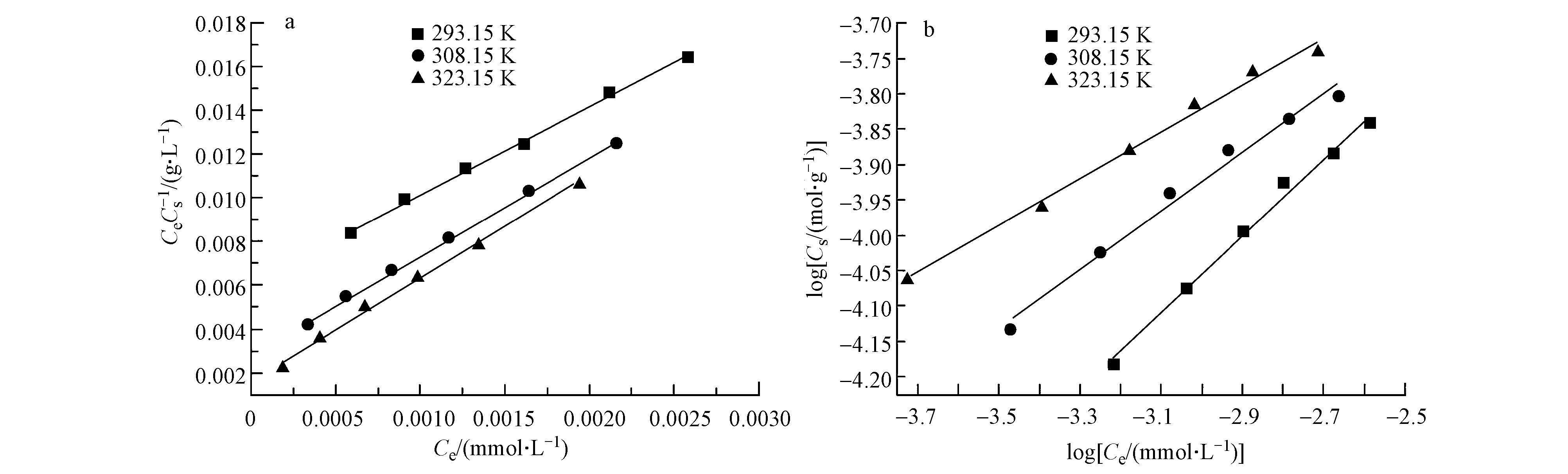 |
| 图9 不同温度下十八烷胺在磁性埃洛石上的吸附模型(实验条件:pH=3.5 ± 0.1,m/V=0.029 g · L-1,I=0.01 mol · L-1 NaCl) Fig.9 Langmuir(a) and Freundlich(b)isotherms of octadecylamine adsorption on magnetic halloysite at different temperature |
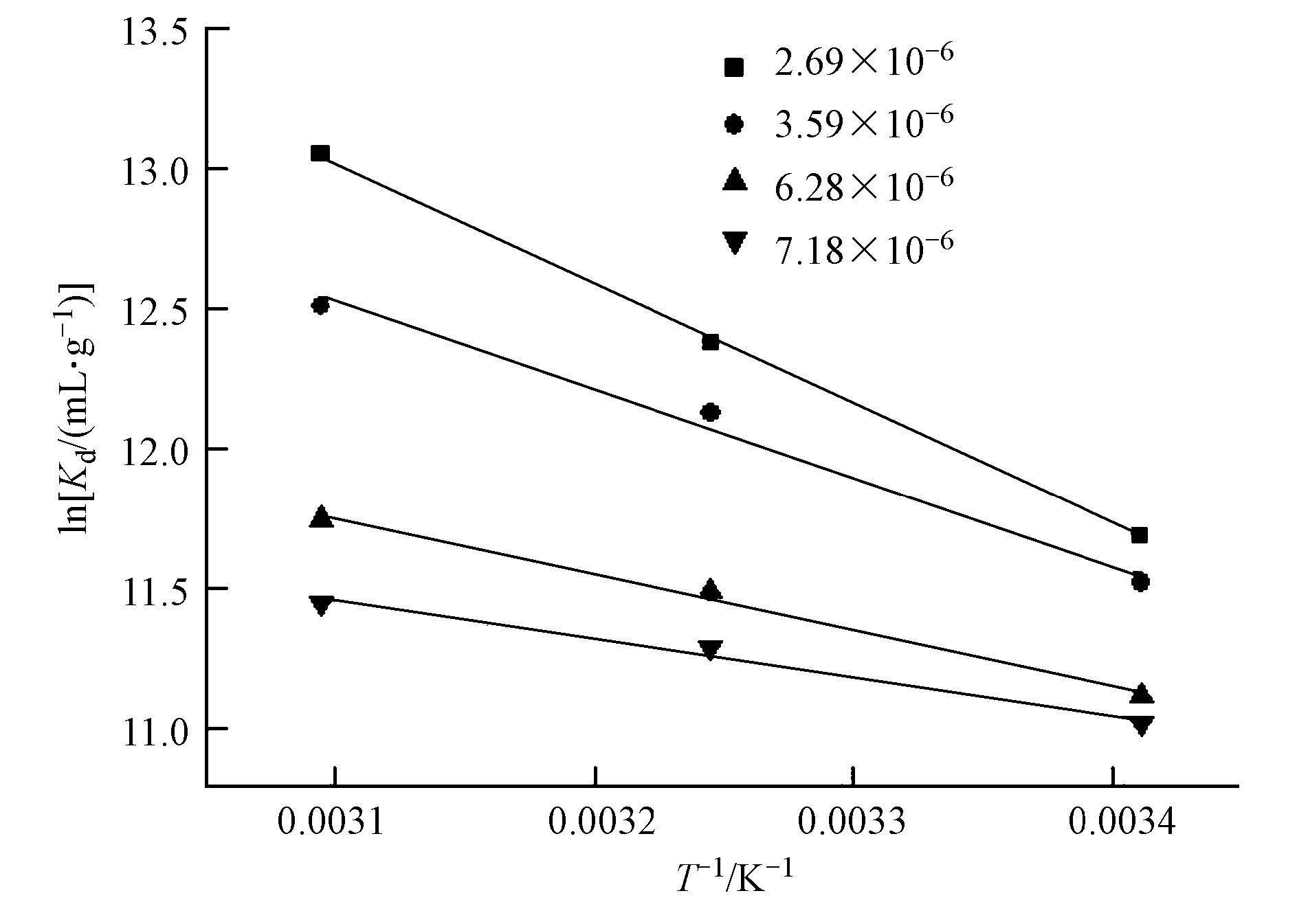 |
| 图10 十八烷胺在磁性埃洛石上吸附的热力学参数(实验条件:pH=3.5 ± 0.1,m/V=0.029 g · L-1,I=0.01 mol · L-1 NaCl) Fig.10 Linear plots of lnKd versus 1/T |
十八烷胺在磁性埃洛石上的吸附相关热力学函数ΔH0,ΔG0,ΔS0,可以由在不同温度下的吸附等温线得到,计算公式见式(6)、式(7):
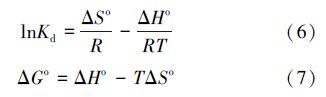
由吸附等温线可以得出表 2中的数据,由表 2可以看出,ΔH0 > 0表明十八烷胺在磁性埃洛石上的吸附是吸热过程,ΔG0 < 0表明十八烷胺在磁性埃洛石上的吸附过程为自发过程,且高温有利于十八烷胺在磁性埃洛石上的吸附.
| 表2 十八烷胺在磁性埃洛石上的吸附热力学参数 Table 2 The thermodynamic data of octadecylamine adsorption on magnetic halloysite at different octadecylamine initial solution concentrations |
1)采用共沉淀法制备Fe3O4/埃洛石复合材料并作为吸附剂,吸附溶液中的十八烷胺.MHNTs具有较高的磁性强度,在外加磁场的条件下,很容易达到固液分离.
2)研究了不同因素对磁性埃洛石吸附十八烷胺的影响,结果表明MHNTs复合材料对十八烷胺具有较好的吸附性能,其最大吸附容量达到66.84 mg · L-1.
3)吸附剂用量、pH值、温度、时间、离子强度等都影响磁性埃洛石对十八烷胺的吸附效果.吸附量随着吸附剂用量、温度和时间的增加,离子强度的减小而增加,pH值为10.6时的吸附效果最好.
| [1] | 卞维柏, 黄卫红, 欧红香, 等. 2014. MY@SiO2-PEI磁性复合生物材料对二元Ce3+/Sr2+混合离子的吸附性能研究[J]. 环境科学学报, 34(7):1716-1723 |
| [2] | 陈进生, 王杭州, 钟爱民. 2003. 十八胺应用中的若干技术问题探讨[J]. 热力发电, 32(5):61-62; 69 |
| [3] | Duan J M, Liu R C, Chen T, et al. 2012. Halloysite nanotube-Fe3O4 composite for removal of methyl violet from aqueous solutions[J]. Desalination, 293:46-52 |
| [4] | 费雯丽, 李贵林. 2012. 大孔树脂吸附法处理卤水中钾盐浮选捕收剂十八胺[J]. 化工矿物与加工, (4):17-20 |
| [5] | 贾佩楠, 马媛媛, 肉斯坦木·热合曼, 等. 2011. 纳米四氧化三铁/埃洛石复合材料及水基磁性流体的制备[J]. 功能材料, 42(3):540-542 |
| [6] | Lee D, Cohen R E, Rubner M F. 2007. Heterostructured magnetic nanotubes[J]. Langmuir, 23(1):123-129 |
| [7] | Liu X, Chen Y T, Chi Y L, et al. 2012. Effect of pH, ionic strength, foreign ions, humic acid and temperature on sorption of radionuclide 60Co(Ⅱ) on illite[J]. Journal of Radioanalytical and Nuclear Chemistry, 292(3):1357-1366 |
| [8] | 刘霞, 陈元涛, 胡君, 等. 2012. pH、离子强度、时间和温度对Cd(Ⅱ)在伊利石上吸附的影响[J]. 核化学与放射化学, 34(6):358-363 |
| [9] | Luo P, Zhao Y F, Zhang B, et al. 2010. Study on the adsorption of neutral red from aqueous solution onto halloysite nanotubes[J]. Water Research, 44(5):1489-1497 |
| [10] | 田犀卓, 金兰淑, 应博, 等. 2015. 钢渣-蒙脱石复合吸附剂对水中Cd2+的吸附去除[J]. 环境科学学报, 35(1):207-214 |
| [11] | Tierrablanca E, Romero-García J, Roman P, et al. 2010. Biomimetic polymerization of aniline using hematin supported on halloysite nanotubes[J]. Applied Catalysis A:General, 381(1/2):267-273 |
| [12] | 夏洋. 2007. 脂肪胺浮选捕收剂光化学降解性能的研究[D]. 武汉:武汉理工大学, 1-60 |
| [13] | Xie Y F, Qian D Y, Wu D L, et al. 2011. Magnetic halloysite nanotubes/iron oxide composites for the adsorption of dyes[J]. Chemical Engineering Journal, 168(2):959-963 |
| [14] | 严荣珍. 2002. 火电机组停用保护剂——十八烷基胺应用商榷[J]. 华北电力技术, (6):32-33 |
| [15] | Yang S T, Zong P F, Hu J, et al. 2013. Fabrication of β-cyclodextrin conjugated magnetic HNT/iron oxide composite for high-efficient decontamination of U (Ⅵ)[J]. Chemical Engineering Journal, 214:376-385 |
| [16] | 袁智成, 董爱娟, 蒋泽权, 等. 2011. Fe3O4/凹凸棒土磁性纳米复合材料的制备与表征[J]. 化学世界, 52(10):603-606 |
| [17] | Zhang C C, Liu Z J, Chen L, et al. 2012. Influence of pH, humic, acid, ionic strength, foreign ions, and temperature on 60Co(Ⅱ) sorption onto γ-Al2O3[J]. Journal of Radioanalytical and Nuclear Chemistry, 292(1):411-419 |
 2016, Vol. 36
2016, Vol. 36


