石墨烯是由sp2杂化的碳原子构成的二维新型材料,具有奇特的物理化学特性.近年来,石墨烯及其衍生物在电子器件、能源、环境等领域得到了广泛关注(Gadipelli et al., 2015; Kucinskis et al., 2013).氧化石墨烯(GO)被认为是表面功能化的石墨烯,除了拥有高比表面积外,表面富有如羟基、羧基、环氧基和羰基等含氧官能团,容易与重金属离子发生络合(Zhang et al., 2011; Zhao et al., 2011);同时,GO结构中的π电子共轭键可以高效吸附带有苯环的有机物(Pei et al., 2013; Wang et al., 2014).例如,Yang等(2010)发现,GO对Cu(Ⅱ)的吸附能力比活性炭高10倍以上;Bradder等(2010)研究表明,GO吸附有机染料的吸附能力也显著高于活性炭,其对亚甲基蓝的吸附量高达351 mg · g-1.上述研究结果均表明,GO在环境修复领域中的应用具有广阔的发展前景.GO对污染物的吸附性能与其比表面积及表面含氧量密切相关,更高的比表面及更多的含氧官能团均能显著增加GO的吸附位点(Zhu et al., 2010; Garcia-Gallastegui et al., 2012).因此,发展一种简便高效的GO制备方法显得尤为重要.Hummers法是最为经典常见的方法,但制备操作过程较为繁琐(Marcano et al., 2010; Dreyer et al., 2010).为了提高制备效率和产品质量,本文拟优化制备过程中的反应条件,通过改良Hummers法(Stankovich et al., 2006; Chen et al., 2009)制备GO,并对其微观结构及表面官能团进行表征.
实际污染水体中不会仅有单一污染物,而是常以有机物-重金属复合污染的形式存在(Brown et al., 2006; Scheibye et al., 2014).不同类型的污染物在水体中的环境化学行为不仅相互独立而又相互联系(Haarstad et al., 2011),因此,进一步探究其在吸附剂表面的吸附行为对于寻求切实有效的环境修复途径具有重要意义.到目前为止,有关GO对有机物-重金属复合污染的吸附特征和机理的研究鲜见报道,限制了GO作为新型高效吸附剂的应用拓展.因此,本文分别选取亚甲基蓝(MB)和Cu(Ⅱ)作为有机物及重金属离子的典型污染物,研究其在GO表面上的单独吸附和共吸附行为,并探讨可能存在的吸附过程及机制,以期为发展石墨烯基吸附剂治理实际水体污染提供理论基础.
2 材料与方法(Materials and methods) 2.1 试剂与仪器试剂:石墨粉购自阿拉丁试剂(上海)公司;浓硫酸购自衡阳市凯信化工试剂有限公司;高锰酸钾购自天津市博迪化工有限公司;30%过氧化氢、无水乙醇购自广东光华科技股份有限公司;硝酸铜亚甲基蓝购自国药集团化学试剂有限公司;所有化学试剂均为分析纯,使用前未做任何进一步纯化.
仪器:UV-752 紫外可见分光光度计(上海凤凰光学科仪有限有限公司);AA240 火焰原子吸收光谱仪(美国瓦里安(中国)有限公司);LGJ-12 冷冻干燥机(北京松源华兴科技发展有限公司);ThZ-320 台式恒温振荡器(上海精宏实验设备有限公司).
2.2 氧化石墨烯(GO)的制备采用改良Hummers法氧化石墨粉合成GO.具体操作为:将2.00 g石墨粉加入到含有35 mL的浓硫酸中,均匀搅拌2 h;缓慢加入6 g KMnO4使得混合物的温度保持在293 K以下,然后放在308 K的水浴锅中保持4 h后,缓慢加入90 mL去离子水稀释,充分搅拌1 h,便可得到深褐色悬浮液;再逐渐加入30%的H2O2,直到颜色变为亮黄色,趁热抽滤;再用5%的盐酸进行洗涤,去除其中的锰盐,并使得溶液变为中性,然后用超声波使之分散,冷冻干燥,即可得到固态GO.
2.3 GO的表征采用日本JEOL公司的JSM-7500 型扫描电子显微镜(SEM)考察样品的表面形貌和微观形态.采用美国FEI公司的FEI Tecnai G20 型透射电子显微镜(TEM)对样品的微观结构进行分析.采用美国THERMO NICOLET公司的Thermo Nicolet 5700 红外光谱仪测定试样的傅里叶变换红外光谱(FTIR)谱图,KBr压片,扫描范围4000~400 cm-1.采用荷兰帕纳科公司的X′Pert PRO型X射线粉末衍射仪(Cu Kα)对试样进行晶相分析,管电压40 kV,管电流40 mA,扫描范围2θ为5°~80°,扫描速度5.3° · min-1.采用Horiba Jobin Yvon 公司的LabRAM HR800型激光共聚焦拉曼光谱仪对样品结构进行分析.
2.4 单独吸附实验Cu(Ⅱ)的吸附实验:吸附实验在锥形瓶中进行,称取0.02 g GO投加到含20 mL 50 mg · L-1Cu(Ⅱ)的锥形瓶中,在温度为303 K、250 r · min-1摇床中振荡,分别在0、2、10、30、60、90、120、150 min时各取样2 mL;然后将样液稀释,0.45 μm滤膜过滤,取滤液用火焰原子吸收法测定各样液Cu(Ⅱ)浓度,以吸附量来评价GO对Cu(Ⅱ)的吸附性能.
MB的吸附实验:吸附实验在锥形瓶中进行,称取0.02 g GO投加到含20 mL 500 mg · L-1MB的锥形瓶中,在温度为303 K、250 r · min-1摇床中振荡,分别在0、2、10、30、60、90、120、150 min时各取样2 mL,然后将样液稀释,0.45 μm滤膜过滤,取滤液用紫外可见分光光度计于665 nm处测定各样液吸光度,通过MB浓度对吸光度的标准曲线计算出MB的浓度,以吸附量来评价GO对MB的吸附性能.
2.5 共吸附试验 2.5.1 不同浓度Cu(Ⅱ)对MB吸附性能影响实验吸附实验在锥形瓶中进行,分别称取0.02 g GO投加到20 mL含有400、500 mg · L-1 MB与0、10、20、30、40和50 mg · L-1Cu(Ⅱ)混合液的锥形瓶中,在温度为303 K、250 r · min-1摇床中振荡150 min后达到吸附平衡;取样稀释,0.45 μm滤膜过滤,取滤液用紫外可见分光光度计于665 nm处测定样液中MB吸光度,并根据MB浓度对吸光度的标准曲线计算出各样液MB浓度,通过吸附量来分析Cu(Ⅱ)浓度对MB吸附性能影响关系.
2.5.2 不同浓度MB对Cu(Ⅱ)吸附性能影响实验吸附实验在锥形瓶中进行,分别称取0.02 g GO投加到20 mL含有30、50 mg · L-1 Cu(Ⅱ)与0、100、200、300、400、500 mg · L-1MB混合液的锥形瓶中,在温度为303 K、250 r · min-1摇床中振荡150 min后达到吸附平衡;取样稀释,0.45 μm滤膜过滤,取滤液用火焰原子吸收法测定样液中Cu(Ⅱ)浓度,以吸附量来分析MB浓度对Cu(Ⅱ)吸附性能影响关系.
3 结果与讨论(Results and discussion) 3.1 氧化石墨烯(GO)结构表征图 1a是GO的SEM图,可以明显看出其表面存在波纹和褶皱.这是由于GO具有自发降低表面能的趋势,导致表面收缩卷曲,使得其二维结构趋于稳定(Kim et al., 2012);同时也说明了改良Hummers法制备的GO有较高的比表面积和良好的柔性(Wang et al., 2012).相应的TEM图像(图 1b)显示出制备的GO为高度褶皱且衬度较低的薄纱状形貌,片层厚度很小,说明改良Hummers法能有效实现对石墨的氧化剥离,形成寡层或单层的GO.上述实验结果证实,本文采用的改良Hummers法成功制备出了薄层GO.
 |
| 图 1 GO的扫描电镜图(a)和透射电镜图(b) Fig.1 The SEM(a) and TEM(b)images of GO |
为了进一步探究GO表面含有的官能团,对制备原料石墨粉及GO进行了FTIR测试.由图 2可见,石墨粉并不存在明显的特征吸收峰,而GO在3403 cm-1处有一个宽强峰,为O—H的伸缩振动峰,在1729、1620、1382和1051 cm-1处分别是C O伸缩振动峰、C C的伸缩振动峰、叔羟基的特征峰和C—O的伸缩振动峰(Marcano et al., 2010; Chen et al., 2012).上述结果表明,改良Hummers法将石墨充分氧化剥离,成功制备出了富含氧化官能团的GO.
 |
| 图 2 GO与石墨粉的红外光图谱 Fig.2 FTIR spectra of graphite and GO |
石墨被氧化剥离成寡层的GO后,结构中引入了大量的含氧官能团,导致内部的原子排列方式发生变化(Kudin et al., 2008; Yang et al., 2009).为了探析这些理化性质变化对吸附性能的影响,本文对石墨粉和GO进行了XRD和Raman分析.图 3a为石墨粉及GO的XRD谱图,通过对比可以看出,石墨粉在2θ= 26.6°处出现一个明显的特征峰,对应石墨结构的(002)晶面(Krishnamoorthy et al., 2013).GO在该处并未出现特征峰,而是在2θ = 10.0°处出峰,这对应GO的(100)晶面(Marcano et al., 2010).特征衍射峰向小角度方向偏移,说明碳结构发生了晶格畸变,氧化过程将大量官能团并入石墨的层间,改变了石墨的固有结构,使得单原子层或寡层的GO被剥离,增加了材料的比表面积和吸附位点(Yang et al., 2009; Wang et al., 2009).
 |
| 图 3 GO与石墨粉的XRD图(a)和拉曼光谱图(b) Fig.3 XRD patterns(a) and Raman spectra(b)of GO and graphite |
图 3b为Raman谱图,从图中可以看出,石墨粉与GO均出现了D峰(~1360 cm-1)和G峰(~1580 cm-1),相比石墨粉,GO的峰形宽钝,峰位置发生了红移,且D峰明显强于石墨粉.D峰是由sp2杂化的碳原子呼吸振动产生,反映了石墨内部结构的缺陷情况,G峰的产生是碳环或长链中sp2杂化的原子对拉伸运动所致,代表着石墨结构的对称性和有序度(Kudin et al., 2008).Raman分析中常以D峰与G峰的峰强比值(ID/IG)来表示石墨的无序度,比值越高说明无序度越大、缺陷越多(Kudin et al., 2008; Marcano et al., 2010).通过计算发现,石墨粉的ID/IG=0.37,而GO的ID/IG=0.91.显然,石墨被氧化后结构的无序度增加,这是由于石墨在氧化剥离的过程中,含氧官能团与表面碳原子连结,形成无序结构的sp3杂化键,破坏了石墨晶格的有序结构;同时,D峰与G峰的非对称宽化和红移也进一步证明了石墨结构无序度的增加(Chen et al., 2012).由上述结果可知,改良Hummers成功制备出了富有含氧官能团和结构缺陷的GO,为下一步探究GO对有机物-重金属复合污染的共吸附行为奠定了基础.
3.2 GO单独吸附行为根据以上对GO结构表征结果可知,改良Hummers法制备的GO为高度褶皱的薄纱状结构,且富有含氧官能团及结构缺陷,能为污染物吸附提供大量的吸附位点,说明GO是潜在的一种高效吸附剂(Li et al., 2013; Zhao et al., 2011).为了进一步探讨GO的吸附性能,对GO分别进行了单独吸附重金属Cu(Ⅱ)和亚甲基蓝(MB)的实验,结果如图 4所示.从图 4可以看出,在2 min内GO对Cu(Ⅱ)和MB的吸附率就分别达到49.7%和80.8%,并在90 min和60 min时达到吸附平衡,这说明GO具有很好的吸附性能.此外,通过对比发现,GO对MB的吸附速率和吸附量都明显高于对Cu(Ⅱ)的吸附,GO对Cu(Ⅱ)的平衡吸附量为29.1 mg · g-1,而对MB的平衡吸附量高达424.2 mg · g-1,说明GO表面对MB的吸附性能显著强于Cu(Ⅱ).GO对Cu(Ⅱ)与MB的吸附是多种作用力共同作用的结果:GO表面富有大量含氧官能团,呈现负电性,而水溶液中Cu(Ⅱ)与MB均带正电,这使得GO能够通过静电吸引与污染物发生吸附;GO表面的含氧官能团(如羧基、羟基等)能够与Cu(Ⅱ)发生络合吸附(Zhao et al., 2011; 王建龙等,2015);同时,MB的分子结构中存在苯环结构的大π共轭体系,极易与GO的π网络结构形成π-π堆积效应(Li et al., 2013; Yang et al., 2011),导致GO对MB的强吸附.
 |
| 图 4 GO吸附Cu(Ⅱ)(a)与MB(b)的吸附量与吸附率变化曲线 Fig.4 The adsorption of Cu(Ⅱ)(a) and MB(b)by GO |
然而,在自然环境的污染水体中,常常是以重金属及有机物复合污染的形式存在.根据GO单独吸附的研究结果可知,GO对Cu(Ⅱ)与MB都具有很好的吸附性能.探究GO对Cu(Ⅱ)与MB复合污染的共吸附行为具有更重要的理论价值.本文进一步研究了Cu(Ⅱ)与MB同时存在时,不同浓度的Cu(Ⅱ)对GO吸附MB的影响,以及不同浓度的MB对Cu(Ⅱ)吸附效果的作用.
3.3.1 不同浓度的Cu(Ⅱ)对GO吸附MB的影响在不改变反应温度(303 K)和GO投加量(1 g · L-1)的条件下,本文探讨了一系列不同浓度(0~50 mg · L-1)的Cu(Ⅱ)对GO吸附MB(C0 = 400~500 mg · L-1)的影响,结果如图 5所示.从图中可以发现以下现象:首先,吸附量变化曲线与溶液中的Cu(Ⅱ)浓度密切相关,随着Cu(Ⅱ)浓度的增加,GO对MB的吸附量逐渐降低,MB的初始浓度为500 mg · L-1时,吸附量由424.2 mg · g-1降至322.6 mg · g-1,初始浓度为400 mg · L-1时,吸附量由326.6 mg · g-1降为286.2 mg · g-1,这说明了Cu(Ⅱ)与MB存在竞争吸附关系,Cu(Ⅱ)与GO表面的含氧官能团发生络合吸附,导致GO部分吸附位点被Cu(Ⅱ)占据,产生空间位阻效应,弱化了GO与MB之间的π-π堆积效应,使得GO对MB的吸附量下降;其次,两条曲线的变化率随着Cu(Ⅱ)浓度的增加而减小,这可能是由于在高浓度的Cu(Ⅱ)溶液中,GO表面的含氧官能团均与其发生络合,吸附位点不再因Cu(Ⅱ)浓度增加而损减,MB的吸附量也趋于稳定;最后,在复合污染水体中,高浓度的MB仍然保有很高的吸附量,这说明π-π堆积效应使得GO与MB之间存在强烈的相互吸引力(Li et al., 2013).综上,Cu(Ⅱ)对GO吸附MB起着一定的抑制作用,这可能是由于被吸附在GO表面的Cu(Ⅱ)所产生的空间位阻效应所致.
 |
| 图 5 不同浓度Cu(Ⅱ)对MB吸附量的影响 Fig.5 Effect of different concentrations of Cu(Ⅱ)on the adsorption of MB |
与前文研究类似,本文进一步探讨了不同浓度(0~500 mg · L-1)的MB对GO吸附Cu(Ⅱ)(C0 = 30~50 mg · L-1)的影响,得到的实验结果如图 6所示.两条吸附量变化曲线都是随着MB浓度的增加而迅速下降,最后趋于平稳;Cu(Ⅱ)的初始浓度为50 mg · L-1时,吸附量由29.1 mg · g-1减到2.4 mg · g-1,初始浓度为30 mg · L-1时,则由19.1 mg · g-1降到2.0 mg · g-1.当复合污染水体中的MB浓度达到200 mg · L-1时,GO对Cu(Ⅱ)的吸附量几乎完全受到抑制,这可能是由于GO与MB之间存在强烈的π-π堆积效应,导致GO表面的含氧官能团被吸附的MB分子层掩盖,丧失了GO络合吸附Cu(Ⅱ)的活性位点.以上结果说明,MB对GO吸附Cu(Ⅱ)也具有明显的抑制作用,同时比Cu(Ⅱ)对吸附MB的影响要强,这也间接证实了GO对MB的共轭吸附作用明显强于对Cu(Ⅱ)的络合吸附.与已经报道的同时吸附MB和Cu(Ⅱ)的其他材料相比,GO具有更好的吸附能力,不同吸附剂对MB和Cu(Ⅱ)吸附能力比较见表 1.
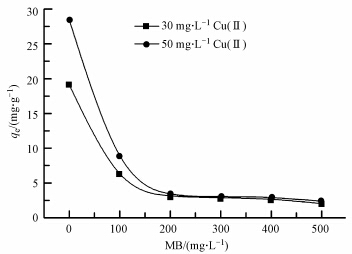 |
| 图 6 不同浓度MB对Cu(Ⅱ)吸附量的影响 Fig.6 The effect of different concentrations of MB on the adsorption of Cu(Ⅱ) |
| 表 1 不同吸附剂对MB和Cu(Ⅱ)吸附能力的比较 Table 1 Adsorption capacities of various adsobents for MB and Cu(Ⅱ) |
本文采用改良Hummers法成功制备了高比表面积并富有含氧官能团的GO,通过SEM、TEM、FTIR、XRD和Raman等手段对其微观形貌及结构进行了表征,并研究了GO对有机物及重金属污染物的单独和共吸附行为.在单独吸附研究中,GO对Cu(Ⅱ)及MB都具有较高的吸附性能,对MB(qe≈424.2 mg · g-1)的吸附性能显著强于Cu(Ⅱ)(qe≈29.1 mg · g-1).在GO的共吸附行为研究中,发现Cu(Ⅱ)与MB在GO表面的吸附存在竞争关系,主要表现在MB与Cu(Ⅱ)彼此互相抑制对方的吸附行为,且MB对Cu(Ⅱ)吸附的抑制作用明显较强,这可能是由于GO与MB之间的π-π堆积效应强于对Cu(Ⅱ)的络合吸附作用.下一步工作将针对Cu(Ⅱ)与MB的吸附机理及竞争原理进行深入研究.
| [1] | Bradder P,Ling S K,Wang S B,et al.2010.Dye adsorption on layered graphite oxide[J].Journal of Chemical & Engineering Data,56(1):138-141 |
| [2] | Brown J N,Peake B M.2006.Sources of heavy metals and polycyclic aromatic hydrocarbons in urban stormwater runoff[J].Science of the Total Environment,359(1/3):145-155 |
| [3] | Chen T,Zeng B Q,Liu J L,et al.2009.High throughput exfoliation of graphene oxide from expanded graphite with assistance of strong oxidant in modified Hummers method[J].Journal of Physics:Conference Series,188(1):012051 |
| [4] | Chen D,Feng H B,Li J H.2012.Graphene oxide:preparation,functionalization,and electrochemical applications[J].Chemical Reviews,112(11):6027-6053 |
| [5] | Dreyer D R,Park S,Bielawski C W,et al.2010.The chemistry of graphene oxide[J].Chemical Society Reviews,39(1):228-240 |
| [6] | Fan H W,Zhou L M,Jiang X H,et al.2014.Adsorption of Cu2+ and methylene blue on dodecyl sulfobetaine surfactant-modified montmorillonite[J].Applied Clay Science,95:150-158 |
| [7] | Gadipelli S,Guo Z X.2015.Graphene-based materials:Synthesis and gas sorption,storage and separation[J].Progress in Materials Science,69:1-60 |
| [8] | Garcia-Gallastegui A,Iruretagoyena D,Gouvea V,et al.2012.Graphene oxide as support for layered double hydroxides:enhancing the CO2 adsorption capacity[J].Chemistry of Materials,24(23):4531-4539 |
| [9] | Haarstad K,Bavor H J,Maehlum T.2011.Organic and metallic pollutants in water treatment and natural wetlands:a review[J].Water Science & Technology,65(1):76-99 |
| [10] | Kim J,Cote L J,Huang J X.2012.Two dimensional soft material:new faces of graphene oxide[J].Accounts of Chemical Research,45(8):1356-1364 |
| [11] | Krishnamoorthy K,Veerapandian M,Yun K,et al.2013.The chemical and structural analysis of graphene oxide with different degrees of oxidation[J].Carbon,53:38-49 |
| [12] | Kucinskis G,Bajars G,Kleperis J.2013.Graphene in lithium ion battery cathode materials:A review[J].Journal of Power Sources,240:66-79 |
| [13] | Kudin K N,Ozbas B,Schniepp H C,et al.2008.Raman spectra of graphite oxide and functionalized graphene sheets[J].Nano Letters,8(1):36-41 |
| [14] | Li Y H,Du Q J,Liu T H,et al.2013.Comparative study of methylene blue dye adsorption onto activated carbon,graphene oxide,and carbon nanotubes[J].Chemical Engineering Research and Design,91(2):361-368 |
| [15] | Marcano D C,Kosynkin D V,Berlin J M,et al.2010.Improved synthesis of graphene oxide[J].ACS Nano,4(8):4806-4814 |
| [16] | Pei Z G,Li L Y,Sun L X,et al.2013.Adsorption characteristics of 1,2,4-trichlorobenzene,2,4,6-trichlorophenol,2-naphthol and naphthalene on graphene and graphene oxide[J].Carbon,51:156-163 |
| [17] | Scheibye K,Weisser J,Borggaard O K,et al.2014.Sediment baseline study of levels and sources of polycyclic aromatic hydrocarbons and heavy metals in Lake Nicaragua[J].Chemosphere,95:556-565 |
| [18] | Stankovich S,Piner R D,Chen X Q,et al.2006.Stable aqueous dispersions of graphitic nanoplatelets via the reduction of exfoliated graphite oxide in the presence of poly (sodium 4-styrenesulfonate)[J].Journal of Materials Chemistry,16(2):155-158 |
| [19] | Wang G X,Wang B,Park J,et al.2009.Synthesis of enhanced hydrophilic and hydrophobic graphene oxide nanosheets by a solvothermal method[J].Carbon,47(1):68-72 |
| [20] | Wang H B,Maiyalagan T,Wang X.2012.Review on recent progress in nitrogen-doped graphene:synthesis,characterization,and its potential applications[J].ACS Catalysis,2(5):781-794 |
| [21] | 王建龙,徐乐瑾.2015.石墨烯材料去除重金属及放射性核素的研究[J].环境科学学报,doi:10.13671/j.hjkxxb.2015.0067 |
| [22] | Wang J,Chen Z M,Chen B L.2014.Adsorption of polycyclic aromatic hydrocarbons by graphene and graphene oxide nanosheets[J].Environmental Science & Technology,48(9):4817-4825 |
| [23] | Wu Y J,Zhang L J,Gao C L,et al.2009.Adsorption of copper ions and methylene blue in a single and binary system on wheat straw[J].Journal of Chemical & Engineering Data,54(12):3229-3234 |
| [24] | Yang D X,Velamakanni A,Bozoklu G,et al.2009.Chemical analysis of graphene oxide films after heat and chemical treatments by X-ray photoelectron and Micro-Raman spectroscopy[J].Carbon,47(1):145-152 |
| [25] | Yang S T,Chang Y L,Wang H F,et al.2010.Folding/aggregation of graphene oxide and its application in Cu2+ removal[J].Journal of Colloid and Interface Science,351(1):122-127 |
| [26] | Yang S T,Chen S,Chang Y L,et al.2011.Removal of methylene blue from aqueous solution by graphene oxide[J].Journal of Colloid and Interface Science,359(1):24-29 |
| [27] | Zhang N N,Qiu H X,Si Y M,et al.2011a.Fabrication of highly porous biodegradable monoliths strengthened by graphene oxide and their adsorption of metal ions[J].Carbon,49(3):827-837 |
| [28] | Zhang W J,Zhou C J,Zhou W C,et al.2011b.Fast and considerable adsorption of methylene blue dye onto graphene oxide[J].Bulletin of Environmental Contamination and Toxicology,87(1):86-90 |
| [29] | Zhang R Z,Zhou Y B,Gu X C,et al.2015.Competitive adsorption of methylene blue and Cu2+ onto citric acid modified pine sawdust[J].CLEAN-Soil,Air,Water,43(1):96-103 |
| [30] | Zhao G X,Li J X,Ren X M,et al.2011.Few-layered graphene oxide nanosheets as superior sorbents for heavy metal ion pollution management[J].Environmental Science & Technology,45(24):10454-10462 |
| [31] | Zhu Y W,Murali S,Cai W W,et al.2010.Graphene and graphene oxide:synthesis,properties,and applications[J].Advanced Materials,22(35):3906-3924 |
 2015, Vol. 35
2015, Vol. 35


