2. 湖南农业大学资源环境学院, 长沙 410128;
3. 辽宁石油化工大学化学化工与环境学部, 抚顺 113001;
4. 辽宁省抚顺市林业科学研究所, 抚顺 113008
2. College of Resources and Environment, Human Agricultural University, Changsha 410128;
3. School of Chemistry, Chemical Engineering and Environment, Liaoning Shihua University, Fushun 113001;
4. Fushun Institute of Forestry, Fushun 113008
大型底栖动物是维系河流水生态系统结构和功能的重要组成部分,其生活史的全部或大部分时间生活在河流水体中,具有分布范围广、生物种类丰富、生活周期较长、生活场所较固定及对河流生境受干扰反应敏感的特点,能够响应长时间内流域生境条件的变化(Lewin et al., 2013; Tullos et al., 2006).大型底栖动物群落组成及特征与河流生境因子关系密切,其中河流底质类型、流速、水深及植被等生境条件及DO、TP、TN、BOD5等水质化学因子均在不同程度上影响大型底栖动物群落结构组成、特征与分布(张勇等,2012; Johnson et al., 2012).
大型底栖动物已广泛应用于水环境生物监测与评价.《欧盟水框架指令》(EU Water Framework Directive)采用大型底栖动物种类、生物指数及多元综合指数指示不同程度人类活动压力及环境影响因素(Boix et al., 2005; Solimini et al., 2008; Oliveira et al., 2011).不同土地利用方式可反映人类活动对流域内生态系统的干扰强度(Brown et al., 2013).Arle及渠晓东等研究了不同形式及强度的人类活动对大型底栖动物群落结构与特征的影响(渠晓东等,2013; Arle and Wagner, 2013).吴璟等(2008)研究表明耕地在亚流域、河岸带、局部3个尺度上对大型底栖动物完整性的影响存在差异.在农业区或人居区,人类活动频繁,对河流水质及生境条件影响较大,从而影响大型底栖动物的群落组成及不同生物类群的百分比(Wittman et al., 2013; Sutherland et al., 2012; Rasmussen et al., 2012).Rasmussen及Kibena等通过土地利用方式和格局变化与河流水质及大型底栖动物响应关系研究表明,当原有森林和草地比例减少,农田和城市用地增加对河流水质产生严重影响,使大型底栖动物群落组成发生强烈变化(Kibena et al., 2014; Rasmussen et al., 2012).以森林植被为主的区域,生境条件较为优越,河流底质以不同粒径石质为主,水深较浅,流速较快,河岸带植被覆盖度高,且人类活动较少,对河流生境条件影响小,河流生态系统处于稳定状态,大型底栖动物群落物种丰富(Rasmussen et al., 2013; 王强等,2012).城市与工业生产的发展对河流水质及河流生态环境带来不可避免的影响,城市河岸带人工固化又一定程度削减了河岸植被缓冲带对地表径流污染的净化作用,间接加剧了河流生态系统水体污染程度(Wang et al., 2012).此外,我国北方城市由于“亲水“景观建设的需要,在河流城市段大量建设橡胶坝,使得河流水面扩大,流速变缓,河流水体氧交换能力降低,水体中溶解氧含量下降常导致好氧性生物类群减少或消失(Chessman and McEvoy, 2012).
辽河流域水生态环境整体受人为活动干扰较大,区域内工业及农业活动频繁,人居密度较大,点源污染、农业面源污染及生活垃圾等均对河流水质造成影响,工程设施建设、挖沙等活动破坏河道原有生境条件.本研究选择辽河流域东部典型支流4种不同土地利用方式为主的区域,对大型底栖动物群落结构及特征进行研究,通过对比不同土地利用方式下大型底栖动物群落特征的差异性反映河流生境受干扰程度,旨在揭示土地利用方式-人类活动压力-大型底栖动物群落特征三者之间的相互关系,为实施流域水生态系统目标管理提供科学依据.
2 材料与方法(Materials and methods) 2.1 研究区域概况本研究主要选择辽宁省辽河流域东部清河、凡河(123°38′25"~125°13′42",42°02′13"~ 42°54′38"),区域面积7948.28 km2.研究区域年均气温6.5 ℃,年均降雨量500~650 mm,降水集中在夏季.地势整体呈现为丘陵、山地到冲积平原的变化特征,植被覆盖度由东向西依次降低.土地利用方式主要包括林地、耕地、村落用地及城市用地.其中,区域东部地区以林地为主,河道坡度大,河流流速快,河床底质粒径均值大于西部地区,林地区域人类活动较少,其功能定位多以生物多样性保护为主,以耕地及居民点为主的区域人类活动增多,农业面源污染程度及水土流失现象加重.城区工业发展迅速且人居密度大,河岸带多固化,河流污染负荷较大.
2.2 采样点位布设首先,在Arcgis环境中,以清河、凡河及主要支流水系为中心进行各河岸缓冲区操作,在河岸带设置1000 m缓冲区,再将缓冲区边界与辽宁省土地利用数据相结合处理,得出1000 m河岸缓冲区范围内的土地利用数据.通过河岸缓冲区内不同土地利用方式及面积的计算,得出主要土地利用类型包括林地(15.2%)、旱田(26.8%)、水田(11.9%)、村落用地(28.6%)、城市用地(17.5%),将旱田与水田统称为耕地.在林地、耕地、村落用地(以下称为居民点)及城市用地每种土地利用类型区布设5个采样点,结合野外调查的实际情况,进行适当调整,共布设20个采样点位(见图 1),分为4组,分别为组1、组2、组3及组4,土地利用类型及采样点位分组情况见表 1.
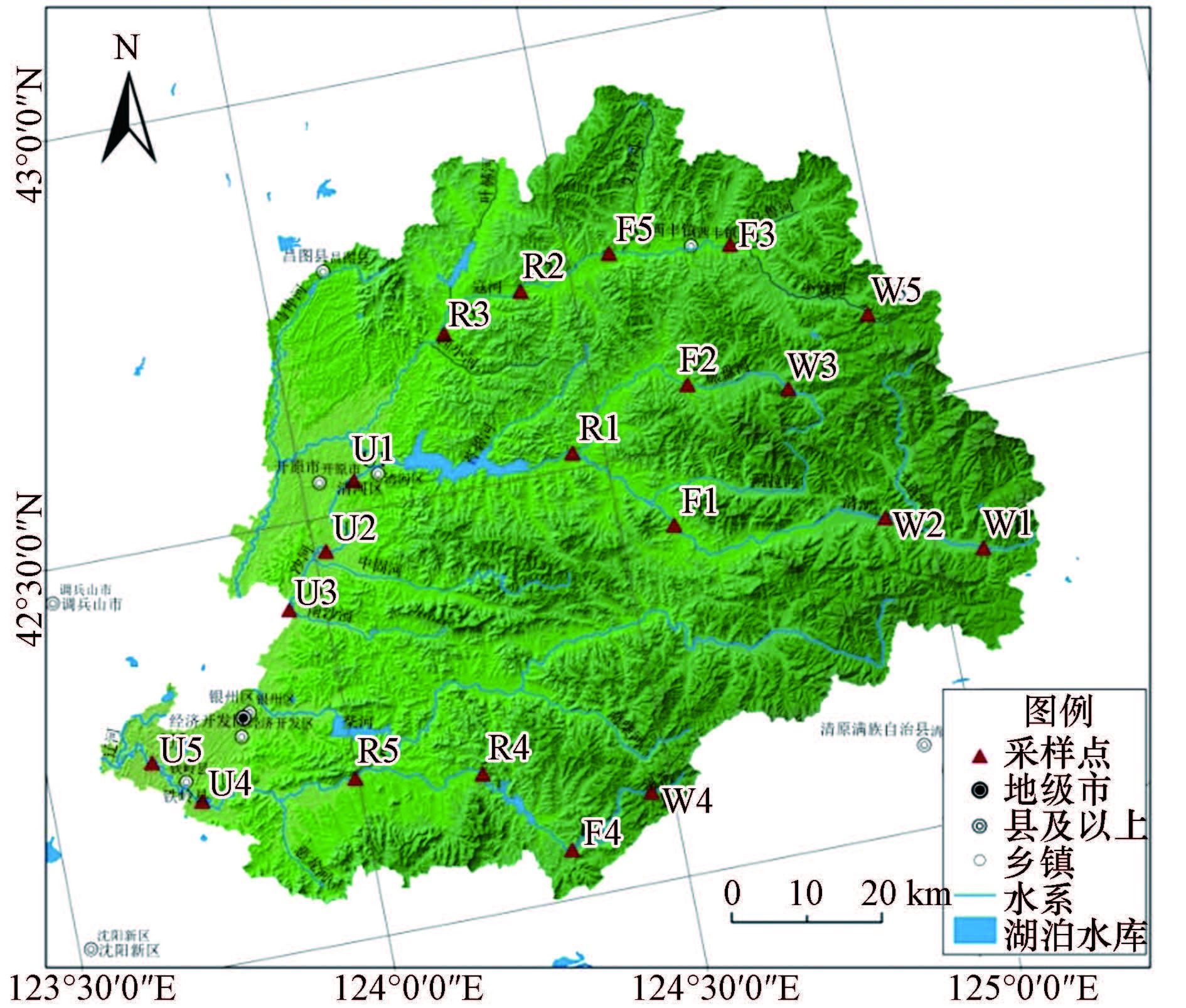 |
| 图1 4种不同土地利用类型区采样点位分布图 Fig.1 Sampling sites in four major l and -use types |
| 表1 不同土地利用类型及采样点位分组 Table 1 Different kinds of l and -use types and sampling sites groups |
采用索伯网(40 cm×40 cm,425 μm)采集大型底栖动物样品,每个点位分别选择不同的微生境重复采样3次.样品采集时,将索伯网下边框固定在水底,将边框内的石块捡至采样桶内,洗净,并搅动边框内底质,将索伯网内生物清洗到采样桶内,过40目筛,放入500 mL塑料瓶中并加固定剂保存.大型底栖动物样品分离及镜检,大型底栖动物分类及鉴定主要参考《Aquatic insects of China useful for monitoring water quality》(Morse et al., 1994)及《淡水生物学》(大连水产学院,1982).
对采样点的底质粒径、流速、水深、DO等生境指标通过流速仪、便携式溶氧仪现场测定与记录.其中底质根据不同等级粒径百分比及其对大型底栖动物生存适宜性进行综合评分,总氮(TN)、总磷(TP)、氨氮(NH3-N)、5日生化需氧量(BOD5)、重铬酸钾指数(CODCr)等水质化学指标分别采用碱性过硫酸钾消解紫外分光光度法、钼酸铵分光光度法、纳氏试剂比色法、稀释与接种法、重铬酸盐法在实验室内测定.野外调查分别于2010年10月(平水期)、2011年5月(枯水期)和8月(丰水期)进行,对各采样点大型底栖动物及环境因子进行样品采集与测定.
2.4 数据处理
通过大型底栖动物基础数据整理得到群落组成及生物指数,包括Shannon-Wiener多样性指数(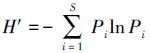 ,S为物种丰度,Pi为第i种个体数占样品总个体数N的比例,下同)、改进Shannon-Wiener多样性指数(
,S为物种丰度,Pi为第i种个体数占样品总个体数N的比例,下同)、改进Shannon-Wiener多样性指数(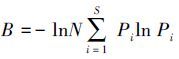 )、丰富度指数(dm=(S-1)/lnN)、均匀度指数(J=H′/lnS)、FBI(Family Biotic Index,
)、丰富度指数(dm=(S-1)/lnN)、均匀度指数(J=H′/lnS)、FBI(Family Biotic Index,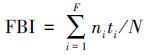 ,ni为第i科的个体数,ti为第i科的耐污值(段学花等,2010)).运用SPSS对不同时空尺度大型底栖动物群落组成及多样性指数与生境因子进行双因素方差分析,采用Tukey HSD法对双因素方差分析结果进行差异性检验.将各组分的不同生境指标与大型底栖动物多样性指数进行Spearman相关性分析,NMDS(Non-metric Multidimensional Scaling)应用于不同组分间底栖动物群落相似性分析,BIO-ENV方法应用于大型底栖动物群落组成影响最大及最优环境因子组合的筛选,其中NMDS及BIO-ENV分析均在Primer5.0中完成.
,ni为第i科的个体数,ti为第i科的耐污值(段学花等,2010)).运用SPSS对不同时空尺度大型底栖动物群落组成及多样性指数与生境因子进行双因素方差分析,采用Tukey HSD法对双因素方差分析结果进行差异性检验.将各组分的不同生境指标与大型底栖动物多样性指数进行Spearman相关性分析,NMDS(Non-metric Multidimensional Scaling)应用于不同组分间底栖动物群落相似性分析,BIO-ENV方法应用于大型底栖动物群落组成影响最大及最优环境因子组合的筛选,其中NMDS及BIO-ENV分析均在Primer5.0中完成.
在4种土地利用方式下,20个点位共采集大型底栖动物42种,隶属3门4纲24科.物种丰度最大值出现在以林地利用为主的河流中,丰度均值为23;最小丰度在城市组,丰度值为11(图 2).由表 2可知,4种土地利用方式及不同水期物种丰度呈显著性差异(p=0.000,p=0.015).时空双因素综合分析表明,大型底栖动物物种丰度在时间、空间双因素作用下差异不显著.
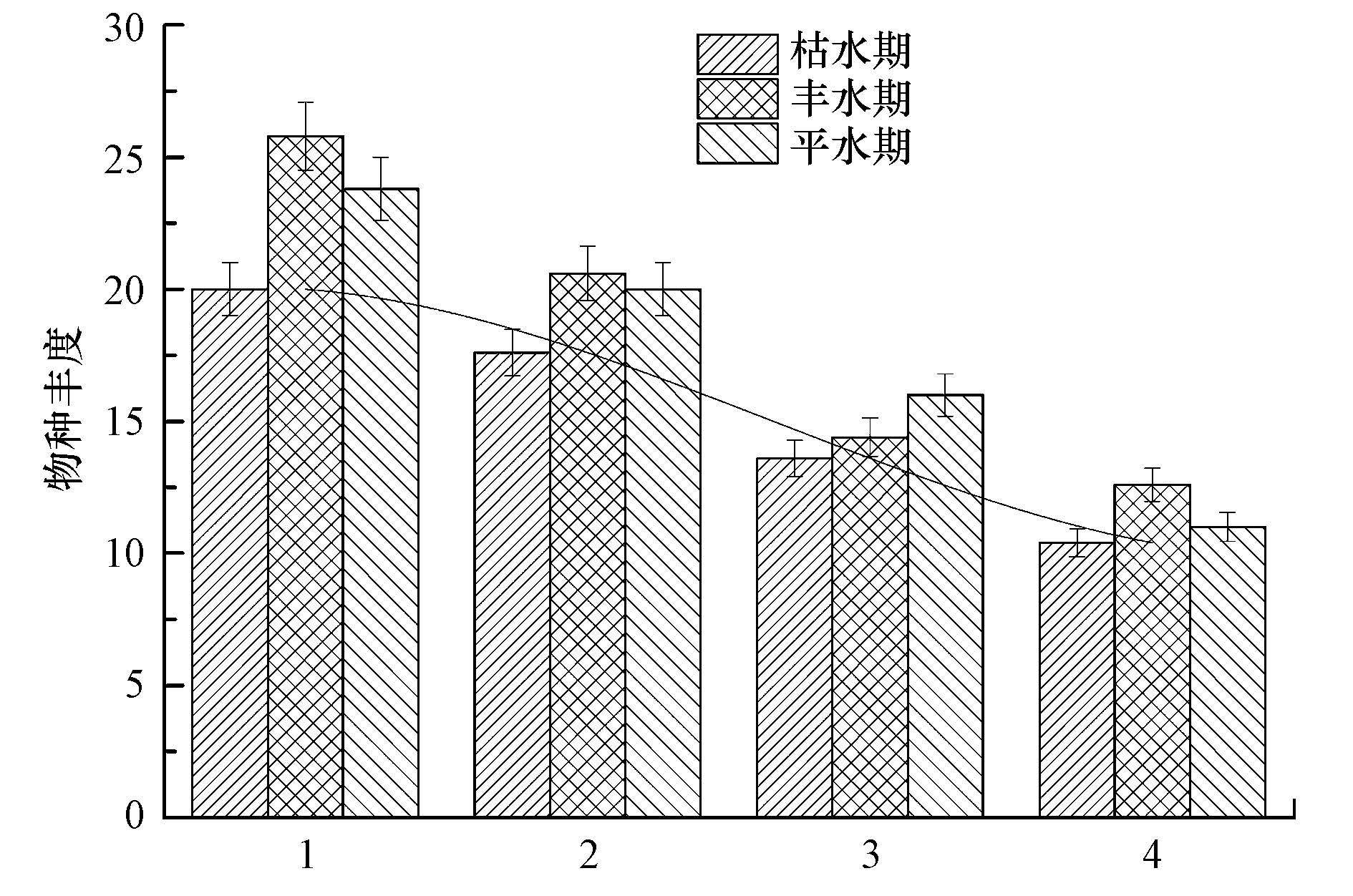 |
| 图2 不同组分大型底栖动物物种丰度 Fig.2 Species abundance of macroinvertebrates in different groups |
| 表2 大型底栖动物物种丰度双因素方差分析及显著性检验 Table 2 Two-way ANOVA of species abundance of macroinvertebrates and test of significance |
对4种土地利用方式下大型底栖动物主要类群进行统计分析表明,林地组中蜉蝣目的四节蜉科(Baetidae)、扁蜉科(Heptageniidae)、二尾蜉科(Siphluridae),襀翅目的石蝇科(Perlidae),毛翅目的纹石蛾科(Hydropsychidae)、沼石蛾科(Limnephilidae)百分比较大,是该组分的优势生物类群.耕地组或居民点组中四节蜉科(Baetidae)、扁蜉科(Heptageniidae)、二尾蜉科(Siphluridae),纹石蛾科(Hydropsychidae)、沼石蛾科(Limnephilidae)生物类群百分比均有所下降,下降幅度为6%~12%,石蝇科(Perlidae)生物在耕地组或居民点组中百分比小于1.0或无分布,双翅目摇蚊科(Chironomidae)成为主要优势类群,所占比例达25%以上,大蚊科(Tipulidae)、虻科(Tabanidae),鞘翅目长角泥甲科(Elmidae)、沼梭科(Haliplidae)、龙虱科(Dytiscidae),椎实螺科(Lymnaeidae)比例上升.在城市组中,颤蚓科(Tubificidae)百分比高达45%,其次为摇蚊科(Chironomidae),百分比约为25%,仙女虫科(Naididae),石蛭科(Erpobdellidae)生物比例高于前3组.对不同土地利用类型区大型底栖动物类群及时空双因素方差分析可知(表 3),各主要生物类群百分比在4个组分间呈显著性差异,其中蜉蝣目、襀翅目、毛翅目的生物类群在空间上差异显著性较大(p<0.01),不同类群大型底栖动物在各水期间无显著性差异.通过NMDS排序分析(图 3),可知林地组、城市组与耕地组及居民点组大型底栖动物群落特征差异性较大,耕地组与居民点组大型底栖动物群落组成相似,各组分内部大型底栖动物群落特征相似性较高.
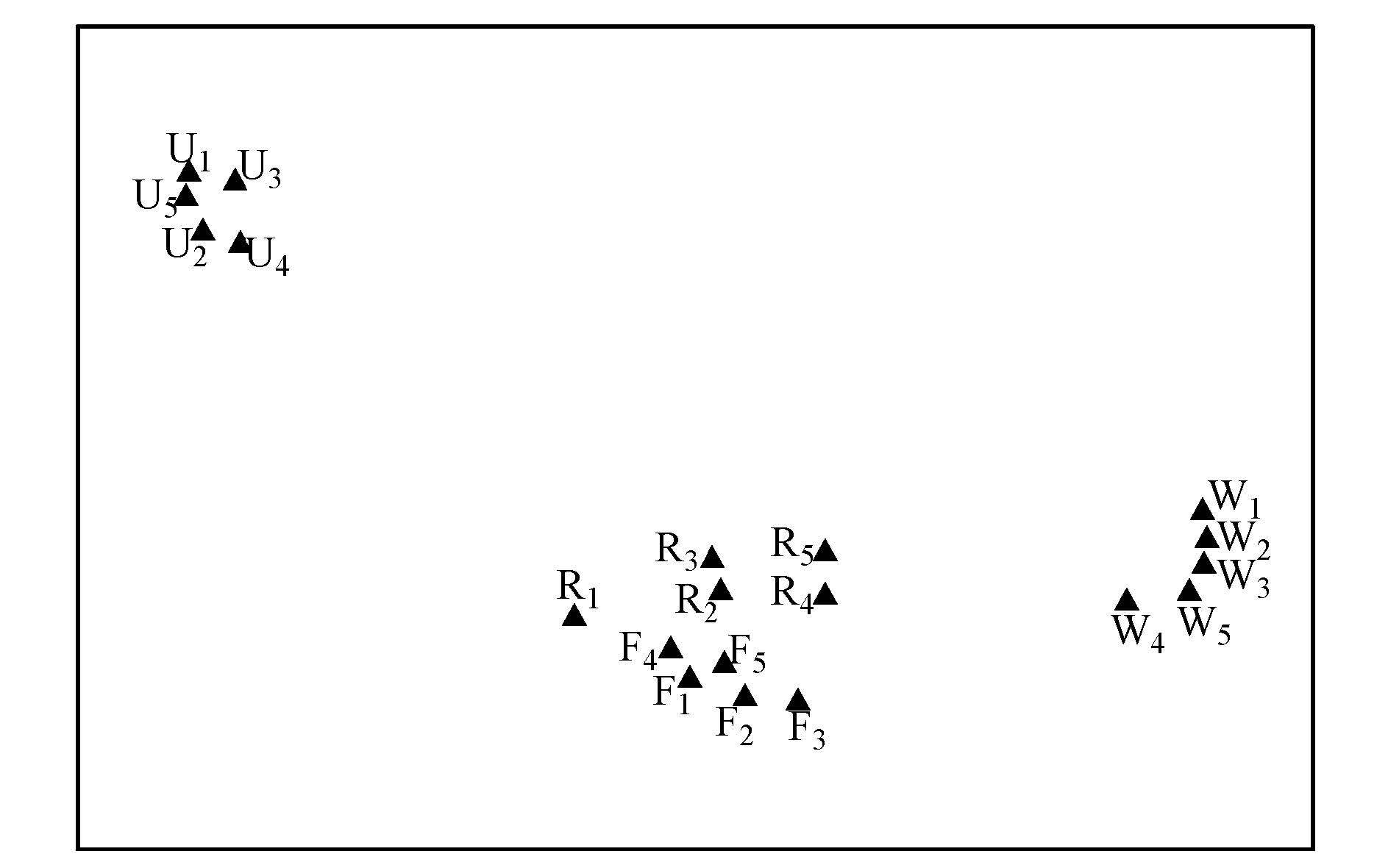 |
| 图3 不同组分大型底栖动物群落相似性分析 Fig.3 Similarity analysis of macroinvertebrate communities in different groups |
| 表3 不同土地利用类型各水期大型底栖动物主要类群百分比及双因素方差分析 Table 3 Percentage of the most common macroinvertebrate families at four major l and -use types in different periods |
不同土地利用方式下大型底栖动物各水期生物密度平均值为1391.33 ind · m-2(图 4),在空间分布上,耕地组生物密度最高,密度平均值为1764.91 ind · m-2,城市组生物密度最低为730.85 ind · m-2,城市组与其他3个组分间生物密度呈显著性差异(p=0.000).在时间尺度上,枯水期耕地组生物密度最高,其次为居民点组、林地组,最低值出现在城市组,各土地利用方式下枯水期平均生物密度为1332.45 ind · m-2,丰水期林地组生物密度增加,林地、耕地、居民点之间生物密度差异减小,各组分平均生物密度为1310.40 ind · m-2,平水期不同组分间生物密度差异增大,各组分密度大小依次为耕地、居民点、林地、城市,平均值为1531.15 ind · m-2,大型底栖动物生物密度在各水期间差异不显著.
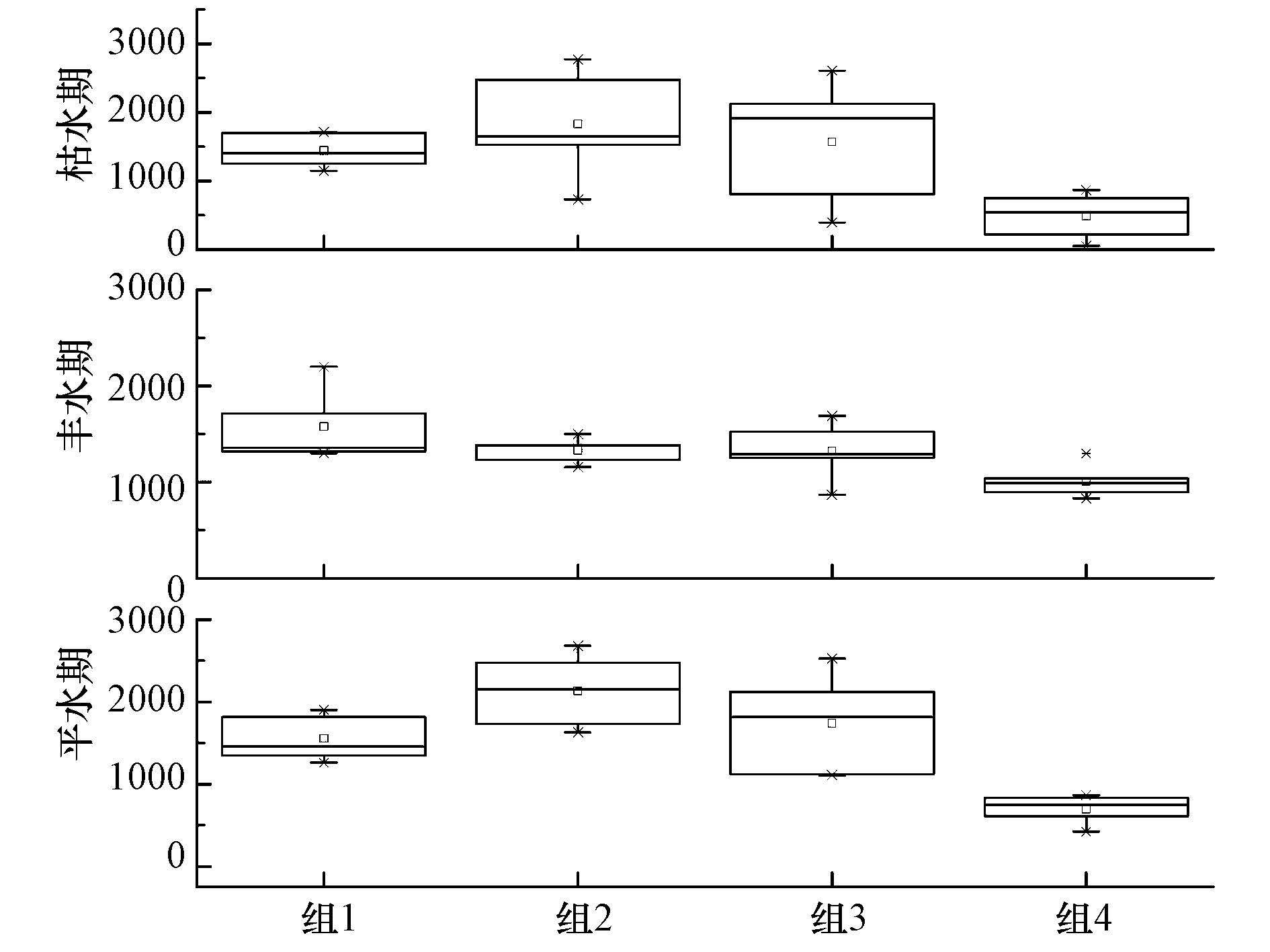 |
| 图4 大型底栖动物生物密度时空变化 Fig.4 Temporal and spatial variation of macroinvertebrates density |
生物指数H′、B、dm、J、FBI指数以及EPT(Ephemeroptera,Plecoptera and Tricoptera)是表征不同土地利用方式间大型底栖动物群落特征变化的重要指标.图 5与表 4结果表明,大型底栖动物多样性指数H′在林地到城市组间呈下降趋势,组分间多样性差异显著(p=0.000).耕地组与居民点组趋势平稳,两者差异较小,同一组分不同水期间生物多样性差异不显著,枯水期H′小于平水期及丰水期.综合考虑大型底栖动物样品个体数量,林地组多样性B值显著高于其他3组(p=0.000).大型底栖动物物种丰富度的空间分布及时空交互作用呈显著性差异(p=0.000,p=0.004).大型底栖动物均匀度在空间分布及时间差异上均不显著(p>0.05).林地组到城市组大型底栖动物FBI指数呈上升趋势,在空间与时间尺度上差异性均显著(p=0.000,p=0.011).大型底栖动物EPT%在空间上呈显著下降趋势,各组分间EPT%差异均显著(p=0.000).
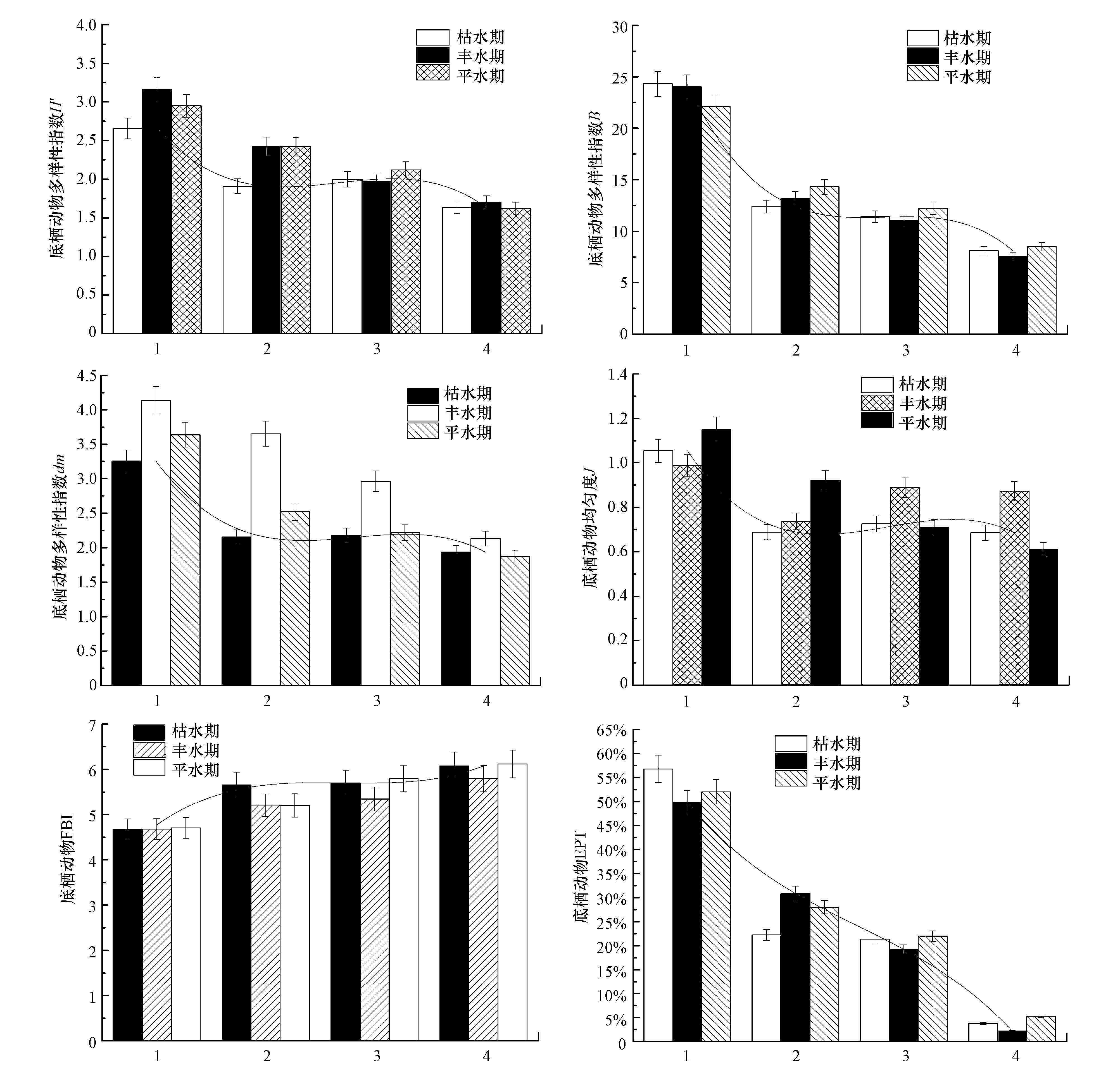 |
| 图5 大型底栖动物生物指数时空变化特征 Fig.5 Characteristics of macroinvertebrate community indices in spatial and temporal scale |
| 表4 大型底栖动物生物指数双因素方差分析 Table 4 Two-way ANOVA of macroinvertebrate community indices and test of significance |
大型底栖动物生存的生境因子时空双因素方差分析结果表明(表 5),不同土地利用方式下底质、流速、水深3个生境指标及DO、TP、TN、NH3-N、BOD5、CODCr水质化学指标在空间上呈显著性差异,其中底质、TP、CODCr显著性差异水平为p<0.01,其余指标显著性水平为p<0.05.4个组分间温度的空间差异不显著,在时间上呈显著性差异(p<0.05),其余各生境因子在时间上差异不显著.
| 表5 不同组分生境因子变化及双因素方差分析 Table 5 Variation of environmental variables in different groups and two-way ANOVA analysis |
大型底栖动物生物指数与生境因子相关性分析表明(见6),底质、DO与除均匀度外各生物指数间呈显著正相关,其中大型底栖动物FBI指数、EPT%与底质相关性较高.河流流速、水深与大型底栖动物丰富度、FBI指数及EPT%呈显著正相关.水温对大型底栖动物多样性有显著影响.TP、TN与大型底栖动物FBI指数及EPT%呈负相关关系,NH3-N、BOD5、CODCr与FBI指数及EPT%呈显著负相关,且相关性较高.
| 表6 大型底栖动物生物指数与生境因子相关性分析 Table 6 Correlation analysis between macroinvertebrate community indices and environmental variables |
对大型底栖动物群落结构特征与生境因子的BIO-ENV可知(表 7),在单因子中,底质因素是影响大型底栖动物群落结构特征的主要因子,且3个不同水期内底质与大型底栖动物群落特征的相关性均较高,相关系数可达到0.5.双因子分析可得,在各生境因子中,影响大型底栖动物群落特征的因素除底质外,DO、TN、BOD5对大型底栖动物群落组成及分布也有较大影响,且双因子组合的相关系数高于单一生境因子.不同水期对大型底栖动物群落特征影响最大的生境因子组合中,在枯水期主要为底质、DO、水温,相关系数0.723;丰水期主要为底质、TN、NH3-N,相关系数0.778;平水期主要为底质、流速、BOD5,相关系数0.758,综合不同组分及水期的大型底栖动物群落特征及影响因素分析可得,底质、DO、TN、BOD5是影响该研究区域大型底栖动物群落特征的最优环境因子组合,相关系数达0.795.
| 表7 大型底栖动物群落结构特征与生境因子BIO-ENV分析 Table 7 BIO-ENV analysis of macroinvertebrate communities and environmental variables |
在研究区域内,林地、耕地、居民点和城市用地主导的4种土地利用方式下河流底质、DO、TP、TN、CODCr等生境及水质指标存在明显差异.由于采样点河岸缓冲区土地利用方式不同,对河流生境及水质也产生不同影响.以林地为主要土地利用方式的区域,人类活动少,河岸带植被覆盖率高,底质多为卵石,河流深度小,流速快,水质清洁,DO含量高,N、P及有机污染物指标值显著低于其他类型区.以耕地为主的研究区域,河岸缓冲区多以玉米、水稻等农田为主,农药、化肥施用较多,农田与河流之间河岸带宽度较低,主要为草本植物,对降雨形成的地表径流中的N、P含量及污染物不能起到有效的过滤作用,因此,河流N、P、BOD5、CODCr指标值增大;另外,该类型区底质中砂和泥沙含量增多,卵石比例明显减少.居民点区域主要为分散性分布的村落,存在零散畜禽养殖现象,养殖废水、废弃物、生活污水及垃圾无统一处理设施,会直接或间接入河,对河流水质影响较大;该区人类干扰较大,河道受损,底质扰动明显.城市聚居区人口密度大,周边有工业及娱乐设施,河岸带几乎全部人工化,河道原有自然形态已发生强烈变化,河底多为淤泥,河流深度大,流速缓,溶解氧含量低,CODCr值明显高于其他区域.
通过对大型底栖动物与环境因子的相关性分析及BIO-ENV分析,不同土地利用类型区中底质、DO、TN、BOD5是影响大型底栖动物群落特征的最优环境因子组合,且底质、DO与大型底栖动物各生物指数相关性均较高.因此,当不同土地利用类型区环境条件发生变化时,大型底栖动物群落特征也会相应发生变化,本研究中由于不同类型区底质、溶解氧等环境因子差异显著,进而对大型底栖动物群落组成及分布产生明显影响.大型底栖动物物种丰度在林地、耕地、居民点和城市组之间差异显著,群落相似性表现为组内相似性较大,耕地组和居民点组组间相似性大于其余土地利用类型.耕地组大型底栖动物生物密度平均值最高,城市组最低.大型底栖动物多样性(H′和B)、丰富度和均匀度从林地到城市组间整体呈下降趋势,其中耕地组与居民点组基本一致.FBI指数和EPT%在空间上分别呈上升和下降趋势,且组分间差异显著.
在以林地为主的研究区域,河流生境条件较好,人为干扰小,无污染或污染程度低,适合敏感生物类群及耐污值较低的大型底栖动物生存(Suga and Tanaka, 2013).大型底栖动物主要以蜉蝣目、襀翅目和毛翅目的四节蜉科、扁蜉科、纹石蛾科及石蝇科等生物类群为主,生物多样性指数及EPT%显著高于其他组分,且FBI值在4个组分中最低.底质是影响大型底栖动物分布的关键因子(殷旭旺等,2013),不同土地利用类型间河流底质表现明显差异,林地组中底质多以不同粒径的石质为主,为大型底栖动物的筑巢、攀附提供环境条件,有利于附石性大型底栖动物生存.溶解氧是影响大型底栖动物生存的重要条件,林地区域河流深度较小,且流速较快,增加了水体中溶解氧的交换量,因此,该组分好氧性大型底栖动物类群比例较高.同时东部区域的林地在水土保持方面起重要作用,使得河流中悬沙及细沙含量较少,有利于大型底栖动物生存.
以耕地和居民点为主要类型的研究区域,大型底栖动物类群以摇蚊科为主,且百分比远高于其他生物类群,EPT生物类群及百分比显著下降,FBI值升高,说明该区域内耐污性大型底栖动物生物类群高于林地区.耕地组与居民点研究区域内农业面积所占比例较大,人类活动频繁,农业耕作、农药、化肥施用及生活污水等面源污染对河流水质造成影响,BOD5高于林业用地,进而影响某些种类大型底栖动物的生存,耐污值较高的生物类群比例上升(De Klerk and Wepener, 2013; Selala et al., 2013; 迟国梁等,2010),同时区域内修筑堤坝、引水灌溉等工程措施,破坏了河流生境条件,致使河流生态系统退化,大型底栖动物生境条件适宜性下降,因而该区域内生存的主要生物类群耐污性及抗干扰性均高于林地类型的主要生物类群(Pierri-Daunt and Tanaka, 2014;韩鸣花等,2012).同时,频繁的农业活动及土地垦殖,降低了植被覆盖率,造成水土流失、河床升高等河岸带生境条件变化,且河道内石质减少,地表径流及河流冲积造成的河道内泥沙淤积或流动对靠腮呼吸的大型底栖动物生存构成威胁,降低了该区域内生物多样性及对环境条件要求较高的敏感生物类群的比例.
以城市河段为主的区域,人口密度大,工业发达,工业废水及大量生活污水对河流水质造成严重影响,同时河岸带硬质化现象普遍,减少了河岸带植被对入河污染物的净化作用.该区域河流水量大、流速缓,河流底质以泥质为主,大型底栖动物多生活在水体与底质相交面及以下的底质中,水中溶解氧交换量低,对大型底栖动物的生存影响较大(Chessman and McEvoy, 2012),此类生境条件下生存的大型底栖动物多以需氧量低、耐污性强的寡毛类生物类群为主(Cabral-Oliveira et al., 2014),如颤蚓科可达到城市组生物总数的45%,EPT生物类群不能生存(Lill et al., 2012).不同土地利用方式对大型底栖动物群落组成及分布影响较大,土地利用方式的差异通过影响河流生态系统生境及水质进而影响大型底栖动物的群落特征,合理规划与优化流域土地利用方式对河流生态系统保护具有重要作用.
5 结论(Conclusions)1)土地利用方式对辽河流域中辽宁东部河流大型底栖动物群落特征具有明显影响.大型底栖动物物种组成及群落相似性、生物密度、多样性、丰富度、FBI指数以及EPT%在林地、耕地、居民点及城市为主的土地利用方式之间空间差异性显著,而不同水期之间河流大型底栖动物群落特征差异不显著,其中林地与其他3种土地利用方式差异较大,且敏感物种及耐污值低的大型底栖动物类群百分比较大.
2)以林地、耕地、居民点及城市为主的土地利用方式下,生境因子(底质、流速、水深)和水化学指标(DO、TP、TN、NH3-N、BOD5、CODCr)差别较大,其中林地区生境条件良好,耕地和居民点类型次之,城市区水质污染较重.
3)不同土地利用方式下,环境因子对大型底栖动物的影响程度不同,对大型底栖动物群落特征及分布影响最优的环境因子组合为底质、DO、TN、BOD5,其中底质为影响作用较大的河流物理生境因子,DO、BOD5与大型底栖动物多样性、FBI指数及EPT%等相关性较高,建议可将底质、DO、TN、BOD5确定为辽宁东部山地区域河流水生态系统的管理目标.
| [1] | Arle J, Wagner F. 2013. Effects of anthropogenic salinisation on the ecological status of macroinvertebrate assemblages in the Werra River (Thuringia, Germany)[J]. Hydrobiologia, 701(1):129-148 |
| [2] | Boix D, Gascón S, Sala J, et al. 2005. A new index of water quality assessment in Mediterranean wetlands based on crustacean and insect assemblages:the case of Catalunya (NE Iberian peninsula)[J]. Aquatic Conservation-Marine and Freshwater Ecosystems, 15(6):635-651 |
| [3] | Brown L E, Johnston K, Palmer S M, et al. 2013. River ecosystem response to prescribed vegetation burning on blanket peatland[J]. PLoS One, 8(11):e81023 |
| [4] | Cabral-Oliveira J, Mendes S, Maranhão P, et al. 2014. Effects of sewage pollution on the structure of rocky shore macroinvertebrate assemblages[J]. Hydrobiologia, 726(1):271-283 |
| [5] | Chessman B C, McEvoy P K. 2012. Insights into human impacts on streams from tolerance profiles of macroinvertebrate assemblages[J]. Water, Air, & Soil Pollution, 223(3):1343-1352 |
| [6] | 迟国梁, 赵颖, 官昭瑛, 等. 2010. 广东横石水河大型底栖动物群落与环境因子的关系[J]. 生态学报, 30(11):2836-2845 |
| [7] | 大连水产学院. 1982. 淡水生物学[M]. 北京:农业出版社 |
| [8] | De Klerk A R, Wepener V. 2013. Macroinvertebrate assemblage changes as an indicator of water quality of perennial endorheic reed pans on the mpumalanga highveld, South Africa[J]. Journal of Environmental Protection, 4:10-21 |
| [9] | 段学花, 王兆印, 徐梦珍. 2010. 底栖动物与河流生态评价[M]. 北京:清华大学出版社. |
| [10] | 韩鸣花, 于海燕, 周斌, 等. 2012. 城市溪流中径流式低坝对底栖动物群落结构的影响[J]. 生态学报, 32(2):380-385 |
| [11] | Johnson R C, Carreiro M M, Jin H S, et al. 2012. Within-year temporal variation and life-cycle seasonality affect stream macroinvertebrate community structure and biotic metrics[J]. Ecological Indicators, 13(1):206-214 |
| [12] | Kibena J, Nhapi I, Gumindoga W. 2014. Assessing the relationship between water quality parameters and changes in landuse patterns in the Upper Manyame River, Zimbabwe[J]. Physics and Chemistry of the Earth, Parts A/B/C, 67-69:153-163 |
| [13] | Lewin I, Czerniawska-Kusza I, Szoszkiewicz K, et al. 2013. Biological indices applied to benthic macroinvertebrates at reference conditions of mountain streams in two ecoregions (Poland, the Slovak Republic)[J]. Hydrobiologia, 709:183-200 |
| [14] | Lill A W T, Closs G P, Schallenberg M, et al. 2012. Impact of berm breaching on hyperbenthic macroinvertebrate communities in intermittently closed estuaries[J]. Estuaries and Coasts, 35(1):155-168 |
| [15] | Morse J C, Yang L F, Tian L X. 1994. Aquatic Insects of China Useful for Monitoring Water Quality[M]. Nanjing:Hohai University Press |
| [16] | Oliveira R B S, Baptista D F, Mugnai R, et al. 2011. Towards rapid bioassessment of wadeable streams in Brazil:Development of the Guapiaçu-Macau Multimetric Index (GMMI) based on benthic macroinvertebrates[J]. Ecological Indicators, 11(6):1584-1593 |
| [17] | Pierri-Daunt A B, Tanaka M O. 2014. Assessing habitat fragmentation on marine epifaunal macroinvertebrate communities:an experimental approach[J]. Landscape Ecology, 29(1):17-28 |
| [18] | 渠晓东, 张远, 马淑芹, 等. 2013. 太子河流域大型底栖动物群落结构空间分布特征[J]. 环境科学研究, 26(5):509-515 |
| [19] | Rasmussen J J, Wiberg-Larsen P, Baattrup-Pedersen A, et al. 2012. Stream habitat structure influences macroinvertebrate response to pesticides[J]. Environmental Pollution, 164:142-149 |
| [20] | Rasmussen J J, McKnight U S, Loinaz M C, et al. 2013. A catchment scale evaluation of multiple stressor effects in headwater streams[J]. Science of the Total Environment, 442:420-431 |
| [21] | Selala M C, Botha A M, De Klerk A R, et al. 2013. Effects of vegetable oil pollution on aquatic macroinvertebrate assemblage in a freshwater wetland and its use as a remediation tool[J]. Water, Air, & Soil Pollution, 224:1650 |
| [22] | Solimini A G, Bazzanti M, Ruggiero A, et al. 2008. Developing a multimetric index of ecological integrity based on macroinvertebrates of mountain ponds in central Italy[J]. Hydrobiologia, 597(1):109-123 |
| [23] | Suga C M, Tanaka M O. 2013. Influence of a forest remnant on macroinvertebrate communities in a degraded tropical stream[J]. Hydrobiologia, 703(1):203-213 |
| [24] | Sutherland A B, Culp J M, Benoy G A. 2012. Evaluation of deposited sediment and macroinvertebrate metrics used to quantify biological response to excessive sedimentation in agricultural streams[J]. Environmental Management, 50(1):50-63 |
| [25] | Tullos D D, Penrose D L, Jennings G D. 2006. Development and application of a bioindicator for benthic habitat enhancement in the North Carolina Piedmont[J]. Ecological Engineering, 27(3):228-241 |
| [26] | Wang B X, Liu D X, Liu S R, et al. 2012. Impacts of urbanization on stream habitats and macroinvertebrate communities in the tributaries of Qiangtang River, China[J]. Hydrobiologia, 680(1):39-51 |
| [27] | 王强, 袁兴中, 刘红. 2012. 山地河流浅滩深潭生境大型底栖动物群落比较研究——以重庆开县东河为例[J]. 生态学报, 32(21):6726-6736 |
| [28] | Wittman J, Weckwerth A, Weiss C, et al. 2013. Evaluation of land use and water quality in an agricultural watershed in the USA indicates multiple sources of bacterial impairment[J]. Environmental Monitoring and Assessment, 185(12):10395-10420 |
| [29] | 吴璟, 杨莲芳, 姜小三, 等. 2008. 浙江西苕溪土地利用变化对溪流大型底栖无脊椎动物完整性的影响[J]. 生态学报, 28(3):1183-1191 |
| [30] | 殷旭旺, 徐宗学, 高欣, 等. 2013. 渭河流域大型底栖动物群落结构及其与环境因子的关系[J]. 应用生态学报, 24(1):218-226 |
| [31] | 张勇, 刘朔孺, 于海燕, 等. 2012. 钱塘江中游流域不同空间尺度环境因子对底栖动物群落的影响[J]. 生态学报, 32(14):4309-4317 |
 2016, Vol. 36
2016, Vol. 36


