2. 暨南大学环境学院, 广州 510632;
3. 暨南大学化学系, 广州 510632
2. College of Environment, Jinan University, Guangzhou 510632;
3. Department of Chemistry, Jinan University, Guangzhou 510632
多环芳烃(polycyclic aromatic hydrocarbons,PAHs)是一类含有2个或2个以上苯环的持久性有机污染物,具有潜在的致畸、致癌和致突变特性,因而对生态环境和人类健康构成了巨大的威胁(Wang et al., 2013; Xu et al., 2006).芘是由4个苯环对称排列组成的稠环芳烃,结构稳定,在环境中广泛存在,是检测PAHs污染的指示物(Yuan et al., 2000).微生物降解PAHs具有环境友好、成本低等特点,被认为是去除环境中PAHs的主要途径(Haritash and Kaushik, 2009).然而,微生物降解PAHs过程中产生的部分代谢产物依然具有危害性和持久性,其毒性甚至比母体污染物更高,例如芘的代谢产物醌具有强致突变性,其毒性比芘更大(Ravelet et al., 2000),此类代谢产物同样会对环境造成严重危害(Šepičet al., 2003; Parikh et al., 2004; Carney et al., 2008).目前的研究工作主要集中在PAHs高效降解菌的筛选、降解机理和降解基因等方面,而关于PAHs微生物降解过程代谢产物及其生物可利用性等方面的研究还有待深化.
微生物对PAHs的降解利用主要依靠其酶系统内多种酶的催化作用,关键降解酶对高毒性PAHs的安全、高效去除起到了决定性的作用(Wu et al., 2008).目前,关于PAHs降解酶的研究包括双加氧酶(Selvakumaran et al., 2011; Jurelevicius et al., 2012)、锰过氧化物酶(Eibes et al., 2006)、木质素过氧化物酶(Verdin et al., 2004)等.邻苯二酚1,2-双加氧酶和邻苯二酚2,3-双加氧酶存在于大量PAHs降解菌中,分别催化苯环的邻位和间位开环,是芳香族化合物及其衍生物降解途径中的关键酶,此外,NahAc,phnAc,NidA和pdoB等双加氧酶编码基因也被用于检测PAHs降解菌(Bourguignon et al., 2014; Chen et al., 2013).
虽然已有不少关于PAHs微生物降解代谢途径以及关键酶的研究报道,但这些研究主要集中于萘,菲等低分子量PAHs,与之相比,芘作为高分子量PAHs其水溶性更差,生物可利用性更低,一些水溶性较高的PAHs还可通过与高分子量PAHs竞争加氧酶的活性位点,或积累有毒的共代谢产物来抑制高分子量PAHs的生物降解(Mishra and Singh, 2014).因此,明确修复菌株在降解高分子量PAHs过程中代谢产物及关键酶活变化,将有助于微生物修复PAHs等环境污染在实际应用中的调控.本文以芘为高分子量PAHs典型代表物,探讨了1株蜡状芽胞杆菌对水体中芘的降解特性及对其单羟基多环芳烃代谢产物的利用情况,同时考察该菌株在降解芘过程中相关降解酶的活性变化,明确降解过程中的关键酶,以期为PAHs污染水体的微生物修复和降解工程菌的构建提供科学依据.
2 材料与方法(Materials and methods) 2.1 材料实验菌株:蜡状芽胞杆菌(Bacillus cereus),由本实验室筛选获得.
化学试剂:芘(99%)、1-萘酚(98%)、2-萘酚(99%)、9-羟基菲(99%)、1-羟基芘(98%)、甲醇(HPLC级)、乙腈(HPLC级)均购自于Sigma-Aldrich公司(St. Louis,MO,USA),其余试剂购自于天津市富宇精细化工有限公司,均为AR级.
牛肉膏蛋白胨培养基:牛肉膏5 g、蛋白胨10 g、NaCl 5 g、双蒸水1000 mL、pH 7.0~7.2.
无机盐培养基: K2HPO4 100 mg,KH2PO4 100 mg,MgSO4 · 7H2O 20 mg,柠檬酸钠100 mg,双蒸水1000 mL.
芘储备液:用甲醇(HPLC级)溶解,配制成0.1 g · L-1的芘储备液,4 ℃保存备用.
实验时所有培养基均121 ℃高压蒸汽灭菌30 min.
2.2 实验方法 2.2.1 菌悬液的配制将B. cereus接种到牛肉膏蛋白胨培养液中,于30 ℃,130 r · min-1摇床中振荡培养24 h,6000 r · min-1条件下高速离心10 min,弃上清液,收集菌体,用无菌水洗涤3次后再用灭菌无机盐培养基重悬,配成20 g · L-1菌悬液待用.
2.2.2 不同体系中芘的微生物降解在总体积为20 mL的灭菌无机盐培养基中加入芘储备液和菌悬液,使其终浓度分别为2.5 μmol · L-1和1 g · L-1.同时分别加入①鼠李糖脂,②葡萄糖,③Mn2+和Fe3+混合液,④Mn2+、Fe3+和鼠李糖脂混合液,⑤Mn2+、Fe3+和葡萄糖混合液,其中鼠李糖脂和葡萄糖浓度均为10 mg · L-1,Mn2+和Fe3+浓度分别为1 mg · L-1和0.1 mg · L-1,所有样品于30 ℃,130 r · min-1摇床中振荡反应120 h后取样测定芘的残余量.设置只加芘和菌悬液的样品作为对照组.
2.2.3 芘及其代谢产物的微生物降解在总体积为20 mL的灭菌无机盐培养基中分别加入芘、1-萘酚、2-萘酚、9-羟基菲和1-羟基芘,含量均为2.5 μmol · L-1,同时在体系中加入菌悬液(1 g · L-1)、Mn2+(1 mg · L-1)、Fe3+(0.1 mg · L-1)和葡萄糖(10 mg · L-1).将样品置于30 ℃,130 r · min-1摇床中避光振荡培养,分别在第24、48、72、96、120、144和168 h取样,测定芘及其代谢产物的残余量.设置未加菌样品作为对照组.
2.2.4 芘及其代谢产物的提取和检测样品取出后用6 mol · L-1 HCl溶液调节pH至2,之后转入分液漏斗,加入等体积的乙酸乙酯萃取,充分混合后静置分层,收集上层有机相,下层水相依前法再萃取1次,合并2次萃取液,用无水硫酸钠脱水,于35 ℃旋转蒸发至干,用甲醇(HPLC级)洗涤、浓缩定容至10 mL,取1 mL于进样瓶中上机分析(邓军等,2010).
芘浓度测定(邱云云等,2013):采用高效液相色谱仪(HPLC,Shimadzu,Japan).分析条件为: InertsilODS-SP C18反相色谱柱(4.6 mm×250 mm,5 μm);流动相V甲醇/V水=90/10;流速1 mL · min-1;紫外检测波长254 nm;分析时间7 min;进样体积为20 μL.
芘的代谢产物浓度测定:利用液相色谱-质谱/质谱(LC-MS/MS,ABSciex,4000QTRAP,USA)分析.色谱条件为Agilent Elipse Plus C18(2.1 mm×150 mm,5 μm)色谱柱;流动相为高纯水为A相,乙腈为B相;梯度洗脱程序为0~0.5 min,40% B; 0.5~2.5 min,60% B; 2.5~6.6 min,95% B; 6.6~10 min,40% B;流速0.3 mL · min-1;进样量10 μL.
质谱条件:电喷雾离子源(ESI),负离子方式,多反应监测(MRM)扫描.喷雾电压-4500 V,气帘气(CUR)压力为1.38×105 Pa,雾化气(GS1)压力为4.48×105 Pa,干燥气(GS2)压力为3.45×105 Pa;离子源温度(TEM)600 ℃,驻留时间(Dwell Time)为200 ms.其它质谱条件见表 1.
| 表1 4种芘代谢产物的质谱检测参数 Table 1 LC-MS/MS parameters for the determination of 4 pyrene metabolites by |
将样品于4 ℃,8000 r · min-1离心10 min收集B. cereus细胞,用磷酸盐缓冲液(PBS,50 mmol · L-1,pH 7.5)洗涤3次,再加入PBS重悬,制备成菌悬液.用超声破碎仪进行细胞破壁(450 W,破碎3 s,间歇3 s,工作150次),之后于4 ℃,12000 r · min-1离心30 min,收集上清液作为粗酶液用于酶活实验.同时用Bradford法(Bradford,1976)定量粗酶液中蛋白含量. 2.2.6 酶活测定 在无机盐反应体系中加入芘作为酶活性的诱导物,分析B. cereus粗酶液中水杨酸羟化酶,邻苯二酚1,2-双加氧酶和邻苯二酚2,3-双加氧酶的活性.设置未加芘的无机盐培养基作为对照组.
水杨酸羟化酶测定(Zhou et al., 2002):将适量粗酶液加入到含50 μmol · L-1水杨酸和0.1 mmol · L-1 还原型辅酶Ⅰ(NADH)的PBS(50 mmol · L-1,pH 7.5)中,体系为1 mL,分析酶反应底物NADH在340 nm处的消耗情况,摩尔消光系数 ε340=6220 L · mol-1 · cm-1.水杨酸羟化酶酶活单位定义为: 30 ℃下,每min消耗1 μmol NADH所需的酶量.
邻苯二酚1,2-双加氧酶测定(Guzik et al., 2013):将适量粗酶液加入到含0.1 mmol · L-1邻苯二酚和10 μmol · L-1 EDTA的PBS(50 mmol · L-1,pH 7.5)中,体系为1 mL,分析酶反应产物顺,顺-己二烯二酸在260 nm处的生成情况,ε260=16800 L · mol-1 · cm-1. 邻苯二酚1,2-双加氧酶酶活单位定义为: 30 ℃下,每min生成1 μmol顺,顺-己二烯二酸所需的酶量.
邻苯二酚2,3-双加氧酶测定(Wojcieszyńska et al., 2012):将适量粗酶液加入到含0.1 mmol · L-1邻苯二酚的PBS(50 mmol · L-1,pH 7.5)中,体系为1 mL,分析酶反应产物2-羟基粘糠酸半醛在375 nm处的生成情况,ε375=36000 L · mol-1 · cm-1.邻苯二酚2,3-双加氧酶酶活单位定义为: 30 ℃下,每min生成1 μmol 2-羟基粘糠酸半醛所需的酶量.
3 结果与讨论(Results and discussion) 3.1 不同处理体系中B. cereus对芘的降解芘具有生物毒性,一般情况下难以被微生物完全分解利用.为了促进B. cereus对水体中芘的降解,本实验在修复体系中添加了生物表面活性剂鼠李糖脂,葡萄糖,Mn2+和Fe3+等,这些物质对B. cereus降解芘的影响见图 1.从图上可知,在反应120 h后,与对照组相比,添加鼠李糖脂,葡萄糖,Mn2+和Fe3+实验组均对B. cereus降解芘有不同程度的促进作用,其中同时添加Mn2+、Fe3+和葡萄糖混合物对芘降解的促进最为明显,体系中芘的降解率由44.7%提高到60%左右,而单独添加葡萄糖,Mn2+和Fe3+,或Mn2+、Fe3+和鼠李糖脂混合物对芘降解的影响作用差别不大,芘降解率维持在51.7%~53.9%之间.芘是4环芳香烃,水溶性较差,而且溶液中芘浓度较低,菌体与芘的接触量较小,抑制其对芘的分解利用.鼠李糖脂是一类生物表面活性剂,能够降低芘的表面张力,具有增溶的特点,因此在体系中添加鼠李糖脂可以增强芘的生物可利用性(张娜等,2010).葡萄糖是易被生物利用的单糖,添加到溶液中可以作为碳源促进B. cereus生长,从而促进芘的分解利用.在微生物降解PAHs的过程中,其产生的各种酶起着关键的作用,而Mn2+和Fe3+作为芘降解过程中关键酶锰过氧化物酶和邻苯二酚1,2-双加氧酶的激活剂,可以明显提高该两种酶的活性(Zheng and Obbard, 2002; Tekere et al., 2005; Lange and Que, 1998),从而促进B. cereus对芘的降解.吴蔓莉等对Flavobacterium sp. FCN2降解芘研究发现,适当浓度的Mn2+加入可以促进体系中芘的微生物降解(吴蔓莉等,2008).
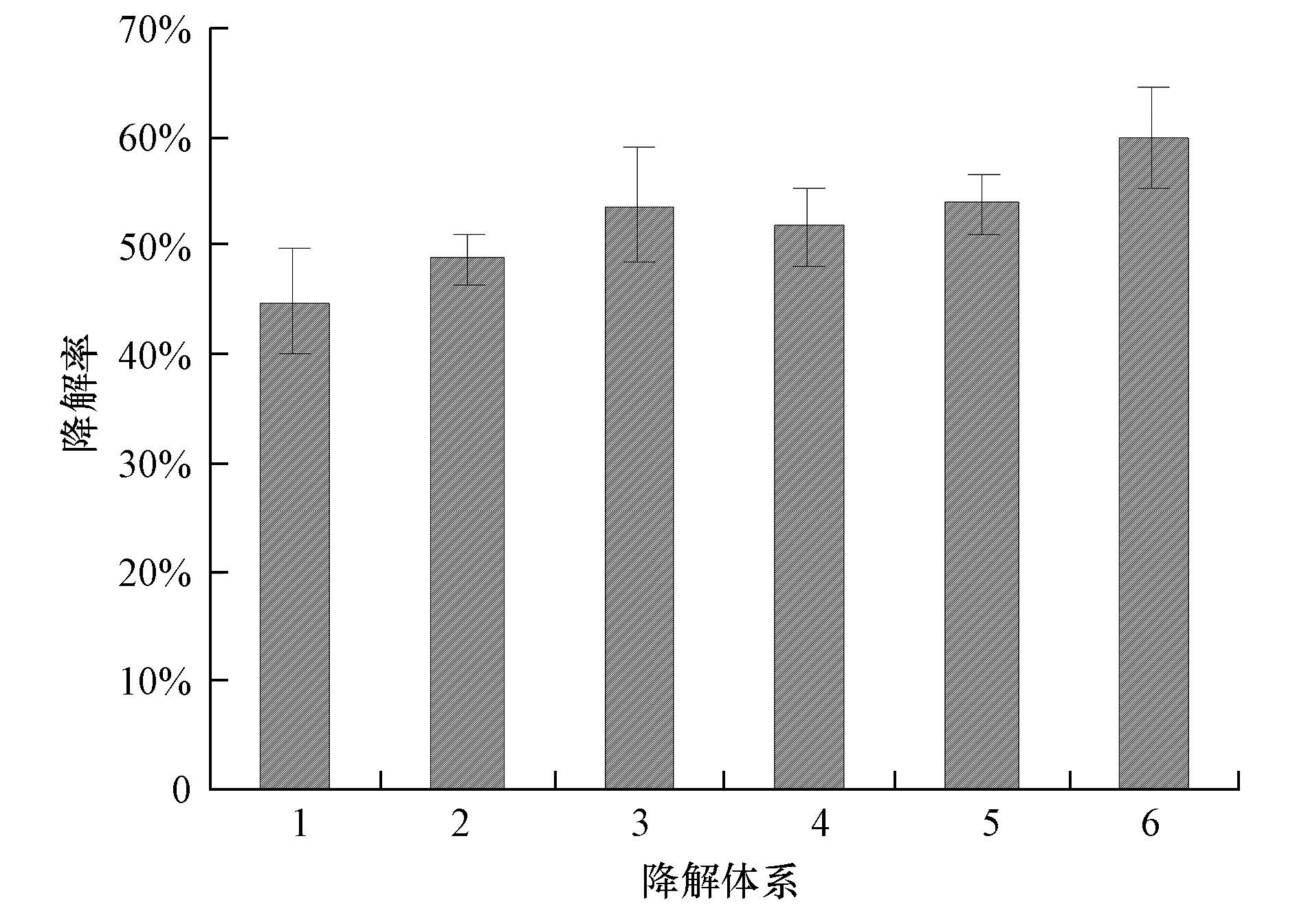 |
| 图1 不同处理体系中B. cereus对芘的降解效果(1.对照组; 2.鼠李糖脂; 3.葡萄糖; 4.Mn2++Fe3+; 5.Mn2++Fe3++鼠李糖脂; 6.Mn2++Fe3++葡萄糖) Fig.1 Degradation efficiency of pyrene by B. cereus under different treatments |
从本组实验结果可以看出,在芘污染的修复体系中B. cereus起关键作用,且菌体的代谢活性是主要限制因素.外加碳源和酶活诱导因子相较于表面活性剂,其对B. cereus降解芘的影响更明显.
3.2 时间对B. cereus降解芘的影响在添加了葡萄糖,Mn2+和Fe3+混合物的修复体系中,考察1 g · L-1 B. cereus对2.5 μmol · L-1芘的降解随时间的变化情况.由实验结果(图 2)可知,随着时间的延长,溶液中芘的浓度逐渐降低,从第120 h开始这种降低趋于平稳,此时体系中芘的残余浓度约为0.67 μmol · L-1,降解率达到最大,为61.4%,说明在修复体系中芘可以被B. cereus分解利用.
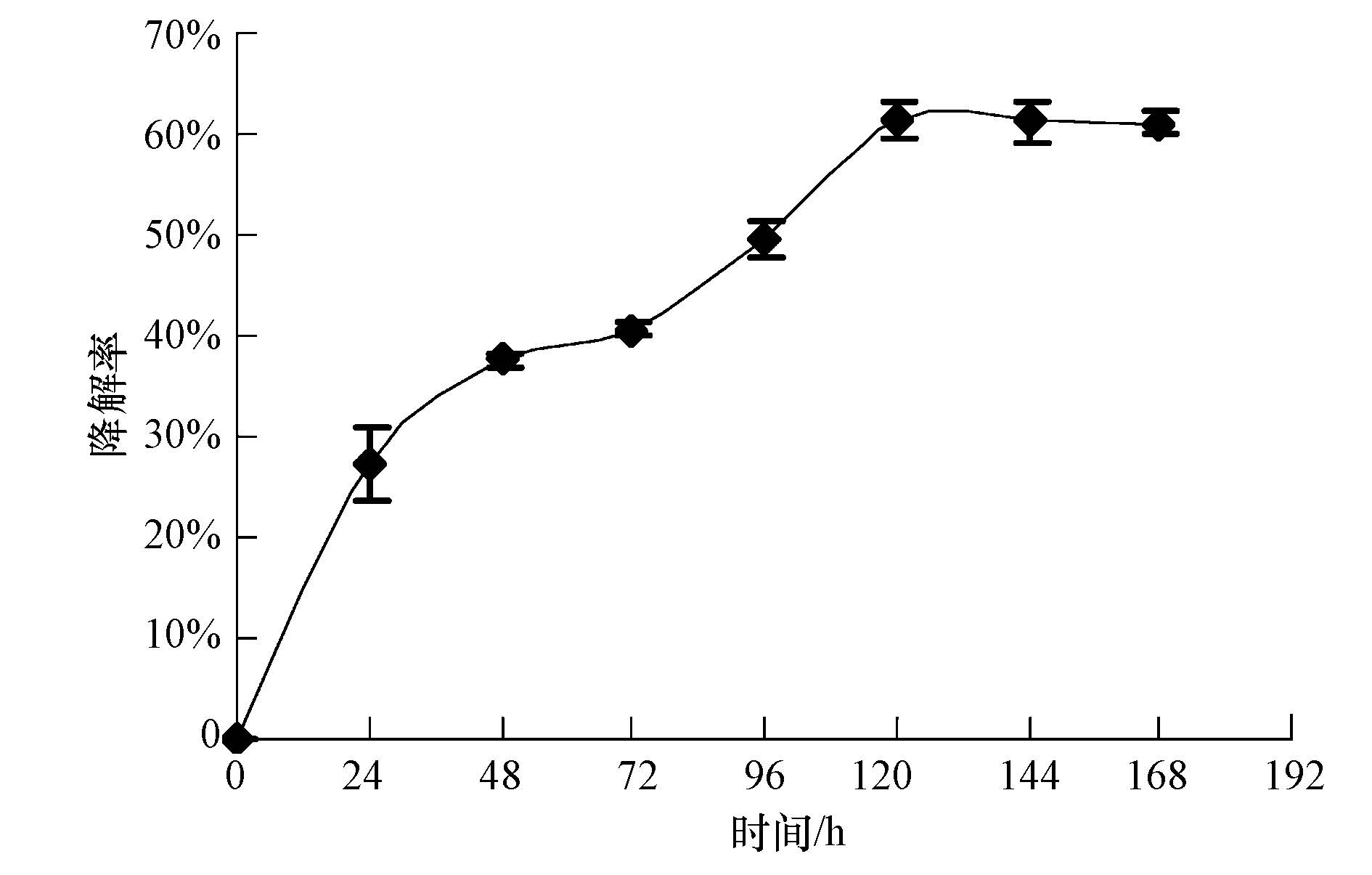 |
| 图2 芘降解随时间的变化 Fig.2 Biodegradation rate of pyrene over time |
随着芘逐渐被消耗,溶液中芘含量降低,当芘浓度过低时不利于与菌体细胞充分接触,这也使得B. cereus可利用的能源物质减少,菌体的生长代谢受影响;同时,受芘诱导产生的降解酶也相应减少,使得芘的降解受到抑制.因而,在后续的研究中将选取120 h作为芘最优的微生物降解周期.
3.3 B. cereus降解芘的代谢产物分析利用LC-MS/MS对B. cereus降解芘120 h后的代谢产物进行分析,得到4种单羟基多环芳烃,分别是1-萘酚、2-萘酚、9-羟基菲和1-羟基芘,其色谱出峰情况见图 3.该实验结果表明芘在B. cereus作用下被分解.已有文献报道(Zhong et al., 2006),环境中的芘首先在多种单加氧酶和双加氧酶的作用下,其4号和5号C位最先被氧化,然后邻位开裂形成三环化合物菲-4,5-二羧酸,之后进一步发生脱羧反应将芘逐步分解.根据本实验结果,水体中的芘在B. cereus单加氧酶的作用下,首先在芘的1号C位加入氧,形成1-羟基芘,之后在单加氧酶或双加氧酶的作用下,苯环进一步发生氧化和脱羧反应,进而开环、断裂、分解,生成更容易被B. cereus代谢利用的9-羟基菲、1-萘酚和2-萘酚等低分子量化合物,最后在一系列酶的作用下分解为二氧化碳和水.
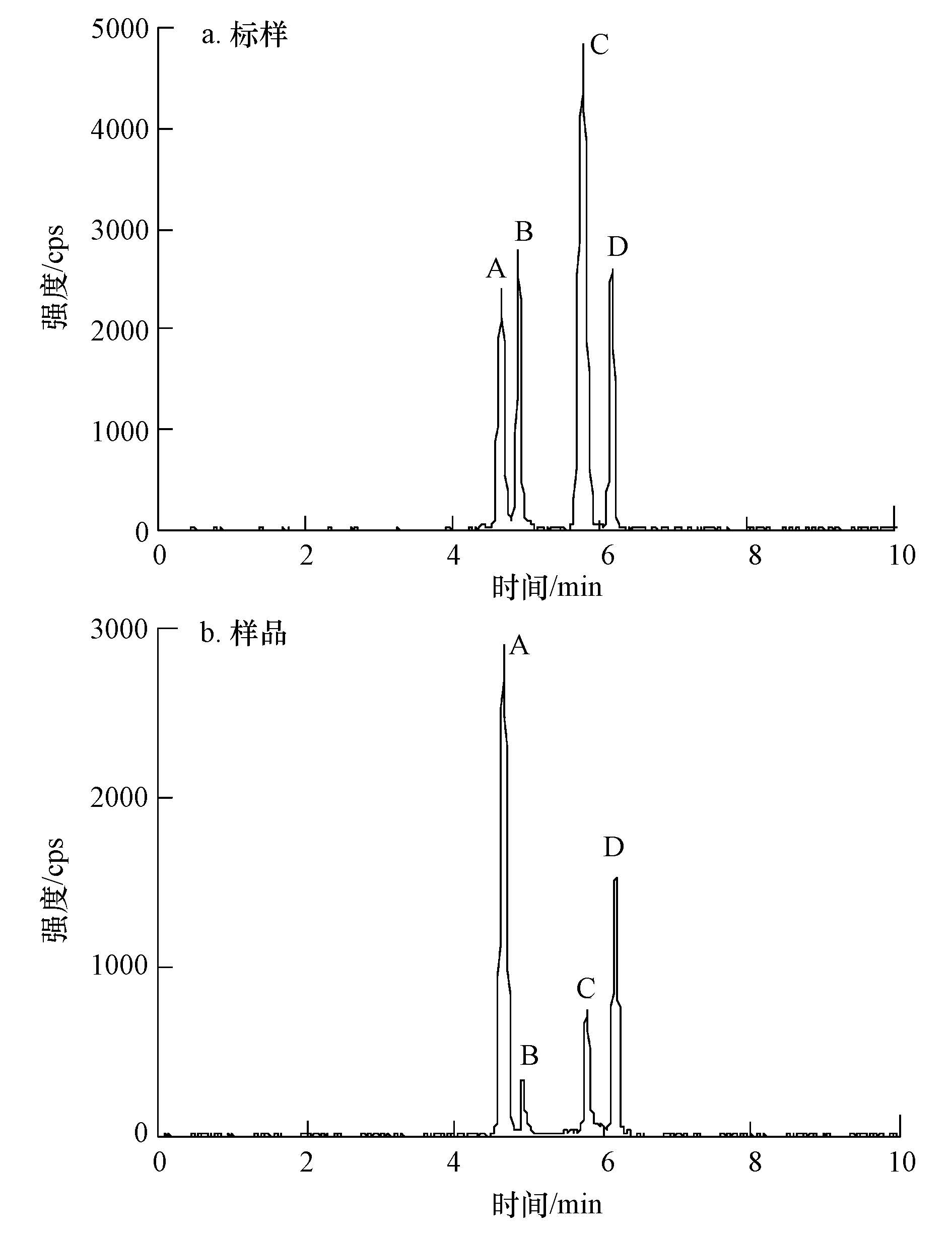 |
| 图3 芘代谢产物色谱图(A.2-萘酚; B.1-萘酚; C.9-羟基菲; D.1-羟基芘) Fig.3 Chromatogram of pyrene metabolites |
由质谱分析结果表明,芘降解过程中生成1-萘酚、2-萘酚、9-羟基菲和1-羟基芘4种单羟基多环芳烃,为了进一步验证这些低环的代谢产物能否最终被B. cereus彻底分解利用,本实验设置了4组降解体系,分别考察B. cereus对这4种芘中间代谢产物的降解情况,实验结果如图 4所示.
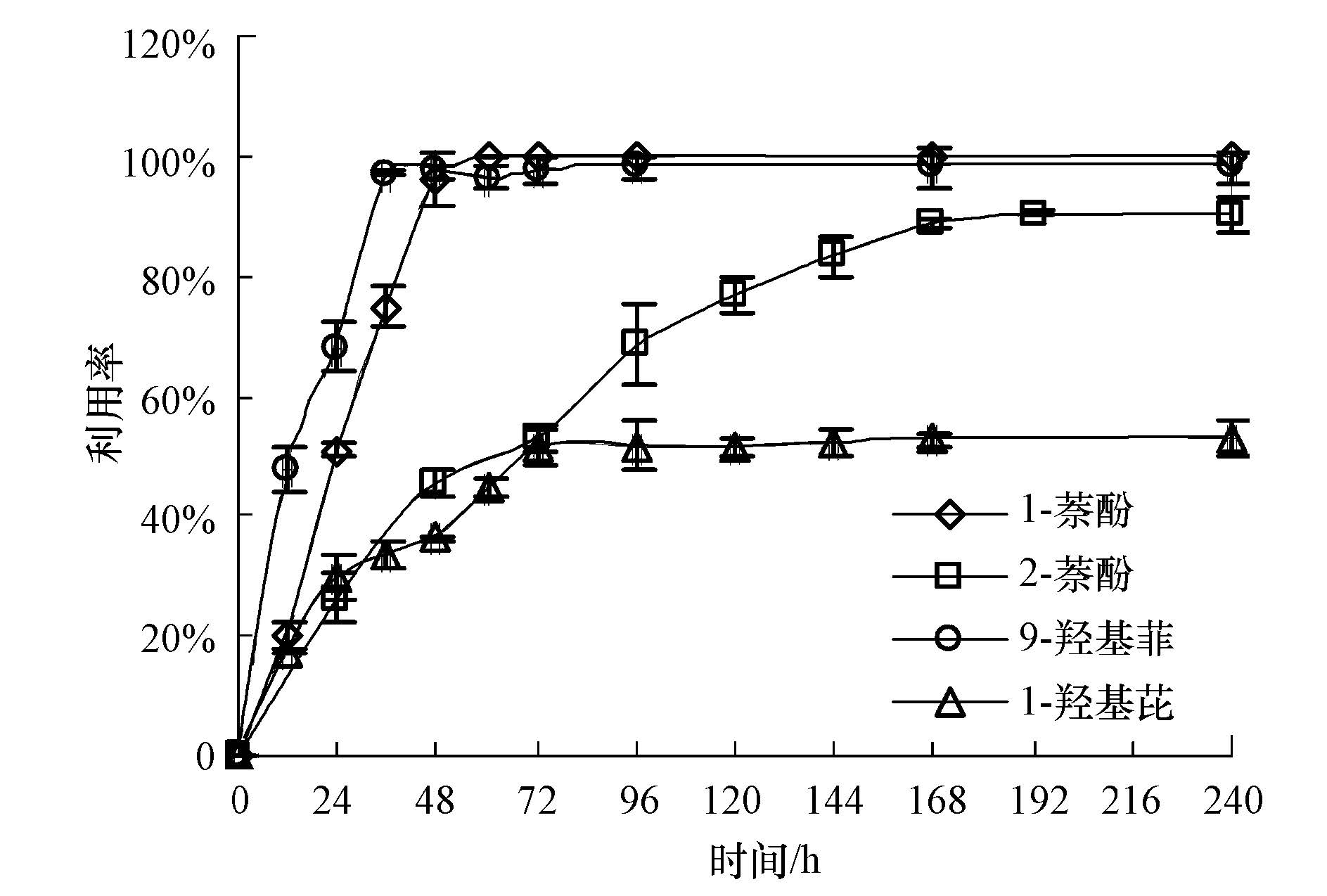 |
| 图4 单羟基多环芳烃利用率随时间的变化 Fig.4 Utilization rate of monohydroxy-PAHs over time |
从图 4看出,B. cereus对1-萘酚的分解利用效果明显,在第48 h时,溶液中1-萘酚的残余浓度仅为0.07 μmol · L-1,被利用率达到96.3%,到了第60 h,样品中的1-萘酚浓度已低于仪器检出限.而相比之下,2-萘酚却不易被B. cereus分解利用,在48 h时,体系中2-萘酚的利用率只有45.4%,明显低于1-萘酚.之后随着时间延长,溶液中2-萘酚还是被逐渐分解,到第168 h趋于平稳,240 h时溶液中2-萘酚残余浓度达最低为0.21 μmol · L-1,降解率最高为90.3%.可见,相对于2-萘酚,B. cereus更容易分解利用1-萘酚.有研究报道,2-萘酚比1-萘酚的生物毒性更大,生物降解相对缓慢(Zang and Lian, 2009).说明2-萘酚对B. cereus细胞的毒害作用是影响其被利用效率的重要因素. B. cereus对9-羟基菲的分解速率更快速,在36 h时,体系中9-羟基菲降解率已达到97.2%.在反应的前96 h内,溶液中残余9-羟基菲的最低浓度为0.03 μmol · L-1.由此可见,微生物对PAHs的降解效率并不一定只和苯环数以及污染物的化学结构有关,还可能与微生物本身对不同污染物分解利用特性有关.对于含有4个苯环的1-羟基芘,虽然相对于芘,其生物毒性降低了,但B. cereus对其的降解利用仍较为缓慢,到第72 h,1-羟基芘的去除率才开始趋于稳定,在降解过程中,其降解率最高为52.7%,此时残余的1-羟基芘浓度为0.83 μmol · L-1,明显高于其它几种物质的残余量.
在修复过程中,随着芘被开环分解,生成各种更容易被微生物利用的低环化合物,在B. cereus降解芘的同时也分解利用这些代谢产物,并优先利用更适宜的且容易被分解的化合物,因此,在3.3节的实验中,我们检测到反应120 h后,溶液中1-萘酚和9-羟基菲的含量相对较低.而具有一定生物毒性的2-萘酚的残余浓度最大,这是因为随着4环和3环物质逐渐被菌体分解,势必生成低环的化合物,从而使分解利用效率低的2-萘酚在溶液中积累.而1-羟基芘是芘生物解毒第一步的代谢产物,随着低环物质的生成,其利用也会受到影响.
3.5 B. cereus降解芘关键酶的活性分析芘的微生物降解主要依靠菌体细胞的关键酶起作用.在提取的降解了芘后B. cereus的细胞粗酶液中,检测到水杨酸羟化酶,邻苯二酚1,2-双加氧酶和邻苯二酚2,3-双加氧酶的活性,且经过芘诱导后,这3种酶的活性均有明显提高,说明水杨酸羟化酶,邻苯二酚1,2-双加氧酶和邻苯二酚2,3-双加氧酶都是B. cereus降解芘的关键酶,其活性变化见表 2.
| 表2 修复体系中B. cereus细胞关键酶活性分析 Table 2 Activity analysis of key enzyme in B. cereus cell |
有文献报道(张丹等,2010),PAHs的微生物降解途径可分为水杨酸代谢途径和邻苯二甲酸代谢途径. Bourguignon等通过研究分析Rhodococcus sp.降解萘、菲和芘过程中邻苯二酚1,2-双加氧酶的基因片段,推断萘、菲和芘在Rhodococcus sp.体内是通过水杨酸途径代谢(Bourguignon et al., 2014).因此,从本实验中检测到的芘降解过程中菌体细胞相关酶活性的变化可以推测,B. cereus主要通过水杨酸-邻苯二酚途径降解芘.由于邻苯二酚在邻苯二酚1,2-双加氧酶和邻苯二酚2,3-双加氧酶的作用下可以形成邻位和间位两种结构,从而又可以分为两种不同的代谢途径,因此B. cereus降解芘的途径并不是只有单一1种.根据所检测到的代谢产物以及降解过程中相关酶活性变化,推测B. cereus降解芘可能存在的降解途径,如图 5所示.
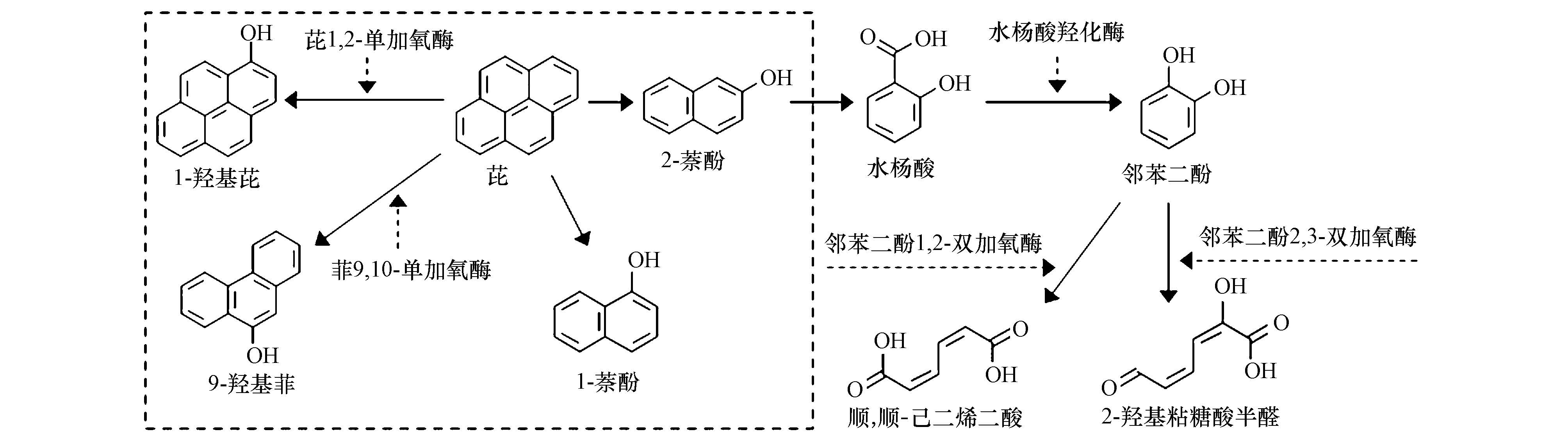 |
| 图5 B. cereus降解芘的可能降解途径 Fig.5 Degradation pathway of pyrene by B. cereus |
另外,PAHs的微生物降解过程,一般是通过双加氧酶或单加氧酶的催化作用来使苯环羟基化和开环裂解,进而形成水杨酸和邻苯二甲酸等三羧酸循环的中间产物,再通过进入三羧酸循环而最终氧化成二氧化碳和水( da Silva et al., 2004). Stingley等研究表明,M. vanbaalenii PYR-1在降解PAHs的初始阶段就是由单加氧酶和双加氧酶同时起作用攻击苯环,进而发生开环裂解反应(Stingley et al., 2004).结合3.3节实验中检测到的4种单羟基多环芳烃代谢产物的生成情况(主要由菌体单加氧酶作用下生成),以及反应体系中菌体细胞中双加氧酶的活性变化,可以推断B. cereus对芘的降解是由单加氧酶和双加氧酶联合作用的.
4 结论(Conclusions)1)蜡状芽胞杆菌(Bacillus cereus)能利用芘作为唯一碳源和能源生长. 10 mg · L-1葡萄糖,1 mg · L-1 Mn2+和0.1 mg · L-1 Fe3+的加入能促进B. cereus对芘的降解;投菌量1 g · L-1条件下,反应120 h,B. cereus对2.5 μmol · L-1芘的降解率达到61.4%.
2)根据建立的LC-MS/MS芘代谢产物分析方法,检测到反应120 h后体系中生成1-萘酚、2-萘酚、9-羟基菲和1-羟基芘4种单羟基多环芳烃代谢产物.B. cereus对4种代谢产物的最高利用率分别为100%、90.3%、98.3%和52.7%. 说明B. cereus在降解芘同时也分解更容易被利用的代谢产物.
3)水杨酸羟化酶,邻苯二酚1,2-双加氧酶和邻苯二酚2,3-双加氧酶是B. cereus降解芘的关键酶,经芘诱导后3种酶的活性均有明显提高.综合代谢产物分析及酶活变化,推断出B. cereus对芘的降解途径以及降解过程是由单加氧酶和双加氧酶联合起作用.
| [1] | Bourguignon N, Isaac P, Alvarez H, et al. 2014. Enhanced polyaromatic hydrocarbon degradation by adapted cultures of actinomycete strains[J]. Journal of Basic Microbiology, 54(12):1288-1294 |
| [2] | Bradford M M. 1976. A rapid and sensitive method for the quantitation of microgram quantities of protein utilizing the principle of protein-dye binding[J]. Analytical Biochemistry, 72(1/2):248-254 |
| [3] | Carney M W, Erwin K, Hardman R, et al. 2008. Differential developmental toxicity of naphthoic acid isomers in medaka (Oryzias latipes) embryos[J]. Marine Pollution Bulletin, 57(6/12):255-266 |
| [4] | Chen K, Zhu Q, Qian Y G, et al. 2013. Microcalorimetric investigation of the effect of non-ionic surfactant on biodegradation of pyrene by PAH-degrading bacteria Burkholderia cepacia[J]. Ecotoxicology and Environmental Safety, 98(12):361-367 |
| [5] | da Silva M, Esposito E, Moody J D, et al. 2004. Metabolism of aromatic hydrocarbons by the filamentous fungus Cyclothyrium sp.[J]. Chemosphere, 57(8):943-952 |
| [6] | 邓军, 尹华, 叶锦韶, 等. 2010. 氧化节杆菌与苯并[a]芘-镉交互作用机理[J]. 化工学报, 61(3):747-753 |
| [7] | Eibes G, Cajthaml T, Moreira M T, et al. 2006. Enzymatic degradation of anthracene, dibenzothiophene and pyrene by manganese peroxidase in media containing acetone[J]. Chemosphere, 64(3):408-414 |
| [8] | Guzik U, Hupert-Kocurek K, Sitnik M, et al. 2013. High activity catechol 1, 2-dioxygenase from Stenotrophomonas maltophilia strain KB2 as a useful tool in cis,cis-muconic acid production[J]. Antonie van Leeuwenhoek, 103(6):1297-1307 |
| [9] | Haritash A K, Kaushik C P. 2009. Biodegradation aspects of polycyclic aromatic hydrocarbons(PAHs):a review[J]. Journal of Hazardous Materials, 169(1/3):1-15 |
| [10] | Jurelevicius D, Alvarez V M, Peixoto R, et al. 2012. Bacterial polycyclic aromatic hydrocarbon ring-hydroxylating dioxygenases (PAH-RHD) encoding genes in different soils from King George Bay, Antarctic Peninsula[J]. Applied Soil Ecology, 55:1-9 |
| [11] | Lange S J, Que Jr L. 1998. Oxygen activating nonheme iron enzymes[J]. Current Opinion in Chemical Biology, 2(2):159-172 |
| [12] | Mishra S, Singh S N. 2014. Biodegradation of benzo(a)pyrene mediated by catabolic enzymes of bacteria[J]. International Journal of Environmental Science & Technology, 11(6):1571-1580 |
| [13] | Parikh S J, Chorover J, Burgos W D. 2004. Interaction of phenanthrene and its primary metabolite (1-hydroxy-2-naphthoic acid) with estuarine sediments and humic fractions[J]. Journal of Contaminant Hydrology, 72(1/4):1-22 |
| [14] | 邱云云, 尹华, 叶锦韶, 等. 2013. 嗜麦芽窄食单胞菌去除水中芘-镉复合污染的特性[J]. 农业环境科学学报, 32(3):629-634 |
| [15] | Ravelet C, Krivobok S, Sage L, et al. 2000. Biodegradation of pyrene by sediment fungi[J]. Chemosphere, 40(5):557-563 |
| [16] | Selvakumaran S, Kapley A, Kashyap S M, et al. 2011. Diversity of aromatic ring-hydroxylating dioxygenase gene in Citrobacter[J]. Bioresource Technology, 102(7):4600-4609 |
| [17] | Šepič E, Bricelj M, Leskovšek H. 2003. Toxicity of fluoranthene and its biodegradation metabolites to aquatic organisms[J]. Chemosphere, 52(7):1125-1133 |
| [18] | Stingley R L, Brezna B, Khan A A, et al. 2004. Novel organization of genes in a phthalate degradation operon of Mycobacterium vanbaalenii PYR-1[J]. Microbiology, 150(11):3749-3761 |
| [19] | Tekere M, Read J S, Mattiasson B. 2005. Polycyclic aromatic hydrocarbon biodegradation in extracellular fluids and static batch cultures of selected sub-tropical white rot fungi[J]. Journal of Biotechnology, 115(4):367-377 |
| [20] | Verdin A, Sahraoui A L H, Durand R. 2004. Degradation of benzo[a]pyrene by mitosporic fungi and extracellular oxidative enzymes[J]. International Biodeterioration & Biodegradation, 53(2):65-70 |
| [21] | Wang Y L, Xia Z H, Liu D, et al. 2013. Multimedia fate and source apportionment of polycyclic aromatic hydrocarbons in a coking industry city in Northern China[J]. Environmental Pollution, 181(6):115-121 |
| [22] | Wojcieszyńska D, Hupert-Kocurek K, Jankowska A, et al. 2012. Properties of catechol 2, 3-dioxygenase from crude extract of Stenotrophomonas maltophilia strain KB2 immobilized in calcium alginate hydrogels[J]. Biochemical Engineering Journal, 66:1-7 |
| [23] | 吴蔓莉, 聂麦茜, 王晓昌, 等. 2008. Mn2+在黄杆菌FCN2菌株降解芘过程中的作用研究[J]. 环境科学, 29(7):1982-1985 |
| [24] | Wu Y C, Teng Y, Li Z G, et al. 2008. Potential role of polycyclic aromatic hydrocarbons (PAHs) oxidation by fungal laccase in the remediation of an aged contaminated soil[J]. Soil Biology and Biochemistry, 40(3):789-796 |
| [25] | Xu S S, Liu W X, Tao S. 2006. Emission of polycyclic aromatic hydrocarbons in China[J]. Environmental Science & Technology, 40(3):702-708 |
| [26] | Yuan S Y, Wei S H, Chang B V. 2000. Biodegradation of polycyclic aromatic hydrocarbons by a mixed culture[J]. Chemosphere, 41(9):1463-1468 |
| [27] | Zang S Y, Lian B. 2009. Synergistic degradation of 2-naphthol by Fusarium proliferatum and Bacillus subtilis in wastewater[J]. Journal of Hazardous Materials, 166(1):33-38 |
| [28] | 张丹, 李兆格, 包新光, 等. 2010. 细菌降解萘,菲的代谢途径及相关基因的研究进展[J]. 生物工程学报, 26(6):726-734 |
| [29] | 张娜, 尹华, 彭辉, 等. 2010. 嗜麦芽窄食单胞菌J12对芘的降解特性[J]. 环境科学与技术, 33(4):6-9 |
| [30] | Zheng Z M, Obbard J P. 2002. Oxidation of polycyclic aromatic hydrocarbons (PAH) by the white rot fungus, Phanerochaete chrysosporium[J]. Enzyme and Microbial Technology, 31(1/2):3-9 |
| [31] | Zhong Y, Luan T G, Zhou H W, et al. 2006. Metabolite production in degradation of pyrene alone or in a mixture with another polycyclic aromatic hydrocarbon by Mycobacterium sp.[J]. Environmental Toxicology and Chemistry, 25(11):2853-2859 |
| [32] | Zhou N Y, Al-Dulayymi J, Baird M S, et al. 2002. Salicylate 5-hydroxylase from Ralstonia sp. strain U2:a monooxygenase with close relationships to and shared electron transport proteins with naphthalene dioxygenase[J]. Journal of Bacteriology, 184(6):1547-1555 |
 2016, Vol. 36
2016, Vol. 36


