2. 中国科学院生态环境研究中心, 北京 100085
2. Research Center for Eco-Environmental Sciences, Chinese Academy of Sciences, Beijing 100085
多溴二苯醚(Polybrominated diphenyl ethers,PBDEs)作为溴代阻燃剂被广泛应用于纺织、建材、家居装饰和电子产品等领域(Darnerud,2003). 由于PBDEs具有价格便宜、热稳性好、阻燃效率高等特点,故其使用量逐年增加(Reiner et al., 2011).其中,在商业产品中主要用到的3种PBDEs混合物分别是五溴二苯醚、八溴二苯醚和十溴二苯醚(Zhang et al., 2013). 近年来的研究表明,PBDEs不都是以化学键形式与本体材料结合,大多采用“添加式”加入本体材料中,故其很容易渗透、挥发到环境介质中(Reiner et al., 2011). 目前,全球范围内都能检测到痕量的PBDEs,例如,胚胎和儿童体内(万斌等,2011),以及海洋、湖泊等水体(Li et al., 2014)和北极地区(Schecter et al., 2005)等.同时,PBDEs可通过食物链逐级放大,并长距离迁移,也可通过“蚱蜢跳效应”广域迁移,导致全球污染(Reiner et al., 2011;Li et al., 2014;Schecter et al., 2005). 然而,生物积累性、持久性和生物毒性是PBDEs的主要环境特征(万斌等,2011). PBDEs可对人的大脑、肝脏和肾脏等器官及神经系统、内分泌系统、生殖系统产生急性或慢性毒性,对试验动物有致癌性、生殖毒性、神经毒性和内分泌干扰毒性(Mhadhbi et al., 2012). 近年来,PBDEs的毒性研究已经成为热点,而2,2′,4,4′,5-五溴二苯醚(BDE-99)是PBDEs家族中最具代表性的多溴二苯醚(Mhadhbi et al., 2012;Li et al., 2014;Schecter et al., 2005),在环境中检出频次较高,具有较强的毒性,且检测含量高.
人血清白蛋白(Human Serum Albumin,HSA),是人血浆中含量最为丰富的可溶性载体蛋白,它兼具着吸收、运输、分布和代谢外源性物质等功能(Khan et al., 2008). HSA由3个类似的结构域组成,每个区域又分为A、B两个子区域,外源物质进入血液后主要结合在HSA的IIA(Site 1)和IIIA(Site 2)两个疏水腔内(Tabassum et al., 2012). 研究外源性物质与HSA的相互作用有助于更好地了解人血清白蛋白的生理活动和作用机制. 因此,本文以BDE-99为例,采用计算模拟和光谱实验相结合的方法,从多个角度研究多溴二苯醚与HSA作用机制,这在环境毒理学上具有十分重要的意义,也可为后人研究环境污染物多溴二苯醚与人血清白蛋白之间的作用机理提供多角度的分析手段指导.
2 实验部分(Experimental) 2.1 仪器和试剂仪器:RF-5301PC荧光光度计(日本岛津公司),TU-1901双光束紫外可见分光光度计(北京普析通用仪器有限公司),EL204电子分析天平(梅特勒-托利多仪器(上海)有限公司),pHS-3C精密pH计(上海雷磁仪器厂).
试剂:BDE-99购自德国DR公司,先用200 μL乙腈溶解12 μL BDE-99原液(50 μg · mL-1),再用pH=7.4的Tris-HCl缓冲溶液(含NaCl 0.15 mol · L-1)定容至10 mL,配制1.0×10-6 mol · L-1储备液;人血清白蛋白溶液购自美国sigma公司,使用Tris-HCl缓冲溶液配制成1.0×10-5 mol · L-1的储备液,4 ℃以下冰箱保存备用;实验所用试剂均为分析纯;用水均为二次水.
2.2 计算模拟本文所有的计算工作均在DELL服务器、RedHat Linux(版本,5.0)系统上完成.首先使用Sybyl x 1.1软件进行分子对接,然后将对接结果导入软件GROMACS(版本,4.5.5)进行分子动力学模拟,最后利用软件VMD和LIGPLOT进行结果图形展示和分析.所用的HSA晶体结构(PDB代码:1O9X,1O9X由去掉波动区域较大C、N-末端氨基酸残基的579个氨基酸构成,残基区域为4~582,结构相对完整,在位点I和位点II处均含有对应配体,便于计算模拟)从Brookhaven蛋白质数据库(http://www.rcsb.org/pdb)获得.
2.3 实验过程荧光光谱:在10 mL的比色管中分别加入1 mL 1.0×10-5 mol · L-1 HSA溶液,以及不同量的1.0×10-6 mol · L-1 BDE-99溶液,用pH=7.4 Tris-HCl缓冲溶液定容至刻度,摇匀.在290、300、310 K下恒温反应5 min后,于λex=295 nm处测定体系荧光强度.使用上述溶液测定△λ = 15 nm及△λ = 60 nm时的同步荧光光谱及激发波长每增加5 nm的发射光谱绘制三维荧光(λex=260~500 nm,λem=260~500 nm).仪器的激发和发射荧光狭缝均为5 nm.
3 结果与讨论(Results and discussion) 3.1 HSA与BDE-99复合物结构特征 3.1.1 分子动力学模拟利用分子动力学模拟可以研究水溶液中BDE-99与HSA结合时的动力学情况(Gumbart et al., 2005),通过计算均方根偏差(RMSD)、均方根波动(RMSF)、回旋半径(Rg)等参数分析结构的稳定性,观察其结构波动,从而判断其构象变化.
图 1为HSA体系和BDE-99-HSA体系的RMSD和RMSF波动情况.图 1a的RMSD值是反映体系原子相对与平衡位置的波动情况,由图可知,两个体系在整个模拟过程中RMSD值变化幅度不大,且BDE-99-HSA体系的RMSD值要小于HSA体系的RMSD值,这反映了BDE-99能与HSA形成稳定的复合物,使BDE-99-HSA体系更趋于稳定. 图 1b 的均方根波动(RMSF)是基于残基分析蛋白质柔性的变化情况,由图可知,总体上两体系的残基相对于平衡位置的波动相似且变化较小,但在位点I(残基196~297)处BDE-99-HSA体系的RMSF值均大于HSA体系,表明BDE-99与HSA结合后趋使其内部氨基酸残基的柔性发生变化,致使HSA内部微环境发生改变,进而诱导HSA的构象发生变化.
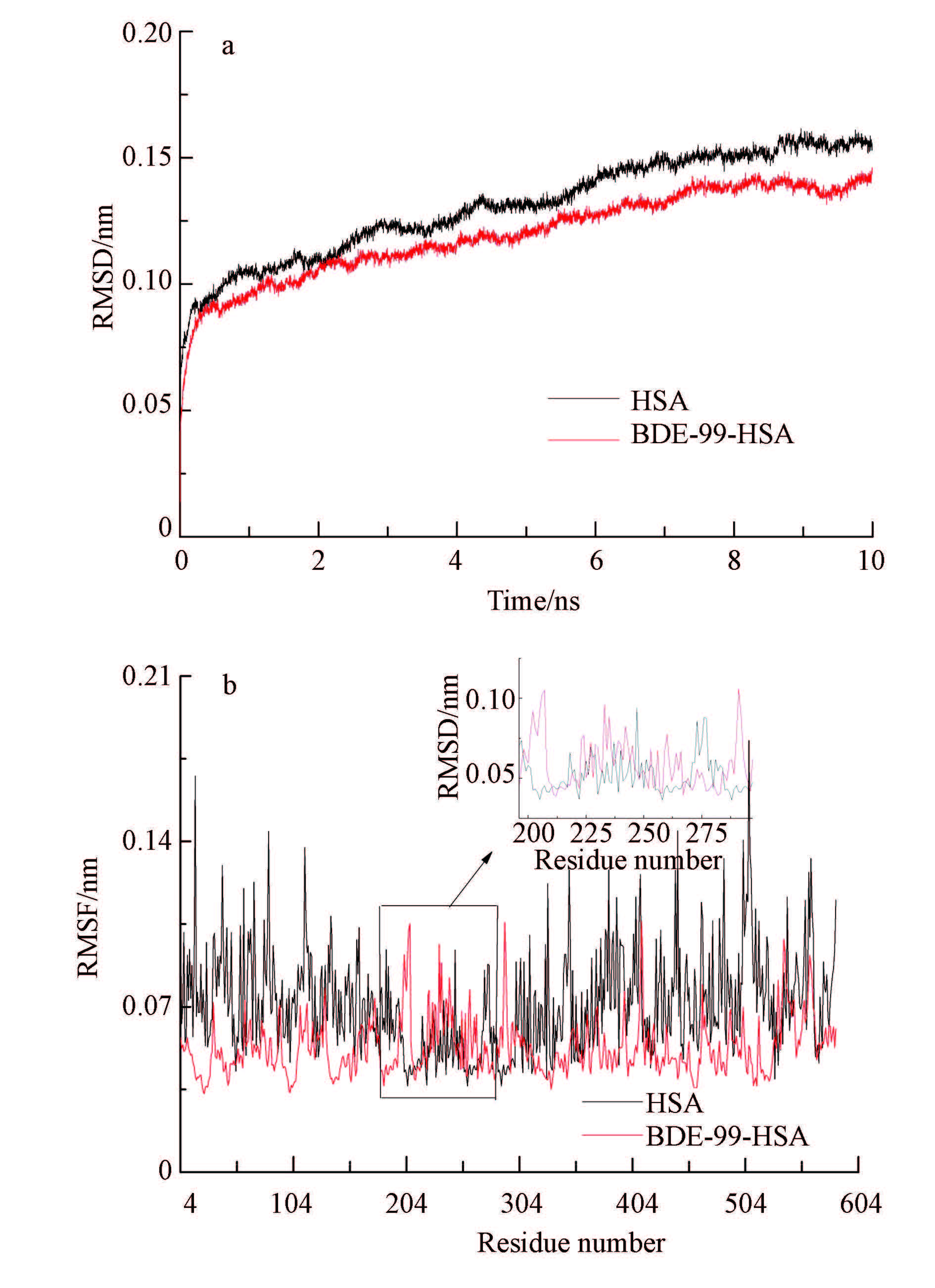 |
| 图1 10 ns MD的HSA和BDE-99-HSA体系RMSD(a)和RMSF(b) Fig.1 Root mean square atomic positional deviation(RMSD)(a) and root mean square atomic positional fluctuations(RMSF)(b)of acid residues of HSA and HSA-BDE-99 averaged over 10 ns of MD simulation |
图 2为两个体系Rg值的波动情况和提取不同时间的HSA的构象叠加. Rg值可分析蛋白质结构的紧凑程度. 由图可以看到HSA-BDE-99复体系的Rg值高于HSA的Rg值,说明BDE-99与HSA结合时改变了HSA的紧凑程度,驱使α-螺旋、β-折叠等发生变化,使得HSA的结构变得松散、膨胀,这与HSA构象叠加图变化相一致. 因此,得出BDE-99使HSA的构象发生改变.
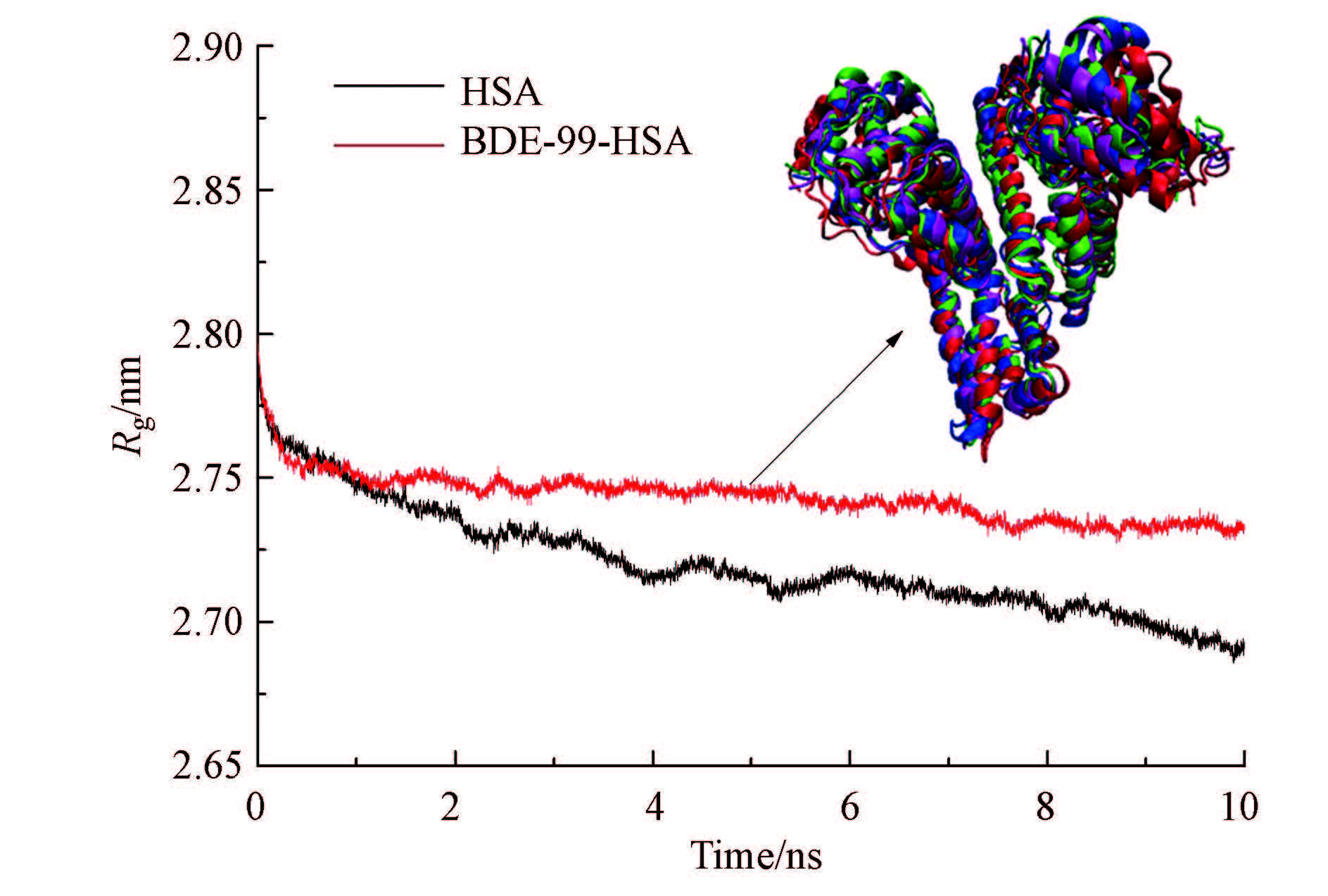 |
| 图2 10 ns MD的HSA和BDE-99-HSA体系的Rg值和不同时间的HSA的结构叠加图 Fig.2 Rg of free HSA and BDE-99-HSA complexes and structural superposition of HSA at specific time from 10 ns MD(0 ns(red),3 ns(purple),7 ns(blue),10 ns(green)) |
图 3为HSA和BDE-99-HSA体系的疏水性残基和亲水性残基的可及表面积(SASA)变化情况. 由图可知,BDE-99-HSA体系的疏水性残基的SASA为198.81 nm2,比HSA体系的156.04 nm2增加了27.41%,而BDE-99-HSA体系的亲水性残基的SASA为130.81 nm2,比HSA体系的142.46 nm2减少了8.18%. 综合以上分析得出,BDE-99与HSA的结合使HSA内部的疏水性增强,残基间的疏水力相互排斥,导致其结构变得松散,进而影响其构象变化.
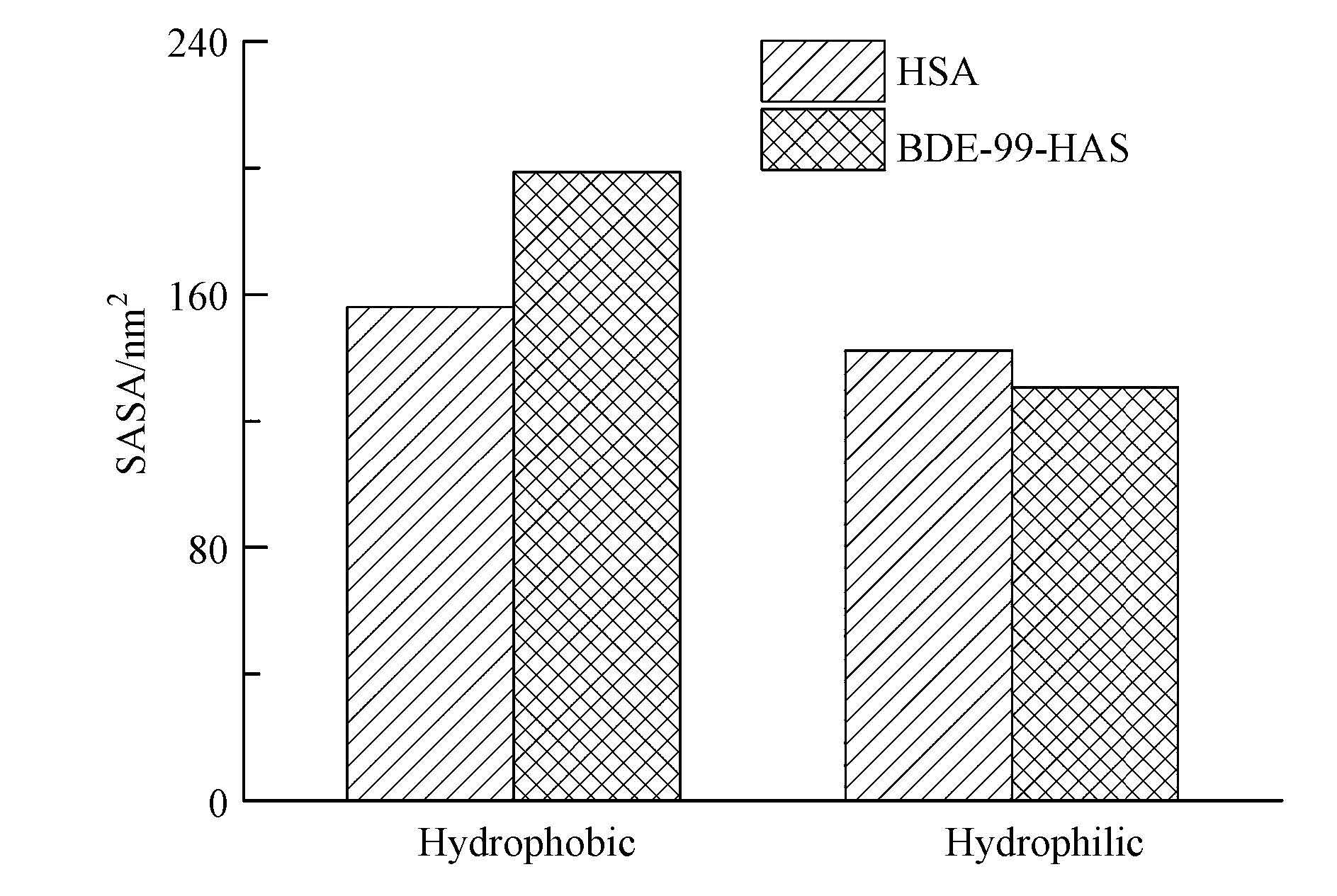 |
| 图3 HSA和BDE-99-HSA体系的疏水基团和亲水基团的可及表面积 Fig.3 Solvent accessible surface areas for hydrophobic and hydrophilic moieties in the HSA and BDE-99-HSA |
利用三维荧光光谱可以直观有效的判断生物大分子的构象变化(Gumbart et al., 2005). 由图 4可以看出,BDE-99-HSA体系比HSA体系的峰B(瑞利散射峰)强度明显增强,由此可判断BDE-99与HSA发生了相互作用,生成了颗粒较大的复合物,使其体系的瑞利散射强度增大.而HSA-BDE-99体系相比HSA体系的峰A(荧光峰)的强度则由616.97降低到531.74且出现蓝移,表明BDE99与HSA结合导致氨基酸之间的疏水性增强,疏水作用力变大,使体系结构发生变化.
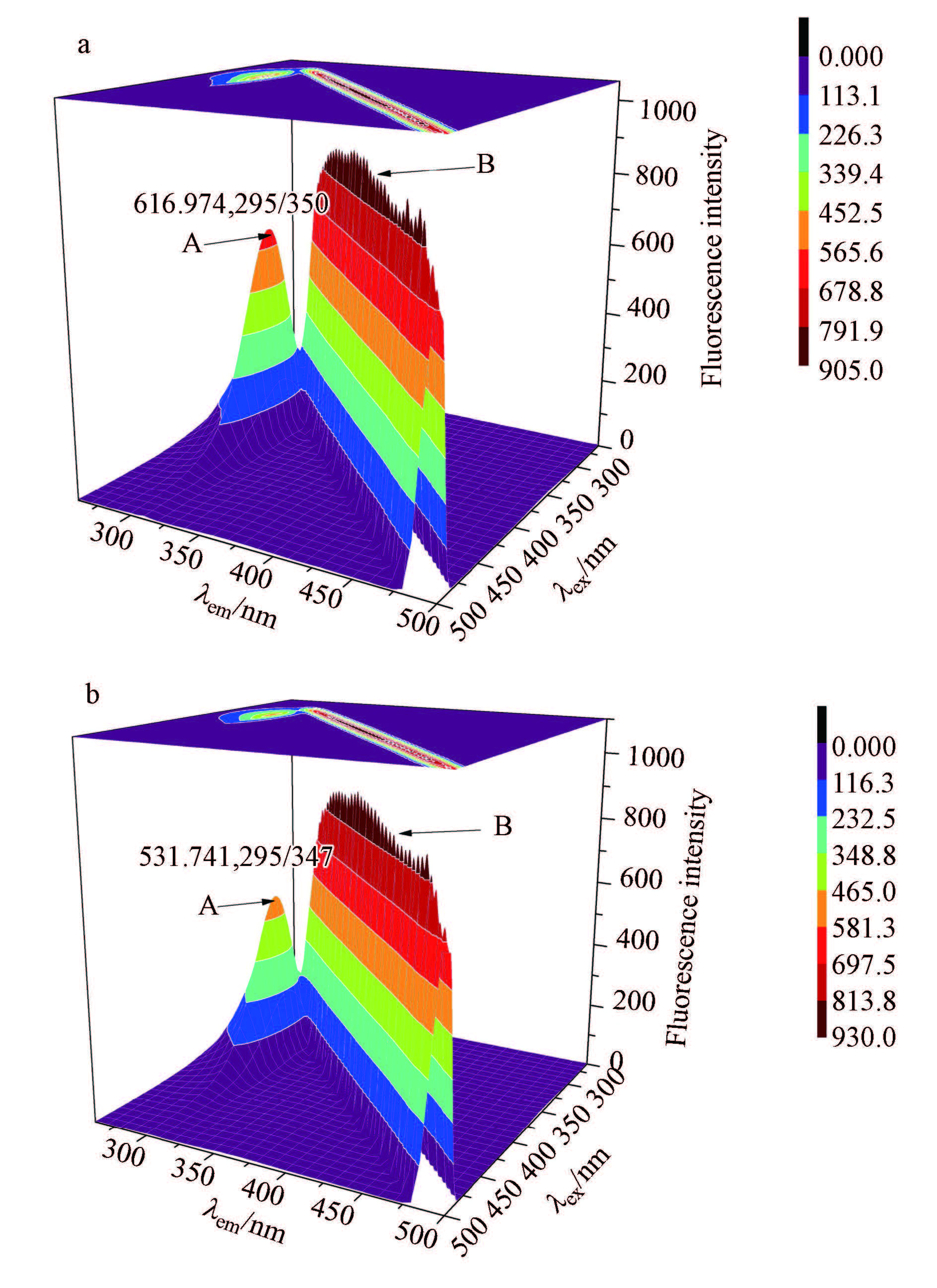 |
| 图4 HSA体系(a)和HSA -BDE-99体系(b)的三维荧光光谱(cHSA=1.0×10-5 mol · L-1;cBDE-99=3.0×10-9 mol · L-1) Fig.4 Three-dimensional fluorescence spectra and contour diagrams of HSA(a) and BDE-99- HSA(b) |
利用同步荧光光谱法(Tabassum et al., 2012)从氨基酸残基的角度分析结合体系的光谱性质. 如图 5所示,随着BDE-99浓度的增加,酪氨酸残基光谱(图 5a)和色氨酸残基光谱(图 5b)的荧光强度都发生有规律的猝灭,说明BDE-99的加入对酪氨酸和色氨酸残基微环境构象都造成了影响. 图 5b中色氨酸残基荧光强度变化幅度较大,且出现明显的蓝移(Δλ=4 nm),说明BDE-99使其疏水性增强,疏水作用力增大. 由此推断BDE-99使HSA的构象发生了变化,且HSA的荧光猝灭主要由色氨酸残基所贡献,结合位点也更接近色氨酸残基.
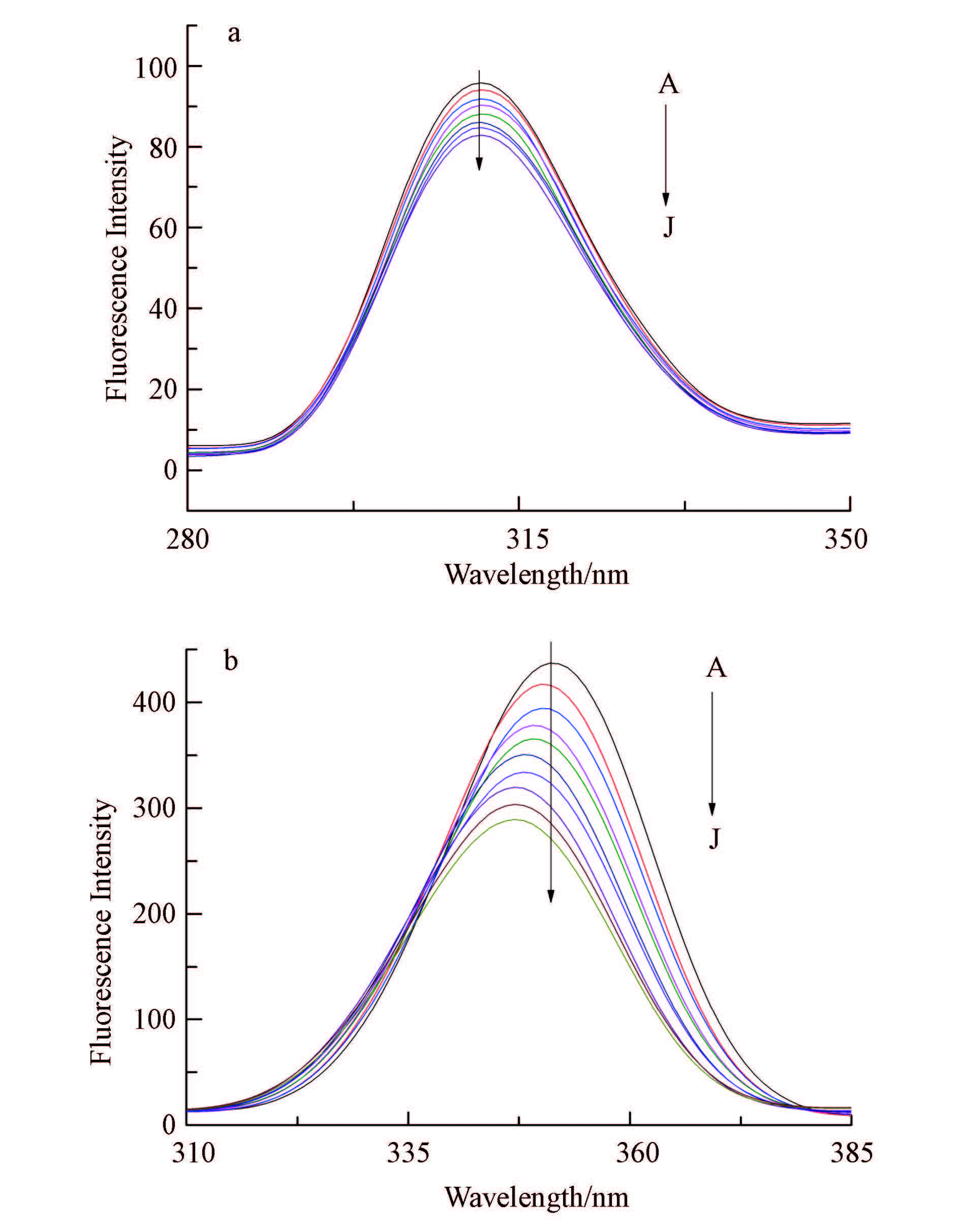 |
| 图5 HSA-BDE-99的同步荧光光谱(a.Δλ = 15 nm; b.Δλ = 60 nm;cHSA=1.0×10-6 mol · L-1; A~J: cBDE-99= 0~9×10-9 mol · L-1) Fig.5 Synchronous fluorescence spectra of BDE-99-HSA(a.Δλ = 15 nm; b.Δλ = 60 nm;cHSA=1.0×10-6 mol · L-1; A~J: cBDE-99= 0~9×10-9 mol · L-1) |
HSA的内源性荧光主要是由色氨酸、酪氨酸和苯丙氨酸提供(Zohoorian-Abootorabi et al., 2012).图 6为在不同浓度BDE-99下的HSA的荧光猝灭图.由图可以得出,BDE-99进入了HSA的疏水性空腔并与其发生了相互作用,使其疏水性增强致使HSA的荧光强度有规律地猝灭且出峰位置发生蓝移现象(Δλ = 3nm). 为了判断BDE-99与HSA相互作用的荧光猝灭机制,通常进行猝灭速率常数的计算. 猝灭速率常数可由Stern-Volmer方程(Chen et al., 2013)得出:
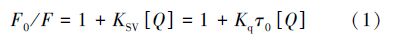
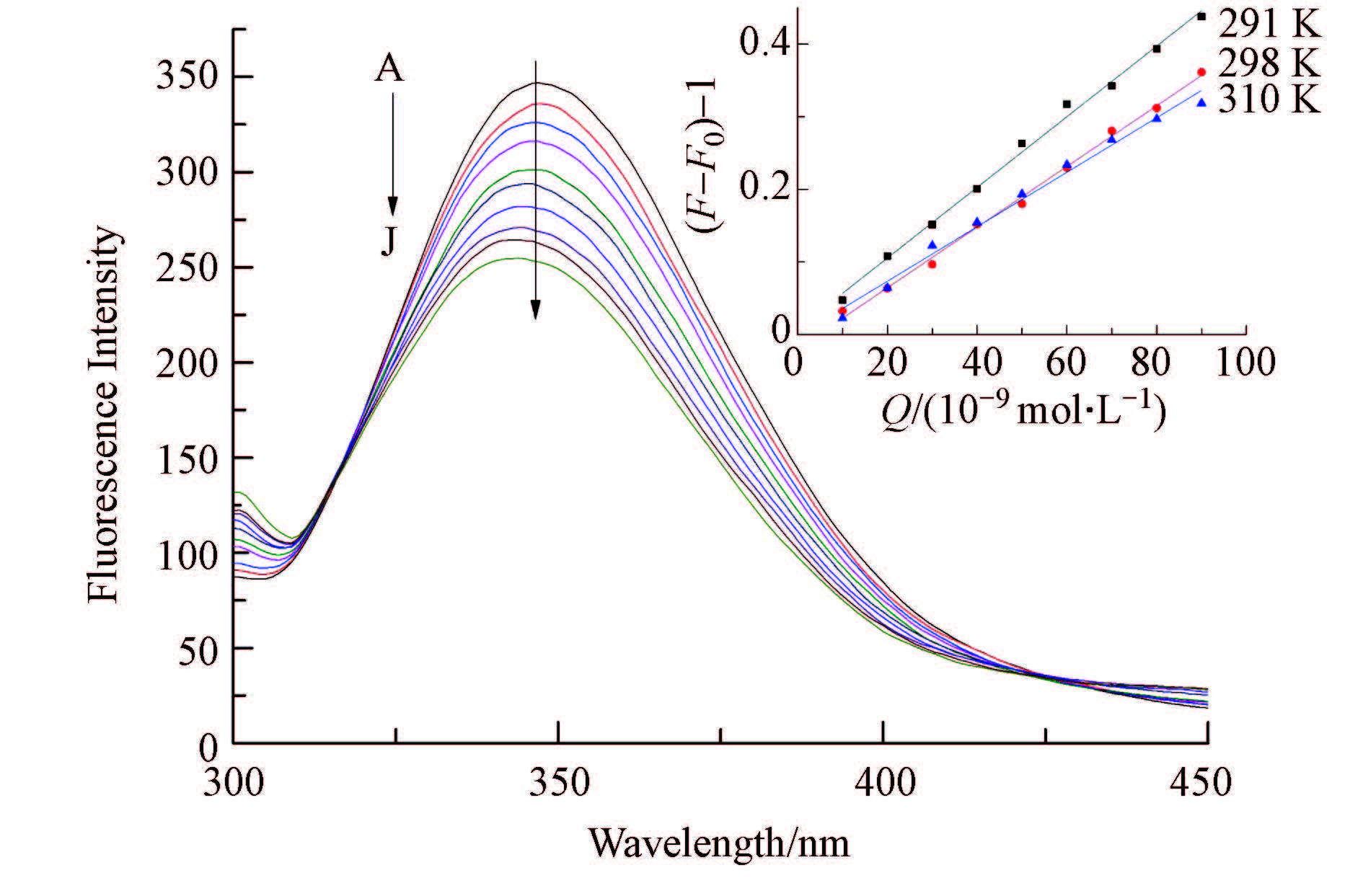 |
| 图6 BDE-99对HSA的荧光猝灭图(T = 298 K, cHSA = 1.0×10-6 mol · L-1,A~J:cBDE-99 =0~9×10-9 mol · L-1) Fig.6 Fluorescence quenching spectra of HSA |
由Stern-Volmer方程求得的猝灭速率常数KSV,结果表明,KSV随着温度升高而降低(见图 6小图),且BDE-99对HSA的Kq值也远大于各类猝灭剂对生物大分子最大动态的猝灭常数2.0×1010 L · mol-1 · s-1(Zohoorian-Abootorabi et al., 2012),故判断该猝灭机制是静态猝灭.这也说明BDE-99进入HSA的疏水腔内,两者之间发生了相互作用生成了不具有荧光的复合物,引起了HSA构象的变化,最终导致HSA的荧光发生猝灭.
3.2.2 BDE-99与HSA作用的能量转移Frster偶极-偶极非辐射能量转移(Chen et al., 2013)也是导致荧光发生猝灭的一种机制. 根据Frster偶极-偶极非辐射能量转移理论判断两种化合物是否发生非辐射能量转移. 同时结合计算公式(2)~(4)还可以得出能量给体与受体间的能量转移效率E,以及临界距离R0和二者间结合距离r等信息.
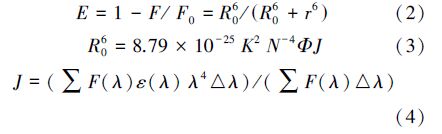
图 7为BDE-99的紫外吸收光谱图与HSA的荧光光谱图的重叠图谱.分析数据得出两光谱重叠区的重叠积分J=1.91×10-12 cm3 · L · mol-1,临界距离R0= 3.18 nm,能量转移效率E=0.42和BDE-99与HSA中的结合位置距离色氨酸残基的距离r=3.47 nm,且r<7 nm并满足0.5R<r<1.5R,符合非辐射能量转移的条件(Chen et al., 2013). 因此,进一步说明BDE-99与HSA结合时也通过能量转移机制引起其荧光猝灭,并且能量转移的效率较高. 故BDE-99是通过静态猝灭和能量转移两种方式导致HSA的荧光猝灭.
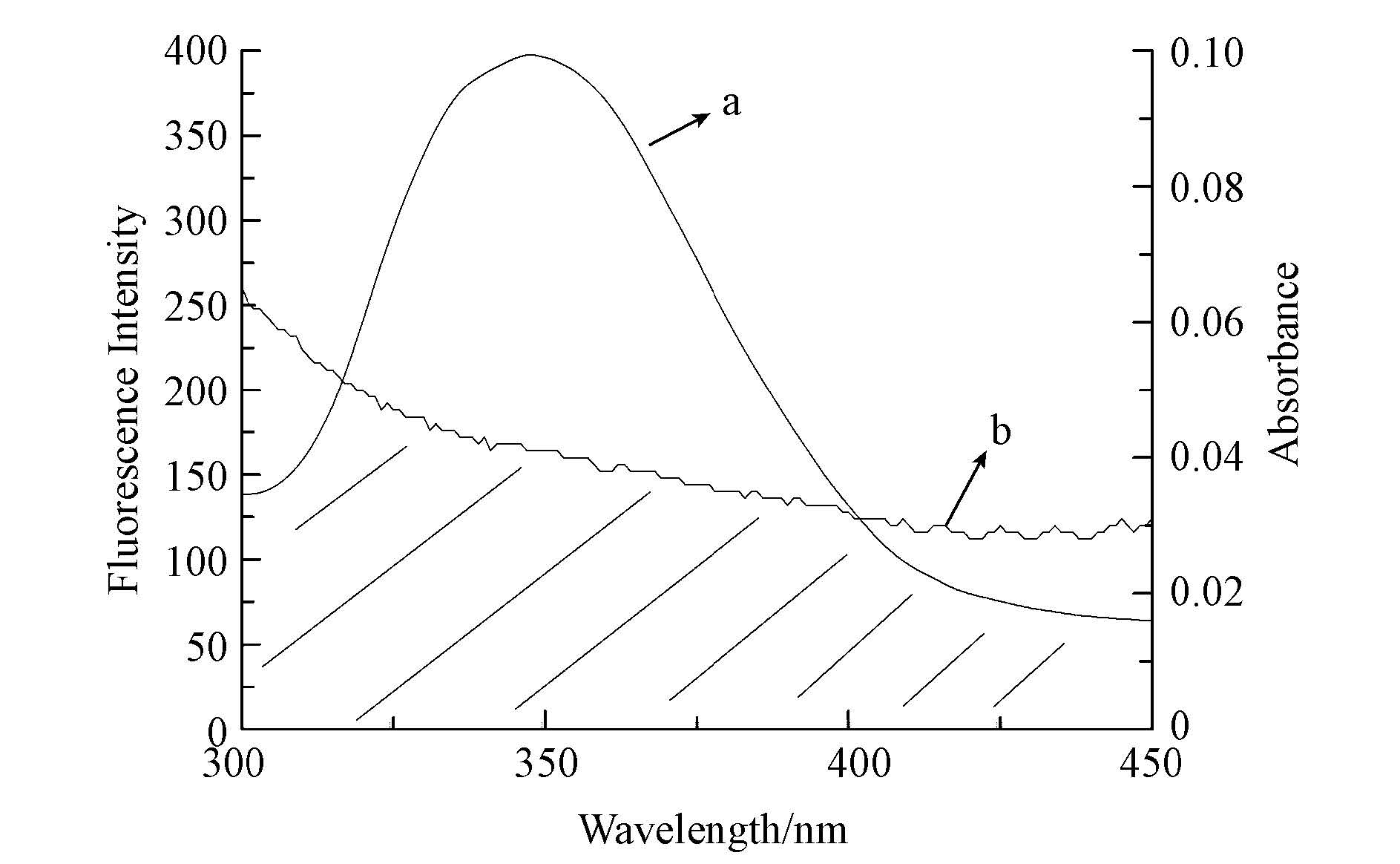 |
| 图7 HSA的荧光光谱(a)和BDE-99的紫外吸收光谱(b)(T=300 K,cHSA = cBDE-99 = 1.0×10-6 mol · L-1) Fig.7 Overlap of fluorescence spectrum of HSA(a) and absorbance spectrum of BDE-99(b) |
分子对接是用来分析小分子与HSA的结合情况,探讨其结合位信息(Zohoorian-Abootorabi et al., 2012). 运用Sybyl x 1.1软件,将BDE-99分别与HSA的位点I、位点II进行对接,选取较高得分位点并分析结果. 对接结果表明,BDE-99在HSA的位点I处,其0.5 nm范围内的氨基酸残基(图 8a),键合形式主要是苯环部分的π-π堆积作用(图 8b)、疏水作用力(图 8c)和弱的静电引力(图 8d),其中,疏水作用力较大且对配合物的稳定性起着重要作用.由图 8b可以看出,TRP 214与BDE-99的a环形成一个错位面对面的堆积(即F型堆积)作用,而PHE211则与BDE-99形成一个边对面堆积(即T型堆积)作用,这两种常见的π-π堆积作用对BDE-99-HSA复合物的稳定性起着一定的作用.同时,由于LYS199和ARG218都是带有—NH2的极性氨基酸且极性较大,这些极性基团与BDE-99表面发生静电作用,极性基团间通过静电引力使之聚集而排斥疏水基团而产生疏水作用力,而TRY214和PHE211都是疏水性氨基酸且带有较强的疏水作用力,从图 8c的小图得出,LYS199、PHE211、TRP214和ARG218在BDE-99周围形成一个疏水性力场,将其包裹在其中心.此外,通过对接也可测出BDE-99与TRP214的距离为0.247 nm,完全符合能量转移条件.
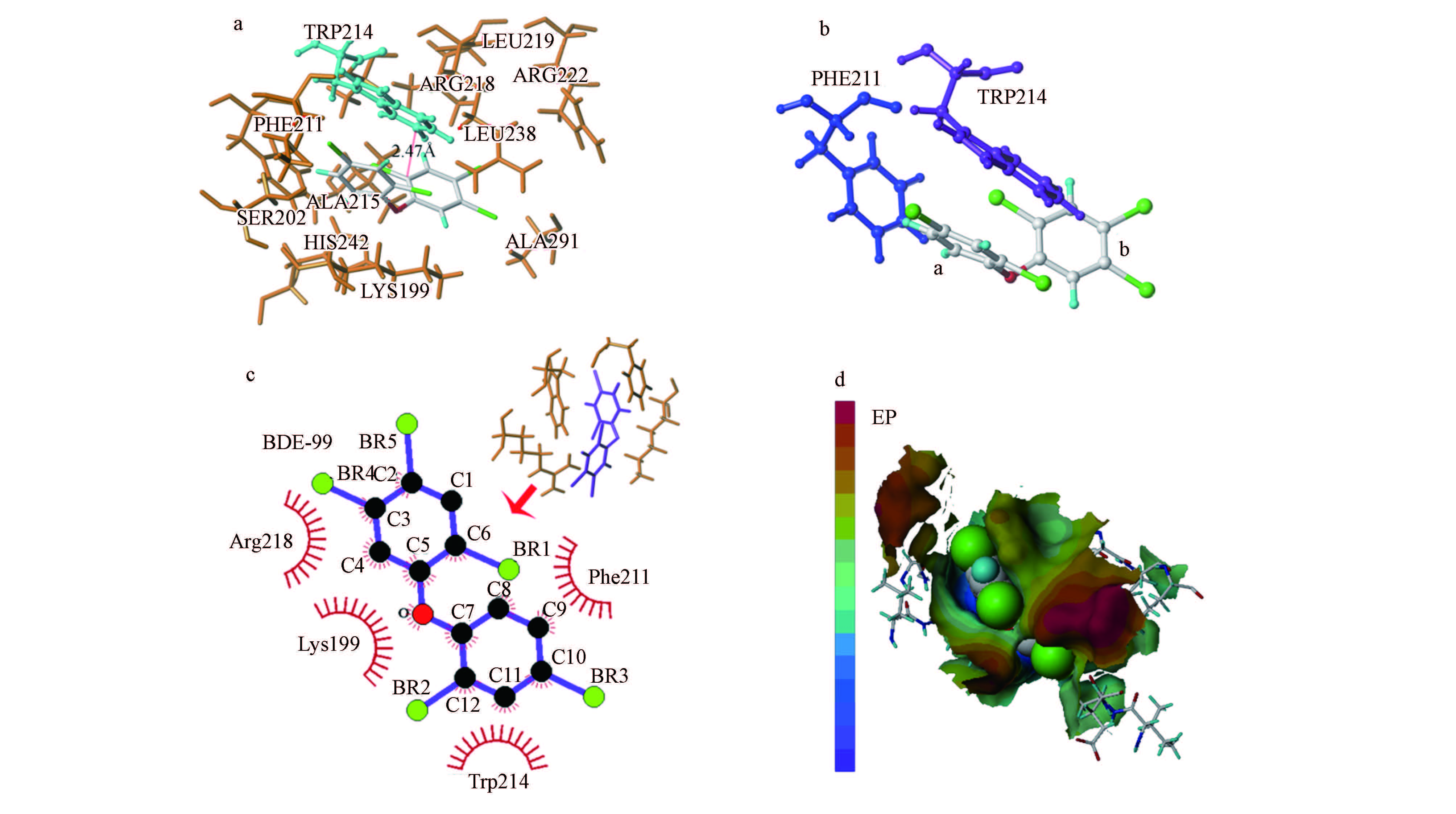 |
| 图8 BDE-99在HSA位点I处的分子对接分析图(a.0.5 nm范围内与BDE-99作用的残基,b. π-π堆积作用,c.疏水作用,d.静电作用) Fig.8 Molecular docking and detailed view |
BDE-99与HSA相互作用时的表观结合常数Ka与结合位点数n可以通过双对数公式(Neamtu et al., 2013)求得:
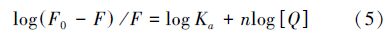
| 表1 不同温度下BDE-99-HSA体系的结合常数(Ka)、结合位点(n)和热力学参数 Table 1 Binding constants(Ka),number of binding sites(n) and thermodynamic parameters of BDE-99-HSA system at different temperatures |
从表 1可以看出,BDE-99与HSA结合位点数n约为1,表明在BDE-99与HSA作用时只有一个结合位点. BDE-99与HSA的结合常数较大,在106数量级以上,说明两者的结合能力较强,在其与HSA发生相互作用结合后可被蛋白质吸收、储存和转运.
3.3.3 热力学参数和结合力的确定药物分子与蛋白之间结合的相互作用力主要有静电引力、氢键、范德华力和疏水作用力等(Zohoorian-Abootorabi et al., 2012). 通过热力学方程,可计算焓变(△H)、熵变(△S)和自由能变化(△G),从而分析BDE-99与HSA之间结合的相互作用力类型.
根据文献(Tian et al., 2010),在一定温度和压力的条件下,ΔG<0可以促进自发反应;ΔH和ΔS的相对大小可以判断小分子和蛋白质的主要角色类型. 如表 1所示,实验结果表明,该体系的ΔG<0,ΔH<0,△S>0,可以推断,BDE-99和HSA之间的相互作用是一种自发的放热过程,且其结合的主要驱动力为静电引力和疏水作用力,这也验证了分子对接结果.
3.3.4 BDE-99与HSA的竞争结合位点的确定竞争试验是一种有效、快捷判断药物小分子与蛋白质的结合区域和结合位点的方法(Tian et al., 2010). 通常采用布洛芬、华法林等荧光探针对蛋白质不同区域进行特异性结合来确定药物小分子与蛋白质作用的结合区域和结合位点(Ye et al., 2014). 竞争试验的结合常数可以通过修正的Stern-Volmer方程(Ye et al., 2014)得出:
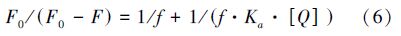
经计算得出,加入Warfarin探针后BDE-99与HSA的结合常数为8.14×105 L · mol-1,明显比未加入探针的结合常数9.92×106 L · mol-1小很多,而加入Ibuprofen探针后的结合常数为2.04×106 L · mol-1,与未加入探针的相差不多,因此,说明BDE-99与HSA的结合位置是位点I,这与分子对接结果相一致. 另外,BDE-99能猝灭HSA的内源性荧光,故可以推断出BDE-99可与HSA的位点I处的色氨酸残基作用,这也与同步荧光结果相吻合.
4 结论(Conclusions)利用分子对接、动力学模拟和光谱法探讨了BDE-99与HSA的相互作用.动力学模拟研究表明,BDE-99使HSA的疏水性增强,结构膨胀、松散,导致其二级结构发生变化. 三维荧光与同步荧光结果与动力学模拟相一致,分子对接得到BDE-99通过疏水作用力和静电引力结合在位点I处,热力学参数与竞争实验也验证了这一结果. 此外,荧光光谱和紫外光谱还得出BDE-99猝灭HSA荧光的作用机制是静态猝灭和能量转移;BDE-99与TRY214的结合距离为3.47 nm,与分子对接结果(r=0.247 nm)相吻合均小于7 nm. 研究结果较为深入全面地探讨了BDE-99与HSA的毒理机制,能为HSA结构变化方面提供可靠信息.
| [1] | Chen R R, Jiang H, Pu H L. 2013. Interaction of artemisinin and its derivatives with human serum albumin studied using spectroscopies and molecular modeling methods[J]. Molecular Biology Reports, 40(8):4791-4804 |
| [2] | Darnerud P O. 2003. Toxic effects of brominated flame retardants in man and in wildlife[J]. Environment International, 29(6):841-853 |
| [3] | Gumbart J, Wang Y, Aksimentiev A, et al. 2005. Molecular dynamics simulations of proteins in lipid bilayers[J]. Current Opinion in Structural Biology, 15(4):423-431 |
| [4] | Khan S N, Islam B, Yennamalli R, et al. 2008. Interaction of mitoxantrone with human serum albumin:spectroscopic and molecular modeling studies[J]. European Journal of Pharmaceutical Sciences, 35(5):371-382 |
| [5] | Li H J, Lan J, Li G L, et al. 2014. Distribution of polybrominated diphenyl ethers in the surface sediment of the East China Sea[J]. Chinese Science Bulletin, 59(4):379-387 |
| [6] | Mhadhbi L, Fumega J, Beiras R. 2012. Toxicological effects of three polybromodiphenyl ethers (BDE-47, BDE-99 and BDE-154) on growth of marine algae Isochrysis galbana[J]. Water, Air, & Soil Pollution, 223(7):4007-4016 |
| [7] | Neamtu S, Tosa N, Bogdan M. 2013. Spectroscopic investigation of tolmetin interaction with human serum albumin[J]. Journal of Pharmaceutical and Biomedical Analysis, 85:277-282 |
| [8] | Reiner J L, Phinney K W, Keller J M. 2011. Determination of perfluorinated compounds in human plasma and serum Standard Reference Materials using independent analytical methods[J]. Analytical and Bioanalytical Chemistry, 401(9):2899-2907 |
| [9] | Schecter A, Päepke O, Tung K C, et al. 2005. Polybrominated diphenyl ether flame retardants in the U.S. population:current levels, temporal trends, and comparison with dioxins, dibenzofurans, and polychlorinated biphenyls[J]. Journal of Occupational and Environmental Medicine, 47(3):199-211 |
| [10] | Tabassum S, Al-Asbahy W M, Afzal M, et al. 2012. Synthesis, characterization and interaction studies of copper based drug with Human Serum Albumin (HSA):spectroscopic and molecular docking investigations[J]. Journal of Photochemistry and Photobiology B:Biology, 114:132-139 |
| [11] | Tian F F, Jiang F L, Han X L, et al. 2010. Synthesis of a novel hydrazone derivative and biophysical studies of its interactions with bovine serum albumin by spectroscopic, electrochemical, and molecular docking methods[J]. The Journal of Physical Chemistry B, 114(46):14842-14853 |
| [12] | 万斌,郭良宏. 2011.多溴联苯醚的环境毒理学研究进展[J].环境化学,30(1):143-152 |
| [13] | Ye Z W, Ying Y, Yang X L, et al. 2014. A spectroscopic study on the interaction between the anticancer drug erlotinib and human serum albumin[J]. Journal of Inclusion Phenomena and Macrocyclic Chemistry, 78(1/4):405-413 |
| [14] | Zhang L, Li J G, Zhao Y F, et al. 2013. Polybrominated diphenyl ethers (PBDEs) and indicator polychlorinated biphenyls (PCBs) in foods from China:levels, dietary intake, and risk assessment[J]. Journal of Agricultural and Food Chemistry, 61(26):6544-6551 |
| [15] | Zohoorian-Abootorabi T, Sanee H, Iranfar H, et al. 2012. Separate and simultaneous binding effects through a non-cooperative behavior between cyclophosphamide hydrochloride and fluoxymesterone upon interaction with human serum albumin:Multi-spectroscopic and molecular modeling approaches[J]. Spectrochimica Acta (Part A:Molecular and Biomolecular Spectroscopy), 88:177-191 |
 2016, Vol. 36
2016, Vol. 36


