2. 福州大学食品科学技术研究所, 福州 350108
2. Institute of Food Science and Technology, Fuzhou University, Fuzhou 350108
石墨烯是由sp2杂化的碳原子紧密排列而形成的蜂窝状的二维层状晶体,由于其独特的电学、光学、热学及机械性能,因而备受学术界的关注( vanden Brink,2007).自2004年以来,各种形式的石墨烯片被广泛地应用于晶体管、太阳能电池和生物传感器的探索研究中(Hu et al.,2010). 随着全球每年几十甚至几百吨由石墨烯作为基本构建块构成的所有维度的碳纳米材料(零维的富勒烯、一维的碳纳米管及三维的叠加石墨)的生产(Jia et al.,2005),倍受公众关注的生态环境及生物健康问题正在迅速扩大.近年来,研究人员陆续开展了对石墨烯的毒性的研究,发现石墨烯对微生物、植物、动物甚至人体均有潜在的毒性. 如Liu 等(2011)用40 μg · mL-1的石墨烯与大肠杆菌培养2 h后发现,大肠杆菌的活性从69.3%降低至47.4%,推断石墨烯主要通过其锋利的边缘切割细胞,造成细胞器、细胞膜的破损,细胞代谢能力下降,最终抑制细胞生长.Begum等(2011)研究表明,石墨烯处理后的白菜和西红柿根须长度、叶片数量、植株高度及地下生物量均明显减少. 然而,有关石墨烯对一些环境功能微生物菌群的毒性效应报道相对较少.
本课题组前期工作发现,嗜酸氧化亚铁硫杆菌(Acidithiobacillus ferrooxidans)可以用于污泥重金属生物淋滤(甘莉等,2014). Acidithiobacillus ferrooxidans广泛分布于自然界中,对多种重金属离子都具有较强的耐受能力(Novo et al.,2000),并且作为生物淋滤的主要细菌而被大量用于河流底泥、污水污泥中重金属的修复. 随着石墨烯在各个领域的应用,其在生产、使用、废弃过程中,必然会通过各种途径进入环境. 石墨烯进入土壤后可能通过地表径流方式进入水体(Nowack et al.,2007),最终沉积到河流底泥中(Geranio et al.,2009). 此外,石墨烯还会通过污水处理系统进入污泥中,但其如何影响污泥中工作的微生物的机理尚不清楚. 在本课题组前期研究污泥中的Acidithiobacillus ferrooxidans 对重金属离子溶出的工作基础上(Wen et al.,2013),本文开展石墨烯对Acidithiobacillus ferrooxidans生长的影响研究,以期为石墨烯的合理利用及其生态毒性评价提供理论依据.
2 材料与方法(Materials and methods) 2.1 试剂与仪器试剂:考马斯亮蓝G-250购自国药集团化学试剂有限公司;Tris-HCl、牛血清蛋白(BSA)均购自华美生物工程公司,进口分装;L-13152型Live/Dead Bacterial Viability Kit荧光染料购自Probes Molecular公司;氢氧化钠、无水乙醇、磷酸、盐酸购自天津市福晨化学试剂三厂,均为分析纯.
本实验所用的石墨烯购自北京德科岛金科技有限公司,厚度0.55~1.2 nm,直径0.5~3.0 μm,层数1~5层,纯度> 99%.
仪器:722N型可见分光光度计,PHS-3C型精密pH计,422型氧化还原电位仪(ORP复合电极),BS-224S型电子天平,SKY-2102型立式双层恒温培养摇床,JSM7500F型扫描电镜(SEM)(日本电子(JEOL)公司),TE2000-S型倒置荧光显微镜(日本尼康(Nikon)公司),LGJ-12型冷冻干燥机(北京松源华兴科技发展有限公司).
2.2 试验菌种与培养基本试验所用菌种为嗜酸氧化亚铁硫杆菌(Acidithiobacillus ferrooxidans),由本课题组分离自福州市金山污水处理厂回流污泥.
9K培养基(g · L-1):(NH4)2SO4 3.00,KCl 0.1,Ca(NO3)2 · 4H2O 0.0144,K2HPO4 0.50,MgSO4 · 7H2O 0.50,FeSO4 · 7H2O 44.30,蒸馏水1 L,pH=2.0.
2.3 试验方法 2.3.1 Acidithiobacillus ferrooxidans菌液的制备将Acidithiobacillus ferrooxidans菌株接种于90 mL的9K培养基中,在30 ℃、150 r · min-1的恒温培养振荡箱中培养72 h后,收获菌液,离心弃上清液,用无菌水稀释制备菌悬液,4 ℃保存备用. 用分光光度计测定420 nm处的光密度(OD420)以表征细菌的生物量.
2.3.2 不同浓度石墨烯对Acidithiobacillus ferrooxidans生长的影响在9K培养基中接种10%(体积比) Acidithiobacillus ferrooxidans菌液,并分别加入50、10、1 mg · L-1的石墨烯,于30 ℃、150 r · min-1恒温摇床中培养,每隔一定时间取样测定培养液的OD420、pH、氧化还原电位(ORP). ORP用422型氧化还原电位仪测定,以不加石墨烯的游离菌为空白对照组,每个处理重复3次.
2.3.3 可溶性蛋白测定在9K培养基中接种10%(体积比) Acidithiobacillus ferrooxidans菌液,分别加入50、10、1 mg · L-1的石墨烯,于30 ℃、150 r · min-1恒温摇床中培养,每隔一定时间取样分析可溶性蛋白. 可溶性蛋白提取步骤如下:移取培养液到50 mL的塑料离心管中,经低速、高速离心后弃上清液,精确加入1 mL蒸馏水溶解离心管底部菌体,加入10.5 mL Tris-HCl缓冲液(pH=7)和1 mL NaOH(6.25 mol · L-1),在100 ℃水浴中保持30 mim后取出摇匀,再静置冷却至室温,从中取1 mL上清液至玻璃管中,加入5 mL考马斯亮蓝显色剂,摇匀,室温下显色10 min后于波长595 nm下测定吸光度,以牛血清蛋白为标准物,用外标法计算体系中可溶性蛋白含量. 每个处理重复3次.
2.4 扫描电镜(SEM)样品的制备与测定两种浓度(1 mg · L-1和50 mg · L-1)石墨烯处理下的Acidithiobacillus ferrooxidans于30℃、150 r · min-1恒温摇床培养48 h,培养前后的菌液离心富集后用无菌水洗涤3次,再次离心去除上清液,菌体用2.5%的戊二醛缓冲液(pH=7.2)浸泡1 h固定,固定后的菌体进行冷冻干燥48 h. 干燥后样品置于金属载物圆台上进行喷金处理,最后通过SEM观察石墨烯作用前后菌体的表面形貌和微观形态变化.
2.5 荧光显微镜样品的制备与测定实验处理、菌体培养、收集方法同2.4节. 取经3次洗涤的菌体,用无菌水调节OD420=1,将配比好的LIVE/DEAD染色液与菌液按1∶1混合,置于暗处避光染色15 min后,取出10 μL用1 mL的无菌水稀释后,用Millipore GTTP02500 0.22 μm聚碳酸酯滤膜抽滤,再将滤膜制片,最后通过倒置荧光显微镜观察视野中死活菌比例.
3 结果与讨论(Results and discussion) 3.1 石墨烯对Acidithiobacillus ferrooxidans 生长的影响Acidithiobacillus ferrooxidans的生长曲线如图 1a所示. 由图可知,石墨烯对菌体的生长有一定的抑制作用. 随着石墨烯的浓度降低,对微生物的抑制作用逐渐增大,其中,1 mg · L-1的石墨烯对微生物的抑制作用最为显著. 对照组生长良好,培养3 h后菌体生长进入对数期,在48 h时OD420达到最大值0.163. 而添加石墨烯的试验组均出现延滞期延长、对数期缩短、最高生长量减少的情况,说明石墨烯对试验菌株具有毒性. 由于石墨烯溶解度低,高浓度的石墨烯较低浓度的石墨烯碰撞机率增大,更易团聚(Radic et al.,2013),而低浓度石墨烯在菌液中分散性好,在与细菌接触过程中,石墨烯片层结构通过其尖锐的边角对细菌细胞膜造成机械损伤,抑制其生理行为(Zhao et al.,2014). 因此,低浓度的石墨烯毒性更大,这些结果将在SEM和荧光显微镜表征数据中得到支持.
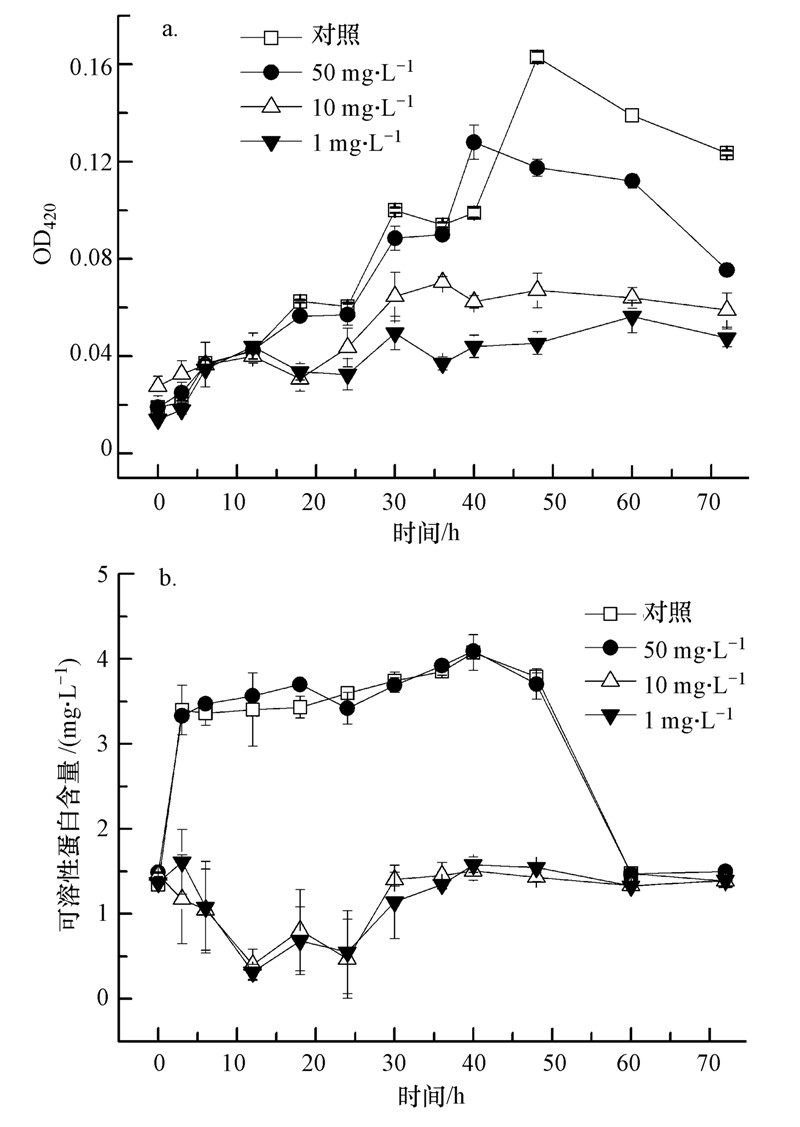 |
| 图 1 不同初始浓度的石墨烯对氧化亚铁硫杆菌生长的影响(a.OD420;b.可溶性蛋白) Fig. 1 Effect of graphene on the growth of Acidithiobacillus ferrooxidans under different initial concentration(a.OD420;b.soluble protein) |
不同浓度石墨烯处理下培养体系可溶性蛋白含量如图 1b所示. 由图可知,对照组的蛋白质含量在培养3 h后达到3.360 mg · L-1,随着时间的增长体系内蛋白质含量呈现缓慢上升趋势,于48 h时达到最大值3.789 mg · L-1,48 h后呈现下降趋势. 由于经过48 h,培养基被消耗,不能为微生物的生长提供足够的养分,导致体系内微生物死亡,细胞破裂,蛋白质含量降低. 在石墨烯处理试验组,当石墨烯投加量为1 mg · L-1和10 mg · L-1时,体系中可溶性蛋白含量呈现先减少后增大的现象. 而高浓度(50 mg · L-1)石墨烯试验组的蛋白质含量变化趋势与对照组的趋势近乎一致. 可解释为高浓度石墨烯在菌液中易团聚,能够作为细菌生长的载体,并吸附细菌生长所需要的营养物质,为细菌的繁殖提供了营养丰富的附着基底(Chen et al.,2008;Ruiz et al.,2011). 本文实验结果发现,高浓度石墨烯处理的菌的生长状况比低浓度好,这可能是低浓度的石墨烯分散性相对好于高浓度的石墨烯,与游离菌接触更加充分,分散在菌液中的石墨烯通过氧化应激、凝聚作用及物理接触的方式的联合作用对细胞产生毒性(Zhang et al.,2010),而高浓度的石墨烯反而由于团聚作用形成菌的生长载体,毒性不明显. 细菌OD420和蛋白质均是表征生物量的重要指标(Long et al.,2014). 然而,两种指标呈现的结果存在共同点时也有不同之处. 由于可溶性蛋白还代表各种酶和代谢调节物,与生物对环境胁迫的响应有关,细胞在适应石墨烯胁迫的生理过程中调节酶的合成与降解以适应新的环境.
3.2 石墨烯对培养体系氧化还原状况的影响图 2显示了在培养过程中体系pH和ORP的变化. 由图 2a可知,在培养的前期,所有处理的pH均逐渐增加,在24 h时(前)达到最大值,空白处理pH值要明显高于石墨烯处理试验组. 培养24 h后,所有处理pH均呈现下降趋势. 造成这种现象的原因可能是Acidithiobacillus ferrooxidans 是一株自养菌,在代谢过程中通过将Fe2+氧化成Fe3+来获取能量,生成的Fe3+最后经水解而释放出H+. 其生长过程可概括为两个阶段,可用以下两个反应方程表示(Zlatev et al.,2006):
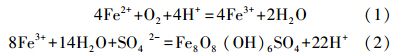
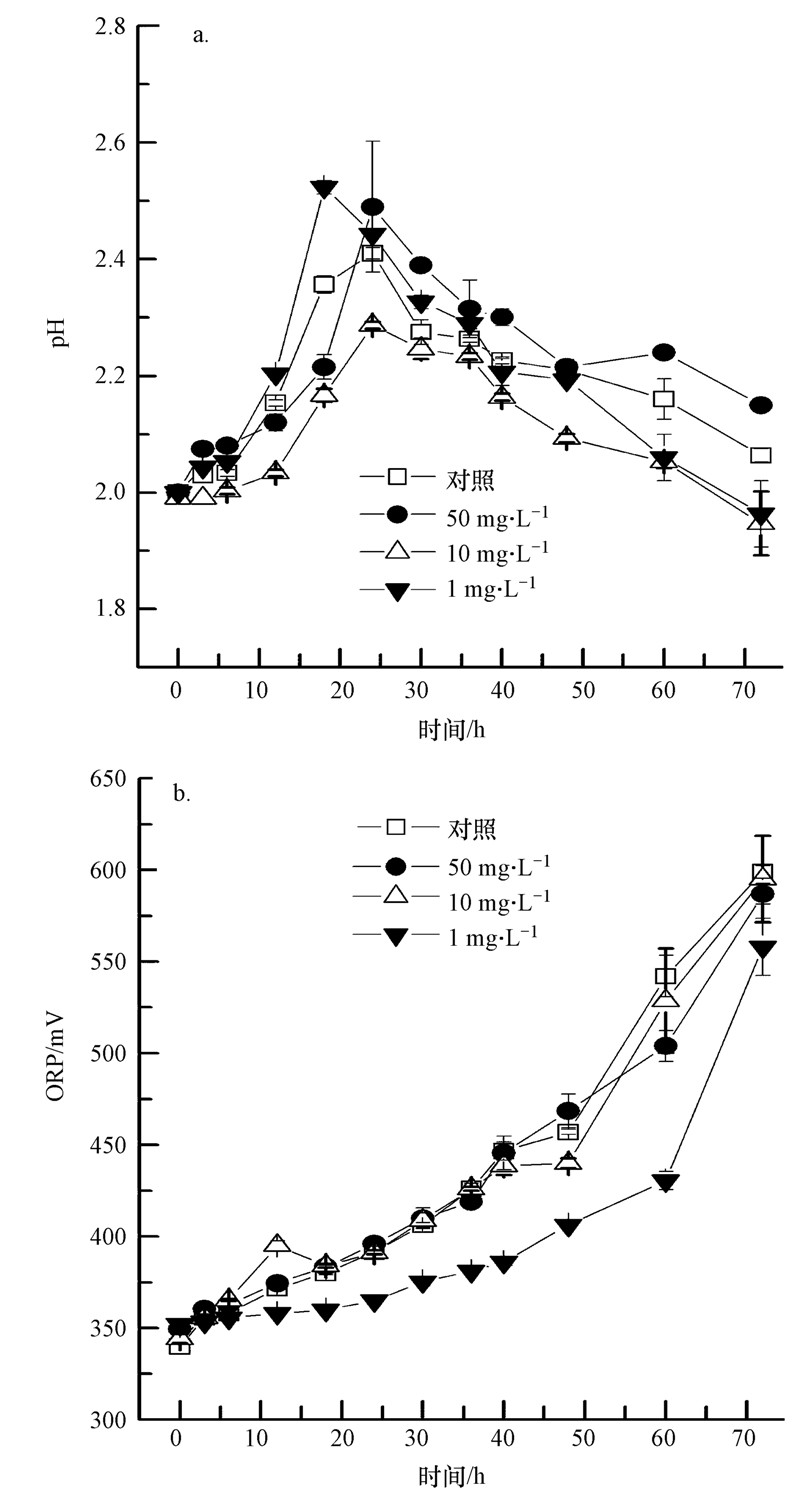 |
| 图 2 不同初始浓度的石墨烯下氧化亚铁硫杆菌的pH(a)和ORP(b)变化曲线 Fig. 2 The change of pH(a) and ORP(b)of Acidithiobacillus ferrooxidans under different initial concentration of graphene |
第一阶段质子被大量消耗,使培养液的pH在一定程度上迅速增大;第二阶段,Fe3+水解释放质子,导致pH在一定程度上急剧下降. pH的变化范围在1.9~2.6之间,仍为Acidithiobacillus ferrooxidans生长的最适pH范围(Nemati et al.,1998),说明并不是因为体系pH的改变造成菌体的死亡. 而溶液的pH变化可能与石墨烯的投加量有关,Machida等(2006)研究发现,石墨烯能够有效吸附水体中的重金属离子,在培养液中大量分散的石墨烯与Fe3+发生吸附作用,导致第一阶段的反应向生成Fe3+方向移动. 当石墨烯投加量为1 mg · L-1时,第一阶段的pH在一定程度上上升更迅速. 可能是因为低浓度的石墨烯在菌液中不易团聚,比高浓度的石墨烯有更大的比表面积,能更充分地吸附体系中的Fe3+,促使第一阶段的反应向生成Fe3+方向移动,从而加大对H+的消耗. 因此,在这一浓度石墨烯处理下pH在18 h达最高点,相比其它处理要提前6 h. 由于细菌表面的细胞壁含有肽聚糖、脂多糖、磷壁酸和胞外多糖,且羟基、磷酰基、羧基等带负电荷的化学基团丰富,因此,细菌会与体系中的Fe3+发生离子交换反应,从而吸附体系中Fe3+(Machida et al.,2006). 在第二阶段,由于低浓度石墨烯的毒性效应,使细胞大量死亡,细胞表面吸附态Fe3+被释放到培养体系中发生水解. 此外,石墨烯吸附态Fe3+再次进入水体发生水解,使pH快速下降且最终低于对照处理. 而高浓度(50 mg · L-1)石墨烯处理由于发生团聚作用,使Fe3+被包覆到团聚体内层结构中,无法再次水解,导致培养结束时pH值高于对照处理.
由图 2b可以看出,所有处理的ORP均呈不断上升趋势直至培养结束(72 h).石墨烯投加量为50和10 mg · L-1试验组的ORP均低于空白处理体系的ORP,但培养结束后3个体系的ORP都维持在600 mV左右. 当石墨烯的投加量为1 mg · L-1时,培养体系的ORP上升速度要明显低于其他处理. 说明高浓度的石墨烯对Acidithiobacillus ferrooxidans的氧化还原反应影响较小,而低浓度的石墨烯则抑制了它的活性. ORP上升主要由两种机制引起:第一种为生物反应主导的电子传递过程,是由于菌体在第一阶段的生长中能将Fe2+氧化为Fe3+失去电子使ORP迅速提高(Li et al.,2007),这一机制适用于对照组及50和10 mg · L-1试验组;第二种机制为化学反应主导的电子传递过程,是由于Fe2+通过利用空气中的分子氧进行化学氧化为Fe3+使ORP得到提高,这一机制适用所有处理. 因此,1 mg · L-1试验组的ORP上升较为缓慢.
3.3 石墨烯对菌体的毒理表征 3.3.1 SEM结果不同浓度石墨烯处理前后的菌体SEM分析结果如图 3所示. 与石墨烯接触前,菌体呈杆状,细胞结构完整,表面纹路清晰(图 3a). 而在石墨烯作用后(图 3b、图 3c),菌体表面变得粗糙,菌体之间发生挤压粘结. 图 3b中可观察到菌体细胞发生变形并且表面产生不规则的凸起,部分菌体细胞甚至裂解成不规则细胞碎片. 这一结果进一步肯定了前文中提出的论点,低浓度石墨烯在菌液中分散性好,不易团聚,能与菌体细胞充分接触而破坏细胞. 经过50 mg · L-1石墨烯处理后(图 3c),菌体细胞仍然呈杆状,结构相对完整,细胞表面纹路相对清晰,菌体相互粘连并附着在石墨烯上生长状况良好. Chen 等(2008)研究发现,小鼠成纤维细胞可以黏附在大尺寸石墨烯上生长,说明大尺寸石墨烯与生物具有相容性. 这一结论与本文的研究结果相吻合,这也进一步肯定了高浓度的石墨烯形成团聚体作为微生物生长的载体,而低浓度石墨烯因分散性较好,优先与微生物细胞接触,起到抑菌作用. 推测石墨烯对Acidithiobacillus ferrooxidans的伤害主要为物理损伤而非化学损伤,进入环境的石墨烯的分散性、稳定性是其毒性效应的主导因子.
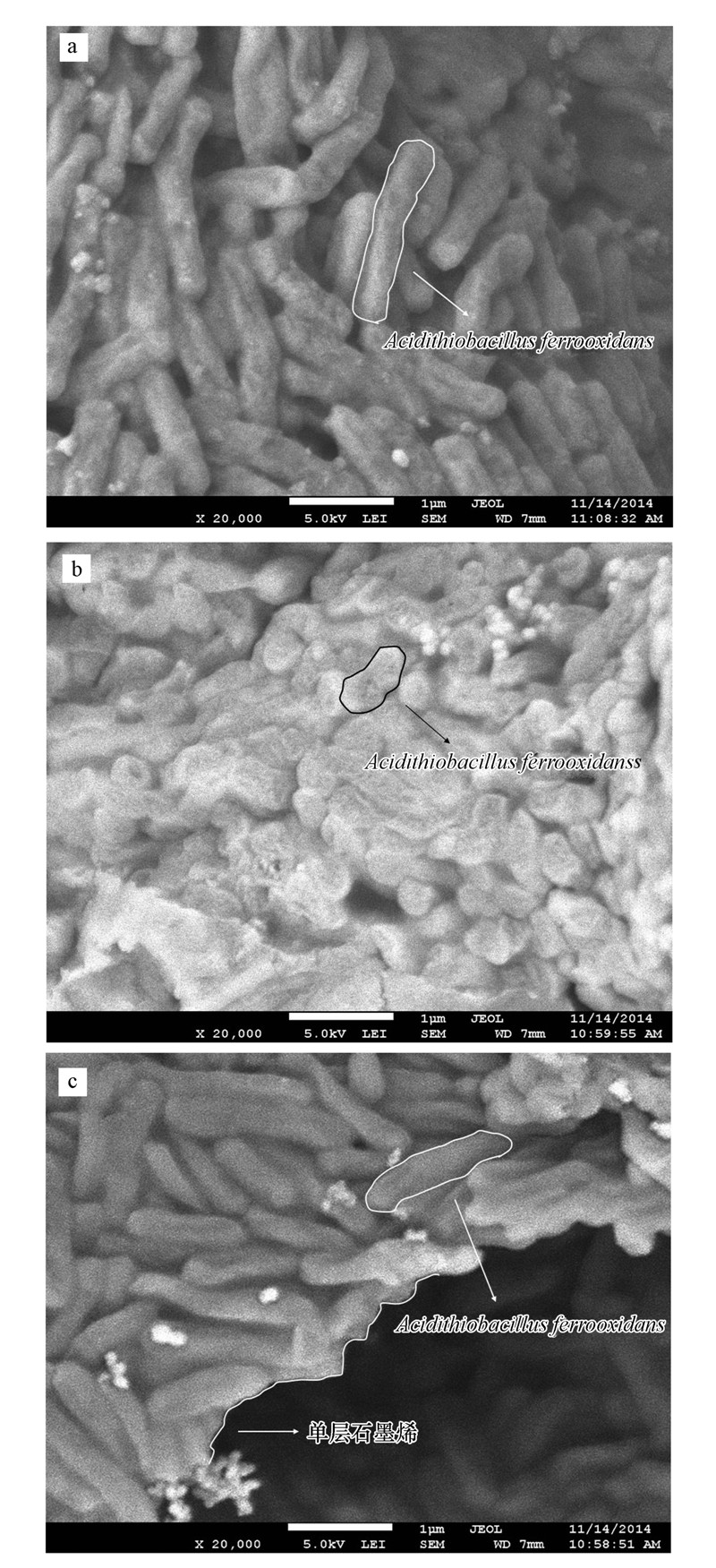 |
| 图 3 菌体接触石墨烯前后SEM图(×20 000)(a.游离菌;b. 游离菌+1 mg · L-1石墨烯;c. 游离菌+50 mg · L-1石墨烯) Fig. 3 The SEM of Acidithiobacillus ferrooxidans treated cells with different concentration of graphene(a.native cells; b.cells with 1 mg · L-1graphene; c.cells with 50 mg · L-1 graphene) |
为进一步证实不同浓度石墨烯对菌体的的毒性差异,对不同浓度石墨烯处理后的菌体进行荧光分析. 图 4分别是未添加石墨烯对照组、添加1 mg · L-1和50 mg · L-1石墨烯实验组的结果.Live/Dead荧光染料用于检测细胞内酯酶的活性和细胞膜的完整性,活细胞显绿色荧光,受损细胞显红色荧光(Boulos et al.,1999). 由图 4a可知,未添加石墨烯菌体在培养48 h后,菌体以显绿色荧光为主,说明绝大多数菌体为活菌. 由图 4c可见,50 mg · L-1石墨烯处理后菌体呈绿色荧光强度较对照组弱,说明高浓度的石墨烯对细菌有一定的抑制作用. 从图 4b可知,视野内总菌量相对较少,并且大部分为死菌,说明1 mg · L-1石墨烯抑制Acidithiobacillus ferrooxidans的繁殖并最终破坏细胞结构,使菌体大量死亡. 这一结果与前文所述可溶性蛋白含量相符. 纳米级石墨烯对能够切割微生物细胞膜并使其裂解从而导致细胞死亡(Pretti et al.,2014). 进一步证实低浓度石墨烯对Acidithiobacillus ferrooxidans的毒性更大.
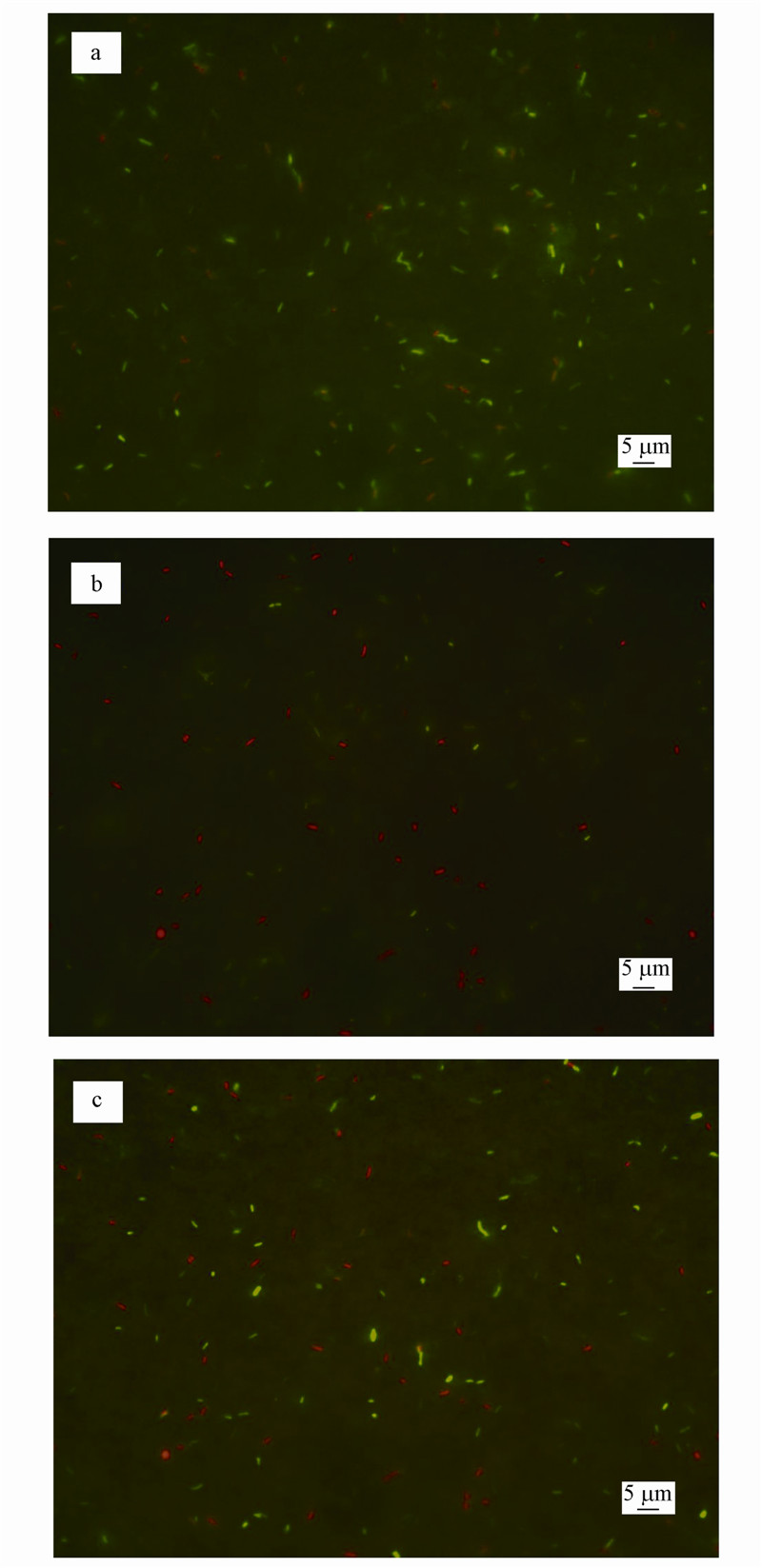 |
| 图 4 菌体接触石墨烯前后荧光显微镜图(1000×)(a.培养前;b.菌+1 mg · L-1石墨烯;c.菌+50 mg · L-1石墨烯) Fig. 4 The fluorescence microscope images of normal Acidithiobacillus. ferrooxidans and treated cells with different concentration of graphene(a.native Acidithiobacillus. ferrooxidans cells; b.cells with 1 mg · L-1 graphene; c.cells with 50 mg · L-1 graphene) |
1)通过研究不同浓度(1、10 、50 mg · L-1)石墨烯对Acidithiobacillus ferrooxidans的生长毒性可知,不同投加量的石墨烯对菌体的生长均有抑制作用,石墨烯投加量为1 mg · L-1时,抑制作用最大,其次分别是10 mg · L-1、50 mg · L-1体系. 不同浓度石墨烯对体系pH和ORP均存在不同程度的影响,低浓度(1 mg · L-1)下的石墨烯影响最为显著.
2)SEM结果证实,1 mg · L-1石墨烯对Acidithiobacillus ferrooxidans生长的毒性更大,50 mg · L-1石墨烯为Acidithiobacillus ferrooxidans生长提供载体,使得菌体能够附着在团聚的石墨烯上,因而生长状况良好. 荧光显微镜图显示,低浓度石墨烯处理后的死菌数量明显大于对照组和高浓度石墨烯处理,进一步说明低浓度石墨烯对Acidithiobacillus ferrooxidans细胞活性的抑制作用更为显著.
3)研究发现,石墨烯对Acidithiobacillus ferrooxidans的生长有抑制作用,并且浓度越低抑制作用越明显. 推测其毒性机制为:低浓度的石墨烯在水中碰撞机会少,不易团聚,石墨烯片层结构通过其尖锐的边角对细胞造成机械损伤,导致细胞膜无法进行传质,抑制其生理行为从而杀死细胞.
| [1] | Begum P, Ikhtiari R, Fugetsu B. 2011. Graphene phytotoxicity in the seedling stage of cabbage, tomato, red spinach, and lettuce[J]. Carbon, 49(12): 3907-3919 |
| [2] | Boulos L, Prévost M, Barbeau B, et al. 1999. LIVE/DEAD® BacLightTM: application of a new rapid staining method for direct enumeration of viable and total bacteria in drinking water[J]. Journal of Microbiological Methods, 37(1): 77-86 |
| [3] | Chen H Q, Müller M B, Gilmore K J, et al. 2008. Mechanically strong, electrically conductive, and biocompatible graphene paper[J]. Advanced Materials, 20(18): 3557-3561 |
| [4] | 甘莉, 刘贺琴, 王清萍, 等. 2014. 氧化亚铁硫杆菌生物浸出污泥中的重金属离子[J]. 中国环境科学, 34(10): 2617-2623 |
| [5] | Geranio L, Heuberger M, Nowack B. 2009. The behavior of silver nanotextiles during washing[J]. Environmental Science & Technology, 43(21): 8113-8118 |
| [6] | Hu W B, Peng C, Luo W J, et al. 2010. Graphene-based antibacterial paper[J]. ACS Nano, 4(7): 4317-4323 |
| [7] | Jia G, Wang H F, Yan L, et al. 2005. Cytotoxicity of carbon nanomaterials: single-wall nanotube, multi-wall nanotube, and fullerene[J]. Environmental Science & Technology, 39(5): 1378-1383 |
| [8] | Li J G, Sun H W, Zhang Y. 2007. Desorption of pyrene from freshly-amended and aged soils and its relationship to bioaccumulation in earthworms[J]. Soil and Sediment Contamination: An International Journal, 16(1): 79-87 |
| [9] | Liu S B, Zeng T Y, Hofmann M, et al. 2011. Antibacterial activity of graphite, graphite oxide, graphene oxide, and reduced graphene oxide: membrane and oxidative stress[J]. ACS Nano, 5(9): 6971-6980 |
| [10] | Long C P, Antoniewicz M R. 2014. Quantifying biomass composition by gas chromatography/mass spectrometry[J]. Analytical Chemistry, 86(19): 9423-9427 |
| [11] | Machida M, Mochimaru T, Tatsumoto H. 2006. Lead(II) adsorption onto the graphene layer of carbonaceous materials in aqueous solution[J]. Carbon, 44(13): 2681-2688 |
| [12] | Nemati M, Harrison S T L, Hansford G S, et al. 1998. Biological oxidation of ferrous sulphate by Thiobacillus ferrooxidans: a review on the kinetic aspects[J]. Biochemical Engineering Journal, 1(3): 171-190 |
| [13] | Novo M T M, Da Silva A C, Moreto R, et al. 2000. Thiobacillus ferrooxidans response to copper and other heavy metals: growth, protein synthesis and protein phosphorylation[J]. Antonie van Leeuwenhoek, 77(2): 187-195 |
| [14] | Nowack B, Bucheli T D. 2007. Occurrence, behavior and effects of nanoparticles in the environment[J]. Environmental Pollution, 150(1): 5-22 |
| [15] | Pretti C, Oliva M, Di Pietro R, et al. 2014. Ecotoxicity of pristine graphene to marine organisms[J]. Ecotoxicology and Environmental Safety, 101: 138-145 |
| [16] | Radic S, Geitner N K, Podila R, et al. 2013. Competitive binding of natural amphiphiles with graphene derivatives[J]. Scientific Reports, 3: 2273 |
| [17] | Ruiz O N, Fernando K A S, Wang B J, et al. 2011. Graphene oxide: a nonspecific enhancer of cellular growth[J]. ACS Nano, 5(10): 8100-8107 |
| [18] | van den Brink J. 2007. Graphene: from strength to strength[J]. Nature Nanotechnology, 2(4): 199-201 |
| [19] | Wen Y M, Cheng Y, Chen Z L, et al. 2013. Bioleaching of heavy metals from sewage sludge using indigenous iron-oxidizing microorganisms[J]. Journal of Soils and Sediments, 13(1): 166-175 |
| [20] | Zhang Y B, Ali S F, Dervishi E, et al. 2010. Cytotoxicity effects of graphene and single-wall carbon nanotubes in neural phaeochromocytoma-derived PC12 cells[J]. ACS Nano, 4(6): 3181-3186 |
| [21] | Zhao J, Wang Z Y, White J C, et al. 2014. Graphene in the aquatic environment: adsorption, dispersion, toxicity and transformation[J]. Environmental Science & Technology, 48(17): 9995-10009 |
| [22] | Zlatev R, Magnin J -P, Ozil P, et al. 2006. Bacterial sensors based on Acidithiobacillus ferrooxidans: Part I. Fe2+ and S2O32- determination[J]. Biosensors and Bioelectronics, 21(8): 1493-1500 |
 2015, Vol. 35
2015, Vol. 35


