长久以来,人们一直认为铵(NH4+)和甲烷(CH4)在厌氧条件下是稳定的,因此,厌氧氨氧化和厌氧甲烷氧化曾经被认为在生物化学上是不可行的并且在自然界是不存在的(Jetten,2008;Strous et al., 2004).但这一结论随着厌氧氨氧化(anaerobic ammonium oxidation,anammox)和反硝化厌氧甲烷氧化(nitrite-dependent anaerobic methane oxidation,n-damo)在自然界中的发现而被推翻(Kuypers et al., 2003;Mulder et al., 1995;Raghoebarsing et al., 2006;Thamdrup et al., 2002),并且它们都已经被证明是地球生物氮、碳循环的重要组成部分(Strous et al., 2004).厌氧氨氧化和反硝化厌氧甲烷氧化分别指在厌氧条件下铵和甲烷被亚硝酸盐(NO2-)氧化生成氮气(N2)和二氧化碳(CO2)的过程(Zhu et al., 2010).厌氧氨氧化可以使氮的化合物以氮气的形式返回大气,并且相比完成类似过程的反硝化其中间代谢过程不产生氧化亚氮(N2O)这一强势温室气体(Dalsgaard et al., 2003;Kartal et al., 2011;Kuypers et al., 2003).反硝化厌氧甲烷氧化可以在厌氧条件下将温室效应强烈的甲烷氧化成温室效应较弱的二氧化碳(Zhou et al., 2014).厌氧氨氧化细菌和反硝化厌氧甲烷氧化菌特殊的代谢途径及它们在全球变暖温室气体减排中的积极作用,引起了人们的广泛兴趣.
随着厌氧氨氧化细菌分子标记物和同位素示踪方法的开发,厌氧氨氧化细菌在海洋生态系统中的大量存在及厌氧氨氧化在海洋氮循环中发挥的重要作用陆续被证明(Dalsgaard et al., 2003;Kuypers et al., 2003,2005;Schmid et al., 2007).同时,厌氧氨氧化细菌在湖泊(Schubert et al., 2006;Yoshinaga et al., 2011;Zhu et al., 2013)、河流(Wang et al., 2012a)、人工湿地(Zhu et al., 2011a)、沼泽(Hu et al., 2011a)和地下水(Moore et al., 2011)等淡水生态系统中也有广泛的分布,且厌氧氨氧化过程对氮气生成的贡献率分布在0.5%~40%的范围内.虽然也有少量对厌氧氨氧化细菌在土壤表层和垂向分布规律的研究,但厌氧氨氧化细菌在岸边带土壤垂向分布规律仍不是十分清楚(Zhu et al., 2011b;Shen et al., 2013;2014a).
主导反硝化厌氧甲烷氧化发生的微生物全基因序列第一次被获取,并被命名为“Candidatus Methylomirabilis oxyfera”(Ettwig et al., 2010).同样针对反硝化厌氧甲烷氧化菌的分子标记物开发,证明反硝化厌氧甲烷氧化与硫酸盐型厌氧甲烷氧化(Sulphatedependent anaerobic methane oxidation,SAMO)主要分布在海洋中不同(Martens et al., 1974),其主要分布在淡水生态系统.反硝化厌氧甲烷氧化菌在生物反应器(Ettwig et al., 2009;Haroon et al., 2013;Raghoebarsing et al., 2006;Zhu et al., 2012b)、稻田(Hu et al., 2014;Wang et al., 2012b;Zhou et al., 2014)、河流(Shen et al., 2014b)、湖泊(Deutzmann et al., 2014;Hu et al., 2014;Kojima et al., 2012;朱群等,2013)、泥炭沼泽(Zhu et al., 2012a)和海洋沉积物(Chen et al., 2014)中均有分布,并且在生物碳循环和全球变暖中具有积极作用(Deutzmann et al., 2014;Ettwig et al., 2010;Hu et al., 2014).但反硝化厌氧甲烷氧化菌在土壤中的分布规律还不甚清楚,特别是对其在岸边带土壤中的垂向分布规律更是罕有研究.
基于此,本文通过采集白洋淀典型的岸边带垂向深层土壤样品,综合应用分子生物学方法,研究厌氧氨氧化细菌和反硝化厌氧甲烷氧化细菌的存在和分布规律,并结合土壤理化性质探讨影响两者分布的环境因素.
2 材料和方法(Materials and methods) 2.1 样品采集白洋淀是华北平原最大的淡水湖泊湿地,位于华北平原中部,地理位置为北纬38°43′~39°02′,东经115°38′~116°07′,总面积366 km2.白洋淀是渤海湾西面低洼地经海陆变迁形成的特殊生态系统,淀区地形复杂,淀内纵横沟壕3700余条交织错落,将全淀分割成143个大小不等的淀泊.其岸边带发育相对较好,在全淀范围内,以芦苇植被为景观特征的岸边带湿地系统约占36%,主要由芦苇群落、苇地间小沟及浅水区组成,是研究岸边带的理想地点(王衫允等,2012).在分析了大量背景资料和野外调查的基础上,在白洋淀湖区选择了坐标为北纬38°54′20″、东经115°55′30″的岸边带作为采样点.采样点如图 1所示,在距离岸边带表层湖水/岸边土壤交界面水平距离为1、3、6和12 m的位置,每20 cm 分为一层分别采集了4根100 cm深的垂向土壤样品柱,一共20个样品.分别将距离岸边带表层湖水/岸边土壤交界面水平距离为1、3、6和12 m的4根样品柱命名为1#、2#、3#和4#.该采样点的水位为地下50 cm左右.采集土壤样品后立即将其混匀置于无菌聚乙烯自封袋中排尽空气再密封,放置于黑暗冷藏箱中4 ℃保存至运回实验室.然后将样品分为两份,一部分样品立即进行理化性质测定,另外一部分样品用冷干机冷冻干燥后保存于-80 ℃冰箱中用于DNA提取和后续分子生物学实验.
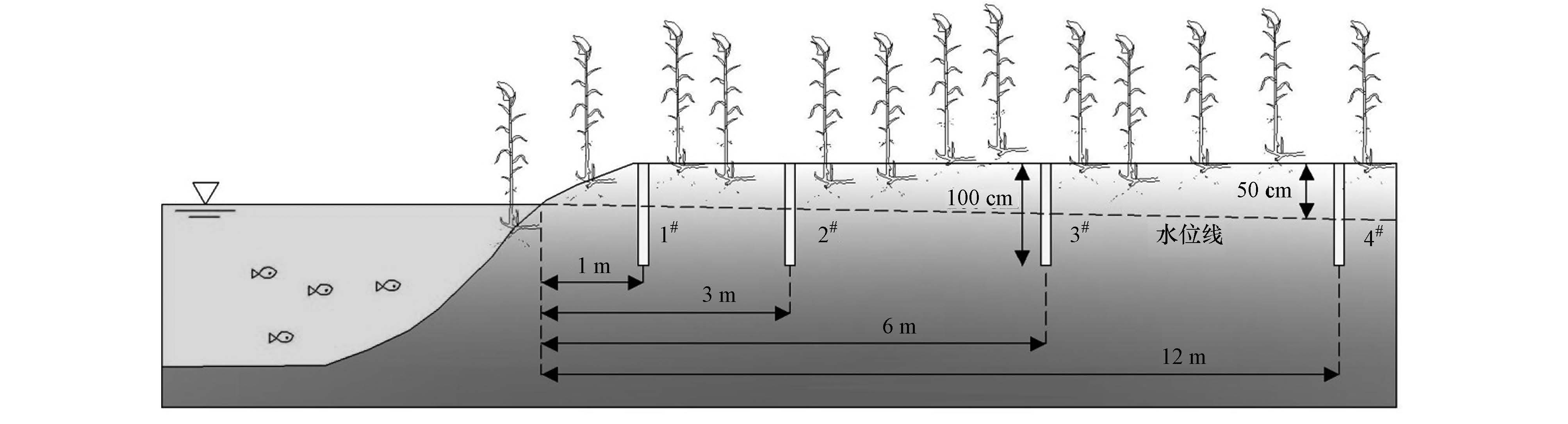 |
| 图1 白洋淀岸边带采样点布设 Fig.1 Geographical distribution of sampling sites in the riparian zone of Baiyangdian Lake |
对土壤样品NH4+-N、NO3--N和NO2--N的测定参考《土壤农化分析》中的方法,经2 mol · L-1 KCl溶液浸提、0.45 μm微孔滤膜过滤后,用连续流动分析仪(SAN plus,Skalar Analytical B.V.,Breda,the Netherlands)测定.土壤总氮(TN)、总硫(TS)和总碳(TC)的测定也参考标准方法(鲍士旦,2000).向土壤中加入超纯水使土壤/水的质量比为1 ∶ 2.5后测定土壤的pH值.测定LOI550(550 ℃的烧失量)代表土壤总有机质(张文河等,2007).样品的所有理化性质指标都进行3次重复测定.
2.3 DNA提取和PCR扩增使用FastDNA SPIN Kit for Soil土壤 DNA提取试剂盒(QBIOgene Inc.,Carlsbad,CA,USA),按照说明书的方法,称取0.33 g冷冻干燥的土壤样品提取土壤总DNA,所得DNA在冰箱-20 ℃保存待用.
在厌氧氨氧化细菌研究中,采用了新设计的针对羟铵合成酶hzsB功能基因的引物HSBeta396F/HSBeta742R进行扩增的方法(Harhangi et al., 2012;Kartal et al., 2011;Wang et al., 2012b).在反硝化厌氧甲烷氧化菌研究中,利用针对M.oxyfera-like细菌的16S rRNA基因的特异性引物对其进行巢式PCR 扩增,第一步使用引物202F/630R(Ettwig et al., 2009;Juretschko et al., 1998),第二步使用引物p1F/p2R(Ettwig et al., 2009).PCR反应体系为50 μL,其中,10×buffer 5 μL,2.5 mol · L-1 dNTP 4 μL,10 mmol · L-1正反向引物各1 μL,BSA 0.25 μL,Taq酶0.5 μL,DNA模板2 μL,用无核酸酶纯水补足至50 μL.引物序列及PCR扩增程序见表 1.
| 表1 本研究中用到的引物及相应PCR程序 Table 1 Primers used in this study and correspondent thermal profiles |
PCR扩增产物用Promega Agarose Gel DNA纯化试剂盒(Promega,Madison,WI)进行切胶纯化回收,将回收的PCR扩增产物与pGEM-Teasy载体(Promega,Madison,WI)连接,转入JM109感受态细胞(Takara,大连),涂布于Luria-Bertani(LB)培养基上培养,最后进行蓝白斑筛选.用载体通用引物T7、SP6对随机选取的2个白色克隆进行PCR扩增,以鉴定阳性克隆,将阳性克隆进行测序(擎科新业生物技术有限公司,北京).得到的序列在GenBank数据库中进行BLAST比对,并选取相关参比序列,使用Clustal_X程序进行序列对齐,应用MEGA4.1软件以邻接法(Neighbor-Joining)构建系统发育树.
2.5 定量PCR分析采用实时荧光定量PCR方法对白洋淀湖泊岸边带土壤中厌氧氨氧化细菌和M. oxyfera-like细菌进行定量分析,使用ABI 7300 Real-Time PCR System扩增仪(Applied Biosystems,CA,USA)进行定量扩增,定量方法为SYBR Green法.选择HSBeta396F /HSBeta742R引物对厌氧氨氧化细菌的hzsB基因进行特异性定量扩增(Kartal et al., 2011;Wang et al., 2012b).由于目前还没有成熟的针对反硝化厌氧甲烷氧化菌功能基因的定量引物,故本研究中使用M. oxyfera-like 细菌的16S rRNA基因进行定量分析,并使用两对不同的引物(p1F/R、p2F/R)对土壤样品进行定量PCR分析以保证丰度测定的准确性(Ettwig et al., 2009;Zhou et al., 2014),引物序列和扩增程序见表 1.定量PCR扩增体系为20 μL,其中,SYBR Premix Ex Taq酶(Takara,大连)10 μL,ROX 50(Takara,大连)0.4 μL,浓度为10 mmol · L-1的正反向引物(生工生物工程(上海)股份有限公司,上海)各1 μL,稀释10倍的土壤总DNA模板2 μL,用无核酸酶纯水补足至20 μL.使用GeneJet Plasmid Miniprep Kit 试剂盒(Fermentas MBI,Lithuania)对厌氧氨氧化细菌hzsB功能基因和M. oxyfera-like细菌16S rRNA基因的阳性克隆的质粒进行纯化,纯化产物作为定量标准样品的母液.为了定量计算样品DNA的目的基因的拷贝数,标准样品的母液浓度使用NanoDrop 2000紫外可见分光光度计(Thermo Fisher Scientific,Wilmington,DE,USA)测量.然后用10倍梯度稀释法稀释得到标准样品.实验设置阴性对照组,同时将得到的7个梯度的标准样品同样进行定量扩增,得到标准曲线.所有样品做3次重复.将定量结果为阳性的样品的总DNA分别稀释10、20、60、100、500倍,把能检测到的最大稀释倍数的样品的丰度数据作为定量检测下限.定量PCR结果用7300 SDS System配套软件进行分析计算,得出厌氧氨氧化细菌和M. oxyfera-like细菌丰度值.要求标准样品扩增效率为90%~110%,标准曲线可决系数大于0.98,土壤DNA样品扩增溶解曲线为单一峰.
2.6 数据统计分析使用PASW Statistics 18.0 软件(Predictive Analytics Software Statistics),因素间的相关性选择Spearmen非参数相关性分析方法进行分析.本文中显著性水平为α=0.05.作图使用Origin 8.0软件.
3 结果(Results) 3.1 白洋淀岸边带土壤理化性质白洋淀湖泊岸边带深层土壤样品的基本理化性质如表 2所示,4根深层土壤样品柱的同种理化性质变化规律类似.4根土壤样品柱NH4+-N、NO3--N和NO2--N含量分别为1.09~3.78 mg · kg-1、0.78~5.67 mg · kg-1和0.02~0.22 mg · kg-1.除1#样品柱外,剩余样品柱的表层NH4+-N含量都为最高.土壤NO3--N含量变化无明显规律,但第一、二层样品基本高于更深层的样品.样品的NO2--N含量均较低,除1#样品柱外,剩余样品柱NO2--N含量均有随着深度的增加而降低的趋势.
4根土壤样品柱的总氮(TN)、总碳(TC)和总硫(TS)分别为0.59~1.44 mg · kg-1、15.66~23.72 mg · kg-1和0.17~0.28 mg · kg-1.TN在每根样品柱的表层最高,并且随着样品深度的增加逐渐减小.TC的变化规律与TN类似,但其变化趋势较TN的小.TS在每根样品柱的表层最高,但无明显变化规律.
4根土壤样品柱的总有机质(LOI550)、含水率和pH分别为3.62%~6.61%、26.68%~42.21%和5.90~7.38.不同样品柱内LOI550无明显的变化规律,1#样品柱的LOI550稍高于剩于样品柱.含水率在每根样品柱的表层最高,并且随着样品深度的增加有逐渐减小的趋势.
| 表2 白洋淀湖泊岸边带深层土壤样品理化性质 Table 2 Chemical characteristics of the deep soil profile in the riparian zone of Baiyangdian Lake |
为了证明白洋淀岸边带深层土壤样品中厌氧氨氧化细菌的存在,运用分子生物学方法,对土壤样品总DNA进行了针对厌氧氨氧化细菌功能基因的特异性扩增.为了增强扩增的特异性,选择了最新设计针对hzsB基因的引物(Wang et al., 2012b).每个样品柱的表面两层样品(0~20 cm和20~40 cm)PCR呈阴性,剩余深层样品均获得了阳性结果.每个阳性样品获得2条序列,共得到24条序列.将这24条序列在GenBank数据库中进行BLAST比对,结果表明其均为厌氧氨氧化细菌的hzsB基因序列.将这些hzsB基因序列与已经发表的来自生物反应器、沟渠土壤、湿地土壤、稻田土壤(Wang et al., 2012b)和珠江河口沉积物(Wang et al., 2012a)的hzsB基因序列一起进行系统发育分析(图 2).从系统发育树中可以看出,本文中获得的24条基因序列均属于厌氧氨氧化细菌hzsB基因.这些结果证明在白洋淀岸边带垂向土壤表层土壤(0~20 cm和20~40 cm)未检测到厌氧氨氧化细菌,地下水位(50 cm)附近及以下深层土壤均存在厌氧氨氧化细菌.
为了证明白洋淀岸边带深层土壤样品中M. oxyfera-like细菌的存在,运用分子生物学方法,对土壤样品总DNA进行了针对M. oxyfera-like细菌16S rRNA基因的特异性扩增(Ettwig et al., 2009;Juretschko et al., 1998).所有样品均呈阳性,每个样品获得2条序列,共得到40条序列.将这40条序列在GenBank数据库中进行BLAST比对,结果表明其均为M. oxyfera-like细菌的16S rRNA基因序列.将这些16S rRNA基因序列与已经发表的来自嘉兴稻田(Wang et al., 2012b)、生物反应器(Ettwig et al.,2009)和琵琶湖(Kojima et al., 2012)的M. oxyfera-like细菌16S rRNA基因序列一起进行系统发育分析(图 3).从系统发育树中也可以看出,实验获得的40条序列均属于M. oxyfera-like细菌的16S rRNA基因序列.这些结果证明在白洋淀岸边带的20个土壤样品中均存在M. oxyfera-like细菌.
 |
| 图2 白洋淀岸边带土壤hzsB基因系统发育树(本文中的参比序列引自GenBank数据库,序列名称后的字母加数字为提交序号,分支节点上的数字表示每1000次bootstrap分析所支持的次数,小于50不显示;发育树左下方标尺表示2%序列差异的分支长度;括号内的数字(1和2)表示从同一个样品中获得的不同克隆子序列的编号) Fig.2 Phylogenetic tree of hzsB gene sequences from sampling sites in the riparian zone of Baiyangdian Lake(The reference sequences were gained from GenBank; letters and numbers in brackets represent the sequences accession number; the numbers next to the nodes represent the bootstrap values of 1000 replications; values less than 50 were not listed; the scale bar at the bottom-left of phylogenetic tree represents 2 nucleotide substitutions per 100 nucleotides) |
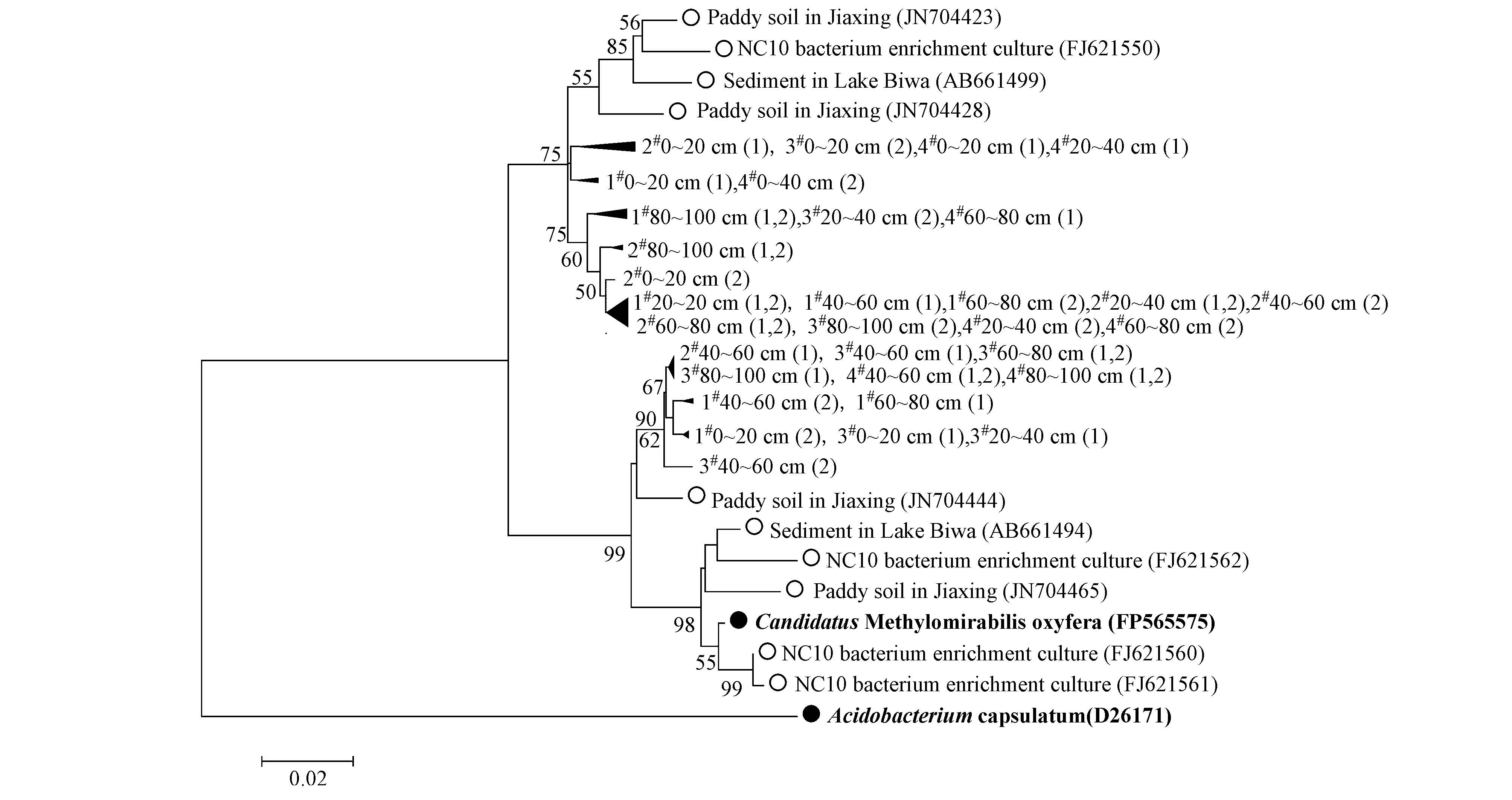 |
| 图3 白洋淀岸边带土壤M. oxyfera-like细菌16S rRNA基因系统发育树(本文中的参比序列引自GenBank数据库,序列名称后的字母加数字为提交序号,分支节点上的数字表示每1000次bootstrap分析所支持的次数,小于50不显示;发育树左下方标尺表示2%序列差异的分支长度) Fig.3 Phylogenetic tree of 16S rRNA gene sequences of M. oxyfera-like bacteria from sampling sites in the riparian zone of Baiyangdian Lake(The reference sequences in this study were gained from GenBank; letters and numbers in brackets represent the sequences accession number; the numbers next to the nodes represent the bootstrap values of 1000 replications; values less than 50 were not listed; the scale bar at the bottom-left of phylogenetic tree represents 2 nucleotide substitutions per 100 nucleotides) |
采用靶向hzsB基因的引物对白洋淀岸边带土壤样品厌氧氨氧化细菌进行实时荧光定量PCR分析,定量检测下限为8.88 copies · μL-1(2.28×103 copies · g-1,以干土计,下同).白洋淀岸边带垂向土壤厌氧氨氧化细菌丰度为0~6.10×107 copies · g-1.从图 4中可以明显看出,4根样品柱水位线(50 cm)以上的0~20 cm和20~40 cm部分均未检测到厌氧氨氧化细菌,而水位线附近及以下的深层样品中,都检测到了厌氧氨氧化细菌.说明在白洋淀湖泊岸边带垂向土壤中,表层未检测到厌氧氨氧化细菌,厌氧氨氧化细菌主要分布在水位线附近及以下的深层土壤中.并且能够检测到厌氧氨氧化细菌部分的丰度值均处于同一数量级,丰度差异较小,不存在厌氧氨氧化细菌丰度随着深度增加而递增的规律.1#、2#、3#和4#四根土壤样品柱的厌氧氨氧化细菌丰度最大值分别为4.94×107、3.59×107、2.73×107和6.10×107 copies · g-1.除3#样品柱厌氧氨氧化细菌丰度最大值出现在40~60 cm处,剩余3根样品柱厌氧氨氧化细菌丰度最大值出现在60~80 cm处.
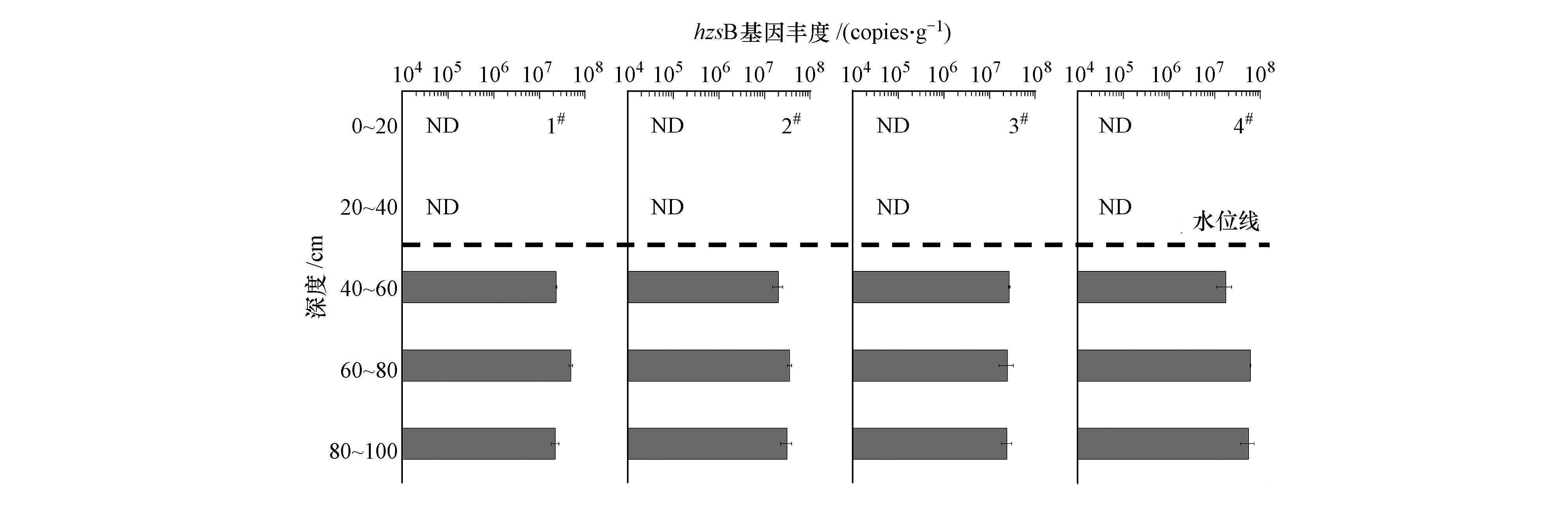 |
| 图4 白洋淀岸边带厌氧氨氧化细菌hzsB基因丰度(ND表示未检测到) Fig.4 Anammox bacterial abundance targeting on hzsB gene from sampling sites in the riparian zone of Baiyangdian Lake(ND,not detected) |
由于目前还没有成熟的针对反硝化厌氧甲烷氧化菌功能基因的定量引物,故采用M. oxyfera-like细菌16S rRNA基因的两对引物对白洋淀岸边带土壤样品进行实时荧光定量PCR分析,p1F/R和p2F/R定量检测下限分别为10.69和6.21 copies · μL-1(3.15×103和1.83×103 copies · g-1). 由图 5可看出,两对引物的定量结果差别较小,因而取两者的平均值进行分析.白洋淀岸边带土壤M. oxyfera-like细菌丰度为9.74×103~1.49×106 copies · g-1.4根样品柱中,除了1#样品柱M. oxyfera-like细菌丰度最大值出现在60~80 cm之外,剩余3根样品柱的M. oxyfera-like细菌丰度都随着深度的增加而递增.4根样品柱的表面两层样品虽然也检测到了M. oxyfera-like细菌,但丰度都小于1.00×105 copies · g-1,相对于深层样品1.05×105~1.49×106 copies · g-1的丰度值,明显处于较低水平.每根样品柱的M. oxyfera-like细菌丰度的热区也是地下水位附近及以下的深层区域.
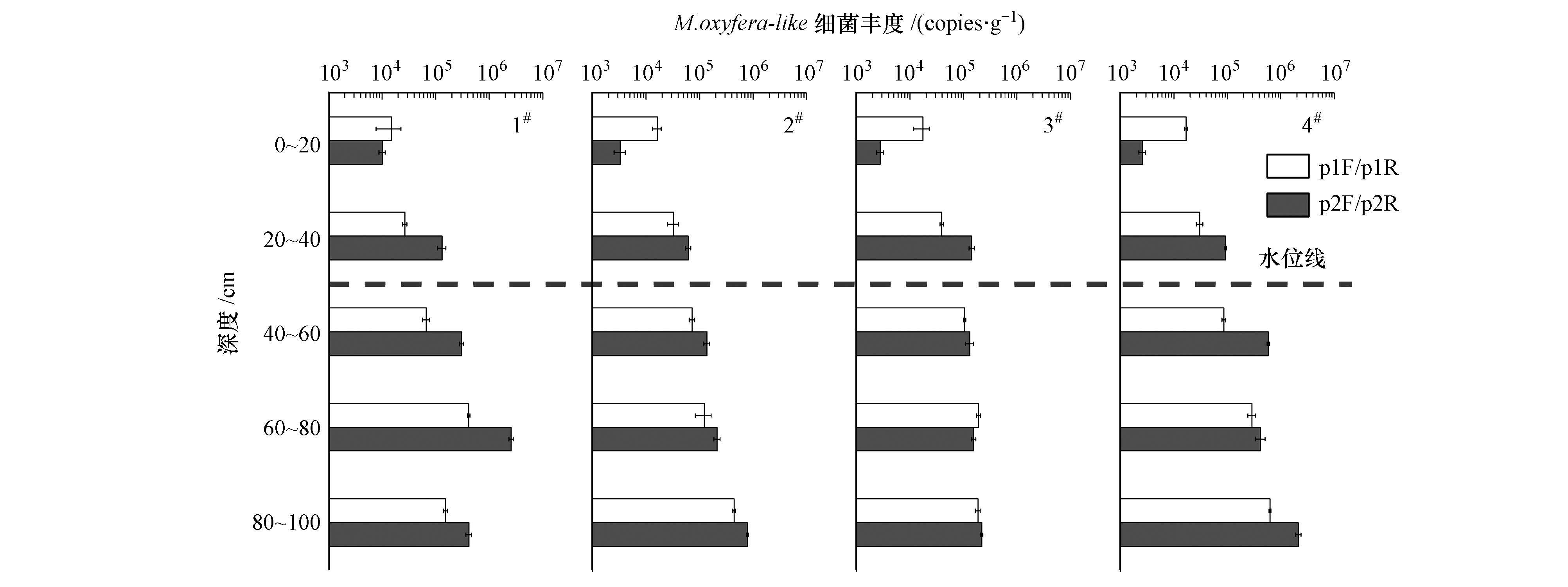 |
| 图5 白洋淀湖泊岸边带M. oxyfera-like细菌16S rRNA基因丰度 Fig.5 M. oxyfera-like bacterial abundance targeting on 16S rRNA gene from sampling sites in the riparian zone of Baiyangdian Lake |
将白洋淀岸边带厌氧氨氧化细菌hzsB基因丰度与环境理化因子进行Spearman相关性分析(表 3),结果显示,hzsB基因丰度和厌氧氨氧化反应底物NH4+(r=-0.525*,p=0.017)、NO3-(r=-0.860* *,p=0.000)成显著负相关,与含水率(r=-0.825* *,p=0.000)、TN(r=-0.836* *,p=0.000)、TC(r=-0.698* *,p=0.001)也成显著负相关.
| 表3 白洋淀岸边带厌氧氨氧化细菌、反硝化厌氧甲烷氧化细菌丰度与物理化学环境因素的相关性分析(n=20) Table 3 Correlation analysis between abundance of anammox,M. oxyfera-like bacteria and environmental variables in the riparian zone of Baiyangdian Lake(n=20) |
将白洋淀岸边带M. oxyfera-like细菌16S rRNA基因丰度与环境理化因子进行Spearman相关性分析(表 3),结果显示,16S rRNA基因丰度和反应底物NO3-(r=-0.793* *,p=0.000)成显著负相关,与NH4+(r=-0.480*,p=0.032)、含水率(r=-0.865* *,p=0.000)、TN(r=-0.880* *,p=0.000)、TC(r=-0.731* *,p=0.000)、TS(r=-0.565* *,p=0.000)也成显著负相关,和样品深度(r=0.895* *,p=0.000)成显著正相关.
4 讨论(Discussion)本文综合应用分子生物学方法,使用针对厌氧氨氧化细菌和M. oxyfera-like细菌的特异性引物,探讨了厌氧氨氧化细菌和M. oxyfera-like细菌在白洋淀湖泊岸边带深层土壤样品中的存在和分布规律.
在白洋淀湖泊岸边带4根土壤样品柱表面两层土壤(0~40 cm)中均未检测到厌氧氨氧化细菌的存在,这和之前对白洋淀岸边带表层土壤(0~60 cm)的研究结果类似(Zhu et al., 2013).但是,不同类型的表层沉积物(Hu et al., 2011b;Wang et al., 2012a;Yoshinaga et al., 2011)和稻田表层土壤(Shen et al., 2014a;Wang et al., 2014;Wang et al., 2012b;Zhu et al., 2011b)普遍能检测到厌氧氨氧化细菌.厌氧氨氧化细菌在海洋生态系统中是广泛分布的(Schmid et al., 2007),但在陆地生态系统中不是无处不在的,而只在某些类型土壤或者深度中存在(Humbert et al., 2010).厌氧氨氧化细菌在陆地生态系统需要特定的生态位可能是造成未在白洋淀湖泊岸边带表面两层土壤中检测到厌氧氨氧化细菌的原因.从4根样品柱整体来看,未从样品柱表面两层土壤中检测到厌氧氨氧化细菌,而在地下水位(50 cm)附近及以下区域检测到了丰度为1.75×107~6.10×107 copies · g-1的厌氧氨氧化细菌,但厌氧氨氧化细菌丰度与样品深度之间无明显联系(r=0.384,p=0.217,n=12).而在长期施肥的嘉兴稻田,表层土壤(0~40 cm)能检测到厌氧氨氧化细菌,厌氧氨氧化细菌丰度在40~50 cm达到最大值(1.1×107 copies · g-1,以干土计)后逐渐降低(Zhu et al., 2011b);杭州稻田表层土壤(0~10 cm)检测到厌氧氨氧化细菌的最大丰度((2.0±0.14)×106 copies · g-1)后,厌氧氨氧化细菌丰度值随着样品深度的增加有降低的趋势(Shen et al., 2014a).这些对厌氧氨氧化细菌在土壤中垂向分布规律的研究得到了不同的结论,说明厌氧氨氧化细菌在不同类型土壤中的分布规律不同,其分布规律比较复杂还有待深入研究.
目前已知反硝化厌氧甲烷氧化可以由细菌或者古菌驱动发生(Raghoebarsing et al., 2006;Ettwig et al., 2010),但由于方法所限本文仅研究了反硝化厌氧甲烷氧化细菌.此外,由于研究反硝化厌氧甲烷氧化细菌的引物是根据“Candidatus Methylomirabilis oxyfera”设计的并且本文并未从细菌代谢角度直接证明样品中存在反硝化联合厌氧甲烷氧化(Ettwig et al., 2009,2010),故全文用M. oxyfera-like细菌表征反硝化厌氧甲烷氧化细菌.M. oxyfera-like细菌在白洋淀湖泊岸边带表面两层土壤(0~40 cm)中有少量的分布(9.74×103~9.04×104 copies · g-1),这和嘉兴稻田相同深度土壤中的分布规律类似((7.5±0.4)×104~(1.0±0.1)×105 copies · g-1,以干土计)(Wang et al., 2012b),但丰度值比日本琵琶湖(2.0×104~1.0×106 copies · mL-1,以sediment计,1~14 cm)(Kojima et al., 2012)、钱塘江((1.32±0.16)×106~(1.03±0.12)×107 copies · g-1,以干土计,0~3 cm)(Shen et al., 2014b)等表层沉积物低.从垂向样品柱整体来看,白洋淀湖泊岸边带深层土壤样品(0~100 cm)M. oxyfera-like细菌丰度随着深度的增加有明显增加的趋势(r=0.895* *,p=0.000,n=20),这与杭州某稻田(0~100 cm)的研究结果类似(Shen et al., 2014a).而对杭州该稻田(0~100 cm)和湿地(0~100 cm)的另一次研究却出现了M. oxyfera-like细菌丰度先增大后减小的规律(Hu et al., 2014);对嘉兴稻田M. oxyfera-like细菌的研究显示,其表层(0~40 cm)丰度较高深层(40~100 cm)丰度较低(Wang et al., 2012b).这些对M. oxyfera-like细菌在土壤中垂向分布规律的研究得到了不同的结论,说明M. oxyfera-like细菌在不同土壤、不同时间的分布规律不完全相同,其分布规律比较复杂也有待深入研究.
比较厌氧氨氧化细菌和M. oxyfera-like细菌在白洋淀湖泊岸边带土壤中的分布规律,可以发现虽然两者的分布热区均位于地下水位线(50 cm)附近及以下的深层土壤(40~100 cm)中,但两者的分布规律还是有明显的区别:厌氧氨氧化细菌在表面两层土壤(0~40 cm)中未检测到,但M. oxyfera-like细菌在该区域有少量分布;M. oxyfera-like细菌的丰度随着深度的增加有明显的增加趋势(r=0.895* *,p=0.000,n=20),而厌氧氨氧化细菌在其存在的区域丰度值处于同一数量级并没有随着深度的增加而增加的规律(r=0.384,p=0.217,n=12).
虽然白洋淀岸边带表面两层土壤(0~40 cm)中存在厌氧氨氧化反应的底物NH4+和NOx-,但在该区域并未检测到厌氧氨氧化细菌的存在.这可能是由在陆地生态系统中厌氧氨氧化细菌需要好氧/缺氧界面、无机氮底物等特定的生态位这一原因导致的(Humbert et al., 2010).但至今这种决定厌氧氨氧化细菌在土壤中存在和活性的环境因子还未知.而较深的土壤样品(40~100 cm)处于地表水/地下水交错带区域,该区域具有良好的微生物过程基础和环境条件(Zhu et al., 2010;2011a),有利于厌氧氨氧化细菌的生长和规模性厌氧氨氧化反应的发生,造成白洋淀湖泊岸边带厌氧氨氧化细菌分布的热区位于该区域.同样生存在厌氧环境中的M. oxyfera-like细菌在白洋淀岸边带0~40 cm的表面两层土壤中却有少量存在,这一结果和以往对河流、湖泊岸边带表层土壤的研究类似(Zhu et al., 2015).但另外一方面,这种现象也可能是由于缺少对M. oxyfera-like细菌功能基因的特异引物而使用16S rRNA基因的定量PCR结果高估了其在0~40 cm的表面两层土壤中的丰度造成的(Wang et al., 2012b).
在白洋淀岸边带地下水位附近及以下的深层土壤(40~100 cm)中,厌氧氨氧化细菌和M. oxyfera-like细菌共存.厌氧氨氧化细菌和M. oxyfera-like细菌在该区域的丰度分别为1.75×107~ 6.10×107 copies · g-1和1.05×105~1.49×106 copies · g-1. 运用同位素示踪法对两者反应活性的研究也显示,在稻田深层土壤中厌氧氨氧化速率要明显高于反硝化厌氧甲烷氧化速率(Shen et al., 2014a).从化学反应热力学角度分析,比较厌氧氨氧化反应公式(1)(Kartal et al., 2012)和反硝化厌氧甲烷氧化公式(2)(Raghoebarsing et al., 2006)可以发现,在相同浓度底物NO2-条件下,厌氧氨氧化反应更容易发生,这也说明了在深层土壤两者共同发生的区域,厌氧氨氧化反应可能占主导.
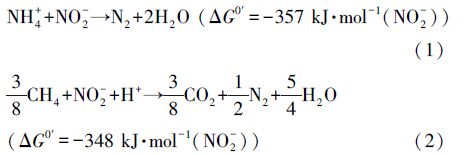
厌氧氨氧化和反硝化厌氧甲烷氧化不仅可以在同一环境中共同发生,而且在反应器中还观察到了厌氧氨氧化细菌和反硝化厌氧甲烷氧化古菌的协同作用(Haroon et al., 2013).Shi等(2013)还提出了在MBfR反应器中厌氧氨氧化细菌、反硝化厌氧甲烷氧化古菌和反硝化厌氧甲烷氧化细菌协同作用的模型.这表明在适宜的环境和底物条件下,厌氧氨氧化和反硝化厌氧甲烷氧化不仅在环境中可以共存、同时发生,还可以通过底物供给和传递协同发生.
厌氧氨氧化和反硝化厌氧甲烷氧化在多种生态系统有广泛的分布,在地球氮、碳循环中也发挥着重要作用,与反应相关的氧化亚氮、甲烷等强势温室气体也与全球变暖密切相关(Zhu et al., 2010),对它们的研究尤其是其在土壤中的存在和发生具有重要意义.但由于缺少相关的特异性引物,以及对它们分布规律、发生机理和关键调控因子研究的不足,还有很多问题有待深入探究.
| [1] | 鲍士旦.2000.土壤农化分析(第3版)[M].北京:中国农业出版社 |
| [2] | Chen J,Zhou Z C,Gu J D.2014.Occurrence and diversity of nitrite-dependent anaerobic methane oxidation bacteria in the sediments of the South China Sea revealed by amplification of both 16S rRNA and pmoA genes[J].Applied Microbiology and Biotechnology,98(12):5685-5696 |
| [3] | Dalsgaard T,Canfield D E,Petersen J,et al.2003.N2 production by the anammox reaction in the anoxic water column of Golfo Dulce,Costa Rica[J].Nature,422(6932):606-608 |
| [4] | Deutzmann J S,Stief P,Brandes J,et al.2014.Anaerobic methane oxidation coupled to denitrification is the dominant methane sink in a deep lake[J].Proceedings of the National Academy of Sciences of the United States of America,111(51):18273-18278 |
| [5] | Ettwig K F,van Alen T,van de Pas-Schoonen K T,et al.2009.Enrichment and molecular detection of denitrifying methanotrophic bacteria of the NC10 phylum[J].Applied and Environmental Microbiology,75(11):3656-3662 |
| [6] | Ettwig K F,Butler M K,Le Paslier D,et al.2010.Nitrite-driven anaerobic methane oxidation by oxygenic bacteria[J].Nature,464(7288):543-548 |
| [7] | Harhangi H R,Le Roy M,van Alen T,et al.2012.Hydrazine synthase,a unique phylomarker with which to study the presence and biodiversity of anammox bacteria[J].Applied and Environmental Microbiology,78(3):752-758 |
| [8] | Haroon M F,Hu S H,Shi Y,et al.2013.Anaerobic oxidation of methane coupled to nitrate reduction in a novel archaeal lineage[J].Nature,500(7464):567-570 |
| [9] | Hu B L,Rush D,van der Biezen E,et al.2011a.New anaerobic,ammonium-oxidizing community enriched from peat soil[J].Applied and Environmental Microbiology,77(3):966-971 |
| [10] | Hu B L,Shen L D,Xu X Y,et al.2011b.Anaerobic ammonium oxidation (anammox) in different natural ecosystems[J].Biochemical Society Transactions,39(6):1811-1816 |
| [11] | Hu B L,Shen L D,Lian X,et al.2014.Evidence for nitrite-dependent anaerobic methane oxidation as a previously overlooked microbial methane sink in wetlands[J].Proceedings of the National Academy of Sciences of the United States of America,111(12):4495-4500 |
| [12] | Humbert S,Tarnawski S,Fromin N,et al.2010.Molecular detection of anammox bacteria in terrestrial ecosystems:distribution and diversity[J].The ISME Journal,4(3):450-454 |
| [13] | Jetten M S M.2008.The microbial nitrogen cycle[J].Environmental Microbiology,10(11):2903-2909 |
| [14] | Juretschko S,Timmermann G,Schmid M,et al.1998.Combined molecular and conventional analyses of nitrifying bacterium diversity in activated sludge:Nitrosococcus mobilis and Nitrospira-like bacteria as dominant populations[J].Applied and Environmental Microbiology,64(8):3042-3051 |
| [15] | Kartal B,Maalcke W J,de Almeida N M,et al.2011.Molecular mechanism of anaerobic ammonium oxidation[J].Nature,479(7371):127-130 |
| [16] | Kartal B,van Niftrik L,Keltjens J T,et al.2012.Anammox-growth physiology,cell biology,and metabolism[J].Advances in Microbial Physiology,60:211-262 |
| [17] | Kojima H,Tsutsumi M,Ishikawa K,et al.2012.Distribution of putative denitrifying methane oxidizing bacteria in sediment of a freshwater lake,Lake Biwa[J].Systematic and Applied Microbiology,35(4):233-238 |
| [18] | Kuypers M M M,Sliekers A O,Lavik G,et al.2003.Anaerobic ammonium oxidation by anammox bacteria in the Black Sea[J].Nature,422(6932):608-611 |
| [19] | Kuypers M M M,Lavik G,Woebken D,et al.2005.Massive nitrogen loss from the Benguela upwelling system through anaerobic ammonium oxidation[J].Proceedings of the National Academy of Sciences of the United States of America,102(18):6478-6483 |
| [20] | Martens C S,Berner R A.1974.Methane production in the interstitial waters of sulfate-depleted marine sediments[J].Science,185(4157):1167-1169 |
| [21] | Moore T A,Xing Y P,Lazenby B,et al.2011.Prevalence of anaerobic ammonium-oxidizing bacteria in contaminated groundwater[J].Environmental Science & Technology,45(17):7217-7225 |
| [22] | Mulder A,van de Graaf A,Robertson L A,et al.1995.Anaerobic ammonium oxidation discovered in a denitrifying fluidized bed reactor[J].FEMS Microbiology Ecology,16(3):177-184 |
| [23] | Raghoebarsing A A,Pol A,van de Pas-Schoonen K T,et al.2006.A microbial consortium couples anaerobic methane oxidation to denitrification[J].Nature,440(7086):918-921 |
| [24] | Schmid M C,Risgaard-Petersen N,van de Vossenberg J,et al.2007.Anaerobic ammonium-oxidizing bacteria in marine environments:widespread occurrence but low diversity[J].Environmental Microbiology,9(6):1476-1484 |
| [25] | Schubert C J,Durisch-Kaiser E,Wehrli B,et al.2006.Anaerobic ammonium oxidation in a tropical freshwater system (Lake Tanganyika)[J].Environmental Microbiology,8(10):1857-1863 |
| [26] | Shen L D,Liu S,Lou L P,et al.2013.Broad distribution of diverse anaerobic ammonium-oxidizing bacteria in Chinese agricultural soils[J].Applied and Environmental Microbiology,79(19):6167-6172 |
| [27] | Shen L D,Liu S,Huang Q,et al.2014a.Evidence for the cooccurrence of nitrite-dependent anaerobic ammonium and methane oxidation processes in a flooded paddy field[J].Applied and Environmental Microbiology,80(24):7611-7619 |
| [28] | Shen L D,Liu S,Zhu Q,et al.2014b.Distribution and diversity of nitrite-dependent anaerobic methane-oxidizing bacteria in the sediments of the Qiantang river[J].Microbial Ecology,67(2):341-349 |
| [29] | Shi Y,Hu S H,Lou J Q,et al.2013.Nitrogen removal from wastewater by coupling anammox and methane-dependent denitrification in a membrane biofilm reactor[J].Environmental Science & Technology,47(20):11577-11583 |
| [30] | Strous M,Jetten M S M.2004.Anaerobic oxidation of methane and ammonium[J].Annual Review of Microbiology,58:99-117 |
| [31] | Thamdrup B,Dalsgaard T.2002.Production of N2 through anaerobic ammonium oxidation coupled to nitrate reduction in marine sediments[J].Applied and Environmental Microbiology,68(3):1312-1318 |
| [32] | Wang J,Dong H L,Wang W D,et al.2014.Reverse-transcriptional gene expression of anammox and ammonia-oxidizing archaea and bacteria in soybean and rice paddy soils of Northeast China[J].Applied Microbiology and Biotechnology,98(6):2675-2686 |
| [33] | 王衫允,祝贵兵,曲冬梅,等.2012.白洋淀富营养化湖泊湿地厌氧氨氧化菌的分布及对氮循环的影响[J].生态学报,32(21):6591-6598 |
| [34] | Wang S Y,Zhu G B,Peng Y Z,et al.2012a.Anammox bacterial abundance,activity,and contribution in riparian sediments of the Pearl River estuary[J].Environmental Science & Technology,46(16):8834-8842 |
| [35] | Wang Y,Zhu G B,Harhangi H R,et al.2012b.Co-occurrence and distribution of nitrite-dependent anaerobic ammonium and methane-oxidizing bacteria in a paddy soil[J].FEMS Microbiology Letters,336(2):79-88 |
| [36] | Yoshinaga I,Amano T,Yamagishi T,et al.2011.Distribution and diversity of anaerobic ammonium oxidation (anammox) bacteria in the sediment of a eutrophic freshwater lake,Lake Kitaura,Japan[J].Microbes and Environments,26(3):189-197 |
| [37] | 张文河,穆桂金.2007.烧失法测定有机质和碳酸盐的精度控制[J].干旱区地理,30(3):455-459 |
| [38] | Zhou L L,Wang Y,Long X E,et al.2014.High abundance and diversity of nitrite-dependent anaerobic methane-oxidizing bacteria in a paddy field profile[J].FEMS Microbiology Letters,360(1):33-41 |
| [39] | Zhu B L,van Dijk G,Fritz C,et al.2012a.Anaerobic oxidization of methane in a minerotrophic peatland:enrichment of nitrite-dependent methane-oxidizing bacteria[J].Applied and Environmental Microbiology,78(24):8657-8665 |
| [40] | Zhu G B,Jetten M S M,Kuschk P,et al.2010.Potential roles of anaerobic ammonium and methane oxidation in the nitrogen cycle of wetland ecosystems[J].Applied Microbiology and Biotechnology,86(4):1043-1055 |
| [41] | Zhu G B,Wang S Y,Feng X J,et al.2011a.Anammox bacterial abundance,biodiversity and activity in a constructed wetland[J].Environmental Science & Technology,45(23):9951-9958 |
| [42] | Zhu G B,Wang S Y,Wang Y,et al.2011b.Anaerobic ammonia oxidation in a fertilized paddy soil[J].The ISME Journal,5(12):1905-1912 |
| [43] | Zhu G B,Wang S Y,Wang W D,et al.2013.Hotspots of anaerobic ammonium oxidation at land-freshwater interfaces[J].Nature Geoscience,6(2):103-107 |
| [44] | Zhu G B,Zhou L L,Wang Y,et al.2015.Biogeographical distribution of denitrifying anaerobic methane oxidizing bacteria in Chinese wetland ecosystems[J].Environmental Microbiology Reports,7(1):128-138 |
| [45] | 朱群,沈李东,胡宝兰,等.2013.西湖底泥中的反硝化型甲烷厌氧氧化菌的分子生物学检测[J].环境科学学报,33(5):1321-1325 |
 2015, Vol. 35
2015, Vol. 35


