随着经济的快速增长,能源消耗持续增加(Tao et al., 2000),NOx的排放量也随之持续增加,成为了我国主要控制的大气污染物之一.NO直接催化分解为N2和O2,由于其不消耗NH3、CO和CH4等还原剂,不产生二次污染(Latimer,1952;Garin,2001),一直被认为是一种最具吸引力的NOx去除方式.但NO分解反应需要364 kJ · mol-1的活化能,且催化剂存在下,也必须在500~600 ℃高温下才有较高的催化活性(臧玉魏等,2009),因此,在工业推广过程中有很大困难.
近年来,低温等离子体(NTP)技术在气态污染物处理中逐渐引起人们的重视(Chen et al., 2002;Kogelschatz.,2003),尤其是等离子体协同催化剂脱除NOx(Akira,2013;Moscosa-Santillan et al., 2008;Wang et al., 2013).与工业常用的SCR脱硝技术相比,低温等离子体协同催化脱硝技术通常在常温下进行反应,在实际运行过程中无需对烟气进行二次升温,可以有效降低运行费用,且等离子体协同催化分解脱硝无需液氨等还原剂,不存在氨泄漏等危险隐患,同时还可以减少装置占地面积,更加有利于实际工业应用.Rajanikanth等(2001)采用Al2O3、BaTiO3和Al2O3-Pd 3种催化剂研究了在NTP协同催化分解去除NOx,结果表明,催化剂BaTiO3有更好的NO分解活性.但实际工业废气中,常有O2存在,使得NOx分解性能和产物选择性有很大下降.
基于此,本文选用NaY分子筛作为催化剂载体,以Cu、Ce和La作为活性组分,与NaY分子筛进行离子交换制得活性组分含量不同的催化剂.同时,对比了不同催化剂在富氧条件下等离子体协同催化分解NOx性能,以确定具有较好NOx分解性能的催化剂.
2 材料与方法(Material and methods) 2.1 实验材料以南开大学催化剂厂生产的NaY分子筛(Si/Al=5.3)作为催化剂载体.将分子筛研磨筛分,选取40~60目颗粒,用去离子水先后洗净,110 ℃烘干,然后在马弗炉中550 ℃焙烧活化3 h备用.
离子交换催化剂改性:以固液比为10 g · L-1将NaY分子筛放入一定量的Cu(NO3)2溶液中,在温度为40 ℃的水浴中离子交换24 h,用去离子水洗涤,在110 ℃下干燥12 h,将制得的催化剂记为x%Cu-NaY.将上述制得的催化剂,放入一定量的Ce(NO3)3或La(NO3)3溶液中,在相同操作条件下进行二次离子交换,将制得的催化剂记为y% Ce-x%Cu-NaY或y%La-x%Cu-NaY.之后用去离子水洗净,烘干.最后,将催化剂在空气氛围下,400 ℃焙烧4 h.
2.2 催化剂性能评价实验模拟的NO/O2/N2由动态配气系统控制产生,实验装置如图 1所示.气体流量为300 mL · min-1,反应空速为6000 h-1,进口的NO浓度为0.05%,O2为3%,N2作为平衡气.烟气中NOx(NO和NO2)浓度由KM9106便携式综合烟气分析仪(Kane)测得,N2O浓度由在线质谱(Extrel CMS,LLC,MAX300-LG)检测.等离子发生电源为CTP-2000P等离子体实验电源(南京苏曼电子有限公司),示波器为DS1000E数显示波器(北京普源精电科技有限公司).
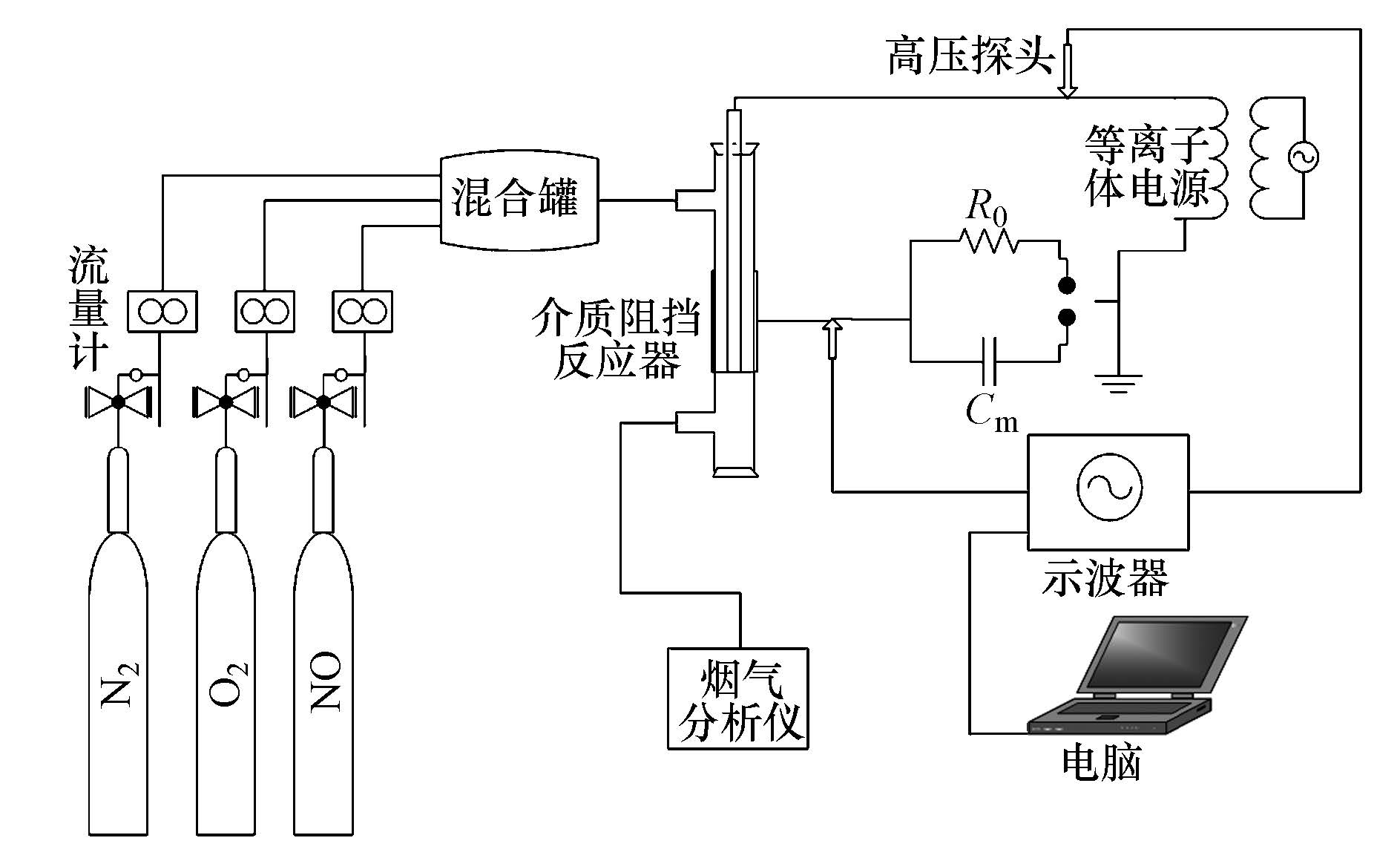 |
| 图1 实验系统流程图 Fig.1 Flow chart of experimental system |
反应器为自制的同轴筒状介质阻挡放电反应器:采用外径为10 mm的石英管固定床反应器,高压电极为3 mm铜棒,在石英管外包裹铝箔作为低压电极.在反应过程中,固定放电频率8.9 kHz,改变放电电压,测试不同电压下NOx的分解效率.
NOx转化率η和放电功率P的定义为:
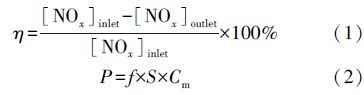
由于NaY分子筛在有氧条件下对NOx有一定的吸附量,为了消除吸附对NOx分解效率的影响,本文中所有实验使用的催化剂都提前进行NOx吸附,达吸附饱和后再进行实验操作.
实验研究了Cu含量为3%、5%、8%、16%进行离子交换的NaY分子筛对NOx分解效率,结果如图 2所示.从图中可以看出,等离子体放电电压和放电功率对NOx分解反应用有重要影响,随着放电电压和功率的增加,各种催化剂的NOx转化率先增大后减小.放电电压增大时反应体系中高能粒子数目增加,分解反应增强,当放电电压10 kV,放电功率为7.6 W时,NOx转化效率达最大值,但放电电压和功率过大时可能会发生NOx合成的副反应,导致大量的N2、O2反应,使得NOx转化率降低.
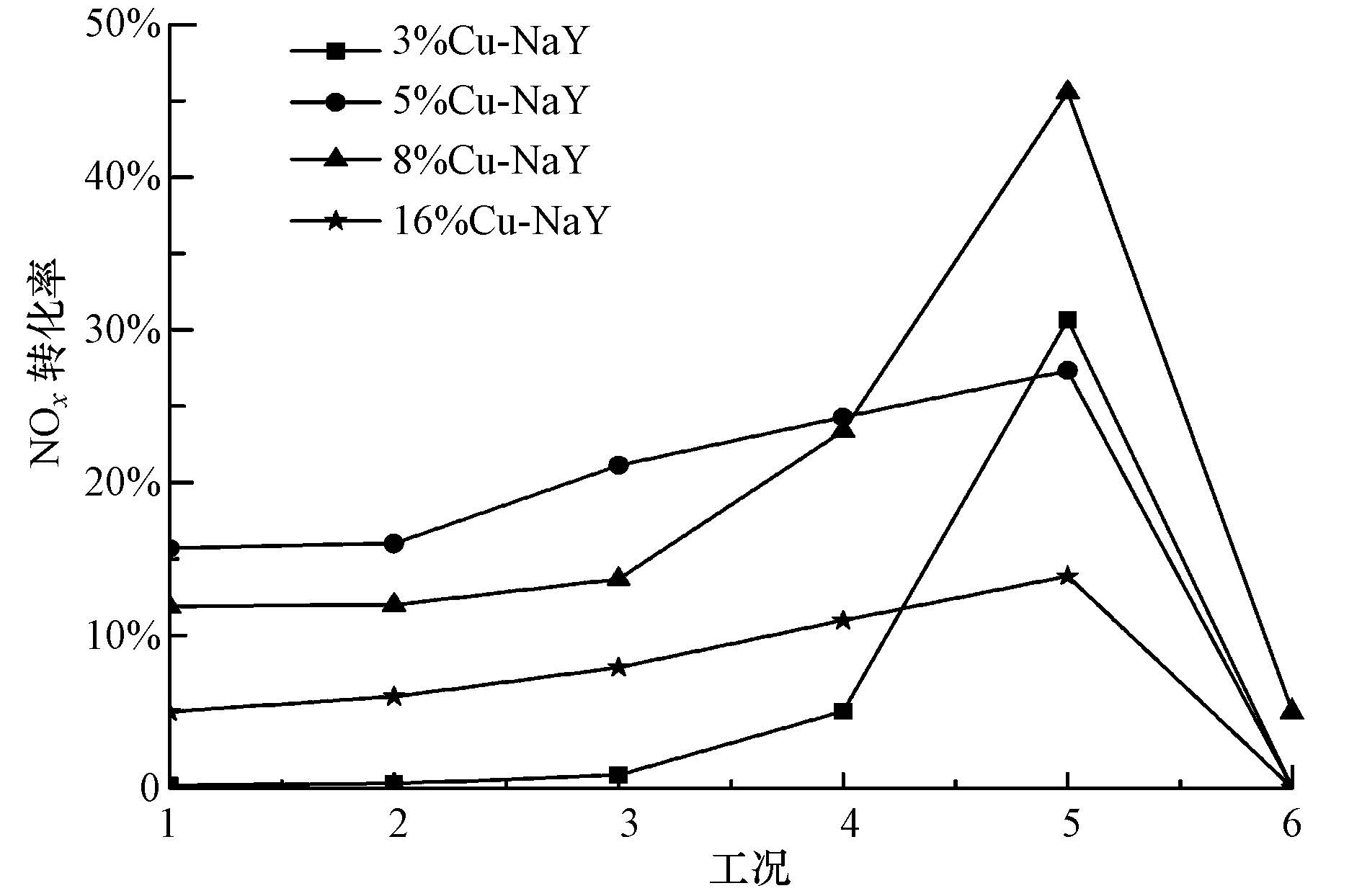 |
| 图2 不同Cu负载量对催化剂活性的影响 (工况1: 4.6 kV,0.9 W; 工况2: 5.4 kV,1.4 W; 工况3: 6.8 kV,3.2 W; 工况4: 7.8 kV,3.6 W; 工况5: 10 kV,7.6 W; 工况6: 12 kV,14 W;下同) Fig.2 Effect of different Cu content on catalyst activity |
随着催化剂中Cu含量的增加,NOx转化率逐渐提升,说明Cu物种是NOx催化分解反应所必需的催化活性组分(Valyon et al., 1993;阳鹏飞等,2011).当催化剂中Cu含量达8%时,8%Cu-NaY催化剂活性最高,放电电压为10 kV,放电功率为7.6 W时,NOx转化率达46.3%.其主要反应途径为NO先吸附在催化剂活性位上分解为N和O,而O和活性位Cu+结合,将Cu+氧化为Cu2+,然后NO与再吸附的氧及催化剂上超晶格氧反应形成NO2或NO-3,之后此种吸附的NO2以NO和O2形式脱附,将Cu2+还原为Cu+(Wang et al., 1997).当催化剂中Cu含量达16%时,NOx转化率明显低于8%Cu-NaY,NOx转化率只有12.5%,这可能是由于Cu含量过大并聚集使得催化剂部分孔道堵塞,导致催化剂活性下降(朱君江等,2004).
由于等离子体引发的化学过程非常复杂,形成的“协同”效应不仅有利于污染物的脱除,也有可能发生副产物的生成反应.实验是在含O2、N2条件下进行,可能产生NOx的生成反应,出现NO、N2O、NO2反应副产物.图 3所示为不同Cu负载量时,NOx分解过程中的产物分析.
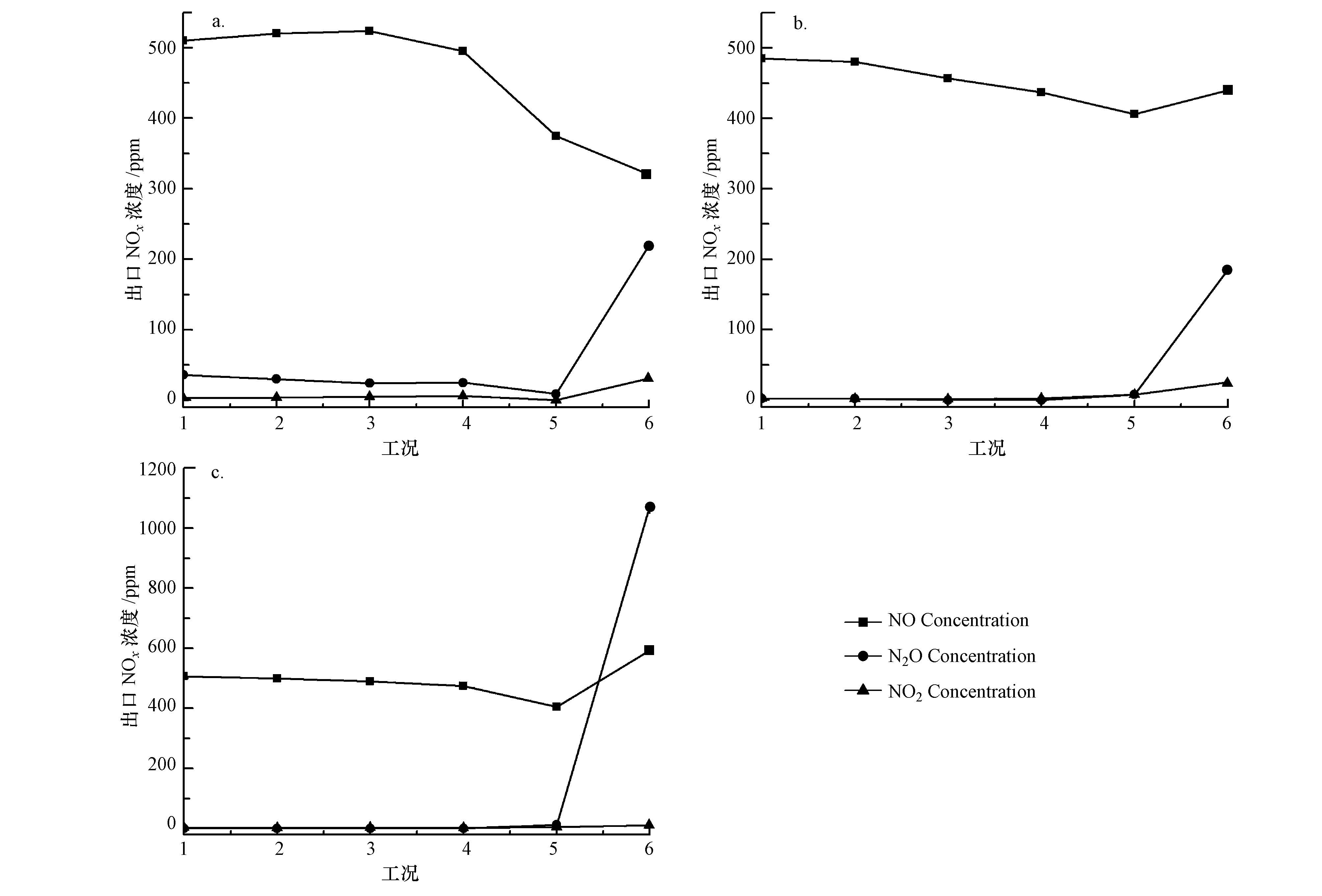 |
| 图3 不同Cu负载量下NOx催化分解产物分析(a.3%Cu-NaY;b.5%Cu-NaY;c.8%Cu-NaY) Fig.3 Analysis of NOx catalytic decomposition products of different Cu contents(a.3%Cu-NaY;b.5%Cu-NaY;c.8%Cu-NaY) |
从图中可以看出,当放电电压低于10 kV时,出口中NO的浓度逐渐减小.当电压为12 kV时,5%Cu-NaY和8%Cu-NaY催化剂上,出口中NO浓度急剧上升.这可能是等离子体和催化剂结合过程中,气相中的N原子和催化剂上的吸附O2相互作用发生基元反应:N+O2(ads)→NO+O(ads),使得吸附在催化剂表面的O—O键被活化,加快反应N+O(ads)→NO进行,导致NO生成.或者吸附在催化剂表面的NOx在等离子体作用下发生脱附作用,造成出口中NO浓度增加(孙琪等,2009).在整个反应过程中,各种催化剂出口中NO2生成量非常少,均低于50 ppm.
N2O作为反应的主要副产物,当电压小于10 kV时,各催化剂出口中N2O浓度均低于40 ppm,但当放电电压为12 kV时,3%Cu-NaY、5%Cu-NaY、8%Cu-NaY 3种催化剂上,出口中N2O浓度分别达到了220、185、1072 ppm.这可能是因为当等离子体放电强度过强时,基元反应e*+N2→N+N+e增强,与体系中存在的NO和NO2发生反应:N+NO→N2O,N+NO2→N2O+O,使得N2O生成量迅速增长(孙琪等,2009),甚至超过了进气中NO的量.
3.2 Ce/Cu改性NaY分子筛对脱硝性能的影响氧对催化剂的活性有很大影响,其容易在催化剂表面吸附形成“氧阻抑”,研究表明,氧会强烈吸附在催化剂表面,使得活性位再生困难,影响NOx在催化剂表面的吸附分解过程(孙琪等,2009;朱君江等,2005).Winter(1971)做的动力学研究指出,NO分解反应为一级反应,而氧的脱附是NO分解反应的速率决定步骤.用Ce交换后的催化剂,由于Ce具有可变价态,有很好的贮放氧性能,能参与反应而形成一个新的有利于氧流动和脱附的活性位,从而提高NOx分解性能(Zhu et al., 2005;朱君江等,2005).
实验采用不同含量的Ce(NO3)3溶液与8%Cu-NaY催化剂进行二次离子交换,制得Ce含量不同的催化剂,实验结果如图 4所示.Ce的引入明显提高了催化剂在有氧条件下的催化活性,当电压小于10 kV时,各催化剂NOx转化率在30%~70%之间,比Cu-NaY催化剂催化活性有很大提升.3% Ce-8%Cu-NaY催化剂在电压为6.8 kV时,NOx转化率达最大值56.1%.5% Ce-8%Cu-NaY有较高的催化效率,随着放电电压的增大,NOx转化率先增大后在减小,当放电电压为7.8 kV,功率为3.6 W时,NOx转化率达67.3%.根据图 3中的产物分析可知,当放电电压大于10 kV时,反应产物中的N2O浓度会持续上升,可能发生NOx合成等其他副反应,使得NOx分解率降低.
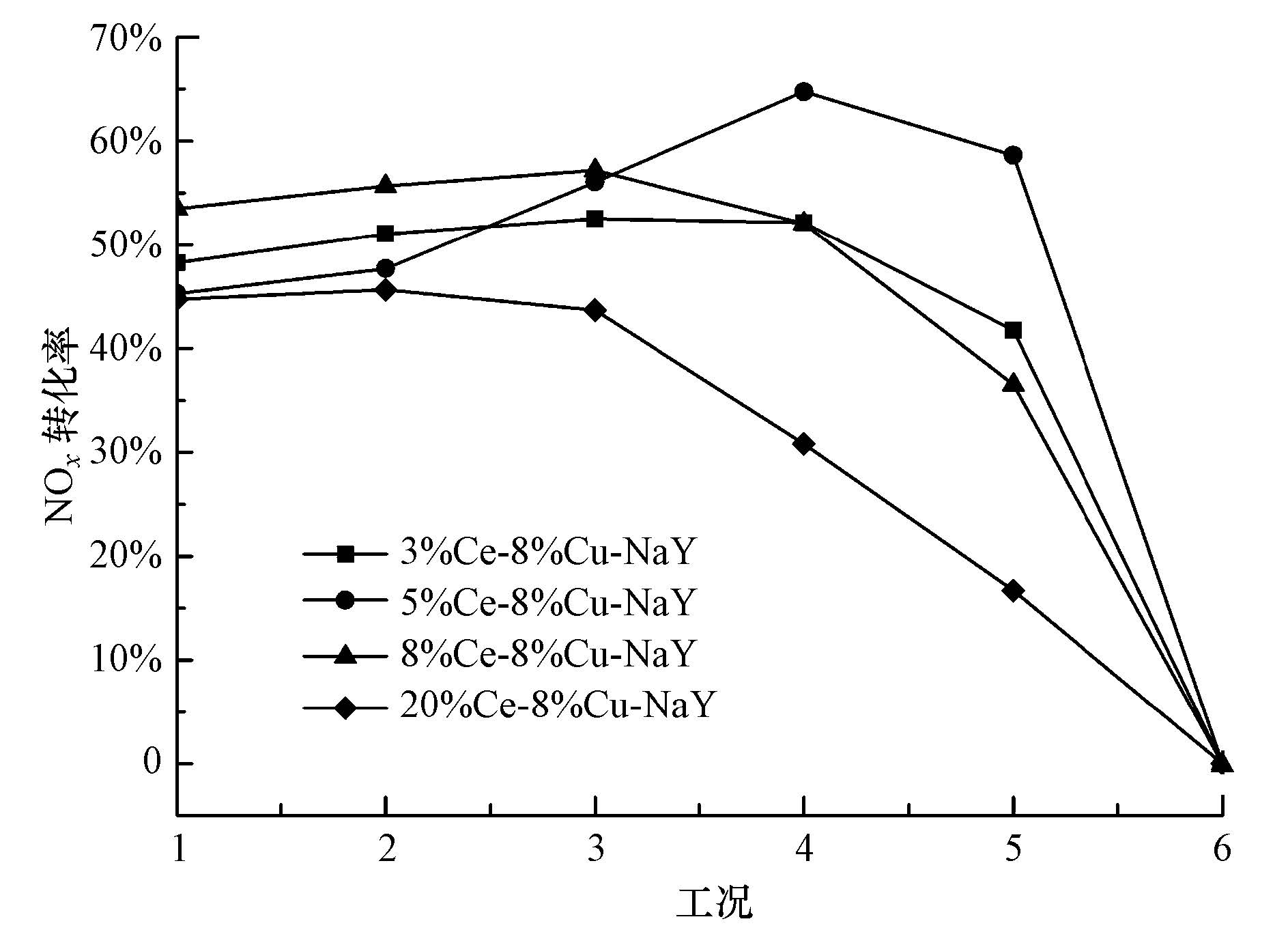 |
| 图4 不同Ce/Cu负载量对催化剂活性的影响 Fig.4 Effect of different Ce/Cu content on catalyst activity |
随着Ce的交换量进一步增加,NOx转化率进一步减小.20% Ce-8%Cu-NaY催化剂在电压为7.8 kV时,NOx转化率只有34.7%,远小于相同条件下5% Ce-8%Cu-NaY催化剂的NOx转化率.这主要是因为过多的Ce离子交换使得催化剂上活性组分Cu的量降低,使得催化活性降低,而且过量的Ce掺入,催化剂上的氧空穴将会大大减少,使催化剂活性降低(Zhu et al., 2005;朱君江等,2005).
图 5为不同Ce/Cu 负载量时NOx分解产物分析.从图中可以看出,当放电电压小于10 kV时候,各催化剂反应出口NO浓度随着放电电压增大逐渐减小,且反应生成的NO2和N2O也较少,均小于43 ppm,反应主要以NOx分解为主.但当放电电压大于10 kV时,等离子体放电强度过大,催化剂选择性降低,使得反应体系中的N2和吸附在催化剂表面的O2发生反应,使得反应出口的NO、N2O浓度急剧增加,甚至超出了进口的NO浓度.
3.3 La/Cu改性NaY分子筛对脱硝性能的影响La和Ce同为稀土元素,且Ce3+和La3+的半径也相似,分别为0.101和0.103 nm(付延俊等,2011),La掺杂到Cu-NaY催化剂上,催化剂活性的改变与Ce的掺杂很相似,对比图 5和图 4可以看出,当电压小于10 kV时,NOx的转化率都在30%~60%,但两种催化剂的最佳的反应电压不同.
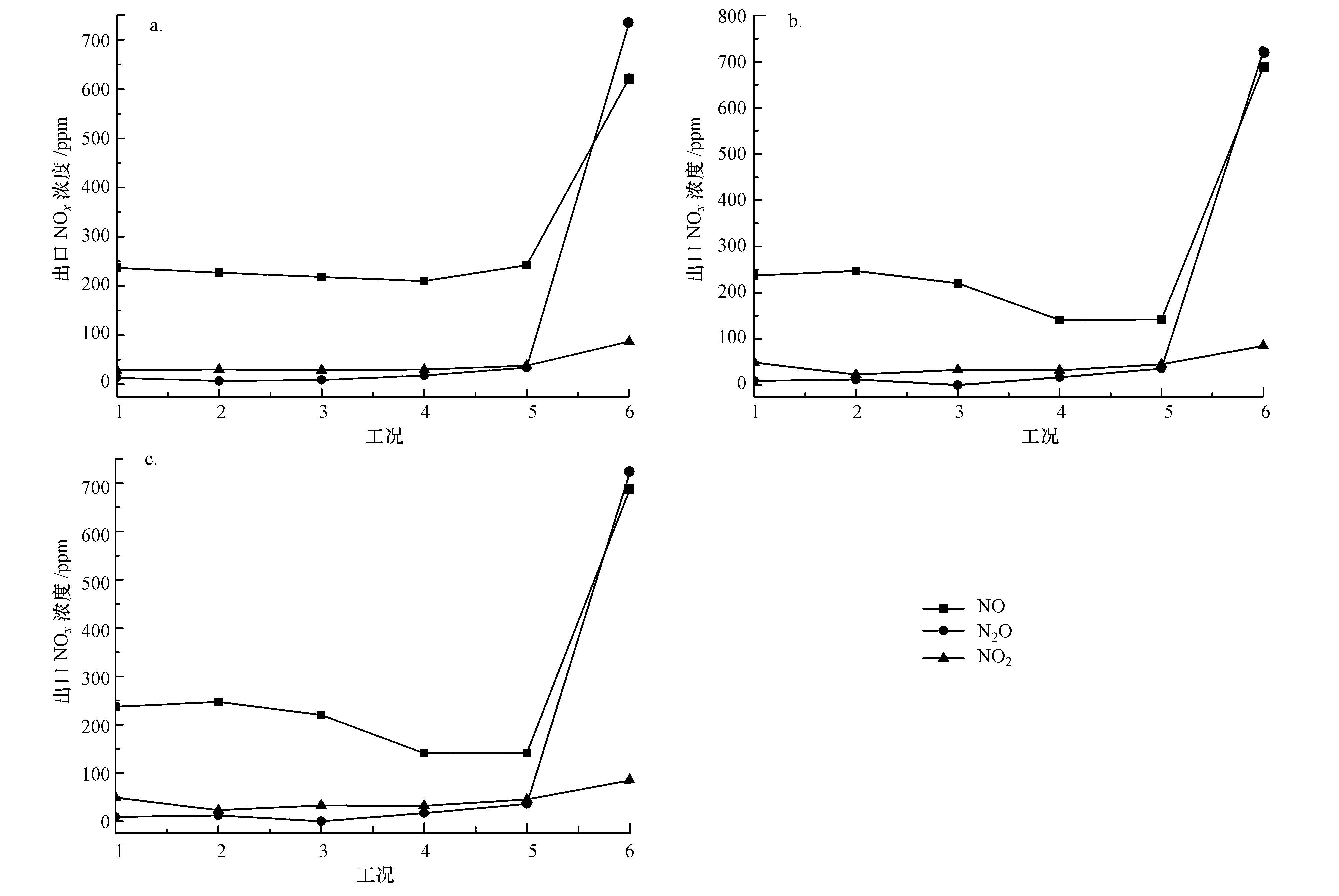 |
| 图5 不同Ce/Cu负载量NOx催化分解产物分析(a.3% Ce-8%Cu-NaY;b.5% Ce-8%Cu-NaY;c.20% Ce-8%Cu-NaY) Fig.5 Analysis of NOx catalytic decomposition products of different Ce/Cu contents(a.3% Ce-8%Cu-NaY;b.5% Ce-8%Cu-NaY; c.20% Ce-8%Cu-NaY) |
从图中6可以看出,不同的La交换量下的催化剂催化效率相近,随着放电电压的增加,最开始吸附在催化剂上的NOx有少许脱附,使得NOx转化率降低.随着放电电压增强,NOx分解效率增加,当放电电压为10 kV,放电功率为7.6 W时,NOx转化率达最大值.由于La3+的f亚层为全空状态,会使得La相对于Ce更容易进入分子筛(付延俊等,2011),使得催化剂上La的离子交换更大,造成催化剂上Cu含量降低,与Ce改性后的催化剂对比,NOx分解活性较差.
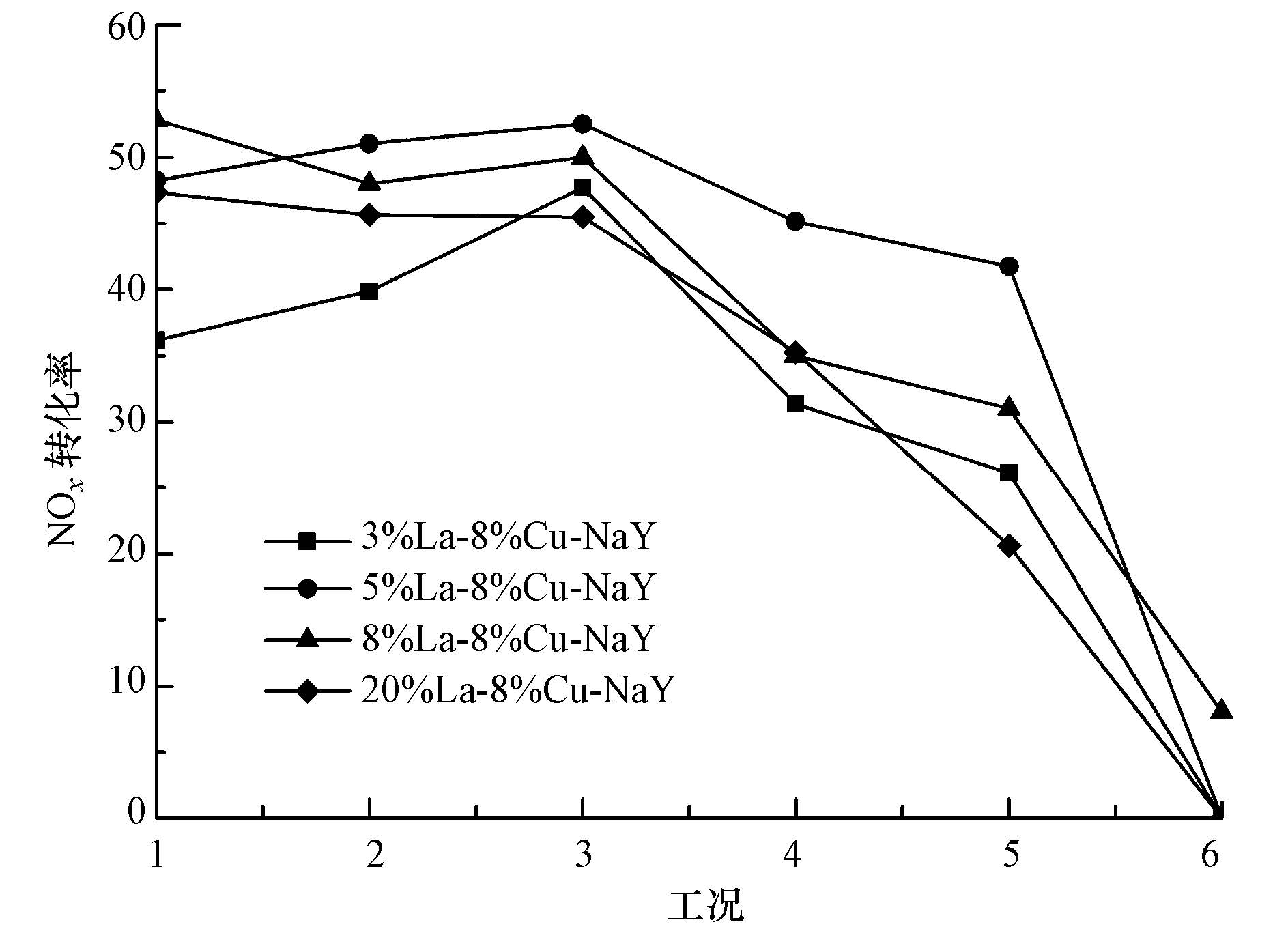 |
| 图6 不同La/Cu负载量对催化剂活性的影响 Fig.6 Effect of different La/Cu content on catalyst activity |
对比图 7和图 5,与Ce/Cu离子交换改性的NOx催化剂分解产物分析相似,当电压小于10 kV时,La/Cu离子交换催化剂在等离子体作用下主要以NOx分解为主,反应产生的NO2和N2O量均小于46 ppm.但当放电电压为12 kV时,由于放电强度过大,使得反应体系中的N2和O2参与反应,反应产物中的NO2、N2O和NO浓度急剧上升,催化剂分解活性降低.
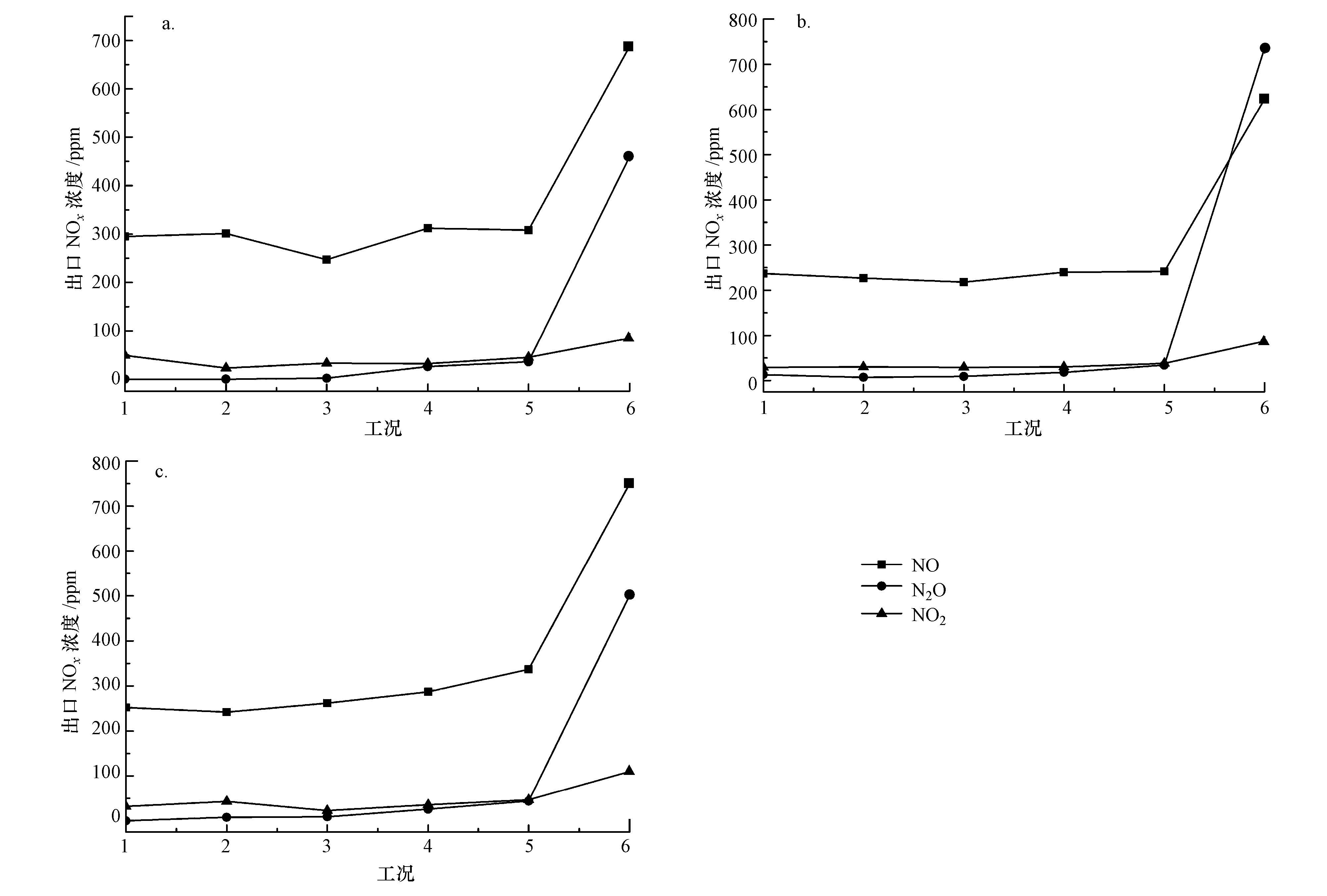 |
| 图7 不同La/Cu负载量下NOx催化分解产物分析(a.3%La-8%Cu-NaY;b.5%La-8%Cu-NaY;c.20%La-8%Cu-NaY) Fig.7 Analysis of NOx catalytic decomposition products of different La/Cu contents(a.3%La-8%Cu-NaY;b.5%La-8%Cu-NaY; c.20%La-8%Cu-NaY) |
1)Cu是NOx催化分解的主要活性组分,对于8%Cu-NaY催化剂,当放电电压为10 kV,放电功率为7.6 W时,NOx转化率达46.3%,且较好的产物选择性,N2O生成量只有11 ppm,而且没有NO2生成.
2)Ce的加入可以有效提高催化剂催化活性,对于5% Ce-8%Cu-NaY催化剂,当放电电压为7.8 kV,功率为3.6 W时,NOx转化率达67.3%.但当Ce的交换量过大时,会使得催化剂上活性组分Cu的量降低,造成催化剂活性降低.
3)La的加入同样可以使催化剂活性上升,但并没有最佳的La交换量,不同La含量催化剂的NOx转化率相差较小.
| [1] | Akira M.2013.Generation of non-thermal plasma combined with catalysts and their application in environmental technology[J].Catalysis Today, 211:2-8 |
| [2] | Chen Z,Mathur V K.2002.Nonthermal plasma for gaseous pollution control[J].Industrial & Engineering Chemistry Research,41(9):2082-2089 |
| [3] | Fang Z,Qiu Y,Luo Y.2003.Surface modification of polytetrafluoroethylene film using the atmospheric pressure glow discharge in air[J].Journal of Physics (D:Applied Physics),36(23):2980-2985 |
| [4] | Fridman A,Chirokov A,Gutsol A.2005.Non-thermal atmospheric pressure discharges[J].Journal of Physics (D:Applied Physics),38(2):1-24 |
| [5] | 付延俊,郑华艳,牛燕燕,等.2011.Ce,La和Cs离子对CuY催化甲醇氧化羰基化活性中心的影响[J].化学学报,69(15):1765-1772 |
| [6] | Garin F.2001.Mechanism of NOx decomposition[J].Applied Catalysis (A:General),222(1/2):183-219 |
| [7] | Kogelschatz U.2003.Dielectric-barrier discharges:their history discharge physics and industrial applications[J].Plasma Chemistry and Plasma Processing,23(1):1-46 |
| [8] | Latimer W M.1952.The Oxidation States of the Elements and Their Potentials in Aqueous Solutions[M].Englewood Cliffs:Prentice Hall |
| [9] | Moscosa-Santillan M,Vincent A,Santirso E,et al.2008.Design of a DBD wire-cylinder reactor for NOx emission control:experimental and modelling approach[J].Journal of Cleaner Production,16(2):198-207 |
| [10] | Rajanikanth B S,Satyabrata R.2001.Studies on nitric oxide removal in simulated gas compositions under plasma-dielectric/catalytic discharges[J].Fuel Process Technology,74(3):177-195 |
| [11] | 孙琪,杨佳,石雷,等.2009.介质阻挡放电和Cu-ZSM-5结合体系中等离子体对C2H4的作用[J].化学学报,67(15):1779-1783 |
| [12] | Tao F L,Feng Z W.2000.Critical loads of SO2 dry deposition and their exceedance in south China[J].Water,Air,and Soil Pollution,124(3/4):429-438 |
| [13] | Valyon J,Hall W K.1993.Studies of the desorption of oxygen from Cu-Zeolites during NO decomposition[J].Jourmal of Catalysis,143(2):520-532 |
| [14] | Wang H,Li X X,Chen P,et al.2013.An enhanced plasma-catalytic method for DeNOx in simulated flue gas at room temperature[J].Chemical Communication,49(81):9353-9355 |
| [15] | Wang Z Q,Sklyarov A V,Keulks G W.1997.TPD study of the interaction of oxygen and NO with reduced Cu/ZSM-5[J].Catalysis Today,33(1/3):291-302 |
| [16] | Winter E R S.1971.The catalytic decomposition of nitric oxide by metallic oxides[J].Journal of Catalysis,22(2):158-171 |
| [17] | 阳鹏飞,周继承,任文明.2011.不同方法制备的Cu/HZSM-5催化剂上NO的催化分解反应[J].燃料化学学报,39(2):122-127 |
| [18] | 朱君江,肖德海,李静,等.2004.(类)钙钛石型催化剂上NO分解反应机理[J].科学通报,49(23):2501-2503 |
| [19] | 朱君江,肖德海,吴越,等.2005.La1-xCexSrNiO4(0 ≤ x ≤ 0.7)的合成、表征及NOx分解催化性能的研究[J].高等化学学报,26(3):503-506 |
| [20] | Zhu J J,Xiao D H,Li J,et al.2005.Effect of Ce on NO direct decomposition in the absence/presence of O2 over La1-xCexSrNiO4(0 ≤ x ≤ 0.3)[J].Journal of Molecular Catalysis (A:Chemical),234(1/2):99-105 |
| [21] | 臧玉魏,钟秦.2009.改性Cu-ZSM-11和Cu-ZSM-5分子筛催化分解一氧化氮性能[J].硅酸盐学报,37(11):1853-1858 |
 2015, Vol. 35
2015, Vol. 35


