2. 常州大学, 环境与安全工程学院, 常州 213164
2. School of Environmental and Safety Engineering, Changzhou University, Changzhou 213164
地表水天然水化学是相对于污染物水化学的概念,通常指天然水体中8种主要离子(K+、Na+、Ca2+、Mg2+、Cl-、SO42-、HCO3-、CO32-)的含量及比例关系(Chen et al., 2002).天然水化学反映了流域自然地理、水文循环、气候植被、生物化学等综合作用的结果,其各项指标是研究水化学变化过程和评价水环境及水体水化学类型的重要依据(Brezonik et al., 2012). 人类最早对天然水化学的研究始于欧洲,至今已有100多年的历史(夏星辉,1998). 而且,不同的研究阶段具有不同的特点,早期的研究以描述水体天然水化学特征为主.例如,早在1888年,美国地质勘探局(USGS)描述了纽约附近一些河流的水化学状况,并认为污水排放会影响河流水化学特征(Brezonik et al., 2012). Gibbs(1970)首次把天然水化学成因和流域的自然地理条件联系起来,提出天然水化学特征主要受流域岩石风化、蒸发-结晶和大气降水等自然因素控制,为之后的水化学研究奠定了新的基础.随着社会经济的发展,在最近几十年里,受人类活动等因素的影响,全球范围内地表水水化学特征较过去已发生了很多变化.例如,化石燃料的大量使用导致淡水湖泊水体酸化(Neary et al., 1988; Heard et al., 2014),全球范围内陆地水质含盐量增高和次生盐碱化等问题(Meybeck,2003;Cañedo-Argüelles et al., 2013).因此,人们越来越重视人为活动对天然水化学的影响.近年来,国际上关于天然水化学的代表性研究涉及了气候变化对天然水化学的影响(Delpla et al., 2009; Houle et al., 2010),水化学变化对饮用水质量和人体健康的影响(Khan et al., 2011),以及水化学变化与水体生态系统变化的关系(Battarbee et al., 2014)等. 而我国在这些领域的研究还缺乏深入性和系统性.
我国较早的系统性天然水化学研究是20世纪50、60年代开展的全国地表水调查,该成果描述了全国地表水和地下水水化学类型和空间分布特征(中国科学院中国自然地理编辑委员会,1981;乐嘉祥等,1963),为此后的相关研究提供了大量的基础资料. Hu等(1982)研究了中国主要大河水系的水化学成因特征,认为我国主要河流水化学成分主要起源于流域碳酸盐岩和蒸发岩的风化溶解作用,而受硅酸盐的影响较小.
陈静生等(1998a;1998b)是国内较早将河流水化学变化同流域人为活动影响联系起来研究的学者,通过对主要流域的水化学研究,得出长江水系水质由于受燃煤影响有弱酸化趋势,黄河水系水质由于农业活动有盐渍化趋势(陈静生等,2000)等结论. 但这些研究没有涉及我国湖泊水体的天然水化学变化.
太湖是我国第三大淡水湖,是周边城市重要的饮用水水源地. 近30年来,由于太湖流域农业和工业的迅速发展,使得水体富营养化、重金属和有机污染物风险等问题受到了广泛关注(秦伯强等,2007; Stone,2011; Yu et al., 2012). 太湖作为典型的淡水湖泊,天然水化学变化对湖泊生态环境具有十分重要的意义.然而,目前对太湖天然水化学特征的研究十分有限,特别是流域污水排放对水化学影响的定量研究尚未见报道.近年来,Yu等(2013)研究讨论了太湖水化学变化与流域生活污水排放的关系,但仍未涉及定量计算和说明工业废水排放对湖水天然水化学的影响.
本文在上述研究的基础上,基于太湖60年以来的水化学变化情况,结合太湖周边生活和工业污水处理厂进口(处理前)、出口(处理后)污水的水化学(主要离子)特征,通过计算说明流域污水排放对湖泊天然水化学的影响,探讨太湖天然水化学与人为影响下的水化学之间的差异. 一方面可以补充现有研究的不足,另一方面可以为湖泊水化学演化的研究及强烈人为干预条件下的饮用水管理提供基础资料.
2 材料和方法(Materials and methods) 2.1 研究区位置和概况太湖位于我国长江中下游地区,水域面积2338 km2,平均水深1.9 m,属于典型的大型浅水湖,2012年末储水量52.1亿m3,目前水体交换周期大约309 d. 太湖流域气候温暖湿润,降水充沛,河网密布,水系发达,平均人口密度为1500人· km-2,是全国平均值的10倍,城市化率高达73%,是我国经济最发达的地区之一. 随着太湖流域人口增长,社会用水量进一步加大,整个太湖流域的污水排放量呈显著增长趋势(程声通等,2013),对当地水环境产生了严重的压力.
2.2 采样分析和数据来源本研究于2011—2014年期间在太湖及其周边开展样品采集,其中包括20个点的湖水和18个点的主要入湖河水样品采集(图 1). 具体采样时间分别为2011年6、8、11月和2012年1、11月及2014年11月底. 雨水样品分别于2011年11月、2012年1、11月及2014年7月在宜兴大浦镇采集;19个污水处理厂的进出口水样主要在2012年1、11月、2013年11月及2014年7月采集. 这些污水处理厂主要分布于太湖北部和西北部的上游区,其中包括12个代表性的生活污水处理厂和7个代表性工业废水处理厂的进水和出水. 一些生活污水处理厂在运行时约有20%~40%工业废水混入(以印染废水为主),可能对计算会产生影响.各污水处理厂排放的污水通过河网、沟渠等最终直接或间接排入太湖.所有水样均用预先处理好的500 mL聚乙烯塑料瓶采集,并于0~4 ℃冷藏保存带回实验室分析.
水质参数(pH、溶解氧、电导率、温度)均在现场使用YSI水质参数仪测试,水化学测试分析项目为主要离子(K+、Na+、Ca2+、Mg2+、Cl-、SO42-、HCO3-)和总硬度.K+、Na+、Ca2+、Mg2+采用美国戴安公司产的ICS-900型离子色谱仪测定,Cl-采用硝酸银滴定法(GB11896-89)测定,SO42-采用铬酸钡分光光度法(HJ/T 342—2007)测定,HCO3-采用酸碱指示剂滴定法(《水和废水监测分析方法》(第4版))测定. 总溶解性固体(Total Dissolved Solids,TDS)是上述主要离子的加和.总硬度(Total Hardness)采用EDTA滴定法(《水和废水监测分析方法》(第4版))测定. 测试之前,所有的水样都经0.45 μm的醋酸纤维微孔滤膜过滤,为保证数据的精确性,每个样品均做一个平行样,并有重复测试,相对标准差均控制在20%以内.
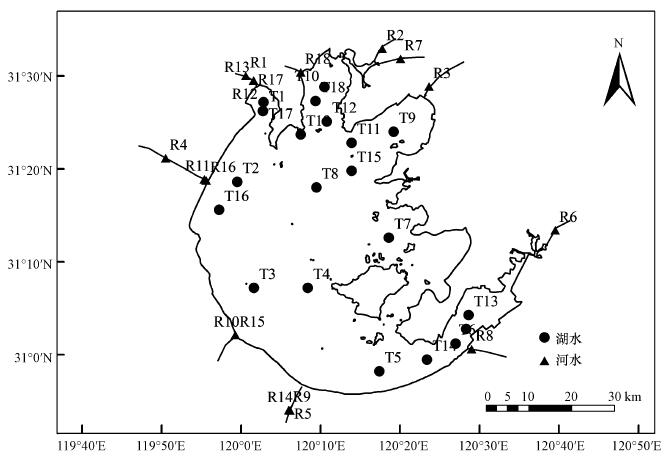 |
| 图 1 太湖采样点位图 Fig.1 Lake Taihu and sampling sites in this study |
太湖天然水化学历史数据分别收集自长江流域水文统计年鉴(1950s—1970s),全球水质监测系统(GEMS,1980s—1990s)和中国生态系统定位观测与研究数据集(2000s)(秦伯强等,2010),2010s(2011—2012年)的数据由本研究现场采样分析测试得出. 流域污水排放量数据收集自流域内各省市的统计年鉴.
2.3 数据处理与计算由于主要离子的非降解性,考虑到太湖属于浅水湖泊,风浪扰动较大且水体交换周期较长(309 d),可假设入湖污水与湖水完全混合,且混合过程中主要离子没有损失. 因此,污水排放对湖水影响的计算借鉴完全混合断面污染物平均浓度计算模型(张自杰,2000).在考虑污水入湖系数后,将原方法修正后用于污水与湖水混合后太湖主要离子平均浓度的计算.计算考虑只有生活污水影响和同时只有生活污水和工业污水影响两种情况,相应的计算公式如下:
| CS=(CSCVSC×80%+ClakeVlake)/(Vlake+VSC)×T/365 | (1) |
| CS+G=(CSCVSC×80%+CGCVGC×80%+ClakeVlake)/(Vlake+VSC +VGC)×T/365 | (2) |
受人类活动影响,太湖水化学变化是一个连续渐变的过程,因此,将(2000—2006年)太湖水化学数据作为污水与湖水混合前的湖水水化学数据参与计算,将2011—2012年太湖实测水化学数据作为现在湖水水化学真实值与模拟计算结果进行比较.
运用SPSS17.0软件对数据进行均值、标准差等统计分析.在正态检验的基础上选择Pearson相关分析检测变量之间的相关性;不同来源水样的水化学差异比较采用独立样本T检验,显著性水平选择0.05. 采用Origin 8.0进行绘图.
3 结果(Results) 3.1 太湖目前的水化学类型及与1950s年代对比水中阴阳离子浓度与离子之间的比例关系反映了水体的水化学类型,而水化学三角图不仅可以用来表征地表水体的主要离子和优势离子的组成情况,还可以反映水化学的成因(Hu et al., 1982). 图 2是目前太湖水化学与1950s年代水化学阴离子组成(图 2a)和阳离子组成(图 2b)的对比情况. 由图可见,1950s年代的阴离子组成中,所有的水样点均靠近HCO3-一端,但目前所有的水样点已明显偏离1950s年代水质,而且靠近Cl-一端(图 2a). 1950s年代的阳离子组成图中,水样点虽分布较为分散,但大多主要靠近Ca2+和Mg2+端元,而目前所有水样点分布较为集中,且靠近K++Na+端元(图 2b). 2个三角图均表明,与1950s年代相比,湖水的优势阴阳离子组分均已发生了显著变化.
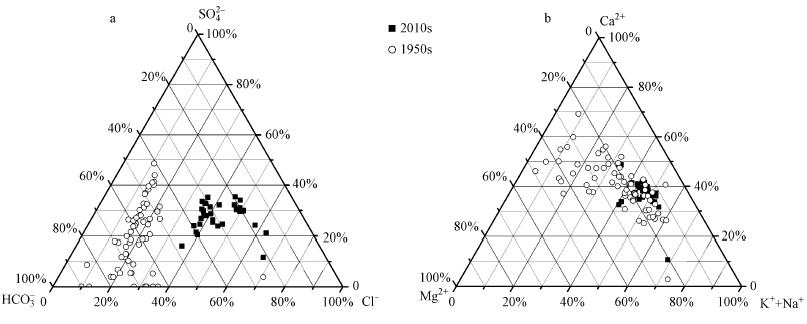 |
| 图 2 太湖湖水阴离子(a)和阳离子(b)组成三角图 Fig.2 Triangle of anions(a) and cations(b)in Taihu water |
对湖水中优势离子的计算表明:1950s年代阳离子中,Ca2+占40.93%,Mg2+占23.54%,Na+占37.68%;而目前Ca2+占37.91%,Mg2+占15.99%,Na+占43.41%. 对于阴离子,1950s年代,Cl-占18.56%,SO42-占23.00%,HCO3-占61.54%;而目前Cl-占42.98%,SO42-占28.27%,HCO3-只占28.75%. 与1950s年代相比,目前湖水中Cl-和Na+分别成为优势阴、阳离子,太湖天然水化学类型已发生显著变化,从1950s年代的碳酸盐钙型水转变为目前的氯化物钠型水.
3.2 太湖周边污水处理厂排放污水的主要离子特征12个生活污水处理厂进水(处理前)阳离子中,Na+浓度最高((7.68±6.80)mmol · L-1),K+浓度最低((0.41±0.36)mmol · L-1);阴离子中HCO3-浓度最高((6.55±1.82)mmol · L-1),其次是Cl-((3.60±1.84)mmol · L-1),而SO42-浓度最小((2.23±2.86)mmol · L-1)(图 3a). 与进水相比,生活污水处理厂出水(处理后)主要离子中,HCO3-浓度显著下降(n=12, p<0.01)((3.19±1.74)mmol · L-1),仅为进水的1/2左右,这是因为在污水二级处理过程中,HCO3-作为碳源被微生物利用而消耗. 其它离子在进出水中的浓度没有显著性差异.
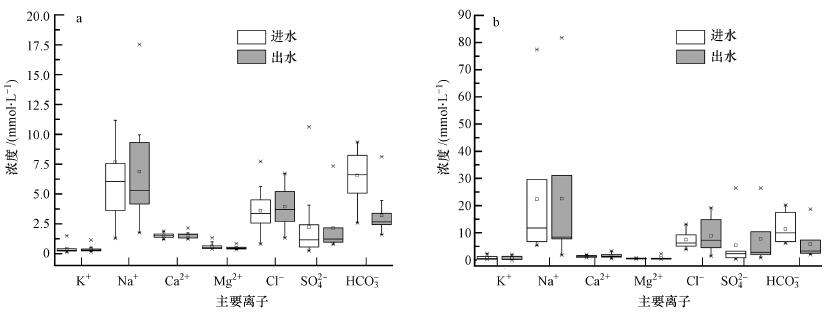 |
| 图 3 污水处理厂进水、出水中主要离子浓度对比(a.生活污水,b.工业污水) Fig.3 Concentration of major ions in influent and effluent of the sewage treatment plants(a.domestic sewage,b.industrial wastewater) |
与生活污水相似,7个工业污水处理厂进水(处理前)阳离子中Na+浓度最高((22.31±25.55)mmol · L-1),K+浓度最低((0.80±0.76)mmol · L-1); 阴离子中HCO3-浓度最高((11.31±5.47)mmol · L-1),其次是Cl-(7.45±3.16)mmol · L-1),而SO42-浓度最低((5.39±9.35)mmol · L-1)(图 3b). 与进水相比,工业污水出水(处理后)主要离子中HCO3-浓度显著下降(n=7,p<0.05)((5.82±5.94)mmol · L-1),仅为进水的1/2左右,这与生活污水中HCO3-浓度变化较为相似. 其它离子在进出水中的浓度没有显著性差异. 对比生活污水和工业污水处理厂主要离子浓度发现,Cl-浓度具有显著性差异(p<0.05),其它离子浓度均没有显著性差异.
从不同水的水化学Gibbs分布模式图可以看出(图 4),生活污水和工业污水处理厂出水与湖水和河水相比,溶解性固体含量较高,具有较高的Na+/
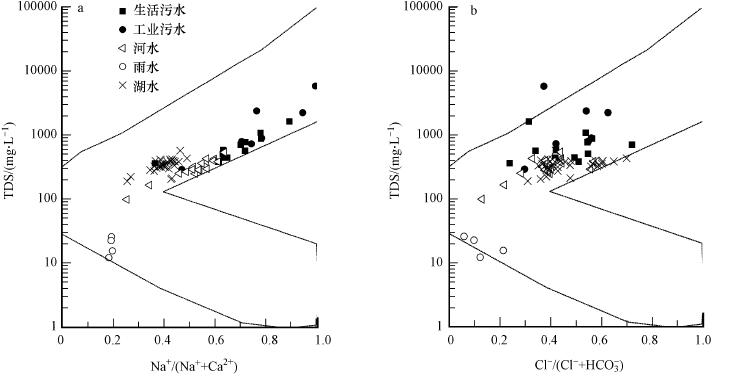 |
| 图 4 太湖流域不同来源水阴阳离子的Gibbs分布模式图(a.阳离子,b.阴离子) Fig.4 Gibbs model of different water from Taihu basin(a.cations,b. anions) |
当仅考虑生活污水排入太湖的影响时,完全混合模型计算结果显示(表 1),大部分主要离子浓度计算值与湖水实测值的相对误差在15%以内,只有阳离子中Ca2+、Mg2+和阴离子中的Cl-浓度计算值与实测值相对误差大于15%,说明仅考虑生活污水排放可以较好地说明对湖水中这些主要离子的影响,但不能很好解释对湖水Ca2+、Mg2+和Cl-浓度的影响.
| 表 1 完全混合模型计算的湖水主要离子浓度及实测湖水主要离子浓度对比(平均值±标准差) Table 1 Concentration of major ions calculated with completely mixing model and comparison with measured concentration of the major ions in Taihu water |
当同时考虑生活污水和工业污水排入太湖的影响时,计算结果显示,Na+和SO42-计算值与实测值的相对误差反而远高于仅考虑生活污水的情况,这反映了两种成分在不同来源工业污水中的显著差异,同时说明工业污水排放不能很好解释两种离子的变化.而Cl-的计算值与实测值相对误差比仅考虑生活污水的情况减小了约1半,说明工业污水排放也是湖水Cl-离子浓度变化的一个显著影响因素.此外,同时考虑生活污水和工业污水时,Ca2+和Mg2+的误差与只考虑生活污水的情况并没有显著差别,说明流域污水排放不是这两种离子的变化的主要影响因素(见讨论).
4 讨论(Discussion) 4.1 太湖主要离子来源和水化学变化的原因水体主要离子组成可用于分析水体水化学成因的控制因素. 一般认为:自然状态下,水体Na+和K+主要来源于蒸发岩和硅酸盐的风化,Ca2+和Mg2+主要来源于碳酸盐岩、蒸发岩及硅酸盐的溶解,HCO3-主要源于碳酸盐岩的溶解,而Cl-和SO42-主要来自蒸发岩的溶解(Chen et al., 2002). Gibbs分布模式图(图 4)显示,太湖流域主要河流和大部分湖水水化学的特征为:TDS平均值为340.09 mg · L-1,Na+/(Na++Ca2+)的比值和Cl-/(Cl-+HCO3-)的比值较小,说明太湖流域河湖水化学主要受岩石风化控制,受雨水和蒸发-结晶作用影响较弱(图 4).
水体中(Ca2++Mg2+)与HCO3-的比例是否近似1 ∶ 1可作为判断水体是否受碳酸盐岩溶解控制的一个依据(Xu et al., 2010). 太湖处于我国长江流域,流域内碳酸盐岩分布较广,主要以白云石和方解石为主(Hu et al., 1982; Chetelat et al., 2008).受碳酸盐岩风化控制的水体水化学主要是碳酸盐钙型水(Huang et al., 2008),这与1950s年代湖水水化学特征较为一致.对太湖的分析显示,1950s年代,(Ca2 ++Mg2+)-HCO3-在1 ∶ 1线两侧(图 5a),可以认为湖水(Ca2++Mg2+)-HCO3-基本接近平衡,即Ca2+、Mg2+和HCO3-主要来源于碳酸盐岩的溶解. 目前,太湖湖水中Ca2 +、Mg2+和HCO3-浓度较过去相比显著升高,且(Ca2++Mg2+)-HCO3-远在1 ∶ 1线上侧(图 5b). 陈静生等(1998b;2006)对长江干流水化学的研究指出,受碳酸盐岩控制地区水体酸化的趋势是HCO3-浓度下降,而Ca2+、Mg2+浓度升高,充分说明太湖水体Ca2+、Mg2+浓度升高受污水排放影响较弱(表 1),而主要是因流域酸沉降引起的碳酸盐岩溶蚀(Yu et al., 2013).
水体中(Na++K+)与Cl-的比例是否接近1 ∶ 1可作为可作为判断水体是否受蒸发岩溶解控制的一个依据(Xu et al., 2010). 对太湖分析结果显示,1950s年代,(Na++K+)-Cl-在1 ∶ 1线两侧,但部分水样点偏离1 ∶ 1线上侧(图 5c),可能是因为太湖局部水域有时以Na+最高(中国科学院中国自然地理编辑委员会,1981),可以认为湖水(Na++K+)-Cl-基本接近平衡,即Na+、K+和Cl-主要来源于蒸发岩的溶解.目前,湖水中Na+、K+和Cl-浓度较过去相比显著升高,(Na++K+)-Cl-均在1 ∶ 1线上侧(图 5d). 已有研究表明,水体中Na+和Cl-浓度变化最容易受到人类活动的影响(Chetelat et al., 2008),而Na+和Cl-浓度升高主要是因为流域污水排放(陈静生等,1998a),充分说明除了蒸发岩的溶解,湖水Na+、Cl-浓度升高主要是因为太湖流域污水排放,特别是Cl-浓度增长很大程度上还受工业污水排放影响(表 1).
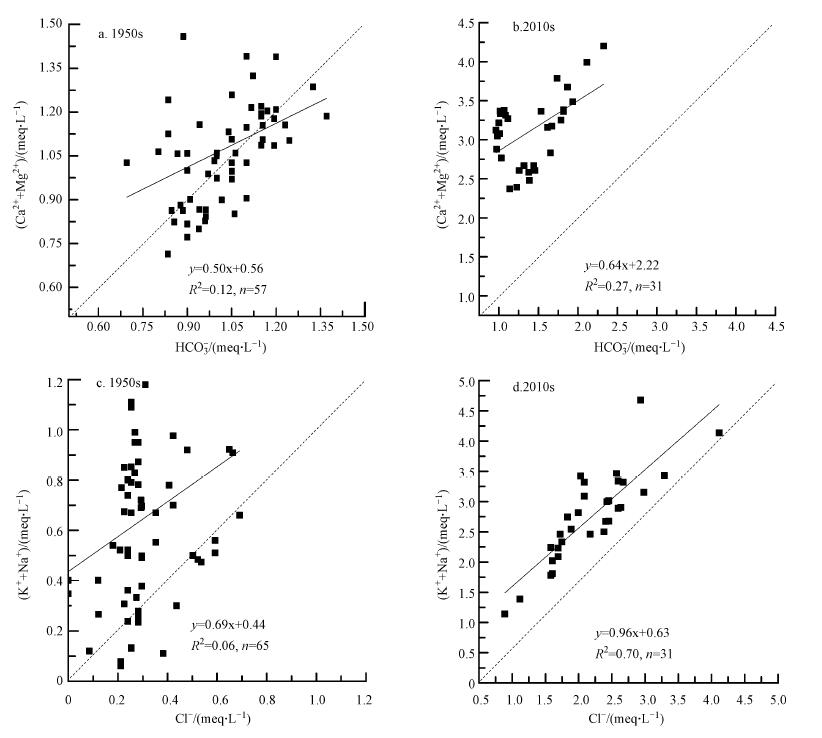 |
| 图 5 太湖水体(Ca2 ++Mg2+)-HCO3-和(Na++K+)-Cl-不同年代的对比 Fig.5 (Ca2 ++Mg2+)vs HCO3- and (Na++K+)vs Cl- at different time for Lake Taihu |
综上,与1950s年代相比,太湖水化学特征已不再是以岩石风化为主导,人类活动已经成为影响太湖水化学变化的主要原因.
4.2 太湖水体Cl-/Na+长期变化的原因和对太湖水环境的影响水体(Ca2++Mg2+)/(Na++K+)比值可以作为判别流域不同岩石风化相对强度的指标(Xu et al., 2010). 受碳酸盐岩风化控制的河流(Ca2++Mg2+)/(Na++K+)往往较高,例如,印度一些受碳酸盐岩风化控制的河流中(Ca2++Mg2+)/(Na++K+)高达5.2~11.5(Sarin et al., 1984),而受蒸发岩控制的水体其(Ca2++Mg2+)/(Na++K+)比值较低(Xu et al., 2010). 对于太湖,1950s年代的湖水(Ca2++Mg2+)/(Na++K+)平均值为2.10(图 6a),接近世界河流均值的2.2(侯昭华等,2009),而Cl-/Na+相对较小,多数情况下小于0.6. 而目前湖水(Ca2++Mg2)/(Na++K+)平均值仅为1.14(图 6b),Cl-/Na+比值(0.85)显著高于1950s年代. 充分说明自然条件下太湖水化学特征主要受碳酸盐岩溶解控制,而受蒸发岩的影响较小.
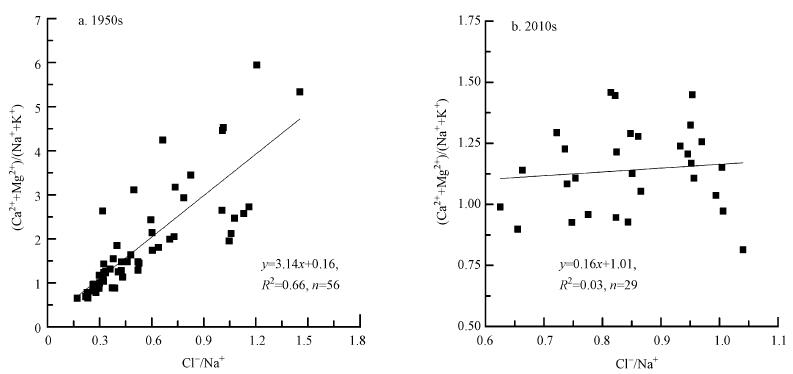 |
| 图 6 太湖水体(Ca2++Mg2+)/(Na++ K+)-(Cl-/Na+)不同年代对比 Fig.6 (Ca2++Mg2+)/(Na++ K+)vs(Cl-/Na+)of Taihu water at different time |
太湖作为淡水湖泊,自然条件下Cl-和Na+并非是湖水主要离子的优势组分.但对两种离子的长期变化趋势分析发现,它们是太湖水体中浓度最高增长最快的阴阳离子,目前已变成优势离子,且两种离子变化趋势显著相关(r=0.96,p<0.05);同时,Cl-/Na+比值也有显著的升高趋势(图 7). Chetelat等(2008)研究表明,Cl-/Na+比值升高主要是受人类活动影响,本研究的数据也充分证明这一点.
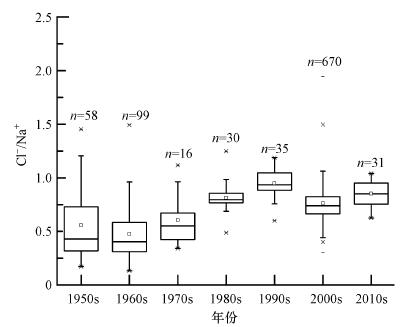 |
| 图 7 太湖水体(Ca2++Mg2+)/(Na++ K+)-(Cl-/Na+)不同年代对比 Fig.7 (Ca2++Mg2+)/(Na++ K+)vs(Cl-/Na+)of Taihu water at different time |
图 7表明,1950s年代,湖水受污水排放影响较小(Na+和Cl-主要来源于蒸发岩的溶解),Cl-/Na+比值平均值为0.58,但Cl-/Na+比值在1960s年代之后有显著升高趋势,在1990s年代末达到最高值0.98,年均增长率为0.004. 目前,Cl-/Na+比值平均为0.85,高于全球河流Cl-/Na+的中值0.68(陈静生等,2006). Chetelat等(2008)研究指出,因农业生产过程中肥料的使用,由农业输入水的Cl-/Na+比值是5,可见太湖Cl-/Na+比值增长上受农业生产影响较小. 在自然状态下,蒸发岩的溶解速率基本是一定的,长江干流Cl-浓度变化并未与海盐循环显著相关(Chen et al., 2002),而流域生活污水输入的Cl-占湖水Cl-总量的23%(Yu et al., 2013),且工业污水处理厂排放大量的Cl-(图 3),必然也是Cl-/Na+增长的一个重要原因. 由此可见,污水排放已经成为影响太湖Cl-/Na+变化的主要原因(图 3,表 1).
水体中Cl-浓度升高不仅会影响淡水水质,危及饮用水安全和人体健康(Khan et al., 2011),而且会对水环境和水生态产生不利影响(Kaushal et al., 2005). 因此,太湖Cl-和Na+浓度及Cl-/Na+比值的不断升高值得关注.
4.3 湖水总硬度变化趋势天然水体的总硬度是评价饮用水水质的一个重要指标(WHO,2008). 60年以来湖水的总硬度已经发生了显著变化(图 8),从1950s的平均55.10 mg · L-1(30.00~103.50 mg · L-1)升高到现在的155.77 mg · L-1(118.05~210.00 mg · L-1),远高于全球河流(47.1 mg · L-1)(陈静生等,2006)和鄱阳湖(40~60 mg · L-1)的总硬度(胡春华等,2011). 60年以来,太湖总硬度升高了2.83倍,年平均增长率为1.62 mg · L-1. 我国《生活饮用水卫生标准》(GB 5749—2006)总硬度的限值是450 mg · L-1,总溶解性固体是1000 mg · L-1. 总硬度和总溶解性固体的增长直接关系到饮用水的质量,目前太湖湖水总溶解性固体平均为353.43 mg · L-1,超过鄱阳湖(60~100 mg · L-1)(胡春华等,2011)的3倍,全球河流中值(65 mg · L-1)(陈静生等,2006)的6倍左右. 研究表明,长江干流天然水质受人为酸化影响的一个指标就是总硬度升高(陈静生等,1998b),湖水总硬度的升高很好地说明了人类活动引起的酸沉降对湖水天然水化学的影响.
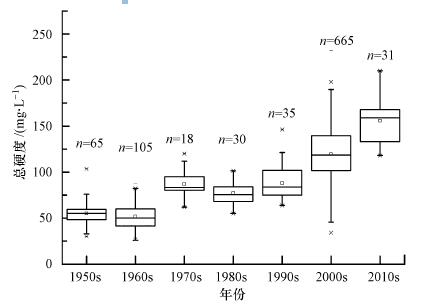 |
| 图 8 太湖水体总硬度的变化趋势 Fig.8 Long term trend of total hardness of Taihu water |
如果以目前的速率增长,湖水总硬度和总溶解性固体将分别在180年和160年之后超过国家《生活饮用水卫生标准》规定的限值,湖水将丧失其饮用水水源的功能. Kaushal等(2005)对美国东北部的淡水研究也得出类似的结论,可见这是一个具有广泛性的问题. 因此,太湖总硬度和总溶解性固体的增长应受到重视.
5 结论(Conclusions)1)太湖水体天然水化学类型受流域碳酸盐岩风化作用控制,而受雨水影响较小;60年来受流域不断升高的污水排放影响,太湖水体的优势阴阳离子组分均已发生了显著变化,阴离子中Cl-浓度超过了HCO3-,阳离子中Na+浓度超过了Ca2+,湖水天然水化学类型已从60年前的碳酸盐钙型水转变为目前的氯化物钠型水.
2)流域排放的污水主要离子特征类似于干旱地区的河水,部分工业污水甚至具有海水水化学特征. 修正的完全混合断面污染物浓度模型计算显示,生活污水排放可以解释对太湖多数主要离子的影响,而生活和工业污水的排放可以更好地解释Cl-的变化,Ca2+和Mg2+浓度增长则受污水影响较小,主要受流域酸沉降引起的碳酸盐岩溶蚀影响.
3)目前湖水(Ca2++Mg2+)-HCO3-和(Na++K+)-Cl-均分布在1 ∶ 1线上侧,而(Ca2++Mg2+)/(Na++K+)比值则下降了约1半,同时,湖水的Cl-/Na+比值显示出显著的升高趋势,说明人类活动已经成为影响太湖水化学变化的主要因素.
致谢: 感谢江苏省环境保护厅苏南环境保护督查中心在污水采样过程中给予的帮助.| [1] | Battarbee R W,Shilland E M,Kernan M,et al.2014.Recovery of acidified surface waters from acidification in the United Kingdom after twenty years of chemical and biological monitoring (1988-2008)[J].Ecological Indicators,37:267-273 |
| [2] | Brezonik P L,Arnold W A.2012.Water chemistry:fifty years of change and progress[J].Environmental Science & Technology,46(11):5650-5657 |
| [3] | Cañedo-Argüelles M,Kefford B J,Piscart C,et al.2013.Salinisation of rivers:An urgent ecological issue[J].Environmental Pollution,173:157-167 |
| [4] | 陈静生,关文荣,夏星辉,等.1998a.长江干流近三十年来水质变化探析[J].环境化学,17(1):8-13 |
| [5] | 陈静生,关文荣,夏星辉,等.1998b.长江中、上游水质变化趋势与环境酸化关系初探[J].环境科学学报,18(3):265-270 |
| [6] | 陈静生,夏星辉,洪松.2000.长江水质酸化与黄河水质浓化趋势及成因探讨[J].中国工程科学,2(3):54-58 |
| [7] | Chen J S,Wang F Y,Xia X H,et al.2002.Major element chemistry of the Changjiang (Yangtze River)[J].Chemical Geology,187(3/4):231-255 |
| [8] | 陈静生,王飞越,夏星辉.2006.长江水质地球化学[J].地学前缘,13(1):74-85 |
| [9] | 程声通,钱益春,张红举.2013.太湖总磷、总氮宏观水环境容量的估算与应用[J].环境科学学报,33(10):2848-2855 |
| [10] | Chetelat B,Liu C Q,Zhao Z Q,et al.2008.Geochemistry of the dissolved load of the Changjiang Basin rivers:Anthropogenic impacts and chemical weathering[J].Geochimica et Cosmochimica Acta,72(17):4254-4277 |
| [11] | Delpla I,Jung A V,Baures E,et al.2009.Impacts of climate change on surface water quality in relation to drinking water production[J].Environment International,35(8):1225-1233 |
| [12] | Gibbs R J.1970.Mechanisms controlling world water chemistry[J].Science,170(3962):1088-1090 |
| [13] | Heard A M,Sickman J O,Rose N L,et al.2014.20th Century atmospheric deposition and acidification trends in Lakes of the Sierra Nevada,California,USA[J].Environmental Science & Technology,48(17):10054-10061 |
| [14] | 侯昭华,徐海,安芷生.2009.青海湖流域水化学主离子特征及控制因素初探[J].地球与环境,37(1):11-19 |
| [15] | Houle D,Couture S,Gagnon C.2010.Relative role of decreasing precipitation sulfate and climate on recent lake recovery[J].Global Biogeochemical Cycles,24(4):4029-4039 |
| [16] | Hu M H,Stallard R F,Edmond J M.1982.Major ion chemistry of some large Chinese rivers[J].Nature,298(5874):550-553 |
| [17] | 胡春华,周文斌,夏思奇.2011.鄱阳湖流域水化学主离子特征及其来源分析[J].环境化学,30(9):1620-1626 |
| [18] | Huang X,Sillanpää M,Duo B,et al.2008.Water quality in the Tibetan Plateau:Metal contents of four selected rivers[J].Environmental Pollution,156(2):270-277 |
| [19] | 江苏省环境科学研究院.2008.太湖流域主要入湖河流水环境综合整治规划编制技术规范[OL].江苏:环境保护厅,http://www.doc88.com/p-9562931294785.html |
| [20] | Kaushal S S,Groffman P M,Likens G E,et al.2005.Increased salinization of fresh water in the northeastern United States[J].Proceedings of the National Academy of Sciences of the United States of America,102(38):13517-13520 |
| [21] | Khan A E,Ireson A,Kovats S,et al.2011.Drinking water salinity and maternal health in Coastal Bangladesh:implications of climate change[J].Environmental Health Perspectives,119(9):1328-1332 |
| [22] | 乐嘉祥,王德春.1963.中国河流水化学特征[J].地理学报,29(1):1-13 |
| [23] | Meybeck M.2003.Global analysis of river systems:from earth system controls to anthropocene syndromes[J].Philosophical Transactions of the Royal Society of London Series (B:Biological Sciences),358(1440):1935-1955 |
| [24] | Neary B P,Dillon P J.1988.Effects of sulphur deposition on lake-water chemistry in Ontario,Canada[J].Nature,333(6171):340-343 |
| [25] | 秦伯强,胡维平,刘正文,等.2007.太湖水源地水质净化的生态工程试验研究[J].环境科学学报,27(1):5-12 |
| [26] | 秦伯强,胡春华.2010.中国生态系统定位观测与研究数据集.湖泊湿地海湾生态系统卷.江苏太湖站:1991-2006[M].北京:中国农业出版社.157-270 |
| [27] | Sarin M M,Krishnaswami S.1984.Major ion chemistry of the Ganga-Brahmaputra river systems,India[J].Nature,312(5994):538-541 |
| [28] | Stone R.2011.China aims to turn tide against toxic lake pollution[J].Science,333(6047):1210-1211 |
| [29] | WHO.2008.Guidelines for Drinking-water Quality(3rd ed)[M].Geneva:World Health Organization.1-215; 382 |
| [30] | 夏星辉.1998.60-90年代长江水系河水水质(主要离子)变化研究[D].北京:北京大学.1-10 |
| [31] | Xu H,Hou Z H,An Z S,et al.2010.Major ion chemistry of waters in Lake Qinghai catchments,NE Qinghai-Tibet plateau,China[J].Quaternary International,212(1):35-43 |
| [32] | Yu T,Zhang Y,Hu X N,et al.2012.Distribution and bioaccumulation of heavy metals in aquatic organisms of different trophic levels and potential health risk assessment fromTaihu lake,China[J].Ecotoxicology and Environmental Safety,81:55-64 |
| [33] | Yu T,Zhang Y,Wu F C,et al.2013.Six-decade change in water chemistry of large freshwater Lake Taihu,China[J].Environmental Science & Technology,47(16):9093-9101 |
| [34] | 张自杰.2000.排水工程(第4版)[M].北京:中国建筑工业出版社.20-43 |
| [35] | 中国科学院中国自然地理编辑委员会.1981.中国自然地理-地表水[M].北京:科学出版社.155 |
 2015, Vol. 35
2015, Vol. 35


