2. 工业聚集区污染控制与生态修复教育部重点实验室, 广州 510006;
3. 华南理工大学生物科学与工程学院, 广州 510006;
4. 昆明理工大学环境科学与工程学院, 昆明 650500
2. The Key Lab of Pollution Control and Ecosystem Restoration in Industry Clusters, Ministry of Education, Guangzhou 510006;
3. School of Bioscience and Bioengineering, Guangzhou, South China University of Technology, Guangzhou 510006;
4. Faculty of Environmental Science and Engineering, Kunming University of Science and Technology, Kunming 650500
多溴联苯醚(polybrominated diphenyl ethers,PBDEs)属于溴系阻燃剂(brominated flame retardants,BFRs)的一类,由于其阻燃效率高,热稳定性好,对材料性能影响小,价格便宜,因而作为添加型阻燃剂被广泛地应用在电子、电器、化工、交通、建材、纺织、石油、采矿等领域中(Rahman et al., 2001; De Wit,2002).常用多溴联苯醚主要包括四溴联苯醚(Tetra-bromodiphenyl ether,Tetra-BDE)、五溴联苯醚(Penta-bromodiphenyl ether,Penta-BDE)、六溴联苯醚(Hexa-bromodiphenyl ether,Hexa-BDE)、八溴联苯醚(Octa-bromodiphenyl ether,Octa-BDE)及十溴联苯醚(Deca-bromodiphenyl ether,Deca-BDE)等,电器泡沫塑料中高达5%~30%的成分是含PBDEs的材料,其中用量最大的为Deca-BDE(Jessica et al., 2008).PBDEs的生产应用、物理化学性质以及毒性危害构成环境风险的综合效应,是理解环境分布与污染控制原理的重要前提.
PBDEs作为非反应性添加型阻燃剂,以物理方式结合到产品中,由于缺乏化学键的束缚作用,添加于产品中的PBDEs很容易在生产、使用以及处置过程中通过挥发、渗出等方式释放而进入环境.1981年,瑞典科学家首次在梭鱼、鳗鲡和海鳟中检出了PBDEs的存在,之后又在海鱼、贻贝、底泥中检测到了PBDEs(Andersson and Blomkvist, 1981; Watanabe et al., 1987).目前在水体、大气、土壤、动物、人体等的环境介质中都能检测到PBDEs(Akutsu et al., 2003),甚至在北极地区都能监测到PBDEs(Ikonomou et al., 2002a; Betts,2002),PBDEs在环境中的浓度在过去几十年内迅速增长.因此,人们越来越关注PBDEs在环境中的分布如何与生产场地、应用过程、生态传递、人体健康发生关系,构建全生命过程的预防和预测策略.
基于PBDEs在环境中已经暴露的浓度及其风险,点源污染控制的原位技术,不同介质中低剂量组分的分离与毁毒技术,都有可能依赖于对象体系相互作用的分子性质.各国环境学者开展了一系列关于PBDEs的降解研究,其中主要有生物法(Andreas et al., 2005; Tokarz et al., 2008; Chang et al., 2012; Kim et al., 2007)、光化学降解法(Eriksson et al., 2004; Bendig and Vetter, 2010; Kuivikko et al., 2007)以及零价铁还原法(Keum and Li, 2005; Shih and Tai, 2010; Lin et al., 2012)等.这些研究过程主要是基于PBDEs分子的化学结构与物理性质,通过酶促反应、光催化氧化以及零价铁还原反应来实现C—Br取代和C—C断裂.PBDEs不与基质材料形成化学键,电子废弃产品的堆放与拆解场地容易成为污染源,通过各种途径释放到土壤、河流水体及沉积物中,在鱼、哺乳动物、人血浆和母乳中被检出,表明了存在生物富集作用(Ward et al., 2008).当前,PBDEs的致毒机制和免疫毒性效应虽还未被完全了解,但关于PBDEs对人类的健康和环境的危害已有大量报道.PBDEs进入环境随着介质迁移并富集,最终通过一些途径进入人体并危害人类的健康,包括引起肝脏毒性、内分泌干扰、生殖和神经发育毒性等,严重的还会引起致癌(Vonderheide et al., 2008).因此,点源、面源与生态过程的污染控制与防范技术需要深入思考.
研究工作的有效性如何建立在PBDEs的基本化学性质、各种环境中的分布、不同介质中控制方法原理的针对性与可行性的结合.本文从分子性质,环境不同介质浓度分布,厌氧/好氧的生物降解、光化学氧化、零价铁还原的化学过程3个方面讨论PBDEs的来源特征、环境分布及污染控制.作为分析的案例,把电子垃圾塑料中PBDEs的原位回收与销毁、水体中微量或衡量浓度成分的富集分离、超临界水氧化作为单元技术如何结合起来解决一个具体的环境问题,构想PBDEs全程回用与无害化的技术方向.
2 PBDEs的来源与分子性质(Source and molecular property of PBDEs) 2.1 PBDEs的来源PBDEs作为阻燃剂,其阻燃机理是:高温下,PBDEs分解产生强还原性的溴原子,可以捕获 · OH和O · 等燃烧反应的核心游离基,同时,· Br易形成HBr,在氧化过程中能隔离氧,从而使氧化过程难以进行,进而达到阻燃灭火的目的(Rahman et al., 2001).PBDEs被大量生产并用于聚合物中作阻燃剂,尤其在电器制造(电视机、计算机线路板和外壳)、建筑材料、泡沫、室内装潢、家具、汽车内层、装饰织物纤维等.虽然PBDEs有209种同系物,但商品中PBDEs的种类是有限的,常见的PBDEs阻燃剂工业品主要有3种:
(1)Penta-BDEs
Penta-BDEs阻燃剂产品的主要构成部分为2,2',4,4'-四溴联苯醚(BDE-47)和2,2',4,4',5-五溴联苯醚(BDE-99).Penta-BDEs阻燃剂主要用于环氧树脂、酚类树脂、聚酯、聚氨酯泡沫以及纤维中.当前,为了增加家具的防火安全性,大部分添加Penta-BDEs的聚亚胺酯和聚氨酯泡沫用于室内装潢和家具制作,其添加含量为10%~30%.
(2)Octa-BDEs
白色粉末,主要由六、八溴联苯醚单体组成,熔点约为200 ℃,可在>330 ℃时分解,在水中溶解度低,可溶于丙酮(20 g · L-1)、苯(200 g · L-1)和甲醇(2 g · L-1)中.Octa-BDEs主要用于丙烯睛-丁二烯-苯乙烯树脂、聚碳酸酯和热固塑料中,作为电话、传真机、台灯等小家电外壳、电器接插件、汽车零部件和一些办公用具生产的原材料,添加量范围为12%~18%.
(3)Deca-BDEs
白色至淡白色结晶粉末,是一种目前使用最广泛的高效添加型溴代阻燃剂,主要由九、十溴联苯醚单体组成,具有添加量少,阻燃性强、热稳定性高等特点.Deca-BDEs主要添加于各种纺织品和电路板聚酯中(电视、电脑等电子产品).
迄今,PBDEs阻燃剂的产量依然保持上升的趋势,据报道,1990年世界上阻燃剂的年产量是60万t,其中含溴的阻燃剂是15万t,PBDEs是4万t.8个生产PBDEs的公司分布在法国、英国、以色列、日本、荷兰和美国.1999年世界上PBDEs的需求量超过6万t.2001年世界市场供应Deca-BDEs 46500 t,Octa-BDEs 12000 t,Penta-BDEs 7500 t.2008年,世界Deca-BDEs产量增至65000 t,Octa-BDEs 18000 t和Penta-BDEs 9800 t.由于意识到PBDEs的环境危害性,近几年的产量维持在基本稳定并成下降趋势.
2.2 PBDEs的分子性质 2.2.1 PBDEs的物理性质PBDEs的物理性质主要涉及溶解性、密度、颜色、气味、挥发性、熔点、沸点、导热性和导电性等方面,其中,溶解性、分子密度、导热性以及导电性对PBDEs在产品中的应用影响较大,制约其在环境中的迁移转化行为,影响其在各环境介质中的含量分布.PBDEs的沸点为310~425 ℃,通常为可燃的液体,在电子塑料外壳中通过固化剂与塑料分子紧密结合,在垃圾拆解过程中容易被释放进入大气、水体和土壤环境.PBDEs在室温下蒸气压较低,具有一定的挥发性,可以散逸到空气中,并随大气长距离迁移.PBDEs还具有脂溶性、高蓄积性和环境持久性,可以随着食物链富集放大,最终进入人体并危害人类的健康(Rahman et al., 2001).
PBDEs在水中溶解度很小,主要与其正辛醇/水分配系数(logKow)有关,大多数在2~10之间,且logKow随着溴原子数增加而增加,溶解度随着溴原子数的增加逐渐减小(Chen et al., 2008),能溶解于有机溶剂如甲苯和正己烷等介质中,水中的PBDEs主要通过附着颗粒进行迁移转化.包含PBDEs的塑料本身不具有导电性,导热性也差,PBDEs分子具有吸收光、电、波等特性.微波、超声波、等离子体放电等能使极性分子发生剧烈振荡,促使化学键断裂,还能使极性分子发生高速旋转碰撞从而产生热效应,改变体系的热力学函数,降低反应活化能和分子的化学键强度.将微波、超声波等技术与其它化学手段结合用于PBDEs的降解,能达到协同效应,可以加快反应速度,提高反应处理效率(黄俊等,2001; 肖松文和肖晓,2006).PBDEs的物理性质主要是控制着其在环境介质中的存在状态和迁移方式,从而决定着修复过程提取方式的选择.PBDEs具有相当稳定的化学结构,很难通过普通的物理、化学或生物方法降解,在一定条件(如燃烧)下,可形成毒性更强的多溴联苯二 英以及多溴代二苯并呋喃等物质.将PBDEs的物理性质归纳于表 1中.
| 表 1 PBDEs各同系物的物理性质 Table 1 The physical properties of PBDEs |
PBDEs的化学性质主要包括分子的稳定性、可燃性、酸碱性、氧化性、还原性、腐蚀性和脱水性等.PBDEs的化学通式为C12H(0-9)Br(1-10)O(其中氢原子和溴原子之和为10),是一类包含有209种同系物的溴代二苯醚类化合物.PBDEs分子结构如图 1所示,两个苯环之间由共轭键(C—O—C)相连,溴原子和苯环之间又形成p-π共扼(C—Br)键,特殊的结构使各个键之间的链接非常牢固,分子中平均键能达到488.6 kJ · mol-1,决定了它具有非常稳定的理化性质,很难通过一般的氧化反应破坏PBDEs的化学键(Chen et al., 2008).PBDEs按IUPAC编号系统编号,在PBDEs的209种同类物中,有6种化合物被科学家研究得最为普遍和深入,它们分别是BDE-47、BDE-99、BDE-100、BDE-153、BDE-154和BDE-209.在化学结构上,PBDEs与多氯联苯(PCBs)和DDT相似,它们的化学性质、环境中的持久性和分布情况也是相似的.
从图 1中可以看出,PBDEs是一类芳香卤代醚,分子键包括C C、C—C、C—O—C、C—Br、C—H等化学键,表 2列出了各键的键长和键能,其中C—O键最短,键能最大,达到748.9 kJ · mol-1,最难断键,C—Br键能最小,为284.5 kJ · mol-1,相对最易被破坏.由分子性质还可知,PBDEs在微生物、光照射等作用下能发生脱溴反应,生成低溴代产物,但由于电子传递速率慢,限制因素多,自发性的脱溴反应速度较慢,随着溴原子数的减少,反应进行难度变大.
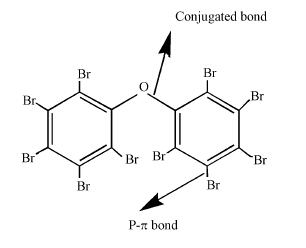 |
| 图 1 PBDEs的化学结构简图 Fig. 1 The chemical structure of PBDEs |
| 表 2 PBDEs分子键长及键能 Table 2 Molecular bond length and energy of PBDEs |
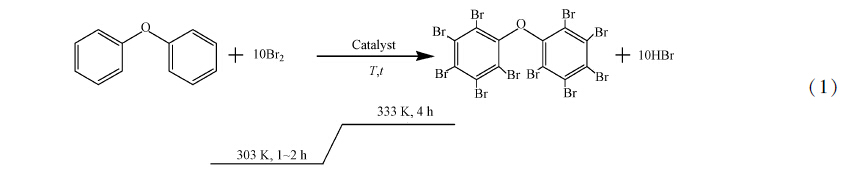
常用的多溴联苯醚主要是以联苯醚作为材料与溴合成得到的.PBDEs分子中C—Br键键能低于C—H键,键长更长,将Br取代H需要提供大量的热,该反应时间较长,通常需要使用适当的催化剂(黄俊等,2001).以十溴联苯醚为例,PBDEs合成反应式表示为式(1).
PBDEs的阻燃性并不能说明PBDEs不能发生氧化还原反应.有研究报道,在850 ℃以上的温度条件下,PBDEs可以发生氧化反应,即通过火焰燃烧破坏分子结构,随着分子中溴原子数的增加,其需要的完全燃烧温度越高,不过,燃烧过程中很容易产生多溴联苯二 英以及多溴代二苯并呋喃等剧毒物质,反应难以控制,并且设备要求高,能耗大,安全防范难(黄俊等,2001).是否存在低温燃烧的催化反应以及可能的环境条件实现PBDEs的污染控制是值得探索的问题,分子性质起着决定性的作用.区别对待PBDEs的阻燃化学性质、化学分解性质、生物降解性质,就有可能调控其生产应用与环境管理.
在PBDEs的毒性研究中,动物实验相对较多,针对职业人群的研究正在广泛化,但已经积累的数据对于解释现象还欠充分.体内和体外实验初步揭示,PBDEs的健康危害包括肝脏毒性、内分泌干扰作用、生殖和神经发育毒性、致癌等.不同PBDEs同系物的健康危害差异性很大.商业产品中工业五溴联苯醚毒性最大,在很低的剂量下就可以引起毒性,而十溴联苯醚则需很大剂量才能表现出毒性.老鼠和兔子的敏感性研究发现,五溴联苯醚的影响主要是对神经系统的损害,浓度在0.6~0.8 mg · kg-1表现出毒性,浓度在6~10 mg · kg-1表现出对后代的甲状腺激素的破坏; 八溴联苯醚浓度大于2 mg · kg-1开始会引起对胎儿的毒性和致畸性,浓度越大,引起毒性危害也越大; 十联苯醚浓度大于80 mg · kg-1时对成熟动物的甲状腺、肝和肾都会引起形态的改变(Vonderheide et al., 2008).目前,PBDEs对人类的危险评价是建立在动物模型基础上的,人体组织中PBDEs的含量是否己达到对人类健康造成危害的水平还处在不确定的阶段.人类每天摄入PBDEs的量远低于对动物产生影响的最低剂量,这两种剂量相差106倍.由于研究PBDEs在人体内的毒理动力学的数据很少,如果基于人体的承受水平或PBDEs在某个器官中的浓度来评价,可能对于人体的真正的安全限值会更低.与此同时,高溴代的联苯醚降解为低溴代的联苯醚或其它溴代有机物时,毒性可能会增大或产生其他毒性效应也是非常难以确定和敏感的问题.
PBDEs可在动物体内蓄积,在鼠类脂肪组织中的半衰期为19-119 d.STASKAL等观察了小鼠连续染毒状态下的代谢动力学特点.他们将1.0 mg · kg-1的BDE-47经口连续5 d染毒小鼠,分析BDE-47在体内分布与排泄特点.发现与单次染毒相比,连续染毒状态下,BDE-47在体内呈非线性分布,体内停留时间更长,脂肪组织中蓄积更多、排泄更少.表明连续暴露可以造成更多的体内蓄积和更持久的毒性.PBDEs的肝脏毒性表现为肝微粒体酶活性诱导、肝肿大、退行性组织病理学改变和肝癌(Rahman et al., 2001; Covaci et al., 2007).
己有充分的实验证据,一些PBDEs同系物是内分泌干扰物,可干扰甲状腺激素和性激素,慢性染毒可导致大鼠甲状腺肥大.由于PBDEs的分子结构与甲状腺激素T3和T4非常相似,一些PBDEs同系物可以增强、降低或模仿甲状腺激素的生物学作用.无论是低溴联苯醚还是高溴联苯醚的暴露,均可以引起甲状腺激素失衡,影响其功能.一些PBDEs具有雌激素和雄激素干扰作用,但研究结论不一致.在神经发育早期,暴露于PBDEs环境中可损害感觉运动、学习与记忆、自主行为发育.PBDEs染毒新生小鼠可导致成年鼠自主行为、学习和记忆能力的持久改变,成年期可发生神经行为改变,在非常低的暴露水平下(相当于人类实际暴露水平的6~29倍),BDE-99也可以导致子代小鼠神经发育障碍,表现为活动亢进.PBDEs至少可能通过3个途径影响脑发育,即甲状腺激素干扰、第二信使信号干扰、神经递质改变(De Wit,2002; Chen et al., 2012).
PBDEs的毒性效应研究还非常有限,主要针对单一因素,即PBDEs自身,尚未进入到复杂体系.PBDEs与其他污染物之间的联合作用以及污染物的剂量-效应之间的关系等应当能够给出更多不同的结果.
3 PBDEs的环境分布(Environmental distribution of PBDEs) 3.1 沉积物基于PBDEs的疏水性以及沉积物的附着性强的特点,河口和海湾中的沉积物可能成为PBDEs归趋的主要场所,是目前各类刊物大量报道PBDEs含量数据和时间趋势的原因.当前,世界范围内的河流、湖泊和海洋沉积物中PBDEs都已经被检出,这点必须引起注意,然而不同地区沉积物中PBDEs含量差异较大,由未检出到数万纳克.欧洲地区沉积物中PBDE含量较高,虽然北美是五溴联苯醚的最主要使用地,但北美沉积物中的PBDEs含量却相对较低(Gallego et al., 2007; Allchin et al., 1999; Samara et al., 2006; Hale et al., 2003).亚洲沉积物中PBDEs污染水平总体上低于欧洲和北美,但高浓度的PBDEs也相继被报道在污水排放区和电子废弃物污染地区(Wang et al., 2007; Luo et al., 2007; Moon et al., 2007).沉积物中PBDEs的来源较复杂,受纺织厂、PBDEs制造厂及大量使用的企业、污水处理厂出水、电子电器废弃地等影响较大.沉积物中发现PBDEs同系物的指纹特征通常和工业产品极为相似,一般以BDE-209最高,BDE-47、BDE-99等低溴代联苯醚也常被检出(Jin et al., 2008).此外,长距离大气迁移后的干湿沉降也被发现是沉积物中PBDEs的重要来源(Cetin et al., 2009).可能存在更多的迁移模式尚未被研究者发现.
不同地区沉积物中PBDEs污染时间趋势是科学家们的一个兴趣点.20世纪80年代以来,波罗的海南部沉积物中四溴联苯醚增长了4~8倍,五溴联苯醚增长了10~20倍.美国密执安湖和伊利湖中BDE-209的倍增时间分别为7.5年和5.3年,其它PBDEs总含量倍增时间也仅为11.4年和6.4年,大湖沉积物中PBDEs沉积通量也呈指数增长,其中三到七溴联苯醚的倍增时间为9~43年(Zhu and Hites, 2005; Li et al., 2006).由于PBDEs继续大量生产和使用以及进口电子产品废弃物,亚洲沉积物中的PBDEs增长趋势更明显.中国珠三角电子产业高速发展,珠江口沉积物中BDE-209的含量及通量从1990年以后快速增加,倍增时间仅为2.6~6.4年(Chen et al., 2007).PBDEs的环境问题正在蔓延全球,我国必须高度警觉.
3.2 水体由于PBDEs的水溶性较低以及水体的流动性,水相中PBDEs含量的报道缺乏统计性.已有的研究表明自然水体中PBDEs含量一般不高,多为未检出到几百皮克,较高的浓度一般出现在污水处理厂出水和河口地区(Nylund et al., 1992; Wurl et al., 2006).Oros等(Oros et al., 2005)调查了旧金山河口区水、颗粒物和沉积物中PBDEs的含量与分布情况,水中主要含有BDE-47,BDE-99和BDE-209,浓度范围在3~513 pg · L-1,浓度最大值出现在高度城市化的南部海域(103~513 pg · L-1),浓度最小值则是在城市化程度很低的北部海域(3~43 pg · L-1),其中BDE-209主要通过吸附在悬浮颗粒上而存在.Booij等(Booij et al., 2002)用半透膜被动采样的方法研究了北海荷兰近海和斯凯尔特河河口水相浓度,浓度范围为0.1~9.0 pg · L-1,最高浓度出现在斯凯尔特河河口; 目前全世界研究的结论基本一致,水中PBDE主要集中在悬浮颗粒物中,悬浮颗粒物成为了PBDE的主要载体.Kuch等(Kuch et al., 2001)发现德国污水处理厂污水中BDE-47和BDE-99的浓度达到1.1 ng · L-1,其中污水中97%的PBDEs是和悬浮颗粒物结合的.Deboer等(De Boer et al., 2003)全面调查了荷兰不同地点悬浮颗粒物和污水处理厂出水中PBDEs,发现悬浮颗粒物是高溴联苯醚的主要载体,沿岸纺织工业使用阻燃剂的泄露和上游污染是悬浮物中BDE-209的主要贡献者.北美水中PBDEs分布与欧洲大体相似.Stapleton等(Stapleton and Baker, 2001)发现Michigan湖中上覆水PBDEs的总浓度从1997年的0.03 ng · L-1上升到1999年的0.16 ng · L-1,仅次于水中PCBs水平.Ikonomou等(Ikonomou et al., 2002b)用半透膜研究了加拿大Fraser River 中PBDEs同系物组成,获知BDE-47占主要的成分,BDE-99和BDE-100次之,BDE-209没有检出.一般情况下,BDE-47和BDE-99通常是水相PBDEs最主要组成,工业废水、污水处理厂出水以及其它未经处理废水通常是水中PBDEs污染的主要来源.基于点源、城市源为对象的连续监测仍然是未来工作的难点.
3.3 大气大气环境中PBDEs的污染取决于电子产品的普遍存在与PBDEs分子固有的挥发性.在气相环境中监测到低溴代联苯醚并发现其远距离迁移的现象,高溴代联苯醚如BDE-209容易结合在空气中的粉尘颗粒上,也能进行近距离迁移.大气运动会影响空气中PBDEs浓度,而平流更是控制空气中PBDEs浓度的主要原因.夏季时温度对空气中PBDEs的浓度有巨大的影响,大气表面交换过程起着重要作用; 在冬季,平流是影响PBDEs浓度的更主要的因素.夏天检测到空气中PBDEs浓度普遍高于冬天,认为温度是影响空气中PBDEs浓度的因素,高温还提高PBDEs的挥发性,同时改变土壤的条件,影响了吸附/解吸作用,使原来吸附在土壤中的PBDEs又解吸回到空气中(Wilford et al., 2004; Harrad et al., 2006).
从已报道的监测数据看,室外空气中PBDEs的水平在5~300 pg · m-3,城市高于农村地区.现代人每天有80%以上的时间是在室内度过,室内空气中PBDEs的暴露成为大气中PBDEs研究的重点.加拿大的监测发现,普通居民家庭室内空气PBDEs的平均浓度约为100 pg · m-3,是室外浓度的约50倍,这些家庭室内灰尘中PBDEs的含量平均为1800 ng · g-1(Wilford et al., 2005; Lee et al., 2004).表明PBDEs室内浓度分布与室外分布存在显著差异.室内空气和灰尘是重要的暴露来源,对室内活动时间相对多的儿童非常有害.Stapleton等(Stapleton et al., 2005)测定华盛顿家庭室内灰尘中总PBDEs含量为780~30100 ng · g-1干重,儿童通过灰尘摄入的PBDEs约为120~6000 ng · d-1,特别对初学走路的孩子,根据体重的不同,可能摄入大约100 mg · d-1的室尘(相对于成人50 mg · d-1).Deng等(Deng et al., 2007)检测广东贵屿大气灰尘,测定了22种同系物,PBDEs总量为1618 ng · m-3,其中毒性最强的低溴代联苯醚占79.14%~95.16%,总量是对照组的58~691倍.
室内空气中PBDEs含量一般高于室外,这是由于室内装饰材料、家具和电器中大都添加PBDEs作为阻燃剂,在使用过程中随温度变化等因素而不同程度地逸散到空气中.Wilford等(Wilford et al., 2004)比较了墨西哥城区、瑞典的哥特堡和英国兰卡斯特室内和室外空气中PBDEs的浓度,也发现室内污染物浓度明显高于室外.一般情况下,室内空气中的PBDEs浓度普遍比室外高出1~2个数量级,室内通风显得非常重要.
3.4 水生生物水生生物能够通过食物链,或者直接从水和沉积物中吸收并富集可生物累积的污染物.在水生生物体内,从浮游动植物到海洋哺乳动物,PBDEs均被检出(Kajiwara et al., 2006; Johnson-Rstrepo et al., 2005).由于生物种类不同和地区差异,生物体内PBDEs含量差异较大,一般在ng · g-1~μg · g-1脂肪范围内.研究发现,水生生物体内PBDEs同系物组成极为相似,以BDE-47、BDE-99、BDE-100、BDE-153、BDE-154为主,其中以BDE-47为最高,一般占总PBDEs的50%以上.这种相似性可能是由于生物对4~6溴联苯醚吸收强且代谢慢,生物富集性强(Wolkers et al., 2004; Burreau et al., 2004)有关,也可能为高溴代BDE降解为低溴代BDE所致.Bragigand 等对幼小鲤鱼的BDE-209食物暴露研究中也发现了BDE-209能脱溴生成低溴代联苯醚,对其体内的BDE-99和BDE-183进一步研究时发现其发生了脱溴反应,产物分别是BDE-154和BDE-47(Bragigand et al., 2006).不同生物以及生物体内不同部位的PBDEs富集效应是值得深入研究的方向.
3.5 人体PBDEs在大气环境及水生生物中普遍存在,人类暴露其中且存在于生物链的末端,人体内富集了PBDEs并且逐渐诱发体征效应.到目前为止,PBDEs在人体脂肪、母乳和血清中都能被检出.几乎所有的人都暴露在低剂量的PBDEs下,人体内PBDEs的浓度范围大致是1~400 ng · g-1脂肪.Oros(Oros et al., 2005)报道在电子垃圾高风险区工人血清中BDE-209最高达3436.3 ng · g-1.斯德哥尔摩大学环境化学部的Thuresson等(Thuresson et al., 2006)随机检测了有职业暴露的工人体内最先出现浓度高峰的是高溴类的PBDEs,认为BDE-209是人类最常见暴露的PBDEs,但BDE-209在人体中的半衰期短,可能更容易转化为低溴类的PBDEs,对于BDE-209的危害性应该重新评估.PBDEs具有生物累积及生物放大效应,人体中的浓度也在不断增长.在人类与PBDEs接触的约25年时间里,PBDEs在人体内的浓度水平已经增长了100多倍.虽然目前的环境暴露浓度还不会导致明显的健康影响,但很多因素可能会很快加速这个过程,对于PBDEs强暴露区域的敏感人群如孕妇,发育中的胎儿、婴儿等将存在重大的遗传与健康隐患.
人体中的PBDEs主要来源于饮食摄入、母乳摄入和呼吸摄入.对于一般人群来说,食物摄入被认为是PBDEs进入人体内的最主要途径.PBDEs的最高浓度出现在鱼和肉、油等脂肪含量高的食物以及一些动物的肝脏内(Schecter et al., 2006).在北美,肉和油脂是主要的食物.Frederiksen(Frederiksen et al., 2009)发现禽肉和肉制品占美国人饮食摄入PBDEs总量的60%~70%,而通过鱼的摄入仅仅占10%~20%.蔬菜中也含有PBDEs,Ohta等(Ohta et al., 2002)的实验表明蔬菜叶会吸收空气中PBDEs,虽然蔬菜中PBDEs的浓度较低,但是通过蔬菜摄入到人体的PBDEs的量也不能忽视.由此看来,我们在日常饮食中难免会摄入PBDEs.PBDEs进入人体的另一个来源为呼吸摄入,含PBDEs的家具及电子电器产品例如电脑、电视机、电冰箱等在使用过程中会释放PBDEs,必须引起注意.
4 PBDEs的污染控制(Pollution control of PBDEs) 4.1 PBDEs生物降解微生物细胞将污染物吸收后在细胞内通过功能酶促反应实现目标物的氧化或是还原而脱毒,直至彻底矿化或甲烷化,好氧和厌氧作用过程的结合是微生物降解有机物的最好手段.目前,PBDEs的生物降解菌种已经被分离出来.其中,厌氧微生物通过还原酶作用于高溴代同系物PBDEs分子的C—Br键,使PBDEs分子得到电子的同时释放出溴离子,转化为低溴代同系物后易于进一步降解.在厌氧环境中,由于氧化还原电位较低,电子云密度较低的苯环在酶的作用下易受到还原剂的亲核攻击,溴原子容易被亲核原子取代(Gerecke et al., 2005).微生物厌氧降解BDE-15的途径如图 2所示(Sierra et al., 2003).好氧降解则是通过羟基化或甲基化分解PBDEs,主要代谢途径是通过2,3-双加氧酶攻击2,3-碳键,生成2,3-二羟基联苯醚,然后邻位或间位裂解开环(Pfeifer et al., 1993).微生物降解PBDEs的过程中,分子的溶解性和氧化还原电位起决定作用,分子结构和溴原子数影响降解过程,键能是关键参数.在污染物混合体系中,还需要考虑PBDEs与其他分子的作用力,体现在溶解度与水合键能的差异性.Trametes Versicolor菌降解4-PBDE的路径如图 3所示(Hundt et al., 2000).
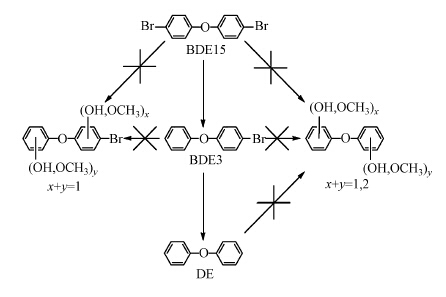 |
| 图 2 厌氧生物降解BDE-15的途径 Fig. 2 Anaerobic biodegradation pathway of BDE-15 |
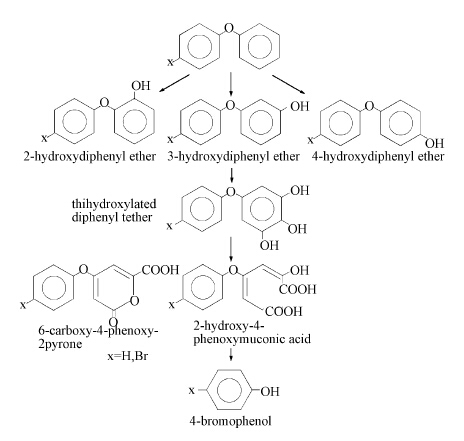 |
| 图 3 T. versicolor.降解4-BDE的途径 Fig. 3 The degradation pathway of 4-BDE by T. versicolor. |
表 3归纳了PBDEs生物降解的一些最新报道.研究的基本思路是从被污染的土壤和河流沉积物的微生物中筛选和驯化降解PBDEs的功能菌种,通过大量繁殖并且强化功能,再将其应用于污染修复.高溴代PBDEs的生物降解产物多为低溴代物,当降解的起始物为低溴代醚时,通过专性好氧降解菌作用则可以完全脱溴生成联苯,或是开环生成其它中间代谢产物.从不同污染水体、沉积物、土壤或是污泥中筛选出的微生物的功能存在差异,发现从污染程度高的环境中筛选出来的微生物其酶活性也高.当环境存在复合污染,单种功能微生物的降解效果差或是被抑制,共基质效应或是多种功能菌协同修复,更适合于含PBDEs的实际环境.
| 表 3 PBDEs生物降解最新研究进展统计 Table 3 The statistics of the latest research progress on biodegradation of PBDEs |
PBDEs的生物降解速率通常是随着溴取代原子的数目的增加而降低,在有外源强化物质加入时,其降解速率会不同程度的增加,如果在两个苯环上都有溴取代,PBDEs携带溴原子较少的苯环优先通过羟基化或甲基化开环,在没有取代基的环上更易发生开环.PBDEs的好氧降解过程相对于厌氧过程其速率通常会高些,厌氧降解通常需要添加共代谢底物,且厌氧还原脱溴的难易程度与溴的取代位点有关,脱溴的优先顺序一般是间位>对位>邻位,PBDEs生物降解普遍遵循一级反应动力学(郭杨和王世和,2008).容易理解,溴取代数决定了分子内原子间的键能大小,分子溴数越多,结构越紧密,破坏分子所需要的活化能就越高,产生的中间产物也越多,完全矿化需要的降解能也会越多.
PBDEs生物降解主要的优势在于成本低,不需要复杂的操作,也不需要外界能源的加入.在水污染控制中,PBDEs由于其强的疏水性而附着在悬浮物上,增加了与微生物的接触,有利于微生物的吸收.生物降解需要考虑的因素包括微生物的活性、菌落结构、电子给体、共基质溶剂等.已经证明,细胞融合技术、酶的固定化技术、活性酶分子亚基置换与定点突变技术、代谢途径的基因改造等分子生物学手段能够使PBDEs的降解成为可能.随着PBDEs在生态环境中的普遍检出,基于PBDEs分子结构特征阐明的生物降解强化机理包含微生物对对象污染物的捕获与传质、共基质原理、酶活因子识别、转化与脱毒等的研究,为解决污染问题提供创新的空间.
4.2 PBDEs光化学分解光化学分解是污染物分子吸收光子使电子激发,分子由基态提升到激发态,而引起物质自身分解或是与其他物质发生化学反应,反应活性取决于PBDEs分子的氧化还原特性.分子激发时的初始状态与终止状态不同时,所要求的光子能量也不同,光子的能量ε=hv=hc/λ(h为普朗克常数; v为光频率; λ为光波长; c为光速),所以,需要寻找与PBDEs分子能量匹配的一定波长的光.PBDEs的光化学降解研究较为广泛,原因是在UV-B(280~315 nm)和UV-A(315~400 nm)段光谱波长范围内,PBDEs能吸收光子而获得能量,在光与催化剂的协同作用下,实现C—Br键的断裂与氢取代反应,最终实现逐级脱溴(Bezares-Cruz et al., 2004).图 4为PBDEs光反应脱溴路径(Bieniek et al., 1989).也有报道说,PBDEs能被光直接催化氧化,只是PBDEs的强疏水和亲脂性,需要选择适合的媒介溶剂(Kuivikko et al., 2007).影响光化学降解PBDEs的因素较多,包括光源及强度、反应媒介溶剂、PBDEs附着物和PBDEs的分子性质等.
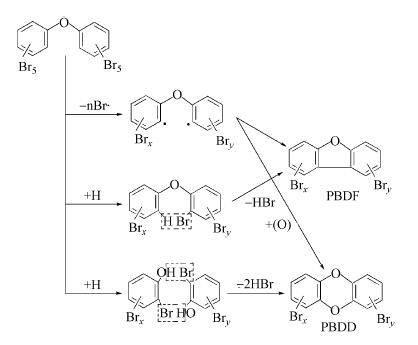 |
| 图 4 PBDEs光反应脱溴路径 Fig. 4 Debromination pathway of PBDEs by photoreaction |
光源及光强和反应媒介溶剂对PBDEs光解影响较大,光强决定供给反应的能量,而反应媒介与分子性质中的密度和溶解性关联,影响分子的附着状态,媒介溶剂还决定传递电子的速率,通常,二者对光解反应的影响是交互的.Watanabe等(Watanabe and Sakai, 2006)比较了光源对十溴联苯醚降解在混合体系(正己烷、苯、丙酮的体积比为8 ∶ 1 ∶ 1)中的影响.发现汞灯和太阳光下光解产物主要为低溴代PBDEs,还有少量PBDFs生成,使用汞灯时,生成的PBDFs为一至五溴取代物,最大产率约20%,而太阳光照射时,生成的PBDFs为一至四溴取代物,最大产率约10%.Rayne等(Rayne and Ikonomou, 2009)研究了BDE-153在乙腈溶剂中紫外光照射下的降解效果,发现其先脱溴得到BDE-99、BDE-101和BDE-118等3种五溴联苯醚,再脱溴得到BDE-47、BDE-49、BDE-66和BDE-77等4种四溴联苯醚,还有少量一至五溴取代的PBDFs和四溴-2-羟基联苯的生成.
PBDEs附着物对其光解也有很大影响,由于PBDEs疏水性强,需要选择适合的吸附材料.Kajiwara等(Kajiwara et al., 2008)进行BDE-209太阳光降解,假设过程为一级反应,按动力学方程〖BDE-209〗t =〖BDE-209〗0e-kt估算,溶液中或附着在颗粒表面的BDE-209降解半衰期为51 d,当PBDEs以聚合物形式存在,或与其他高分子有机物混合,将减少与光接触的表面积,半衰期延长.Ahn(Ahn et al., 2011)等研究了吸附在6种固态基质上的BDE-209紫外光照分解反应,发现蒙脱石和高岭石表面BDE-209能够发生脱溴反应生成三溴至九溴产物,半衰期分别为36 d和44 d,而在自然沉积物表面其脱溴反应速率较慢,半衰期为150 d,吸附在氢氧化铝、氢氧化铁和二氧化锰表面不会发生分解,认为由于后三者属于单纯吸附,不具有二氧化硅的吸收紫外光特性,因而不会发生紫外光降解.
PBDEs分子的含溴数和溴代结构的差异在光解反应中表现出不同的途径,分子的稳定性以及键能的差异性决定了PBDEs脱溴是一个逐级脱溴的过程.溴取代数和不同溴取代位置PBDEs的光解半衰期相差较大,原因是溴取代数大时,其结合力相对较弱,容易断键,随着溴取代数的减少,反应需要的活化能升高,反应变得缓慢.分子内多种能级的存在使PBDEs光解产生系列低溴代产物.Lucia等(Sanchez-Prado et al., 2005)用紫外光降解5种PBDEs(BDE-47,BDE-99,BDE-100,BDE-153,BDE-154),获知BDE-153最先被光解,其次是BDE-154,反应1 h的产物是BDE-47,符合一级动力学.Schenker U等(Schenker et al., 2008)利用模型分析证明了光解能形成大量的低溴代联苯醚,计算了环境中PBDEs的浓度.根据模型估计,环境中大约有13%的五溴联苯醚和2%的四溴联苯醚来自十溴联苯醚的光降解.可见,研究PBDEs的降解时,需要考虑中间产物的毒性和危害,要求完全毁毒.
近年来,PBDEs光解的研究逐渐深入到源污染控制,比如汽车尾气、纺织棉物品和冰川中.Anthony F. Lagalante等(Lagalante et al., 2011)采集了66个私人汽车尾气样品,分析其中PBDEs的含量,发现其中主要以BDE-209为主,平均含量为8.12 μg · Nm-3; 以汽车尾气为对象进行光解,56 d后BDE-209并没有减少,当用硫酸钠吸收尾气后,发现却有BDE-209光解反应发生.Raed Ghanem等(Ghanem and Delmani, 2012)研究了纺织品中BDE-209的光解,发现其降解速率很慢,起始质量分数分别为8.4%、24%、39.4%、28.5%时,每天的降解速率分别是3.60×10-3,1.03×10-2,3.60×10-2和3.94×10-2,反应符合一级动力学.Lucia Sanchez-Prado等(Sanchez-Prado et al., 2012)研究了冰固体样品中的BDE-100的光降解反应,发现其降解规律和在液相中相似,符合一级动力学,并且是逐级脱溴,产物形成HBr并溶于水.
光降解PBDEs的半衰期较长,通常几天甚至几十天,降解不彻底且效率较低,因此,催化剂及载体促进光解效率的研究越来越被重视.Chunyan Sun等(Sun et al., 2012)利用BDE-209的强疏水性,在水溶液中TiO2表面进行光解,以甲醇为电子供体,发现底物降解快速,反应受pH的影响很小,TiO2表面的H+/OH-加快电子传递,加快反应速度.An等(An et al., 2008)将TiO2与蒙脱石负载在一起,从而增加疏水性物质的亲和力,制备一种兼具吸附与光催化作用的材料,以BDE-209为模型污染物,发现其降解速度大大提高,3 h能达到完全降解.Chow等(Chow et al., 2012)研究了以纳米TiO2为催化剂进行的BDE-209光解反应,发现随着催化剂颗粒的减小,催化剂的活性增大,BDE-209的光解速率加快,可见光作用下的半衰期为3.05 d,产物主要是四溴和五溴联苯醚.
PBDEs在水环境中通常以聚合物形式存在而极其稳定,光解反应仅在聚合物表面进行,因接触面积小而降解半衰期长,反应不彻底,自然条件下PBDE的光降解效率非常低.对此,选择合适的溶剂环境,把PBDEs从聚合形态转变为分子形态,改变反应的传质过程,提高光强或通过介质强化对有效波长光的吸收,有可能从机理上改变反应的历程,获得光解效率的提高.
4.3 PBDEs零价铁还原利用零价铁的还原性与污染物组分反应,生成的铁中间态化合物又能与污染物再次发生化学反应,所生成的铁沉淀还具有吸附作用,电子还原作用、活泼氢作用、吸附作用和絮凝作用的协同实现污染物的转化与去除构成了零价铁的修复作用(Gillham and O'Hannesin,1994).零价铁法修复PBDEs污染是近几年发展起来的一种化学方法.零价铁具有很强的还原性,又具有电化学性质,其电极反应的产物中新生态〖H〗和Fe2+能与废水中很多组分发生氧化还原作用,使PBDEs大分子物质分解成小分子中间体,主要攻击的是键能相对较低的C—Br键,逐级脱溴生成低取代物质,最终实现目标物完全脱溴; 铁氧化物本身具有多孔性质,吸附性能良好,能修复部分污染物; 此外,铁在水体中容易产生絮状物Fe(OH)2和Fe(OH)3,具有很强的絮凝作用,可以去除一部分污染物,而PBDEs不溶于水,很容易吸附在固体颗粒和悬浮物上,更容易被絮凝沉淀,因此能提高其去除效果(吴继锋,2001).图 5为BDE-100零价铁还原脱溴路径(Keum and Li, 2005).PBDEs零价铁修复普遍符合一级动力学,说明脱溴反应是逐级进行.影响修复效率的主要因素有材料本身和PBDEs的分子性质.其中,溶解性和脱水性影响分子在材料上的附着,而溴原子数和分子结构影响修复时间的长短,含溴原子数越多,溴取代位点越对称,需要的活化能越多,产生的中间产物数量也越多,脱溴过程越复杂.
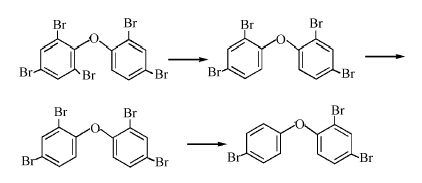 |
| 图 5 BDE-100零价铁还原脱溴路径 Fig. 5 Debromination pathway of BDE-100 by zero valent iron |
表 4归纳了零价铁修复PBDEs污染的文献.从表中可以看出,零价铁修复PBDEs的研究内容集中在寻找新的载体、制备新功能性的零价铁材料、提高材料的稳定性、提高材料与被修复水体或是沉积物的分离度方面上.其中,载体的选择逐渐向矿物粘土类发展,价格便宜,无二次污染; 双金属或多金属的复合材料被较多研究,原因是多金属在水体环境相互之间容易产生电势差,加强电子〖H〗的传递,表现出催化协同的效果,使还原脱溴反应更彻底与高效.零价铁修复PBDEs反应过程通常比较长,材料的稳定性尤为重要,零价铁载体的选择决定着修复方法的应用前景.
| 表 4 零价铁对PBDEs的修复材料与效果 Table 4 The material effect on PBDEs debromination by zero-valent iron |
与其他物化法相比,零价铁修复PBDEs不需要消耗光、电等其他能源,处理成本较低,材料绿色环保,反应过程中不产生二次污染.然而,随着反应的进行,铁屑易结块,出现沟流等现象,铁表面形成的铁氧化物及羟基氧化物比铁的还原性低很多,阻碍电子的转移,降低反应效率.因此,载体的优选与多金属复合材料的制备是技术获得应用突破的关键.
利用PBDEs具有吸收光、电、波等特性,将这些能量引入到零价铁协同修复PBDEs的污染,能加快反应的进程.微波、超声波、等离子体放电等能使PBDEs分子发生剧烈震荡,促使C—Br键断裂,还能使PBDEs分子发生高速旋转碰撞从而产生热效应,改变体系的热力学函数,降低反应活化能以及PBDEs分子的各个化学键强度.Luo等(Luo et al., 2012)用Fe-Ag联合金属纳米材料在微波能的作用下降解BDE-209,8 min的时候,BDE-209的转化率达到97%,产物中检出BDE-15,随着微波功率的提高,其降解效率还有所增加,甚至达到完全脱溴,其脱溴路径如图 6所示.此外,零价铁修复法能与微生物降解法、光催化分解法协同处理PBDEs的环境污染,有可能获得成倍的效率.
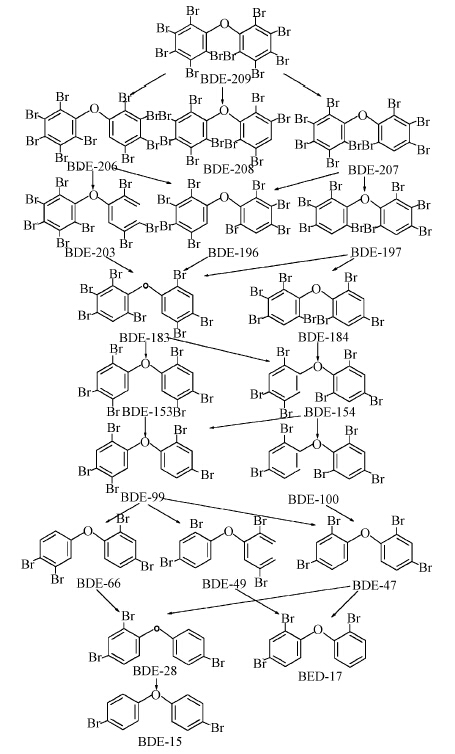 |
| 图 6 Fe-Ag联合纳米材料微波催化降解BDE-209过程 Fig. 6 Microwave catalytic debromination of BDE-209 with Fe-Ag nano materials |
从上述讨论的PBDEs的生物处理法、光化学分解法和零价铁还原法的污染控制技术中发现,尽管每一种方法表现出各自的优点,但它们都停留在实验室的研究阶段,缺乏与实际环境的结合,尚未考虑介质、剂量、相态等方面因素的综合影响.据2010联合国环境规划署发布的报告,我国已成为世界第二大电子垃圾生产国,每年生产超过230万t电子垃圾,仅次于美国的300万t; 到2020年,我国的废旧电脑将比2007年翻两番,废弃手机将增长7倍.塑料占总电子垃圾的30%,这些塑料若全部销毁,一方面带来严重的环境污染,另一方面也造成巨大的资源浪费.对此,分离其中的主要污染物,回收塑料原料,能极大地优化资源利用,带来经济效益.PBDEs主要存在于电子废物塑料中,其中PBDEs约占阻燃剂总量的30%.PBDEs在电子垃圾回用、拆解和销毁的过程中被释放出来,随着载体逐渐迁移和富集到水体、大气、土壤以及河流沉积物中,进而转移到动物体内和人体(任金亮和王平,2006).因而,针对电子行业废弃物需要研究污染物质的富集提取、分离以及完全毁毒技术,再将分离的塑料进行再加工或作为原料再利用.下面以电子垃圾塑料和水体沉积物中PBDEs的污染控制为例,描述分离提取-富集-超临界催化还原和氧化耦合方法在实际环境中PBDEs污染控制中的应用过程.
4.4.1 电子垃圾塑料中PBDEs的污染控制针对电子垃圾塑料中PBDEs的污染控制,主要过程是先将PBDEs与塑料原料分离,然后将富集的PBDEs进行完全毁毒.在我们承担的课题中,把电子废弃塑料作为研究的原材料,将整个污染控制过程分为3个阶段,具体过程如图 7所示.第一,预处理阶段,包括物料的分选、破碎和爆破,主要目的是将塑料与金属分离,然后将塑料破碎成小颗粒或粉末; 第二,PBDEs的提取阶段,选取适当的萃取剂和夹带剂,将塑料小颗粒进行超临界流体萃取,从而分离出有机物料中的PBDEs; 第三,PBDEs完全毁毒阶段,即在超临界水体系中进行反应,分为还原和氧化两个步骤.初步研究结果为可以分离60%~85%的PBDEs,还原脱溴率达到95%以上,催化氧化过程可以完全无害化PBDEs分子.整个过程耗时不到1 h.具体的物理化学机理与耗能分析需要更深入的研究数据证明.
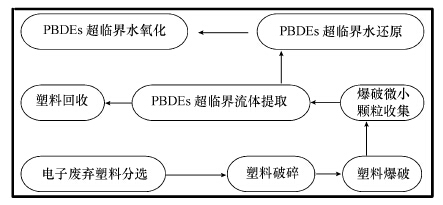 |
| 图 7 电子垃圾塑料中PBDEs的污染控制流程 Fig. 7 Pollution control process of PBDEs in electronic waste plastic |
针对流域水体及沉积物中PBDEs的污染控制,主要过程是先将PBDEs从水体及其沉积物中吸附分离,然后将富集的PBDEs进行完全毁毒.以流域水体中PBDEs为污染控制对象,整个过程分为4个阶段,具体过程如图 8所示.第一,流域水体及沉积物中PBDEs的检测,目的是探明流域污染的现状及污染程度; 第二,PBDEs的性质分析,选定对应的功能单体模板分子,构建分子印迹材料(袁琼辉和汤又文,2009); 第三,PBDEs功能吸附剂的制备,以磁性铁或是PHB(Zhang et al., 2010; 杨清玉等,2012)等为载体将分子印迹材料负载上去,使材料能够良好地吸附PBDEs,并且材料又能在磁力作用下从水体及沉积物中分离; 第四,将回收的材料进行洗脱,富集分离其中的PBDEs,然后在超临界水体系中进行完全毁毒,分为超临界水还原和氧化两个步骤.
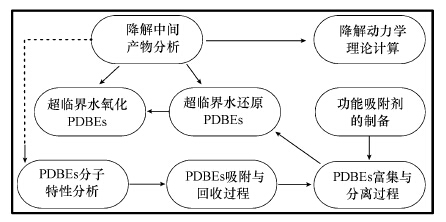 |
| 图 8 流域水体及沉积物中PBDEs的污染控制流程 Fig. 8 Pollution control process of PBDEs in water and sediment |
通过上述两个案例,分离得到含有PBDEs的溶剂介质,为实现超临界条件下的非选择性反应提供了可行性.针对高溴代PBDEs催化还原脱溴的过程描述为:首先,不同工艺条件(温度、停留时间等)下PBDEs的脱溴反应过程,建立脱溴的总动力学及分步动力学; 其次,结合脱溴的催化过程,考察不同金属催化剂对催化过程的影响,获得有效还原脱溴的金属催化剂.电子垃圾塑料超临界萃取回收液中,PBDEs浓度高,在高温高压的条件下,会发生逐级脱溴反应,随着取代的溴原子数减少,反应进行的越来越难,需要在催化剂的作用下才能高效反应.在金属催化作用下,化合物能发生水汽重整、裂解反应,最终获得溴离子、氢气及低溴代中间产物.推测的机理为金属在超临界水中与水发生反应形成金属氧化物,通过置换并脱附水中的氧,之后金属氧化物吸附有机物并与有机物发生反应,使有机化合物进一步还原脱溴(Wei et al., 2010).以BDE-209为例,在超临界水体系中,反应120 s时,基本检测不到BDE-209,中间产物分析生成有BDE-99,BDE-100,BDE-15,DE等产物.PBDEs降解的动力学方程表现为多级并与催化模型相耦合(Guan et al., 2011):
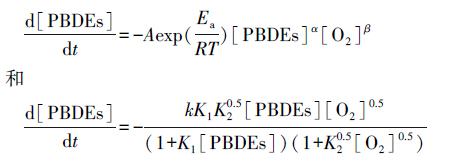
针对实际过程,影响参数更多,识别催化剂筛选与种类、超临界还原、超临界氧化、中间产物的生成的动力学研究与应用,动力学方程的表达可能还有更多的形式.
针对低溴代PBDEs催化氧化毁毒的过程描述为:经过催化还原以后的水样中,PBDEs所含的溴代数很低,在氧化剂和催化剂的作用下,低溴代PBDEs或是DE逐渐开环断键,最终生成CO、CO2和H2O.其原因是,溴被脱除后,原本易形成 · Br自由基并生成HBr的量大大减少,使氧能与污染物充分接触.超临界水体系表现出传质阻力小,氧化剂与有机物能均相混合,反应充分进行,效率是常温常压反应的1000倍以上.改变反应过程的另一个重要因素是催化剂的作用,通过构建不同的催化反应体系,降低反应的能垒,获得基于目标污染物的选择性效率.很多因素决定不同金属的催化活性(赵国华等,2001),如图 9所示,部分金属及合金的催化活性存在一定的规律.图中所示贵金属Ru和Rh具有高催化活性,复合金属能进一步提高活性,部分非贵金属合金同样能产生高催化活性.关于催化剂的选择,在兼顾脱溴效果的同时,还需考察催化剂的使用寿命,重复使用的稳定性,经济性与二次环境污染等,存在巨大的优化空间.
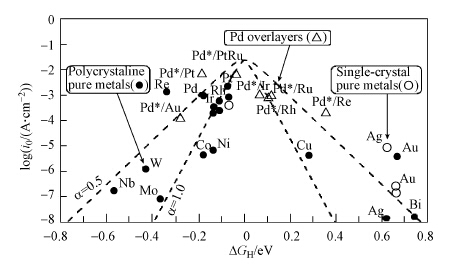 |
| 图 9 部分金属及合金的催化活性 Fig. 9 The catalytic activity of some metals and alloys |
PBDEs在我国环境中的污染扩散是否沿袭国外模式,其污染的环境风险在时间尺度、空间尺度、经济尺度、健康预测方面的未来发展的确令人迷惑,如何通过现状分析与未来预测实现PBDEs及其产品的可控应用是摆在我们眼前的关键问题.管理层面,基于国内的生产与使用量、应用行业、应用途径、进口的产品与原材料、电子垃圾进口量、收集的规范等方面持续开展物料流与质量衡算的统计,结合法律法规与鼓励性措施,建立长效机制,使标准、规范、应用、回收、预防污染扩散的基本概念深入民间; 产品研究层面,作为阻燃剂PBDEs的替代品的研发是首要,生产过程如何充分利用PBDEs的物理化学性质,制造出添加量少而阻燃效果好的产品,区别对待不同成分的组合效果,充分考虑后续处理的可行性,与此同时,建立产品质量标准,基于产品与环境暴露的极限低浓度PBDEs灵敏快速即高通量分析检测方法的开发,满足生产企业与环境检测部门以至于家庭的需求; 生态风险层面,随着我国经济的发展和消费产品的丰富,家用电子电器产品拥有量增加致使数量增加、新房建设与装饰、室内纺织品使用量增加等原因,同时我国还是承接发达国家电子垃圾的主要国家,将导致我国人群PBDEs暴露水平的持续增高,目前我国有关PBDEs环境暴露及其健康危害的研究资料非常有限,政府缺乏是否限制PBDEs的生产与使用的决策依据,因此,在积极开展不同环境污染水平与人群暴露的健康风险评价的同时,提出基于介质、对象与接触环境的标准,强调标准的实用性与科学性; 污染控制技术层面,通过深入了解PBDEs的分子性质来理解迁移转化规律和环境危害性,使用针对性的方法实现从点源到面源的逐级有效控制,考虑浓度水平、介质差异、化学化工与工程的影响传递、单元技术到复合集成技术的系列问题,集成信息,优化与分类,寻找关键,从基本原理上取得突破,形成生产企业、应用场地、回收基地、受纳空气与水体环境联合防范的网络技术.
| [1] | Ahn M Y, Filley T R, Jafvert C T, et al. 2011. Photodegradation of decabromodiphenyl ether adsorbed onto clay minerals, metal oxides, and sediment[J]. Environmental Science & Technology, 40(1):215-220 |
| [2] | Akutsu K, Kitagawa M, Nakazawa H, et al. 2003. Time-trend(1973-2000) of polybrominated diphenyl ethers in Japanese mother's milk[J]. Chemosphere, 53(6):645-654 |
| [3] | Allchin C R, Law R J, Morris S. 1999. Polybrominated diphenylethers in sediments and biota downstream of potential sources in the UK[J]. Environmental Pollution, 105(2):197-207 |
| [4] | An T C, Chen J X, Li G Y, et al. 2008. Characterization and the photocatalytic activity of TiO2 immobilized hydrophobic montmorillonite photocatalysts degradation of decabromodiphenyl ether (BDE 209)[J]. Catalysis Today, 139(1/2):69-76 |
| [5] | Andersson Ö, Blomkvist G. 1981. Polybrominated aromatic pollutants found in fish in Sweden[J]. Chemosphere, 10(9):1051-1060 |
| [6] | Bendig P, Vetter W. 2010. Photolytical transformation rates of individual polybrominated diphenyl ethers in technical octabromo diphenyl ether (DE-79)[J]. Environmental Science & Technology, 44(5):1650-1655 |
| [7] | Betts K S. 2002. Flame-proofing the Arctic?[J]. Environmental Science and Technology, 36(9):188A-192A |
| [8] | Bezares-Cruz J, Jafvert C T, Hua I. 2004. Solar photodecomposition of decabromodiphenyl ether:products and quantum yield[J]. Environmental Science & Technology, 38(15):4149-4156 |
| [9] | Bieniek D, Bahadir M, Korte F. 1989. Formation of heterocyclic hazardous compounds by thermal degradation of organic compounds[J]. Heterocycles, 28(2):719-722 |
| [10] | Booij K, Zegers B N, Boon J P. 2002. Levels of some polybrominated diphenyl ether (PBDE) flame retardants along the Dutch coast as derived from their accumulation in SPMDs and blue mussels(Mytilus edulis)[J]. Chemosphere, 46(5):683-688 |
| [11] | Bragigand V, Amiard-Triquet C, Parlier E, et al. 2006. Influence of biological and ecological factors on the bioaccumulation of polybrominated diphenyl ethers in aquatic food webs from French estuaries[J]. Science of the Total Environment, 368(2/3):615-626 |
| [12] | Burreau S, Zebhr Y, Broman D, et al. 2004. Biomagnification of polychlorinated biphenyls (PCBs) and polybrominated diphenyl ethers (PBDEs) studied in pike (Esox lucius), perch (Perca fluviatilis) and roach (Rutilus rutilus) from the Baltic Sea[J]. Chemosphere, 55(7):1043-1052 |
| [13] | Cetin B, Odabasi M. 2007. Air-water exchange and dry deposition of polybrominated diphenyl ethers at a coastal site in Izmir Bay, Turkey[J]. Environmental Science & Technology, 41(3):785-791 |
| [14] | Chang B V, Yuan S Y, Ren Y L. 2012. Aerobic degradation of tetrabromobisphenol-A by microbes in river sediment[J]. Chemosphere, 87(5):535-541 |
| [15] | Chen J W, Yang P, Chen S, et al. 2008. Quantitative structure-property relationships for vapor pressures of polybrominated diphenyl ethers[J]. SAR and QSAR in Environmental Research, 14(2):97-111 |
| [16] | Chen S J, Luo X J, Lin Z, et al. 2007. Time trends of polybrominated diphenyl ethers in sediment cores from the Pearl river estuary, South China[J]. Environmental Science & Technology, 41(16):5595-5600 |
| [17] | Chen Y, Li J H, Liu L L, et al. 2012. Polybrominated diphenyl ethers fate in China:A review with an emphasis on environmental contamination levels, human exposure and regulation[J]. Journal of Environmental Management, 113(6):22-30 |
| [18] | Chow K L, Man Y B, Zheng J S, et al. 2012. Characterizing the optimal operation of photocatalytic degradation of BDE-209 by nano-sized TiO2[J]. Journal of Environmental Sciences, 24(9):1670-1678 |
| [19] | Covaci A, Voorspoels S, Ramos L, et al. 2007. Recent developments in the analysis of brominated flame retardants and brominated natural compounds[J]. Journal of Chromatography A, 1153(1/2):145-171 |
| [20] | De Boer J, Wester P G, Van Der Horst A, et al. 2003. Polybrominated diphenyl ethers in influents, suspended particulate matter, sediments, sewage treatment plant and effluents and biota from the Netherlands[J]. Environmental Pollution, 122(1):63-74 |
| [21] | De Wit C A. 2002. An overview of brominated flame retardants in the environment[J]. Chemosphere, 46(5):583-624 |
| [22] | Deng D Y, Guo J, Xu M Y, et al. 2011. Aerobic debromination of deca-BDE:Isolation and characterization of an indigenous isolate from a PBDE contaminated sediment[J]. International Biodeterioration & Biodegradation, 65(3):465-469 |
| [23] | Deng W J, Zheng J S, Bi X H, et al. 2007. Distribution of PBDEs in air particles from an electronic waste recycling site compared with Guangzhou and Hong Kong, South China[J]. Environment International, 33(8):1063-1069 |
| [24] | Eriksson J, Green N, Marsh G, et al. 2004. Photochemical decomposition of 15 polybrominated diphenyl ether congeners in methanol/water[J]. Environmental Science & Technology, 38(11):3119-3125 |
| [25] | Fang Z Q, Qiu X H, Chen J H, et al. 2011a. Debromination of polybrominated diphenyl ethers by Ni/Fe bimetallic nanoparticles:Influencing factors, kinetics, and mechanism[J]. Journal of Hazardous Materials, 185(2):958-969 |
| [26] | Fang Z Q, Qiu X H, Chen J H, et al. 2011b. Degradation of the polybrominated diphenyl ethers by nanoscale zero-valent metallic particles prepared from steel pickling waste liquor[J]. Desalination, 267(1):34-41 |
| [27] | Frederiksen M, Vorkamp K, Thomsen M, et al. 2009. Human internal and external exposure to PBDEs-A review of levels and sources[J]. International Journal of Hygiene and Environmental Health, 212(2):109-134 |
| [28] | Gallego E, Grimalt J O, Bartrons M, et al. 2007. Altitudinal gradients of PBDEs and PCBs in fish from European high mountain lakes[J]. Environmental Science & Technology, 41(7):2196-2202 |
| [29] | Gerecke A C, Hartmann P C, Heeb N V, et al. 2005. Anaerobic degradation of decabromodiphenyl ether[J]. Environmental Science & Technology, 39(4):1078-1083 |
| [30] | Ghanem R, Delmani F A. 2012. Kinetics of thermal and photolytic degradation of decabromodiphenyl ether (BDE 209) in backcoated textile samples[J]. Journal of Analytical and Applied Pyrolysis, 98:79-85 |
| [31] | Gillham R W, O'Hannesin S F. 1994. Enhanced degradation of halogenated aliphatics by zero-valent iron[J]. Ground Water, 32(6):958-967 |
| [32] | Guan Q Q, Wei C H, Shi H S, et al. 2011. Partial oxidative gasification of phenol for hydrogen in supercritical water[J]. Applied Energy, 88(8):2612-2616 |
| [33] | 郭杨, 王世和. 2008. 多溴联苯醚的微生物降解研究[J]. 中国沼气, 26(4):3-6 |
| [34] | Hale R C, Alaee M, Manchester-Neesvig J B, et al. 2003. Polybrominated diphenyl ether flame retardants in the north American environment[J]. Environment International, 29(6):771-779 |
| [35] | Harrad S, Hazrati S, Ibarra C. 2006. Concentrations of polychlorinated biphenyls in indoor air and polybrominated diphenyl ethers in indoor air and dust in Birmingham, United Kingdom:implications for human exposure[J]. Environmental Science & Technology, 40(15):4633-4638 |
| [36] | Huang H W, Chang B V, Cheng C H. 2012. Biodegradation of dibromodiphenyl ether in river sediment[J]. International Biodeterioration & Biodegradation, 68:1-6 |
| [37] | 黄俊, 余刚, 钱易. 2001. 我国的持久性有机污染物问题与研究对策[J]. 环境保护, (11):3-6 |
| [38] | Hundt K, Martin D, Hammer E, et al. 2000. Transformation of triclosan by Trametes versicolor and Pycnoporus cinnabarinus[J]. Applied and Environmental Microbiology, 66(9):4157-4160 |
| [39] | Ikonomou M G, Rayne S, Addison R F. 2002a. Exponential increases of the brominated flame retardants, polybrominated diphenyl ethers, in the Canadian Arctic from1981 to 2000[J]. Environmental Science & Technology, 36(9):1886-1892 |
| [40] | Ikonomou M G, Rayne S, Fischer M, et al. 2002b. Occurrence and congener profiles of polybrominated diphenyl ethers (PBDEs) in environmental samples from coastal British Columbia, Canada[J]. Chemosphere, 46(5):649-663 |
| [41] | Jin J, Liu W Z, Wang Y, et al. 2008. Levels and distribution of polybrominated diphenyl ethers in plant, shellfish and sediment samples from Laizhou Bay in China[J]. Chemosphere, 71(6):1043-1050 |
| [42] | Johnson-Restrepo B, Kannan K, Addink R, et al. 2005. Polybrominated diphenyl ethers and polychlorinated biphenyls in a marine foodweb of coastal Florida[J]. Environmental Science & Technology, 39(21):8243-8250 |
| [43] | Kajiwara N, Kamikawa S, Ramu K, et al. 2006. Geographical distribution of polybrominated diphenyl ethers (PBDEs) and organochlorines in small cetaceans from Asian waters[J]. Chemosphere, 64(2):287-295 |
| [44] | Kajiwara N, Noma Y, Takigami H. 2008. Photolysis studies of technical decabromodiphenyl ether (DecaBDE) and ethane (DeBDethane) in plastics under natural sunlight[J]. Environmental Science & Technology, 42(12):4404-4409 |
| [45] | Keum Y S, Li Q X. 2005. Reductive debromination of polybrominated diphenyl ethers by zerovalent iron[J]. Environmental Science & Technology, 39(7):2280-2286 |
| [46] | Kim Y M, Nam I H, Murugesan K, et al. 2007. Biodegradation of diphenyl ether and transformation of selected brominated congeners by Sphingomonas sp. PH-07[J]. Applied Microbiology and Biotechnology, 77(1):187-194 |
| [47] | Kuch B, Hagenmaier H, K rner W. 2001. Determination of brominated flame retardants in sewage sludges and sediments in southwest Germany[A]. Presented at the 11th Annual European Society of Environmental Toxicology and Chemistry Meeting[C]. Madrid, Spain |
| [48] | Kuivikko M, Kotiaho T, Hartonen K, et al. 2007. Modeled direct photolytic decomposition of polybrominated diphenyl ethers in the Baltic Sea and the Atlantic Ocean[J]. Environmental Science & Technology, 41(20):7016-7021 |
| [49] | Lagalante A F, Shedden C S, Greenbacker P W. 2011. Levels of polybrominated diphenyl ethers (PBDEs) in dust from personal automobiles in conjunction with studies on the photochemical degradation of decabromodiphenyl ether (BDE-209)[J]. Environment International, 37(5):899-906 |
| [50] | Lee R G M, Thomas G O, Jones K C. 2004. PBDEs in the atmosphere of three locations in Western Europe[J]. Environmental Science & Technology, 38(3):699-706 |
| [51] | Li A, Rockne K J, Sturchio N, et al. 2006. Polybrominated diphenyl ethers in the sediments of the Great lakes. 4. Influencing factors, trends, and implications[J]. Environmental Science & Technology, 40(24):7528-7534 |
| [52] | Lin K D, Ding J F, Huang X W. 2012. Debromination of tetrabromobisphenol A by nanoscale zerovalent iron:kinetics, inuencing factors, and pathways[J]. Industrial and Engineering Chemistry Research, 51(25):8378-8385 |
| [53] | Luo Q, Cai Z W, Wong M H. 2007. Polybrominated diphenyl ethers in fish and sediment from river polluted by electronic waste[J]. Science of the Total Environment, 383(1/3):115-127 |
| [54] | Luo S, Yang S G, Sun C, et al. 2012. Improved debromination of polybrominated diphenyl ethers by bimetallic iron-silver nanoparticles coupled with microwave energy[J]. Science of the Total Environment, 429:300-308 |
| [55] | Moon H B, Kannan K, Choi M, et al. 2007. Polybrominated diphenyl ethers (PBDEs) in marine sediments from industrialized bays of Korea[J]. Marine Pollution Bulletin, 54(9):1402-1412 |
| [56] | Nyholm J R, Lundberg C, Andersson P L. 2010. Biodegradation kinetics of selected brominated flame retardants in aerobic and anaerobic soil[J]. Environmental Pollution, 158(6):2235-2240 |
| [57] | Nylund K, Asplund L, Jansson B, et al. 1992. Analysis of some polyhalogenated organic pollutants in sediment and sewage sludge[J]. Chemosphere, 24(12):1721-1730 |
| [58] | Ohta S, Ishizuka D, Nishimura H, et al. 2002. Comparison of polybrominated diphenyl ethers in fish, vegetables, and meats and levels in human milk of nursing women in Japan[J]. Chemosphere, 46(5):689-696 |
| [59] | Oros D R, Hoover D, Rodigari F, et al. 2005. Levels and distribution of polybrominated diphenyl ethers in water, surface sediments, and bivalves from the San Francisco estuary[J]. Environmental Science & Technology, 39(1):33-41 |
| [60] | Pfeifer F, Trüper H G, Klein J, et al. 1993. Degradation of diphenylether by Pseudomonas cepacia Et4:enzymatic release of phenol from 2, 3-dihydroxydiphenylether[J]. Archives of Microbiology, 159(4):323-329 |
| [61] | Qiu X H, Fang Z Q, Liang B, et al. 2011. Degradation of decabromodiphenyl ether by nano zero-valent iron immobilized in mesoporous silica microspheres[J]. Journal of Hazardous Materials, 193:70-81 |
| [62] | Rahman F, Langford K H, Scrimshaw M D, et al. 2001. Polybrominated diphenyl ether (PBDE) flame retardants[J]. Science of the Total Environmental, 275(1/3):1-17 |
| [63] | Rayne S, Ikonomou M G, Whale M D. 2003. Anaerobic microbial and photochemical degradation of 4, 4'-dibromodiphenyl ether[J]. Water Research, 37(3):551-560 |
| [64] | Rayne S, Wan P, Ikonomou M. 2009. Photochemistry of a major commercial polybrominated diphenyl ether flame retardant congener:2, 2', 4, 4', 5, 5'-Hexabromodiphenyl ether (BDE153)[J]. Environment International, 32(5):575-585 |
| [65] | 任金亮, 王平. 2006. 多溴联苯醚环境行为的特征与研究进展[J]. 化工进展, 25(10):1152-1156 |
| [66] | Robrock K R, Coelhan M, Sedlak D L, et al. 2009. Aerobic biotransformation of polybrominated diphenyl ethers (PBDEs) by bacterial isolates[J]. Environmental Science & Technology, 43(15):5705-5711 |
| [67] | Samara F, Tsai C W, Aga D S. 2006. Determination of potential sources of PCBs and PBDEs in sediments of the Niagara river[J]. Environmental Pollution, 139(3):489-497 |
| [68] | Sanchez-Prado L, Llompart M, Lores M, et al. 2005. Investigation of photodegradation products generated after UV-irradiation of five polybrominated diphenyl ethers using photo solid-phase microextraction[J]. Journal of Chromatography A, 1071(1/2):85-92 |
| [69] | Sanchez-Prado L, Kalafata K, Risticevic S, et al. 2012. Ice photolysis of 2, 2', 4, 4', 6-pentabromodiphenyl ether (BDE-100):Laboratory investigations using solid phase microextraction[J]. Analytica Chimica Acta, 742:90-96 |
| [70] | Schecter A, Harris R T, Päpke O, et al. 2006. Polybrominated diphenyl ether (PBDE) levels in the blood of pure vegetarians (vegans)[J]. Toxicological and Environmental Chemistry, 88(1):107-112 |
| [71] | Schenker U, Soltermann F, Scheringer M, et al. 2008. Modeling the environmental fate of polybrominated diphenyl ethers (PBDEs):the importance of photolysis for the formation of lighter PBDEs[J]. Environmental Science & Technology, 42(24):9244-9249 |
| [72] | Shih Y H, Tai Y T. 2010. Reaction of decabrominated diphenyl ether by zerovalent iron nanoparticles[J]. Chemosphere, 78(10):1200-1206 |
| [73] | Shih Y H, Chou H L, Peng Y H. 2012. Microbial degradation of 4-monobrominated diphenyl ether with anaerobic sludge[J]. Journal of Hazardous Materials, 213-214:341-346 |
| [74] | Stapleton H M, Baker J E. 2001. Comparing the temporal trends, partitioning and biomagnification of PBDEs and PCBs in Lake Michigan[A]. Presented at the 3rd Annual Workshop on Brominated Flame Retardants in the Environment. Burlington[C]. Canada:National Water Research Institute. 22-25 |
| [75] | Stapleton H M, Dodder N G, Offenberg J H, et al. 2005. Polybrominated diphenyl ethers in house dust and clothes dryer lint[J]. Environmental Science & Technology, 39(4):925-931 |
| [76] | Sun C Y, Zhao J C, Ji H W, et al. 2012. Photocatalytic debromination of preloaded decabromodiphenyl ether on the TiO2 surface in aqueous system[J]. Chemosphere, 89(4):420-425 |
| [77] | Thuresson K, Bergman Å, Rothenbacher K, et al. 2006. Polybrominated diphenyl ether exposure to electronics recycling workers——a follow up study[J]. Chemosphere, 64(11):1855-1861 |
| [78] | Tokarz J A, Ahn M Y, Leng J, et al. 2008. Reductive debromination of polybrominated diphenyl ethers in anaerobic sediment and a biomimetic system[J]. Environmental Science & Technology, 42(4):1157-1164 |
| [79] | Vonderheide A P, Mueller K E, Meija J, et al. 2008. Polybrominated diphenyl ethers:Causes for concern and knowledge gaps regarding environmental distribution, fate and toxicity[J]. Science of the Total Environment, 400(1/3):425-436 |
| [80] | Wang Y W, Jiang G B, Lam P K S, et al. 2007. Polybrominated diphenyl ether in the East Asian environment:A critical review[J]. Environment International, 33(7):963-973 |
| [81] | Ward J, Mohapatra S P, Mitchell A. 2008. An overview of policies for managing polybrominated diphenyl ethers (PBDEs) in the Great Lakes basin[J]. Environment International, 34(8):1148-1156 |
| [82] | Watanabe I, Kashimoto T, Tatsukawa R. 1987. Polybrominated biphenyl ethers in marine fish, shellfish and river and marine sediments in Japan[J]. Chemosphere, 16(10/12):2389-2396 |
| [83] | Watanabe I, Sakai S. 2006. Environmental release and behavior of brominated flame retardants[J]. Environment International, 29(6):665-682 |
| [84] | Wei G T, Wei C H, Wu C F, et al. 2010. Reductive dechlorination of chlorobenzene in supercritical water catalyzed by Fe/ZrO2[J]. Environmental Chemistry Letters, 8(2):165-169 |
| [85] | Wilford B H, Harner T, Zhu J P, et al. 2004. Passive sampling survey of polybrominated diphenyl ether flame retardants in indoor and outdoor air in Ottawa, Canada:implications for sources and exposure[J]. Environmental Science & Technology, 38(20):5312-5318 |
| [86] | Wilford B H, Shoeib M, Harner T, et al. 2005. Polybrominated diphenyl ethers in indoor dust in Ottawa, Canada:implications for sources and exposure[J]. Environmental Science & Technology, 39(18):7027-7035 |
| [87] | Wolkers H, Van Bavel B, Derocher A E, et al. 2004. Congener-specific accumulation and food chain transfer of polybrominated diphenyl ethers in two arctic food chains[J]. Environmental Science & Technology, 38(6):1667-1674 |
| [88] | 吴继锋. 2001. 零价铁处理废水的机理及应用[J]. 安庆师范学院学报(自然科学版), 7(2):78-79 |
| [89] | Wurl O, Lam P K S, Obbard J P. 2006. Occurrence and distribution of polybrominated diphenyl ethers (PBDEs) in the dissolved and suspended phases of the sea-surface microlayer and seawater in Hong Kong, China[J]. Chemosphere, 65(9):1660-1666 |
| [90] | 肖松文, 肖晓. 2006. 持久性有机污染物机械化学无害化处理的研究进展[J]. 矿冶工程, 26(2):53-56 |
| [91] | 杨清玉, 易欣怡, 于旭彪, 等. 2012. 聚羟基丁酸酯(PHB)对水中微量多环芳烃的仿生吸附[J]. 环境化学, 31(10):1518-1526 |
| [92] | Yen J H, Liao W C, Chen W C, et al. 2009. Interaction of polybrominated diphenyl ethers (PBDEs) with anaerobic mixed bacterial cultures isolated from river sediment[J]. Journal of Hazardous Materials, 165(1/3):518-524 |
| [93] | Yu K, Gu C, Boyd S A, et al. 2012. Rapid and extensive debromination of decabromodiphenyl ether by smectite clay-templated subnanoscale zero-valent iron[J]. Environmental Science & Technology, 46(16):8969-8975 |
| [94] | 袁琼辉, 汤又文. 2009. 新型功能单体分子印迹聚合物的研究进展[J]. 化学通报, 72(8):707-712 |
| [95] | Zhang S W, Xia X H, Xia N, et al. 2013. Identification and biodegradation efficiency of a newly isolated 2, 2', 4, 4'-tetrabromodiphenyl ether (BDE-47) aerobic degrading bacterial strain[J]. International Biodeterioration & Biodegradation, 76:24-31 |
| [96] | Zhang X X, Wei C H, He Q C, et al. 2010. Enrichment of chlorobenzene and o-nitrochlorobenzene on biomimetic adsorbent prepared by poly-3-hydroxybutyrate (PHB)[J]. Journal of Hazardous Materials, 177(1/3):508-515 |
| [97] | 赵国华, 孙云平, 朱仲良, 等. 2001. 利用化学计量学方法解析有机污染物降解的动力学过程[J]. 计算机与应用化学, 18(1):64-68 |
| [98] | Zhu L Y, Hites R A. 2005. Brominated flame retardants in sediment cores from lakes Michigan and Erie[J]. Environmental Science & Technology, 39(10):3488-3494 |
| [99] | Zhuang Y, Ahn S W, Luthy R G. 2010. Debromination of polybrominated diphenyl ethers by nanoscale zerovalent iron:pathways, kinetics, and reactivity[J]. Environmental Science & Technology, 44(21):8236-8242 |
| [100] | Zhuang Y, Jin L T, Luthy R G. 2012. Kinetics and pathways for the debromination of polybrominated diphenyl ethers by bimetallic and nanoscale zerovalent iron:Effects of particle properties and catalyst[J]. Chemosphere, 89(4):426-432 |
 2015, Vol. 35
2015, Vol. 35


