2. 环境污染过程与基准教育部重点实验室, 天津市城市生态环境修复与污染防治重点实验室, 南开大学环境科学与工程学院, 天津 300071
2. Key Laboratory of Pollution Process and Environmental Criteria, Ministry of Education, Tianjin Key Laboratory of Urban Ecology Environmental Remediation and Pollution Control, College of Environmental Science and Engineering, Nankai University, Tianjin 300071
微生物燃料电池(Microbial fuel cells,MFCs)是利用微生物作为催化剂氧化有机物并直接将化学能转化成电能的新型装置(Logan,2009).它具有废水处理与联产电能的双重功效,近年来在缓解能源紧张和废水资源化处理等方面表现出广阔的应用前景(Osman et al., 2010; Qiao et al., 2010; Zhou et al., 2011).
产电微生物(Exoelectrogens)是指那些能够在厌氧条件下完全氧化有机物,把氧化有机物获得的电子通过电子传递链传递到细胞外,直接或间接地通过介质(Mediator)将电子传递到电极上产生电流的微生物,同时微生物在电子传递过程中获得能量支持生长(Logan et al., 2006; Lovley,2006).产电微生物种类不同,其产生电子和传递电子的速率也不同,表现出的电化学活性亦存在明显差异.因此,产电微生物研究对改善和提高MFCs的产电性能具有重要意义.
目前,产电微生物的发现途径一般可以分为两类:一是从环境中分离得到的纯培养菌株在电化学系统中验证其是否具有电化学活性;另一种是直接在电化学系统中富集,然后进行分离、纯化和鉴定.其中,后一种方法已成为产电微生物分离培养的主流方法(Park et al., 2001;Pham et al., 2003; Rezaei et al., 2009).
迄今为止,已报道的产电微生物已达到30余种,主要包括地杆菌属(Geobacter)(Bond et al., 2003; Ishii et al., 2008; Nevin et al., 2008)、希瓦氏菌属(Shewanella)(Kim et al., 1999; Ringeisen et al., 2006)、假单胞菌属(Pseudomonas)(Rabaey,2004; Jayapriya et al., 2012)、弓形菌属(Arcobacter)(Fedorovich et al., 2009)、红育菌属(Rhodoferax)(Chaudhuri et al., 2003)等.此外,许多其他产电菌也已被分离和鉴定,例如:嗜酸菌属(Acidiphilium sp.)(Borole et al., 2008)、嗜水气单胞菌(Aeromonas hydrophila)(Pham et al., 2003)、气单胞菌属(Aeromonas sp.)(Chung et al., 2009)、枯草芽孢杆菌(Bacillus subtilis)(Nimje et al., 2009)、丁酸梭菌(Clostridium butyricum)(Park et al., 2001)、氧化乙酸脱硫单胞菌(Desulfuromonas acetoxidans)(Bond et al., 2002)、硫酸盐还原菌(Desulfobulbus propionicus)(Holmes et al., 2004a)、脱硫弧菌(Desulfovibrio desulfuricans)(Zhao et al., 2008)、大肠杆菌(Escherichia coli)(Zhang et al., 2006)、阴沟肠杆菌(Enterobacter cloacae)(Nimje et al., 2011)、地发菌(Geothrix fermentans)(Bond et al., 2005)、耐寒细菌(Geopsychrobacter electrodiphilus)(Holmes et al., 2004b)、克雷伯氏菌(Klebsiella pneumonia)(Zhang et al., 2008)、人苍白杆菌(Ochrobactrum anthropic)(Zuo et al., 2008)、异常汉逊酵母(Pichia anomala)(Prasad et al., 2007)、沼泽红假单胞菌(Rhodopseudomonas palustris)(Xing et al., 2008)、Thermincola sp.(Wrighton et al., 2008)、甲苯单胞菌(Tolumonas osonensis)(Luo et al., 2013)等.总体而言,已知的产电微生物种类仍然非常有限,有必要开展产电微生物资源的发掘工作.
基于此,本研究以天津泰达污水处理厂污泥浓缩间的污泥为接种物,启动并运行MFCs.从富集的阳极生物膜上分离得到一株纯培养的微生物菌种(P2-A-5),通过形态学观察、生理生化实验和分子鉴定等方法确定其种属信息,并将其接种MFCs验证其产电性能.然后,通过化学剂处理、底物种类和浓度优化等方法进一步提高其产电性能.以期为丰富产电微生物的多样性,挖掘更多具有高电化学活性的微生物菌种,提高其产电性能提供参考.
2 材料与方法(Materials and methods) 2.1 产电微生物的富集与分离菌株P2-A-5分离自本实验室接种天津泰达污水处理厂污泥的单室空气阴极MFC 阳极生物膜.该MFC以1.0 g · L-1葡萄糖为电子供体,待其运行至稳定期后,取阳极生物膜进行菌株P2-A-5的分离.分离所用的液体培养基为PBBM培养基(Kim et al., 2004),其中,添加1.0 g · L-1葡萄糖和5.0 g · L-1柠檬酸铁分别作为电子供体和电子受体,并用NaOH调节该培养基的pH=7.2.若配制固体培养基则加入2%的琼脂粉.具体操作步骤如下:在无菌操作台上用接种针刮取阳极生物膜若干,重悬于4 mL无菌水中制备成均匀的菌悬液,将其进行梯度稀释后涂布于分离固体培养基上,30 ℃厌氧条件下培养3 d,根据菌落形态、颜色、大小等特征,挑取表面特征差异明显的菌落,分别接种于PBBM液体培养基中再次富集培养,如此反复传代5~6次,得到一个纯培养菌株,命名为P2-A-5.
2.2 微生物燃料电池的构建、启动和运行采用空气阴极单室型MFCs反应器,具体构建过程参考文献(Zhou et al., 2012).
将LB固体培养基上的菌体P2-A-5接种一环到装有50 mL LB液体培养基的250 mL三角瓶中,28 ℃、120 r · min-1下振荡培养24 h,5000×g离心20 min后收集菌体并用50 mmol · L-1的PBS缓冲液(NH4Cl 0.31 g · L-1,KCl 0.13 g · L-1,NaH2PO4·2H2O 3.32 g · L-1,Na2HPO4·12H2O 10.36 g · L-1,pH=7.0)洗涤3次.将菌体重悬于阳极液中(PBBM液体培养基中加入终浓度为1.0 g · L-1的葡萄糖作为底物,pH=7.2,电导率为7.8 mS · cm-1),使其初始OD600为1.0,然后接种到MFCs反应器中.反应器分别与外电阻(无特殊说明时外电阻均为1000 Ω)和数据采集装置连接好,室温下运行,运行过程中定期更换接种液.当出现连续两个稳定电压时即认为启动成功.当监测的输出电压低于50 mV时,开始更换阳极液.当获得稳定可重复的输出电压后,按照文献(Luo et al., 2013)的方法进行电流密度(I)和功率密度(P)等相关电化学参数的测定.
2.3 菌种的鉴定 2.3.1 形态观察在营养琼脂固体培养基上划线接种,28 ℃恒温培养2 d,观察其生长情况及菌落特征,革兰氏染色(按照革兰氏染色试剂盒进行)后光学显微镜下观察其形态和染色特征.采用S-4200 FE-SEM扫描电子显微镜观察单个菌体的形态,电镜样品的预处理参考文献(Holmes et al., 2004b).
2.3.2 生理生化特征P2-A-5在LB培养基中进行富集和培养.生理生化试验参考文献(Kovács et al., 1999)上的标准方法进行,主要包括明胶水解实验、尿素酶实验、精氨酸水解实验、吐温80水解实验、柠檬酸盐实验及吲哚产生实验.菌株利用葡萄糖、果糖、蔗糖、木糖醇、乳糖、麦芽糖、甘露醇、山梨醇和甘油等碳源发酵产酸实验参照文献(Hugh et al., 1953).
2.3.3 菌株的 16S rDNA 基因序列分析及系统发育树构建采用EasypureTM Genomic DNA kit试剂盒(北京全式金生物技术有限公司)提取菌株总DNA并以之为模板,对16S rDNA基因序列进行PCR 扩增.引物对为通用引物27F(5′-AGA GTT TGA TCC TGGCTC AG-3′)和1492R(5′-GGT TAC CTT GTT ACGACT T-3′).PCR反应程序和反应体系参考文献(Luo et al., 2013).PCR 扩增产物经试剂盒纯化,用0.8%琼脂糖凝胶电泳检测合格后委托华大基因研发中心进行测序.测序结果提交NCBI GenBank(National Center of Biotechnology Information),用BLAST进行相似性检索和同源性比较.利用MEGA5.0软件,采用基于Kimura 2-parameter模型的邻接法(Neighbor-joining method)构建系统发育树,进化树分枝稳定性用Bootstrap分析,重复1000次.
2.4 细胞的化学剂处理分别采用5种化学剂对细胞进行处理,包括壳聚糖溶液(溶于10 mmol · L-1 HEPES缓冲液(含50 mmol · L-1 NaCl))、乙二胺四乙酸(EDTA)溶液(溶于10 mmol · L-1 Tris溶液)、聚乙烯亚胺(PEI)溶液(溶于10 mmol · L-1 HEPES缓冲液(含50 mmol · L-1NaCl))、溶菌酶溶液(溶于无菌水)、甘氨酸(溶于无菌水)溶液.
2.4.1 不同化学剂处理条件对菌体存活的影响将收集到的菌体分别悬浮于10 mL浓度为0.001、0.003、0.005、0.007、0.010 g · L-1的壳聚糖溶液中,制备成菌体细胞干重为3.394 g · L-1的菌悬液,分别取200 μL加入96微孔板中,28 ℃、100 r · min-1下振荡处理,在不同时间点(0、10、20、30、40、50和60 min)将微孔板置于酶标仪上测定OD600,绘制菌体在不同壳聚糖处理条件下的生长曲线.EDTA、PEI、溶菌酶和甘氨酸对菌体的处理方法同上,其中,EDTA的浓度分别为5、10、20、30、40、50 mmol · L-1,PEI的浓度分别为1、4、7、10、20、30、40、50 mg · L-1,溶菌酶的浓度分别为1、3、5、7、10 mg · L-1,甘氨酸的浓度分别为4%、10%、15%、20%、25%.实验中以PBS缓冲溶液处理的菌体细胞作为对照.
2.4.2 化学剂处理对细胞通透性的影响化学剂处理后的菌体经5000×g离心20 min进行收集,并悬浮于50 mmol · L-1的PBS(pH=7.0)中制得浓度为108 CFU · mL-1的菌悬液,采用FDA法进行细胞通透性的测定.具体实验过程和FDA相对荧光强度的计算方法参考文献(Luo et al., 2014).
2.5 底物种类和浓度的优化为研究菌株P2-A-5利用不同底物产电的性能,在PBBM培养基中分别以1 g · L-1乙酸钠、蔗糖、海藻糖、糊精、木糖醇、吐温80代替葡萄糖作为底物,运行MFCs,进行底物种类的优化.在确定了最适底物后,进一步考察不同底物浓度对P2-A-5产电性能的影响.
3 结果与讨论(Results and discussion) 3.1 菌株P2-A-5的分离和鉴定 3.1.1 形态学观察从稳定运行14 d的MFC阳极生物膜中分离得到了一株纯培养菌株P2-A-5.由图 1a可知,菌株P2-A-5在营养琼脂培养基上培养2 d后,菌落形态呈圆形凸起,为淡黄色,直径为2~3 mm,边缘整齐、表面光滑.革兰氏染色反应为阳性(图 1b).由扫描电镜照片可知(图 1c),菌体呈球状(半径约2.5 μm),成对或四联球菌,无鞭毛,不产生芽孢.
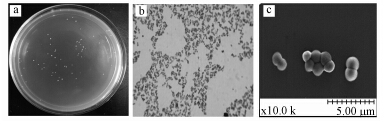 |
| 图 1 菌株P2-A-5的菌落形态(a)、革兰氏染色反应(b)、扫描电镜图像(c) Fig.1 Colony morphology(a),Gram staining(b) and scanning electron microscopy(c)of the isolate P2-A-5 |
菌株P2-A-5的的部分生理生化特性研究结果见表 1.由表 1可知,菌株P2-A-5的明胶酶实验、吐温80水解实验、柠檬酸盐实验结果均为阳性;吲哚实验、脲酶实验、精氨酸水解实验为阴性.在底物发酵产酸实验中,菌株P2-A-5可利用葡萄糖、果糖、蔗糖发酵产酸,而不能利用木糖、乳糖、麦芽糖、甘露醇、山梨醇、甘油发酵产酸.该菌株的生理生化特性同《伯杰氏系统细菌学手册》中的Kocuria rhizophila的结果一致.
| 表 1 菌株P2-A-5和Kocuria rhizophila 生理生化特性比较 Table 1 Comparison of physiological and biochemical characteristics between the isolate P2-A-5 and Kocuria rhizophila |
PCR 扩增获得的菌株P2-A-5的16S rDNA 基因片段大小为1320 bp,将序列提交至NCBI,BLAST结果显示,菌株P2-A-5 的16S rDNA 序列与已知菌株Kocuria rhizophila DC2201具有100%的同源性.从构建的系统发育树(图 2)可知,菌株P2-A-5与Kocuria rhizophila DC2201 处在系统发育树的同一分支,亲缘关系最为接近.综合上述形态学观察、生理生化实验结果和16S rDNA序列分析结果,将分离株P2-A-5鉴定为Kocuria rhizophila (Kovács et al., 1999).
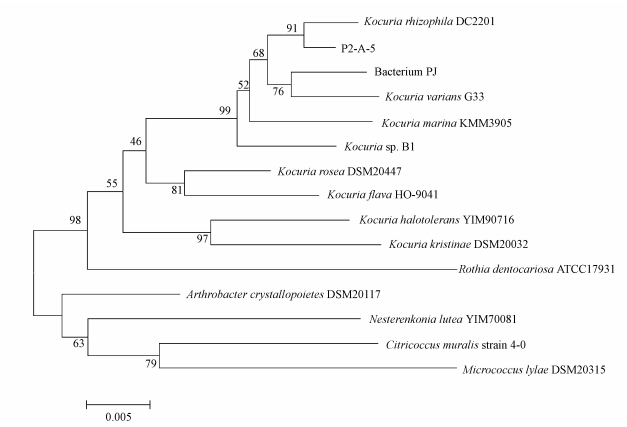 |
| 图 2 菌株P2-A-5及其亲属的系统发育树 Fig.2 Phylogenetic tree showing the relationships between strain P2-A-5 and the related species based on 16S rDNA gene sequencing analysis |
以1 g · L-1葡萄糖为底物,将分离得到的菌株P2-A-5接种至单室空气阴极MFC 中检测其产电特性,其输出电压如图 3a所示.由图 3a可知,以菌株P2-A-5启动的MFC在运行315 h后达到稳定,稳定电压约215 mV.在MFC输出电压达到稳定可重复后,绘制了极化曲线和功率密度曲线.由图 3b可知,P2-A-5运行MFC在外阻为500 Ω时功率密度最大,达到74.9 mW · m-2.嗜根考克氏菌(Kocuria rhizophila)最初是从狭叶香蒲的土壤根面中分离得到的,其广泛分布于自然环境、哺乳动物的皮肤、土壤、根际、发酵食品、临床标本、淡水、海洋沉积物等(Kovács et al., 1999; Takarada et al., 2008).K. rhizophila是革兰氏阳性菌,目前,仅有少数革兰氏阳性菌应用于MFC中,主要是Bacillus subtilis(Nimje et al., 2009)、 Clostridium beijerincki(Dobbin et al., 1999)、Clostridium butyricum(Park et al., 2001)、Corynebacterium sp.(Liu et al., 2010)、Thermincola ferriacetica(Marshall et al., 2009)等.本文首次报道了K. rhizophila在不添加外源中介体的MFC中表现出良好的产电能力,丰富了产电微生物的多样性.
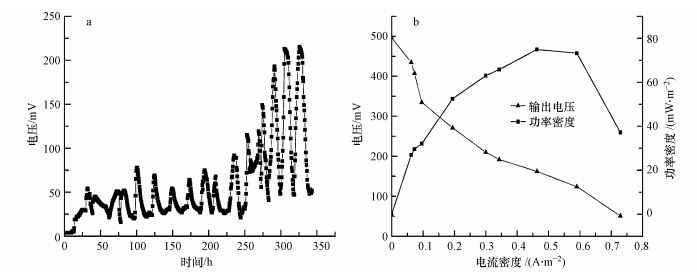 |
| 图 3 菌株P2-A-5以1 g · L-1葡萄糖为底物时的MFC电压变化曲线(a)、极化曲线和功率密度曲线(b) Fig.3 Voltage output of stain P2-A-5 with 1 g · L-1 glucose as substrate(a),polarization and power density curves of P2-A-5(b) |
由图 4可知,EDTA浓度不超过50 mmol · L-1,处理时间不超过75 min时,菌体的OD600值变化不大,在0.8011~0.8804间波动;壳聚糖浓度不超过0.003 g · L-1,处理不超过75 min时,菌体的OD600值变化不大,在0.8031~0.8500之间波动,当壳聚糖浓度超过0.003 g · L-1且处理时间超过15 min时,菌体的OD600值随着处理浓度的增加和处理时间的延长明显下降;PEI浓度低于4 mg · L-1,处理时间不超过75 min时,菌体的OD600值变化不大,在0.7996~0.8760之间波动,当PEI浓度超过4 mg · L-1且处理时间超过15 min时,菌体的OD600值随着处理浓度的增加和处理时间的延长表现出下降的趋势;甘氨酸浓度低于20%,处理时间不超过60 min时,菌体的OD600值没有明显变化,当甘氨酸浓度超过20%且处理时间超过15 min时,菌体的OD600明显下降;溶菌酶浓度不超过1 mg · L-1,处理时间不超过60 min时,菌体的OD600值无明显变化,溶菌酶浓度超过1 mg · L-1且处理时间超过在15 min时,菌体的OD600值开始下降.
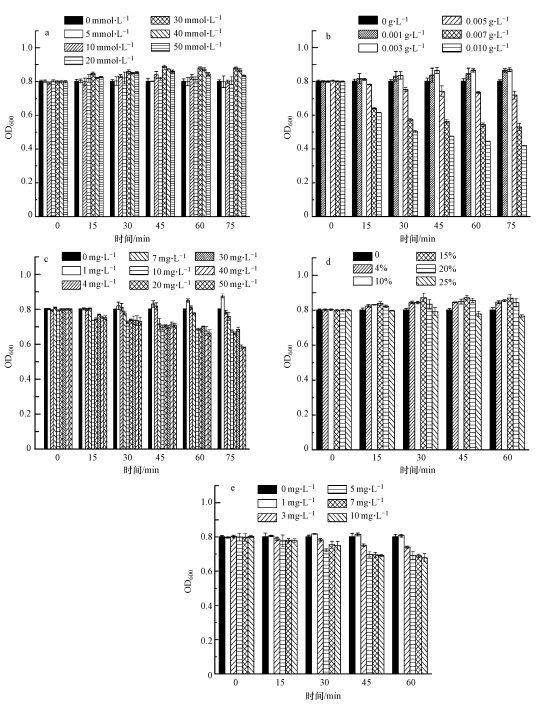 |
| 图 4 EDTA(a)、壳聚糖(b)、PEI(c)、甘氨酸(d)和溶菌酶(e)处理后菌株P2-A-5的细胞存活情况 Fig.4 The survival of the strain P2-A-5 after the treatments of EDTA(a),chitosan(b),PEI(c),glycine(d) and lysozyme(e) |
因此,在不影响菌体存活的情况下,5种化学剂处理菌体的合适条件分别为:0~50 mmol · L-1 EDTA,处理0~75 min;0~0.003 g · L-1壳聚糖,处理0~75 min;0~4 mg · L-1 PEI,处理0~75 min;0~20%甘氨酸,处理0~60 min;0~1 mg · L-1溶菌酶,处理0~60 min.
3.3.2 化学剂处理对菌体细胞通透性的影响由图 5可知,5种化学剂处理后细胞的FDA相对荧光强度都大于1,说明样品组的细胞通透性(与荧光强度成正比)均高于对照组.在不影响菌体存活且获得最大的细胞通透化作用的要求下,5种化学剂的最佳处理条件分别为:50 mmol · L-1 EDTA处理45 min(FDA相对荧光强度为2.2),0.002 g · L-1壳聚糖处理30 min(FDA相对荧光强度为2.9),3 mg · L-1 PEI处理30 min(FDA相对荧光强度为3.8),10%甘氨酸处理30 min(FDA相对荧光强度为3.6),0.5 mg · L-1溶菌酶处理45 min(FDA相对荧光强度为4.87).其中,以0.5 mg · L-1溶菌酶处理45 min对细胞的通透化作用最强.
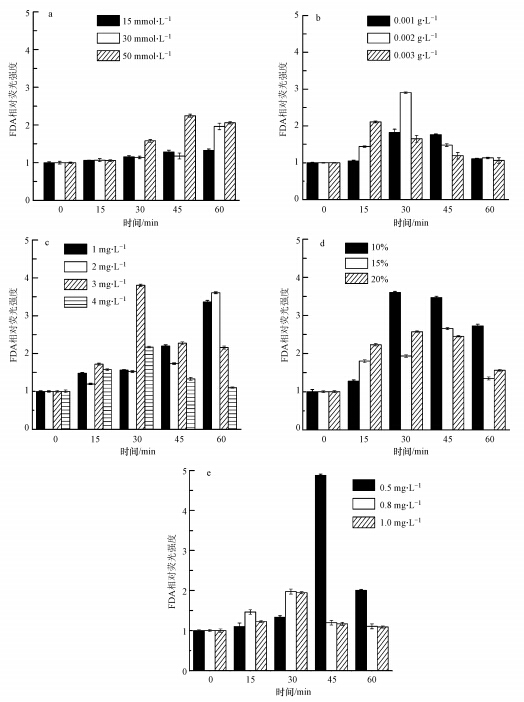 |
| 图 5 不同EDTA(a)、壳聚糖(b)、PEI(c)、甘氨酸(d)和溶菌酶(e)处理条件下菌株P2-A-5的FDA 相对荧光强度 Fig.5 FDA relative fluorescence intensities of the strain P2-A-5 after treatments with EDTA(a),chitosan(b),PEI(c),glycine(d) and lysozyme(e) |
将上述5种化学剂最适处理条件下得到的菌体分别接种于MFCs中,通过测定极化曲线和功率密度曲线研究化学剂处理对菌体产电性能的影响.由表 2可知,菌体经过不同化学剂处理后运行MFCs产生的开路电压没有明显的差异;0.5 mg · L-1溶菌酶处理45 min后,产生的功率密度最大,为206 mW · m-2,同对照(74.9 mW · m-2)相比提高了175%.这可能是因为化学剂处理使细胞的通透性增大,有利于氧化还原介体穿过细胞膜传递电子,从而提高了其产电性能(Liu et al., 2012;Luo et al., 2013).
| 表 2 不同化学剂处理后菌株P2-A-5运行MFCs产生的电压值和功率密度 Table 2 The voltage and power density of the strain P2-A-5 treated with different chemical reagents in MFCs |
菌体经溶菌酶最佳条件处理后接种于MFCs中,此时,阳极液中的底物由最初的葡萄糖分别替换成等浓度的乙酸钠、蔗糖、海藻糖、糊精、木糖醇、吐温80,考察菌株K. rhizophila P2-A-5利用不同底物产电的情况.由图 6a可知,海藻糖作为底物时K.rhizophila P2-A-5的产电能力最高,达到241.7 mW · m-2;其它底物下依次为乙酸钠224.6 mW · m-2、葡萄糖206 mW · m-2、蔗糖181.4 mW · m-2、吐温80 142.5 mW · m-2、 木糖醇87.3 mW · m-2、糊精64.1 mW · m-2.
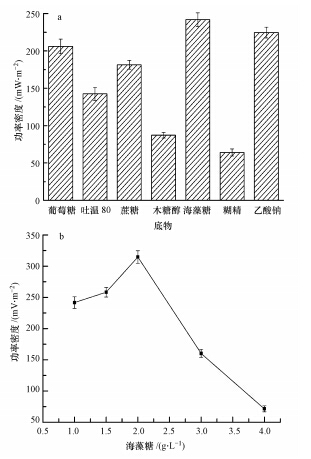 |
| 图 6 不同底物种类(a)和浓度(b)对菌株K. rhizophila P2-A-5功率密度的影响 Fig.6 The effects of different substrates(a) and their concentrations(b)on the power density of the strain K. rhizophila P2-A-5 in MFCs |
进一步研究了不同海藻糖浓度对菌株K. rhizophila P2-A-5产电性能的影响.由图 6b可知,随着海藻糖浓度的增加,菌株运行MFCs后所产生的功率密度逐渐增大.海藻糖浓度为2.0 g · L-1时,其功率密度值达到最大,为314.8 mW · m-2,之后继续增大海藻糖浓度,MFCs功率密度显著下降,当海藻糖浓度为4.0 g · L-1时,功率密度仅为71.4 mW · m-2.
4 结论(Conclusions)1)从MFCs阳极生物膜中分离出一株产电微生物P2-A-5,其16S rDNA序列与菌株Kocuria rhizophila DC2201具有100% 的序列相似度,且处在系统发育树的同一分支,结合形态学观察、生理生化实验结果,将其归属为Kocuria rhizophila.并将其接种于MFCs,验证了其产电性能(74.9 mW · m-2).
2)细胞通透化处理是提高菌株K. rhizophila P2-A-5产电性能的有效手段.其中,0.5 mg · L-1溶菌酶处理45 min对细胞的存活没有明显影响,但通透化作用最强,处理后的菌体运行MFCs产生的功率密度最大,为206 mW · m-2,比未经处理的对照组提高了175%.
3)底物种类和浓度对菌株K. rhizophila P2-A-5的产电性能具有显著影响.其中,以2.0 g · L-1海藻糖为底物运行MFCs产生的功率密度最大,达到314.8 mW · m-2.经过化学剂处理、底物种类和浓度优化后,菌株的产电性能比优化前提高了320.3%.
| [1] | Bond D R, Holmes D E, Tender L M, et al. 2002. Electrode-reducing microorganisms that harvest energy from marine sediments[J]. Science, 295(5554):483-485 |
| [2] | Bond D R, Lovley D R. 2003. Electricity production by Geobacter sulfurreducens attached to electrodes[J]. Applied and Environmental Microbiology, 69(3):1548-1555 |
| [3] | Bond D R, Lovley D R. 2005. Evidence for involvement of an electron shuttle in electricity generation by Geothrix fermentans[J]. Applied and Environmental Microbiology, 71(4):2186-2189 |
| [4] | Borole A P, O'Neill H, Tsouris C, et al. 2008. A microbial fuel cell operating at low pH using the acidophile Acidiphilium cryptum[J]. Biotechnology Letters, 30(8):1367-1372 |
| [5] | Chaudhuri S K, Lovley D R. 2003. Electricity generation by direct oxidation of glucose in mediatorless microbial fuel cells[J]. Nature Biotechnology, 21(10):1229-1232 |
| [6] | Chung K, Okabe S. 2009. Characterization of electrochemical activity of a strain ISO2-3 phylogenetically related to Aeromonas sp. isolated from a glucose-fed microbial fuel cell[J]. Biotechnology and Bioengineering, 104(5):901-910 |
| [7] | Dobbin P S, Carter J P, Juan C G S S, et al. 1999. Dissimilatory Fe (III) reduction by Clostridium beijerinckii isolated from freshwater sediment using Fe (III) maltol enrichment[J]. FEMS Microbiology Letters, 176(1):131-138 |
| [8] | Fedorovich V, Knighton M C, Pagaling E, et al. 2009. Novel electrochemically active bacterium phylogenetically related to Arcobacter butzleri, isolated from a microbial fuel cell[J]. Applied and Environmental Microbiology, 75(23):7326-7334 |
| [9] | Holmes D E, Bond D R, Lovley D R. 2004a. Electron transfer by Desulfobulbus propionicus to Fe(III) and graphite electrodes[J]. Applied and Environmental Microbiology, 70(2):1234-1237 |
| [10] | Holmes D E, Nicoll J S, Bond D R, et al. 2004b. Potential role of a novel psychrotolerant member of the family Geobacteraceae, Geopsychrobacter electrodiphilus gen. nov., sp. Nov., in electricity production by a marine sediment fuel cell[J]. Applied and Environmental Microbiology, 70(10):6023-6030 |
| [11] | Hugh R, Leifson E. 1953. The taxonomic significance of fermentative versus oxidative metabolism of carbohydrates by various Gram negative bacteria[J]. Journal of Bacteriology, 66(1):24-26 |
| [12] | Ishii S, Watanabe K, Yabuki S, et al. 2008. Comparison of electrode reduction activities of Geobacter sulfurreducens and an enriched consortium in an air-cathode microbial fuel cell[J]. Applied and Environmental Microbiology, 74(23):7348-7355 |
| [13] | Jayapriya J, Ramamurthy V. 2012. Use of non-native phenazines to improve the performance of Pseudomonas aeruginosa MTCC 2474 catalysed fuel cells[J]. Bioresource Technology, 124:23-28 |
| [14] | Kim B H, Kim H J, Hyun M S, et al. 1999. Direct electrode reaction of Fe(III)-reducing bacterium, Shewanella putrefacience[J]. Journal of Microbiology and Biotechnology, 9:127-131 |
| [15] | Kim B H, Park H S, Kim H J, et al. 2004. Enrichment of microbial community generating electricity using a fuel-cell-type electrochemical cell[J]. Applied Microbiology and Biotechnology, 63(6):672-681 |
| [16] | Kovács G, Burghardt J, Pradella S, et al. 1999. Kocuria palustris sp. nov. and Kocuria rhizophila sp. nov., isolated from the rhizoplane of the narrow-leaved cattail (Typha angustifolia)[J]. International Journal of Systematic Bacteriology, 49(1):167-173 |
| [17] | Liu J, Qiao Y, Lu Z S, et al. 2012. Enhance electron transfer and performance of microbial fuel cells by perforating the cell membrane[J]. Electrochemistry Communications, 15(1):50-53 |
| [18] | Liu M, Yuan Y, Zhang L X, et al. 2010. Bioelectricity generation by a Gram-positive Corynebacterium sp. strain MFC03 under alkaline condition in microbial fuel cells[J]. Bioresource Technology, 101(6):1807-1811 |
| [19] | Logan B E, Regan J M. 2006. Electricity-producing bacterial communities in microbial fuel cells[J]. Trends in Microbiology, 14(12):512-518 |
| [20] | Logan B E. 2009. Exoelectrogenic bacteria that power microbial fuel cells[J]. Nature Reviews Microbiology, 7(5):375-381 |
| [21] | Lovley D R. 2006. Microbial fuel cells:novel microbial physiologies and engineering approaches[J]. Current Opinion in Biotechnology, 17(3):327-332 |
| [22] | Luo J M, Yang J, He H H, et al. 2013. A new electrochemically active bacterium phylogenetically related to Tolumonas osonensis and power performance in MFCs[J]. Bioresource Technology, 139:141-148 |
| [23] | Luo J M, Ning J, Wang Y X, et al. 2014. The effect of ethanol on cell properties and steroid 1-en-dehydrogenation biotransformation of Arthrobacter simplex[J]. Biotechnology and Applied Biochemistry, 61(5):555-564 |
| [24] | Marshall C W, May H D. 2009. Electrochemical evidence of direct electrode reduction by a thermophilic Gram-positive bacterium, Thermincola ferriacetica[J]. Energy and Environmental Science, 2(6):699-705 |
| [25] | Nevin K P, Richter H, Covalla S F, et al. 2008. Power output and columbic efficiencies from biofilms of Geobacter sulfurreducens comparable to mixed community microbial fuel cells[J]. Environmental Microbiology, 10(10):2505-2514 |
| [26] | Nimje V R, Chen C Y, Chen C C, et al. 2009. Stable and high energy generation by a strain of Bacillus subtilis in a microbial fuel cell[J]. Journal of Power Sources, 190(2):258-263 |
| [27] | Nimje V R, Chen C Y, Chen C C, et al. 2011. Microbial fuel cell of Enterobacter cloacae:Effect of anodic pH microenvironment on current, power density, internal resistance and electrochemical losses[J]. International Journal of Hydrogen Energy, 36(17):11093-11101 |
| [28] | Osman M H, Shah A A, Walsh F C. 2010. Recent progress and continuing challenges in bio-fuel cells. Part II:Microbial[J]. Biosensors and Bioelectronics, 26(3):953-963 |
| [29] | Park H S, Kim B H, Kim H S, et al. 2001. A Novel Electrochemically Active and Fe (III)-reducing Bacterium Phylogenetically Related to Clostridium butyricum Isolated from a Microbial Fuel Cell[J]. Anaerobe, 7(6):297-306 |
| [30] | Pham C A, Jung S J, Phung N T, et al. 2003. A novel electrochemically active and Fe(III)-reducing bacterium phylogenetically related to Aeromonas hydrophila, isolated from a microbial fuel cell[J]. FEMS Microbiology Letters, 223(1):129-134 |
| [31] | Prasad D, Arun S, Murugesan M, et al. 2007. Direct electron transfer with yeast cells and construction of a mediatorless microbial fuel cell[J]. Biosensors and Bioelectronics, 22(11):2604-2610 |
| [32] | Qiao Y, Bao S J, Li C M. 2010. Electrocatalysis in microbial fuel cells-from electrode material to direct electrochemistry[J]. Energy and Environmental Science, 3(5):544-553 |
| [33] | Rabaey K, Boon N, Siciliano S D, et al. 2004. Biofuel cells select for microbial consortia that self-mediate electron transfer[J]. Applied and Environmental Microbiology, 70(9):5373-5382 |
| [34] | Rezaei F, Xing D F, Wagner R, et al. 2009. Simultaneous cellulose degradation and electricity production by Enterobacter cloacae in a microbial fuel cell[J]. Applied and Environmental Microbiology, 75(11):3673-3678 |
| [35] | Ringeisen B R, Henderson E, Wu P K, et al. 2006. High power density from a miniature microbial fuel cell using Shewanella oneidensis DSP10[J]. Environmental Science and Technology, 40(8):2629-2634 |
| [36] | Takarada H, Sekine M, Kosugi H, et al. 2008. Complete genome sequence of the soil actinomycete Kocuria rhizophila[J]. Journal of Bacteriology, 190(12):4139-4146 |
| [37] | Wrighton K C, Agbo P, Warnecke F, et al. 2008. A novel ecological role of the Firmicutes identified in thermophilic microbial fuel cells[J]. The ISME Journal, 2(11):1146-1156 |
| [38] | Xing D F, Zuo Y, Cheng S A, et al. 2008. Electricity generation by Rhodopseudomonas palustris DX-1[J]. Environmental Science and Technology, 42(11):4146-4151 |
| [39] | Zhang L X, Zhou S G, Zhuang L, et al. 2008. Microbial fuel cell based on Klebsiella pneumoniae biofilm[J]. Electrochemistry Communications, 10(10):1641-1643 |
| [40] | Zhang T, Cui C Z, Chen S L, et al. 2006. A novel mediatorless microbial fuel cell based on biocatalysis of Escherichia coli[J]. Chemical Communications, (21), 2257-2259 |
| [41] | Zhao F, Rahunen N, Varcoe J R, et al. 2008. Activated carbon cloth as anode for sulfate removal in a microbial fuel cell[J]. Environmental Science and Technology, 42(13):4971-4976 |
| [42] | Zhou M H, Chi M L, Luo J M, et al. 2011. An overview of electrode materials in microbial fuel cells[J]. Journal of Power Sources, 196(10):4427-4435 |
| [43] | Zhou M H, Chi M L, Wang H Y, et al. 2012. Anode modification by electrochemical oxidation:A new practical method to improve the performance of microbial fuel cells[J]. Biochemical Engineering Journal, 60:151-155 |
| [44] | Zuo Y, Xing D F, Regan J M, et al. 2008. Isolation of the exoelectrogenic bacterium Ochrobactrum anthropi YZ1 by using a U-tube microbial fuel cell[J]. Applied and Environmental Microbiology, 74(10):3130-3137 |
 2015, Vol. 35
2015, Vol. 35


